Результат интеллектуальной деятельности: ПИТАТЕЛЬНЫЕ КОМПОЗИЦИИ И ДЕТСКИЕ СМЕСИ, СОДЕРЖАЩИЕ ОЛИГОФРУКТОЗУ, ДЛЯ СНИЖЕНИЯ НАГРУЗКИ ПАТОГЕННЫХ БАКТЕРИЙ В КИШЕЧНИКЕ МЛАДЕНЦЕВ И ДЕТЕЙ МЛАДШЕГО ВОЗРАСТА
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к питательным композициям для младенцев и детей младшего возраста и их воздействию на здоровье младенцев. В частности, оно относится к детской смеси, содержащей относительно высокое количество олигофруктозы и необязательно относительно высокое количество триглицеридов с высоким содержанием sn-2-пальмитата.
Уровень техники
Когда матери не могут кормить грудью младенцев, детская смесь обеспечивает подходящую альтернативу естественному грудному вскармливанию человеческим грудным молоком. Питательные композиции для младенцев и детей младшего возраста часто поступают в продажу в виде порошков для растворения в воде или в некоторых случаях - в виде готового к употреблению напитка или концентрированных жидких композиций. Эти композиции предназначены для удовлетворения большинства или всех потребностей в питании младенцев или детей младшего возраста.
Однако известно, что человеческое грудное молоко представляет собой неоспоримый «золотой стандарт» питания младенцев. Производители детских смесей делали много попыток обеспечить питательное воздействие на здоровье, близкое к или аналогичное полезному воздействию человеческого грудного молока.
Материнское молоко рекомендовано всем младенцам. Однако в некоторых случаях грудное вскармливание является недостаточным или неуспешным по медицинским причинам или мать отказывается от грудного вскармливания. Для этих ситуаций были разработаны детские смеси. Были также разработаны обогатители для обогащения материнского молока или детской смеси определенными ингредиентами.
Однако во многих случаях исследования показали, что детская смесь не обеспечивает в отношении организма воздействие, идентичное тому, которое обеспечивается человеческим грудным молоком. Например, у младенцев, находящихся на вскармливании детской смесью, и младенцев, находящихся на вскармливании человеческим грудным молоком (HBM), может наблюдаться различная кишечная микробиота.
Здоровая кишечная флора является показателем здоровья младенца, а измененная кишечная микробиота может быть показателем (и/или причиной) аномальных состояний здоровья, таких как диарея, недостаточное всасывание питательных веществ, колики, нарушение сна и нарушение роста и развития.
Известно, что способ родоразрешения может повлиять на исходную кишечную микробиоту младенцев: было показано, что младенцы, рожденные с помощью кесарева сечения, имеют другую кишечную микробиоту по сравнению с младенцами, рожденными с помощью вагинальных родов.
Известно, что на активацию конкретной микробиоты, помимо прочих ингредиентов, особенно могут повлиять неперевариваемые углеводы (пребиотики). Например, было показано, что определенные галактоолигосахариды (GOS) и/или определенные фруктоолигосахариды (FOS) могут активировать рост и распространение бифидобактерий в кишечнике, особенно у младенцев.
Однако кишечная микробиота и ее эволюция в течение развития младенца представляют собой тонкий баланс между наличием и уровнем распространения (количеством) многих популяций кишечных бактерий. Некоторые кишечные бактерии относят к категории «в целом полезных», а другие - «в целом вредных» (или патогенных) из-за их воздействия на общее состояние здоровья младенца.
Определенные виды бактерий, такие как бифидобактерии, могут быть недостаточно представлены у младенцев, находящихся на вскармливании традиционной детской смесью, по сравнению с таковыми у младенцев, находящийся на грудном вскармливании. Аналогичным образом некоторые популяции бактерий считаются патогенными, и необходимо поддерживать низкий уровень их распространения в кишечной микробиоте.
Многие исследования позволили определить способы активизации роста и распространения полезных бактерий в кишечнике младенцев, но при этом мало что известно о способах сокращения роста и распространения патогенных бактерий в кишечнике младенцев и детей младшего возраста.
Существует необходимость снижения или подавления роста патогенных бактерий в кишечнике младенцев и детей младшего возраста.
Существует необходимость угнетения развития и роста патогенных бактерий, или вредных бактерий, в кишечнике младенцев и детей младшего возраста.
Существует необходимость избирательного воздействия на рост патогенных бактерий в кишечнике младенцев и детей младшего возраста, при котором не изменяется рост полезных кишечных бактерий.
Существует необходимость усиления оптимального баланса в общей кишечной микробиоте младенцев и детей младшего возраста. Существует необходимость обеспечения такого оптимального баланса таким образом, чтобы положительно воздействовать на общее здоровье и развитие младенцев и детей младшего возраста.
Существует необходимость усиления оптимального баланса в общей кишечной микробиоте младенцев, особенно путем угнетения или подавления роста патогенных бактерий, в течение первых недель жизни, когда устанавливается такой баланс.
Существует необходимость усиления такого оптимального баланса путем хорошо переносимых, мягко воздействующих средств, не имеющих или практически не имеющих побочных эффектов.
Существует необходимость негативного воздействия на рост патогенных бактерий в кишечнике младенцев и детей младшего возраста, особенно без обеспечения активизации твердого стула, спазмов и колик.
В WO2013068879A2, Manjiang Yao et al., опубликованной 16 мая 2013 г., сообщается о воздействии рациона питания с высоким содержанием sn-2-пальмитата (в присутствии или в отсутствие олигофруктозы) на степень мягкости стула и введении полезных бактерий, таких как бифидобактерии, младенцам.
Сущность изобретения
Изобретение относится к питательной композиции для младенцев и детей младшего возраста, такой как детская смесь или смесь для прикармливаемых детей. Композиция может быть представлена в порошкообразной форме или жидкой форме. Если композиция находится в готовой к употреблению жидкой форме, она содержит по меньшей мере 3 г/л или по меньшей мере 5 г/л олигофруктозы. Если композиция находится в порошкообразной форме или концентрированной жидкой форме, т.е. требует разбавления перед употреблением, она содержит достаточное количество олигофруктозы для получения соответственно по меньшей мере 3 г/л или 5 г/л олигофруктозы в композиции после растворения. Предпочтительно композиция находится в порошкообразной форме.
Композиция изобретения имеет эффект угнетения, снижая или ингибируя рост, а также снижая численность патогенных бактерий в кишечнике младенцев и детей младшего возраста. Предпочтительно младенцы или дети младшего возраста представляют собой младенцев в возрасте 0-12 месяцев.
Краткое описание фигур
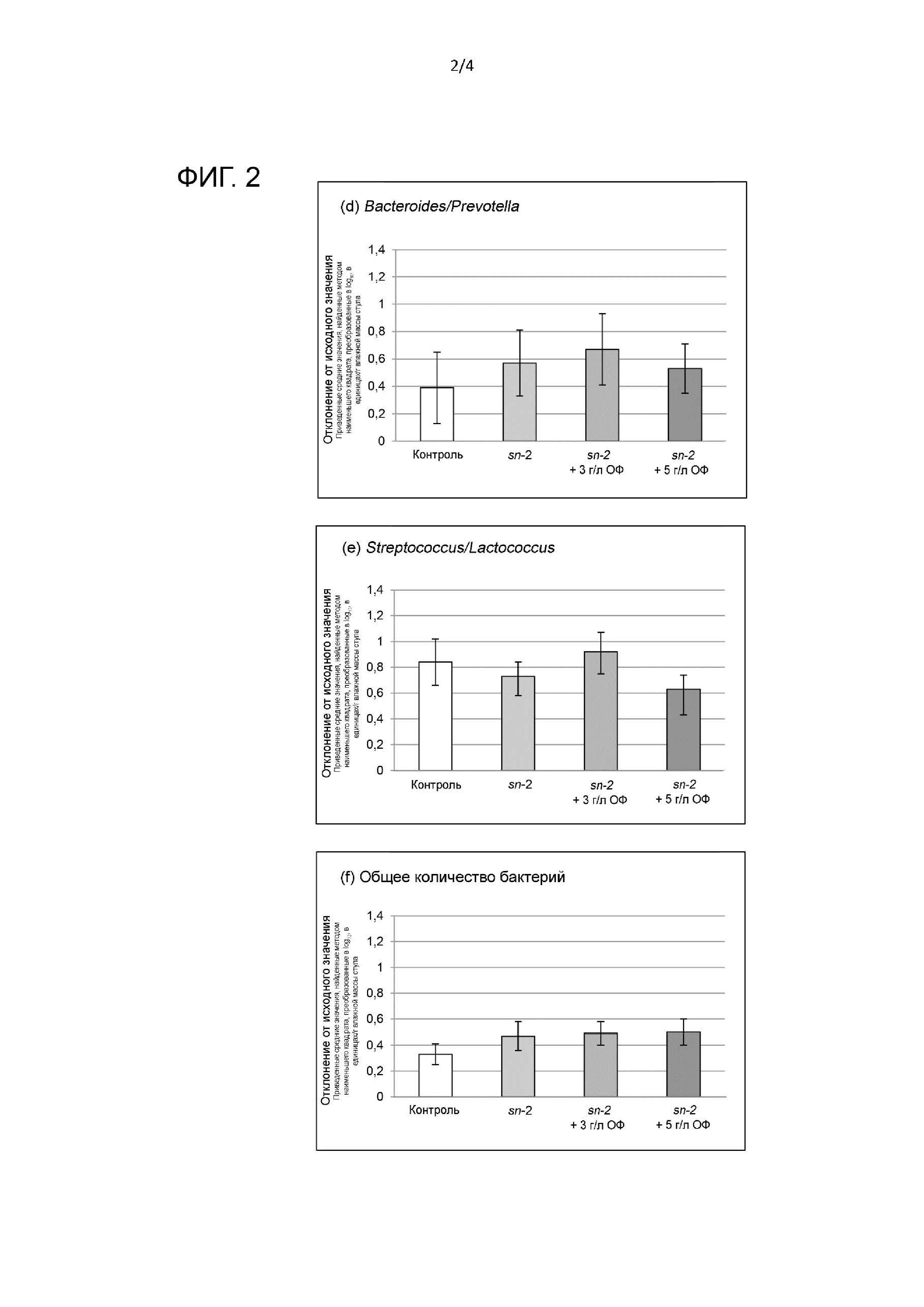
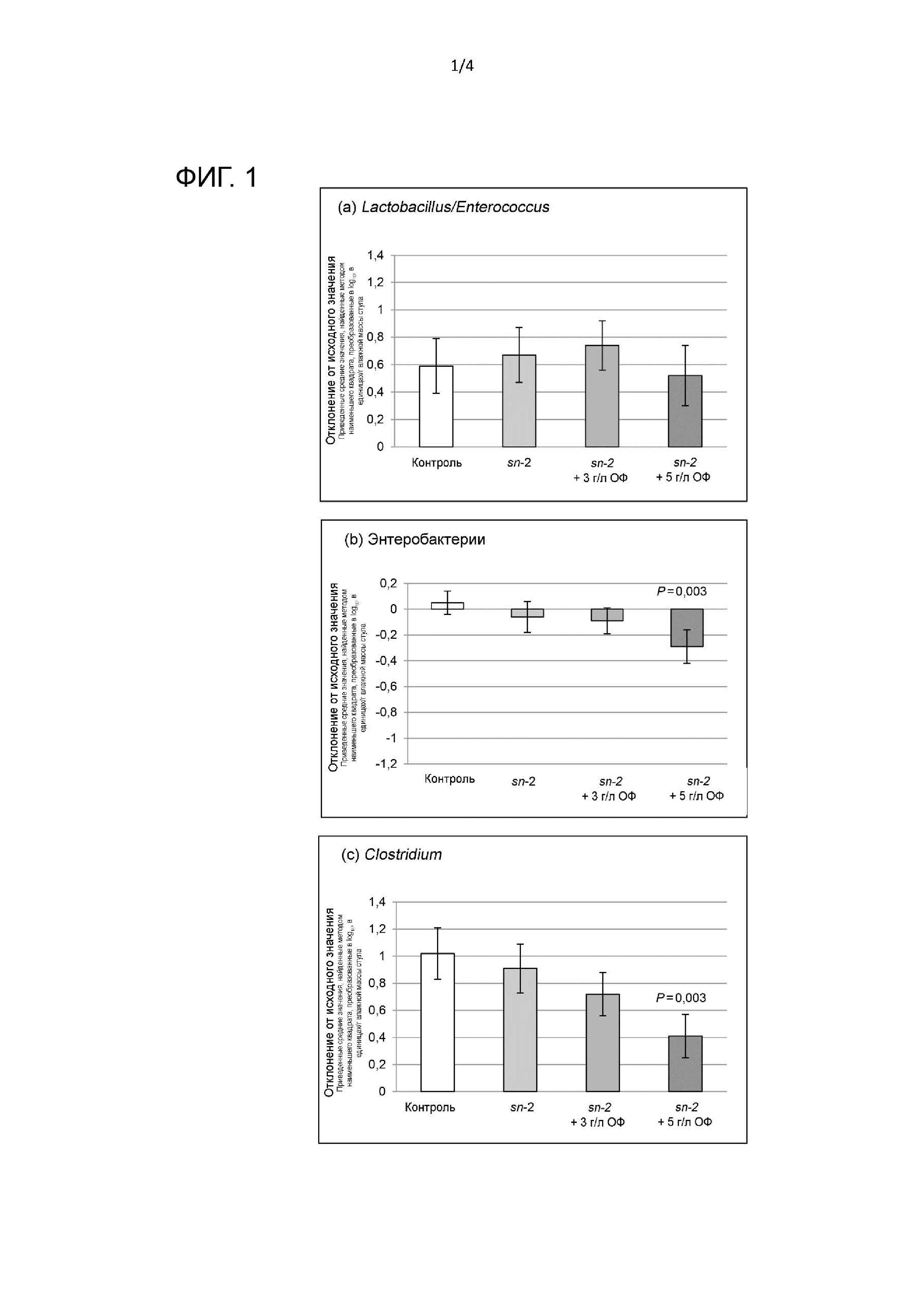
На фиг. 1 и 2 показано воздействие различных питательных композиций на микробиоту младенцев.
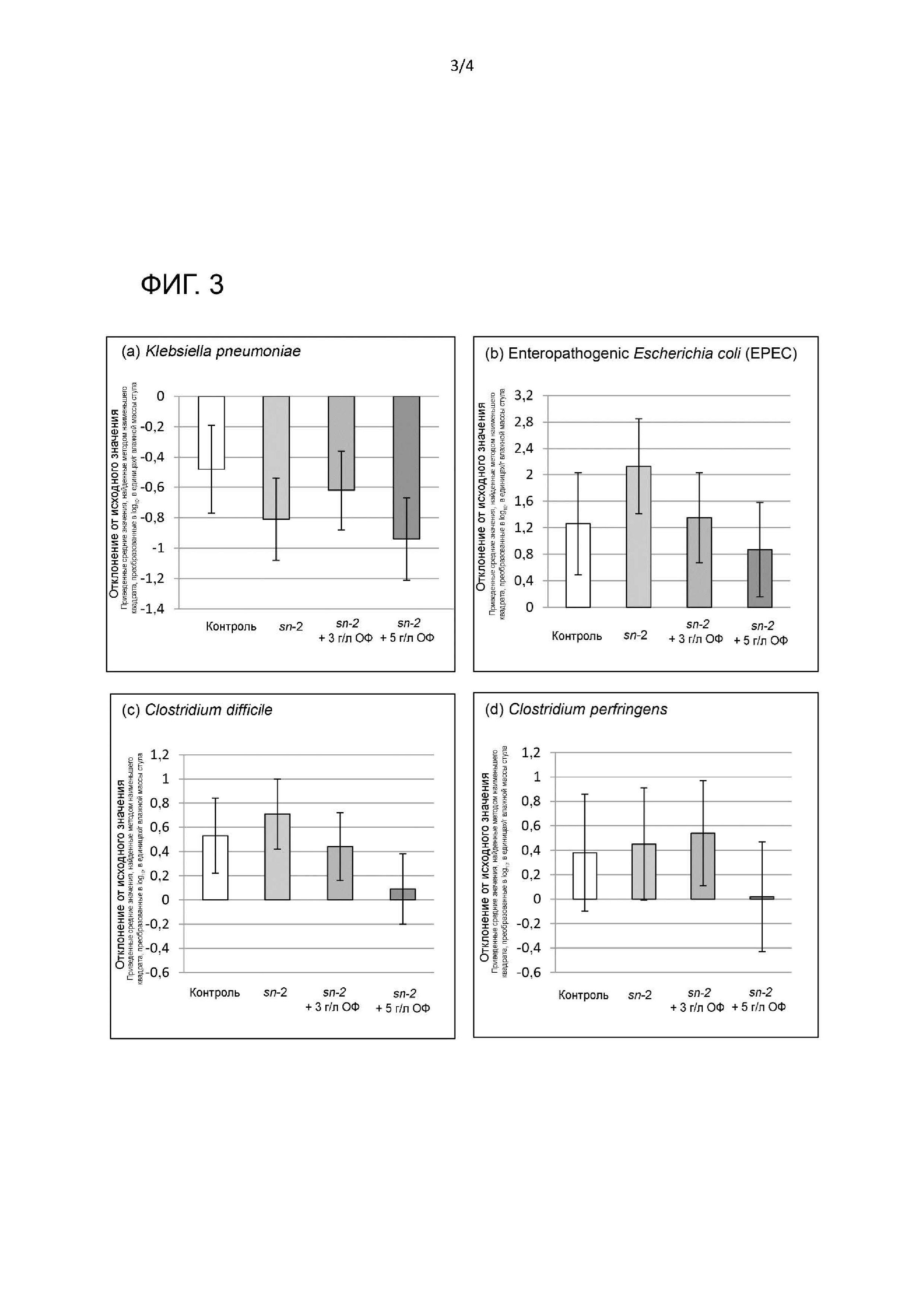
На фиг. 3 показано отклонение концентрации выбранных патогенных фекальных видов патогенных бактерий относительно исходного уровня, по группам кормления. Представленные бактериальные популяции включают как непатогенные, потенциально патогенные и патогенные бактериальные популяции, так и общее количество бактерий.
На фиг. 4 показано отклонение общего измеренного содержания патогенных бактерий относительно исходного уровня, по группам кормления. Изменение приведенного среднего количества фекальных бактерий от общего измеренного содержания патогенных бактерий [суммарное количество всех 4 патогенных организмов, включая Escherichia coli (энтеропатогенная кишечная палочка, EPEC), Klebsiella pneumoniae, Clostridium difficile и Clostridium perfringens] рассчитывали как разницу между логарифмом общего содержания патогенных бактерий на исходном уровне и на неделе 8.
Данные на всех 4 фигурах (фиг. 1,2,3,4) иллюстрируют отклонение концентраций фекальных групп бактерий относительно исходного уровня, по группам кормления. Показанные данные представляют разницу (между исходным уровнем и неделей 8) в log10 приведенных средних значений, найденных методом наименьшего квадрата, концентрации бактерий (выраженных в ед/г влажной массы стула). P-значение представляет сравнение с контролем.
Определения
В настоящем документе следующие термины имеют приведенные ниже определения.
Термин «младенец» означает ребенка в возрасте до 12 месяцев.
Выражение «ребенок младшего возраста» означает ребенка в возрасте от одного до трех лет (также называется ребенком, начинающим ходить).
«Младенец или ребенок младшего возраста, рожденный с помощью кесарева сечения» означает, что ребенок был рожден с помощью кесарева сечения. Это означает, что младенец не был рожден с помощью вагинальных родов.
«Недоношенный» или «преждевременно родившийся» относится к младенцу или ребенку младшего возраста, который родился не в срок. По существу, этот термин относится к младенцу, рожденному до 36 недели беременности.
Выражение «питательная композиция» означает композицию, которой вскармливают субъекта. Указанная питательная композиция обычно предназначена для энтерального, перорального, парентерального или внутривенного применения и обычно включает источник липидов или жиров и источник белков. Предпочтительно питательная композиция предназначена для перорального применения.
Выражение «гипоаллергенная питательная композиция» означает питательную композицию, которая с малой вероятностью может вызывать аллергические реакции.
Выражение «искусственная композиция» означает смесь, полученную с помощью химических и/или биологических средств, которая может быть химически идентична смеси природного происхождения, присутствующей в молоке млекопитающих.
Выражение «детская смесь» означает продукт питания, специально предназначенный для применения в пищу младенцами в течение первых четырех-шести месяцев жизни и сам по себе удовлетворяющий потребности в питании этой категории лиц (статья 1.2 Директивы Европейской комиссии 91/321/EEC от 14 мая 1991 г. о детских смесях и смесях для прикармливаемых детей).
Выражение «начальная детская смесь» означает продукт питания, специально предназначенный для применения в пищу у младенцев в течение первых четырех месяцев жизни.
Выражение «смесь для прикармливаемых детей» означает продукт питания, специально предназначенный для применения в пищу у младенцев старше четырех месяцев и составляющий основной жидкий компонент в рационе питания этой категории лиц, который предполагает постепенно увеличиваемое разнообразие.
Выражение «детское питание» означает продукт питания, специально предназначенный для применения в пищу у младенцев в течение первых лет жизни.
Термин «обогатитель» относится к жидким или сухим питательным композициям, подходящим для смешивания с грудным молоком или детской смесью.
Термин «период отлучения от груди» означает период, в течение которого в рационе питания младенца материнское молоко замещают другой пищей.
Под «материнским молоком» (также «человеческое грудное молоко», HBM) следует понимать грудное молоко или молозиво матери.
В настоящем документе термин «олигофруктоза» относится к олигомерам фруктозы. Это может быть длинная цепь или короткая цепь, в зависимости от степени полимеризации олигофруктозы (числа мономеров). Предпочтительно олигофруктоза изобретения представляет собой короткоцепочечную олигофруктозу, наиболее предпочтительно она имеет степень полимеризации от 2 до 10, например, степень полимеризации от 2 до 8.
В настоящем документе термин «sn-2-пальмитат» относится к пальмитиновой кислоте в положении sn-2 триглицерида, с которым она связана.
«Триглицерид с высоким содержанием sn-2-пальмитата» относится к триглицериду (ТГ), содержащему более 30% пальмитиновых кислот в положении sn-2. Например, в продаже доступен ингредиент с высоким содержанием sn-2-пальмитата от компании Lipid Nutrition, который называется Betapol™ B-55. Это смесь триглицеридов, полученная из растительного масла, в которой по меньшей мере 54% пальмитиновой кислоты находятся в положении sn2 молекулы глицерина.
«Альфа-лактальбумин» относится к высококачественному, легкоперевариваемому сывороточному белку, который составляет 20-25% от общего количества белка человеческого грудного молока (HBM) и является основным белком, присутствующим в HBM . Структура альфа-лактальбумина состоит из 123 аминокислот и 4 дисульфидных мостиков, а молекулярная масса этого белка составляет 14,2 килодальтона. Благодаря высокому содержанию незаменимых аминокислот, особенно триптофана, альфа-лактальбумин идеально подходит для детских смесей с пониженным содержанием белка.
Термин «пребиотик» означает неперевариваемые углеводы, которые благоприятно влияют на организм-хозяина, избирательно стимулируя рост и/или активность полезных для здоровья бактерий, например бифидобактерий, в толстом кишечнике человека (Gibson GR, Roberfroid MB. Dietary modulation of the human colonic microbiota: introducing the concept of prebiotics. J Nutr. 1995; 125:1401-12).
Термин «пробиотик» означает препараты из клеток микроорганизмов или компоненты клеток микроорганизмов, которые оказывают благоприятное воздействие на здоровье или самочувствие организма-хозяина. (Salminen S, Ouwehand A. Benno Y. et al. Probiotics: how should they be defined, Trends Food Sci. Technol. 1999:10 107-10). Клетки микроорганизмов, по существу, представляют собой бактерии или дрожжи.
Под термином «КОЕ» следует понимать колониеобразующую единицу.
Если не указано иное, все приводимые процентные соотношения представляют собой мас.%.
Изобретение будет более подробно описано ниже. Следует отметить, что различные аспекты, признаки, примеры и варианты осуществления, описанные в настоящей заявке, могут быть совместимыми и/или комбинироваться друг с другом.
Дополнительно в контексте изобретения термины «содержащий» или «содержит» не исключают других возможных элементов. Композиция настоящего изобретения, включая многие варианты осуществления, описанные в настоящем документе, может содержать существенные элементы и ограничения изобретения, описанные в настоящем документе, а также любые дополнительные или необязательные ингредиенты, компоненты или ограничения изобретения, описанные в настоящем документе, или иные в зависимости от потребностей, состоять или, по существу, состоять из них.
Раскрытие изобретения
Как правило, детская смесь в готовой к употреблению жидкой форме (например, после растворения порошка) обеспечивает 60-70 ккал/100 мл. Детская смесь, как правило, содержит на 100 ккал: около 1,8-4,5 г белка; около 3,3-6,0 г жира (липидов); около 300-1200 мг линолевой кислоты; около 9-14 г углеводов, выбранных из группы, состоящей из лактозы, сахарозы, глюкозы, глюкозного сиропа, крахмала, мальтодекстринов и мальтозы и их комбинации; и незаменимые витамины и минеральные вещества. Лактоза может быть преобладающим углеводом в детской смеси. Например, жидкая детская смесь может содержать около 67 ккал/100 мл. В некоторых вариантах осуществления детская смесь может содержать около 1,8-3,3 г белка на 100 ккал. Детская смесь может быть представлена в форме порошка, который можно растворять в готовой к употреблению жидкости путем добавления количества воды, которое приводит к получению, например, жидкости, с показателем около 67 ккал/100 мл.
Детская смесь также может содержать нуклеотиды, выбранные из цитидин-5’-монофосфата (ЦМФ), уридин-5’-монофосфата (УМФ), аденозин-5’-монофосфата (АМФ), гуанозин-5’-монофосфата (ГМФ) и инозин-5’-монофосфата (ИМФ) и их смесей. Детская смесь также может содержать лютеин, зеаксантин, фруктоолигосахариды, галактоолигосахариды, сиалиллактозу и/или фукозиллактозу. В детскую смесь можно включать длинноцепочечные полиненасыщенные жирные кислоты, такие как докозагексаеновая кислота (DHA) и арахидоновая кислота (АА). Детская смесь также может включать свободные аминокислоты. Детская смесь также может включать другие ингредиенты, хорошо известные в данной области.
В одном варианте осуществления детская смесь настоящего изобретения содержит около 5-6 г на 100 ккал жира (триглицеридов), с по меньшей мере около 7,5 мас.% этого жира, например около 7,5-12,0%, состоящего из пальмитиновой кислоты в положении sn2 триглицерида. В некоторых вариантах осуществления около 7,8-11,8%, около 8,0-11,5 мас.%, около 8,5-11,0% или около 9,0-10,0 мас.% жира представляет собой пальмитиновую кислоту в положении sn-2 триглицерида.
В некоторых вариантах осуществления пальмитиновая кислота составляет от около 15 до около 25%, например от около 15 до около 20 мас.%, от общего содержания жирных кислот в смеси, и по меньшей мере от около 30%, например от около 35, до около 43% от общего содержания пальмитиновой кислоты находится в положении sn-2.
В некоторых вариантах осуществления детская смесь дополнительно содержит по меньшей мере одну жирную кислоту омега-6 и по меньшей мере одну жирную кислоту омега-3 в соотношении около 6 к около 1. В одном варианте осуществления по меньшей мере одна жирная кислота омега-6 составляет от около 10 до около 15 мас.% от общего содержания жирных кислот, и по меньшей мере одна жирная кислота омега-3 составляет от около 1,2% до около 3,6% от общего содержания жирных кислот. В некоторых вариантах осуществления детская смесь содержит по меньшей мере одну жирную кислоту омега-6, составляющую от около 2 до около 4% от общей массы, и по меньшей мере одну жирную кислоту омега-3, составляющую от около 0,3% до около 0,6% от общей массы.
Жир в детской смеси настоящего изобретения содержит разнообразные триглицериды, как правило, присутствующие в молоке и/или детской смеси. Наиболее распространенными остатками жирных кислот в триглицеридах являются пальмитиновая и олеиновая кислоты. Помимо олеиновой и пальмитиновой кислот присутствующие остатки жирных кислот включают, без ограничений, линолевую кислоту, альфа-линолевую кислоту, лауриновую кислоту, миристиновую кислоту, докозагексаеновую кислоту и арахидоновую кислоту.
Недавние клинические исследования с участием младенцев показали, что питательные смеси, содержащие по меньшей мере одну жирную кислоту омега-6 и по меньшей мере одну жирную кислоту омега-3 в соотношении около 6 к около 1, повышают накопление DHA в эритроцитах и плазме крови. Сбалансированное соотношение около 6 : 1 жирной кислоты омега-6 и жирной кислоты омега-3 также может обеспечивать долговременные полезные для здоровья эффекты, включая защиту от сердечно-сосудистых заболеваний. Такой баланс будет достигаться путем составления композиций настоящего изобретения с источниками жира из растительных масел, которые в своем составе имеют жирные кислоты омега-6, такие как, например, соевое масло и подсолнечное масло, и которые в своем составе имеют жирные кислоты омега-3, такие как рапс, канола, льняное семя, чиа, перлла или грецкие орехи. Для обеспечения модифицированной смеси жиров будет применяться уникальная смесь жиров с 5 разными маслами.
В одном варианте осуществления детская смесь настоящего изобретения содержит от около 1,8 до около 2,2 г общего количества белка на 100 ккал, например от около 1,8 до около 2,1 г или от около 1,9 до около 2,1 г белка на 100 ккал, причем от около 0,3 до около 0,4 г/100 ккал белка представляет собой альфа-лактальбумин. Детская смесь настоящего изобретения может быть представлена в форме готовой к употреблению жидкости, или это может быть жидкий концентрат или порошкообразная смесь, которые можно растворять в готовой к употреблению жидкости путем добавления количества воды, которое приводит к получению жидкости с около 67 ккал/100 мл. Детская смесь настоящего изобретения включает все ингредиенты, которые требуются в соответствии с законодательством США или ЕС, включая, без ограничений, определенные витамины, минеральные вещества и незаменимые аминокислоты. Она также может включать нуклеотиды, такие как ЦМФ, УМФ, АМФ, ГМФ и ИМФ, лютеин, зеаксантин и другие ингредиенты, известные в данной области.
Олигофруктоза (ОФ)
Детская смесь настоящего изобретения может содержать по меньшей мере около 0,4 г или по меньшей мере 0,7 г олигофруктозы на 100 ккал композиции. В некоторых вариантах осуществления она содержит от около 0,4 до около 0,9 г, от около 0,4 до около 0,7 г, от около 0,4 до около 0,5 г, от около 0,7 до около 0,8 г или от около 0,7 до около 0,9 г олигофруктозы на 100 ккал.
В некоторых вариантах осуществления олигофруктоза имеет степень полимеризации от 2 до 10. В некоторых вариантах осуществления по меньшей мере 80%, 90%, 95%, 99% или 100% олигофруктозы имеют степень полимеризации от 2 до 8 (в диапазоне от 2 до 8).
В одном варианте осуществления композиция изобретения включает
- по меньшей мере 3 г/л или по меньшей мере 5 г/л олигофруктозы (ОФ), если композиция представляет собой готовую к употреблению жидкую композицию, или
- достаточное количество олигосахарида для получения соответственно по меньшей мере 3 г/л или 5 г/л олигофруктозы в композиции после растворения, если указанная питательная композиция представляет собой энергетическую или концентрированную композицию.
В некоторых вариантах осуществления питательная композиция изобретения содержит по меньшей мере 0,4 г ОФ/100 ккал композиции или по меньшей мере 0,7 г, или по меньшей мере 0,75 г, или по меньшей мере 0,8 г, или по меньшей мере 0,9 г ОФ/100 ккал композиции.
С учетом результатов, продемонстрированных в примерах, общепризнанным является то, что высокое количество олигофруктозы обеспечивает более сильный эффект. Однако может существовать верхний предел полезного эффекта олигофруктозы, когда появляется неблагоприятный побочный эффект. Такой верхний предел может, например, составлять 2,2 г/100 ккал, 2,0 г/100 ккал, 1,8 г/100 ккал, 1,5 г/100 ккал или 1,2 г/100 ккал. Предпочтительно композиция изобретения содержит 5 г ОФ/л или 0,75 или 0,9 г ОФ/100 ккал композиции, или, наконец, такие количества.
Воздействие на здоровье
Композиция изобретения оказывает положительное воздействие на микробиоту младенцев или детей младшего возраста. Такое положительное воздействие характеризуется угнетением, снижением или ингибированием роста патогенных бактерий. Такие патогенные бактерии могут естественным образом локализоваться в кишечнике или могут иметь экзогенное происхождение.
Такое угнетение, снижение или ингибирование роста можно измерять, например, посредством анализа стула. Такое угнетение, снижение или ингибирование роста можно измерять предпочтительно в возрасте 4 недель, 8 недель, 12 недель, 16 недель или 24 недель. Такое угнетение, снижение или ингибирование роста можно, например, оценивать путем сравнения с кишечной микробиотой младенцев, находящихся на вскармливании традиционной питательной композицией (например, детской смесью), не содержащей олигофруктозы, присутствующей в изобретении.
Композиция изобретения оказывает общее воздействие на разнообразные патогенные кишечные бактерии. В различных вариантах осуществления изобретения угнетение, снижение или ингибирование роста особенно эффективны (видимы/измеряемы) в отношении Klebsiella pneumoniae, и/или E. coli, и/или Enteropathogenic E. coli, и/или Clostridium difficile, и/или Clostridium perfringens, а также общего измеренного содержания патогенных бактерий (см. фигуры).
Путем угнетения, снижения и/или ингибирования роста популяций патогенных бактерий композиция изобретения обеспечивает положительное воздействие на здоровье и способствует введению и поддержанию здоровой кишечной микробиоты. Такая здоровая кишечная микробиота в конечном счете связана с надлежащим всасыванием питательных веществ, адекватным ростом, уменьшением колик, уменьшением диареи и оптимальным состоянием кишечника.
Воздействие изобретения может быть профилактическим (например, предотвращение дисбаланса кишечной микробиоты, предотвращение кишечных инфекций, поддержание здоровой кишечной микробиоты, введение здоровой кишечной микробиоты) или лечебным (восстановление здоровой кишечной микробиоты при ее нарушении, помощь в устранении или сокращении популяций патогенных бактерий в кишечнике, введение здоровой микробиоты после ожидаемых нарушений, например из-за диареи или инфекций).
В одном варианте осуществления композиция изобретения отличается тем, что воздействие на здоровье, наблюдаемое в отношении микробиоты (т.е. угнетение, снижение или ингибирование роста патогенных бактерий в кишечнике младенцев или детей младшего возраста), дополнительно обеспечивает кишечную микробиоту, аналогичную или приближенную к микробиоте младенцев или детей младшего возраста, находящихся исключительно на грудном вскармливании (по сравнению с микробиотой младенцев, находящихся на вскармливании традиционной композицией, т.е. композицией, не содержащей основных признаков изобретения, например не содержащей олигофруктозы). Понятно, что введение кишечной микробиоты, которая подобна/аналогична кишечной микробиоте младенцев, находящихся на грудном вскармливании, является полезной, поскольку человеческое грудное молоко представляет собой «золотой стандарт» питания младенцев.
Целевая группа младенцев
В одном варианте осуществления младенцы или дети младшего возраста родились в срок. Все младенцы могут получать пользу от изобретения, поскольку все младенцы являются или могут быть, в определенном возрасте, подвержены возникновению дисбаланса кишечной микробиоты. В одном варианте осуществления младенцы или дети младшего возраста родились преждевременно (являются недоношенными). В одном варианте осуществления младенцы или дети младшего возраста были рождены с помощью вагинальных родов. В одном варианте осуществления младенцы или дети младшего возраста были рождены с помощью кесарева сечения. Ожидается, что композиция изобретения может быть еще полезнее для младенцев, рожденных с возможным нарушением кишечной микробиоты, или ослабленных младенцев (таких как преждевременно родившиеся младенцы и/или младенцы, рожденные с помощью кесарева сечения). Кроме того, ожидается, что композиция изобретения может быть еще полезнее для младенцев, у которых наблюдаются кишечные расстройства (такие как диарея, инфекции или колики) после рождения, например, в течение первых 4 недель после рождения.
В вариантах осуществления изобретения младенцы родились преждевременно, или были рождены с помощью кесарева сечения, или имеют несбалансированную или аномальную кишечную микробиоту, или страдают кишечной инфекцией; необязательно вышеуказанные состояния являются объектом воздействия композиции изобретения при возрасте младенцев 0-6 месяцев. Без стремления к ограничению какой-либо теорией считается, что младенцы младшего возраста получают еще большую пользу от изобретения, особенно если младенцы имеют (или подвержены риску иметь) несбалансированную кишечную микробиоту и/или имеют ослабленное состояние здоровья (примерами которого являются вышеприведенные состояния).
В одном варианте осуществления младенцы или дети младшего возраста находятся в возрасте 0-6 месяцев, или 0-12 месяцев, или 0-36 месяцев. Ожидается, что композиция изобретения может быть еще полезнее для новорожденных младенцев (в возрасте 0-4 недели или 0-8 недель), поскольку их кишечный тракт может быть более ослаблен.
Следующие примеры представлены для иллюстрации определенных вариантов осуществления и признаков настоящего изобретения, но их не следует толковать как ограничивающих объем настоящего изобретения.
Предполагаемый режим кормления
В одном варианте осуществления композицию изобретения дают (или предписывают давать, или назначают) младенцу или детям младшего возраста в течение 2, 4, 8, 12 недель или в течение по меньшей мере 2, 4, 8, 12 недель. В предпочтительных вариантах осуществления ее дают (или предписывают давать, или назначают) в течение первых 4, 8 или 12 недель жизни младенца. Считается, что раннее начало (при рождении или вскоре после рождения) является предпочтительным для обеспечения предполагаемого воздействия.
Белки/альфа-лактальбумин
Композиция изобретения содержит источник белка. Такой источник белка может, например, обеспечивать от 1,6 до 3 г белка/100 ккал. В одном варианте осуществления, предназначенном для преждевременно родившихся младенцев, такое количество может составлять от 2,4 до 4 г/100 ккал или более 3,6 г/100 ккал. В одном варианте осуществления количество может быть ниже 2,0 г на 100 ккал, например ниже 1,8 г на 100 ккал.
Тип белка не считается в высокой степени критическим для настоящего изобретения, при условии что соблюдены минимальные требования к содержанию незаменимых аминокислот и обеспечен удовлетворительный рост. Однако конкретные белки могут обеспечивать наиболее подходящий субстрат для микробиоты. Таким образом, можно применять источники белка на основе молочной сыворотки, казеина и их смесей, а также источники белка на основе сои. Что касается сывороточных белков, источник белка может быть основан на кислой сыворотке или сладкой молочной сыворотке или их смесях и может включать альфа-лактальбумин и бета-лактальбумин в любых желаемых пропорциях.
В источнике белка предпочтительно преобладают белки молочной сыворотки (более 50% белков происходят от сывороточных белков). В одном варианте осуществления белок композиции представляет собой нативные белки или преимущественно (более 90%) нативные белки.
Белки могут быть нативными или гидролизованными, либо они могут представлять собой смесь нативных и гидролизованных белков. Под термином «нативный» подразумевается, что основная часть белков нативна, т.е. их молекулярная структура не изменена, например не изменено по меньшей мере 80% белков, например не изменено по меньшей мере 85% белков, предпочтительно не изменено по меньшей мере 90% белков, еще более предпочтительно не изменено по меньшей мере 95% белков, например не изменено по меньшей мере 98% белков. В конкретном варианте осуществления 100% белков не изменено.
Термин «гидролизованный» в контексте настоящего изобретения означает белок, который был гидролизован или расщеплен на составляющие его аминокислоты.
Белки могут быть полностью или частично гидролизованными. Может быть желательно вводить частично гидролизованные белки (степень гидролиза от 2 до 20%), например, младенцам, предположительно подверженным риску развития аллергии на коровье молоко. При необходимости использования гидролизованных белков процесс гидролиза может проводиться по желанию и способом, известным в данной области. Например, гидролизаты сывороточного белка можно приготовить ферментативным гидролизом фракции молочной сыворотки в одну или более стадий. Если фракция молочной сыворотки, применяемая в качестве исходного материала, по существу, не содержит лактозы, то установлено, что в процессе гидролиза блокировка лизина белка проявляется в гораздо меньшей степени. Это позволяет снизить степень блокирования лизина с около 15 мас.% общего лизина до менее около 10 мас.% лизина; например, около 7 мас.% лизина, что значительно улучшает питательное качество источника белка.
В одном предпочтительном варианте осуществления белки композиции гидролизованы, полностью гидролизованы или частично гидролизованы. Степень гидролиза (DH) белка может находиться в диапазоне от 8 до 40, или от 20 до 60, или от 20 до 80 или может составлять более 10, 20, 40, 60, 80 90. Следует понимать, что гидролизованные белки могут оказывать на аллергию несколько действий: гидролизованные белки могут быть менее аллергенными, вызывая, таким образом, меньше иммунных аллергических реакций. Гидролизованные белки, особенно небольшие пептиды (длиной менее 20, 10 или 5 аминокислот), могут индуцировать толерантность при пероральном введении, влияя, таким образом, на будущий аллергический статус субъекта. Следует понимать, что гидролизованные белки можно эффективно комбинировать с фукозилированным (-ыми) олигосахаридом (-ами) настоящего изобретения, обеспечивая двойной эффект, возможно синергический эффект, действуя по меньшей мере на 2 разных уровня при установлении аллергических симптомов или аллергического статуса.
В одном варианте осуществления изобретения по меньшей мере 70% белков гидролизовано, предпочтительно по меньшей мере 80% белков гидролизовано, например по меньшей мере 85% белков гидролизовано, даже более предпочтительно по меньшей мере 90% белков гидролизовано, например по меньшей мере 95% белков гидролизовано, в частности по меньшей мере 98% белков гидролизовано. В конкретном варианте осуществления 100% белков гидролизовано.
В одном варианте осуществления гидролизованные белки являются единственным источником белка (т.е. 100% или по меньшей мере 90% белка гидролизовано).
В одном варианте осуществления гидролизованные белки являются основным источником белка (т.е. по меньшей мере 50%, предпочтительно 60% белков гидролизовано).
В одном варианте осуществления питательная композиция изобретения содержит альфа-лактальбумин в количестве по меньшей мере 0,2 или 0,3, или 0,4 г/100 ккал, или по меньшей мере 1,7 г, или 2,0, или 2,3, или 2,6 г/л. Считается, что наличие альфа-лактальбумина в определенном количестве усиливает воздействие олигофруктозы, обеспечивая, например, необходимый питательный субстрат для микробиоты.
Дополнительные пребиотики
Композиция изобретения может также содержать дополнительно нерасщепляемые олигосахариды (например, пребиотики). Они, как правило, присутствуют в количестве от 0,3 до 10 мас.% композиции.
Пребиотики, как правило, являются неперевариваемыми в том смысле, что они не расщепляются и не всасываются в желудке или тонком кишечнике и, таким образом, остаются в нативном виде при переходе в толстый кишечник, в котором они селективно ферментируются полезными бактериями. Примеры пребиотиков включают в себя некоторые олигосахариды, такие дополнительные фруктоолигосахариды (FOS) и/или галактоолигосахариды (GOS). Можно использовать комбинацию пребиотиков, такую как 90% GOS с 10% короткоцепочечных фруктоолигосахаридов. Другая комбинация пребиотиков представляет собой 70% короткоцепочечных фруктоолигосахаридов и 30% инулина (длинноцепочечного FOS). Оба этих пребиотика, а также олигофруктоза (ОФ) доступны для приобретения, в частности, у компании BENEO (Beneo GmbH, Maximilianstrasse, 68165, г. Мангейм, Германия).
Предпочтительная матрица питательной композиции
Композиция в соответствии с изобретением может представлять собой искусственную питательную композицию. Это может быть детская смесь, начальная детская смесь, смесь для прикармливаемых детей, или обогатитель, такой как обогатитель грудного молока, или добавка. Композиция изобретения предпочтительно представляет собой детскую смесь, или обогатитель, или добавку для употребления в первые 4 или 6 месяцев жизни.
Жир/высокое содержание sn-2-пальмитата
В одном варианте осуществления питательная композиция содержит триглицериды с высоким содержанием sn-2-пальмитата, предпочтительно триглицериды, имеющие более 33% пальмитиновых кислот в положении sn-2.
В одном варианте осуществления детская смесь настоящего изобретения содержит около 5-6 г на 100 ккал жира (триглицеридов) с по меньшей мере около 7,5 мас.% этого жира, например около 7,5-12,0%, состоящего из пальмитиновой кислоты в положении sn2 триглицерида.
В одном варианте осуществления изобретения композиция содержит по меньшей мере 7,5%, предпочтительно 8%, более предпочтительно по меньшей мере 9,6% жира, который представляет собой sn-2-пальмитат.
В некоторых вариантах осуществления около 7,8-11,8%, около 8,0-11,5 мас.%, около 8,5-11,0% или около 9,0-10,0 мас.% жира представляет собой пальмитиновую кислоту в положении sn-2 триглицерида.
В некоторых вариантах осуществления пальмитиновая кислота составляет от около 15 до около 25%, например от около 15 до около 20 мас.%, от общего содержания жирных кислот в смеси, и по меньшей мере от около 30%, например от около 35, до около 43% от общего содержания пальмитиновой кислоты находится в положении sn-2.
В некоторых вариантах осуществления детская смесь дополнительно содержит по меньшей мере одну жирную кислоту омега-6 и по меньшей мере одну жирную кислоту омега-3 в соотношении около 6 к около 1. В одном варианте осуществления по меньшей мере одна жирная кислота омега-6 составляет от около 10 до около 15 мас.% от общего содержания жирных кислот, и по меньшей мере одна жирная кислота омега-3 составляет от около 1,2% до около 3,6% от общего содержания жирных кислот. В некоторых вариантах осуществления детская смесь содержит по меньшей мере одну жирную кислоту омега-6, составляющую от около 2 до около 4% от общей массы, и по меньшей мере одну жирную кислоту омега-3, составляющую от около 0,3% до около 0,6% от общей массы.
Жир в детской смеси настоящего изобретения содержит разнообразные триглицериды, как правило, присутствующие в молоке и/или детской смеси. Наиболее распространенными остатками жирных кислот в триглицеридах являются пальмитиновая и олеиновая кислоты. Помимо олеиновой и пальмитиновой кислот присутствующие остатки жирных кислот включают, без ограничений, линолевую кислоту, альфа-линолевую кислоту, лауриновую кислоту, миристиновую кислоту, докозагексаеновую кислоту и арахидоновую кислоту.
В продаже доступна композиция Betapol™ B-55 от компании Lipid Nutrition, которая представляет собой смесь триглицеридов, полученную из растительного масла, в которой по меньшей мере 54% пальмитиновой кислоты находится в положении sn-2 молекулы глицерина. В одном варианте осуществления содержание жира в композиции изобретения составляет около 40-50 мас.% Betapol™ B-55, например от около 43 до около 45 мас%. Для специалистов в данной области очевидно, что процентное содержание используемого жира с высоким содержанием sn-2-пальмитата и общее количество sn-2-пальмитата в смеси может варьироваться и что можно использовать другое масло, содержащее sn-2-пальмитат, без отступления от сущности и объема изобретения.
Хотя кормление младенца смесью с высоким процентным содержанием sn-2-пальмитата способствует образованию более мягкого стула и росту бифидобактерий в толстом кишечнике, комбинация высокого содержания sn-2-пальмитата с олигофруктозой обеспечивает существенно лучшее смягчение стула, при этом обеспечивая оптимальный баланс кишечной микробиоты и усиливая угнетение патогенных бактерий в толстом кишечнике у младенцев, находящихся на вскармливании смесью.
Пример 1
В следующих экспериментах применяли описанные ниже детские смеси. Композиции 3 и 4 представляют собой примеры изобретения.
1. Контрольная смесь (не являющаяся композицией изобретения), имеет обозначение «контрольная смесь».
Контрольная смесь в виде готовой к употреблению жидкой детской смеси имеет 670 ккал/л. Ингредиенты представлены ниже.
|
Контрольная смесь также включает незаменимые аминокислоты, минеральные вещества и микроэлементы, нуклеотиды и различные необязательные ингредиенты и пищевые добавки, широко используемые в детских смесях.
2. Смесь с высоким содержанием sn-2-пальмитата (не являющаяся композицией изобретения), имеет обозначение «смесь sn-2».
Эта смесь аналогична контрольной смеси, за исключением того, что в ней 9,6 мас.% жира представляет собой sn-2-пальмитат. Это достигается путем использования жира, состоящего из 57% растительного масла и 43% Betapol™ B-55, в котором 55% пальмитиновой кислоты находится в положении sn-2. (Betapol доступен для приобретения у компании Loders Croklaan, Hogeweg 1, 1521 AZ Wormerveer, P.O. Box 4, 1520 AA, г. Вормервер, Нидерланды.)
3. Смесь А с высоким содержанием sn-2-пальмитата + олигофруктоза (композиция изобретения), имеет обозначение «смесь sn-2 + 3 г/л ОФ».
Эта смесь аналогична смеси с высоким содержанием sn-2-пальмитата, за исключением того, что она включает 3,0 г/л (0,4 г на 100 ккал) олигофруктозы.
(Следует отметить, что другим примером композиции изобретения является аналогичная смесь без ингредиента Betapol (который обеспечивает 9,6 мас.% жира в виде sn-2-пальмитата.)
4. Смесь В с высоким содержанием sn-2-пальмитата + олигофруктоза (композиция изобретения), имеет обозначение «смесь sn-2 + 5 г/л ОФ».
Эта смесь аналогична смеси с высоким содержанием sn-2-пальмитата, за исключением того, что она включает 5,0 г/л (0,7 г на 100 ккал) олигофруктозы.
(Следует отметить, что другим примером композиции изобретения является аналогичная смесь без ингредиента Betapol (который обеспечивает 9,6 мас.% жира в виде sn-2-пальмитата.)
Подробный список ингредиентов композиций (1) «контрольная смесь», (2) «смесь sn-2», (3) «смесь sn-2 + 3 г/л ОФ» и (4) «смесь sn-2 + 5 г/л ОФ» представлен ниже в таблице 1.
Таблица 1. Сводная таблица композиций
|
Пример 2. Клиническое исследование
Дизайн и общий обзор
Это исследование представляло собой рандомизированное контролируемое двойное слепое клиническое исследование с продолжительностью наблюдения восемь недель, которое проводили с участием младенцев, находящихся на вскармливании смесью, (n 300) и нерандомизированной референтной группы младенцев, находящихся на вскармливании грудным молоком (HM) (n 75). Данное исследование включало 3 клинических посещения (исходное, неделя 4 и неделя 8) и 3 телефонных звонка (неделя 2, неделя 6, а также звонок последующего наблюдения после исследования, совершенный через 2 недели после последнего клинического посещения). Во время исходного посещения собирали демографические данные и данные о семье участника. Настоящий анализ посвящен выборке младенцев (n 183), включающей 32-40 младенцев в группе, у которых брали образцы стула во время исходного посещения (день 1 исследования) и на неделе 8 для анализа состава фекальной микробиоты и параметров микробной метаболической активности (включая уровень pH и органических кислот).
Исследование проводили в Центре здравоохранения Мунтинлупы, г. Мунтинлупа на Филиппинах, в период с апреля по сентябрь 2009 г. Это исследование проводили в соответствии с рекомендациями, изложенными в Хельсинкской декларации, и все процедуры с участием людей/пациентов были одобрены Национальным комитетом по вопросам этики и Бюро по продуктам питания и лекарственным средствам на Филиппинах. У родителя или законного представителя каждого младенца получали информированное согласие в письменной форме.
Участники
В исследование были включены здоровые доношенные (37-42 недели беременности) младенцы, рожденные в результате одноплодной беременности, в возрасте 7-14 дней с соотношением веса и возраста на уровне 5-го процентиля и выше в соответствии с филиппинскими справочными стандартами. Младенцы должны были демонстрировать переносимость и употреблять только детскую смесь на основе коровьего молока, чтобы соответствовать критериям включения в группы кормления смесью, или употреблять только HM, чтобы соответствовать критериям включения в группу кормления HM. Матерей поощряли к грудному вскармливанию младенцев и приглашали для участия в группах исследования, находящихся на вскармливании смесью, только после того, как мать приняла решение кормить младенца только смесью.
Младенцев исключали из исследования, если они на момент включения или ранее получали лекарственные средства, которые потенциально могли бы повлиять на конечные точки исследования; примеры включают любое лекарственное средство, влияющее или предположительно влияющее на переваривание, всасывание и/или метаболизм жира (например, препараты панкреатических ферментов); любые витаминные и/или минеральные добавки, которые содержат кальций; суппозитории, висмутсодержащие лекарственные средства, растительные добавки или лекарственные средства, которые могут нейтрализовать или подавлять секрецию кислоты желудочного сока. Кроме того, младенцев исключали из исследования, если они на момент включения или ранее получали любые антибиотики или противогрибковые лекарственные средства (за исключением предназначенных для наружного применения), и из исследования исключали младенцев, находящихся на вскармливании HM, если их матери на момент включения или ранее получали эти лекарственные средства после родов.
Набор участников был окончен по достижении запланированного размера выборки. Исследование было завершено, когда последний участник выполнил все требования протокола или выбыл из исследования.
Исследуемые варианты кормления
Младенцев, находящихся на вскармливании смесью, рандомизировали по группам для получения ad libitum (по потребности) 1 из 4 смесей (т.е. композиций, аналогичных композициям из примера 1): 1. детская смесь на основе коровьего молока, с преобладанием молочной сыворотки, обогащенная альфа-лактальбумином, для доношенных младенцев, со 100% смеси растительных жиров (S-26 GOLD, Wyeth Nutrition, г. Аскитон, Ирландия) («контрольная смесь»); 2. смесь с высоким содержанием sn-2-пальмитата (контрольная смесь, модифицированная так, что она содержит 60% смеси растительных жиров и 40% смеси жиров с высоким содержанием sn-2-пальмитата [Betapol™, Loders Croklaan, г. Вормервер, Нидерланды]) («смесь sn-2»); 3. смесь с высоким содержанием sn-2-пальмитата с добавлением ОФ (Orafti® P95, BENEO-ORAFTI, г. Тинен, Бельгия) в концентрации 3,0 г/л («смесь sn-2 + 3 г/л ОФ»); 4. смесь с высоким содержанием sn-2-пальмитата с добавлением ОФ (Orafti® P95) в концентрации 5,0 г/л («смесь sn-2 + 5 г/л ОФ»). Исследуемые смеси получали в порошкообразной форме и, за исключением номера индивидуальной упаковки, фасовали одинаковым способом. Инструкции по приготовлению и хранению смеси были указаны на этикетках смесей на английском и филиппинском языках. Все исследуемые смеси соответствовали требованиям к детским смесям, указанным в сборнике международных стандартов по пищевым продуктам Codex Alimentarius, в отношении удовлетворения потребностей в питании. Композиция питательных веществ смесей была описана ранее. Рандомизацию проводили с применением одобренного рандомизационного программного обеспечения; младенцев в равных пропорциях распределяли в каждую из 4 групп кормления смесью следующим образом: 75 младенцев в группу кормления контрольной смесью, 74 младенца в группу кормления смесью sn-2, 76 младенцев в группу кормления смесью sn2 + 3 г/л ОФ и 75 младенцев в группу кормления смесью sn-2 + 5 г/л ОФ. Младенцев, находящихся на вскармливании HM (n 75) ad libitum, включали в нерандомизированную референтную группу.
Фекальная микробиота и биохимия
В выборке младенцев собирали образцы стула на исходном клиническом посещении (день 1 исследования) и посещении на неделе 8. Родители или законные представители давали согласие на сбор этих образцов. В медицинском учреждении персонал исследования собирал по меньшей мере 3 г свежего стула, используя лопатку, прикрепленную к внутренней части крышки стерильной полипропиленовой виалы, и немедленно отправлял образец в морозильную камеру для хранения при температуре -20°C. Замороженные образцы транспортировали на сухом льду в компанию NIZO Food Research B.V., г. Эде, Нидерланды.
Для определения концентраций групп бактерий применяли анализ методом флуоресцентной гибридизации in situ (FISH). Образцы фиксировали в течение ночи в параформальдегиде, как описано ранее, и хранили до перевозки на сухом льду в отделение медицинской микробиологии Университетского медицинского центра Гронингена, г. Гронинген, Нидерланды, где проводили анализы FISH. Для гибридизации с зондом Lab158 образцы предварительно обрабатывали лизоцимом и липазой, чтобы сделать проницаемыми клеточную оболочку грамположительных бактерий, как описано в другом месте. Количественное определение проводили посредством автоматического процесса; для оценки качества автоматического подсчета применяли кумулятивный коэффициент вариации (CV). Если кумулятивный CV превышал 15%, для образца выполняли пересчет. Данные по фекальным группам бактерий представлены в виде преобразованного в log10 значения, в единицах/г влажной массы стула.
Для дополнительного изучения обнаруженных изменений в фекальных группах бактерий выполняли поисковый анализ конкретных фекальных патогенных бактерий. Обнаружение посредством ПЦР в реальном времени выполняли с использованием доступных в продаже наборов. Целевые бактерии включали: Klebsiella pneumoniae, Clostridium difficile (токсин B) и Clostridium perfringens (все штаммы) (PrimerDesign, г. Саутгемптон, Великобритания) и энтеропатогенную Escherichia coli (EPEC) (Shanghai ZJ Biotech Co., г. Шанхай, Китай). Данные по фекальным патогенным бактериям выражены как преобразованное в log10 число копий гена, в единицах/г влажной массы стула.
Фекальные органические кислоты определяли посредством ВЭЖХ, как описано ранее; данные по ним выражены в мкмоль/г влажной массы стула. Нижний предел обнаружения каждой фекальной органической кислоты варьировался в зависимости от фонового показания для этой кислоты в матрице образца, в диапазоне от 40 мкг/г до 400 мкг/г влажной массы стула. CV для всех анализируемых кислот находился в диапазоне от 3,2% до 5,0%. Контроль качества осуществляли путем включения двух стандартных образцов, содержащий различные концентрации основных органических кислот, в каждый цикл анализа.
Статистические анализы
Анализ данных проводили с помощью программного обеспечения SAS 8.2 или более поздней версии (г. Кэри, штат Северная Каролина, США).
Не все из возможных попарных сравнений среди 5 групп кормления представляли равный интерес. Сравнения, представлявшие главный интерес, включали сравнения между группой, получавшей контрольную смесь, и каждой из трех групп, получавших экспериментальные смеси (только sn-2, sn-2 + 3 г/л ОФ и sn-2 + 5 г/л ОФ), а также сравнения между младенцами, находящимися на вскармливании HM, и каждой из четырех групп младенцев, находящихся на вскармливании смесью. Данные по фекальным группам бактерий (полученные методом FISH) у младенцев, находящихся на вскармливании смесью, анализировали посредством ковариационного анализа (ANCOVA) с включенными в модель исходными значениями и способом родоразрешения (вагинальные роды или кесарево сечение), с последующими сравнениями изменений (между исходным уровнем и неделей 8) приведенных средних значений, полученных методом ANCOVA. Используя модель ANCOVA, аналогичную описанной выше, на неделе 8 выполняли отдельные анализы, сравнивая каждую группу кормления смесью с младенцами, находящимися на вскармливании HM. В каждом из этих анализов определяли приведенные средние значения для группы кормления смесью и группы кормления HM, таким образом рассчитывали всего 4 разных средних значения, приведенных к HM. Приведенные средние значения для группы кормления HM незначительно отличались, в зависимости от того, какую группу кормления смесью включали в попарное сравнение, а P-значение для сравнения с группой кормления HM представляет разницу между приведенным средним значением для указанной группы кормления смесью и приведенным средним значением для группы кормления HM, соответствующим этому сравнению. Анализы фекальных групп бактерий выполняли с использованием логарифмически преобразованных значений.
Данные по численности фекальных патогенных бактерий (полученные методом количественной ПЦР) анализировали способом, аналогичным вышеописанному способу, примененному для анализа данных по фекальным группам бактерий. Анализы фекальных патогенных бактерий выполняли с использованием логарифмически преобразованных значений, а также рангов логарифмически преобразованных значений. В обоих случаях ковариационный анализ выполняли с исходным значением в качестве ковариаты и способа родоразрешения в качестве фактора в модели (Примечание. Для 3 из 4 видов патогенных бактерий большинство зарегистрированных значений было равно 0. Для целей анализа все значения 0 были приняты как 1, поскольку log 0 невозможно рассчитать). Оба анализа показали аналогичные результаты; однако анализ на основе рангов был предпочтительным, поскольку даже после логарифмического преобразования данные имели ненормальное распределение. Следовательно, представленные данные по патогенным бактериям представляют собой логарифмически преобразованные значения численности патогенных бактерий с P-значениями, определенными на основе рангов.
Популяция участников, завершивших участие в исследовании в соответствии с протоколом, (популяция PP) для фекальной микробиоты (n 170) состояла из младенцев, находящихся на вскармливании смесью, которые получали только исследуемую смесь в течение всего исследования, или младенцев, находящихся на вскармливании HM, которые употребляли только HM; младенцев, которые завершили все посещения исследования до недели 8 включительно; младенцев, для которых было доступно измерение на неделе 8 для анализа конечной точки; и младенцев, для которых не было зафиксировано серьезных нарушений протокола (например, младенцы, которые соответствовали критериям включения и исключения). Младенцев исключали из популяции для анализа PP, если они получали лекарственные средства, которые потенциально могли бы повлиять на конечные точки исследования (перечисленные выше); также исключали младенцев, находившихся на вскармливании HM, и младенцев, находившихся на вскармливании смесью, если их матери применяли эти лекарственные средства в то время, как младенцы находились на грудном вскармливании. Установление факта нарушения протокола младенцем и его исключение из анализа PP осуществляли до раскрытия кода кормления. Статистические анализы выполняли для популяций EA и PP. Результаты по фекальным группам бактерий в обеих популяциях были аналогичными, статистическая значимость и заключения согласовались практически для всех сравнений и параметров, с 4 исключениями. В настоящем документе представлены результаты, полученные в популяции для анализа PP, поскольку эти данные не включают младенцев, которые получали запрещенные лекарственные средства, которые могли бы повлиять на конечные точки исследования, включая антибиотики. Для 4 сравнений, которые отличаются для популяций EA и PP, представлены оба результата. Из-за того что анализы патогенных бактерий проводились в форме ретроспективных исследований различий между группами бактерий, которые были аналогичными в популяциях PP и EA, а также из-за того что виды бактерий могут быть чувствительны к влиянию антибиотиков, эти анализы проводили только в популяции PP. Все статистические исследования были двусторонними. Уровень статистической значимости составлял 0,05.
Результаты
Исследуемая популяция
В первоначальном исследовании триста младенцев, находящихся на вскармливании смесью, рандомизировали по группам для получения контрольной смеси, смеси sn-2, смеси sn-2 + 3 г/л ОФ или смеси sn-2 + 5 г/л ОФ. В исследование включили семьдесят пять младенцев, находившихся на вскармливании HM. Настоящий анализ представляет выборку из 170 младенцев с образцами стула исходного уровня и недели 8, которые составили популяцию для анализа PP (30-37 в каждой группе кормления для анализов фекальных групп бактерий, а также фекального уровня pH и органических кислот, и 23-27 в каждой группе кормления с образцами, достаточными для анализа фекальных патогенных бактерий). В общем младенцы, участвовавшие в различных группах кормления, были, по существу, похожими по различным исходным характеристикам, хотя младенцы, находящиеся на вскармливании HM, были незначительно младше, с большей вероятностью были рождены с помощью вагинальных родов и с меньшей вероятностью были мужского пола или перворожденными. По сравнению с 375 младенцами, участвовавшими в полном исследовании, у младенцев, состоявших в выборке, отсутствовали существенные различия в исходных характеристиках. В общем доля младенцев в каждой группе кормления с поддающимся обнаружению уровнем фекальных патогенных бактерий на неделе 8 составляла 81-100% для Klebsiella pneumoniae, 19-54% для EPEC, 0-15% для Clostridium difficile и 8-40% для Clostridium perfringens.
Результаты исследования представлены на фиг. 1 (a)-(c), 2 (d)-(f), 3 (a)-(d), 4 и в таблице 2. На фигурах представлена численность различных бактериальных популяций (как отклонение относительно исходного уровня, т.е. популяции в день 1 исследования). Численность популяций представлена для 4 групп: «контрольная смесь» (не являющаяся композицией изобретения), «смесь sn-2» (не являющаяся композицией изобретения), «смесь sn-2 + 3 г/л ОФ» (композиция изобретения) и «смесь sn-2 + 5 г/л ОФ» (композиция изобретения). Статистически значимые различия, если такие имеются, определены P-значениями. В таблице 2 представлена численность различных бактериальных популяций как значения недели 8 (т.е. популяция на момент завершения исследования). Численность популяций представлена для 4 групп: «смесь sn-2» (не являющаяся композицией изобретения), «смесь sn-2 + 3 г/л ОФ» (композиция изобретения), «смесь sn-2 + 5 г/л ОФ» (композиция изобретения) и HM (младенцы, находящиеся на вскармливании грудным молоком, которое считается «золотым стандартом» питания младенцев, не является композицией изобретения).
На фиг. 1(a) и 2(f) показано, что воздействие изобретения является специфичным в отношении потенциально патогенных групп бактерий (особенно энтеробактерий и Clostridium - см. фиг. 1 (b) и (c)).
Численность Lactobacillus/Enterococcus (фиг. 1(a)), а также общая численность популяций бактерий (фиг. 2(f)) не зависит от рационов питания в 4 группах. Другие непатогенные группы не зависят от рационов питания.
На фиг. 1 и 2, а также фиг. 3 и 4 показано следующее:
- рацион питания только с высоким содержанием sn-2-пальмитата не оказывает влияния на угнетение, снижение или ингибирование роста потенциально патогенных или патогенных бактериальных популяций (см., например, фиг. 1(c), 3(b), 3(d), столбцы sn-2);
- олигофруктоза влияет на угнетение, снижение или ингибирование роста как потенциально патогенных, так и патогенных бактериальных популяций. Эти эффекты присутствуют как тенденция в группе с 3 г ОФ/л (не являются статистически значимыми в условиях исследования) и становятся более явными в группе с 5 г ОФ/л (см., в частности, фиг. 4, фиг. 3 (b), (c), (d), фиг. 1(c);
- этот эффект ясно виден в отношении Klebsiella pneumonia, Enteropathogenic Escherichia coli (EPEC), Clostridium difficile и Clostridium perfringens (см. фиг. 3 (a)-(d)) и общего измеренного содержания патогенных бактерий (суммарная численность всех 4 видов патогенных бактерий) (см. фиг. 4). На фиг. 1(c) показано наличие влияния на таксон Clostridium, который включает много разных видов Clostridium.
Таблица 2. Концентрации† выбранных патогенных фекальных видов бактерий на неделе 8, по группам кормления.
|
† Данные по фекальным патогенным бактериям выражены как преобразованные в log10 концентрации бактерий (число копий гена, в единицах/г влажной массы стула).
‡ Показанные значения для грудного молока (HM) представляют диапазон средних значений для HM, найденных методом наименьшего квадрата, для каждого попарного сравнения HM с группой кормления смесью.
§Показаны стандартные ошибки для приведенных средних значений.
ǁP-значения получены с помощью анализа ANCOVA на основании рангов и представляют попарные сравнения с группой HM.
¶Суммарная численность всех 4 видов патогенных бактерий, включая Escherichia coli (EPEC), Klebsiella pneumoniae, Clostridium difficile и Clostridium perfringens.
*Результаты имеют значимые различия при P < 0,05 (относительно группы HM).
В таблице 2 показано следующее:
- рацион питания только с высоким содержанием sn-2-пальмитата не имеет эффекта угнетения численности патогенных бактериальных популяций;
- олигофруктоза влияет на численность патогенных бактериальных популяций таким образом, что они приближаются к таковым у младенцев, находящихся на вскармливании HM, после вскармливания в течение 8 недель. Эффект сходства с младенцами, находящимися на вскармливании HM, присутствует при концентрациях 3 г ОФ/л и 5 г ОФ/л в отношении Clostridium perfringens, а также при концентрации 5 г ОФ/л в отношении Enteropathogenic Escherichia coli (EPEC) и общего измеренного содержания патогенных бактерий (суммарная численность всех 4 видов патогенных бактерий). Этот эффект показан при концентрации 3 г ОФ/л и становится статистически заметным при концентрации 5 г ОФ/л (при p < 0,05).
Следовательно, без стремления к ограничению какой-либо теорией, в таблице 2 показано, что воздействие изобретения проявляется не только в угнетении/ингибировании патогенных бактерий, но изобретение также способствует обеспечению общей численности популяций, приближенной к таковой у младенцев, находящихся на вскармливании человеческим грудным молоком (по сравнению с этим показателем у младенцев, находящихся на вскармливании традиционной смесью, такой как детская смесь только с высоким содержанием sn-2-пальмитата).