Результат интеллектуальной деятельности: СПОСОБ МУЛЬТИПЛЕКСНОГО ИММУНОЛОГИЧЕСКОГО АНАЛИЗА БИОЛОГИЧЕСКИХ ПРОБ ИЗ ВОЗДУХА В АВТОМАТИЧЕСКОМ РЕЖИМЕ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Изобретение относится к области исследований в охране окружающей среды, медицине, микробиологии. Данное изобретение может быть применено для анализа воздуха на наличие в нем биопатогенов, для защиты человека или животных от вредного воздействия бактерий, вирусов, генетических векторов и объектов нанотехнологий.
Уровень техники
Из уровня техники известен способ мультиплексного иммунологического анализа (МИА). Методика мультиплексного иммуноанализа биомаркеров заключается в том, что на первом этапе проводят инкубацию флуоресцентных микросфер, конъюгированных со специфичными аналиту молекулами (антителами или антигенами) с образцом (сыворотка, плазма, супернатант культуры клеток), содержащим искомый аналит, после чего выполняется отмывка не связавшихся с микросферами компонентов. Каждая микросфера содержит внутри себя определенное количество флуоресцентного красителя, тем самым осуществляется их спектральное кодирование, где спектральный код микросферы определяется интенсивностью флуоресценции красителя.
Для отмывки могут быть использованы два способа в зависимости от магнитных свойств используемых микросфер. Если используются немагнитные флуоресцентные полимерные микросферы, то отмывку выполняют путем фильтрации с использованием специального вакуумного коллектора и фильтрационных 96-луночных плоскодонных планшетов. При использовании магнитных флуоресцентных полимерных микросфер отмывку можно проводить двумя способами: фильтрационным и путем магнитной сепарации. Магнитная отмывка заключается в использовании специального магнитного штатива, в который устанавливается плоскодонный 96-луночный планшет, и магнитные микросферы концентрируются на дне лунки планшета, а несвязавшиеся компоненты удаляются переворачиванием планшета вместе с магнитным штативом. Кроме того, возможно выполнение отмывки с помощью автоматической промывочной станции (вошера) полностью в автоматическом режиме. Тип используемых микросфер (магнитные или немагнитные) зависит от производителя конкретных наборов реагентов.
На следующем этапе микросферы с аналитом инкубируют с детекторными биотинилированными антителами. Несвязавшиеся компоненты снова отмываются, после чего к образовавшемуся «сэндвичу» добавляют флуоресцентный краситель – конъюгат стрептавидина с фикоэритрином (SAPE), который связывается с биотиновой меткой на детекторных антителах. Фикоэритрин в данном случае играет роль флуоресцентной метки, которая считывается с использованием репортерного лазера. В некоторых видах анализа используются детекторные антитела, конъюгированные с фикоэритрином напрямую без образования конъюгата «биотин-стрептавидин».
На завершающем этапе анализа для того, чтобы провести детекцию соответствующих аналитов в образце, проводят считывание сигналов флуоресцентных меток в мультиплексном иммунологическом анализаторе, например, проточном цитофлуориметре или планарном иммунологическом анализаторе. Во время измерения каждая микросфера подвергается облучению светом с двумя разными длинами волн (например, красным и зеленым) от двух источников излучения. Тип используемого источника излучения зависит типа анализатора, например, в проточном цитофлуориметре используются твердотельные лазеры, а в планарном иммунологическом анализаторе – светодиоды. Свет от первого лазера (например, красный) служит для возбуждения флуоресценции от микросфер с целью определения кода микросфер и их классификации, а свет от второго лазера (например, зеленый), служит для возбуждения флуоресценции от флуоресцентной метки с целью определения факта связывания с аналитом. Сигнал, испускаемый флуорофорами, регистрируется детекторами анализатора, в качестве которых в проточном цитофлуориметре могут использоваться фотоэлектронные умножители (ФЭУ) или лавинные фотодиоды, а планарном иммунологическом анализаторе – ПЗС-матрица.
Регистрация флуоресценции от фикоэритрина свидетельствует о наличии в исследуемом образце искомого аналита. При этом интенсивность флуоресценции фикоэритрина пропорциональна концентрации искомого аналита. Результаты считывания сигналов выражаются в относительных единицах MFI (медиана интенсивности флуоресценции). Анализатор регистрирует примерно по 100 микросфер с разным спектральным кодом и переходит к следующей лунке. Считывание всего 96-луночного планшета происходит за время от 20 мин до 1 ч в зависимости от вида анализа. Таким образом, анализируется одновременно спектральный код микросферы и наличие (количество) искомого аналита на микросфере. Схема проведения мультиплексного иммуноанализа на платформе Luminex (Рудик Д.В., Гулидова О.В., Мультиплексный анализ на платформе Luminex, Разработка и регистрация лекарственных средств, 2014, №8, 98-104). Однако, указанный способ не позволяет провести автоматический непрерывный мультиплексный иммунологический анализ воздуха на наличие в нем биопатогенов для защиты человека или животных от вредного воздействия бактерий, вирусов, токсинов, генетических векторов и объектов нанотехнологий.
Кроме того, из уровня техники известен способ проведения мультиплексного иммунологического анализа воздуха, раскрытый в WO2007001458 23.08.2007, который выбран в качестве прототипа. Известный способ включает обнаружение и количественное определение множества анализируемых веществ в воздухе. Указанный процесс включает: втягивание потока воздуха в коллектор и обеспечение прохождения указанного потока через нелинейный проход внутри указанного коллектора, в то время как аналиты удерживаются в указанном проходе. Прохождение указанного прохода потоком воздуха необходимо для связывания с жидкостью, которая несет мультиплексированные связывающие элементы, состоящие из множества поднаборов элементов связывания, причем каждое подмножество отличается от всех других подмножеств характеристикой, которая различима при анализе, и каждый содержит отличительный связывающий член, который избирательно связывает один аналит из указанного множества аналитов. Осуществляется обнаружение факта связывания аналита с указанным связывающим членом, который отличает указанные подмножества. Однако известный способ не имеет определенной пробоподготовки к иммунологическому анализу в рамках осуществления исследования воздуха, что снижает достоверность получаемых результатов.
Осуществление изобретения
Заявленный способ мультиплексного иммунологического анализа биологических проб из воздуха в автоматическом режиме, включающий ряд последовательных известных этапов, при которых выполняют сбор частиц биоаэрозоля; переводят их в жидкое состояние; выполняют пробоподготовку образца к анализу; проводят анализ пробы на мультиплексном иммунологическом анализаторе, согласно изобретению, способ включает также следующие этапы:
• пробоподготовка иммунологического анализа включает в себя инкубацию пробы с магнитными микросферами, биотинилированными антителами и флуоресцентными метками, а также промывки между инкубациями;
• при этом иммунологический анализ выполняют в реакторе иммунологического анализа, представляющем собой емкость из химически стойкого материала, объемом 1,5 мл в котором в автоматическом режиме поддерживают температуру 37°C;
• при использовании магнитных микросфер к данной емкости, в автоматическом режиме при помощи электромеханического привода, подводят кольцевой постоянный магнит, удерживающий магнитные частицы во время промывок;
• при этом реактор иммунологического анализа установлен на валу орбитального шейкера, который в автоматическом режиме приводит его в движение со скоростью до 1500 об/мин;
• при этом все режимы работы реактора задаются автоматически управляющим компьютером в соответствии с протоколом анализа;
• реагенты для пробоподготовки иммунологического анализа хранят при 4°С на охлаждаемой платформе, также установленной на валу орбитальной мешалки;
• перед использованием реагентов, платформу приводят в движение с частотой 800 об/мин для получения однородной суспензии микросфер;
• после выполнения всех операций пробоподготовки, суспензию из реактора направляют в мультиплексный иммунологический анализатор;
• манипуляции с жидкостями при пробоподготовке мультиплексного иммунологического анализа выполняют шприцевым насосом и многопортовым клапаном в автоматическом режиме.
Указанные действия осуществляются посредством автоматического анализатора биопатогенов в воздухе, который представляет собой комплекс оборудования, размещенный в едином металлическом корпусе рамной конструкции. Компоновка прибора выполнена в виде двух отсеков. В верхнем отсеке находятся все узлы и подсистемы, непосредственно контактирующие с биологическими образцами и реагентами – от устройства сбора аэрозоля до ПЦР и иммунологического анализатора. В этом отсеке поддерживается контролируемый температурно-влажностный режим. В нижнем отсеке расположено все вспомогательное оборудование и управляющая электроника: источники и распределители питания, резервные аккумуляторные батареи, холодильная установка, управляющий компьютер и блоки автоматики. Холодильная установка обеспечивает охлаждение оборотной воды до температуры +4 °C; эта вода, в частности, используется для охлаждения реагентов, чтобы обеспечить автономность прибора на протяжении до 7 дней. Система пробоподготовки автоматического анализатора биопатогенов в воздухе построена по закрытой схеме.
При этом пробоподготовка иммунологического анализа включает в себя инкубации пробы с магнитными либо немагнитными микросферами, биотинилированными антителами и флуоресцентными метками, такими как коньюгаты стрептавидин-фикоэритрин (SAPE), а также промывки между инкубациями. При этом операции выполняются в реакторе иммунологического анализа, представляющем собой ёмкость из химически стойкого материала, например, полипропилена, объемом 1,5 мл в котором, в автоматическом режиме поддерживается необходимая температура + 37°C. При использовании магнитных микросфер к данной емкости, в автоматическом режиме при помощи электромеханического привода, подводят кольцевой постоянный магнит, удерживающий магнитные частицы во время промывок. Реактор иммунологичекого анализа установлен на валу орбитального шейкера, способного приводить его в движение в автоматическом режиме на скоростях до 1500 об/мин. Все режимы работы реактора задаются автоматически управляющим компьютером в соответствии с протоколом анализа. Реагенты для пробоподготовки иммунологического анализа (микросферы, антитела, SAPE) хранятся при +4°С на охлаждаемой платформе, также установленной на валу орбитальной мешалки. Перед использованием реагентов, платформа приводится в движение с частотой 800 об/мин для получения однородной суспензии микросфер. После выполнения всех операций пробоподготовки, суспензия из реактора направляется в мультиплексный иммунологический анализатор. Все манипуляции с жидкостями при пробоподготовке МИА выполняются шприцевым насосом и многопортовым клапаном в автоматическом режиме.
Задачей настоящего изобретения является осуществление возможности проведения анализа пробы воздуха в автоматическом режиме в реальном времени, что позволит сократить время исследования образца за счет полной автоматизации процесса, обеспечить непрерывный мониторинг состава воздуха, а также повысить точность определения биопатогенов в воздухе.
Техническим результатом изобретения является автоматизация процесса иммунологического исследования пробы воздуха, сокращение времени исследования образца, обеспечение непрерывного мониторинга состава воздуха, а также повышение точности определения биопатогенов в воздухе.
Раскрытие изобретения
Указанный технический результат реализуется за счет следующих приемов. Процесс анализа воздуха начинается со сбора аэрозольной пробы и ее перевода в жидкую фазу. При этом за сбор окружающего воздуха может отвечать импактор – прибор, создающий поток всасываемого воздуха до 4 м3 в минуту и способный концентрировать аэрозольные частицы в диапазоне от 0.3 до 10 мкм приблизительно в 10 раз. Обогащенный такими частицами воздух подается в коллектор аэрозоля, построенный по принципу водяного циклона. Сбор пробы происходит в течение 4-5 минут, после чего, необходимый объем (около 5 мл) жидкости передается на следующие стадии обработки. Следующим этапом является иммунологический анализ пробы, который может быть осуществлен на основе микрофлюидных компонентов, включающих: трубки для подачи жидкости, шприцевые насосы, клапаны, вортексные шейкеры, в ходе которого полностью воспроизводится ручная методика пробоподготовки в автоматическом режиме. При этом компоненты-участники пробоподготовки образца к МИА в соответствии с протоколом добавляются по микротрубочкам в пробирку-реактор, расположенный на шейкере, оборудованном магнитом и подогревом до +37°C. При этом пробоподготовка включает в себя ряд последовательных действий, выполняемых автоматически:
1. Первичное антитело конъюгируют с микросферами (А), для чего емкость с микросферами в концентрации 50000 шт./мл взбалтывают с первичным антителом на шейкере 60 секунд. Затем автоматически переносят по флюидной системе 50 мкл раствора А в полипропиленовый реактор. Туда же по флюидной системе доставляют 50 мкл раствора образца (В). В результате в лунке 50 мкл A + 50 мкл B.
2. Затем выполняют первую инкубацию полученной пробы АВ на шейкере в течении 30 минут, при температуре 37°С и 800 об/мин. В результате в лунке 100 мкл AB + B.
3. Затем выполняют первую промывку: поднимают магнит на 60 сек. Забирают по флюидной системе пробу из реактора АВ. Опускают магнит. Добавляют в реактор 200 мкл промывочного фосфатно-солевого буфера (PBS-TBN). Выполняют взбалтывание промывочного буфера на шейкере в течении 10 сек. Затем опять поднимают магнит на 60 сек. Забирают по флюидной системе жидкость из реактора. Опускают магнит. Добавляют в реактор 200 мкл промывочного буфера PBS-TBN. Осуществляют его взбалтывание на шейкере в течении 10 сек. Поднимают магнит на 60 сек. Забирают по флюидной системе жидкость из реактора. Опускают магнит. Переносят по флюидной системе в лунку 50 мкл промывочного буфера PBS-TBN. Осуществляют его взбалтывание на шейкере в течении 10 сек. В результате данного этапа в лунке 50 мкл AB.
Затем добавляют конъюгированные с биотином детектирующие антитела, (С), для чего выполняют их взбалтывание в емкости при температуре +4 °С на шейкере в течение 20 секунд. После чего переносят по флюидной системе 50 мкл (С) в PBS-TBN в концентрации 8 мкг/мл каждое в реактор. В итоге в лунке 50 мкл AB + 50 мкл С.
4. Выполняют вторую инкубацию на шейкере в течении 30 минут при температуре 37° С и 800 об/мин. По итогу этапа в лунке 100 мкл ABС + С.
5. Выполняют вторую промывку, аналогично первой (см. этап 3). По итогу этапа в лунке 50 мкл ABС.
После чего емкость с конъюгированным раствором фикоэритрина (PE) со стрептавидином (SA) (D) в PBS-TBN в концентрации 8 мкг/мл взбалтывают при температуре +4 ° С на шейкере в течение 20 секунд. После этого по флюидной системе переносят 50 мкл раствора D в реактор. К концу данного этапа в лунке 50 мкл ABС + 50 мкл D.
6. Выполняют третью инкубацию на шейкере в течение 30 минут при температуре 37° С и 800 об/мин. В конце данного этапа в лунке 100 мкл ABСD + D.
7. Выполняют третью промывку, аналогично первой и второй (см. п. 3) После чего переносят по флюидной системе в реактор 100 мкл промывочного буфера PBS-TBN и взбалтывают его на шейкере в течение 10 сек. В результате в лунке 100 мкл ABСD.
8. Затем указанные 100 мкл ABCD образца автоматически переносят по флюидной системе в мультиплексный иммунологический анализатор и проводят анализ.
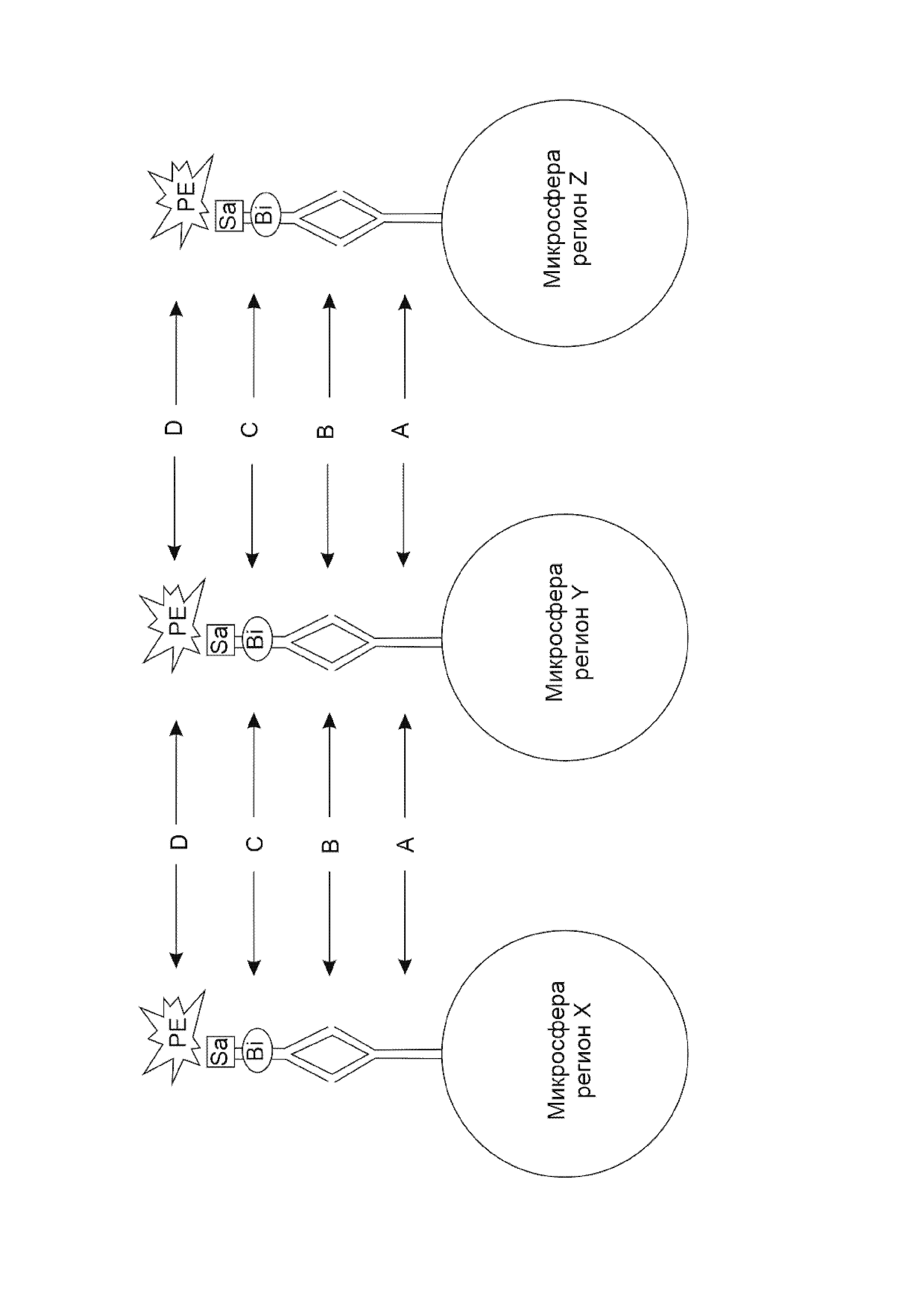
Схема иммунокомплексов, образующихся в результате пробоподготовки, представлена на фиг. 1, где А – первичное антитело, конъюгированное с микросферами, В – антиген/мишень/образец, С – детектирующее антитело, конъюгированное с биотином (Bi), D – фикоэритрин, конъюгированный со стрептавидином (SAPE).
Указанные действия осуществляют посредством автоматического анализатора биопатогенов в воздухе, который включает импактор, коллектор аэрозоля, ультразвуковой гомогенизатор, первый клапан ротационого типа, блок выделения нуклеиновых кислот (НК), содержащий: резервуар с реагентами для выделения НК, третий ротационный клапан, реактор выделения НК, блок пробоподготовки мультиплексного иммуналогического анализа (МИА), включающий: резервуар с микросферами, антителами и красителями, второй ротационный клапан и реактор МИА; резервуар, содержащий промывочные жидкости такие как: буфер, или спирт 70%, или гипохлорит, или щелочь; иммунологический анализатор; резервуар с реагентами ПЦР; ПЦР анализатор; архив проб; резервуар для охлаждаемой оборотной водой; резервуар жидкости предназначенной для слива.
Мультиплексный иммуноанализ проводили при помощи xMAP микросфер производства компании Luminex типу «capture - sandwich».. Первичные антитела в количестве 10 мкг/106 микросфер с тремя спектральными кодами: к коду №45 коньюгировался SY-25 (анти-гексон аденовируса), к коду №72 – ST1 (анти-ЛПС S. typhimurium) и к коду №78 – CT8 (анти-бета-субъединица холерного токсина). Сенсибилизацию микросфер выполняли в соответствии с протоколом, приведенным в официальном издании компании Luminex «xMAP Cookbook, 3rd. edition», методом карбодиимидной химии. Микросферы (1 × 106 шт.) активировали 10 мкл 50 мг/мл (в дистиллированной H2O) 1-Этил-3-[3-диметиламинопропил]карбодиимид гидрохлорид (EDC) (Sigma, #22980) и 10 мкл 50 мг/мл (в дист. H2O) N-гидроксисульфосукцинимида натриевая соль (s-NHS) (Sigma, #24520) в 80 мкл активирующего буферного раствора (0,1 M NaH2PO4, pH 6,2) (Amresco, #Am-O823) в течение 20 мин при 25°С с вращением 20 об/мин на вортексе. После этого активированные микросферы промывали два раза и ресуспендировали в 500 мкл буферного раствора для связывания (50 мM MES, pH 5,0) (Sigma, #M2933) с добавлением каждого из антител к своему региону. После инкубации в течение 2 ч в темноте при 25°С с вращением при 20 об/мин и трех этапов промывки, блокирующим буферным раствором микросферы ресуспендировали в 1 мл буферного раствора для хранения и использовали для анализа не менее чем через 16 ч. В качестве буфера для блокировки и хранения (microsphere blocking/storage buffer) использовались PBS-TBN (PBS, 0.1% BSA, 0.02% Tween-20, 0.05% NaN3) для CT8, PBS-BN (PBS, 1% BSA, 0.05% NaN3) для SY-25 и PierceTM Protein-Free (PBS) Blocking Buffer (Pierce, #37584) для ST1.
Для приготовления PBS-TBN и PBS-BN использовали реактивы: BSA (Sigma, #B-4287); Tween 20 (Amresco, #Am-O777), NaN3 (Amresco, #Am-O639). Подсчет микросфер, оставшихся после процедуры сенсибилизации, осуществляли с помощью автоматического счетчика клеток TC-20 [Bio-RAD, США].
Таким образом, за счет того, что способ мультиплексного иммунологического анализа воздуха выполняется в автоматическом режиме и в следующей последовательности: сбор аэрозольных частиц, перевод их в жидкое состояние, последующий анализ отобранной пробы с помощью мультиплексного иммунологического анализа в автоматическом режиме, со следующими последовательными этапами пробоподготовки: взбалтывание и соединение пробы с микросферами; первая инкубация пробы, первая промывка, взбалтывание и соединение пробы с антителами, вторая инкубация пробы, вторая промывка, взбалтывание и соединение пробы с SAPE, третья инкубация, третья промывка, получение пробы для анализа, который выполняется в мультиплексном иммунологическом анализаторе, что позволяет провести автоматический анализ пробы воздуха, при этом сократить время исследования образца, обеспечить непрерывный мониторинг состава воздуха, а также повысить точность определения биопатогенов воздухе.
Заявленный способ может быть осуществлен специалистом на практике и при осуществлении обеспечивает реализацию заявленного назначения. Возможность осуществления на практике следует из того, что для каждого признака, включённого в формулу изобретения на основании описания, известен материальный эквивалент, что позволяет сделать вывод о соответствии критерию «промышленная применимость» для изобретения и критерию «полнота раскрытия» для изобретения.