Результат интеллектуальной деятельности: Моноклональные антитела с ориентировкой на антиген Р респираторно-синцитиального вируса человека, получаемые и секретируемые из клеточных гибридом, используемые для обнаружения и диагностики инфекции, вызываемой респираторно-синцитиальным вирусом
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к моноклональным антителам или их фрагментам, которые распознают белок Р респираторно-синцитиального вируса человека (RSV), используемый для разработки способов диагностики заражения человека вирусом RSV.
УРОВЕНЬ ТЕХНИКИ ИЗОБРЕТЕНИЯ
Респираторные заболевания, вызываемые вирусом, представляют собой проблему для здоровья населения по всему миру. Основными возбудителями этих инфекций среди пациентов детского возраста являются: респираторно-синцитиальный вирус человека (RSV), аденовирус (ADV), вирусы гриппа А и В (INF А и В), вирус парагриппа (PIV) и метапневмовирус человека (MPV). В настоящее время эффективные механизмы профилактики этих вирусов отсутствуют, и по оценкам ежедневные случаи заражения составляют 94000000 новых случаев (Всемирная организация здравоохранения). Сверхнагрузка на системы здравоохранения, связанная с этими вспышками, также приводит к существенным экономическим потерям.
RSV - вирус, отрицательно воздействующий на дыхательную систему, который в настоящий момент представляет собой проблему огромной экономической и социальной важности, отрицательно сказываясь на детской и взрослой заболеваемости и смертности. В этих группах населения, а в особенности у младенцев и детей возрастом младше двух лет, RSV приводит к возникновению множества клинических заболеваний: от таких легких форм, как ринит, тонзиллит и отит, до других, более тяжелых форм, таких как пневмония, бронхит, бронхиолит и альвеолит. По результатам серологических исследований от 70 до 100% детей как минимум один раз подвергались воздействию вируса в возрасте от 1 до 2 лет соответственно. Было подсчитано, что ежегодно RSV приводит к возникновению приблизительно 34 миллионов случаев заражения, 3,4 миллионов госпитализаций и около 200 тысячам смертей детей в возрасте младше 5 лет. В настоящий момент RSV - вирус эпидемиологической важности в Чили и Латинской Америке. Некоторые исследования показали, что процент случаев заражения респираторными заболеваниями, вызванными RSV у новорожденных и грудных детей, во время вспышек в зимнее время может превышать 70%. Более того, исследования в Латинской Америке подтверждают роль RSV в качестве главного возбудителя инфекций нижних дыхательных путей у пациентов младше 2 лет с частотой более 40%. К сожалению, в настоящее время нет ни вакцин для иммунизации новорожденных, ни эффективных способов лечения для контроля заражения этой группы населения.
RSV - это РНК-вирус с показателем 15,3 кб, инкапсулированный с помощью одноцепочечного генетического материала и отрицательной кодирующей полярности, который относится к семейству Paramyxoviridae и к Pneumovirus. Геном RSV кодирует 10 генов, скомбинированных следующим образом: 5'-NS1-NS2-N-P-M-SH-G-F-M2-L-3', которые транскрибируются РНК-зависимой РНК-полимеразой (белок L) на 10 РНК-независимых мессенджеров. Пять из этих белков отвечают за упаковку генетического материала и определяют структуру вирусной частицы, соответствующей нуклеокапсидному белку N и матриксному белку М, вместе с трансмембранными гликопротеинами F, G и SH соответственно. Другие четыре белка: М2-1, М2-2, L и Р, задействованы в репликации и транскрипции вируса. В дополнение к этому белки NS-1 и NS-2 неструктурны, что снижает экспрессию интерферона типа I зараженной клеткой и, тем самым, предотвращает активацию врожденного иммунного ответа.
Текущие способы в системе общественного здравоохранения включают тесты, основанные на обнаружении вирусных антигенов, для непосредственной иммунофлуоресценции в образцах мазков из носоглотки с помощью полимеразной цепной реакции с обратной транскрипцией (RT-PCR) и иммунохроматографического анализа (быстрые тесты). Среди упомянутых продуктов наиболее эффективны вирусные панели, основанные на иммунофлуоресценции, ввиду того, что они позволяют обнаруживать наибольшее количество респираторных вирусов, которых насчитывается 12 типов в случае PCR респираторной вирусной панели (RPV) с применением технологии люминесцентного анализа xTAG, и 14 типов - в случае респираторной вирусной панели по технологии eSensor. Несмотря на этот широкий диапазон обнаружения, важно упомянуть факторы их стоимости и времени реакции. В случае с первым упомянутым тестом стоимость составляет приблизительно 70 долларов США при времени реакции от 12 до 18 часов, в то время как стоимость второго теста составляет приблизительно 90 долларов США, а время реакции - 60 минут.
Следовательно, крайне важно найти эффективный, быстрый и недорогой диагностический тест для обнаружения RSV, который сможет конкурировать с характеристиками существующих способов диагностики. В качестве реакции на такую проблему в настоящем изобретении описываются моноклональные антитела, необходимые в качестве альтернативы для обеспечения данной потребности, поскольку они обеспечивают специфическое распознавание вирусных антигенов в образцах у пациентов, зараженных RSV. Таким образом, настоящее изобретение включает такие продукты, как моноклональные антитела, и альтернативный способ, который предусматривает их использование для определения и быстрой, эффективной и точной диагностики у пациентов, зараженных RSV, со 100% специфичностью в клинических образцах, и благодаря которому можно определить концентрации, эквивалентные 1,5 нг специфического антигена ELISA. Это позволяет клиническим специалистам назначать раннее и соответствующее лечение.
Моноклональное антитело является видом гомогенного антитела, характеризующегося распознаванием отдельного антигена. Они вырабатываются отдельной гибридной клеткой (гибридомой), которая является продуктом слияния клона лимфоцита В и опухолевой плазматической клетки. Свойство специфической связи и высокого сродства с антигеном обеспечило развитие моноклональных антител как очень полезного средства для обнаружения молекул, которое представляют огромный научный, клинический и промышленный интерес. В настоящее время моноклональные антитела широко используются как в фундаментальных, так и в прикладных исследованиях благодаря своей специфичности и воспроизводимости, что обеспечивает более надежную поддержку исследования. Тем не менее, биомедицина является разделом, в котором моноклональные антитела имеют широкое практическое применение, как для диагностики и лечения разнообразных инфекционных болезней, так и в качестве терапии других патологий. В то время как справедливо использование моноклональных антител во всех видах методик обнаружения и диагностики, наилучшие результаты были достигнуты именно в проектировании наборов для диагностики invitro. Для этого в настоящий момент имеются несколько погружных наборов быстрого обнаружения, таких как тест на определение беременности, который основывается на обнаружении уровней человеческого хорионического гонадотропина (hCG) в моче с помощью анти-hCG антитела. Кроме того, приобрели большую важность моноклональные антитела для терапевтических целей. В настоящее время существуют терапевтические воздействия для различных патологий, в которых используются, помимо прочего, такие коммерческие моноклональные антитела, как: Алемтузумаб, гемтузумабозогамицин, ритуксимаб, трастузумаб.
На предшествующем уровне техники существует публикация WO 2013076702, в которой описывается использование моноклонального антитела, предназначенного специально для обнаружения респираторно-синцитиального вируса; в частности, в ней описывается антитело, направленное на антиген М2-1, получаемый в нашей лаборатории (Гомес и соавт., журнал «Медицинская вирусология», июль 2014; 86(7): 1256-66). Это антитело отличается от настоящего изобретения тем, что у моноклонального антитела для обнаружения RSV в качестве антигена имеется белок Р, а не М2-1, как приводится в противопоставленном документе. Преимуществом генерирования антител на белке Р является то, что это, будучи выполнено с другим антигеном, может быть использовано в иммунологическом анализе наряду с анти-М2-1 антителами (опубликованы ранее), повышая чувствительность при обнаружении антигена, в малых количествах присутствующего в образцах из носоглотки.
В документе US 2014093501 описывается антитело, состоящее из тяжелых и легких вариабельных цепей как минимум одного мышиного моноклонального антитела, действующее против RSV. В частности, это антитело ориентировано на белок F. В отличие от настоящего изобретения моноклональные антитела для обнаружения RSV в качестве антигена имеют белок Р, а не F, как приводится в противопоставленном документе. В первую очередь, антиген Р более консервативен, чем антиген F, что позволяет обнаруживать штаммы RSV, представляющие разные серологические типы.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к двум моноклональным антителам против респираторно-синтициального вируса человека (RSV). В частности, настоящее изобретение относится к двум мышиным моноклональным антителам, которые соответствуют моноклональным антителам, выделяемым клеточными линиями гибридом под названием 2E6/D2 и 6Н5/Н1, которые реагируют на антиген Р RSV. Данные антитела не вступают в конфликт друг с другом за участок связывания, а также не препятствуют одновременному связыванию с ним. Моноклональные антитела могут использоваться в анализах для обнаружения, диагностики и/или определения заражения RSV. Настоящие антитела могут использоваться одновременно для повышения чувствительности обнаружения в клинических образцах с низким содержанием антигена. В частности, антитела из гибридомы 2E6/D2 могут эффективно захватывать белок Р RSV в клинических образцах. Далее данные захваченные и иммобилизированные белки были обнаружены антителами, образованными гибридомой 6Н5/Н1, и связаны с ферментом, воздействующим на хромогенный субстрат. Эта характерная особенность обеспечивает комбинацию обоих антител с различными метками для обнаружения того же антигена в образцах с небольшим его количеством.
В настоящем изобретении также предлагаются способы диагностики exvivo или invitro, предусмотренные для обнаружения вирусного антигена Р RSV, в котором используются моноклональные антитела, вырабатываемые и выделяемые гибридомами 2E6/D2 и 6Н5/Н1, в таких анализах, как ELISA, флуоресцентная микроскопия, иммуноблотирование, иммунофлуоресценция, иммуногистохимия, иммунохроматография, проточная цитометрия, клеточный сортер, иммунопреципитация и/или вестерн-блоттинг. Образцы для анализа отбираются, помимо прочего из: клеток invitro, зараженных RSV, носовых секретов, носовых смывов, фарингеальных секретов и/или бронхиальных смывов или секретов, спинномозговой жидкости, плазмы. Настоящее изобретение предусматривает способ обнаружения RSV в биологических образцах и клеточных культурах при помощи моноклональных антител, вырабатываемых и/или выделяемых вышеуказанными клеточными линиями гибридом, связанными на любой твердой подложке, например, нитроцеллюлозе, найлоновой мембране, магнитных микроносителях, флуоресцентных гранулах или прочих подложках; или связанными с любой другой молекулой, например, ферментами, белками, флуорофорами, радиоактивными изотопами или любым другим химическим соединением. Настоящее изобретение может использоваться при обнаружении для наборов RSV, включающих антитела, вырабатываемые вышеуказанными гибридомами. Также настоящее изобретение включает в свой объем любой тип химически связанной молекулы или субстрата, например, метки, флуорофоры, биотин, радиоизотопы, металлы, ферменты и/или любой химический элемент, связанный с моноклональными антителами, выделяемыми гибридомами 2E6/D2 и 6Н5/Н1, причем химически связанная молекула или субстрат обеспечивает визуализацию или обнаружение антитела. Таким образом, настоящее изобретение также предусматривает антитела, которые отдельно распознают белок Р, связанный с молекулами, субстратами или маркерами, отличными от антитела, выступающими как часть способа обнаружения, анализа и/или диагностики в биологических образцах.
ОПИСАНИЕ ФИГУР
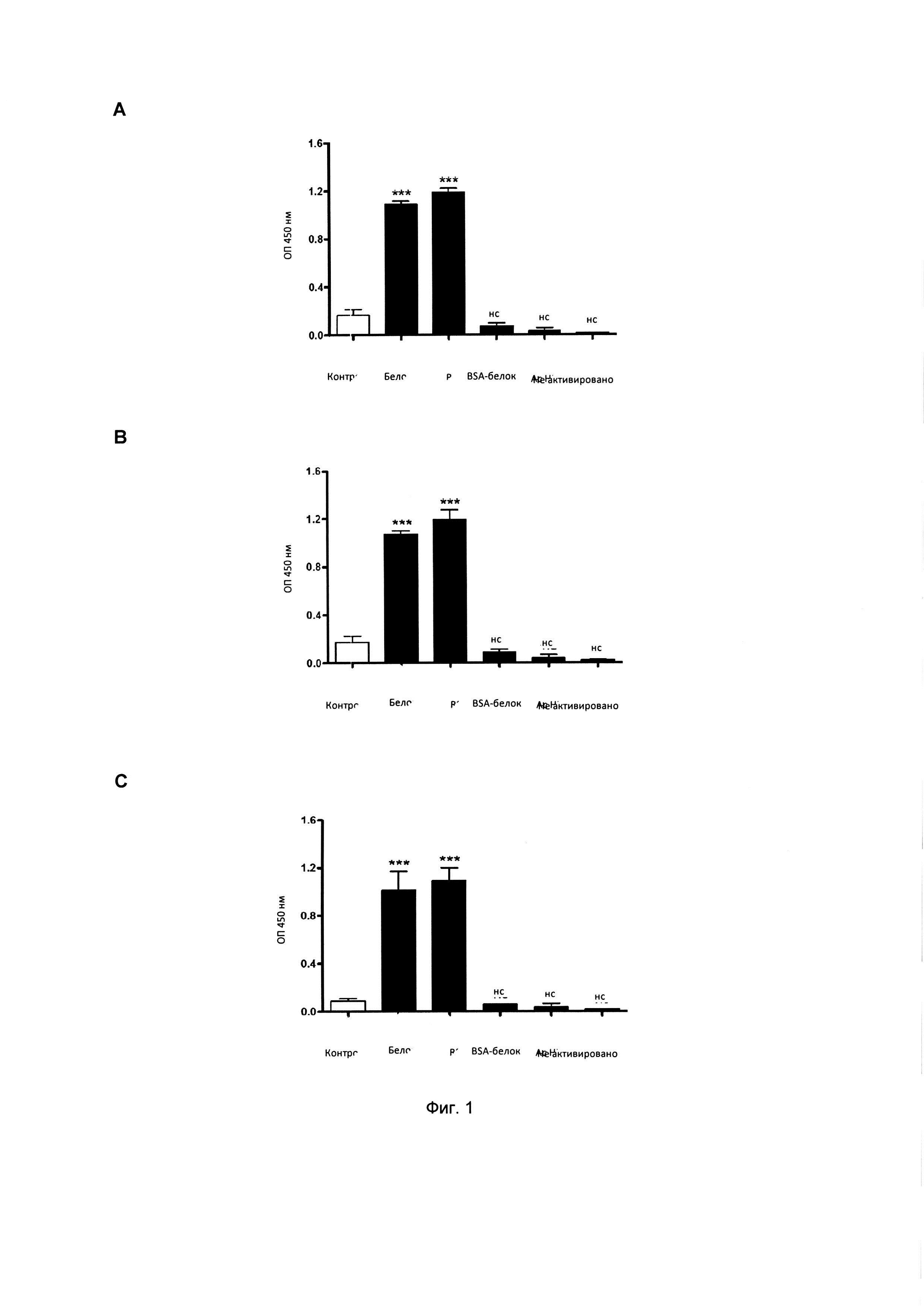
Фиг. 1: Обнаружение белка Р RSV моноклональными антителами, вырабатываемыми гибридомами 2E6/D2 и 6Н5/Н1, с использованием косвенного анализа ELISA. Планшет активировался 50 нг очищенного рекомбинантного белка Р RSV либо с помощью 1×106 БОЕ RSV. В качестве негативного контроля другие лунки активировались с помощью 1×106 БОЕ метапневмовируса (MPV) или 50 нг BSA-белка. Также использовались лунки без антигена, с первичным антителом, с мышиным анти-lgG антителом, связанным с HRP (неактивированным), и лунки как без антигена, так и первичного антитела, а только с мышиными анти-lgG антителами (HRP). Затем в лунки были введены анти-Р антитела из гибридомы 2E6/D2 в объеме 170 нг на лунку (А), из гибридомы 6Н5/Н1 - 170 нг на лунку (В) и анти-Р антитело к фосфорбелку респираторно-синцитиального вируса RSVH102 (номер по каталогу #АВ94965 (Abcam)) - 170 нг на лунку (С). Данные, представленные на столбцовой диаграмме, указывают на оптическую плотность, обнаруженную при 450 нм путем преобразования субстрата тетраметилбензидина в окрашенное соединение, катализированное ферментом пероксидазы хрена (HRP) на вторичном мышином анти-lgG антителе, связанном с конкретными антителами, выделяемыми гибридомами 2E6/D2, 6Н5/Н1 и RSVH102 компании Abcam. Показатели соответствуют средним значениям +/- стандартного отклонения получаемой оптической плотности каждого образца как минимум в двух отдельных анализах. ***Р<0,0001 при дисперсионном анализе одного образца в сопоставлении с негативным контролем и при тестировании с использованием множественных сопоставлений в тесте Даннета, не, существенной разницы в сравнении с негативным контролем не наблюдалось.
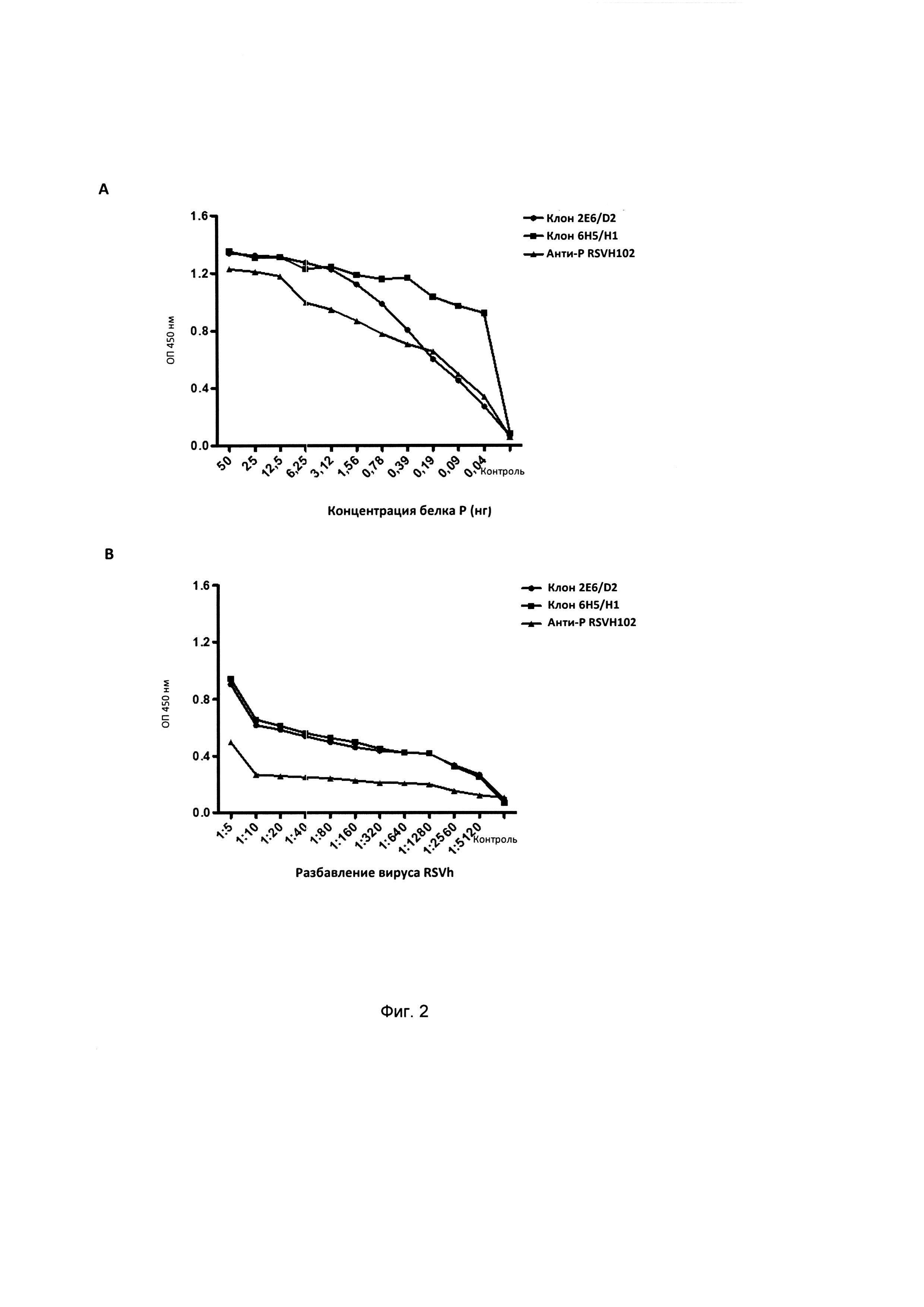
Фиг. 2: Определение чувствительности моноклональных антител, вырабатываемых гибридомами 2E6/D2 и 6Н5/Н1, для обнаружения белка Р RSV. Планшеты ELISA активировались путем последовательных разбавлений в пропорции 1:2, начиная с 50 нг белка Р и заканчивая 0,04 нг (А), и последовательных разбавлений в пропорции 1:2 - с 1×105 БОЕ инокулята RSV до разбавления в пропорции 1:5. 120 (В). Неактивированные лунки были включены в качестве негативного контроля. Данные, приведенные на графике, демонстрируют оптическую плотность 450 нм, получаемую за счет фермента пероксидазы хрена (HRP), наличествующей в анти-Р антителах из гибридом 2E6/D2 и 6Н5/Н1, которые были использованы в концентрации 170 нг на лунку (А и В). Анти-Р антитела RSVH102 к вирусу RSV (номер по каталогу Abcam #АВ94965) также использовались в концентрации 170 нг на лунку (А и В). Показатели соответствуют средним значениям получаемой оптической плотности каждого образца как минимум в двух отдельных анализах.
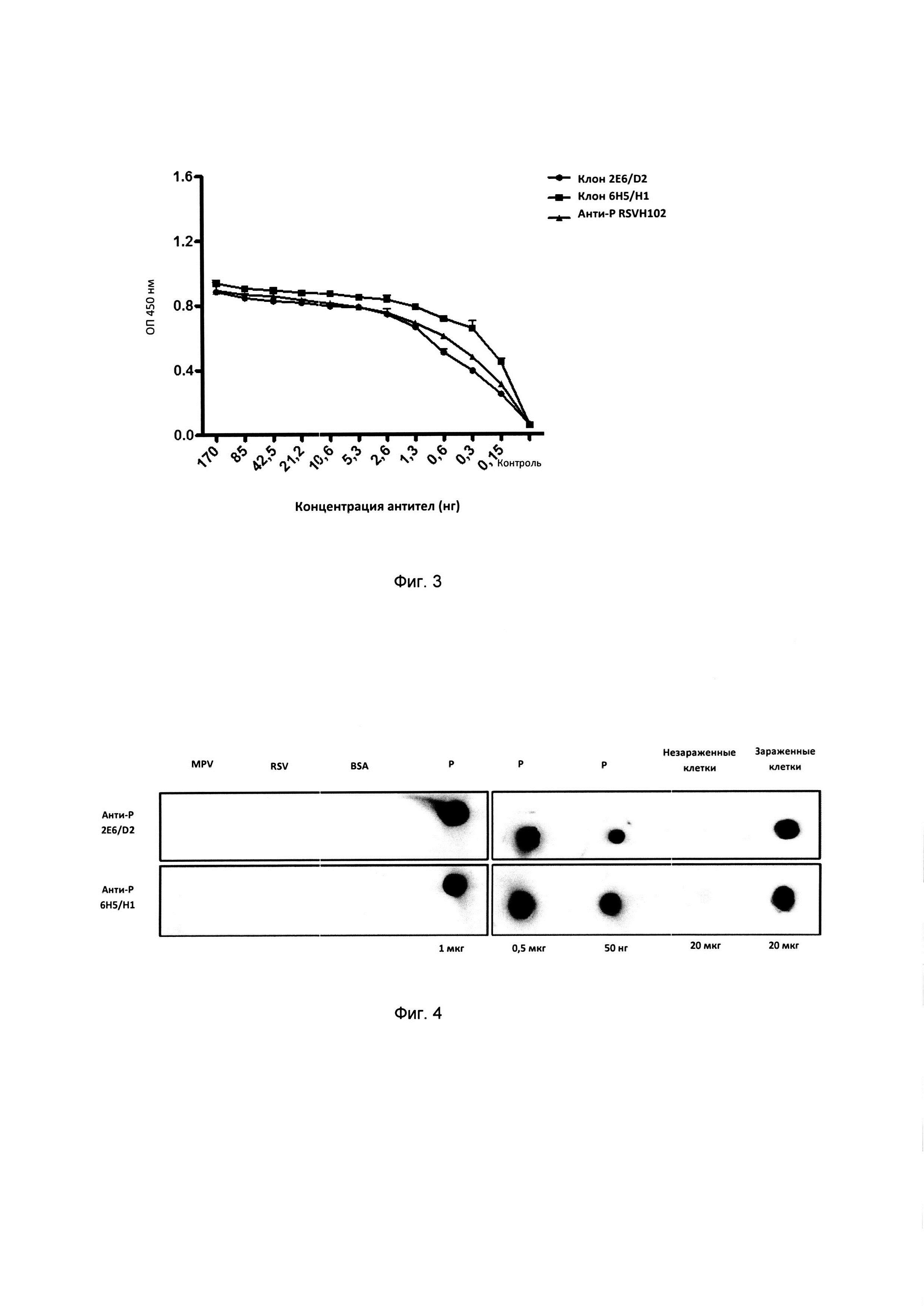
Фиг. 3: Анализ последовательных разбавлений моноклональных анти-Р антител RSV, полученных изгибридом 2E6/D2 и 6Н5/Н1, для обнаружения очищенных антигенов RSV. Планшеты ELISA активировались 50 нг рекомбинантного белка Р RSV, а антиген обнаруживался путем последовательных разбавлений анти-Р антител 2E6/D1 или 6Н5/Н1 в пропорции 1:2, начиная с концентрации 3,4 мкг/мл (170 нг на лунку). Данные выражены в качестве средних значений получаемой оптической плотности при 450 нм каждого образца как минимум в двух отдельных анализах.
Фиг. 4: Подтверждение специфичности моноклональных антител, выделяемых гибридомами 2E6/D2 и 6Н5/Н1, с помощью дот-блоттинга. Анти-Р антитела RSV, вырабатываемые гибридомами 2E6/D2 или 6Н5/Н1, выдерживались на протяжении 1 часа на нитроцеллюлозной мембране, содержащей следующие иммобилизированные образцы (в качестве окраски или «пятен»): MPV (1×106 БОЕ), RSV (1×106 БОЕ), BSA (1 мкг), белок Р RSV (1 мкг, 500 нг и 50 нг), а также 20 мкг экстракта клеток НЕр-2 без заражения или с заражением RSV. После выдерживания мембрану промывали и выдерживали в течение 1 часа с вторичным мышиным анти-lgG антителом, связанным с HRP белка. После выдерживания связывание моноклональных антител с антигеном определяли визуально путем захвата хемилюминесценции, полученной посредством катализа неочищенного субстрата («система обнаружения с вестерн-блоттингом и повышенной хемилюминесценцией» (Amersham ECL, Уппсала, Швеция). Определено, что антитела, вырабатываемые гибридомами 2E6/D2 или 6Н5/Н1, связываются только с пятнами, где присутствуют белок Р RSV, вирус RSV и клетки, зараженные им, что подтверждает специфичность данных антител.
Фиг. 5: Обнаружение белка Р RSV путем иммунофлуоресценции в клетках НЕр-2, зараженных RSV. Клетки НЕр-2 выращивались методом invitro до достижения соединения (70-90%) для заражения RSV в течение 48 часов. Затем их фиксировали с помощью параформальдегида и подготавливали для непрямой иммунофлуоресценции. Для этого в качестве первичного моноклонального антитела использовалось антитело, полученное из гибридомы 2Е6/D2, гибридомы 6Н5/Н1 анти-Р антитела RSVH102 (номер по каталогу Abcam #АВ94965). В качестве вторичного антитела использовалось неочищенное мышиное анти-lgG антитело, связанное с флуорофором AlexaFluor 488, дающим флуоресценцию до 519 нм (интенсивный сигнал). Ядро клетки, окрашенное флуорофором йодид TOPRO-3, дающим флуоресценцию до 661 нм (светло-серые круги, наблюдаемые в незараженных и зараженных клетках). Сильно выраженная химическая активность в цитоплазме (интенсивные обозначения в виде белых стрелок) наблюдается только в зараженных клетках при использовании любого из трех первичных антител.
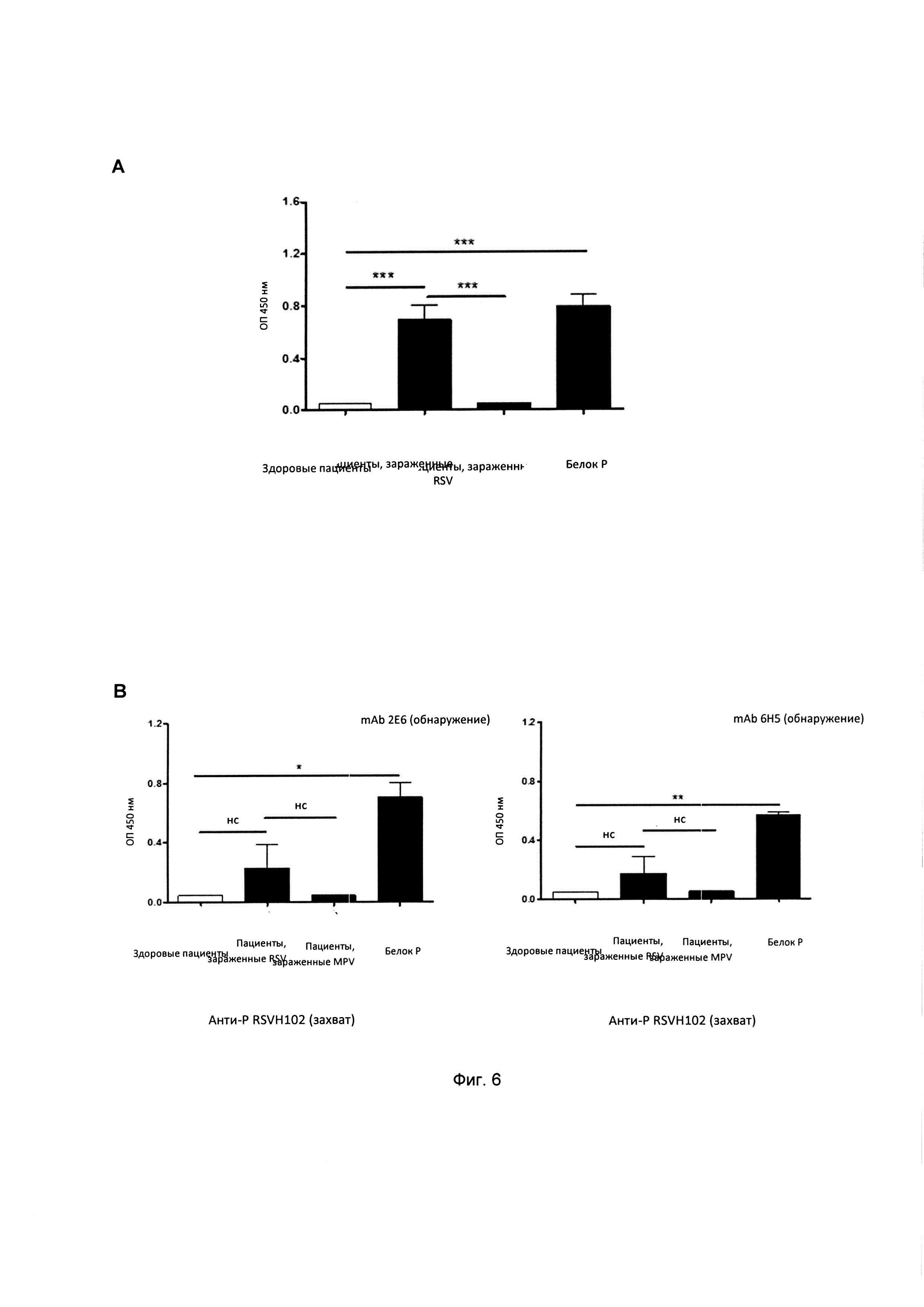
Фиг. 6: Обнаружение RSV в клинических образцах с использованием «сэндвич» - метода ELISA с применением комбинации моноклональных антител, выделяемых гибридомами 2E6/D, 6Н5/Н1, и антитела RSVH102 (номер по каталогу Abcam #АВ94965). Планшеты ELISA были активированы с помощью 170 нг антитела, выделенного гибридомой 2E6/D2 (А) или анти-Р антителом RSVH102 (номер по каталогу Abcam (В) #АВ94965), выступающим в качестве захватывающего антитела. Лунки, активированные захватывающим антителом, выдерживались в 50 мклобразцов мазков из носоглоток (HNF) пациентов с вирусными респираторными симптомами. В качестве средств негативного контроля были проанализированы образцы от здоровых пациентов 10 (А) и 3 (В). В отношении RSV были использованы образцы 20 (А) и 5 (В) от зараженных пациентов, и для метапневмовируса в качестве контроля специфичности были использованы они же. В качестве положительного контроля были включены лунки, в которые был добавлен очищенный белок Р. Для обнаружения захваченного белка антителом 2E6/D2 или неочищенным анти-Р антителом RSVH102 использовались антитела, полученные из гибридом 6Н5/Н1 (А и В) и 2E6/D2 (В), связанных ферментом пероксидазы хрена, при разбавлении в пропорции 1:2000 (75 нг на лунку). Среднее значение +/- по полученным данным значения стандартного отклонения оптической плотности при 450 нг для каждого образца (при *Р<0,05; **Р<0,001; ***Р<0,0001 и нс существенная разница отсутствует; при использовании дисперсионного анализа одного образца в сравнении пациентов, зараженных MPV, или здоровых пациентов).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Настоящее изобретение относится к двум моноклональным антителам или их фрагментам, 2E6/D2 изотипа lgG1 и 6Н5/Н1 изотипа lgG2A, которые распознают белок Р (с обозначением в качестве анти-Р антител) RSV.
Настоящее изобретение описывает два моноклональных антитела, которые распознают белок Р RSV. Как было указано, эти антитела вырабатываются гибридомами 2E6/D2 и 6Н5/Н1. Последовательности аминокислот вариабельных областей обеих цепей антител, вырабатываемых гибридомой 2E6/D2, описаны в SEQ ID №1 для тяжелой цепи и SEQ ID №2 для легкой цепи. Нуклеотидные последовательности, которые кодируют их, описаны в SEQ ID №3 и SEQ ID №4, соответственно. Аналогичным образом, последовательности аминокислот вариабельных областей обеих цепей антител, вырабатываемых гибридомой 6Н5/Н1, описаны в SEQ ID №5 для тяжелой цепи и SEQ ID №6 для легкой цепи. Нуклеотидные последовательности, которые кодируют их, описаны в SEQ ID №7 и SEQ ID №8, соответственно.
По этим вариабельным последовательностям вырабатываются антитела, которые содержат их в себе, включая только одну из вариабельных областей или комбинируя их во всех возможных вариантах. Все подобные варианты осуществления включены в подход настоящего изобретения. При этом, настоящее изобретение включает антитела, содержащие как минимум одну из последовательностей SEQ ID №1, SEQ ID №2, SEQ ID №5 и SEQ ID №6 и аналогичные последовательности со сходством или родством 90%, 95% или 99% с любой из указанных последовательностей аминокислот. Кроме того, нуклеотидные последовательности включают как минимум одну последовательность из SEQ ID №3, SEQ ID №4, SEQ ID №7 и SEQ ID №8, a также их обратнокомплементарные и аналогичные последовательности со сходством или родством 80%, 85%, 90%, 95% и 99% с любой из указанных нуклеотидных последовательностей. Более высокая степень сходства, рассматриваемая в нуклеотидной последовательности, основывается на вырождении генетического кода. Таким образом, настоящее изобретение также включает набор нуклеотидных последовательностей, кодирующих моноклональное антитело или его фрагмент, который распознает белок Р RSV.
В конкретном варианте осуществления настоящего изобретения указанные антитела или их фрагменты связаны с меткой, которая обеспечивает обнаружение, например, биотин, металлы, ферменты, белки, флуорофоры, радиоизотопы или любое другое химическое соединение.
В другом конкретном варианте осуществления настоящего изобретения указанными антителами или их фрагментами являются мышиные или гуманизированные антитела.
Как показано на фигурах, настоящие антитела не вступают в реакцию с другими белками или молекулами, присутствующими в соответствующих вирусах или образцах, взятых у пациентов с другими респираторными инфекциями, связанными с вирусом. Тем самым при использовании в способах диагностики значительно понижается вероятность ложноотрицательных результатов.
В настоящем изобретении также предлагаются способы диагностики exvivo или invitro, а также обнаружение вирусного антигена Р RSV в биологическом образце, в котором используются моноклональные антитела, вырабатываемые и выделенные гибридомами 2E6/D2 и 6Н5/Н1 в анализах на обнаружение связывания антитела с антигеном.
Способ включает контактирование биологического образца, выбранного из группы, включая: клетки invitro, зараженные RSV, ринорею, носовые смывы, фарингеальныесекреты и/или бронхиальные смывы или секреты, среди прочего, с моноклональным антителом к RSV или его фрагменту, выделенным гибридомами 2E6/D2 и 6Н5/Н1, а затем обнаружение связывания антитела с антигеном с выбранным типом анализа: ELISA, флуоресцентная микроскопия, иммуноблотирование, иммунофлуоресценция, иммуногистохимия, иммунохроматография, проточная цитометрия, клеточный сортер, иммунопреципитация и/или вестерн-блоттинг.
Кроме того, способ по настоящему изобретению включает антитела или их фрагменты, вырабатываемые и/или выделяемые вышеуказанными клеточными линиями гибридомы, связанными на любой твердой подложке, например, нитроцеллюлоза, найлоновая мембрана, магнитные микроносители, флуоресцентные гранулы или прочая подложка. В другом конкретном варианте осуществления настоящего изобретения антитела или их фрагменты, используемые в способе, связаны с меткой, которая обеспечивает обнаружение, например, биотин, металлы, ферменты, белки, флуорофоры, радиоизотопы или любое другое химическое соединение.
Настоящее изобретение также описывает набор для удержания RSV, включая как минимум одно антитело, вырабатываемое указанными гибридомами. В конкретном варианте осуществления настоящего изобретения антитела или их фрагменты, вырабатываемые и/или выделяемые указанными, используемыми в наборах клеточными линиями гибридом, связаны с любой твердой подложкой, например, нитроцеллюлоза, найлоновая мембрана, магнитные микроносители, флуоресцентные гранулы или прочая подложка. Кроме того, в конкретном варианте осуществления настоящего изобретения антитела или их фрагменты, используемые в наборе, связаны с меткой, которая обеспечивает обнаружение, например, биотин, металлы, ферменты, белки, флуорофоры, радиоизотопы или любое другое химическое соединение.
В другом конкретном варианте осуществления настоящего изобретения диагностический набор предусматривает иммунохроматографический тест, люминесцентный анализ, проточную цитометрию, иммунофлуоресценцию, радиоиммуноанализ, вестерн-блоттинг, дот-блоттинг, ELISA, иммунодиффузию или иммунопреципитацию. Таким образом, настоящее изобретение также предусматривает антитела, которые распознают белок Р, связанный с молекулами или субстратами или метками, отличными от антитела, выступающими как часть способа обнаружения, анализа и/или диагностики в биологических образцах.
Для демонстрации разных вариантов применения моноклональных антител по настоящему изобретению ниже приведены примеры.
ПРИМЕРЫ ПРИМЕНЕНИЯ
Пример 1: Получение очищенного белка Р RSV.
Для получения очищенного белка Р RSV была предусмотрена стратегия экспрессии гетерологичной формы (рекомбинант) в бактерии Escherichiacoli BL21. Для этого было предусмотрено извлечение РНК из культур клеток НЕр-2, зараженных RSV, а ген, который кодирует белок Р, прошел амплификацию PCR и клонировался в бактериальном экспрессирующем векторе (pET15b), который позволил контролировать экспрессию генов, клонированных с использованием молекулы эвокаторов Изопропил β-D-1-тиогалактопиранозид (IPTG). В качестве стратегии очистки рекомбинантных белков используемый экспрессирующий вектор имеет вставку, которая кодирует шесть последовательных гистидинов, при этом, при сверхэкспрессии белков, они выражаются в виде С-концевой области 6 последовательностей гистидинов. Преимущество использования указанного типа энергии заключается в том, что белок приобретает характерный электрический заряд, который обеспечил очистку посредством аффинной хроматографии по соответствующему уровню рН. Очистка рекомбинантных белков с гистидиновыми хвостами была обеспечена путем десорбции с буферным раствором, который содержит имидазол, аналогичный гистидину, который вступает в конфликт с белками по участкам связывания в колонке со смолой, заполненной Ni+.
В заключение очищенные образцы были проанализированы при помощи гелей SDS-PAGE.
Пример 2: Выработка гибридом, продукта слияния клона лимфоцита В и опухолевой плазматической клетки.
Выработка гибридом была обеспечена посредством иммунизации мышей BALB/c с 1 мг антигена (очищенный рекомбинантный белок Р RSV, эмульгированный в адъюванте Фрейнда) с чистотой более 50%. После иммунизации была выбрана мышь, у которой в сыворотке были обнаружены антитела высшего порядка, для нее была предусмотрена другая бустер-инъекция. По истечении трех дней лимфоциты селезенки были изолированы для обеспечения соматического слияния с клетками линии клеток миеломы без выделения NSO/2. Выработанные гибридомы были отсеяны на 96-луночные планшеты в селективной среде, содержащей гипоксантин, аминоптерин и тимидин (HAT). По истечении 10 дней посредством ELISA была проведена оценка супернатанта жизнеспособных гибридом для обнаружения антител против антигена, используемого для иммунизации. Положительные гибридомы наращивались на 24-луночных планшетах для генерирования большего объема супернатантов, которые использовались позже для проведения анализов характеристик (специфичность, чувствительность, эффективность). В заключение гибридомы с более высокой степенью специфичности клонировались за счет предельного разбавления, т.е. до получения аликвоты, содержащей одну клетку, было предусмотрено последующее разбавление суспензии клеток. Позже у мышей были получены асцитные жидкости и был определен субкласс каждого моноклонального антитела. Концентрация образованных моноклональных антител была определена посредством ELISA с выдержкой антител при различных концентрациях и с использованием мышиного моноклонального антитела анти-Мелан A (SantaCruzBiotechnology, Даллас, Техас) для подготовки стандартной кривой.
Пример 3: Определение нуклеотидной последовательности, кодирующей легкие (VL) и тяжелые (VH) цепи вариабельной области анти-Р антитела RSV, выделяемого гибридомой 2E6/D2 и анти-р антитела RSV, выделяемого гибридомой 6Н5/Н1.
Следующий протокол использовался для гибридом 2E6/D2 и 6Н5/Н1 отдельно. Гибридома была выращена из культуральной среды DMEM с высоким содержанием глюкозы, дополненной бикарбонатом натрия в концентрации 3,7 г/л и 10% эмбриональной телячьей сывороткипри 37°С, 10% CO2, при плотности клеток 700000 клеток/мл. При обработке соединением Тризол (Invitrogen) была получена РНК с общей концентрацией 3,5×106 клеток. Для получения кДНК посредством реакции обратной транскрипции с использованием набора Impron II (Promega) было использовано 0,5 мкг РНК. Вариабельная область генов, кодирующих каппа- и лямбда-цепи иммуноглобулина, была амплифицирована посредством PCR. Для этого были использованы универсальные праймеры из набора Novagenlg-PrimerSet (№69831-3 по каталогу) согласно инструкциям производителя.
Вариабельная область легкой цепи была амплифицированапраймерами MulgkVL5'-В: 5'ACTAGTCGACATGGAGWCAGACACACTSCTGYTATGGGT3' (SEQ ID №:10), а вариабельная область тяжелой цепи была амплифицированапраймерами MulgVH5'-А: 5'GGGAATTCATGRASTTSKGGYTMARCTKGRTTT3' (SEQ ID №:11) и MulgVH5'-F: 5'ACTAGTCGACATGAACTTYGGGYTSAGMTTGRTTT3' (SEQ ID №:12). Продукты PCR были клонированы в клонирующем векторе рТОРО-ТА (Invitrogen) согласно инструкциям производителя и секвенированы службой секвенирования Папского Католического университета Чили в секвенаторе ABI prism 3130xl (AppliedBiosystem). Расшифрованные последовательности аминокислот SEQ ID №:1 и SEQ ID №:2 для гибридомы 2E6/D2 и SEQ ID №:5 и SEQ ID №:6 для гибридомы 6Н5/Н1) были получены с помощью биоинформационной программы Vector NTI (Invitrogen).
Пример 4: Анализ на обнаружение антигенов RSV, определение специфичности моноклональных анти-Р антител RSV для очищенных антигенов RSV, при помощи непрямого анализа ELISA.
Целью данного анализа является демонстрация специфичности белка Р RSV антител, выработанных гибридомами 2E6/D2 и 6Н5/Н1. Обнаружение антигена было осуществлено при помощи непрямого метода ELISA, в котором планшет ELISA был активирован 50 нг очищенного антигена в течение 1 часа при 37°С. Аналогичным образом, планшет был активирован бляшкообразующими единицами (БОЕ) RSV в концентрации 1×106. При аналогичных условиях, в которых выдерживался RSV, в качестве отрицательного контроля был добавлен метопневмовирус (MPV); в отдельную лунку было добавлено 50 нг BSA-белка. Позже планшет дважды промывали с помощью фосфатно-солевого буфера (PBS)/0,05% Tween. Затем планшет блокировали в течение 2 часов при 37°С с помощью 10% FBS/PBS. Позже смывы повторялись, и каждое из антител (2E6/D2 и 6Н5/Н1) выдерживали в окончательной концентрации 3,4 мкг/мл, разбавляя в PBS/10% FBS в течение 1 часа при комнатной температуре (каждое антитело в отдельном планшете). Контрольный анализ проводили в другом планшете в тех же условиях с помощью моноклонального антитела, которое распознает белок Р RSV (антитело RSVH102 к фосфорбелку респираторно-синцатиального вируса, номер по каталогу № АВ94965, Abcam) в концентрации 3,4 мкг/мл. По окончании выдерживания смывы повторили, а вторичное мышиное анти-lgG антитело, помеченное ферментом пероксидазы хрена (фермент пероксидазы хрена, HRP) в разбавлении 1:2000 (25 нг на ячейку) в 10% FBS/PBS, добавляли в каждую ячейку в течение 1 часа при комнатной температуре. В заключение, проводились смывы, и было добавлено 50 мкл цитратного буфера/тетраметилбензидина (ТМВ, 3-3'-5-5'-тетраметилбензидин, 1 мг/мл, BectonDickinson). 50 мкл H2SO4 2N добавили, чтобы остановить реакцию, и результат считывали в считывающем устройстве для планшетов ELISA при 450 нм. Для определения того, была ли реакция вторичного антитела специфичной для распознавания первичного антитела, и не был ли полученный сигнал вызван неспецифическим связыванием вторичного антитела с вирусным антигеном, контроль проводили только с применением вторичного антитела без первичного антитела и образца. Другой контроль для определения того, была ли реакция первичного антитела специфичной для антигена, заключался в использовании антител на планшете ELISA, который не был активирован антигеном (ячейка без антигена), либо с помощью антител на планшете ELISA, имеющем 50 нг BSA-белка или другой вирус (MPV). Результаты свидетельствуют о том, что моноклональные антитела по настоящему изобретению способны точно распознавать 50 нг очищенного антигена, так как они не распознают BSA-белок или белки из другого соответствующего вируса (фиг. 1А и 1В). С другой стороны, было определено, что неочищенное антитело RSVH102 (фиг. 1С), использовавшееся во время анализа в качестве контроля, было специфичным для обнаружения, как вируса, так и белка Р рекомбенированного RSV.
Пример 5: Анализ для определения чувствительности моноклональных антител для обнаружения вирусного антигена.
Анализ проводился для определения максимального уровня разбавления белка и вируса моноклональных анти-Р антител RSV изгибридом 2E6/D2 и 6Н5/Н1 посредством непрямого теста ELISA. С этой целью был использован метод, аналогичный описанному в примере 4. Планшет активировали путем 11 последовательных разбавлений 1:2 белка Р RSV, начиная с 50 нг очищенного антигена. Для вируса планшет активировали путем последовательных разбавлений 1:2, начиная с 1×105 БОЕ вируса. Анти-Р антитела 2E6/D2 или 6Н5/Н1 использовались в концентрации 3,4 мкг/мл (170 нг/ячейка) с разбавлением в 10% FBS/PBS. Позже использовалось мышиное анти-lgG детекторное антитело в разбавлении 1:2000 (25 нг/ячейка). Результаты показали, что анти-Р антитела 2E6/D2 способны распознавать до 40 пикограмм (пг) белка Р RSV. Анти-Р антитело из гибридомы 6Н5/Н1 было более чувствительным и позволяло производить обнаружение до последнего разбавления белка Р RSV с большей интенсивностью в вызванном сигнале (фиг. 2А). Анти-Р антитело RSVH102 (№ АВ94965, Abcam) также было способным к распознаванию всех разбавлений белка Р RSV, с меньшей эффективностью, чем анти-Р антитела из гибридомы 6Н5/Н1.
С учетом чувствительности антител, выраженной их способностью обнаруживать RSV при сильном разбавлении, можно определить, что анти-Р антитела из гибридомы 2E6/D2 могут обнаруживать все разбавления вируса, как и антитело из гибридомы 6Н5/Н1, что эквивалентно приблизительно 390 вирусным частицам. Два моноклональных антитела являются более эффективными, чем неочищенное анти-Р антитело RSV, которое производит обнаружение до последнего разбавления 1:40 (фиг. 2В).
Все группы контроля, которые могли исключить неспецифические реакции антител, были включены во все анализы и содержали все компоненты анализов, кроме образца (белок Р RSV или вирус).
Пример 6: Анализ для обнаружения эффективности моноклональных антител для обнаружения вирусного антигена.
Анализ проводился для определения максимального уровня разбавления моноклональных анти-Р антител RSV изгибридом 2E6/D2 и 6Н5/Н1, которые обеспечивают возможность обнаружения вирусных антигенов при помощи ELISA. С этой целью использовался непрямой метод ELISA, аналогичный описанному в примере 6. Ячейку активировали с помощью 50 нг очищенного антигена, а анти-Р антитела 2E6/D2 или 6Н5/Н1 использовали в разбавлениях 1:2, начиная с рабочей концентрации (3,4 мкг/мл) до 11-го разбавления в 10% FBS/PBS. На фиг. 3 видно, что во всех разбавлениях, которые использовались во время анализа, анти-Р антитела 2E6/D2 и 6Н5/Н1 способны обнаружить белок Р RSV. Анти-Р антитело RSVH102 (номер по каталогу № АВ94965, Abcam) также было способным к распознанию белка Р RSV во всех разбавлениях, но оно было менее эффективным, чем анти-Р антитело 6Н5/Н1.
При негативном контроле, входящем в состав данного анализа, использовалась одна ячейка без образца (белок Р); ее блокировали 10% FBS/PBS; первичное антитело (анти-Р 2E6/D2 или анти-Р 6Н5/Н1) не добавлялось и содержало только мышиные анти-lgG антитела, связанные с HRP.
Пример 7: Клиническая диагностика образцов, взятых у пациентов, зараженных RSV, с помощью моноклональных анти-Р антител RSV и «сэндвич» - метода ELISA.
Из-за дефицита доступности и низкой концентрации вирусных белков в клинических образцах, полученных из мазков из носоглотки, было необходимо изменить способ обнаружения и использовать «сэндвич» - метод ELISA с применением анти-Р антитела из гибридомы 2Е6/D2 в качестве захватывающего антитела или анти-Р антитела RSVH102 (номер по каталогу № АВ94965, Abcam). В качестве антитела обнаружения использовались антитела, выделяемые клонами анти-Р 6Н5/Н1 или клонами анти-Р 2E6/D2, связанные с HRP. В ходе анализа, ячейки планшета ELISA активировались 3,4 мкг/мл (170 нг/ячейка) анти-Р антитела из гибридомы 2E6/D2 или анти-Р антитела RSV RSVH102 (номер по каталогу № АВ94965, Abcam), разбавленной в PBS, в течение 1 часа при 37°С. Было выполнено 2 смыва с помощью PBS 0,05% Tween 20, а затем планшет блокировался 200 мкл 10% FBS/PBS в течение 2 часов при 37°С.Его промывали повторно и выдерживали при 4°С на протяжении ночи, и каждая ячейка содержала 50 мкл носоглоточных аспиратов, взятых у пациентов, зараженных RSV, по способу диагностики «Набор для скрининга и определения респираторных вирусов D3 Ultra DFA компании DHI (DiagnosticsHibryds), США», который обычно называют «вирусной панелью», которые обрабатывались, как описано ниже*. В качестве групп контроля были включены: 1) контроль специфичности (50 мкл образцов, взятых у пациентов с MPV при помощи вирусной панели), 2) положительный контроль (50 нг рекомбенантного белка Р RSV) и 3) негативный контроль, соответствующий образцам, взятым у здоровых пациентов (негативные реакции для вируса при помощи вирусной панели). На следующий день выполнялись смывы, и каждая ячейка выдерживалась в течение 1 часа при 25°С с 50 мкл анти-Р антитела из гибридомы 6Н5/Н1 или 2E6/D2, связанного с HRP. Планшет промывали еще два раза, в него добавляли 50 мкл раствора ТМВ, и выдерживали в течение 10-15 минут в темноте. Реакцию останавливали с помощью 50 мкл H2SO4 2N. Считывание планшета производилось в считывающем устройстве для планшетов ELISA Epoch, сертифицированном для клинической диагностики. Полученные результаты данного анализа показаны на фиг.6, где видно, что «сэндвич» - метод ELISA, в котором антитело из гибридомы 2E6/D2 используется в качестве захватывающего антитела, а антитело из гибридомы 6H5/H1-HRP - в качестве детекторного антитела, позволяет обнаружить антиген в образцах, взятых у пациентов, зараженных RSV (фиг. 6А), которые ранее были определены как положительные путем прямой иммунофлуоресценции в сертифицированной клинической лаборатории посредством вирусной панели. Количество пациентов, включенных в анализ, составляло 20, 17 из которых имели положительные результаты ELISA с оптической плотностью (OD) выше 0,1. Данный анализ показывает универсальность антител из гибридом 2E6/D2 и 6Н5/Н1, поскольку они способны одновременно устанавливаться связь с антигеном, не вступая в конфликт и не препятствуя друг другу, а также обеспечивая захват и последующее обнаружение белка Р в образцах, взятых у пациентов. На фиг. 6В показаны результаты, полученные при помощи неочищенного захватывающего антитела и двух анти-Р клонов 6Н5/Н1 и 2E6/D2 детекторных антител. Результаты показывают, что из 5 пациентов, зараженных RSV, только 1 был обнаружен при помощи «сэндвич» - метода ELISA, как для комбинации анти-Р антител RSV RSVH102 (номер по каталогу № АВ94965, Abeam) захвата с анти-Р клоном 6Н5/Н1, так и с клоном 2E6/D2. Эти результаты свидетельствуют о высокой эффективности моноклональных антител по настоящему изобретению при обнаружении вируса в клинических образцах по сравнению с анти-Р антителом RSV RSVH102 (номер по каталогу № АВ94965, Abcam).
*: Обработка клинических образцов. Образцы, используемые для анализа, были получены из мазков из носоглотки, содержащихся в универсальной транспортной среде. Образцы высушивался в центробежной сушилке на скорости 2000 об/мин в течение 10 минут при 4°С. Впоследствии супернатант (SN1) отделяли от сгустка; последний выдерживали в 100 мкл буфера RIPA (50 ммоль трис-HClpH 8,0, 150 ммоль MaCl, 1% NP-40, 0,5% дезоксихолата натрия, 0,1% SDS и смесь ингибиторов протеазы) в течение 15 минут при 4°С, с перемешиванием вихревым способом каждые 5 минут. Затем его высушивали в центробежной сушилке на скорости 2000 об/мин в течение 10 минут при 4°С. В конечном итоге, полученный супернатант (SN2) собирали и смешивали с SN1.
Пример 8: Анализ специфичности моноклональных анти-Р антител RSV для очищенных антигенов RSV при помощи дот-блот анализа.
Целью данного анализа является подтверждение специфичности белка Р RSV антител, выработанных гибридомами 2E6/D2 и 6Н5/Н1, используя метод иммуноблотирования. Обнаружение антигена выполнялось при помощи методики дот-блоттинга, в которой нитроцеллюлозная мембрана используется в качестве твердой подложки для иммобилизации антигена, присутствующего в одной капле суспензии. С этой целью на нитроцеллюлозную мембрану было нанесено 20 мкл, содержащих: 1×1066 БОЕ MPV, 1×106 БОЕ RSV, очищенный белок Р RSV (1 мкг, 500 нг и 50 нг), 20 мкг экстракта клеток НЕр-2 с заражением RSV и 20 мкг экстракта клеток НЕр-2 без заражения. В качестве негативного контроля наносилось 500 нг BSA, содержащихся в 20 мкл. Растворы, нанесенные на мембрану, высушивали воздухом на протяжении 15 минут. Затем мембрану блокировали с помощью 5% BSA в PBS, содержащем 0,05% Tween-20, в течение 1 ч при 25°С. Мембраны выдерживали с 3,4 мкг/мл моноклонального анти-Р антитела из гибридомы 2Е6/D2 или гибридомы 6Н5/Н1 в блокирующем растворе в течение 1 ч при 25°С. Излишек антитела, не связанного с антигеном, удаляли путем трех смывов с PBS 0,05% Tween-20 при 25°С. Обнаружение антител, связанных с антигеном, производилось при помощи мышиного анти-lgG антитела, связанного с HRP (Invitrogen, LifeTechnologies №62-6520). Их выдерживали в течение 1 ч в блокирующем растворе при 25°С для последующего удаления излишка несвязанного антитела путем трех смывов с PBS 0,05% Tween-20 при 25°С. Определение связи моноклональных антител с антигеном производилось путем захвата хемилюминесценции, полученной посредством катализа неочищенного субстрата («система обнаружения с вестерн-блоттингом и повышенной хемилюминесценцией» Amersham ECL, Уппсала, Швеция) при содействии фермента HRP, связанного с мышиным анти-lgG антителом. Захват хемилюминесценции выполняли посредством системы фотодокументирования MyECL (ThermoFisher). На фиг. 4 видно, что антитела из гибридом 2E6/D2 и 6Н5/Н1 связываются только с «пятнами», содержащими RSV или белок Р, и не связываются неспецифически с «пятнами», содержащими посторонние белки, другие вирусы или незараженные клетки.
Пример 9: Обнаружение заражения RSV в клетках НЕр-2 посредством иммунофлуоресценции, при помощи моноклональных анти-Р антител RSV.
Данный анализ выполнялся для амплификации спектра методов, которые позволяют обнаружить заражения RSV благодаря раскрытому изобретению. Был проведен анализ с флуоресцентной микроскопией, в котором зараженные или незараженные RSV клетки НЕр-2 выдерживались с моноклональными анти-Р антителами RSV, полученными из гибридом 2E6/D2 или 6Н5/Н1. Используемый протокол включал следующее: клетки фиксировали с помощью 4% параформальдегида, разбавленного в PBS, в течение 10 минут при 25°С. Затем клетки промывали PBS и пермеабилизировали с помощью 0,2% сапонина, разбавленного в 10% FBS/PBS, в течение 30 минут при 25°С. Моноклональные антитела, полученные из гибридом 2E6/D2 или 6Н5/Н1, добавляли в концентрации 3,4 мкг/мл, разбавляя в 10% FBS/PBS в течение 1 часа при 25°С. Затем были проведены два смыва с помощью PBS, а вторичное мышиное анти-lgG антитело, связанное с флуорофором AlexaFluor 488 (LifeTechnologies), добавляли в разбавлении 1 к 200 в 10% FBS/PBS в течение 1 часа при 25°С в темноте. Смывы повторяли, а ядра с йодидом TOPRO-3 642/661 (Invitrogen, № Т3605) окрашивали в разбавлении 1:5000 в течение 15 минут при 25°С, в темноте. В заключение, делали промывку PBS и устанавливали покровное стекло для последующего наблюдения в эпифлуоресцентном микроскопе. Полученные результаты демонстрируют, что составляющие антитела по настоящему изобретению также полезны для распознавания специфически зараженных клеток путем иммунофлуоресценции без неспецифического связывания с незараженными клетками (фиг. 5).
Примеры, описанные в настоящем документе, демонстрируют специфичность, эффективность, чувствительность и универсальность, которые имеют данные моноклональные анти-Р антитела RSV, выделяемые клеточными линиями гибридом 2E6/D2 и 6Н5/Н1. В представленных здесь примерах приведены некоторые варианты использования моноклональных анти-Р антител RSV, но они ни в коем случае не ограничивают объем настоящего изобретения.