Результат интеллектуальной деятельности: ПОЛИПЕПТИД ДЛЯ ИНГИБИРОВАНИЯ МИГРАЦИИ И ИНВАЗИИ ПЛОСКОКЛЕТОЧНОГО РАКА ПОЛОСТИ РТА
Вид РИД
Изобретение
Изобретение относится к медицине и молекулярной биофармакологии и может быть использовано в качестве средства для ингибирования плоскоклеточного рака полости рта.
Известен способ ингибирования плоскоклеточного рака полости рта с помощью комбинированного применения препарата Cetuximab, моноклонального антитела к рецепторам эпидермального фактора роста, и циклического пентапептида Cilengitide (EMD121974), селективного ингибитора αvβ3 и αvβ5 интегринов, содержащего в своей структуре аминокислотную последовательность Arg-Gly-Asp (RGD) [Wichmann G. et al. Cilengitide and cetuximab reduce cytokine production and colony formation of head and neck squamous cell carcinoma cell ex vivo. Anticancer research, T. 37, №2, C. 521-527 (2017).]. Показан также способ ингибирования роста опухолей головного мозга с помощью циклического RGD пентапептида EMD 121974, цикло(Arg-Gly-Asp-D-Phe-[N-Me]-Val), за счет прямого антионкогенного эффекта, независимого от подавления ангиогенеза [патент RU 2255765, 2000 г.].
Известен природный ингибитор ангиогенеза эндостатин, обладающий способностью снижать прогрессию злокачественных новообразований различного происхождения путем подавления неоангиогенеза, опухолевого роста и метастазирования [ M.S. et al. Endostatin: an endogenous inhibitor of angiogenesis and tumor growth. Cell, T. 88, №2, C. 277-285 (1997).]. В основе антиканцерогенного механизма эндостатина лежит преимущественно его способность ингибировать пролиферацию и миграцию эндотелиальных клеток кровеносных сосудов путем связывания с α5β1 интегринами RGD-независимым образом [Rehn М. et al. Interaction of endostatin with integrins implicated in angiogenesis. Proceedings of the National Academy of Sciences, T. 98, №3, C. 1024-1029 (2001)]. Так, известно применение слитого белка, состоящего из ангиостатина и эндостатина или их биологически активных фрагментов, которые ковалентно связаны друг с другом и с RGD-фрагментом, и обладающего антиангиогенной активностью [патент RU 2372354, 2009 г.]. Однако данных о прямом противоопухолевом эффекте подобного слитого белка не зарегистрировано. Несмотря на безусловные преимущества эндостатина (минимальная токсичность и отсутствие химиорезистентности опухолей к данному веществу), монотерапия с использованием ингибиторов ангиогенеза не способна оказывать должное противоопухолевое воздействие непосредственно на раковые клетки. Кроме того, характерные для белковых макромолекул большой молекулярный вес, сложная структурная организация, трудность проникновения в клетки, высокая иммуногенность и сложность синтеза ввиду значительной молекулярной массы также ограничивают практическое применение эндостатина. В этой связи обращает на себя внимание тот факт, что основной терапевтический потенциал эндостатина реализуется за счет фрагмента из 27 аминокислотных остатков N-концевой последовательности, обладающего противоопухолевой активностью, свойственной полноразмерной молекуле белка [Sjin R.M.T.T. et al. А 27-amino-acid synthetic peptide corresponding to the NH2-terminal zinc-binding domain of endostatin is responsible for its antitumor activity. Cancer research, т. 65, №9, с. 3656-3663 (2005).].
M.S. et al. Endostatin: an endogenous inhibitor of angiogenesis and tumor growth. Cell, T. 88, №2, C. 277-285 (1997).]. В основе антиканцерогенного механизма эндостатина лежит преимущественно его способность ингибировать пролиферацию и миграцию эндотелиальных клеток кровеносных сосудов путем связывания с α5β1 интегринами RGD-независимым образом [Rehn М. et al. Interaction of endostatin with integrins implicated in angiogenesis. Proceedings of the National Academy of Sciences, T. 98, №3, C. 1024-1029 (2001)]. Так, известно применение слитого белка, состоящего из ангиостатина и эндостатина или их биологически активных фрагментов, которые ковалентно связаны друг с другом и с RGD-фрагментом, и обладающего антиангиогенной активностью [патент RU 2372354, 2009 г.]. Однако данных о прямом противоопухолевом эффекте подобного слитого белка не зарегистрировано. Несмотря на безусловные преимущества эндостатина (минимальная токсичность и отсутствие химиорезистентности опухолей к данному веществу), монотерапия с использованием ингибиторов ангиогенеза не способна оказывать должное противоопухолевое воздействие непосредственно на раковые клетки. Кроме того, характерные для белковых макромолекул большой молекулярный вес, сложная структурная организация, трудность проникновения в клетки, высокая иммуногенность и сложность синтеза ввиду значительной молекулярной массы также ограничивают практическое применение эндостатина. В этой связи обращает на себя внимание тот факт, что основной терапевтический потенциал эндостатина реализуется за счет фрагмента из 27 аминокислотных остатков N-концевой последовательности, обладающего противоопухолевой активностью, свойственной полноразмерной молекуле белка [Sjin R.M.T.T. et al. А 27-amino-acid synthetic peptide corresponding to the NH2-terminal zinc-binding domain of endostatin is responsible for its antitumor activity. Cancer research, т. 65, №9, с. 3656-3663 (2005).].
Наиболее близким аналогом изобретения является peptide 30, соответствующий 1-30 последовательности аминокислот NH2-конца эндостатина, в которой RGIRGA аминокислоты в положении 25-30 заменены на аминокислоты RGDRGD [Li S. et al. RGD-modified endostatin peptide 30 derived from endostatin suppresses invasion and migration of HepG2 through the pathway. Cancer Biotherapy and Radiopharmaceuticals, т. 26, №5, с. 529-538 (2011).]. Показана способность peptide 30 подавлять адгезию, миграцию и инвазию клеток гепатоцеллюлярной карциномы путем ингибирования экспрессии матриксных металлопротеаз и циклооксигеназы-2.
Задачей настоящего изобретения является получение средства для ингибирования плоскоклеточного рака полости рта.
Технический результат - повышение противоопухолевой эффективности белка эндостатина в отношении плоскоклеточного рака полости рта путем интеграции гексапептида RGDRGD с фрагментом NH2-конца эндостатина (с 1 по 24 аминокислотные остатки).
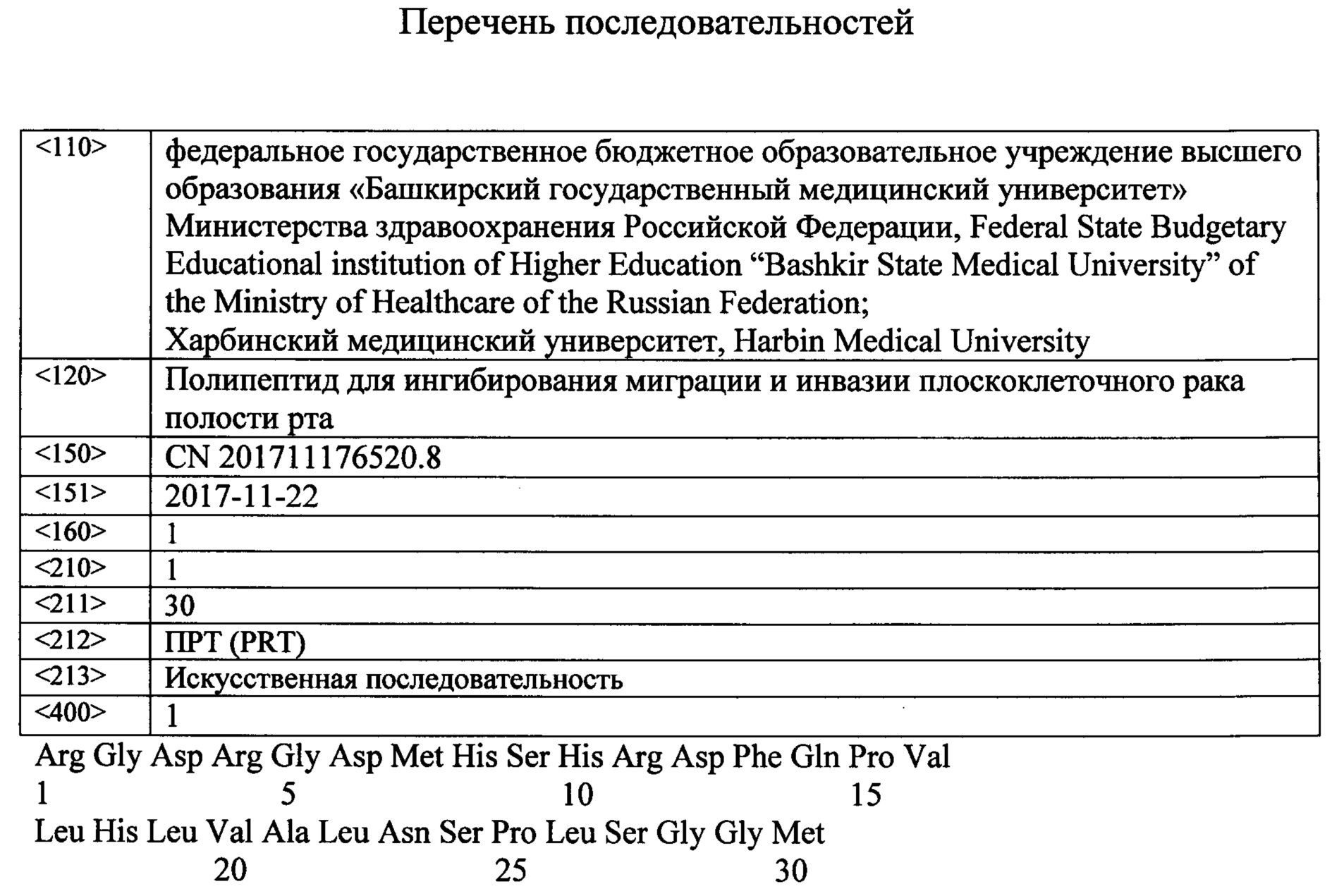
Сущность изобретения: полипептид для подавления жизнеспособности, миграции и инвазии клеток плоскоклеточного рака полости рта, снижения экспрессии онкогенов ITGAV, BCL2 и ММР7, имеющий аминокислотную последовательность, соответствующую SEQ ID NO:1.
Известно применение полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, в качестве антиангиогенного и противоопухолевого средства в отношении клеток рака желудка и шейки матки [патент CN 104530199А от 22.04.2015]. Кроме того, продемонстрировано ингибирующее влияние полипептида на метастазирование колоректальной карциномы in vitro и in vivo [Yu S. et al. PEP06 polypeptide 30 exerts antitumour effect in colorectal carcinoma via inhibiting epithelial mesenchymal transition. British journal of pharmacology, т. 175, №11, с. 3111-3130 (2018).].
В доступной научно-медицинской и патентной литературе сведений об использовании полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1 в качестве средства для ингибирования плоскоклеточного рака полости рта не обнаружено.
Эффекты полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1 на жизнеспособность, миграцию и инвазию клеток плоскоклеточного рака полости рта изучали в ходе MTS анализа, эксперимента «заживления раны» и Transwell инвазии соответственно. Экспрессию генов оценивали с помощью полимеразной цепной реакции в реальном времени.
Краткое описание графических материалов
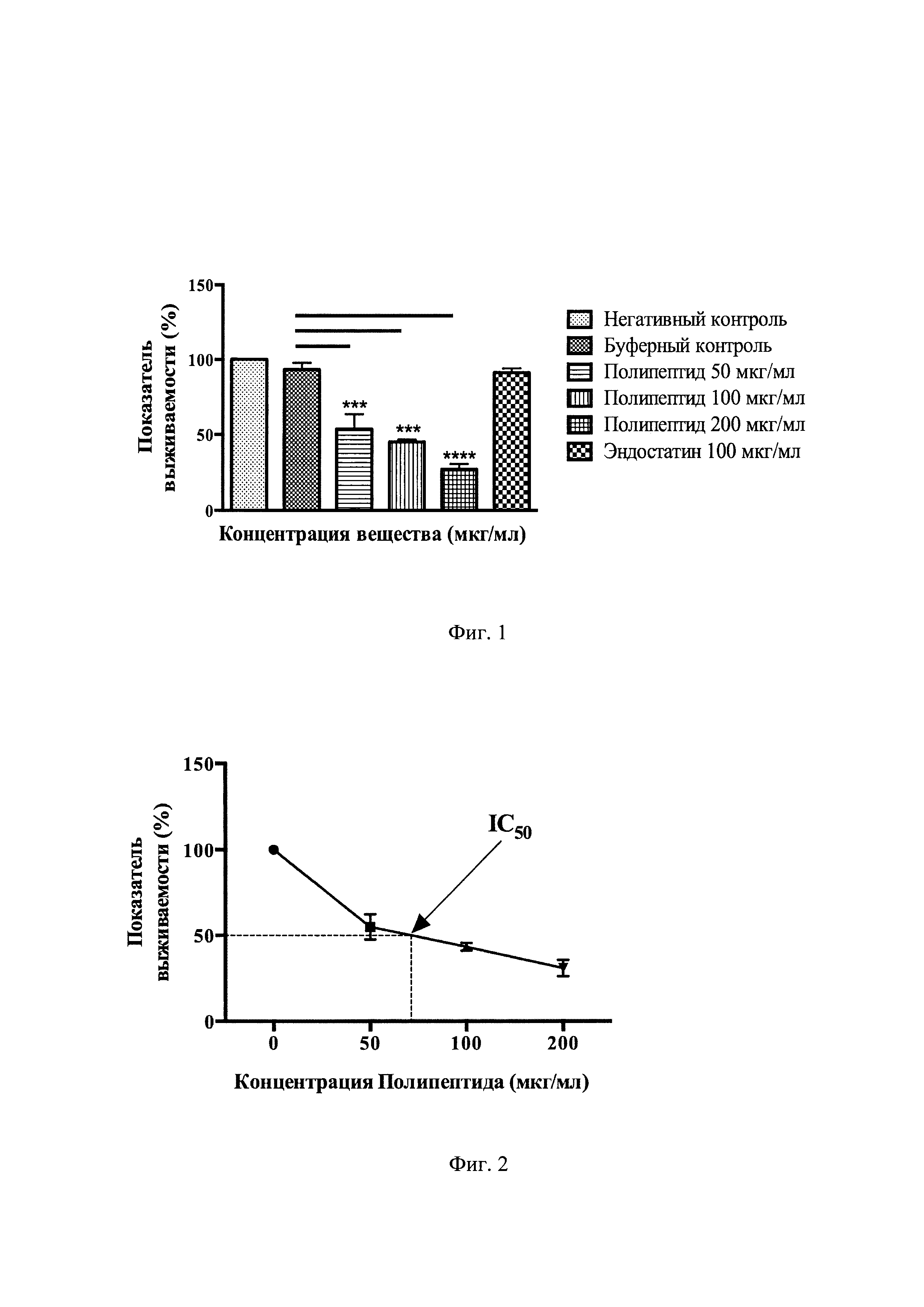
На Фиг. 1 представлен график, показывающий выживаемость CAL 27 клеток (% жизнеспособных клеток в каждой группе, нормированный к группе негативного контроля) при инкубации с указанными веществами в течение 48 часов. ***P<0,001, ****P<0,0001 по сравнению с буферным контролем.
На Фиг. 2 представлен график, демонстрирующий зависимость показателя выживаемости клеток (% жизнеспособных клеток в каждой группе, нормированный к группе негативного контроля) от концентрации полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1 (мкг/мл) при инкубации в течение 48 часов с указанием IC50.
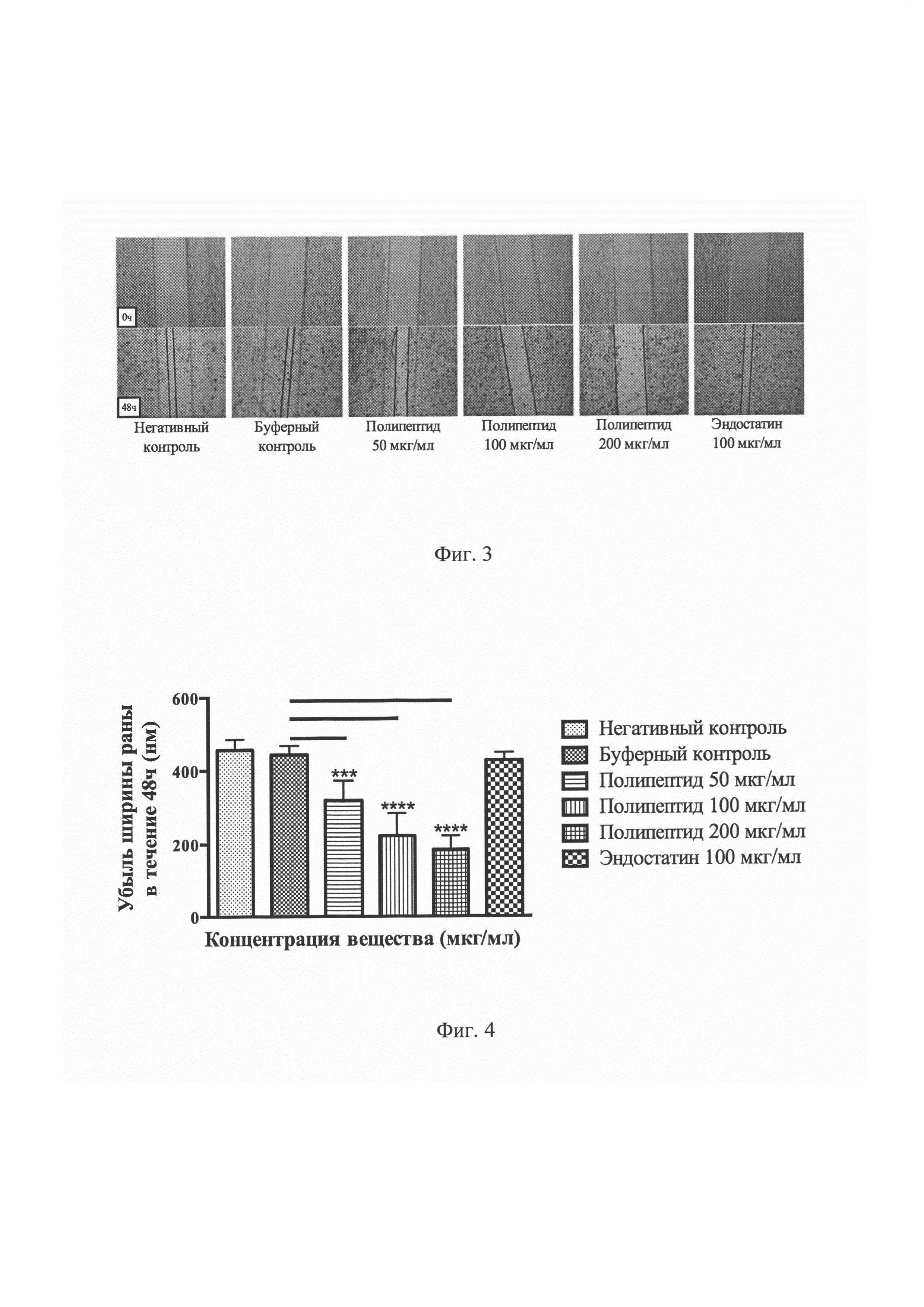
На Фиг. 3 представлены результаты нативной фотомикроскопии, показывающие динамику закрытия экспериментальных царапин-ран на клеточном монослое за счет миграции опухолевых клеток в каждой группе в течение 48 часов.
На Фиг. 4 представлен график, демонстрирующий убыль ширины раны (нм) за счет миграции опухолевых клеток в клеточном монослое в каждой из указанных групп в течение 48 часов. ***P<0,001, ****P<0,0001 по сравнению с буферным контролем.
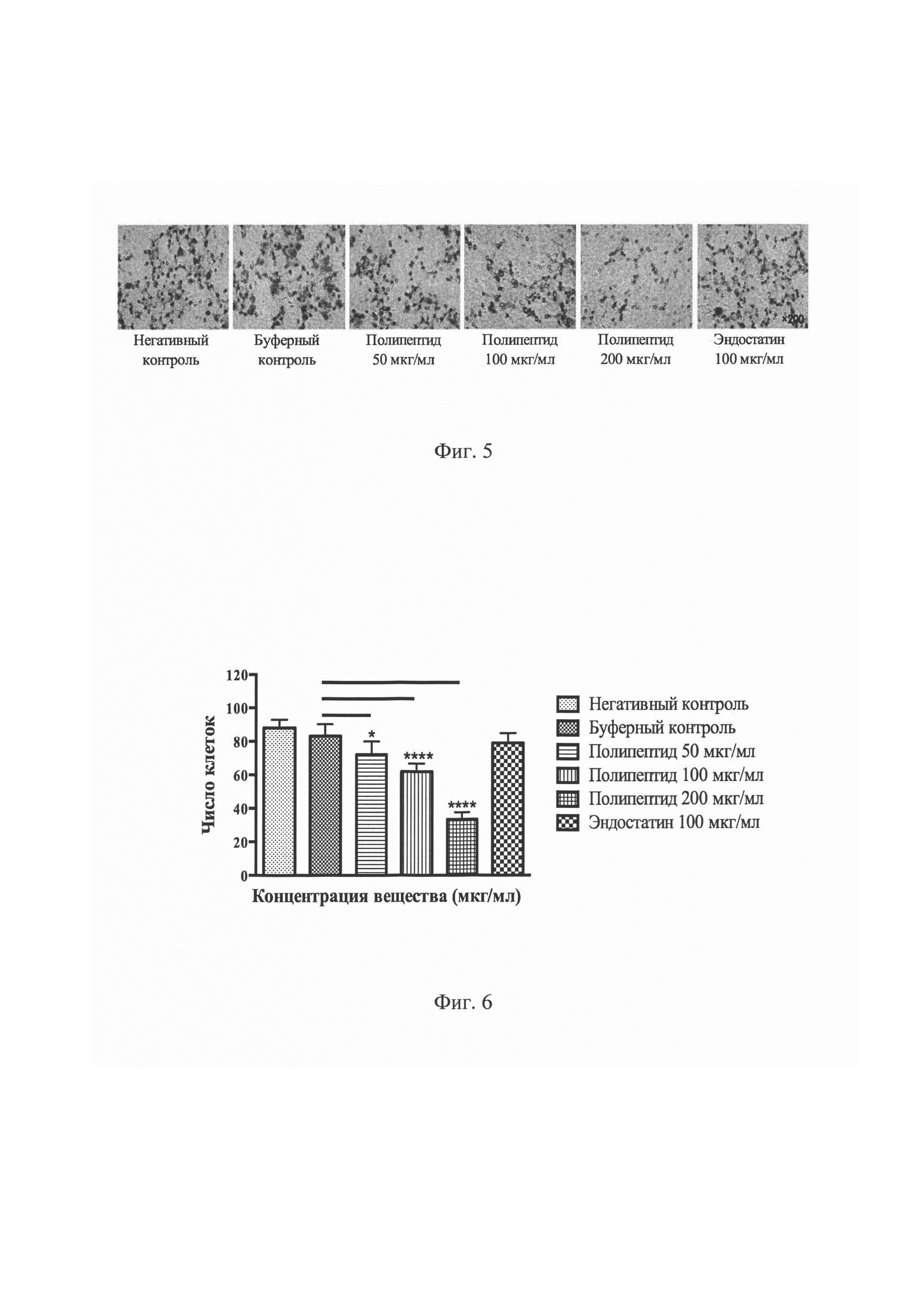
На Фиг. 5 представлены результаты фотомикроскопии мембран в камерах Transwell в каждой из указанных групп. Инвазивные клетки окрашены раствором кристального фиолетового.
На Фиг. 6 представлен график, демонстрирующий число инвазивных CAL 27 клеток в каждой из указанных групп при 48-часовой инкубации в камерах Transwell. *Р<0,05, ****P<0,0001 по сравнению с буферным контролем.
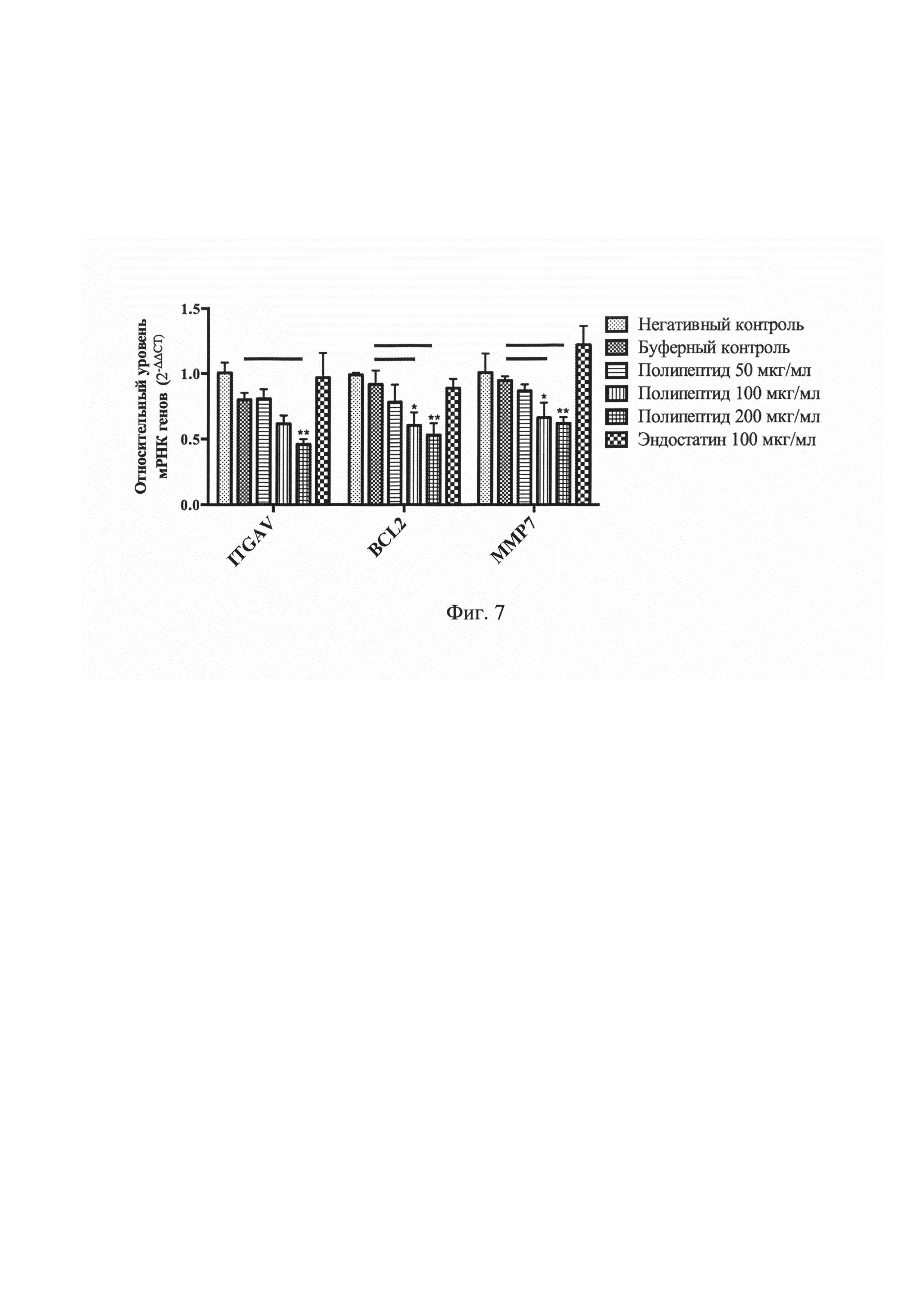
На Фиг. 7 представлен график, показывающий результаты полимеразной цепной реакции к генам ITGAV, BCL2, ММР7 с образцами, полученными из опухолевых клеток CAL 27, инкубированных с указанными веществами в течение 48 часов. *Р<0,05, **Р<0,01 по сравнению с буферным контролем.
Для приготовления стокового раствора полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, с концентрацией 10 мг/мл 20 мг сухого вещества полипептида растворяли в 2 мл 5% раствора глюкозы для инъекций. Полученный раствор фильтровали с помощью 0,22 мкм-микропоровой мембраны (EMD Millipore). Отфильтрованный стоковый раствор хранили при -20°C в недоступном для света месте. Рабочие растворы полипептида готовили путем разведения стокового раствора с питательной средой DMEM (GE Healthcare HyClone). В итоге получали растворы концентраций: низкой (50 мкг/мл), средней (100 мкг/мл) и высокой (200 мкг/мл).
Экспериментальные исследования in vitro проводили с культурами клеточной линии плоскоклеточного рака слизистой оболочки полости рта CAL 27 (АТСС® CRL-2095™). Уровень клеточного метаболизма при инкубации CAL 27 клеток с полипептидом оценивали с помощью колориметрической реакции превращения MTS (3-(4,5-диметилтиазол-2-ил)-5-(3-карбоксиметоксифенил)-2-(4-сульфофенил)-2Н-тетразолиум) в формазан, отражающей активность ферментов митохондрий. Опухолевые клетки инокулировали в 96-луночковый планшет в количестве 1×104/лунку в объеме 200 мкл питательной среды DMEM и оставляли в инкубаторе на ночь, ожидая их прикрепления. На следующий день 200 мкл подготовленной культуральной среды каждой группы вносили в лунки с прикрепленными опухолевыми клетками. В качестве негативного контроля использовали питательную среду DMEM, в группе буферного контроля добавляли 5%-ный раствор глюкозы. Эндостатин ENDOSTAR® (Simcere Pharmaceutical Group) в разведении 100 мкг/мл использовался как контрольный препарат. Инкубацию опухолевых клеток с реагентами проводили в течение 48 часов. По истечении отведенного времени в каждую из лунок добавляли 20 мкл раствора CellTiter 96® AQueous One Solution Reagent (Promega), содержащего MTS, после чего 96-луночковую тарелку возвращали в инкубатор на следующие 2 часа, ожидая проявления колориметрической реакции. Абсорбцию растворов питательных сред проверяли при длине волны 490 нм с помошью автоматического ридера Epoch (BioTek Instruments). Для каждой группы определяли показатель выживаемости клеток как отношение значения абсорбции при длине волны 490 нм в испытуемой группе к значению абсорбции в группе негативного контроля, умноженной на 100%. Также получали показатель IC50 (inhibitory concentration 50), характеризующий значение концентрации вещества, способной ингибировать пролиферацию клеток до 50%.
Действие полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, на миграцию раковых клеток CAL 27 испытывали с помощью Скрэтч эксперимента «заживления раны». Опухолевые клетки линии CAL 27 в количестве 5×105/лунку высеивали в 6-луночковый планшет и оставляли в инкубаторе на ночь, ожидая достижения ими 100%-ной непрерывности монослоя. На следующее утро на клеточном монослое всех лунок наконечником 200 мкл пипетки проводили «царапину». В каждой из лунок, соответствующей определенной группе, культуральную среду заменяли на разведения DMEM с реагентами, после чего клетки инкубировали в течение 48 часов. Первоначальный и конечный уровни границ «царапины-раны» фиксировали с помощью нативной фотомикроскопии под 40-кратным увеличением микроскопа в контрольные временные отрезки: 0 ч и 48 ч. Анализ полученных изображений проводили с помощью программного обеспечения Image-Pro Plus 6.0 (Media Cybernetics).
Определения влияния полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1 на инвазивные свойства плоскоклеточного рака полости рта in vitro проводили в эксперименте с камерами Transwell® (Corning Incorporated), покрытыми Matrigel®. Клетки плоскоклеточного рака полости рта предварительно выдерживали с различными разведениями веществ в течение 48 часов. По окончании инкубации опухолевые клетки обрабатывали 0,25% раствором трипсина, подсчитывали количество клеток в суспензиях каждой из групп. Клетки (1×105) высеивали в объеме 400 мкл питательной среды без эмбриональной телячьей сыворотки (ЭТС) в верхнюю камеру Transwell, покрытую матригелем. В нижней камере использовали среду DMEM с 10% содержанием ЭТС в качестве хемоаттрактанта. После чего 24-луночковую тарелку с камерами Transwell, содержащими опухолевые клетки, возвращали в инкубатор на следующие 48 часов, ожидая инвазии. По истечении отведенного времени не инвазивные опухолевые клетки удаляли со дна камеры Transwell с помощью ватного тампона. Клетки, преодолевшие матригель и проникшие через поры на обратную поверхность камеры, фиксировали 4% раствором параформальдегида, окрашивали раствором кристаллического фиолетового в течение 20 минут. После просыхания образцы фотографировали под 200-кратным увеличением светового микроскопа. В каждой из Transwell камер съемку мембран проводили в пяти произвольных полях зрения. Полученные снимки анализировали с помощью программного обеспечения Image J (U.S. National Institutes of Health).
Оценку влияния полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, на экспрессию онкогенов ITGA, BCL2 и ММР7 в опухолевых клетках линии CAL 27 плоскоклеточного рака полости рта проводили с помощью полимеразной цепной реакции в реальном времени. Из CAL 27 клеток, предварительно инкубированных с различными разведениями веществ в течение 48 часов, была выделена суммарная РНК с помощью реагента TRIzol (Invitrogen). Концентрацию и чистоту выделенной РНК определяли на спектрофотометре NanoDrop 2000 (Thermo Scientific). Тотальную РНК (1 мкг) превращали в кДНК в ходе обратной транскрипции с помощью набора реагентов ReverTra Асе® qPCR RT Kit (Toyobo) согласно рекомендациям производителя.
Экспрессию мРНК изучаемых генов определяли в ходе полимеразной цепной реакцией (ПЦР) в режиме реального времени на приборе ABI 7500 fast Real Time PCR system (Applied Biosystems) с использованием флуоресцентного красителя SYBR®Green Realtime PCR Master Mix (Toyobo). Условия ПЦР были следующими: 95°C в течение 1 мин; 40 циклов: 95°C в течение 15 сек, 60°C в течение 15 сек, 72°C в течение 45 сек. Для ПЦР анализа использовали следующие праймеры: к гену ITGAV, кодирующему белок αv интегрин: прямой  , обратный
, обратный 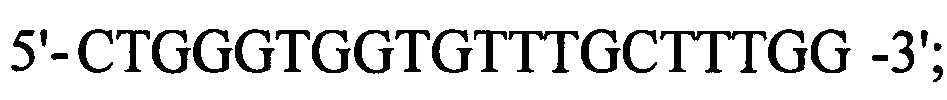 к гену BCL2, кодирующему белок Bcl-2: прямой
к гену BCL2, кодирующему белок Bcl-2: прямой  , обратный
, обратный 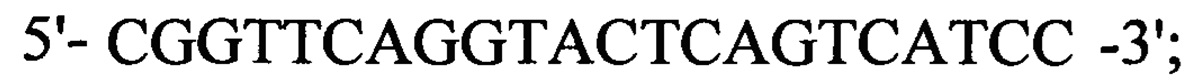 к гену ММР7, кодирующему белок ММР-7: прямой
к гену ММР7, кодирующему белок ММР-7: прямой  обратный
обратный 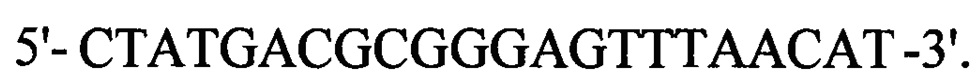 . GAPDH ген (прямой
. GAPDH ген (прямой 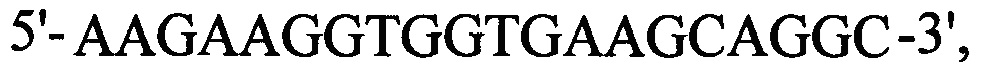 , обратный
, обратный 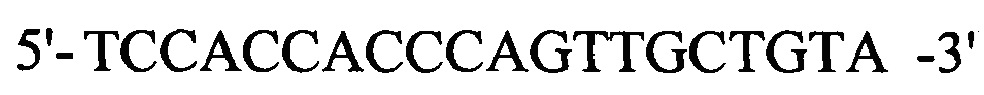 ) использовали в качестве внутреннего контроля. Относительный уровень экспрессии мРНК в каждой из экспериментальных групп определяли методом 2-ΔΔСТ.
) использовали в качестве внутреннего контроля. Относительный уровень экспрессии мРНК в каждой из экспериментальных групп определяли методом 2-ΔΔСТ.
Статистическую обработку результатов исследований проводили с использованием программного обеспечения Graphpad Prism 6 с помощью однофакторного дисперсионного анализа One Way ANOVA. Значение Р<0,05 считали статистически достоверным.
В ходе изучения ингибирующего эффекта полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, было установлено, что инкубация опухолевых клеток линии CAL 27 с соединением 1 в течение 48 часов значительно снизила рост плоскоклеточного рака полости рта in vitro (Фигура №1). Так, выживаемость опухолевых клеток в группе полипептида 50 мкг/мл составила 53,73%, в группе полипептида 100 мкг/мл - 45,24%, а в группе с максимальной концентрацией в 200 мкг/мл показатель выживаемости был снижен в 3,7 раза относительно уровня контрольной группы и имел среднее значение, соответствующее 27,36%. Значение IC50 для полипептида в отношении клеток линии CAL 27 составило 70 мкг/мл (Фигура №2).
Анализ результатов эксперимента «заживления раны» выявил дозозависимый антимиграционный эффект полипептида в отношении опухолевых клеток линии CAL 27 in vitro (Фигуры №3-4).
Результаты эксперимента Transwell инвазии показали выраженный ингибирующий эффект полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, на инвазивные свойства клеток плоскоклеточного рака полости рта (Фигуры №5-6). Так, в группах со средней (100 мкг/мл) и максимальной (200 мкг/мл) концентрациями полипептида число инвазивных клеток было значительно меньше по сравнению с группой буферного контроля (Р<0,0001).
Согласно полученным результатам ПЦР в реальном времени (Фигура №7), при воздействии полипептида экспрессия генов ITGA, BCL2 и ММР7 в клетках CAL 27 была значительно снижена относительно группы буферного контроля (Р<0,01 и Р<0,001).
Таким образом, на основании полученных результатов можно сделать вывод об ингибирующем действии полипептида, имеющего аминокислотную последовательность, соответствующую SEQ ID NO:1, на плоскоклеточный рак полости рта in vitro. Способность полипептида подавлять клеточную пролиферацию, миграцию и инвазию, а также ингибировать экспрессию онкогенов в клетках линии CAL 27 позволяет рассматривать данный полипептид в качестве потенциального противоопухолевого средства для лечения плоскоклеточного рака полости рта.