Результат интеллектуальной деятельности: СПОСОБ ЛЕЧЕНИЯ ПЛОСКОКЛЕТОЧНОГО РАКА ПОЛОСТИ РТА И ГЛОТКИ В СОЧЕТАНИИ С ЛУЧЕВЫМ И ЛЕКАРСТВЕННЫМ ВОЗДЕЙСТВИЕМ
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к онкологии, и может быть использовано при лечении плоскоклеточного рака полости рта и глотки путем сочетанного лучевого и лекарственного воздействия.
Известен способ повышения эффективности лучевой терапии опухолей различной локализации (RU 2088288 C1), включающий дистанционную γ-терапию в сочетании с химиотерапией, при которой больному вводят 5-фторурацил с 1 по 5 сутки ежедневно в суточной дозе 600 мг/м2, затем в течение 7-9-х суток ежедневно непосредственно перед облучением вводят платидиам в суточной дозе 20 мг/м2. Лучевую терапию начинают на 7-е сутки в режиме динамического мультифракционирования: первые 3 дня фракции по 1,8 Гр два раза через 4-6 час, затем по 1,2 Гр два раза в день через 4-6 часов до суммарной очаговой дозы 30-32,4 Гр. После 10-14-дневного перерыва лечение повторяют по аналогичной схеме до СОД 60-64,8 Гр.
Недостатком этого способа является то, что в 40% случаев возникают лучевые реакции со стороны слизистых орофарингеальной области, требующие незапланированного перерыва в лечении, что негативно сказывается на его эффективности. С другой стороны, не менее 30% пациентов страдают от общих токсических явлений. Кроме того, такой метод химиолучевого лечения, достаточно эффективный в случае первичного очага (78,6% полной резорбции при опухолях ротоглотки), малоэффективен при воздействии на регионарные метастазы.
Также особый интерес представляет работа Sewit Teckie с соавторами 2016, в которой авторы ретроспективно оценили результаты и побочные эффекты лучевого лечения больных опухолями головы и шеи в режиме гипофракционирования, в том числе и ультрагипофракционирования с подведением 8 Гр за фракцию. В исследование включено 48 пациентов со средним сроком наблюдения от 6 до 54,3 мес. Средние дозы составили 30 Гр за 5 фракций, тогда как в 20 случаях разовая очаговая доза (РОД) была 8 Гр. Общий ответ на лечение составил 79%. Одногодичный локорегионарный контроль достигал 50%. Многофакторный анализ показал, что локорегионарный контроль был выше при подведении доз ионизирующего излучения в РОД 6 Гр (р = 0.04). Полный ответ на облучение также был достоверно связан с лучшей выживаемостью больных (р = 0.01).
При этом побочные эффекты не были более выражены даже при облучении в РОД 8 Гр. Таким образом, исследователи подчеркивают положительную роль гипофракционирования (РОД 6 Гр и более) в лечении больных опухолями головы и шеи и предлагают проведение дальнейших научных изысканий в этом направлении.
Известен способ лечения плоскоклеточного рака орофарингеальной области, включающий введение цисплатина и цетуксимаба в сочетании с лучевой терапией (RU 2429032 C1), причем цетуксимаб вводят в течение первого дня первой недели капельно в дозе 400 мг/м2, затем с первого дня второй недели проводят лучевую терапию укрупненными фракциями по 4 Гр с одновременным введением цисплатина по 30 мг 3 дня подряд, со второй по пятую недели в первый день каждой недели вводят капельно цетуксимаб в дозе 250 мг/м2, в последующем лучевую терапию осуществляют по 2 Гр 1 раз в день 5 раз в неделю до суммарной очаговой дозы 30-40 Гр, через 2 недели курс повторяется до суммарной очаговой дозы 70 Гр по той же схеме.
Однако предложенный способ отличается тем, что лекарственный компонент лечения представлен только препаратом цисплатин и в другой дозе 100 мг/м2 1 раз в 3 недели (суммарно 2 введения), а также методикой фракционирования доз, подразумевающей вначале облучение локорегионарной области в режиме традиционного фракционирования в РОД 2 Гр до СОД 50 Гр с последующим интенсивным трехкратным облучением в РОД 6 Гр до СОД 68 Гр.
Известен способ лечения плоскоклеточного рака полости рта и глотки (RU 2018127510 А), включающий введение цетуксимаба в стартовой дозе 400 мг/м2 с последующей дозой 250 мг/м2 1 раз в неделю в сочетании с лучевой терапией локорегионарной области с РОД 1,8 Гр ежедневно до СОД 54 Гр в течение 6 недель и дополнительным облучением опухоли и метастатически измененных лимфоузлов ежедневно, причем с 8 дня лечения цетуксимабом проводят лучевую терапию ежедневно по 5-дневной рабочей неделе на локорегионарную область, включая регионарные лимфоколлекторы: заглоточные лимфоузлы и лимфоколлекторы шеи до I-V групп с обеих сторон (CTV2/PTV2); при этом в течение последних 12 дней, после подведения СОД 32,4 Гр, дополнительно с интервалом, равным или более 6 часам, проводят облучение опухоли и метастатически измененных лимфоузлов (GTV/CTV1/PTV1) в РОД 1,5 Гр до СОД 72 Гр.
Однако, предложенный способ отличается тем, что лекарственный компонент лечения представлен препаратом цисплатин, а не цетуксимаб, в дозе 100 мг/м2 1 раз в 3 недели (суммарно 2 введения), а также методикой фракционирования доз, подразумевающей вначале облучение локорегионарной области в режиме традиционного фракционирования в РОД 2 Гр до СОД 50 Гр с последующим интенсивным трехкратным облучением в РОД 6 Гр до СОД 68 Гр.
За прототип принят способ одновременного химиолучевого лечения больных местнораспространенным раком головы и шеи, указанный в отечественных и мировых рекомендациях как «золотой стандарт» (NCCN Ver. 1, 2019; Практические рекомендации Российского общества клинической онкологии, 2018; Pignon J. Р.,  A. L., Maillard Е., Bourhis J. On behalf of the MACH-NC Collaborative Group. Meta-analysis of chemotherapy in head and neck cancer (MACH-NC): an update on 93 randomised trials and 17,346 patients // Radiother. Oncol. - 2009. - V. 92 (1). - P. 4-14.). Авторы представленного метаанализа указывают на большую относительную эффективность одновременного химиолучевого лечения с цисплатином (облучение в РОД 2Гр по 5-дневной рабочей неделе до СОД 70Гр) в сравнении с последовательной химиолучевой терапии с адьювантной, либо индукционной полихимиотерапией (отношение рисков 0,81). В то же время, в рамках мета-анализа подтвержден 8% абсолютный прирост эффективности преимущественно у больных не старше 70 лет, а показатели 5-летней общей выживаемости составили лишь 33,7%.
A. L., Maillard Е., Bourhis J. On behalf of the MACH-NC Collaborative Group. Meta-analysis of chemotherapy in head and neck cancer (MACH-NC): an update on 93 randomised trials and 17,346 patients // Radiother. Oncol. - 2009. - V. 92 (1). - P. 4-14.). Авторы представленного метаанализа указывают на большую относительную эффективность одновременного химиолучевого лечения с цисплатином (облучение в РОД 2Гр по 5-дневной рабочей неделе до СОД 70Гр) в сравнении с последовательной химиолучевой терапии с адьювантной, либо индукционной полихимиотерапией (отношение рисков 0,81). В то же время, в рамках мета-анализа подтвержден 8% абсолютный прирост эффективности преимущественно у больных не старше 70 лет, а показатели 5-летней общей выживаемости составили лишь 33,7%.
Таким образом, предложенная схема лечения продемонстрировала относительно высокий локальный противоопухолевый эффект за счет агрессивного воздействия двух агентов (цисплатин, ионизирующее излучение) на опухолевые клетки. В то же время нередко эффективность лечения оказывалась недостаточной как за счет локальных рецидивов, так отдаленного метастазирования. Кроме того, побочные эффекты лучевого и лекарственного лечения нередко нивелировали положительные результаты противоопухолевого воздействия, требовали незапланированных перерывов, отдаляли возможность проведения дальнейших этапов комбинированного и комплексного плана, создавали риск развития осложнений, усугубляли психическое состояние пациентов и снижали качество их жизни.
Техническим результатом предлагаемого изобретения является разработка способа лечения с повышенной эффективностью в виде большей степени регрессии первичной опухоли, подавления субклинических диссеминированных метастазов за счет оптимального режима сочетанного лучевого и лекарственного воздействия на опухоль.
Указанный технический результат при осуществлении изобретения достигается за счет того, что также как и в известном способе вводят цисплатин 100 мг/м2 1 раз в 3 недели в сочетании с лучевой терапией в режиме нетрадиционного фракционирования.
Особенностью заявляемого способа является то, что с первого дня лечения проводится лучевая терапия в РОД 2 Гр ежедневно по 5-дневной рабочей неделе до СОД 50 Гр на локорегионарную область, включая регионарные лимфоколлекторы CTV2/PTV2, при этом в течение последующих трех дней ежедневно проводится дополнительное облучение опухоли GTV/CTV1/PTV1 в РОД 6 Гр до СОД 68 Гр.
С первого дня опухолевые клетки подвергают воздействию дозы излучения, необходимой для их разрушения и гибели (2 Гр), с одновременным подключением цитотоксического и радиомодифицирующего действия цисплатина в виде внутривенной инфузии в дозе 100 мг/м2 (в 1-й и 22-й дни). Усиление противоопухолевого воздействия после подведения СОД 50 Гр достигается за счет локального наращивания РОД до 6 Гр до СОД 68 Гр. Указанная доза облучения является допустимой для сохранения жизнеспособности нормальных клеток (с учетом предшествующего режима классического фракционирования по 2 Гр × 1 р/сут). Кроме того, смещение более агрессивного режима облучения на вторую половину курса лучевой терапии позволяет рассчитывать как на преодоление потенциальной радиорезистентности оставшихся к этому времени опухолевых клеток, так и на меньшую выраженность лучевых реакций за счет частичной адаптации нормальных тканей. В результате подведения вначале ионизирующего излучения в режиме традиционного фракционирования (2 Гр) имеет место повреждение опухолевых клеток различной степени - летальное и сублетальное. При этом разрушающему лучевому воздействию в первую очередь подвергаются наиболее активные опухолевые клетки, способные к метастазированию. В то же время менее активные опухолевые клетки переходят в суб- и потенциально летальное состояние. На устойчивые к облучению клетки опухоли оказывает более эффективное воздействие крупные фракции по 6 Гр в конце курса лучевой терапии. Также при гипофракционировании в РОД 6 Гр возникает абскопальный эффект, что позволяет рассчитывать на системное противоопухолевое воздействие на возможно существующие клинически неопределяемые очаги опухоли вне области облучения.
Радиомодифицирующее действие цисплатина выражается в блокировании восстановления суб- и потенциально летальных повреждений в опухоли, что, в конечном итоге, приводит к усилению лучевого разрушения опухоли. Цисплатин наряду с радиомодифицирующим действием характеризуется значительными цитотоксическими свойствами и непосредственно вызывает гибель опухолевых клеток. В связи с выраженной его токсичностью для нормальных тканей, а также расчетом в первую очередь на радиомодифицирующее действие препарата, целесообразно введение цисплатина в дозе 100 мг/м2 один раз в 3 недели в процессе облучения, что, с учетом предложенной схемы фракционирования доз, в итоге соответствует двум введениям препарата.
Такое сочетание лучевого и лекарственного лечения со снижением СОД до 68 Гр и сокращением общей длительности лечения до 5,5 недель, а также уменьшением планируемой суммарной дозы цисплатина относительно стандартной схемы химиолучевой терапии, приводит к повышению противоопухолевого эффекта вкупе со снижением риска развития системных побочных эффектов лечения.
Таким образом, в предложенном способе используется два взаимно дополняющих метода радиомодификации: цисплатин и нетрадиционное фракционирование дозы лучевого воздействия с интенсивным воздействием на массив опухоли.
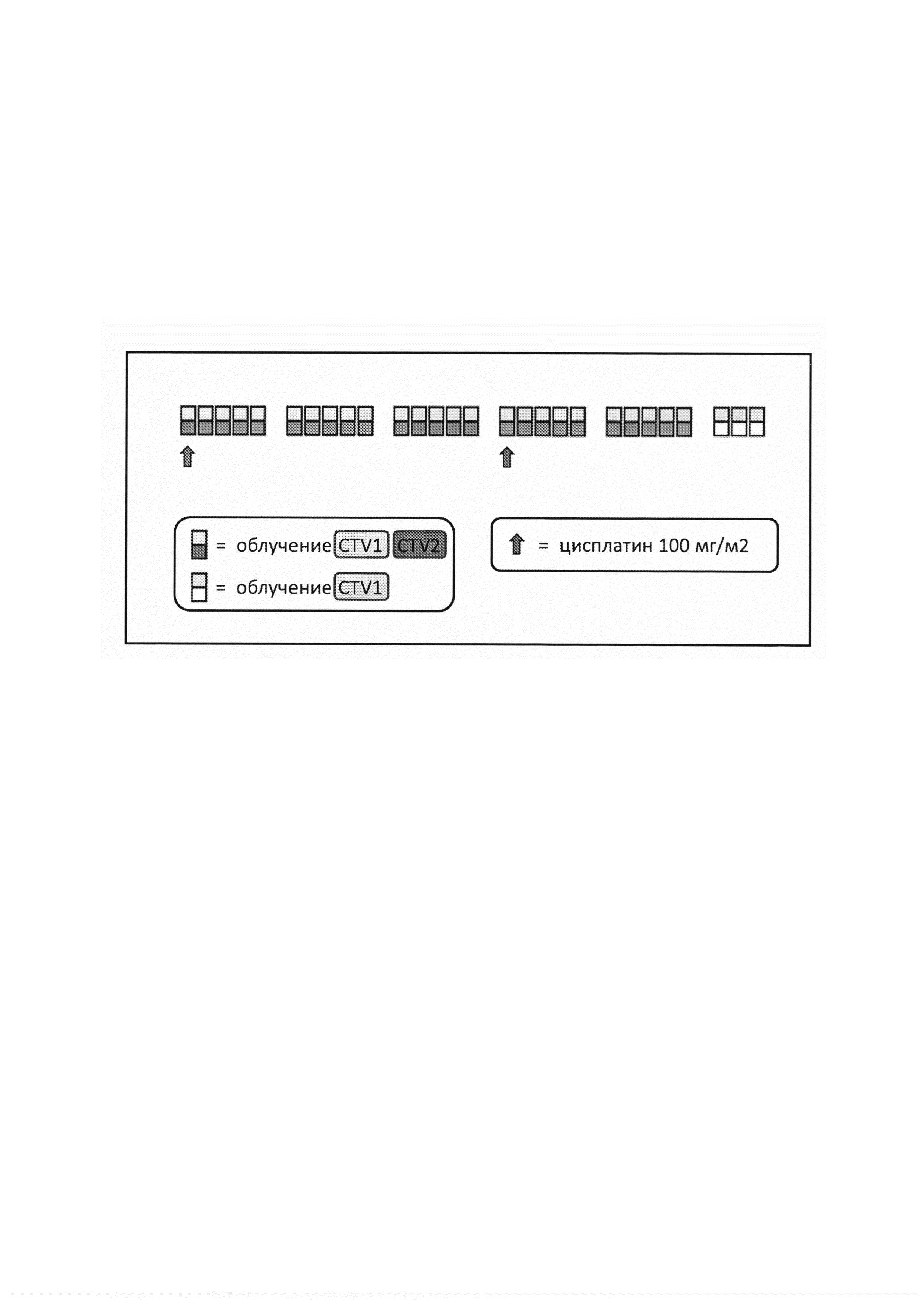
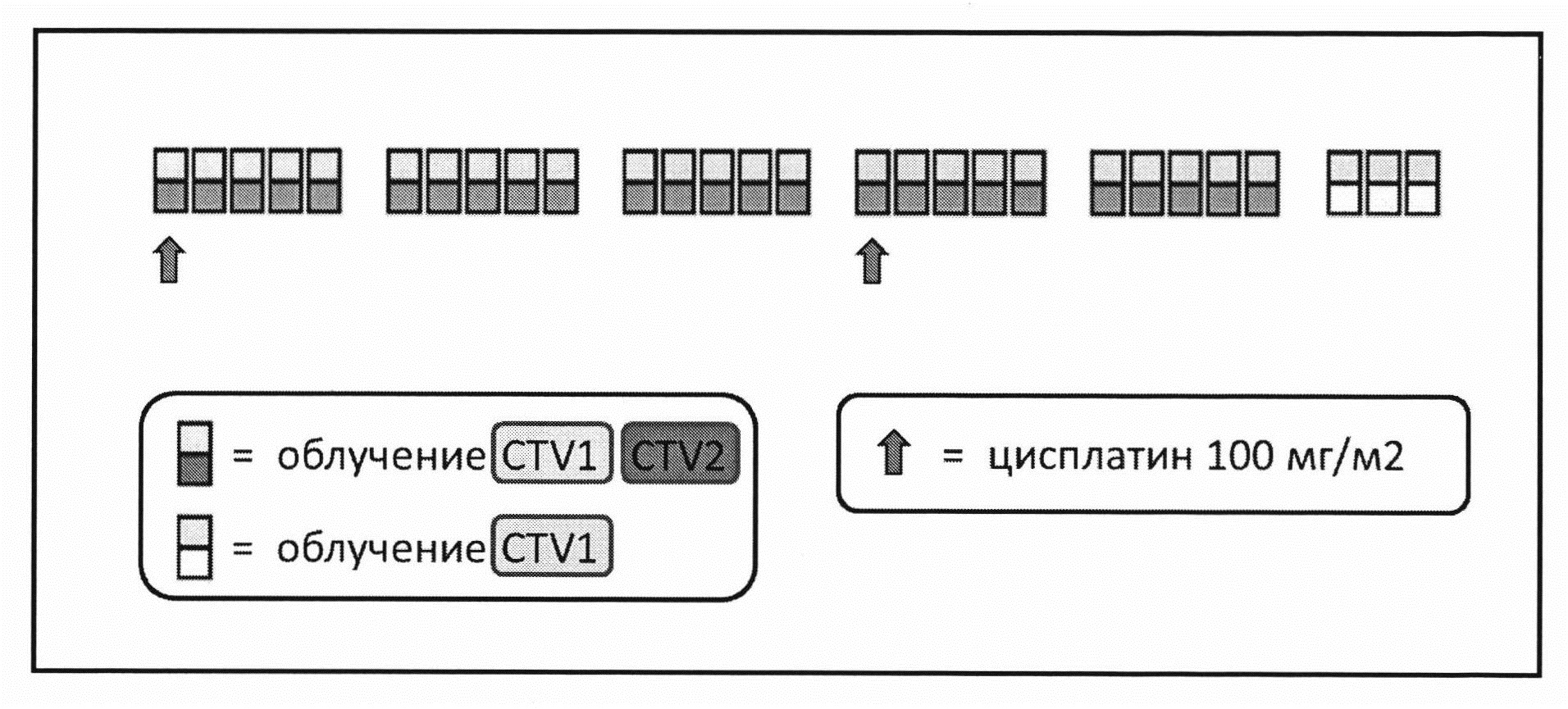
Изобретение поясняется подробным описанием, клиническими примерами и схемой химиолучевого лечения.
Способ осуществляют следующим образом (см. схему):
1-й день: Цисплатин вводится в виде внутривенной инфузии в дозе 100 мг/м2 со скоростью не более 1 мг/мин с пред- и постгидратацией.
22-й день: Цисплатин вводится в виде внутривенной инфузии в дозе 100 мг/м2 со скоростью не более 1 мг/мин с пред- и постгидратацией.
Лучевая терапия: 1-Й-35-Й день - Лучевая терапия в РОД 2 Гр × 1 раз в сутки по 5-дневной «рабочей неделе» на локорегионарную область пораженных структур, включая регионарные лимфоколлекторы (CTV2/PTV2) до СОД 50 Гр.
36-й-38-й день. Лучевая терапия в РОД 6 Гр × 1 раз в сутки на область опухолевого поражения (GTV/CTV1/PTV1) до СОД 68 Гр.
Заявляемый способ с успехом апробирован для лечения больных с местнораспространенным опухолевым поражением орофарингеальной области: плоскоклеточным раком слизистой полости рта и глотки.
Клинический пример 1.
Больной С, 58 лет, поступил с диагнозом: Рак ротоглотки III ст.cT3N0M0. Со слов пациента с августа 2016 года после употребления холодных напитков, появились неприятные ощущения в глотке. Получал симптоматическое лечение у ЛОР врача по месту жительства без эффекта. В декабре 2017 года появилась боль в горле, проведена биопсия (гистологическое исследование 4016 от 13.02.17 г. плоскоклеточный рак), на консилиуме по месту жительства рекомендовано проведение ХЛТ. Направлен для лечения в МНИОИ им. П.А. Герцена, где на консилиуме от 30.05.2017 пациенту рекомендовано проведение химиолучевой терапии по радикальной программе. Гистологическое исследование от 22.05.2017 (биоптат из образования ротоглотки): поверхностные частицы слизистой оболочки почти без подлежащей основы, разрастанием высокодифференцированного плоскоклеточного рака. ИГХ (р16) от 09.06.2017: реакция с р16 отрицательная. Поступил в отделение лучевой терапии.
При осмотре - асимметрии головы и шеи нет. Акт глотания не нарушен. При осмотре через рот: в области задней стенке глотки, больше слева, определяется опухолевое образование, преимущественно эндофитной формы роста, размерами 2,5 × 4,5 см. Образование контактно кровоточит. Кровотечения нет. На шее с обеих сторон без очаговой патологии.
Эндоскопия: При осмотре: носовые ходы свободны, раковины анатомичны, хоаны не сужены. Слизистая носоглотки гладкая. Мягкое небо эластично, небные миндалины не увеличены. Корень языка эластичен, подвижен. Надгортанник обычной формы и размеров. По задней стенке ротоглотки (больше слева) определяется мелкобугристая опухолевая инфильтрация на площади 3,0 × 3,0 см, которая граничит с задней левой небной дужкой и дистальный край которой расположен напротив верхнего края лепестка надгортанника. Все элементы гортани сохранены, четко визуализируются. Обе 1/2 гортани подвижны, голосовые складки полностью смыкаются при фонации. Подскладочный отдел свободен. Грушевидные синусы свободны. Заключение: с-г задней стенки ротоглотки.
МРТ с контрастным усилением: На уровне ротовой полости - артефакты от несъемных ортодонтических конструкций. Слева по задней стенке ротоглотки (скелетотопически от середины позвонка С2) с переходом на левую заднебоковую стенку с вовлечением слизистой левого мйндаликового синуса, левой черпалонадгортанной складки, слизистой левого грушевидного синуса, определяется зона неоднородного контрастирования с патологическим сигналом на ДВИ и ограничением диффузии на карте ИКД. Толщина стенки ротоглотки на этом уровне ~ 7 мм, протяженность выявленных изменений в краниокаудальном направлении ~ 7 см. Ретрофарингеальные лимфоузлы не дифференцируются. Па остальном уровне лимфоузлы поверхностных и глубоких шейных групп не увеличены (до 5-10 мм по короткой оси), их макроструктура не изменена. Небные и язычная миндалины не увеличены, небные - симметричные. Структуры носо- и гортаноглотки не деформированы. Просвет подскладочного отдела гортани и видимых отделов трахеи не изменен, внутрипросветных образований не выявлено. Структура околоушных слюнных желез не изменена, ретенционных изменений протоков не выявлено. Придаточные пазухи носа развиты правильно, пневматизированы. Отмечается утолщение слизистой правой верхнечелюстной пазухи. Щитовидная железа расположена типично, не увеличена, структура однородная, контрастирование равномерное. Признаков костной деструкции на исследованном уровне не выявлено. Заключение: MP картина неравномерного утолщения задней и левой боковой стенки рото- и гортаноглотки может соответствовать основному заболеванию. Лимфаденопатии, костно-деструктивных измененийн исследованном уровне нет. Правосторонний гайморит.
УЗИ: Щитовидная железа расположена типично, подвижна при глотании. Контур ровный четкий. Правая доля размерами 23×17×51 мм. Перешеек до 4,7 мм. Левая доля размерами 16×18×47 мм. Очаговых образований не выявлено. Кровоток не усилен. По ходу сосудов шеи увеличенные и измененные лимфоузлы не определяются. Заключение: эхографическая картина без очаговой патологии.
Проведен 38-дневный курс химиолучевой терапии с применением цисплатина (СД 360 мг) по приведенной выше схеме до СОД 68Гр на область первичной опухоли и до СОД50Гр на локорегионарную область ротоглотки, включая заглоточные лимфоузлы и лимфоколлекторы шеи II-IV групп с обеих сторон. На момент завершения лечения клинически отмечена резорбция опухоли.
Лечение проведено с 12-дневным перерывом в лечении на пике лучевых реакций. По окончании лечения отмечены побочные эффекты в виде эпителиита III ст. СТС АЕ 4 версии выраженности со стороны слизистой глотки, дерматита I ст. СТС АЕ 4 версии на шее с обеих сторон. Питание через рот в полном объеме. Согласно оценке качества жизни переносимость лечения удовлетворительная.
Больной выписан под наблюдение по месту жительства.
При контрольном обследовании через 2 месяца - без признаков рецидива, регионарного и отдаленного метастазирования, а также побочных эффектов проведенного ранее лечения за исключением ксеростомии II ст. СТС АЕ 4 версии. Оставлен под наблюдение. В настоящее время без признаков рецидива в течение 20 месяцев.
Пример 2.
Больная Т., 55 лет, поступила с диагнозом: Рак левой небной миндалины III ст. cT3N0M0.
Из анамнеза: в июле 2016 появились неприятные ощущения в глотке. Обратилась к ЛОР врачу по месту жительства. Получала симптоматическое лечение по поводу острого тонзиллита в течение недели с временным положительным эффектом. В октябре 2016 года обратила внимание на появление помехи и ощущение инородного тела в глотке. В ноябре обратилась к ЛОР врачу по месту жительства. Заподозрен полип левой небной миндалины. Направлена к ЛОР врачу в ГКБ г. Москвы, где в декабре 2016 года, после дообследования заподозрено злокачественное новообразование ротоглотки. В январе 2017 года самостоятельно обратилась в МНИОИ им. Герцена, где был установлен настоящий диагноз и рекомендовано проведение химиолучевой терапии по радикальной программе. Поступила в отделение лучевой терапии.
Гистологическое исследование от 30.01.2017 - биоптат образования левой небной миндалины. Фрагменты слизистой оболочки с покровом из многослойного плоского эпителия, с изъязвлением, инфильтративным ростом умеренно дифференцированного плоскоклеточного рака. ИГХ (р16) от 30.01.2017: реакция с р16 отрицательная.
При осмотре - асимметрии лица и шеи нет. Тризма нет. Мимические пробы выполняет удовлетворительно. Речь не нарушена. Девиации языка нет. В области левой небной миндалины определяется крупнобугристая опухоль, инфильтрирующая небные дужки, левую боковую стенку ротоглотки, размерами до 4,5 см. В верхней трети шее слева пальпируются единичные узлы, плотно-эластичной консистенции, безболезненные, подвижные при пальпации, размерами до 1,0 см. В области шеи справа без очаговой патологии.
Эндоскопия: При осмотре: носовые ходы свободны с обеих сторон, раковины анатомичны слизистая гладкая. Выход из хоан не сужен, Просвет носоглотки свободен. Левая половина мягкого неба с явлениями отека и утолщения слизистой. В области миндаликовой ниши слева и левой задней небной дужки на всем ее протяжении крупнобугристая опухолевая инфильтрация, которая занимает миндаликовую нишу (биопсия + отпечатки). Ткань миндалины отечна, утолщена. Протяженность опухолевых изменений около 4.5 см. Дистальный край опухоли расположен в области левой половины корня, выше надгортанно-глоточной складки на 2 мм. Правая половина корня языка свободна. Правая небная миндалина несколько утолщена, свободна, отечна размерами 2×2 см. Надгортанник обычной формы и размеров. Грушевидные синусы свободны с обеих сторон. Все элементы гортани сохранены, визуализируются. Обе половины гортани подвижны. Подскладочный отдел свободен. При осмотре через рот: небная занавеска не изменена. Передние небные дужки симметричны, анатомичны. Язычок не деформирован. Правая небная миндалина в пределах анатомической нормы с умеренным отеком. Левая миндалина с признаками вышеописанной опухолевой инфильтрации. Заключение: Рак ротоглотки с поражением левой небной миндалины.
МРТ головы и шеи с внутривенным контрастным усилением: в области ротоглотки слева определяется дополнительное мягкотканное образование с четкими неровными контурами, однородной структуры, размерами 31×19×38 мм с признаками нарушения диффузии, деформирующее просвет ротоглотки слева, тесно прилегающие к мягкому небу, корню языка слева, дистально распространяется до уровня лепестка надгортанника слева (расстояние до лепестка надгортанника около 2 мм). Надгортанник не изменен. Область гортани без особенностей. Подчелюстная железа без особенностей. Отмечается лимфоузел до 9×8 мм в области угла нижней челюсти слева, аналогичный справа до 6 мм. Костно-деструктивных изменений не. Заключение: MP-картина объемного образования ротоглотки слева. Единичный регионарный лимфоузел по сравнении с противоположной стороной.
УЗИ шеи: Щитовидная железа расположена типично, подвижна при глотании. Контур ровный. Правая доля размерами 19×15×32 мм. Перешеек 3 мм, левая доля 15×13×32 мм. С четкими ровными контурами, однородной структуры, васкуляризация не усилена, узловые образования не определяются. При исследовании шеи слева в в\трети (Iгр. л\у) - определяется гиперплазированный л\у размерами 12×5 мм. Других очаговых образований в мягких тканях шеи и подчелюстных областях не выявлено. При исследовании брюшной области печень не увеличена, с четкими ровными контурами, диффузно гетерогенной структуры, внутрипеченочные желчные протоки не расширены. Желчный пузырь не визуализируется. Поджелудочная железа не увеличена, с четкими ровными контурами, диффузно гетерогенной структуры. Вирсунгов проток не расширен. Заключение: Эхографическая картина гиперплазированного л\у шеи слева.
Проведен курс химиолучевой терапии с применением цисплатина (СД 300 мг) по приведенной выше схеме до СОД 68 Гр на область первичной опухоли и до СОД 50 Гр на локорегионарную область ротоглотки, включая заглоточные лимфоузлы и лимфоколлекторы шеи II-IV групп с обеих сторон.
Лечение проведено с 14-дневным перерывом в лечении на пике лучевых реакций. По окончании лечения отмечены побочные эффекты в виде эпителиита III ст. СТС АЕ 4 версии выраженности со стороны слизистых полости рта и глотки и дерматита II ст. СТС АЕ 4 версии на шее с обеих сторон. Питание через рот в полном объеме. Согласно оценке качества жизни переносимость лечения удовлетворительная.
Больная выписана под наблюдение по месту жительства.
При контрольном обследовании через 2 месяца - без признаков рецидива, регионарного и отдаленного метастазирования, а также побочных эффектов проведенного ранее лечения за исключением ксеростомии I ст. СТС АЕ 4 версии. Оставлена под наблюдение. В настоящее время без признаков рецидива в течение 21 месяца.
Использование предложенного способа в клинике позволяет достичь излечения больного с минимальными побочными эффектами в отличие от известных схем химиолучевой терапии.
Способ лечения плоскоклеточного рака полости рта и глотки в сочетании с лучевым и лекарственным воздействием, включающий введение цисплатина с первого дня в виде внутривенной инфузии в дозе 100 мг/м 1 раз в 3 недели в сочетании с лучевой терапией, отличающийся тем, что с первого дня лучевое лечение проводят в РОД 2 Гр ежедневно по 5-дневной рабочей неделе до СОД 50 Гр на локорегионарную область, включая регионарные лимфоколлекторы CTV2/PTV2, с последующим ежедневным дополнительным облучением опухоли GTV/CTV1/PTV1 в РОД 6 Гр в течение 3 дней до СОД 68 Гр.