Способ получения ароматических амидов 1-адамантанкарбоновой кислоты
Вид РИД
Изобретение
Изобретение относится к способам получения получения ароматических амидов 1-адамантанкарбоновой кислоты.
Известен способ получения амидов ароматических кислот некаталитическим взаимодействием карбоновых кислот с аминами при температуре не ниже 180-190°С и одновременной отгонке воды из реакционной массы [Лебедев Н.Н. Химия и технология основного органического и нефтехимического синтеза. - М.: Химия, 1988, с. 210-215; А Simple Preparation of Amides from Acids and Amines by Heating of Their Mixture / B.S. Jursic, Z. Zdravkovski // Synthetic Communications. - V. 23. - №19. - 1993. - P. 2761-2770].
Недостатками способа являются невозможность использования в качестве исходных веществ термически нестабильных соединений, а также не применимость для получения амидов адамантанкарбоновой кислоты.
Известны способы получения амидов, заключающиеся в превращении карбоновой кислоты в соответствующий хлорангидрид с его дальнейшим взаимодействием с аммиаком или амином [Пат. US 3173951, МПК С07С 275/00, опубл. 16.03.1965; Адамантан и его производные. XXI. ƒi-Галогензамещенные кетоны и альдегиды ряда адамантана / Степанов Ф.Н., Исаев С.Д., Васильева З.П. // Журн. орган. химии. - 1970. - Т. 6. - Вып. 1. - С. 51-55; Uber Verbindungen mit Urotropin-Struktur, XVII. Zur Kenntnis der 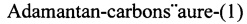 / Stetter H., Rauscher E. // Chem. Ber. - 1960. - Bd. 93. - Issue 5. - S. 1161-1166; Синтез n-нитрофенильных производных 1-адамантилсодержащих амидов / А.А. Горячкина, В.А. Ермохин, П.П. Пурыгин // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2012. - №3/1(94). - С. 180-185; Синтез амидов 1-адамантанкарбоновой кислоты / В.А. Ермохин, П.П. Пурыгин, В.В. Вишняков // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2000. - №2(16). - С. 146-148; Адамантановые производные эфиров и амидов 4-аминобензойной кислоты / В.А. Ермохин, П.П. Пурыгин, Ю.П. Зарубин // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2006. - №9(49). - С. 72-91].
/ Stetter H., Rauscher E. // Chem. Ber. - 1960. - Bd. 93. - Issue 5. - S. 1161-1166; Синтез n-нитрофенильных производных 1-адамантилсодержащих амидов / А.А. Горячкина, В.А. Ермохин, П.П. Пурыгин // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2012. - №3/1(94). - С. 180-185; Синтез амидов 1-адамантанкарбоновой кислоты / В.А. Ермохин, П.П. Пурыгин, В.В. Вишняков // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2000. - №2(16). - С. 146-148; Адамантановые производные эфиров и амидов 4-аминобензойной кислоты / В.А. Ермохин, П.П. Пурыгин, Ю.П. Зарубин // Вестник Самарского госуниверситета. Естественнонаучная серия. - 2006. - №9(49). - С. 72-91].
Недостатками способов является то, что для получения хлорангидридов кислот используются такие соединения, как фосген, хлористый тионил или хлориды фосфора, многостадийность синтеза, а также большая чувствительность промежуточного продукта (хлорангидрида кислоты) к влаге.
Известны способы прямого амидирования первичными или вторичными аминами карбоновых кислот в присутствии катализаторов [Metal-catalysed approaches to amide bond formation / Allen, C.L., Williams J.M.J. // Chem. Soc. Rev. - V. 40. - 2011. - P. 3405-3415; Williams. Direct amide formation from unactivated carboxylic acids and amines / C.L. Allen, A.R. Chhatwal, J.M.J. // Chem. Commun. - 2012. - 48. - P. 666-668] в том числе в условиях азеотропной отгонки воды [Sulfated tungstate: a new solid heterogeneous catalyst for amide synthesis / P.S. Chaudhari, S.D. Salim, R.V. Sawant, K.G. Akamanchi // Green Chem. - V. 12. - 2010. - P. 1707-1710; Пат. RU 2565059, МПК C07C 231/02, C07C 233/06, C07D 211/06, C07D 211/16, C07D 265/30, C07D 295/023, опубл. 2015]. Параллельно с использованием катализатора реакции вели при повышенных температурах [Mesoporous silica МСМ-41 as a highly active, recoverable and reusable catalyst for direct amidation of fatty acids and long-chain amines / K. Komura, Yu. Nakano, M. Koketsu // Green Chem. - V. 13. - 2011. - P. 828-831; Авт. свид. SU 1131871, МПК C07C 103/19, C07C 233/06, C07D 211/06, C07D 211/16, C07D 265/30, C07D 295/023, опубл. 1984]. В большинстве случаев катализаторами амидирования являются протонные кислоты или кислоты Льюиса [Intensified Azeotropic Distillation: A Strategy for Optimizing Direct Amidation / Ch. Grosjean, J. Parker, C. Thirsk, A. R. Wright // Org. Process Res. Dev. - V. 16. - 2012. - P. 781-787; Mechanism of arylboronic acid-catalyzed amidation reaction between carboxylic acids and amines / Chen Wang, Hai-Zhu Yu, Yao Fu, Qing- Xiang Guob // Org. Biomol. Chem. - V. 11. - 2013. - P. 2140-2146; Direct Amidation of Carboxylic Acids Catalyzed by ortho-Iodo Arylboronic Acids: Catalyst Optimization, Scope, and Preliminary Mechanistic Study Supporting a Peculiar Halogen Acceleration Effect / N. Gernigon, M. Al-Zoubi Raed, D.G. Hall // J. Org. Chem. - V. 77. - 2012. - P. 8386-8400; Direct amide bond formation from carboxylic acids and amines using activated alumina balls as a new, convenient, clean, reusable and low cost heterogeneous catalyst / S. Ghosh, A. Bhaumik, J. Mondal, A. Mallik, S. Sengupta (Bandyopadhyay), Ch. Mukhopadhyay // Green Chem. - V. 14. - 2012. - P. 3220-3229; Facile one-pot amidation of carboxylic acids by amines catalyzed by triphenylstibine oxide/tetraphosphorus decasulfide(Ph3SbO/P4S10) / N. Ryoki, N. Takahiro, Y. Yasuhiro, M. Haruo // J. Org. Chem. - V. 56. - №12. - 1991. - P. 4076-4078; XtalFluor-E, an Efficient Coupling Reagent for Amidation of Carboxylic Acids / A. Orliac, P.D. Gomez, A. Bombrun, J. Cossy // Org. Lett. - V. 15. - №4. - 2013. - P. 721-976; H. Lundberg, Tinnis F., H. Adolfsson. Titanium (IV) isopropoxide as an efficient catalyst for direct amidation of non-activated carboxylic acids // Synlett - V. 23. - №15. - 2012. - P. 2201-2204; Исследование каталитического синтеза анилида 1-адмантанкарбоновой кислоты / И.А. Новаков, Б.С. Орлинсон, Е.Н. Савельев, Е.А. Потаенкова, М.А. Наход, Д.П. Тараканов, В.В. Коваленко // Известия ВолгГТУ. Сер. Химия и технология элементоорганических мономеров и полимерных материалов. - Волгоград, 2016. - №12(191). - С. 62-64].
Недостатками указанных способов являются большая длительность и высокая температура процесса.
Известен способ прямого амидирования с использованием катализаторов и микроволнового облучения [Borate esters as convenient reagents for direct amidation of carboxylic acids and transamidation of primary amides / Starkov, P., Sheppard T. D. // Org. Biomol. Chem. - V. 9. - 2011. - P. 1320-1323].
Недостатками способа является большая длительность приготовления катализатора и большая длительность процесса.
Известен способ получения амидов взаимодействием карбоновых кислот с первичными и вторичными аминами в присутствии нейтрального коллоидного медного катализатора с азеотропной отгонкой реакционной воды. В качестве исходных карбоновых кислот были использованы масляная, валериановая и изовалериановая кислоты, в качестве исходных аминов - морфолин, пиперидин, циклогексиламин. Реакция амидирования проводилась в среде бензола при 80°С и мольном соотношении кислота: амин 1:1-1.2 в присутствии наночастиц меди [Прямое амидирование карбоновых кислот первичными и вторичными аминами в присутствии коллоидных частиц меди / В.М. Мохов, Ю.В. Попов, И.И. Будко // Известия ВолгГТУ: межвуз. сб. науч. ст. / ВолгГТУ. - Волгоград, 2014. - вып. 12. - С. 52-56].
Недостатком способа является то, что он требует предварительное приготовление катализатора и низкий выход амида 1-адамантанкарбоновой кислоты.
Наиболее близким является способ получения амидов, основанный на одновременном нагревании эквимольных количеств карбоновой кислоты, первичного амина и предварительно приготовленного из пятихлористого фосфора и 4-диметиламинопиридина комплекса, в присутствии основания - акцептора хлороводорода, с последующим выделением продукта реакции обработкой реакционной массы водным раствором щелочи [Комплексы хлоридов кремния и фосфора с азотистыми основаниями как конденсирующие агенты в синтезе амидов / Л.В. Безгубенко, С.Е. Пипко, А.Д. Синица // Журнал общей химии. - 2012. - Т. 82. - Вып. 8. - С. 1302-1310].
Недостатками способа являются протекающие в реакционной массе конкурирующие процессы, которые снижают выходы продуктов реакции (71-73%).
Задачей является разработка нового способа получения ароматических амидов 1-адамантанкарбоновой кислоты.
Техническим результатом является упрощение способа получения ароматических амидов 1-адамантанкарбоновой кислоты и повышение выхода продукта.
Технический результат достигается в способе получения ароматических амидов 1-адамантанкарбоновых кислот, заключающемся во взаимодействии карбоновой кислоты с ароматическим первичным амином в среде абсолютного ацетонитрила в присутствии основания и комплекса хлорида фосфора с 4-диметиламинопиридином, при этом в качестве карбоновой кислоты используют 1-адамантанкарбоновую кислоту, комплекс получают in situ из трихлорида фосфора с 4-диметиламинопиридином, взятых в мольном отношении 1:1, в качестве основания используют триэтиламин, а реакцию ведут при мольном соотношении кислота: амин: основание: комплекс равном 1:1:1:1.
Сущность изобретения заключается в осуществлении процесса в одну стадию в присутствии образованного in situ комплекса из трихлорида фосфора с 4-диметиламинопиридином, с использованием заявленных соотношений компонентов реакции.
где R=H, CH3, R1=H, CH3, NO2, R2=H, C4H9, Cl, Br, CH3; X=CH2, связь. Способ осуществляется следующим образом. В защищенный от влаги реактор, снабженный мешалкой и обратным холодильником, помещают 1-адамантанкарбоновую кислоту, 4-диметиламинопиридин, далее добавляют смесь ароматического амина и триэтиламина, и приливают осушенный ацетонитрил. К полученной смеси при перемешивании, порциями добавляют трихлорид фосфора и кипятят реакционную массу в течение 8 часов. По окончании процесса, реакционную массу выливают в водный раствор гидроксида натрия. Перемешивают в течение 0,5 ч и отфильтровывают выпавший осадок. Полученный продукт промывают водой и сушат на воздухе. Выход продукта составляет 80-88%.
Пример 1. Синтез г4-фенил-1-адамантанкарбоксамида
В защищенный от влаги реактор, снабженный мешалкой и обратным холодильником, помещают 0,9 г (5 ммоль) 1-адамантанкарбоновой кислоты, 0,61 г (5 ммоль) 4-диметиламинопиридина, далее добавляют смесь 0,47 г (5 ммоль) анилина и 0,51 г (5 ммоль) триэтиламина и приливают 4 мл осушенного ацетонитрила. При перемешивании, к полученной смеси порциями добавляют 0,69 г (5 ммоль) трихлорида фосфора и кипятят реакционную массу в течение 8 часов. По окончании процесса, реакционную массу выливают в 20 мл 10% водного раствора гидроксида натрия. Перемешивают в течение 0,5 ч и отфильтровывают выпавший осадок. Полученный продукт промывают водой и сушат на воздухе. Выход N-фенил-1-адамантанкарбоксамида составляет 81%. Тпл. 196-197°С.
Пример 2. Синтез N-(n-бутилфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,75 г (5 ммоль) n-бутиланилина. Выход N-(n-бутилфенил)-1-адамантанкарбоксамида составляет 86%. Тпл. 125-128°С.
Пример 3. Синтез N-(м-нитрофенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,69 г (5 ммоль) м-нитроанилина. Выход N-(м-нитрофенил)-1-адамантанкарбоксамида составляет 80%. Тпл. 184-186°С.
Пример 4. Синтез N-(n-бромфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,86 г (5 ммоль) n-броманилина. Выход 1 N-(n-бутилфенил)-1-адамантанкарбоксамида составляет 87%. Тпл. 225-227°С.
Пример 5. Синтез N-(n-хлорфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,64 г (5 ммоль) n-хлоранилина. Выход N-(n-хлорфенил)-1-адамантанкарбоксамида составляет 87%. Тпл. 206-209°С.
Пример 6. Синтез N-(о-метилфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,54 г (5 ммоль) о-толуидина. Выход N-(о-метилфенил)-1-адамантанкарбоксамида составляет 88%). Тпл. 188-189°С.
Пример 7. Синтез N-(м-метилфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,54 г (5 ммоль) м-толуидина. Выход N-(м-метилфенил)-1-адамантанкарбоксамида составляет 82%. Тпл. 198-200°С.
Пример 8. Синтез N-(n-метилфенил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,54 г (5 ммоль) n-толуидина. Выход N-(n-метилфенил)-1-адамантанкарбоксамида составляет 87%. Тпл. 195-197°С.
Пример 9. Синтез N-(бензил)-1-адамантанкарбоксамида
Синтез осуществляется аналогично примеру 1 с использованием вместо анилина 0,54 г (5 ммоль) бензиламина, в течение 8 часов. Выход N-(n-бутилфенил)-1-адамантанкарбоксамида составляет 80%. Тпл. 172-173°С.
Таким образом, способ получения ароматических амидов 1-адамантанкарбоновых кислот, заключающийся во взаимодействии 1-адамантанкарбоновой кислоты с ароматическим первичным амином в среде абсолютного ацетонитрила в присутствии триэтиламина и полученного in situ комплекса из трихлорида фосфора с 4-диметиламинопиридином, взятых в мольном отношении 1:1, при котором реакцию ведут при мольном соотношении кислота : амин : основание : комплекс равном 1:1:1:1 является простым и обеспечивает повышение выхода продукта.
Способ получения ароматических амидов 1-адамантанкарбоновых кислот, заключающийся во взаимодействии карбоновой кислоты с ароматическим первичным амином в среде абсолютного ацетонитрила в присутствии основания и комплекса хлорида фосфора с 4-диметиламинопиридином, отличающийся тем, что в качестве карбоновой кислоты используют 1-адамантанкарбоновую кислоту, комплекс получают in situ из трихлорида фосфора с 4-диметиламинопиридином, взятых в мольном отношении 1:1, в качестве основания используют триэтиламин, а реакцию ведут при мольном соотношении кислота : амин : основание : комплекс, равном 1:1:1:1.
