Результат интеллектуальной деятельности: Противовирусная активность водного раствора фуллерена
Вид РИД
Изобретение
Изобретение относится к медицине, а именно к этиотропной химиотерапии вирусных инфекций и касается средства на основе фуллерена С60 для ингибирования герпесвирусных инфекций (ГВИ), вызываемых вирусом простого герпеса (ВПГ). Средство может быть использовано в медицине и ветеринарии, для профилактики, общего и местного лечения при заболеваниях, вызванных герпесвирусами.
ВПГ имеет очень широкое распространение в человеческой популяции, им инфицированы до 80-95% населения в разных регионах мира. Существует две разновидности ВПГ - вирус простого герпеса типа 1 (ВПГ-1) и вирус простого герпеса типа 2 (ВПГ-2). ВПГ-1 передается главным образом через оральный контакт и вызывает в большинстве случаев оролабиальный герпес («простуда на губах»). Однако новые данные свидетельствуют о том, что ВПГ-1 также является причиной генитального герпеса. ВПГ-2 обычно передается половым путем, в результате непосредственного контакта и вызывает генитальный герпес. Распространенность ВПГ-1 огромна, этим вирусом инфицированы более 3,7 млрд человек в возрасте до 50 лет, или 67% населения [1]. По данным ВОЗ, смертность, обусловленная ВПГ, занимает второе место среди вирусных заболеваний после гриппа. На территории России и СНГ различными формами ГВИ ежегодно инфицируется около 20 млн человек. Все вышеизложенное позволяет считать ГВИ, и в частности ВПГ-инфекции, важной медико-социальной проблемой современного здравоохранения.
ВПГ вызывает генитальный герпес и передается половым путем. Особенно опасна ВПГ-инфекция для лиц со сниженным иммунитетом. К группам риска относятся беременные женщины, ВИЧ-инфицированные лица, новорожденные дети. У новорожденных детей ВПГ-инфекция может вызвать хориоретиниты, микроцефалию, респираторные дисфункции, задержку развития, инвалидность и смерть [2]. ГВИ урогенитального тракта являются одной из причин бесплодия [3], что негативно влияет на демографическую ситуацию. Первичная инфекция может протекать как в относительно легкой, так и в клинически тяжелой форме, вплоть до смертельного исхода. У большинства взрослых здоровых людей при первичной герпесвирусной инфекции она переходит в латентную форму, при которой вирус находится в нервных клетках в неактивном состоянии. Под влиянием многих факторов различной природы происходит реактивация ВПГ, приводящая к репликации вируса, к появлению клинически выраженных заболеваний, часто - в рекуррентной форме. ВПГ способен поражать различные органы и ткани, в том числе ЦНС, кожные покровы, слизистые оболочки. При диссеминированной инфекции приблизительно у 60% пациентов наблюдаются повреждения кожных покровов и развиваются тяжелые заболевания [4, 5].
Основные методы медикаментозного лечения сводятся к подавлению репродукции ВПГ в период обострения в виде мазей, гелей, суппозиториев. В то же время известные специфические противовирусные препараты (ацикловир - АЦВ), валацикловир, пенцикловир, тубосан), используемые для лечения герпесвирусных инфекций, имеют ряд существенных недостатков. Основной проблемой является устойчивость вируса к действию препаратов, которая развивается при их длительном применении и при рекуррентных заболеваниях [6-8].
Вероятно, важной частью патогенеза инфекции ВПГ является нарушение противо-инфекционного иммунитета. В литературе имеются данные об изменениях иммунного статуса у больных с ВПГ, касающиеся взаимосвязи клинического течения инфекции и особенностей иммунных нарушений [9]. В ряде работ показана эффективность иммуномодуляторов в качестве средств вспомогательного лечения и профилактики ВПГ, которые оказывают противовирусное и иммуномодуляторное действие [10].
АЦВ является золотым стандартом противогерпетического лечения и применяется в форме таблеток, мази, крема и лиофилизата более 30 лет. Однако, он имеет ряд серьезных недостатков, таких как, приобретенная устойчивость для большой части герпесвирусов, низкая биодоступность, плохая растворимость, короткое время жизни в крови, необходимость частого введения достаточно больших доз, что, в свою очередь, вызывает побочные эффекты. [11].
Не менее важная проблема связана с токсичностью применяемых препаратов [12], которая является причиной целого ряда побочных эффектов, в том числе гематологических, мутагенных, канцерогенных и тератогенных [13-16]. При применении современного комплекса терапевтических средств не всегда удается добиться нормализации иммунологических показателей у больных и избежать рецидива. Поэтому поиск новых эффективных низкотоксичных препаратов для терапии герпеса является высоко актуальной задачей.
Следует отметить, что многие недавно предложенные соединения против герпес-вирусной инфекции характеризуются отсутствием надежно установленной химической структуры, токсичностью для клеток человека и невысокой противовирусной активностью. Поэтому, разработка новых препаратов, особенно с механизмом действия, отличающимся от АЦВ, но обладающих высокой анти-ВПГ-активностью и низкой токсичностью, очень важная задача.
Фуллерен С60 - многообещающая субстанция для высокотехнологичных материалов и новых лекарственных средств. С60 и его производные известны как сильные антиоксиданты, и часть из них обладают заметной противовирусной активностью [17]. Установлено, что некоторые производные С60 (аддукты) оказывают ингибирующий эффект на герпесвирусную инфекцию. Так, наиболее близкими примерами к данному изобретению являются противовирусные водорастворимые аминокислотные или дипептидные производные фуллерена С60 [18]. Указанные соединения содержат амино- и карбоксильные группы, благодаря которым производное фуллерена способно растворяться в водных средах. Эти соединения ингибируют развитие ВИЧ- и ЦМВ-инфекций в клеточных культурах in vitro, однако обладают недостаточной эффективностью и не были испытаны для экстренной профилактики инфекции. Кроме того, их предполагаемая структура не была надежно подтверждена.
Известно противовирусное средство на основе полизамещенного (поликарбоксильного) производного фуллерена С60 и его использование для экстренной профилактики in vitro, что при подтверждении действия in vivo может предотвращать передачу ВПГ- и ЦМВ-инфекций при половом контакте [19]. Это соединение проявляет выраженную противовирусную активность in vitro как при ВПГ-, так и ЦМВ-инфекциях в клеточных культурах. Данное изобретение относится к профилактическому применению производного фуллерена С60 на клеточных культурах in vitro, но не показана его терапевтическая активность in vitro и на зараженных животных in vivo. Одна из проблем, которая может затруднить применение указанных соединений, их очевидно высокая стоимость синтеза.
Задача изобретения - использование (применение) против ВПГ-инфекции водного раствора/дисперсии химически немодифицированного фуллерена С60 (dnС60), обладающего высокой биодоступностью и относящегося к группе нетоксичных субстанций.
Простой и эффективный способ получения dnС60 легко масштабируемым диализным методом был недавно описан [20-22]. В структурном отношении dnС60 представляет собой водную дисперсию наночастиц фуллерена С60, содержащих также N-метилпирролидон (МП) (молярное соотношение С60:МП ~2:1) в форме донорно-акцепторного комплекса. Размер наночастиц - 60-80 нм, дзета-потенциал - около -30 мВ, концентрация С60 - 100-500 мг/л (можно варьировать). Спектральные характеристики dnС60: УФ-вид-спектр: 222, 268, 347, полоса 400-600 нм; ИК-Фурье-спектр: 1181, 1427, 575 and 525 cm-1. Масс-спектр: m/z=720 Да.
В ряде работ установлено, что dnС60 является низкотоксичной субстанцией и обладает также выраженной противовоспалительной активностью [23, 24]. Описаны также иммуномодулирующие свойства фуллерена С60 с использованием животных моделей [25, 26]. Совокупность литературных данных позволяет рассматривать фуллерен в качестве нового потенциального лекарственного средства, эффект которого может реализоваться за счет иммуномодулирующей/антиоксидантной активности, хотя молекулярные механизмы его биологического действия еще не установлены. Рассматривая его эффект на ВПГ, нельзя исключить и прямое воздействие фуллерена на компоненты вирусной оболочки, что может приводить к инактивации вириона.
Технический результат предложенного изобретения заключается в вируснейтрализующем действии водного раствора фуллерена dnС60 в отношении ВПГ-1 в культуре клеток и на лабораторных животных.
Изучение противовирусной активности dnС60 осуществляли поэтапно. На первом этапе определяли цитотоксические и противовирусные свойства dnС60 в чувствительной клеточной культуре. Для сравнения использовали данные по цитотоксичности и противовирусной активности референс-препарата АЦВ (Зовиракс®, ГлаксоСмитКляйнВэллком, Великобритания), обладающего анти-ВПГ активностью. На втором этапе проводили тестирование лечебных свойств dnС60 в отношении кожной ВПГ-1-инфекции мышей. В качестве положительного контроля в опытах in vivo использовали 5%-ную мазь для наружного применения АЦВ-Акрихин (ОАО «Акрихин», Моск.обл).
В экспериментах использовали ВПГ-1 (семейство Herpesviridae, HSV-1, референс штамм F). Выбор ВПГ-1 основывается на результатах, свидетельствующих о том, что начиная с 90-х годов, причиной генитального герпеса в 50% случаях является ВПГ-1 [1]. Противовирусную активность dnС60 in vitro анализировали в 3-х схемах применения: профилактической, вирулицидной и лечебной, которые различаются временем внесения тестируемого вещества до и после заражения [27]. Лечебные свойства dnС60 in vivo изучали на экспериментальной модели кожной ВПГ-1-инфекции мышей [28]. Опыты in vitro проводили на культуре клеток почки зеленой мартышки Vero, которые чувствительны к ВПГ-1 и были получены из коллекции культур тканей Института вирусологии им. Д.И. Ивановского федерального государственного бюджетного учреждения «Национальный исследовательский центр эпидемиологии и микробиологии им. почетного академика Н.Ф. Гамалеи» Министерства здравоохранения Российской Федерации. Опыты in vivo проводили на мышах линии DBA, 18-20 грамм, полученных из питомника «Столбовая», Московская область.
Краткое описание фигур.
Для более ясного понимания заявленного изобретения, которое отражено в формуле изобретения, а также для демонстрации его особенностей и преимуществ далее приводится подробное описание со ссылками на фигуры чертежей.
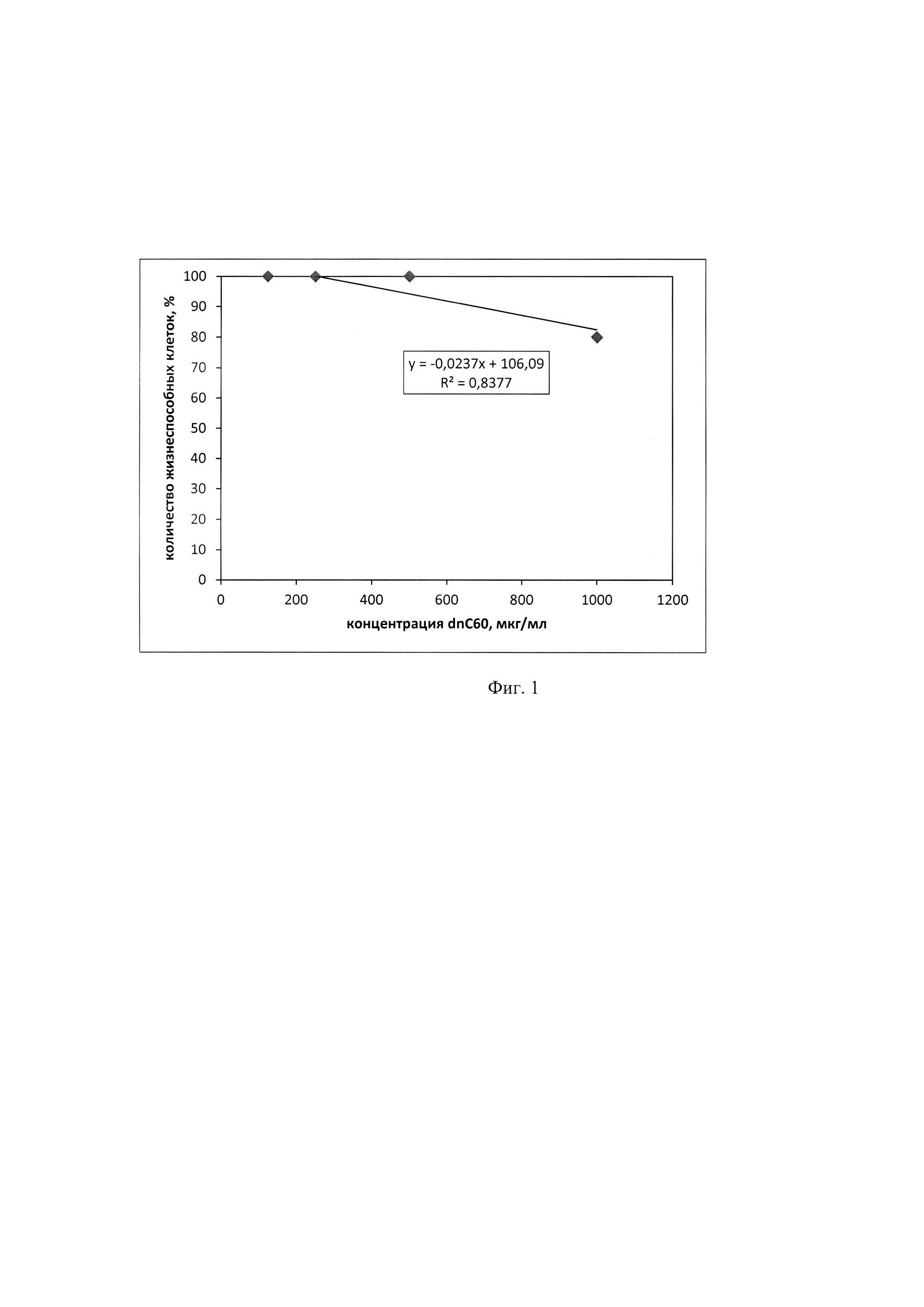
На фиг. 1 представлен график зависимости жизнеспособности клеток Vero от концентрации dnС60 в течение 24 часов воздействия на клетки Vero. На графике показано определение острой цитотоксической дозы (ОЦД50) - концентрации dnС60, при которой наблюдается гибель 50% клеток через 24 часа воздействия. ОЦД50 составила 5300 мкг/мл.
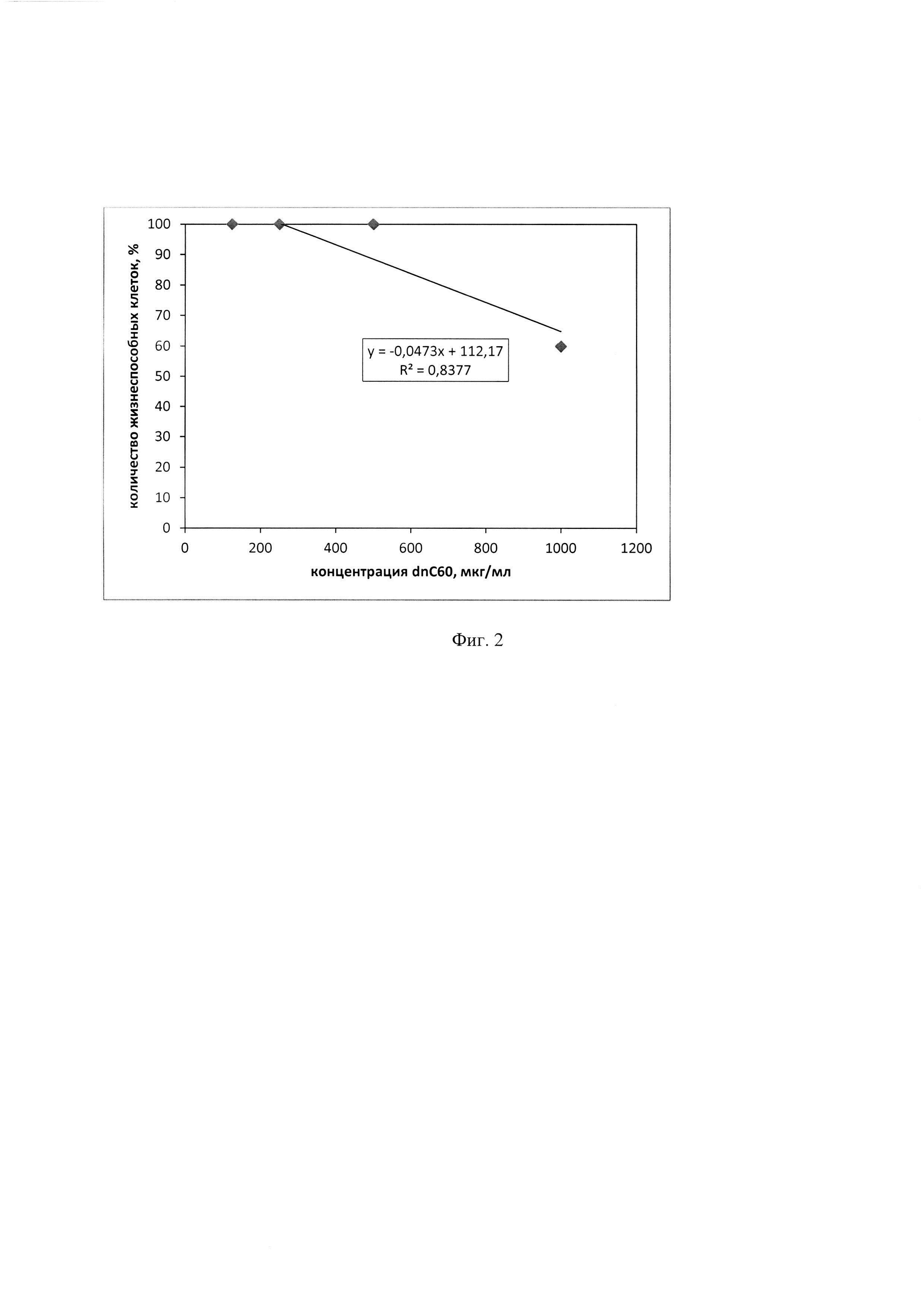
На фиг. 2 представлен график зависимости жизнеспособности клеток Vero от концентрации dnС60 в течение 72 часов воздействия. На графике показано определение хронической цитотоксической дозы (ХЦД50) - концентрации dnС60, при которой наблюдается гибель 50% клеток через 72 часа воздействия. ХЦД50 составила 1240 мкг/мл.
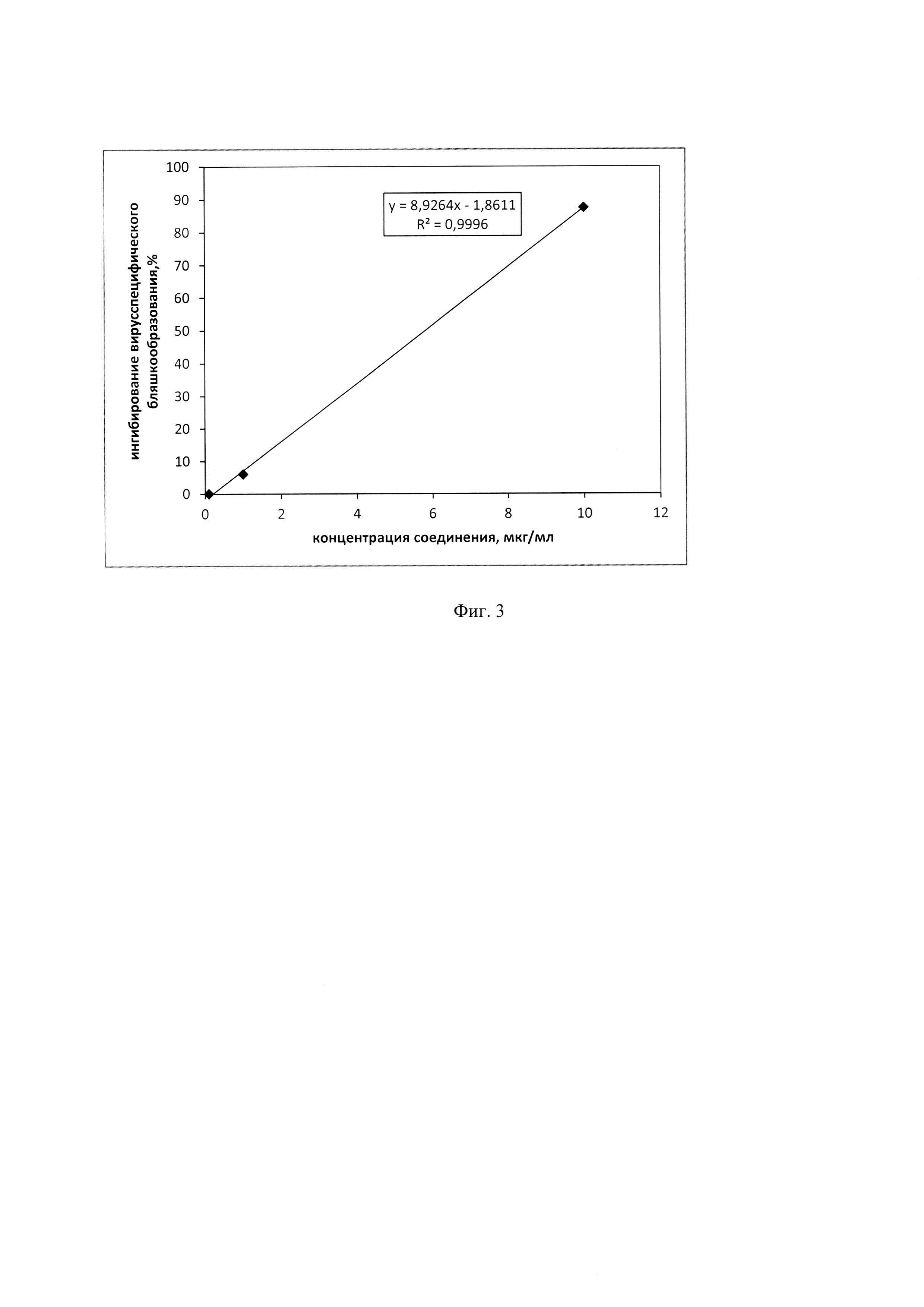
На фиг. 3 представлен график, показывающий зависимость подавления бляшкообразующей способности ВПГ-1 от концентрации dnС60 в профилактической схеме воздействия. На графике показано определение 50% ингибирующей дозы (ИД50) -концентрации dnС60, вызывающей ингибирование бляшкообразования на 50%. ИД50 составила 5,8 мкг/мл.
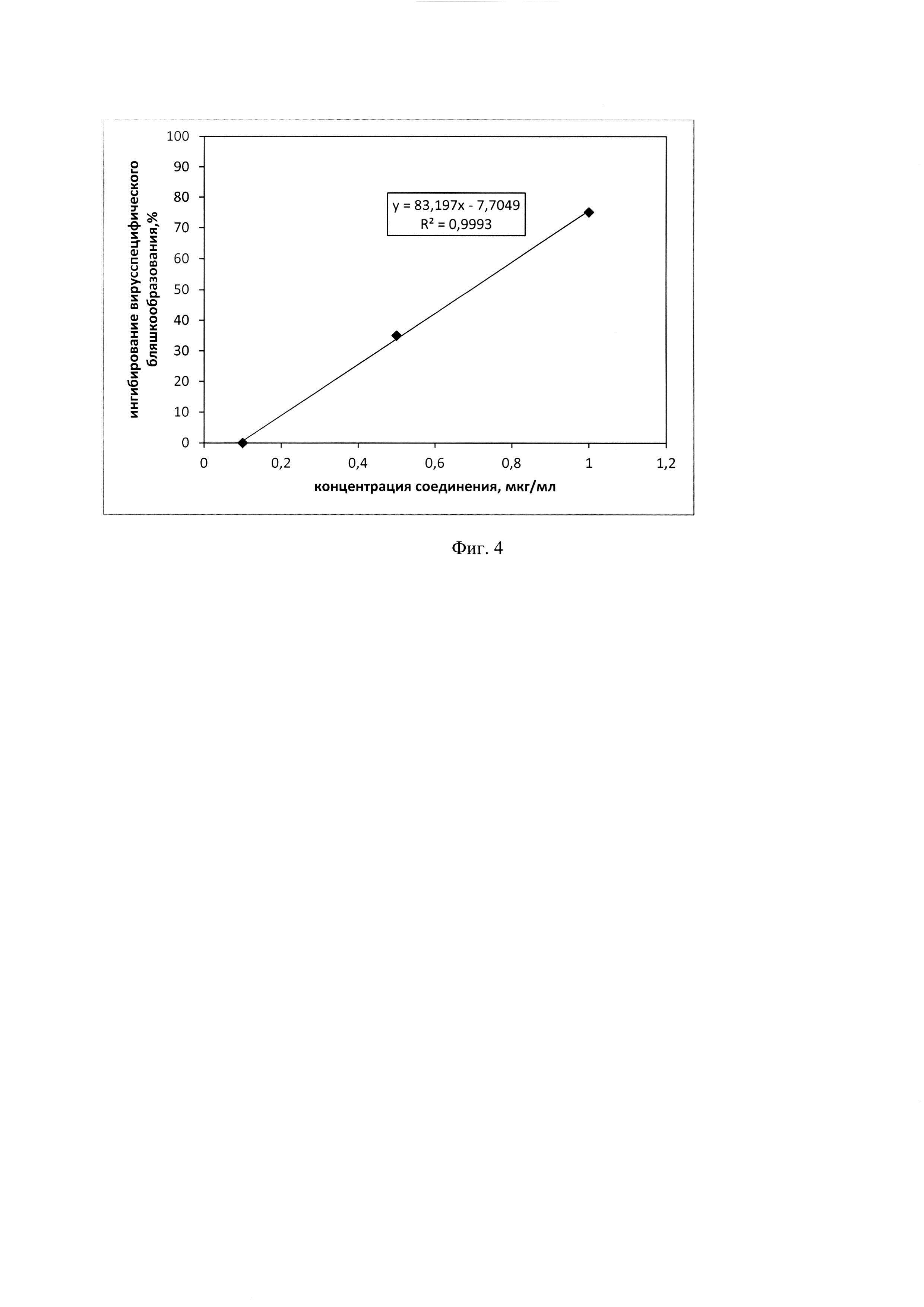
На фиг. 4 представлен график зависимости подавления бляшкообразующей способности ВПГ-1 от концентрации dnС60 в вирулицидной схеме воздействия. На графике показано определение 50% ингибирующей дозы (ИД50) - концентрации dnС60, вызывающей ингибирование бляшкообразования на 50%. ИД50 составила 0,7 мкг/мл.
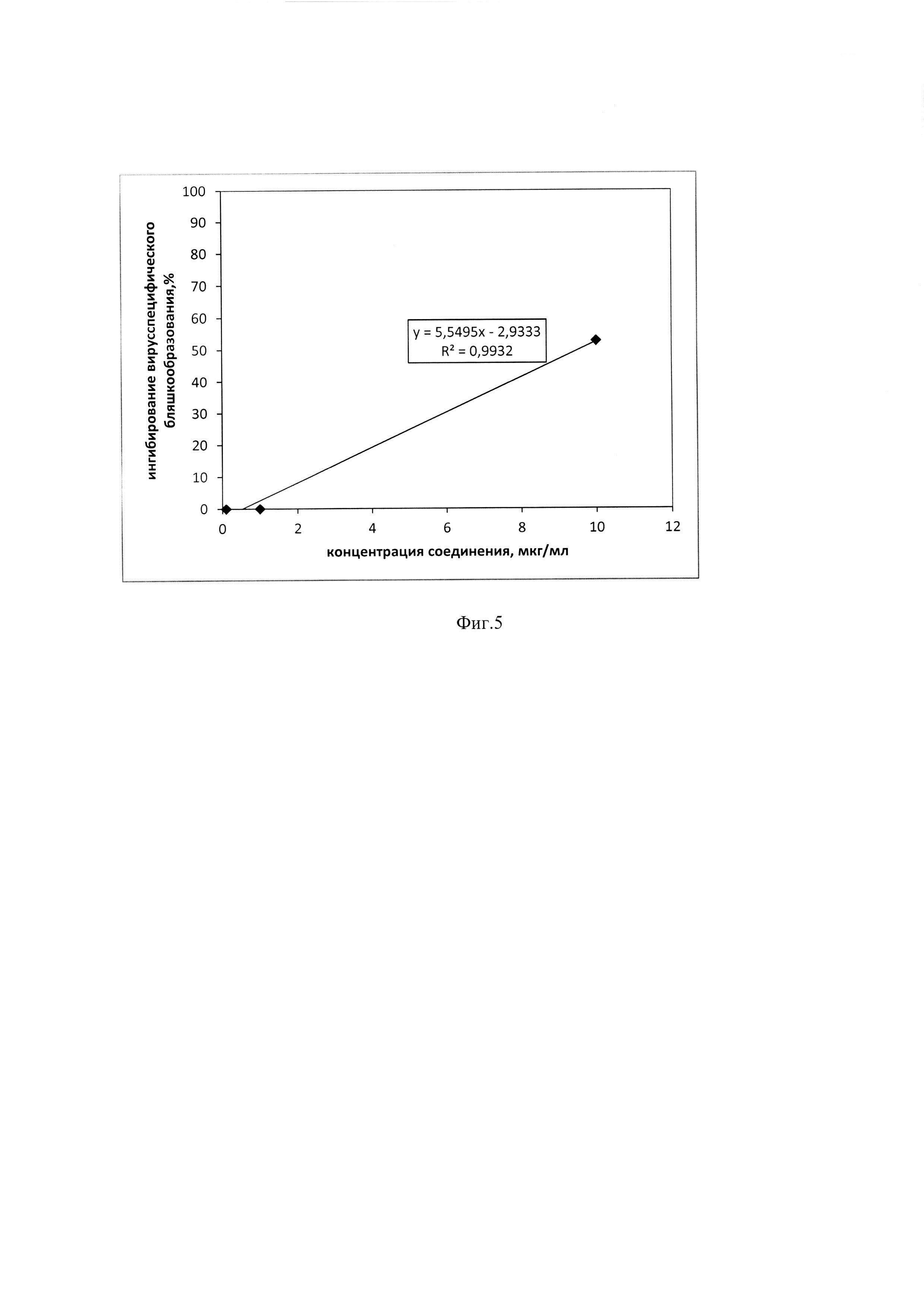
На фиг. 5 представлен график зависимости подавления бляшкообразующей способности ВПГ-1 от концентрации dnС60 в лечебной схеме воздействия. На графике показано определение 50% ингибирующей дозы (ИД50) - концентрации dnС60, вызывающей ингибирование бляшкообразования на 50%. ИД50 составила 9,6 мкг/мл.
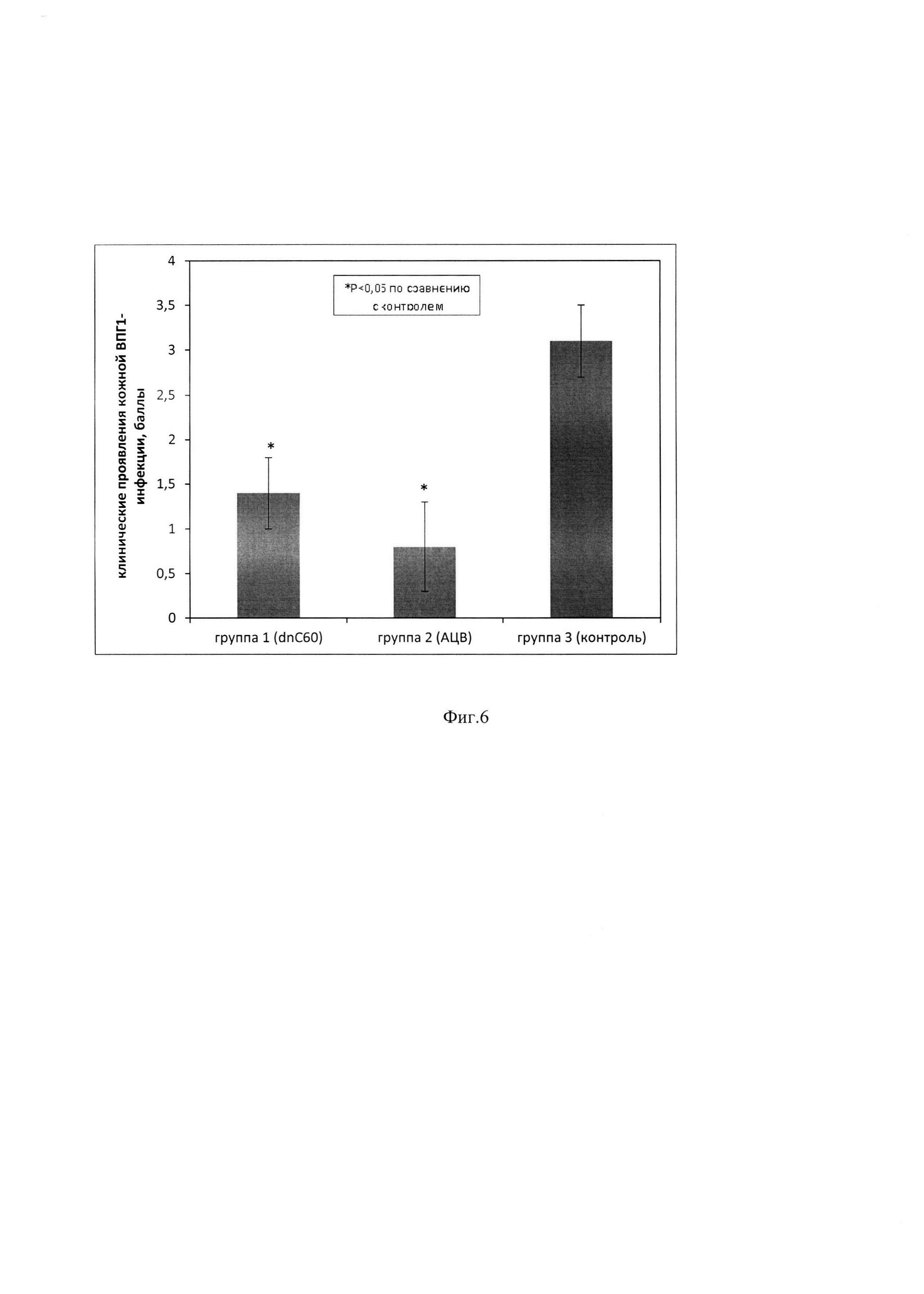
На фиг. 6 представлен график изменений клинических проявлений ВПГ-1-инфекции, оцененных в баллах, при лечении животных dnС60. На графике показано статистически значимое снижение ВПГ-1 специфических поражений кожи у мышей группы 1 и группы 2 по сравнению с контролем (группа 3) и представлено в виде средних значений баллов±стандартное отклонение. Установлено, что на 8 сутки после лечения наступило выздоровление животных.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ ХАРАКТЕРИЗУЕТСЯ СЛЕДУЮЩИМИ ПРИМЕРАМИ.
Получение водной дисперсии фуллерена С60
Для исследования противовирусной активности водную дисперсию фуллерена С60 получали следующим образом. Порошок фуллерена С60 растворяли в N-метилпирролидоне при интенсивном перемешивании на магнитной мешалке до получения раствора с концентрацией 0,8 мг/мл. Полученный темно-фиолетовый раствор фильтровали через стекловолоконный фильтр 3-5 мкм, и к отфильтрованному раствору прибавляли полуторакратный раствор полоксамера 407 в концентрации 0,1 мг/мл. Удаление МП проводили по методу диафильтрации.
Пример 1. Определение цитотоксического действия водной дисперсии фуллерена dnС60 на клетки Vero.
Цитотоксичность определяли по трем параметрам: острая цитотоксическая доза, хроническая цитотоксическая доза и максимально переносимая доза. Клетки инкубировали при температуре 37°С в атмосфере 5% СО2 в присутствии dnС60 в возрастающих концентрациях. Проводили определение острой цитотоксичности через 24 часа после внесения соединения. Хроническую цитотоксичность определяли через 72 часа, максимально переносимую дозу - через 7 суток после внесения соединения. Жизнеспособность клеток определяли по исключению витального красителя трипанового синего. Для этого клетки окрашивали 0,4% раствором трипанового синего и подсчитывали под микроскопом в камере Горяева. Живые клетки оставались неокрашенными, в то время как погибшие в результате токсического действия субстанции окрашивались в ярко-синий цвет. Определяли отношение количества окрашенных клеток к общему количеству клеток в популяции и выражали в процентах (%).
Острая цитотоксическая доза (ОЦД50) dnС60 соответствует концентрации соединения, при которой наблюдалась гибель 50% клеток через сутки после внесения вещества. Хроническая цитотоксическая доза (ХЦД5о) или ЦД50 - концентрации соединения, при которой отмечалась гибель 50% клеток через трое суток после внесения вещества. Максимально переносимая доза (МПД) - концентрация соединения, при которой не выявлено цитопатогенного действия в течение 7 суток после внесения вещества. На основании полученных данных построены графики зависимости количества жизнеспособных клеток от концентраций соединения. Значения ОЦД50 и ЦД50 рассчитаны методом линейной регрессии, с использованием пакета документов Microsoft Excel. Результаты экспериментальной оценки цитотоксического действия соединения -представлены на фиг. 1 и 2.
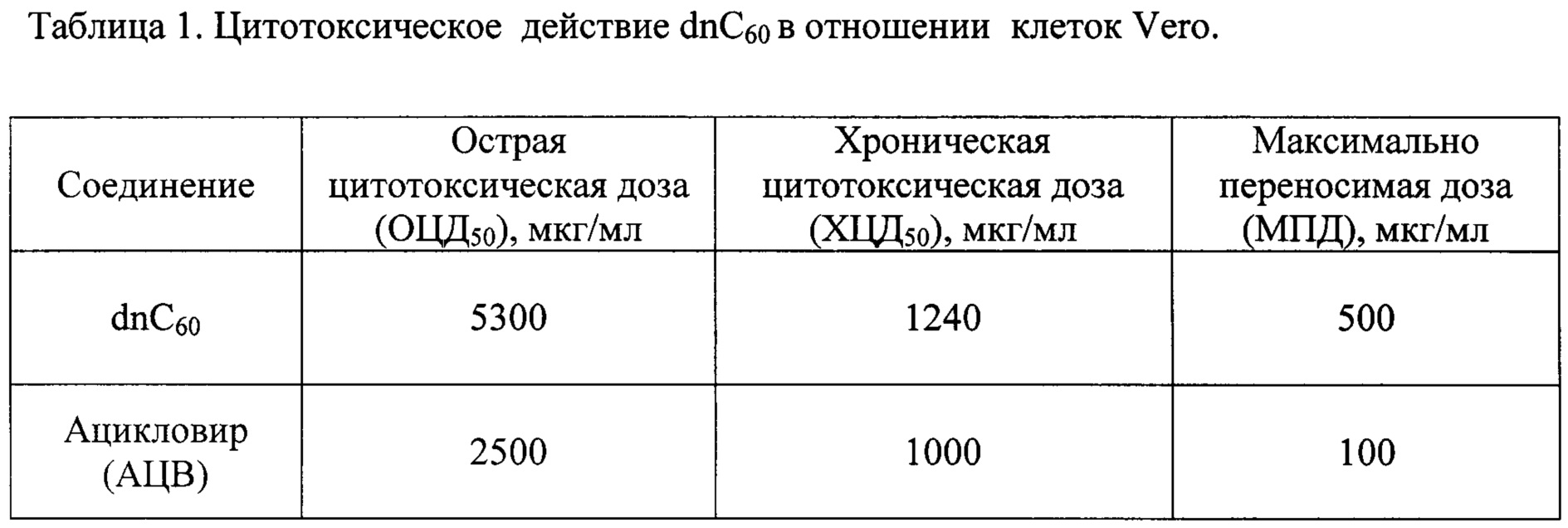
В таблице 1 приведены данные по цитотоксическому действию соединения dnС60 на жизнеспособность клеток Vero. Значения ОЦД50, ХЦД50 (ЦД50) и МПД составили 5300 мкг/мл, 1240 мкг/мл и 500 мкг/мл, соответственно. В качестве сравнения приведены данные о цитотоксичности референс-препарата АЦВ, обладающего анти-ВПГ активностью. Как видно из представленных, цитотоксичность соединения dnС60 ниже, чем токсичность известного патентованного противовирусного препарата АЦВ.
Определение противовирусных свойств dnС60 проведенов клеточной системе in vitro в 3-х схемах применения: профилактической, вирулицидной и лечебной. Для установления противовирусного действия dnС60 определяли концентрацию вещества, вызывающую подавление вирусной активности на 50%. Для оценки вирусной активности использовали способность ВПГ-1 к бляшкообразованию - образованию групп клеток в культуре, содержащих вирусные белки (антигены). Выявление вирусных белков проводили методом иммуноцитохимического окрашивания с использованием моноклональных антител, взаимодействующих с вирусными белками, с последующим подсчетом антиген содержащих клеток (бляшек). Значение концентрации dnС60, вызывающей ингибирование бляшкообразования на 50% по отношению к контролю (ИД50), рассчитывали методом линейной регрессии, с использованием пакета документов Microsoft Excel. Результаты представлены на фиг. 3-5.
Пример 2. Определение противовирусных свойств водной дисперсии фуллерена dnС60 в отношении ВПГ-1-инфекции в профилактической схеме применения.
На монослой клеток Vero наносили соединение dnС60 в различных концентрациях и инкубировали в течение 1 часа при 37°С. Затем соединение отбирали, клетки промывали средой Игла-MEM и заражали ВПГ-1, референс-штамм F, с множественностью инфицирования 10" БОЕ/мл. Контролем служили инфицированные клетки, не обработанные dnС60. Через 48 часов после заражения подсчитывали количество вирусспецифических бляшек в контрольных и опытных образцах. Антивирусную активность соединения оценивали по подавлению способности ВПГ-1 к бляшкообразованию и выражали в процентной доле от контроля. На фиг. 3 представлена зависимость подавления бляшкообразующей способности ВПГ-1 от концентрации dnС60. Концентрацию соединения, вызывающую ингибирование бляшкообразования на 50% по отношению к контролю, принимали за ингибирующую дозу (ИД50). ИД50 dnС60 в профилактической схеме составила 5,8 мкг/мл.
Пример 3. Определение противовирусных свойств водной дисперсии фуллерена dnC6o в отношении ВПГ-1-инфекции в вирулицидной схеме применения.
ВПГ-1, референс-штамм F, с множественностью инфицирования 103- бляшкообразующих единиц в 1 мл (БОЕ/мл) инкубировали совместно с dnС60 в различных концентрациях в течение 1 часа при 37°С. Затем инкубационную смесь наносили на монослой клеток и выдерживали в течение 1 часа при 37°С. Монослой клеток промывали и вносили среду поддержки, состоящую из среды Игла-MEM с добавлением 2% эмбриональной телячьей сыворотки (ЭТС). Контролем служили клетки, не обработанные dnС60. Через 48 часов после заражения подсчитывали количество вирусоспецифических бляшек в контрольных и опытных образцах. Антивирусную активность соединения оценивали по подавлению способности ВПГ-1 к бляшкообразованию и выражали в процентной доле от контроля. На фиг. 4 представлена зависимость подавления бляшкообразующей способности ВПГ-1 от концентраций dnС60. Концентрацию соединения, вызывающую ингибирование бляшкообразования на 50% по отношению к контролю, принимали за ингибирующую дозу (ИД50). ИД50 dnС60 в вирулицидной схеме составила 0,7 мкг/мл.
Пример 4. Определение противовирусных свойств водной дисперсии фуллерена dnС60 в отношении ВПГ-1-инфекции в лечебной схеме применения.
Клеточный монослой Vero заражали ВПГ-1, референс-штамм F, с множественностью инфицирования 10-3 БОЕ/мл и инкубировали в течение 1 часа при 37°С. Затем вирус отбирали, клетки промывали средой Игла-MEM и наносили соединение dnС60 в различных концентрациях на 1 час при 37°С. Затем соединение отбирали, клетки промывали средой Игла-MEM и вносили среду поддержки, состоящую из среды Игла-MEM с добавлением 2% ЭТС. Контролем служили инфицированные клетки, не обработанные dnС60. Через 48 часов после заражения подсчитывали количество вирусспецифических бляшек в контрольных и опытных образцах. Антивирусную активность соединения оценивали по подавлению способности ВПГ-1 к бляшкообразованию и выражали в процентной доле от контроля. На фиг. 5 представлена зависимость подавления бляшкообразующей способности ВПГ1 от концентрации dnС60. Концентрацию соединения, вызывающую ингибирование бляшкообразования на 50% по отношению к контролю, принимали за ингибирующую дозу (ИД50). ИД50 dnС60 в лечебной схеме составила 9,6 мкг/мл.
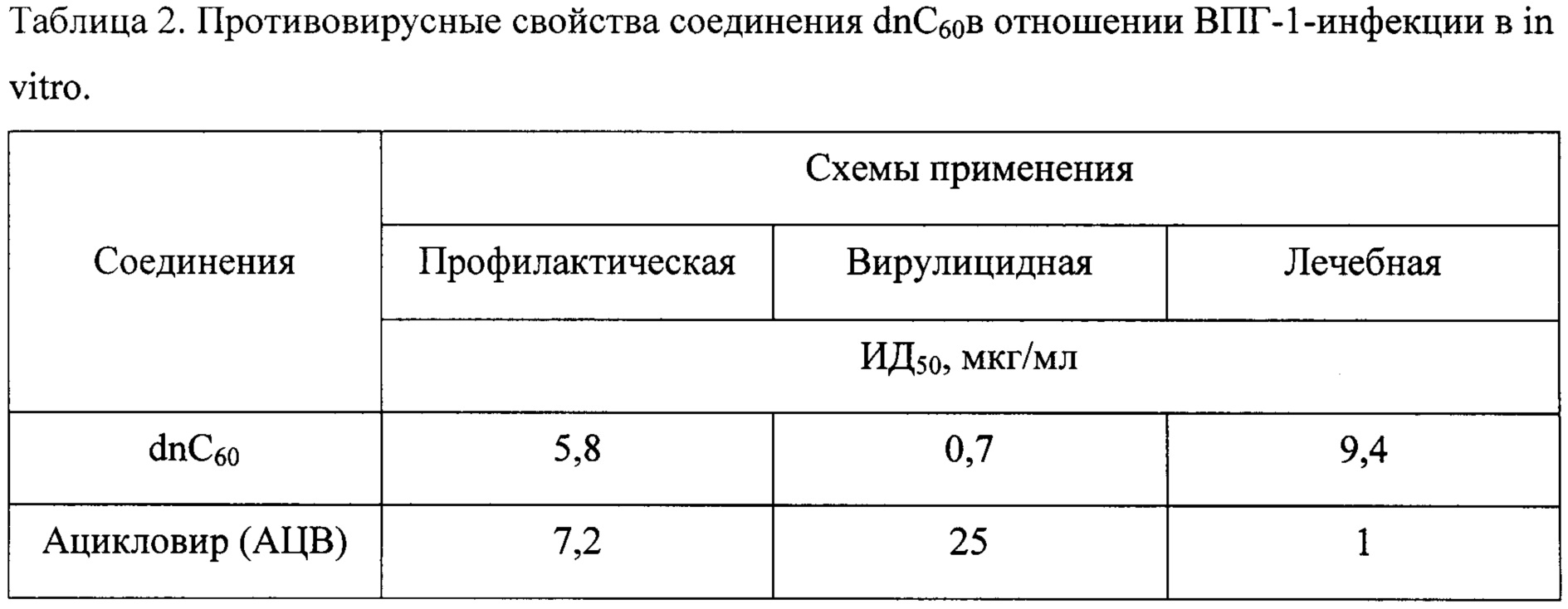
В таблице 2 суммированы данные по противовирусной активности соединения dnС60 в отношении ВПГ1-инфекции в культуре клеток Vero in vitro в 3-х схемах воздействия.
Химиотерапевтическая оценка водной дисперсии фуллерена dnС60.
Для оценки перспективности применения dnС60 как возможного химиотерапевтического средства был рассчитан химиотерапевтический индекс (ХТИ), который характеризует специфическую противовирусную активность препаратов по формуле:
Хти=ХЦД50/ИД50,
где ХЦД50 - концентрация соединения, вызывающая снижение жизнеспособности клеток на 50% через 72 часа после внесения вещества;
ИД50 - концентрация соединения, подавляющая бляшкообразующую способность вируса на 50%.
Установлено, что ХТИ dnС60 в профилактической схеме применения составляет 213, в вирулицидной схеме - 1771, в лечебной схеме - 132. Превышение значения ХТИ, равного 100, свидетельствует о высокой противовирусной активности dnС60.
Определение противовирусной активности dnС60 в отношении кожной ВПГ1-инфекции в лечебной схеме применения invivo.
Для установления лечебного действия водной дисперсии фуллерена dnС60 определяли способность dnС60, нанесенного накожно, снижать клинические проявления ВПГ 1-инфекции, которые оценивали по баллам от 0 до 6: 0 - без изменений, 1 - покраснение, набухание; 2 - единичные эрозии; 3 - многочисленные эрозии; большое эрозивное изъязвление; 5 - паралич задних конечностей, агрессивность, потеря веса на 20%; 6 - смерть.
Оценка противовирусного действия по балльной системе проведена согласно протоколу, опубликованному и апробированному в ряде работ [28].
Пример 5. Определение лечебных свойств dnС60 на модели кожной ВПГ-1-инфекции мышей.
Участки спины мышей химически депилировали, через 24 ч скарифицировали и наносили 0,1 мл ВПГ-1, референс-штамм F, с множественностью инфицирования 1x106 БОЕ/мл. Через 24 часа мышам группы 1 на зараженные участки наносили dnС60 в концентрации 10 мкг/мышь. Мышей группы сравнения (группа 2) обрабатывали 5%-ной АЦВ-мазью, концентрация действующего вещества составила 5 мг/мышь. Мышам контрольной группы 3 наносили 0,1 мл физиологического раствора. Указанную обработку проводили 1 раз в день в течение 3 дней. В каждой группе использовали по 5 животных. Результаты лечения анализировали по развитию ВПГ-1-специфического поражения кожи в течение 10 дней и представляли в баллах. На фиг. 6 представлены данные оценки лечебного эффекта дисперсной формы dnС60 в отношении кожной ВПГ-1-инфекции in vivo. Клинические проявления герпетического поражения кожи в контрольной группе 3 составляли в среднем 3,1±0,4 балла, при этом 2 из 5 животных погибли. В группах 1 и 2 все животные были живы на протяжении всего срока наблюдения. В результате лечения статистически значимое снижение герпетического поражения кожи по сравнению с контролем наблюдали в группе 1 (dnС60) и в группе 2 (АЦВ), средние значения составляли 1.4±0.4 балла и 0.8±0.5 балла соответственно. Статистическая обработка результатов с использованием компьютерных программ Statistica 6,0 показала, что лечебный эффект в группах 1 и 2 был статистически значимым (Р<0,05). Полученные результаты позволяют заключить, что раствор dnС60 проявляет выраженную терапевтическую активность против ВПГ-1-инфекции. При этом его лечебный эффект сопоставим с АЦВ, которой использовался в качестве референс-препарата в форме мази, даже при использовании в 500 раз меньшей концентрации.
Таким образом, водный раствор фуллерена dnС60, применяемый в качестве противовирусного средства, обладает низкой цитотоксичностью in vitro. Хроническая цитотоксическая доза dnС60 составляет 1240 мкг/мл в отношении клеток Vero. Препарат dnС60 проявляет выраженную вирулицидную (вируснейтрализующую), профилактическую, а также лечебную активность в отношении ВПГ-1-инфекции in vitro, ИД50 составляет 0,7 мкг/мл; 5,8 мкг/мл и 9,6 мкг/мл соответственно. Препарат характеризуется высоким ХТИ при профилактическом, вирулицидном и терапевтическом действии - более 100.
Важно отметить, что dnС60, использованный в дозе 10 мкг С60/животное, проявил лечебные эффект в отношении кожной ВПГ-1-инфекции в 500 раз меньшей концентрации по сравнению с АЦВ.
Представленные данные подтверждают перспективность использования соединения dnС60, как обладающего противогерпетическим действием, в качестве химиотерапевтического средства или биологически активной субстанции в составе разных лекарственных форм для профилактики, общего лечения или местного применения при заболеваниях, вызванных герпесвирусами.
Список литературы.
1. Looker K.J., Magaret A.S., May M.T., Turner K.M., Vickerman P., Gottlieb S.L. et al. Global and Regional Estimates of Prevalent and Incident Herpes Simplex Virus Type 1 Infections in 2012. PLoS One. 2015; 10 (10): e0140765.
2. Otto W.R., Myers A.L., L aRussa В., Kimberlin D.W., Jackson M.A. Clinical Markers and Outcomes of Neonates With Herpes Simplex Virus Deoxyribonucleic Acid Persistence in Cerebrospinal Fluid in Disseminated and Central Nervous System Infection. J Pediatric Infect Dis Soc. 2017. May 16. doi: 10.1093/jpids/pix033.
3. Naumenko V.A., Tyulenev Y.A., Yakovenko S.A., Kurilo L.F., Shileyko L.V., Segal.A.S., Zavalishina L.E., Klimova R.R., Tsibizov A.S., Alkhovskii S.V., Kushch A.A. Detection of human cytomegalovirus in motile spermatozoa and spermatogenic cells in testis organotypic culture. Herpesviridae. 2011;2 (1): 7-15.
4. Kimberlin D.W., Lin C.-Y., Jacobs R.F. et al., Natural history of neonatal herpes simplex virus infection in the acyclovir era. Pediatrics. 2001; 108 (2): 223-229.
5. James S.H., Kimberlin D.W. Neonatal Herpes Simplex Virus Infection. Infect_Dis Clin North Am. 2015; 29 (3): 391-400.
6. P.A. Furman, D.M. Coen, M.H. St.Clair and P.A.Schaffer. Acyclovir-resistant mutants of herpes simplex virus type 1 express altered DNA polymerase or reduced acyclovirphosphorylating activities. J. Virol. 1981; 3: 936-941.
7. Erice A. Resistance of human cytomegalovirus to antiviral drugs. Clin Microbiol Rev. 1999; 12: 286-297.
8. Bhorade S.M., Lurain N.S., Jordan A., Leischner J., Villanueva J., Durazo R., Creech S., Vigneswaran W.T., Garrity E.R. Emergence of ganciclovir-resistant cytomegalovirus in lung transplant recipients, J Heart Lung Transplant. 2002; 21: 1274-1282.
9. Любошенко T.M. Клинико-иммунологические аспекты инфекции, вызванной вирусом простого герпеса Международный научно-исследовательский журнал, №1 (43), часть 3. DOI: 10.18454/IRJ.2016.43.053
10. McGowin C.L., PylesR.B. Mucosal treatments for herpes simplex virus: in sight son targeted immunoprophylaxis and therapy. Future Microbiol. 2010; 5: 15-22.
11. A. H. Коровина, M. К. Куханова, С.H. Кочетков. Поиск ингибиторов репликации вируса герпеса: 30 лет после ацикловира. Biotechnologia Acta. 2013; 6 (4): 78-85.
12. Faulds D., Heel R. Ganciclovir. Are view fits antiviral activity, pharmacokinetic properties and therapeutic efficacy in cytomegalovirus infections. Drugs. l990; 39: 597-638.
13. Kimberlin D.W., Whitley R. Antiviral therapy of HSV-1 and -2. In: Human Herpesviruses. Cambridge University press, ed. by Ann Arvin et al. 2007: 1153-1174.
14. Lam N.N., Weir M.A., Yao Z., Blake P.G., Beyea M.M., Gomes Т., Gandhi S., Mamdani M., Wald R., Parikh C.R., Hackam D.G., Garg A.X. Risk of acute kidney injury from oral acyclovir: a population-based study. Am J Kidney Dis. 2013; 61 (5): 723-729.
15. Samir S. Shah, Paul L. Aronson, Zeinab Mohamad, Scott A. Lorch Delayed Acyclovir Therapy and Death Among Neonates With Herpes Simplex Virus Infection. Pediatrics. 2011; 128 (6): 1153-1160.
16. Goli R, Mukku KK, Devaraju SB, Uppin MS Acyclovir-induced thrombotic microangiopathy // Indian J Nephrol. 2017; 27 (2): 131-132.
17. Пиотровский Л.Б., Киселев О.И. Фуллерены в биологии СПб.: Росток. 2006. 336 с.
18. Миллер Г.Г., Кущ А.А., Романова B.C. Средство для ингибирования ВИЧ и ЦМВ-инфекций и способах ингибирования. Патент RU 2196602, 2003.
19. Кущ А.А, Климова P.P., Федорова Н.Е., Трошин П.А., Корнев А.Б. Применение поликарбоксильного производного фуллерена в качестве микробицидного противовирусного средства. Патент RU 2533232, 20.07.2012.
20. Андреев СМ., Башкатова Е.Н., Хаитов М.Р., Пургина Д.Д. Способ получения водных нанодисперсий фуллерена. Патент RU 2548971, 22.04.2013.
21. Андреев СМ., Пургина Д.Д., Башкатова Е.Н., Гаршев А.В., Маерле А.В., Хаитов М.Р. Эффективный способ получения водных нанодисперсий фуллерена С60. Российские нанотехнологии, 2014; 7-8: 11-17.
22. Andreev S., Purgina D., Bashkanova В., Garshev A., Maerle A., Andreev I., Osipova N., Shershakova N., Khaitov M. Study of fullerene aqueous dispersion prepared by novel dialysis method.Simple way to fullerene aqueous solution. Fullerenes Nanotubes and Carbon Nanostructures. 2015. DOI: 10.1080 / 1536383X.2014.998758.
23. Shershakova N., Baraboshkina E., Andreev S., Purgina D., Struchkova I., Kamyshnikov O., Nikonova A., Khaitov M. Anti-inflammatory effect of fullerene С60 in a mice model of atopic dermatitis. Journal of Nanobiotechnology. 2016; 14: 8. DOI: 10.l 186/sl2951-016-0159-z.
24. Шершакова H.H., Барабошкина E.H., Андреев СМ., Шабанова Д.Д., Смирнов В.В., Хаитов М.Р. Отсутствие острой токсичности у водного раствора фуллерена С60-Иммунология. 2016; 37 (6): 325-329.
25. Веснина Л.Э. и др. Фуллерен С60 обладает иммуномодулирующей активностью при адъювантном артрите у крыс. Экспериментальная и клиническая фармакология. 2012; 75 (8): 15-20.
26. Башкатова Е.Н. и др. Изучение модулирующей активности производных фуллерена С60 на реакцию гиперчувствительности замедленного типа. Физиология и патология иммунной системы. 2012; 16 (2): 17-27.
27. Talaei Zanjani N., Miranda-Saksena M., Valtchev P., Diefenbach R.J., Hueston L., Diefenbach E., Sairi F., Gomes V.G., Cunningham A.L., Dehghani F. Abalone Hemocyanin Blocks the Entry of Herpes Simplex Virus 1 into Cells: a Potential New Antiviral Strategy. Antimicrob Agents Chemother. 2015; 60 (2): 1003-12. DOI: 10.1128/AAC.01738-15.
28. Lipipun V., Sasivimolphan P., Yoshida Y., Daikoku Т., Sritularak В., Ritthidej G., Likhitwitayawuid K., Pramyothin P., Hattori M., Shiraki K. Topical cream-based oxyresveratrol in the treatment of cutaneous HSV-1 infection in mice. Antiviral Res. 2011;91(2):154-60.