Результат интеллектуальной деятельности: СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕЦИДИВИРУЮЩЕГО ИНФАРКТА МИОКАРДА ПОСЛЕ ПОВТОРНОГО ИНФАРКТА МИОКАРДА У МУЖЧИН МОЛОЖЕ 60 ЛЕТ
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к области кардиологии и прогнозирования развития исходов повторного инфаркта миокарда (ИМ).
Улучшение результатов лечения ИМ и профилактика его осложнений являются приоритетными задачами отечественного здравоохранения. Это обусловлено высокой инвалидизацией и смертностью от ИМ среди мужчин молодого и среднего возраста (Гарганеева А.А. Догоспитальная летальность от острого инфаркта миокарда среди больных молодого и среднего возраста как индикатор социальной напряженности: можно ли изменить сложившуюся ситуацию? / А.А. Гарганеева, К.Н. Борель, С.А. Округин // Сердце: журнал для практикующих врачей. - 2015. - Т. 14, №5 (85). - С. 281-286). В последние годы отмечается снижение показателей смертности, более выраженное у проживающих в городах мужчин. Однако в целом изменения с 2005 по 2014 г. признаются несущественными (Демографический ежегодник России. 2015: Стат. сб. Росстат. - М., 2015. - 263 с). Число повторных и рецидивирующих ИМ на фоне активного хирургического лечения существенно возросло (Шальнова, С.А. Смертность населения 55 лет и старше и ее ассоциации с ишемической болезнью сердца, традиционными факторами риска и маркерами воспаления: результаты проспективного когортного исследования / С.А. Шальнова, А.Э. Имаева, А.В. Капустина // Рос. кардиол. журн. - 2016. - №6(134). - С. 15-19). В связи с этим в настоящее время необходимость прогнозирования осложнений повторного ИМ увеличивается. Для оценки риска неблагоприятных событий, включающих рецидивирующий ИМ, выбора тактики лечения в практической деятельности в настоящее время используются прогностические индексы (NORRIS, GRACE, TIMI и др.) (Руда, М.Я. Диагностика и лечение больных острым инфарктом миокарда с подъемом сегмента ST электрокардиограммы. Клинические рекомендации/ М.Я. Руда и др. // Кардиол. вестн. - 2014. - №4. - С. 1-58.; Norris, R.M. Prognosis after myocardial infarction. Six-year follow-up / R.M. Norris, D.E. Caughey, C.J. Mercer // Br. Heart. J. - 1974. - Vol. 36, №8. - P. 786-790.; Fox, K.A. Should patients with acute coronary disease be stratified for management according to their risk? Derivation, external validation and outcomes using the updated GRACE risk score [electronic resource] / K.A. Fox, G. Fitzgerald, E. Puymirat // BMJ Open. - 2014. - Vol. 4, №2. - P. e004425). Установлены недостатки шкал GRACE и TIMI из-за несоответствия их результатов реальной российской клинической практике (Особенности прогнозирования при остром коронарном синдроме у мужчин и женщин / Р.Т. Сайгитов, М.Г. Глезер, Д.П. Семенцов и др. // Кардиоваскулярная терапия и профилактика. - 2006. - №1. - С. 63-70.; Эрлих А.Д. Острый коронарный синдром без подъема сегмента ST в реальной практике лечебных учреждений России. Сравнение данных регистров РЕКОРД2 и РЕКОРД / А.Д. Эрлих, Н.А. Грацианский // Кардиология. - 2012. - №52(10). - С. 9-16.; Ложкина, Н.Г. Острый коронарный синдром: клинические, биохимические и молекулярно-генетические аспекты отдаленного прогнозирования: дис. … д-ра мед. наук/ Н.Г. Ложкина. - Новосибирск., 2015. - 248 с). Эти шкалы, в первую очередь, оценивают риск неблагоприятного исхода. Они разработаны на основе изучения американской и европейской популяции. Шкалы NORRIS, TIMI и GRACE обладают небольшой чувствительностью для мужчин моложе 60 лет из-за малого числа «конечных точек» при прогнозировании на ближайший период. Так шкала TIMI дифференцирует риск неблагоприятного исхода, начиная с возраста пациентов 65 лет. Исследователи отмечают недостаточную точность индекса NORRIS (Лещинский Л.А. и соавт., патент РФ №2114552, А61В 5/02, опубл. 10.07.1998). Для повышения точности шкала GRACE требует для расчета вероятности неблагоприятных исходов результаты биохимических исследований крови (кардиоспецифические ферменты, креатинин), а модели Ложкиной Н.Г. (Ложкина, Н.Г. Острый коронарный синдром: клинические, биохимические и молекулярно-генетические аспекты отдаленного прогнозирования: дис. … д-ра мед. наук/ Н.Г. Ложкина. - Новосибирск., 2015. - 248 с.) - высокочувствительного C-реактивного белка и генетических маркеров атеросклероза. Для этого необходимы дополнительное оборудование, умение и время. Ранее для оценки риска неблагоприятных событий (включающих рецидивирующий ИМ) при ИМ и острых коронарных синдромах применялись также системы S. Schnur (Schnur S. Mortality rates in acute myocardial infarction. The normal yearly variation, and the effect of hospital admission policy / S. Schnur // Ann. Intern. Med. - 1953. - Vol. 39, №5. - P. 1014-1017), A.A. Peel et al. (A coronary prognostic index for grading the severity of infarction / A.A. Peel, T. Semple, I. Wang et al. // M. Br. Heart. J. - 1962. Vol. 24, №6. - P. 745-760), J.L. Willems et al. (Willems J.L. Early risk stratification using clinical findings in patients with acute myocardial infarction / J.L. Willems, J. Pardaens, H. De Geest // Eur. Heart J. - 1984. Vol. 5, №2. - P. 130-139.), А.Л. Сыркина и И.М. Гельфанд (Типы клинического течения острого периода инфаркта миокарда и их прогностическое значение / А.Л. Сыркин, И.М. Гельфанд, Б.И. Розенфельд и др. // Кардиология. - 1986. - №9. - С. 9-12.), Дымочкин В.Н. и соавт. (патент РФ №2121691, G01N 33/86, опубл. 10.11.1998), Барбараш О.Л. и соавт. (патент РФ №2436501, А61В 5/02 G01N 33/48, опубл. 20.12.2011), А.А. Дзидзинского и соавт. (патент РФ 22765733 А61В 5/00, А61В 5/02, опубл. 20.05.2006), PREDICT, PURSUIT, GUSTO и др. Эти оценочные системы, главным образом, ориентированы на определение риска неблагоприятного исхода и требуют разнообразных дополнительных исследований.
Другие близкие способы: способ прогнозирования возможности возникновения рецидивирующего ИМ по Н.С. Сазоновой и соавт. (А61В 5/00, опубл. 10.02.2003) учитывает также результаты лабораторных исследований (число лейкоцитов, уровень активности кардиоспецифических ферментов, концентрацию фибриногена), требует оригинального программного обеспечения и несколько громоздкий по вычислению. Он применим ко всем видам ИМ и не дифференцирует риск рецидивирующего ИМ по полу. Алгоритм, предложенный В.М. Клюжевым и соавт. (патент РФ 2197173 А61В 5/02), нацелен на раннее выявление неблагоприятных исходов ИМ, осложнений заболевания для превентивного лечения. Он обладает системным подходом, предусматривает поэтапный анализ клинико-лабораторных и инструментальных данных и требует обучения для своего выполнения. Способ прогнозирования острого ИМ по Чалык Н.Е. (патент РФ 2105981, G01N 33/52, опубл. 27.02.1998) использует для анализа дополнительно результаты определения свечения кэпов мембран нейтрофилов в первые, седьмые, 14 и 21 сутки заболевания. Способ прогнозирования ранней постинфарктной стенокардии у пациентов с острым ИМ с подъемом сегмента ST в госпитальном периоде по Барбараш О.Л. и соавт. (патент РФ №2543356, G01N 33/50, опубл. 27.02.2015) относится только к упомянутой категории пациентов и ситуациям. Он требует выполнения эхокардиографии, параметров липидограммы, в том числе окисленных липопротеинов низкой плотности. Способы прогнозирования развития сердечно-сосудистых осложнений после перенесенного ИМ с подъемом сегмента ST у больных с тревожно-депрессивными расстройствами и без них по М.С. Черняевой и соавт. (патент РФ №2593791, G01N 33/49, опубл. 10.08.2016 и патент РФ №2593791, G01N 33/49, опубл. 10.08.2016) относится только к указанному варианту ИМ. Они оценивают риск сердечно-сосудистых осложнений на основании определения НАДФН-зависимой глутаматдегидрогеназы, НАДН-зависимой глутаматдегидрогеназы, глутатионредуктазы, лактат дегидрогеназы (НАДН-зависимой), малат дегидрогеназы (НАДН-зависимой) и изоцитрат дегидрогеназы (НАДН-зависимой) в тромбоцитах. Способ прогнозирования течения острого ИМ по М.В. Кудряшовой и соавт. (патент РФ 2395088 G01N 33/49, опубл. 20.07.2010) дает возможность оценить вероятность развития осложнений ИМ (аритмий, тромбоза желудочка, аневризмы сердца) и повторного ИМ с помощью показателей агрегации тромбоцитов. Способ прогнозирования риска внезапной смерти после ИМ по B.C. Жук и соавт. (патент РФ 2217044 А61В 5/02, А61В 5/0452 опубл. 27.11.2003) требует для расчетов риска внезапной смерти выполнения ортостатической пробы и пробы с глубоким дыханием. Способ проведения предупреждающего обезболивания у больных осложненным ИМ по Б.И. Барташевич и соавт. (патент РФ 2526801 А61К 31/4748, А61Р 9/10 опубл. 27.08.2014) нацелен на профилактику рецидивирующих поражений. Для его выполнения требуется мониторинговый контроль параметров вегетативной нервной системы, катетеризации эпидурального пространства и выполнение эпидуральной анестезии. Способ прогнозирования повторного ИМ по Гидрасовой Р.А. и соавт. (патент РФ №2424531, G01N 33/72, опубл. 20.07.2011) учитывает вероятность развития рецидивирующих поражений, но он не дает сведений о чувствительности и специфичности методики и для выполнения требует дополнительного определения окисленномодифицированных липопротеидов и внеэритроцитарного гемоглобина.
Таким образом, предложено много способов прогнозирования развития рецидивов ИМ и повторных случаев, однако большинство из них не дифференцированы в отношении именно рецидивирующего поражения, а учитывают сочетания осложнений или все случаи с неблагоприятными исходами. Среди предложенных способов нет тех, которые применимы для мужчин моложе 60 лет и рассчитаны для повторного ИМ. Помимо этого, все перечисленные выше способы требуют дополнительных, (нередко) высокотехнологичных исследований, дополнительных затрат времени и ресурсов.
Следует признать, что результаты современных методов лечения улучшают ситуацию в предупреждении осложнений и смерти от ИМ среди мужчин трудоспособного возраста. Однако широкое внедрение этих методов привело к увеличению числа повторных и рецидивирующих поражений. В связи с этим имеется необходимость научного поиска способов повышения эффективности прогнозирования и профилактики развития рецидивирующего ИМ дифференцировано при первичных и при повторных ИМ.
Цель изобретения - повысить эффективность прогнозирования развития рецидивирующего инфаркта миокарда при повторном инфаркте миокарда у мужчин моложе 60 лет для улучшения профилактики этого состояния. В основу изобретения положена задача - создать такой способ оценки вероятности прогноза развития рецидивирующего ИМ при повторных поражениях, который, используя обычные клинические данные, с учетом особенностей актуальной группы пациентов, дает возможность его расчета и оценки и не требует дополнительных исследований, вмешательств, квалификации и ресурсов для его определения.
Решение поставленной задачи обеспечивается тем, что в способе прогнозирования развития рецидивирующего поражения при повторных ИМ у мужчин моложе 60 лет, для индивидуальной экспресс-оценки вероятности развития этого события используют формулу: p=1/(1+e-z), где е (математическая константа) = 2,72; Z - вспомогательная функция:
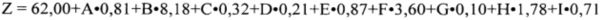
Обозначения в формуле расшифрованы в табл. 1.

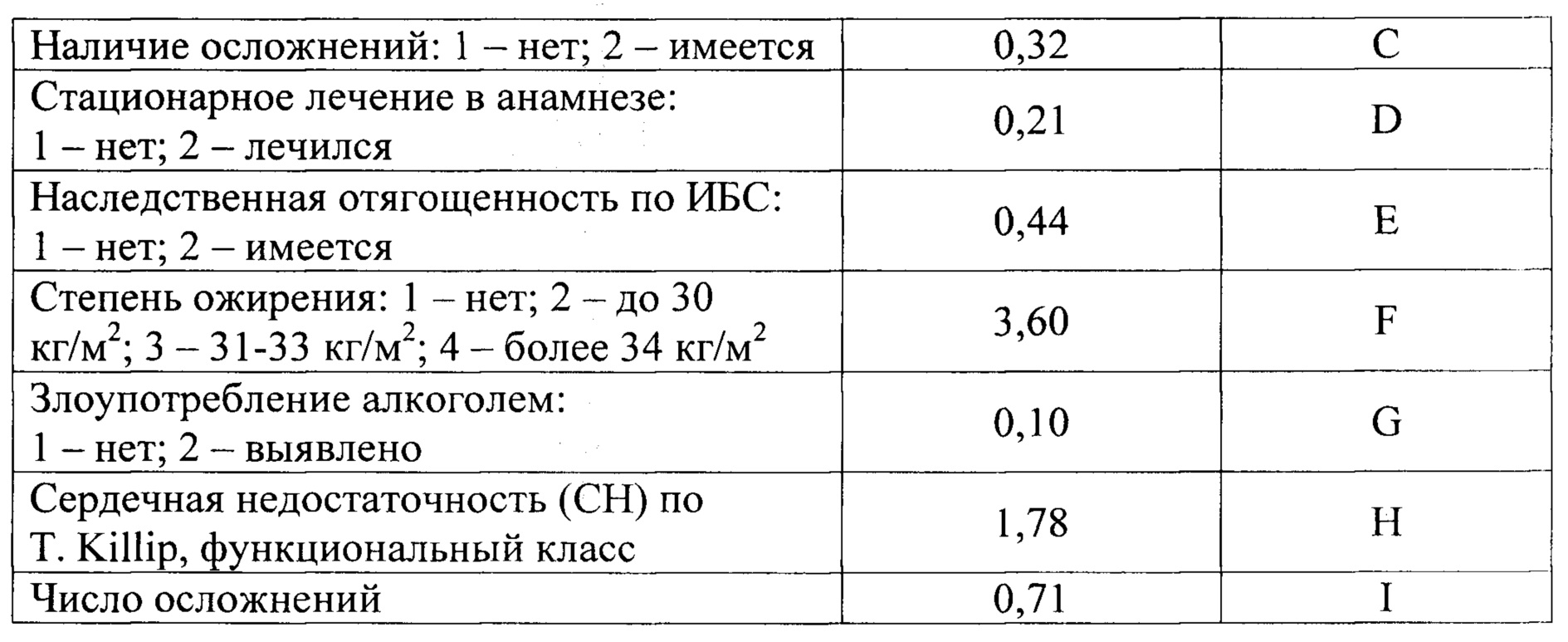
Значение p>0,5 свидетельствует о высоком риске рецидивирующего поражения, p<0,5 - о низком риске.
Заявляемое изобретение решает задачу улучшения раннего прогнозирования риска развития рецидивирующего ИМ у мужчин моложе 60 лет с повторным ИМ. Эта задача решается тем, что предлагаемая математическая модель, полученная в целевой группе, дает возможность быстрой количественной оценки вероятности этого события, начиная с первых часов заболевания на основании анамнестических данных и особенностей клинического течения ИМ без привлечения дополнительных исследований. Это позволяет выделить среди мужчин моложе 60 лет с повторным ИМ, группу риска развития рецидивирующих поражений для ускорения решения вопроса о необходимости и сроках выполнения реваскуляризации и определения объема терапии.
Технический результат, достигаемый в результате использования изобретения, заключается: 1) в максимально раннем получении достоверной индивидуальной экспресс-оценки риска развития рецидивирующего ИМ при повторных ИМ; 2) возможности быстрого выделения группы риска этого события и проведении с ней полного комплекса лечебно-диагностических мероприятий (прежде всего, необходимости реваскуляризации, сроков ее выполнения); 3) в активизации и ускорении процесса принятия решения о тактике лечения и ее контроле; 4) в увеличении степени обоснованности такого решения; 5) в снижении психической нагрузки на участников (лечебный персонал, пациента и его родственников) лечебного процесса и 6) улучшения преемственности между различными этапами лечения пациентов.
СПОСОБ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕЦИДИВИРУЮЩЕГО ИНФАРКТА МИОКАРДА ПОСЛЕ ПОВТОРНОГО ИНФАРКТА МИОКАРДА У МУЖЧИН МОЛОЖЕ 60 ЛЕТ включает расчет вероятности развития повторного (р) пациента по следующей формуле:
p=1/(1+e-z), где е - (константа) = 2,72; а

Обозначения в формуле расшифрованы в табл. 1.
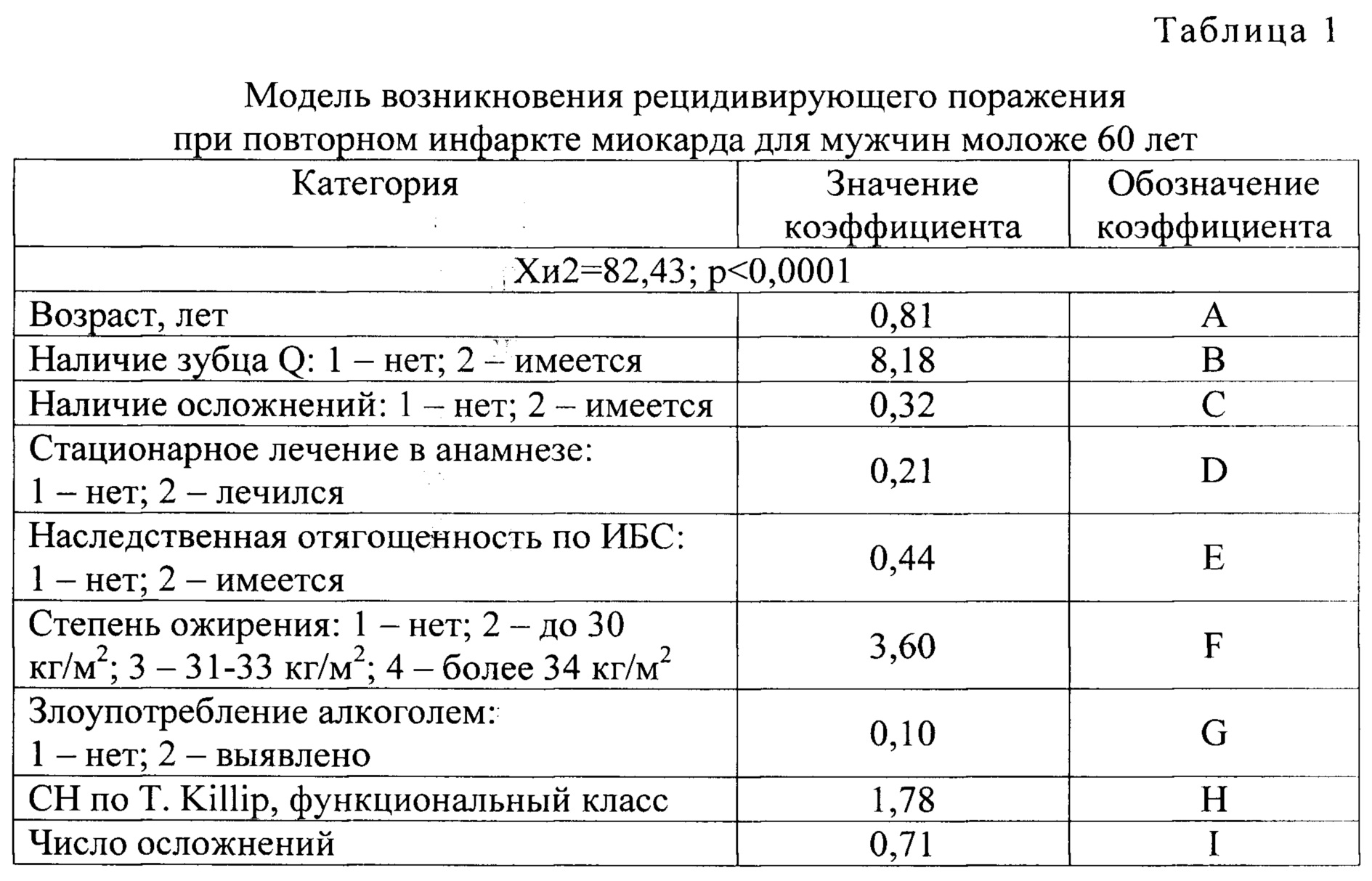
Значение р>0,5 свидетельствует о высоком риске рецидивирующего поражения, p<0,5 - о низком риске.
В представленном уравнении определение значений переменных выполняется следующим образом:
I. Степень ожирения определяется по индексу массы тела (Кетле): масса тела / рост2 (кг/м2).
II. Наследственная отягощенность по ИБС выясняется при уточнении семейного анамнеза.
III. Злоупотребление алкоголем верифицируется при приеме пациентом более 3-4 доз напитка, содержащего 10 г этанола, в день или 21 дозы - в неделю (МКБ-10, ДСМ-V) (Азимова, Ю.Э. Диагностика и лечение неврологических осложнений алкоголизма: «Новое вино в старых бокалах» / Ю.Э. Азимова, К.А. Ищенко, А.П. Рачин. // Поликлиника. - 2016. - №1. - С 50-56.). Для дополнительной диагностики этого состояния применяются опросники CAGE, AUDIT, анкета ПАС, сетка LeGo (Костюкевич, О.И. Алкогольный гепатит: современные алгоритмы диагностики и лечения / О.И. Костюкевич // Рус. мед. журн. - 2016. - Т. 24, №3. - С 177-182.). Признаком наличия злоупотребления расценивается положительный результат хотя бы в одном из них.
IV. Функциональный класс острой СН по Т. Killip определяется обычным способом (Killip Т., Kimball J.T. Treatment of myocardial infarction in a coronary care unit. A two-year experience with 250 patients // Am. J. Cardiol. - 1967. - Vol. 20, №4 - P. 457-464).
Модель может использоваться с первых часов повторного ИМ. Для расчетов необходимы результаты осмотра пациента, сбора анамнеза и физикальных данных, а также электрокардиограммы (ЭКГ) (оценка особенностей анамнеза, выраженности признаков острой СН, наличие хрипов в легких, наличие зубца Q на ЭКГ, числа осложнений заболевания). Таким образом, сведения, необходимые для расчета вероятности рецидивирующего ИМ при повторном поражении доступны, начиная с первых часов заболевания, и уточняются в конце третьей его недели (число осложнений ИМ) без дополнительных лабораторных и инструментальных методов исследования. Вероятность рецидивирующего поражения, выраженная в процентах, при выписке пациента в завершении стационарного этапа лечения ИМ указывается после окончательного диагноза в выписном эпикризе пациента. Все сведения для ее определения могут быть без труда получены и рассчитаны медицинским работником стационарного или амбулаторного этапов лечения с базовым уровнем медицинского образования.
Заявляемый способ ПРОГНОЗИРОВАНИЯ РАЗВИТИЯ РЕЦИДИВИРУЮЩЕГО ИНФАРКТА МИОКАРДА ПОСЛЕ ПОВТОРНОГО ИНФАРКТА МИОКАРДА У МУЖЧИН МОЛОЖЕ 60 ЛЕТ осуществляется с момента первого контакта с пациентом и уточняется на этапе окончания стационарного лечения по поводу повторного ИМ в конце его подостроого периода (окончание третьей недели заболевания). Для удобства расчетов может быть применен электронный калькулятор модели, позволяющий внести в формулу полученные обследовании пациента данные, и сразу получить результат оценки вероятности развития рецидивирующего ИМ при повторных поражениях.
Главным при проведении расчетов является точная оценка медицинским работником данных анамнеза пациента, физикальных данных, клинического течения ИМ и результатов ЭКГ, что входит в перечень обычных навыков для выпускников медицинских учебных заведений и не требует дополнительной подготовки.
Способ осуществляют поэтапно. Каждый этап включает получение сведений для оценки в период лечения пациента.
На первом этапе при сборе жалоб выясняют выраженность острой СН среди симптомов заболевания.
На втором этапе при сборе анамнеза заболевания уточняют у пациента или сопровождающих возраст больного, наличие ИМ и стационарного лечения по поводу ИБС в анамнезе, наличие наследственной отягощенности, ожирения, злоупотребления алкоголем в анамнезе.
На третьем этапе при объективном исследовании уточняют массу тела и рост, наличие ожирения, определяют индекс массы тела по Кетле; при аускультации выясняют наличие и качество хрипов в легких, а также их распространенность с целью определения функционального класса острой СН по Т. Killip. Также уточняют признаки наличия других осложнений ИМ.
На четвертом этапе выполняется регистрация и оценка ЭКГ (наличие или отсутствие зубца Q).
На пятом этапе в конце третьей недели заболевания уточняют анамнестические категории, полученные при предыдущих этапах обследования (ожирение, наличие зубцов Q, наличие осложнений ИМ и их число).
На заключительном этапе осуществляют ввод данных в модель и расчет вероятности рецидивирующего ИМ при повторном ИМ. Полученную величину вероятности развития этого события в процентах с оценкой риска указывают в окончательном диагнозе при выписке пациента на следующий этап реабилитации.
Позитивное терапевтическое отношение, нацеленность на выявление клинической особенностей ИМ - необходимые, но недостаточные условия эффективной оценки вероятности рецидивирующего ИМ после повторного ИМ. Желательно, чтобы этапы оценки проводили в помещении с достаточным освещением и шумоизоляцией, оборудованном для осмотра пациента, оценки роста и массы тела и регистрации ЭКГ пациента в тяжелом и крайне тяжелом состоянии.
Предлагаемый способ оценки вероятности развития рецидивирующего ИМ основан изучении результатов наблюдения 232 мужчин моложе 60 лет по поводу инфаркта миокарда в стационарах Санкт-Петербурга в 2000-2015 гг. Период наблюдения пациентов составил от 56 дней. Рецидивирующие ИМ зарегистрированы в 24 случаях в различные сроки наблюдения. Посмертные диагнозы верифицированы на аутопсии. ИМ диагностировали на основании рекомендаций экспертов Всемирной организации здравоохранения (1981 г.) и национальных рекомендаций Всероссийского научного общества кардиологов (2006, 2007, 2013 гг.) (ВНОК) с учетом третьего универсального определения ИМ (2013) с оценкой в динамике объективных, лабораторных, клинических и инструментальных данных. Модель получена при применении статистического анализа базы данных, включавшей 11 блоков и более 250 показателей. На первом этапе с помощью бинарной логистической регрессии из аналитической базы отбирали показатели, имеющие достоверные связи с тяжестью состояния больных и числом осложнений. После учитывали наиболее чувствительные из них по отношению к рецидивирующим поражениям. Для создания модели с максимальной предсказательной способностью по отношению к этому событию применяли пошаговую логистическую регрессию. Для оценки свойств модели использовали ROC-анализ.
Полученная модель имеет чувствительность 96,3%, специфичность 98,2%. Ее отношение шансов составляет 347,75, а информационная способность (общая доля верно классифицированных исходов) - 96,2%. Доля ложноположительных результатов классификации составляет - 1,8%; ложноотрицательных - 3,7%. Согласно параметрам модели она может использоваться на практике с целью оценки риска возникновения рецидивирующих ИМ после повторных ИМ как дополнение к одобренным в текущее время прогностическим шкалам (GRACE, TIMI, NORRIS). Это особенно необходимо в ситуациях, когда не все параметры для расчетов этого риска с помощью других инструментальных и лабораторных исследований доступны.
Применение предложенной прогностической математической модели, заявленным способом облегчает расчет вероятности рецидивирующего ИМ после повторных случаев. Это позволяет с высокой точностью оценить ее, начиная с первых часов заболевания с уточнением в конце третьей недели ИМ перед выпиской из стационара или на амбулаторном приеме. Включенный в комплексную программу обследования и лечения пациентов с повторными ИМ, данный способ дает возможность формирования среди пациентов группы риска с высокой вероятностью развития рецидивирующих поражений и помогает обосновать принятие решения о тактике лечения, как в острый, так и подострый периоды (необходимости и времени применения реваскуляризации); периодичности контроля эффективности профилактических мероприятий, необходимости дополнительных мероприятий (как медицинского, так и административного и социального характера), начиная с первых часов заболевания. Дополнительными преимуществами предложенного способа является отсутствие необходимости в дополнительных затратах, ресурсах и экономия времени. Способ доступен для большинства медицинских работников стационарного и амбулаторного звеньев оказания помощи. Он безвреден, не инвазивен и не дает побочных эффектов.
Примерами реализации способа стало изучение возможности его использования в отделениях клиники госпитальной терапии Военно-медицинской академии. Его эффективность и организационные аспекты проведения оценивались на практике в период 2010-2018 гг. Описанный способ использован у 42 пациентов с повторным ИМ (22 при применении модели в алгоритме оказания помощи и 20 - без нее). В дальнейшем способ апробировался на госпитальном этапе реабилитации этих больных в кардиологическом отделении клиники. Оценку развития рецидивирующего ИМ выполняли на протяжении этапа стационарного лечения и дальнейшего наблюдения за пациентами на основании непосредственного общения с больным или его родственниками. После выписки из стационара информацию собирали во время визитов пациентов в клинику и/или при телефонном опросе.
Для оценки эффективности в отношении профилактики рецидивирующего ИМ у предлагаемого способа использована в динамике методика оценки качества жизни пациентов, связанная с СН (Ироносов, В.Е. Динамика диастолической функции сердца у больных острым инфарктом миокарда: диагностика и прогноз: автореф. дис. … канд. мед. наук / В.Е. Ироносов. - СПб., 2004. - 26 с). Оценка уровня качества жизни проведена в клинике при поступлении и при выписке и в течение последующих визитов. Сравнивались показатели, полученные при первом и повторном измерениях. Получилось, что связанное с СН качество жизни больных, у которых применяли прогнозирование, придерживались более агрессивной тактики лечения, профилактики и таким образом снижали риск развития рецидивов ИМ, значимо улучшалось в сравнении с группой без моделирования (p<0,05). Значительно уменьшились жалобы, связанные с СН у пациентов с реваскуляризацией, что сыграло существенную роль в улучшении субъективного состояния больных, повышении их жизненного тонуса, появлении правильной самооценки состояния и позитивного настроя на будущее. С учетом санаторного и поликлинического этапов реабилитации, программа оказания помощи с включением предложенного способа прогнозирования оказалась экономически более эффективной, чем при его отсутствии.
Таким образом, новизна и особенность заявляемого способа заключается в том, что он включает в новой последовательности и с новыми компонентами расчет вероятности развития рецидивирующего ИМ после повторных ИМ. Он позволяет в короткий срок без увеличения затрат и с большой достоверностью оценить вероятность этого события и принять правильное решение по тактике лечения и профилактики пациента, начиная с первых часов повторного ИМ (необходимость и сроки реваскуляризации; периодичность контроля эффективности профилактических мероприятий). Использование прогностического моделирования в алгоритма диагностики и лечения мужчин с повторным ИМ моложе 60 лет существенно улучшает результаты лечения и качество жизни этих пациентов. Выполнение этого алгоритма наряду с поэтапной программой реабилитации больных на госпитальном, санаторном и амбулаторном этапах повысит эффективность диагностики, прогнозирования, профилактики и лечения этих пациентов.