Результат интеллектуальной деятельности: СПОСОБЫ ЛЕЧЕНИЯ ПАТОЛОГИЧЕСКИХ СОСТОЯНИЙ ГЛАЗА С ПОМОЩЬЮ ИМПЛАНТАТА С ДОЛГОВРЕМЕННОЙ ДОСТАВКОЙ ЛЕКАРСТВЕННОГО ВЕЩЕСТВА
Вид РИД
Изобретение
ПЕРЕКРЕСТНАЯ ССЫЛКА НА РОДСТВЕННЫЕ ЗАЯВКИ
Настоящая заявка заявляет приоритет по предварительной заявке на патент США №61/904887, зарегистрированной 15 ноября 2013 года, полное содержание которой включено в данный документ посредством ссылки.
УРОВЕНЬ ТЕХНИКИ
Область техники
Описание настоящей заявки в общем относится имплантатам для доставки лекарственных веществ, а более конкретно - к способу лечения патологических состояний глаз с использованием имплантатов для доставки лекарственных веществ.
Описание предшествующего уровня техники
Макулярный отек («МО») представляет собой патологическое состояние глаз, которое может приводить к отеку желтого пятна. Отек возникает вследствие просачивания жидкости из кровеносных сосудов сетчатки. Кровь просачивается сквозь слабые стенки сосудов в очень маленькую область желтого пятна, содержащего большое количество колбочек - нервных окончаний, которые воспринимают цвет, и от которых зависит дневное зрение. Затем в середине или немного в стороне центрального поля зрения возникает затуманивание. Потеря зрения может продолжаться в течение нескольких месяцев. С макулярным отеком могут быть связаны закупорка кровеносных сосудов сетчатки, воспаление глаз и возрастная макулярная дистрофия. Макулярный отек может возникать после удаления катаракты. Симптомы МО включают затуманивание центрального зрения, искажение зрения, слегка окрашенное в розовый цвет изображение и чувствительность к свету. Причины МО могут включать окклюзию вены сетчатки, макулярную дистрофию, утечку в желтое пятно вследствие диабета, воспаление глаз, идиопатическую центральную серозную хориоретинопатию, передний или задний увеит, pars planitis, пигментную дистрофию сетчатки, радиационную ретинопатию, заднее отслоение стекловидного тела, образование эпиретинальной мембраны, идиопатическую юкстафовеальную телеангиэктазию сетчатки, капсулотомию или иридотомию, выполняемую Nd:YAG-лазером. Некоторые пациенты с МО могут иметь в анамнезе местное применение аналогов адреналина или простагландина для лечения глаукомы.
Макулярный отек включает повреждение внутреннего гематоретинального барьера на уровне эндотелия капилляров, приводящее к аномальной сосудистой проницаемости в сетчатке и утечке в прилегающие ткани сетчатки. Желтое пятно становится более толстым вследствие накопления жидкости, что приводит значительным нарушениям остроты зрения.
Макулярный отек может возникать при заболеваниях, которые вызывают нарастание повреждения в течение многих лет, таких как диабетическая ретинопатия, или в результате более острых нарушений, таких как окклюзия центральной вены сетчатки или окклюзия ветви вены сетчатки.
Диабетическая ретинопатия представляет собой частое микрососудистое осложнение диабета 1 и 2 типа и является основной причиной слепоты в мире. Потеря центрального зрения, связанная с диабетом, может возникать или в результате микрососудистой окклюзии (макулярной ишемии), или в результате утечки из мелких сосудов вследствие повреждения внутреннего гематоретинального барьера (ГРБ), что приводит к утолщению или отеку желтого пятна (макулярному отеку). Диабетический макулярный отек (ДМО) поражает приблизительно 21 миллион человек во всем мире.
Существует несколько вариантов лечения, которые приводят к улучшению остроты зрения, в том числе интравитреальное введение агентов, нацеленных на фактор роста эндотелия сосудов (анти-VEGF-агентов), и лазерная фотокоагуляция. Однако эти варианты лечения имеют некоторые недостатки и не действуют на всех пациентов эффективно.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Настоящее изобретение связано с и относится к имплантатам и способам лечения патологического состояния глаз, такого как макулярный отек, в том числе диабетический макулярный отек («ДМО»). В некоторых вариантах реализации изобретения имплантат может содержать кортикостероид. В некоторых вариантах реализации изобретения кортикостероид представляет собой дексаметазон.
Патологическое состояние глаз может включать заболевание, недомогание или состояние, которое поражает или вовлекает глаз или одну из частей или областей глаза. В общем глаз включает глазное яблоко и ткани и жидкости, которые составляют глазное яблоко, окологлазные мышцы (например, косые и прямые мышцы) и часть зрительного нерва, которая находится в пределах или вблизи глазного яблока. Патологическое состояние переднего отрезка глаза представляет собой заболевание, недомогание или состояние, которое поражает или затрагивает переднюю область или участок глазницы (т.е. переднюю часть глаза), такую как окологлазная мышца, глазное веко или ткань или жидкость глазного яблока, расположенные спереди по отношению к задней стенке мембраны хрусталика, или цилиарные мышцы. Таким образом, патологическое состояние переднего отрезка глаза главным образом поражает или затрагивает конъюнктиву, роговую оболочку, конъюнктиву, переднюю камеру, радужную оболочку, заднюю камеру (за сетчаткой, но перед задней стенкой мембраны хрусталика), хрусталик или мембрану хрусталика и кровеносные сосуды и нервы, которые васкуляризируют или иннервируют переднюю область или участок глазницы. Патологическое состояние заднего отрезка глаза представляет собой заболевание, недомогание или состояние, которое поражает или затрагивает главным образом заднюю область или участок глазницы, такую как хориоидея или склера (находятся сзади по отношении к плоскости, проходящей через заднюю стенку мембраны хрусталика), стекловидное тело, стекловидная камера, сетчатка, зрительный нерв (т.е. диск зрительного нерва) и кровеносные сосуды и нервы, которые васкуляризируют или иннервируют заднюю область или участок глазницы.
Патологическое состояние заднего отрезка глаза может включать заболевание, недомогание или состояние, как например: макулярную дистрофию (такую как неэкссудативная возрастная макулярная дистрофия и экссудативная возрастная макулярная дистрофия); хороидальную неоваскуляризацию; острую макулярную нейроретинопатию; макулярный отек (такой как кистозный макулярный отек и диабетический макулярный отек); болезнь Бехчета; заболевания сетчатки, диабетическую ретинопатию (в том числе пролиферативную диабетическую ретинопатию); окклюзионное заболевание артерии сетчатки; окклюзию центральной вены сетчатки; ретинальный увеит; отслоение сетчатки; глазную травму, которая поражает задний участок или область глазницы; патологическое состояние заднего отрезка глаза, вызванное или возникающее под влиянием лазерного лечения глаз; патологическое состояние заднего отрезка глаза, вызванное или возникающее под влиянием фотодинамической терапии; фотокоагуляции; радиационную ретинопатию; образование эпиретинальной мембраны; окклюзию ветви вены сетчатки; переднюю ишемическую нейропатию зрительного нерва; не связанную с ретинопатией диабетическую дисфункцию сетчатки, пигментную дистрофию сетчатки и глаукому.
Патологическое состояние переднего отрезка глаза может включать заболевание, недомогание или состояние, как например: афакию; артифакию; астигматизм; блефароспазм; катаракту; заболевания конъюнктивы; конъюнктивит; заболевания роговой оболочки; язву роговицы; синдром сухого глаза; заболевания века; заболевания слезного аппарата; закупорку слезного протока; миопию; пресбиопию; заболевания зрачка; нарушения рефракции и косоглазие. Глаукому также можно рассматривать как патологическое состояние переднего отрезка глаза, поскольку клиническая цель лечения глаукомы может состоять в снижении гипертензии водной жидкости в передней камере глаза (т.е. понижении внутриглазного давления).
Сильнодействующие кортикостероиды, такие как дексаметазон, подавляют воспаление, ингибируя отек, отложение фибрина, утечку из капилляров и миграцию фагоцитов - все ключевые признаки воспалительного ответа. Кортикостероиды предотвращают высвобождение простагландинов, некоторые из которых идентифицированы как медиаторы кистозного макулярного отека.
Путем доставки лекарственного средства, такого как кортикостероид, непосредственно в стекловидную полость, можно обойти гематоофтальмические барьеры и достигнуть внутриглазных терапевтических уровней с минимальной системной токсичностью. Этот путь введения, как правило, приводит к короткому периоду полувыведения, за исключением случаев, когда лекарственное вещество можно доставлять с использованием состава, который может обеспечивать долговременное высвобождение.
Следовательно, биодеградируемый имплантат для доставки терапевтического агента в глазничную область, такую как стекловидное тело, может принести существенную пользу пациентам, страдающим от медицинского патологического состояния глаза, такого как диабетический макулярный отек.
Согласно варианту реализации изобретения способ лечения диабетического макулярного отека включает введение биоразлагаемого имплантата в стекловидное тело человека, имеющего для этого показания, с частотой от одного раза в примерно шесть месяцев до одного раза в примерно девять месяцев. Биоразлагаемый имплантат может включать сплошной дважды экструдированный стержень, который может содержать активный агент, гомогенно диспергированный в биодеградируемой полимерной матрице. Биодеградируемая полимерная матрица может содержать смесь поли(D,L-лактид-со-гликолида) (ПМГК), содержащего гидрофильные концевые группы, и поли(D,L-лактид-со-гликолида) (ПМГК), содержащего гидрофобные концевые группы. Биоразлагаемый имплантат может иметь размер, подходящий для имплантации в глазничную область. В некоторых вариантах реализации изобретения активный агент представляет собой кортикостероид. Способ может являться терапевтически эффективным для лечения ДМО. В некоторых вариантах реализации изобретения активный агент представляет собой дексаметазон. В некоторых вариантах реализации изобретения макулярный отек представляет собой диабетический макулярный отек. В некоторых вариантах реализации изобретения дексаметазон присутствует в биоразлагаемом имплантате в количестве 60% по массе в пересчете на общую массу биоразлагаемого имплантата. В некоторых вариантах реализации изобретения сополимер ПМГК, содержащий гидрофобные концевые группы, присутствует в биоразлагаемом имплантате в количестве 10% по массе в пересчете на общую массу биоразлагаемого имплантата. В некоторых вариантах реализации изобретения сополимер ПМГК, содержащий гидрофильные концевые группы, присутствует в биоразлагаемом имплантате в количестве 30% по массе в пересчете на общую массу биоразлагаемого имплантата. Согласно варианту реализации изобретения человек имеет псевдофакичную линзу. Согласно варианту реализации изобретения человек имеет факичную линзу.
КРАТКОЕ ОПИСАНИЕ ГРАФИЧЕСКИХ МАТЕРИАЛОВ
Эти и другие признаки будут сейчас описаны со ссылкой на графические материалы, представленные ниже. Данные графические материалы и связанное с ними описание приведены для иллюстрации одного или более вариантов реализации изобретения и не ограничивают объем изобретения.
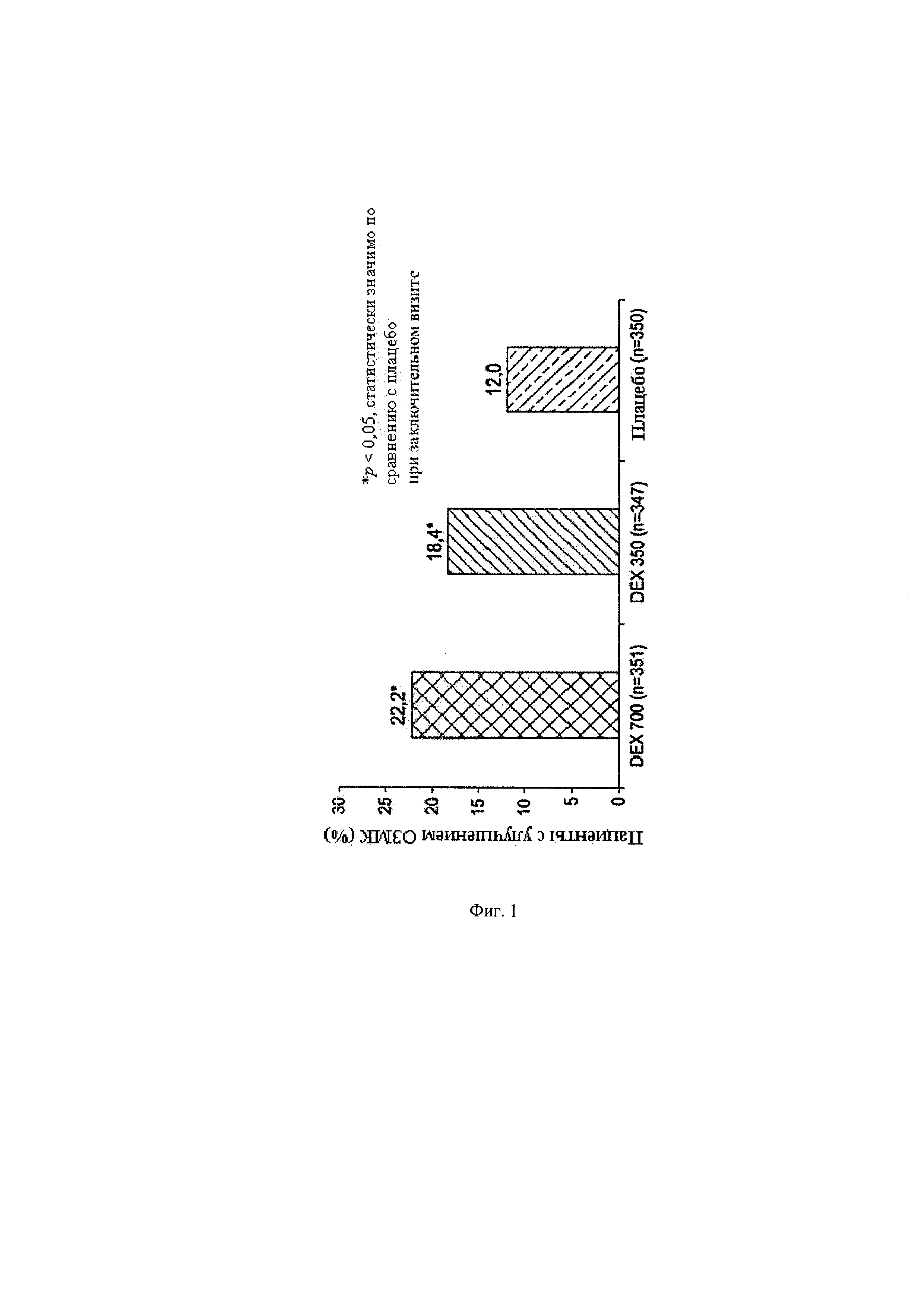
Фиг. 1 иллюстрирует гистограмму, сравнивающую доли пациентов с ДМО, у которых наблюдается улучшение ОЗМК на 15 или более букв в группах пациентов, получавших иллюстративный вариант реализации биоразлагаемых имплантатов согласно иллюстративному варианту реализации способов, раскрытых в данном документе.
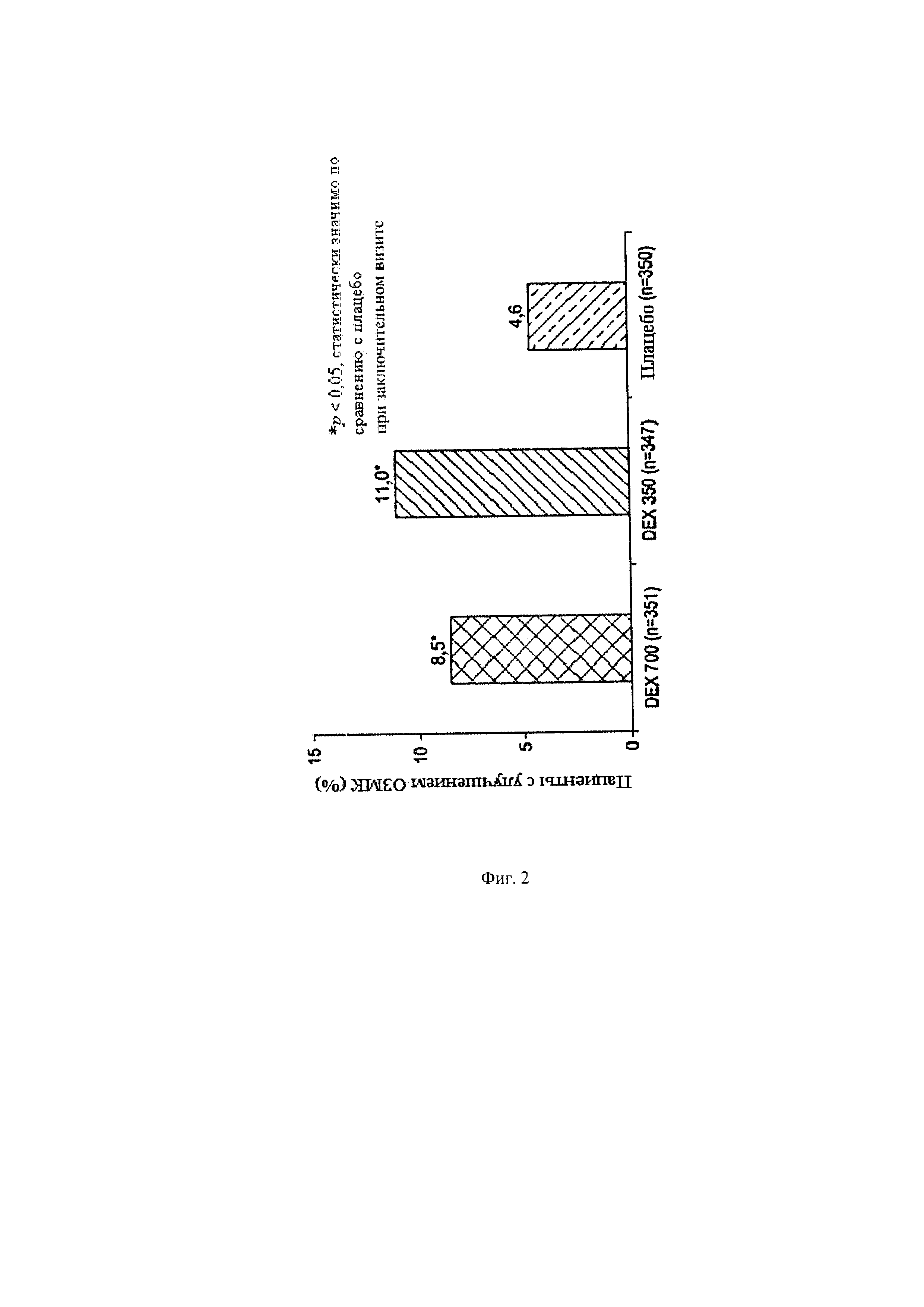
Фиг. 2 иллюстрирует гистограмму, сравнивающую доли пациентов с ДМО, у которых наблюдается улучшение ОЗМК на 20 или более букв в группах пациентов, получавших иллюстративный вариант реализации биоразлагаемых имплантатов согласно иллюстративному варианту реализации способов, раскрытых в данном документе.
Фиг. 3 иллюстрирует линейный график, сравнивающий средние изменения ОЗМК между различными группами пациентов с ДМО, получавших иллюстративный вариант реализации биоразлагаемых имплантатов согласно иллюстративному варианту реализации способов, раскрытых в данном документе.
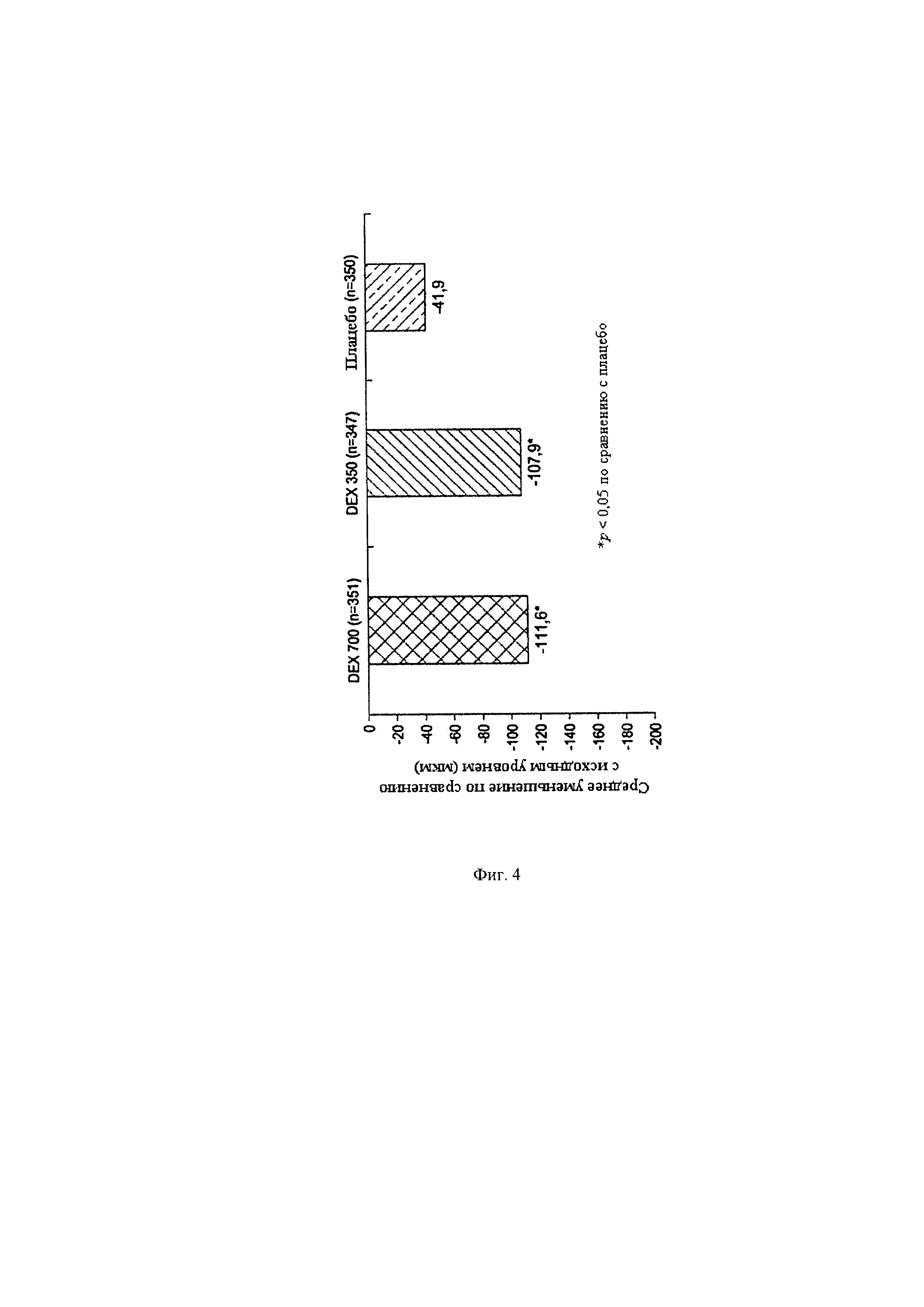
Фиг. 4 иллюстрирует гистограмму, сравнивающую среднее уменьшение CSRT по сравнению с исходным уровнем в группах пациентов с ДМО, получавших иллюстративный вариант реализации биоразлагаемых имплантатов согласно иллюстративному варианту реализации способов, раскрытых в данном документе.
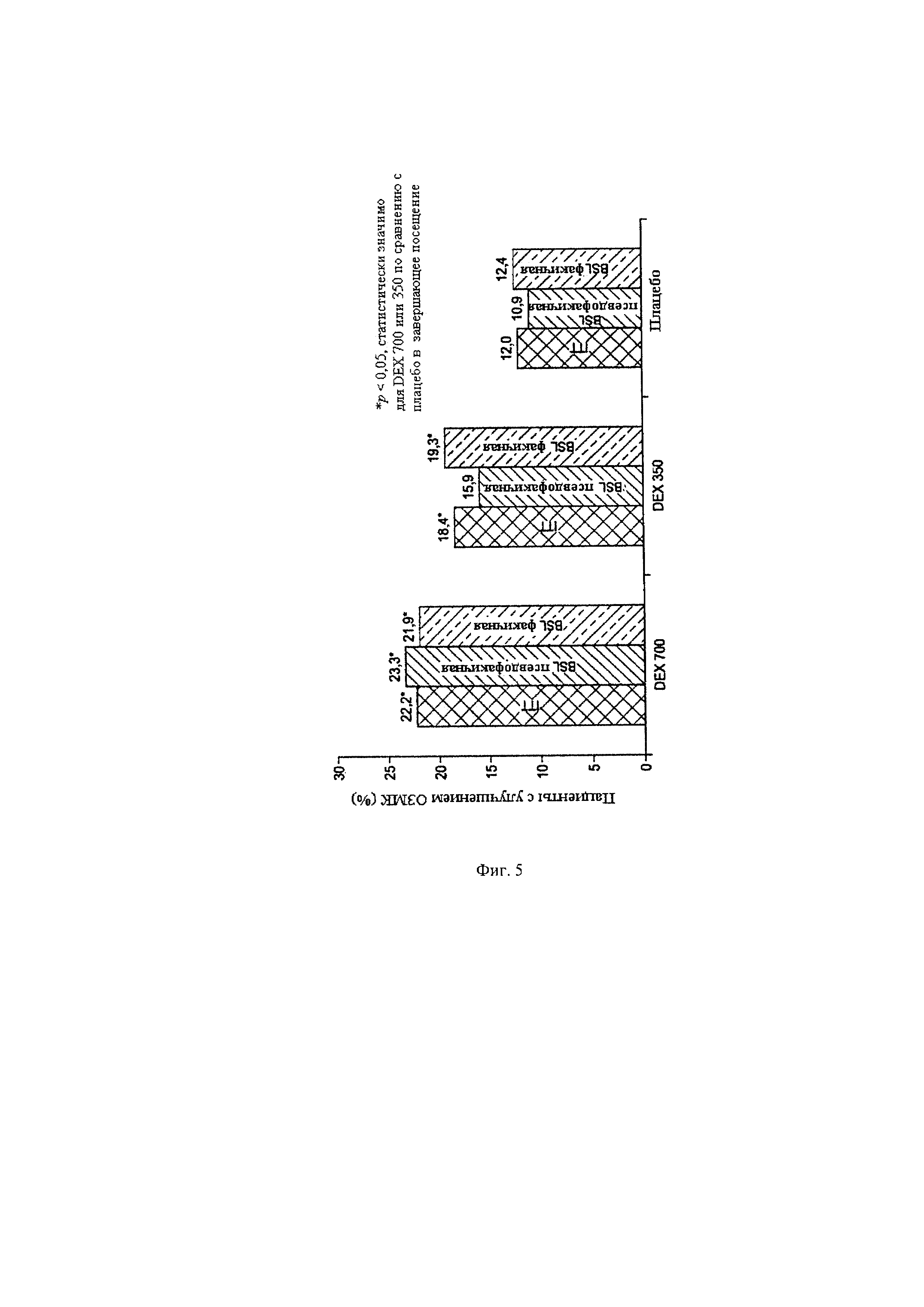
Фиг. 5 иллюстрирует гистограмму, сравнивающую доли пациентов с ДМО, у которых наблюдается улучшение ОЗМК на 15 или более букв в группах пациентов, получавших иллюстративный вариант реализации биоразлагаемых имплантатов согласно иллюстративному варианту реализации способов, раскрытых в данном документе.
Фиг. 6 иллюстрирует таблицу, перечисляющую распространенные нежелательные явления, возникшие во время исследования согласно примерам.
Фиг. 7 иллюстрирует таблицу, перечисляющую хирургические вмешательства на глазах, выполненные для корректирования ВГД в течение исследования согласно примерам.
ПОДРОБНОЕ ОПИСАНИЕ СУЩНОСТИ ИЗОБРЕТЕНИЯ
Определения
Следующие термины, при использовании в данном документе, имеют следующие значения:
«Активный агент» и «лекарственное вещество» используются взаимозаменяемо и относятся к любому веществу, которое используется для лечения патологического состояния глаз.
«Биоразлагаемый полимер» подразумевает полимер, который разлагается in vivo, при этом для получения кинетики высвобождения активного агента согласно настоящему изобретению необходимо разложение полимера в течение некоторого времени. Таким образом, гидрогели, такие как метилцеллюлоза, которые высвобождают лекарственное вещество посредством набухания полимера, исключены из термина «биоразлагаемый (или биодеградируемый) полимер». Слова «биоразлагаемый» и «биодеградируемый» являются синонимами и в настоящем документе используются взаимозаменяемо.
«Поражение» или «повреждение» взаимозаменяемы и относятся к клеточным и морфологическим проявлениям и симптомам, возникающим вследствие патологического состояния, опосредованного воспалением, как например воспаления.
«Патологическое состояние глаз» означает заболевание, недомогание или состояние, которое поражает или затрагивает глаз или одну из частей или областей глаза, такое как заболевание сетчатки. Глаз включает глазное яблоко и ткани и жидкости, которые составляют глазное яблоко, окологлазные мышцы (такие как косые и прямые мышцы) и часть зрительного нерва, которая находится внутри или прилегает к глазному яблоку. «Патологическое состояние глаза» является синонимом «медицинского патологического состояния глаза».
«Множество» означает два или больше.
«Патологическое состояние заднего отрезка глаза» означает заболевание, недомогание или состояние, которое поражает или затрагивает заднюю область или участок глазницы, такую как хориоидея или склера (находятся сзади по отношении к плоскости, проходящей через заднюю стенку мембраны хрусталика), стекловидное тело, стекловидная камера, сетчатка, зрительный нерв (т.е. диск зрительного нерва) и кровеносные сосуды и нервы, которые васкуляризируют или иннервируют заднюю область или участок глазницы.
«Стероидный противовоспалительный агент» и «глюкокортикоид» используют в данном документе взаимозаменяемо и, как подразумевается, включают стероидные агенты, соединения или лекарственные вещества, которые уменьшают воспаление при введении на терапевтически эффективном уровне.
«Пригодный для введения (или имплантации) в область или участок глазницы» в отношении имплантата означает имплантат, который имеет такой размер (параметры), что его можно ввести или имплантировать, не вызывая значительного повреждения тканей и не оказывая значительного влияния на существующее зрение пациента, которому имплантируют или вводят имплантат.
«Терапевтические уровни» или «терапевтическое количество» означает количество или концентрацию активного агента, которую местно доставляют в глазничную область, и которая оптимальна для безопасного лечения патологического состояния глаз, чтобы уменьшить или предотвратить симптом патологического состояния глаз.
Согласно некоторым вариантам реализации изобретения биоразлагаемый имплантат для лечения медицинского патологического состояния глаза содержит активный агент, диспергированный в биодеградируемой полимерной матрице. Пример биоразлагаемых имплантатов и способы их получения таких имплантатов описаны в патенте США №8034370, патенте США №8242099, патенте США №7767223 и патенте США №82577300, все указанные выше патенты включены в данный документ посредством ссылки в полном объеме.
Активный агент может быть выбран из группы, состоящей из ингибиторов АПФ, эндогенных цитокинов, агентов, которые влияют на базальную мембрану, агентов, которые влияют на рост эндотелиальных клеток, адренергических агонистов или блокаторов, холинэргических агонистов или блокаторов, ингибиторов альдоредуктазы, обезболивающих средств, анестезирующих средств, противоаллергических средств, противовоспалительных средств, стероидов (таких как стероидный противовоспалительный агент), гипотензивных средств, лекарственных средств, повышающих кровяное давление, антибактериальных средств, антивирусных средств, противогрибковых средств, антипротозойных средств, противоинфекционных средств, противоопухолевых средств, антиметаболитов и антиангиогенных средств. Таким образом, активный агент может представлять собой кортизон, дексаметазон, флуоцинолон, гидрокортизон, метилпреднизолон, преднизолон, преднизон, триамцинолон и их любое производное.
Биоразлагаемый имплантат имеет размер, подходящий для имплантации в глазничную область. Глазничная область может представлять собой одно или более из следующего: передней камеры, задней камеры, стекловидной полости, хориоидеи, супрахориоидального пространства, конъюнктивы, субконъюнктивального пространства, эписклерального пространства, внутрироговичного пространства, эпикорнеального пространства, склеры, плоской части ресничного тела, бессосудистых областей, вызванных хирургическим путем, желтого пятна и сетчатки.
Способ получения биоразлагаемого имплантата для лечения медицинского патологического состояния глаза может включать несколько циклов экструзии биодеградируемого полимера. Этот способ также может включать стадию размалывания биодеградируемого полимера до экструзии. Биодеградируемый полимер может представлять собой сополимер поли(молочную-со-гликолевую) кислоту (ПМГК). Соотношение мономеров молочной и гликолевой кислот в полимере может составлять около 50/50 по массе. Дополнительно, сополимер ПМГК может составлять от около 20 до около 90% по массе от биоразлагаемого имплантата. С другой стороны, сополимер ПМГК может составлять около 40% по массе от биоразлагаемого имплантата.
В настоящем изобретении предложены биодеградируемые глазные имплантаты и способы лечения медицинских патологических состояний глаза. Как правило, биоразлагаемый имплантат изготавливают сплошным, т.е. частицы активного агента распределены в биодеградируемой полимерной матрице. Кроме того, имплантат изготовлен так, чтобы высвобождать активный агент в глазничную область глаза в течение различных периодов времени. Активный агент может высвобождаться в течение периода времени, включающего, но не ограничиваясь этим, примерно двенадцать месяцев, десять месяцев, девять месяцев, восемь месяцев, шесть месяцев, семь месяцев, восемь месяцев, три месяца, один месяц или менее одного месяца.
Биодеградируемые имплантаты для лечения медицинских патологических состояний глаза
Имплантаты изобретения содержат активный агент, диспергированный в биодеградируемом полимере. В некоторых вариантах реализации изобретения противовоспалительный агент представляет собой стероидный противовоспалительный агент, такой как кортикостероид, например дексаметазон. В некоторых вариантах реализации изобретения дексаметазон является единственным активным агентом, присутствующим в имплантате.
Стероидный противовоспалительный агент, такой как дексаметазон, может составлять от около 10% до около 90% от массы имплантата. В одном варианте агент составляет от около 40% до около 80% от массы имплантата. В предпочтительном варианте агент составляет около 60% от массы имплантата.
Биодеградируемая полимерная матрица
В одном варианте активный агент может быть гомогенно диспергирован в биодеградируемой полимерной матрице имплантата. Выбор используемой биодеградируемой полимерной матрицы будет зависеть от желаемой кинетики высвобождения, переносимости пациентом, природы заболевания, которое лечат, и тому подобного. Рассматриваемые характеристики полимеров включают, но не ограничиваясь ими, биосовместимость и биодеградируемость в месте имплантации, совместимость с целевым активным агентом и температуры обработки. Биодеградирумая полимерная матрица обычно составляет по меньшей мере около 10, по меньшей мере около 20, по меньшей мере около 30, по меньшей мере около 40, по меньшей мере около 50, по меньшей мере около 60, по меньшей мере около 70, по меньшей мере около 80 или по меньшей мере около 90 процентов от массы имплантата. В одном варианте биодеградируемая полимерная матрица составляет около 40% от массы имплантата.
Биодеградируемые полимерные матрицы, которые можно использовать, включают, но не ограничиваясь этим, полимеры, полученные из таких мономеров, как органические сложные или простые эфиры, разложение которых приводит к физиологически приемлемым продуктам. Также могут быть использованы ангидриды, амиды, ортоэфиры и тому подобное непосредственно или в комбинации с другими мономерами. Полимеры, как правило, представляют собой конденсационные полимеры. Полимеры могут быть или не быть поперечно сшитыми. Поперечно сшитые полимеры обычно лишь незначительно сшиты, и степень сшивки может составлять менее 5%, обычно менее 1%.
Особый интерес представляют полимеры гидроксиалифатических карбоновых кислот, как гомо-, так и сополимеры, и полисахариды. Представляющие интерес сложные полиэфиры включают гомо- и сополимеры D-молочной кислоты, L-молочной кислоты, рацемической молочной кислоты, гликолевой кислоты, капролактона и их комбинаций. Сополимеры гликолевой и молочной кислот представляют особый интерес, когда скорость биодеградации контролируется отношением гликолевой кислоты к молочной кислоте. Содержание каждого мономера в сополимере поли(молочной-со-гликолевой)кислоте (ПМГК) может составлять 0-100%, около 15-85%, около 25-75% или около 35-65%. В предпочтительном варианте используется сополимер 50/50 ПМГК. Более предпочтительно используется статистический сополимер 50/50 ПМГК.
Биодеградируемые полимерные матрицы, которые включают смеси ПМГК с гидрофильными и гидрофобными концами, также можно использовать, и они пригодны для изменения скоростей деградации полимерной матрицы. ПМГК с гидрофобной концевой группой (также именуемая блокированной или с блокированной концевой группой) имеет сложноэфирную связь гидрофобной природы в конце полимерной цепи. Типичные гидрофобные концевые группы включают, но не ограничиваясь ими, алкильные сложноэфирные и ароматические сложноэфирные группы. ПМГК с гидрофильной концевой группой (также именуемая неблокированной) имеет концевую группу гидрофильной природы в конце полимерной цепи. Примеры пригодных гидрофильных концевых групп, которые можно присоединять для усиления гидролиза, включают, но не ограничиваясь ими, карбоксильную, гидроксильную и полиэтиленгликолевую. Конкретная концевая группа будет, как правило, обуславливаться инициатором, используемым в полимеризационном процессе. Например, если инициатор представляет собой воду или карбоновую кислоту, образующие концевые группы будут карбоксильными и гидроксильными. Точно так же, если инициатор представляет собой монофункциональный спирт, образующиеся концевые группы будут сложноэфирными или гидроксильными.
Имплантаты могут быть получены из всех ПМГК с гидрофильными концами или всех ПМГК с гидрофобными концами. В общем, однако, соотношение между ПМГК с гидрофильным концом и гидрофобным концом в биодеградируемых полимерных матрицах по данному изобретению изменяется от около 10:1 до около 1:10 по массе. Например, соотношение может составлять 3:1, 2:1 или 1:1 по массе. В предпочтительном варианте используется имплантат, в котором соотношение между ПМГК с гидрофильным концом и гидрофобным концом составляет 3:1 по массе.
Дополнительные агенты
Для различных целей в составе можно использовать другие агенты. Например, можно использовать буферные агенты и консерванты. Консерванты, которые можно использовать, включают, но не ограничиваясь ими, гидросульфит натрия, гидросульфат натрия, тиосульфат натрия, бензалкония хлорид, хлорбутанол, тиомерсал, фенилртути ацетат, фенилртути нитрат, метилпарабен, поливиниловый спирт и фенилэтиловый спирт. Примеры буферных агентов, которые можно использовать, включают, но не ограничиваясь ими, карбонат натрия, борат натрия, фосфат натрия, ацетат натрия, гидрокарбонат натрия и тому подобное, как одобрено FDA для желаемого пути введения. Такие электролиты, как хлорид натрия и хлорид калия, также могут быть включены в состав.
Биодеградируемые глазные имплантаты также могут включать дополнительные гидрофильные или гидрофобные соединения, которые ускоряют или замедляют высвобождение активного агента. Кроме того, авторы предполагают, что так как ПМГК с гидрофильным концом характеризуется более высокой скоростью деградации, чем ПМГК с гидрофобным концом вследствие ее способности более легко поглощать воду, увеличение количества ПМГК с гидрофильным концом в полимерной матрице имплантата будет приводить к увеличение скоростей растворения. Фиг. 9 иллюстрирует, что время от имплантации до значительного высвобождения активного агента (период задержки) увеличивается с уменьшением количеств ПМГК с гидрофильным концом в глазном имплантате. На фиг. 9 показано, что время задержки для имплантатов, содержащих 0% ПМГК с гидрофильным концом (40% по массе полимера с гидрофобным концом), составляет около 21 дня. С другой стороны, наблюдалось значительное уменьшение времени задержки для имплантатов, содержащих 10% по массе и 20% по массе ПМГК с гидрофильной концевой группой.
Область применения
Примеры медицинских патологических состояний глаза, которые можно лечить имплантатами и способами изобретения, включают, но не ограничиваясь ими, увеит, макулярный отек, диабетический макулярный отек, макулярную дистрофию, отслоение сетчатки, опухоли глаза, грибковые или вирусные инфекции, многоочаговый хориоидит, диабетическую ретинопатию, пролиферативную витреоретинопатию (ПВР), симпатическую офтальмию, синдром Фогта-Коянаги-Харада (ФКХ), гистоплазмоз, увеальную диффузию и окклюзию сосудов. В одном варианте имплантаты особенно эффективны для лечения таких медицинских патологических состояний как увеит, макулярный отек, окклюзионные патологические состояния сосудов, пролиферативная витреоретинопатия (ПВР) и различные другие ретинопатии.
Способ имплантации
Биодеградируемые имплантаты могут быть введены в глаз с помощью различных способов, в том числе с помощью пинцета, троакара или устройств для введения другого типа, после выполнения надреза в склере. В некоторых случаях троакар или устройство для введения можно использовать без выполнения надреза. В варианте изобретения используют ручное устройство для введения одного или более биодеградируемых имплантатов в глаз. Ручное устройство для введения, как правило, содержит иглу из нержавеющей стали 18-30 калибра (GA), рычаг, привод и поршень.
Способ имплантации, как правило, во-первых, включает достижение целевого участка в глазничной области с помощью иглы. После попадания в целевую область, например стекловидную полость, нажимают рычаг на ручном устройстве, чтобы привод переместил поршень вперед. По мере движения поршня вперед, он выталкивает имплантат в целевую область.
Согласно варианту реализации изобретения продольную ось устройства с иглой, имеющей скошенный конец, можно удерживать параллельно кайме, а склера может образовывать косой угол со скошенным концом иглы кверху (от склеры) для получения пологой траектории в склере. Конец иглы затем можно продвинуть вперед в склере на около 1 мм (параллельно кайме), затем изменить положение по направлению к центру глаза и продвигать вперед, пока проникновение в склеру не закончится и не будет достигнута стекловидная полость глаза пациента. После этого устройство для введения можно привести в действие, чтобы доставить биодеградируемый имплантат в стекловидное тело пациента.
Способы лечения ДМО
Согласно варианту реализации изобретения способ лечения патологического состояния глаза, например диабетического макулярного отека, включает введение в глаз пациента, имеющего для этого показания, с частотой от одного раза каждые шесть месяцев до одного раза в год биоразлагаемого имплантата, содержащего активный ингредиент, такой как дексаметазон, и биодеградируемую полимерную матрицу. Биоразлагаемый имплантат может быть нескольких типов, описанных в данном документе.
Согласно некоторым вариантам реализации изобретения введение имплантата в глаз пациента может включать инъецирование имплантата в глаз пациента, имеющего для этого показания. Согласно некоторым вариантам реализации изобретения способ лечения патологического состояния глаза может включать инъецирование биоразлагаемого имплантата в стекловидное тело, переднюю камеру глаза, субконъюктивальное пространство или любую другую подходящую область глаза.
Способы можно использовать для лечения некоторых патологических состояний глаза, в том числе тех, которые связаны с ишемической ретинопатией, неоваскулярной ретинопатией, или как ишемической ретинопатией, так и неоваскулярной ретинопатией. Некоторые патологические состояния, связанные с ишемической ретинопатией, которые можно лечить с помощью способов, описанных в данном документе, могут включать диабетический макулярный отек, окклюзию центральной вены и окклюзию ветви вены. Некоторые патологические состояния, связанные с неоваскулярной ретинопатией, которые можно лечить с помощью способов, описанных в данном документе, могут включать пролиферативную диабетическую ретинопатию, экссудативную возрастную макулярную дистрофию, патологическую миопию, хориоидальную неоваскуляризацию на фоне гистоплазмоза, полипообразную хориоидальную неоваскуляризацию и ретинальную ангиоматозную пролиферацию. Способ можно использовать для лечения возрастной макулярной дистрофии, диабетического макулярного отека, патологической миопии, окклюзии ветви вены сетчатки и окклюзии центральной вены сетчатки.
«Лечить», при использовании в данном документе, означает медицинское воздействие. Оно включает, например, введение биоразлагаемого имплантата по данному изобретению для предупреждения наступления ДМО, а также для уменьшения его тяжести.
В одном варианте реализации изобретения биоразлагаемый имплантат вводят один раз каждые 6 месяцев в глаз пациента, имеющего для этого показания, для лечения ДМО. В другом варианте реализации изобретения имплантат вводят один раз каждые 4 месяца, 5 месяцев, 7 месяцев, 8 месяцев, 9 месяцев, 10 месяцев, 11 месяцев или каждые 12 месяцев (или год). В некоторых вариантах реализации изобретения биоразлагаемый имплантат вводят один раз каждые 4-12 месяцев, каждые 5-10 месяцев, каждые 6-9 месяцев или каждые 8-12 месяцев в глаз пациента, имеющего для этого показания, для лечения ДМО. В некоторых вариантах реализации изобретения биоразлагаемый имплантат вводят с одинаковой или различной периодичностью, представленной выше, в течение всей жизни пациента. В других вариантах реализации изобретения биоразлагаемый имплантат вводят с одинаковой или различной периодичностью, представленной выше, в течение 2 лет, 3 лет, 4 лет, 5 лет, 10 лет, 15 лет, всей жизни пациента, или пока патологическое состояние глаза (такое как ДМО) не вылечено в достаточной мере. Такие способы при таких режимах дозирования, которые описаны выше, могут являться терапевтически эффективными для лечения ДМО у пациента, имеющего для этого показания. В некоторых вариантах реализации изобретения способы, описанные в данном документе, могут увеличивать остроту зрения пациента с ДМО.
Так как имплантат является биодеградируемым, последующий(-ие) имплантат(-ы) можно вводить без хирургического извлечения имеющегося имплантата. Так как не наблюдаются максимальные концентрации лекарственного вещества в стекловидном теле, возникающие при необходимости часто повторяющихся инъекций, имплантат может потенциально уменьшать риск возникновения нежелательных побочных эффектов, таких как образование катаракты, возрастание ВГД и глаукома, и он может уменьшать риск возникновения осложнений, связанных с инъекциями, таких как повреждение хрусталика, отслоение сетчатки и инфекционный эндофтальмит.
Согласно некоторым вариантам реализации изобретения биоразлагаемый имплантат может лечить патологическое состояние глаза у пациента с макулярным отеком, таким как диабетический макулярный отек, независимо от типа линз пациента. Например, в некоторых вариантах реализации изобретения лечение ДМО можно проводить, используя имплантаты и способы, описанные в данном документе, вне зависимости от того, факичная или псевдофакичная линза у пациента. Согласно некоторым вариантам реализации изобретения лечение ДМО можно проводить у пациентов с псевдофакичными линзами. Согласно некоторым вариантам реализации изобретения лечение ДМО можно проводить у пациентов с факичными линзами, но у которых запланировано или предполагается хирургическое удаление катаракты.
Согласно некоторым вариантам реализации изобретения биоразлагаемый имплантат может лечить патологическое состояние глаза у пациента, который невосприимчив к другим существующим способам лечения ДМО. Например, согласно некоторым способам пациента с ДМО, который невосприимчив к анти-VEGF внутриглазным инъекциям, можно эффективно лечить с помощью способов, описанных в данном документе. Согласно некоторым другим способам пациента с ДМО, который невосприимчив к лазерной фотокоагуляции, можно эффективно лечить с помощью способов, описанных в данном документе.
ПРИМЕРЫ
Следующие примеры представлены с целью дополнительного описания вариантов реализации изобретения, представленных в данном документе, и не ограничивают объем изобретения.
Многоцентровое маскированное рандомизированное плацебо-контролируемое исследование фазы III было проведено для оценки безопасности и эффективности системы доставки лекарственного средства с содержанием дексаметазона 700 мкг и 350 мкг в задний отрезок глаза пациентов с диабетическим макулярным отеком («ДМО»). Исследование проводили в течение трех лет. Результаты этих исследований показаны на фиг. 1-7.
Имплантаты, используемые в исследовании, состояли из дексаметазона и полимерной матрицы из 50:50 поли(D,L-лактид-со-гликолида) ПМГК, содержащего 2 типа ПМГК (50:50 ПМГК со сложноэфирными группами и 50:50 ПМГК с карбоксильными группами). Подробности см. в Таблице 1. Две комбинации ПМГК, как показано в Таблице 2, были выбраны для биодеградируемой полимерной матрицы. Общие свойства выбранных ПМГК представлены в Таблице 3.



В исследовании пациенты с ДМО получали или биоразлагаемый имплантат, содержащий 700 мкг дексаметазона, биоразлагаемый имплантат, содержащий 350 мкг дексаметазона, или биоразлагаемый имплантат, содержащий 0 мкг дексаметазона (плацебо). Имплантаты инъецировали в стекловидное тело одного глаза каждого пациента. Необходимость повторного лечения пациентов определяли каждые 3 месяца после посещения в 6 месяц. Повторное лечение (т.е. введение другого имплантата) разрешено каждые 6 месяцев. Повторное лечение разрешено, если толщина сетчатки пациента в центральной области была больше 175 мкм, или если наблюдался остаточный отек сетчатки. Максимально допускалось 7 имплантатов в один глаз пациента в течение трехлетнего периода исследования.
Как показано на фиг. 1-2, у пациентов, получавших имплантат с 700 мкг дексаметазона и пациентов, получавших имплантат с 350 мкг дексаметазона наблюдалось статистически значимое улучшение остроты зрения с максимальной коррекцией («ОЗМК») по сравнению с пациентами, получавшими имплантат-плацебо. Фиг. 1 иллюстрирует, что 22,2% пациентов, получавших имплантат с 700 мкг дексаметазона, продемонстрировали улучшение ОЗМК на 15 или более букв, и 18,4% пациентов, получавших имплантат с 350 мкг дексаметазона, продемонстрировали улучшение ОЗМК на 15 или более букв. Фиг. 2 иллюстрирует, что 8,5% пациентов, получавших имплантат с 700 мкг дексаметазона, продемонстрировали улучшение ОЗМК на 20 или более букв, и 11,0% пациентов, получавших имплантат с 350 мкг дексаметазона, продемонстрировали улучшение ОЗМК на 20 или более букв.
Фиг. 3 иллюстрирует, что пациенты в группах, получавших имплантаты, содержащие 700 мкг и 350 мкг дексаметазона, в общем продемонстрировали большее улучшение ОЗМК в течение трехлетнего периода исследования по сравнению с пациентами, получавшими имплантат-плацебо. Как показано на фиг. 3, у пациентов, получавших имплантаты с дексаметазоном, наблюдалось быстрое увеличение ОЗМК. Так, среднее увеличение ОЗМК на около 6 букв по сравнению с исходным уровнем наблюдалось в течение первых около 3 месяцев лечения для пациентов, получавших имплантат с 350 мкг дексаметазона, и среднее увеличение ОЗМК на около 7 букв по сравнению с исходным уровнем наблюдалось в течение первых около 3 месяцев лечения для пациентов, получавших имплантат с 700 мкг дексаметазона.
Как показано на фиг. 4, среднее уменьшение толщины сетчатки в центральном подполе ("CSRT") по сравнению с исходной толщиной было больше у пациентов, получавших имплантаты с дексаметазоном, чем у пациентов, получавших имплантат-плацебо. Фиг. 4 иллюстрирует, что пациенты, получавшие имплантат с 700 мкг дексаметазона, продемонстрировали среднее уменьшение CSRT на 111,6 мкм по сравнению с исходной толщиной, и пациенты, получавшие имплантат с 350 мкг дексаметазона, продемонстрировали среднее уменьшение CSRT на 107,9 мкм по сравнению с исходной толщиной.
Как показано на фиг. 5, имплантаты с дексаметазоном приводили к значительному улучшению ОЗМК вне зависимости от типа линз пациента при определении исходной остроты.
Краткое описание нежелательных явлений, которые наблюдались в исследовании, показано ниже на фиг. 6. Как показано на фигуре, наиболее распространенными нежелательными явлениями, наблюдаемыми в исследовании, были катаракта и внутриглазное давление. Однако, несмотря на возникновения такого нежелательного явления, как увеличенное ВГД, неожиданно, очень небольшое количество пациентов (около 0,3% на каждый тип хирургического вмешательства для каждой группы в исследовании) подвергались хирургическому вмешательству в течение исследования для лечения ВГД. Количество пациентов, которые подвергались хирургическому вмешательству, и тип проведенного хирургического вмешательства представлены на фиг. 7.
Как видно из данных на фигурах, имплантаты и способы, описанные в данном документе, приводили к значительному длительному улучшению зрения у пациентов с диабетическим макулярным отеком. В третий год исследования доля пациентов с улучшением на 15 или более букв была значительно выше для имплантатов с 350 мкг и 700 мкг дексаметазона по сравнению с плацебо. Польза от лечения наблюдалась в среднем от 4,1 инъекции в течение 3 лет.
Таблица 4 ниже иллюстрирует результаты определения остроты зрения в 39 месяц исследования.

Таблица 5 ниже иллюстрирует результаты определения остроты зрения с максимальной коррекцией для подгрупп с псевдофакичными и факичными линзами.

Хотя данное изобретение было раскрыто в контексте некоторых предпочтительных вариантов реализации и примеров, специалистам в данной области будет понятно, что настоящее изобретение выходит за рамки конкретных раскрытых вариантов реализации изобретения в другие альтернативные варианты реализации изобретения и/или способы применения изобретения и их очевидные модификации и эквиваленты. Дополнительно, хотя ряд вариаций изобретения был показан и подробно описан, другие модификации, которые находятся в рамках данного изобретения, будут очевидны для специалистов в данной области техники, исходя из данного описания. Также подразумевается, что могут быть составлены различные комбинации или субкомбинации конкретных признаков или аспектов вариантов реализации изобретения, которые тем не менее находятся в рамках изобретения. Следовательно, следует понимать, что различные признаки и аспекты раскрытых вариантов реализации изобретения могут быть объединены друг с другом или заменены друг на друга для того, чтобы осуществить различные способы раскрытого изобретения. Таким образом, предполагается, что объем настоящего изобретения, раскрытого в данном документе, не должен быть ограничен конкретными раскрытыми вариантами реализации изобретения, описанными выше, а должен определяться только путем тщательного прочтения формулы изобретения.