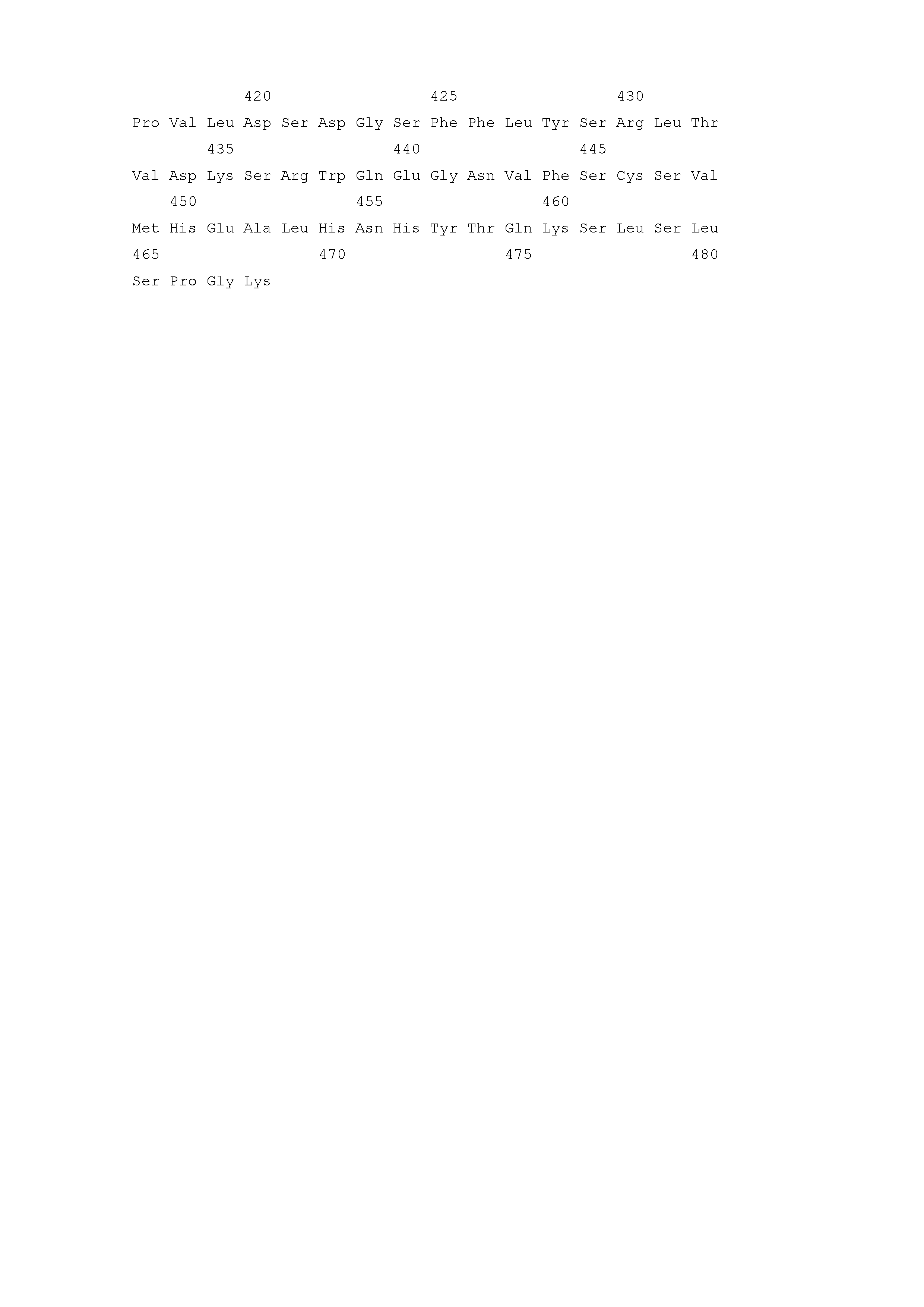Результат интеллектуальной деятельности: НУКЛЕОТИДНАЯ ПОСЛЕДОВАТЕЛЬНОСТЬ, КОДИРУЮЩАЯ СЛИТЫЙ БЕЛОК, СОСТОЯЩИЙ ИЗ РАСТВОРИМОГО ВНЕКЛЕТОЧНОГО ДОМЕНА ЧЕЛОВЕЧЕСКОГО TNFR1 И КОНСТАНТНОЙ ЧАСТИ ТЯЖЁЛОЙ ЦЕПИ ЧЕЛОВЕЧЕСКОГО IGG4
Вид РИД
Изобретение
Область техники
Изобретение относится к биотехнологии, медицинским технологиям, в частности к созданию высокоэффективных лекарственных средств на основе биологических молекул.
Уровень техники
Последние достижения в области молекулярной и клеточной биологии позволили вывести понимание патофизиологических процессов, лежащих в основе большинства социально-значимых заболеваний на качественно новый уровень. В свою очередь это позволило создать новый класс биологических препаратов, специфически воздействующих лишь на ключевые молекулярные звенья патофизиологических процессов. Применение этого класса препаратов в медицине - «таргетная терапия» - по сравнению с предшествующими лекарственными препаратами показывает лучшую эффективность и безопасность за счет узкой направленности конкретные органы, ткани или типы клеток.
На сегодняшний день существует несколько подходов к созданию высоко специфичных препаратов. Из них в качестве лекарственных средств пока зарегистрирован ряд малых молекул, антител и растворимых рецепторов («трапы»). При этом биологические лекарственные препараты, например, на основе антител, в сочетании с равными или более высокими показателями эффективности, имеют лучшую переносимость и меньшие побочные эффекты, чем химические.
Большая часть ключевых игроков на рынке биологических препаратов используют для их создания технологию производства моноклональных антител (Novartis, Roche, Amgen). Она относится к одной из наиболее универсальных для создания лекарственных средств, поскольку позволяет создавать агенты против самых различных терапевтических мишеней. Однако, существенным «минусом» технологии является сложность и высокая стоимость разработки в сочетании с высокой наукоемкостью производством.
Технология, которая решает указанную проблему, это технология производства рецепторов-«трапов». В первую очередь, рецепторы-«трапы» имеют лучшие показатели временных и финансовых затрат на создание и производство терапевтического препарата по сравнению с моноклональными антителами. Это обусловлено отсутствием необходимости проведения длительных и дорогостоящих экспериментов по иммунизации, гуманизации и скринингу антител. Во-вторых, терапевтически агенты рецепторы-«трапы» обладают большей эффективностью. Ключевым игроком на данном рынке является компания Регенерон, имеющая на территории РФ зарегистрированный в качестве лекарственного средства рецептор-«трап» для лечения макулодистрофии - Эйлеа® (Афлиберцепт).
Технология получения рецепторов-«трапов» основана на создании гибридного белка, способного эффективно и быстро связывать молекулу-мишень. Как правило, рецептор-«трап» состоит из двух частей - внеклеточного домена рецептора молекулы-мишени Fc-домена иммуноглобулина. Внеклеточный домен рецептора отвечает за связывание мишени, а Fc-домен осуществляет димеризацию гибридного белка. Последнее необходимо для увеличения эффективности связывания и обеспечения большей стабильности высокомолекулярного комплекса.
Присутствующий на рынке препарат на основе рецептора-«трапа» Etanercept (Enbrel), адресно связывающий фактор некроза опухолей (TNFα, ФНО), характеризуется рядом свойств, которые могут быть существенно превзойдены путем создания новой комбинаторной белковой конструкции, состоящей из частей биологических молекул с заданными свойствами.
Несмотря на наличие нескольких биологических препаратов, нейтрализующих фактор некроза опухолей TNFα, на рынке сохраняется потребность в новых биологических препаратах с улучшенными свойствами. Эта потребность обусловлена высокой стоимостью инновационных препаратов, часто возникающей резистентностью пациентов к определенному препарату (связанную с его иммуногенностью), а также с растущим во всем мире числом аутоиммунных заболеваний, в которых ФНО играет ключевую роль в патологическом процессе. Данное изобретение обладает рядом улучшенных свойств по сравнению с аналогами, и поэтому расширяет круг имеющихся кандидатов для лечения заболеваний, вызванных гиперактивацией ФНО.
Сущность изобретения
Задачей настоящего изобретения является расширение арсенала технических средств для лечения заболеваний, вызванных гиперактивацией TNFα (ФНО), и создание терапевтического агента на основе слитого белка TNFR-Fc с улучшенными свойствами. Указанная задача решается путем создания гибридного полипептид-антагониста фактора некроза опухолей, имеющего аминокислотную последовательность SEQ ID NO: 2, а также создания молекулы нуклеиновой кислоты, кодирующей данный гибридный полипептид-антагонист фактора некроза опухолей. В некоторых вариантах изобретения данная молекулы нуклеиновой кислоты имеет нуклеотидную последовательность SEQ ID NO: 1. Также указанная задача решается путем создания экспрессирующего вектора, содержащего данную молекулу нуклеиновой кислоты под контролем регуляторных элементов, необходимых для экспрессии данной нуклеиновой кислоты в клетке-хозяине. В предпочтительных вариантах изобретения в качестве клетки-хозяина могут выступать клетки яичников китайских хомячков CHO (клеточные линии CHO-К1 или CHO DG44), адаптированные для производства терапевтических белков.
В настоящем изобретении экспрессирующий вектор предпочтительно подбирается для экспрессии гетерологичных последовательностей в клетках млекопитающих, но в некоторых вариантах изобретения экспрессирующий вектор может быть выбран для экспрессии в других системах, таких как, например, клетки насекомых, дрожжевые или бактериальные клетки. Соответственно, каждый экспрессирующий вектор имеет свой набор регуляторных элементов, позволяющих проводить экспрессию гетерологичной последовательности (продукта) в клетке-хозяине, таких как промоторы и/или энхансеры, и/или polyA последовательности.
При осуществлении изобретения достигается следующий технический результат: создан новый вариант терапевтического агента на основе гибридного белка с улучшенными свойствами и с последовательностью SEQ ID NO: 2 для блокировки воспалительного цитокина ФНО, при этом данный гибридный белок обладает: а) только минимальной эффекторной функцией антитело-зависимой клеточной цитотоксичности; б) не обладает комплемент-зависимой цитотоксичностью; в) потенциально улучшенными фармакокинетическими свойствами из-за введения шарнирного участка, позволяющего эктодомену TNFR1 и домену Fc действовать независимо друг от друга.
Краткое описание рисунков
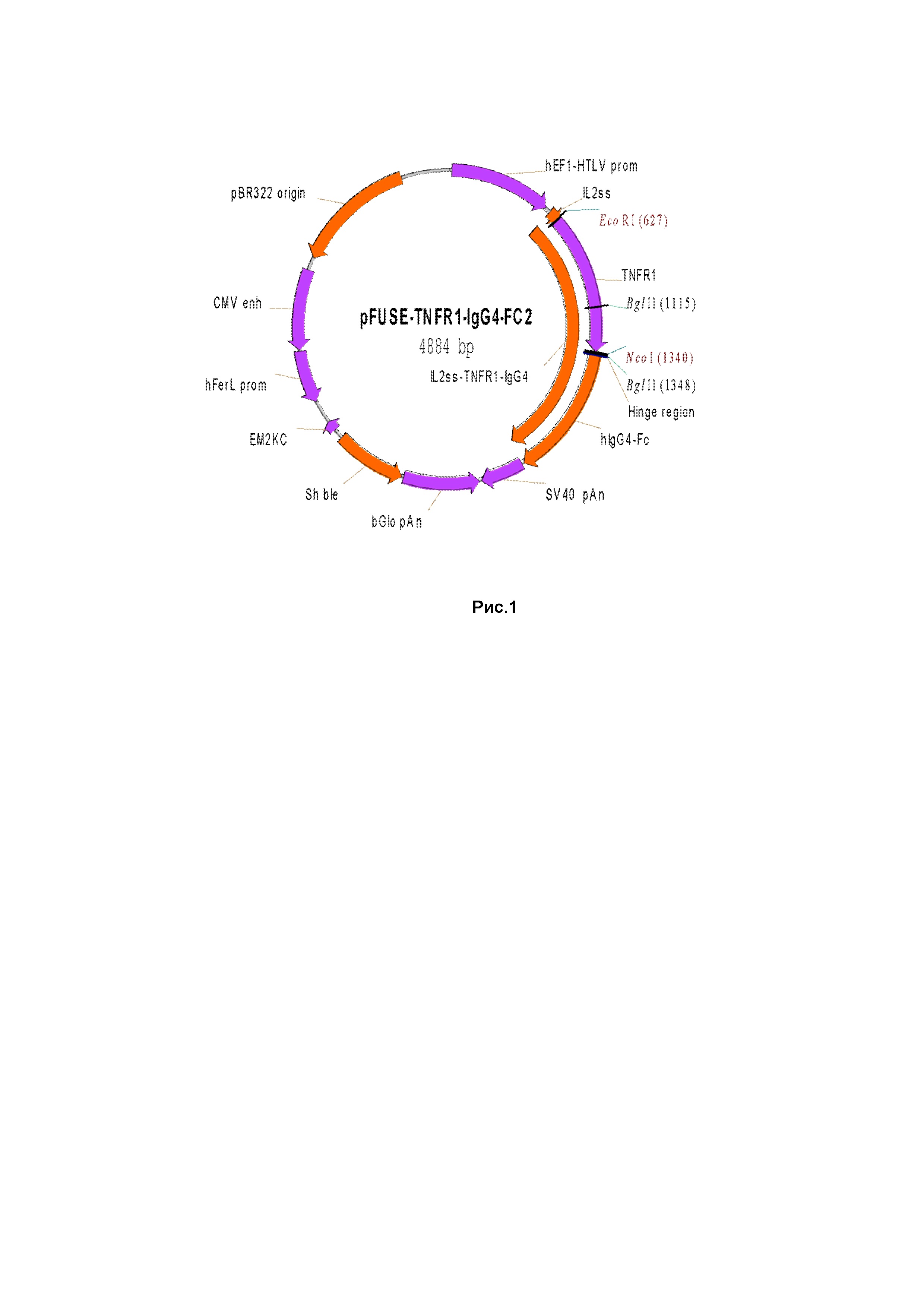
Рис.1. Схема экспрессирующего вектора, содержащего заявляемую нуклеотидную последовательность, кодирующую гибридный полипептид-антагонист фактора некроза опухолей TNFR1-hinge-hIgG4_Fc.
Подробное раскрытие изобретения
В описании данного изобретения термины «включает» и «включающий» интерпретируются как означающие «включает, помимо всего прочего». Указанные термины не предназначены для того, чтобы их истолковывали как «состоит только из».
Сущность технического решения заключается в создании нуклеотидной последовательности (SEQ ID No:1), которая кодирует гибридный белок с последовательностью SEQ ID No:2, состоящий из сигнального пептида (аминокислоты 1 - 20) и трех функциональных частей, первая из которых кодирует растворимый внеклеточный домен человеческого TNFR1 (он же TNFRSF1A, CD120a; FPF; MS5; TBP1; TNF-R; TNF-R-I; TNF-R55; TNFAR; TNFR1; TNFR1-d2; TNFR55; TNFR60; p55; p55-R; p60) (аминокислоты 21 - 255), вторая кодирует шарнирный участок (аминокислоты 261 - 267), а третья кодирует константную часть тяжёлой цепи человеческого IgG4 (аминокислоты 268 - 484).
Кодирующая нуклеотидная последовательность SEQ ID No:1 может быть изменена для оптимизации уровня экспрессии в клетках определенного типа. При использовании гетерологичных систем экспрессии (например, клетки насекомых, бактериальные или дрожжевые клетки) может потребоваться оптимизация кодонов в последовательности (замена редко используемых в организме кодонов на часто используемые). Это можно сделать с помощью алгоритмов, реализованных во многих имеющихся алгоритмах для проектирования последовательностей, например, Codon optimizer, Gene Designer, или OPTIMIZER.
Экспрессия гибридной конструкции в клетках млекопитающих возможна при помощи создания стабильных клонов-продуцентов после трансфекции клеток этой конструкцией. Может быть использована трансфекция электропорацией или с использованием трансфецирующего реагента, такого как Lipofectamine 2000. Данная гибридная конструкция может быть также использована для введения в лентивирусную конструкцию и последующего заражения клеток. Для увеличения выхода гибридного белка в клетках млекопитающих возможно использование различных подходов. Методы оптимизации известны специалистам и описаны, например, в (Almo SC, Love JD. Better and faster: improvements and optimization for mammalian recombinant protein production. Curr Opin Struct Biol. 2014 Jun;26:39-43).
Заявляемый продукт является ранее не создававшейся комбинацией нуклеотидных последовательностей генома человека и призван быть экспрессионной основой для слитого белка с предсказываемыми улучшенными фармакологическими свойствами для блокировки воспалительных цитокина ФНО при лечении ревматоидного артрита и увеита, а именно: (1) минимальной эффекторной функцией для антитело-зависимой клеточной цитотоксичности (antibody-dependent cellular cytotoxicity - ADCC) и комплемент-зависимой цитотоксичности (complement-dependent cytotoxicity - CDC) благодаря использованию константной части иммуноглобулина человека IgG4-изотипа; (2) потенциально улучшенными фармакокинетическими свойствами из-за введения шарнирного участка, который позволяет двум частям молекулы, а именно внеклеточному домену TNFR1 и Fc действовать независимо друг от друга за счет увеличения гибкости молекулы на данном участке. Предполагаемая константа связывания гибридного полипептида с фактором некроза опухолей составляет около 1 нM, что достаточно для осуществления эффективной блокировки ФНО in vivo (Lang I et al., "Binding Studies of TNF Receptor Superfamily (TNFRSF) Receptors on Intact Cells" J Biol Chem, 2016 Mar 4;291(10):5022-37). После прохождения испытаний по безопасности на животных и клинических испытаний, гибридный белок по настоящему изобретению может быть включен в состав фармацевтической композиции для лечения заболеваний человека, таких как ревматоидный артрит и увеит.
Нижеследующие примеры приведены в целях раскрытия характеристик настоящего изобретения и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения.
Пример 1. Конструирование плазмиды.
Для конструирования плазмиды с заявляемой нуклеотидной последовательностью использована плазмида RG208641, содержащая участок, кодирующий рецепторную часть белка hTNFR - TNFRSF1B (NM_001066) Human Tagged ORF Clone (CAT#: RG208641, OriGene, US, https://www.origene.com/catalog/cdna-clones/expression-plasmids/rg208641/tnfrsf1b-nm_001066-human-tagged-orf-clone ). Рецепторная (внеклеточная, растворимая) часть белка TNFR1 была выбран биоинформатическим анализом последовательности и использована для последующего клонирования. Для клонирования этого участка подобраны следующие праймеры:
Lob_TNF_F TATGAATTCGTTGCCCGCCCAGGTGGCA
Lob_TNF_R TATCCATGGCGTCGCCAGTGCTCCCTTCA
В праймеры были включены сайты рестрикции для рестриктаз EcoRI (прямой праймер Lob_TNF_F) и NcoI (обратный праймер Lob_TNF_R)
Проведена ПЦР со следующими условиями: 94 оС 3 мин, 25 циклов (94 оС 15 сек, 61 оС 15 сек, 72 оС 1 мин), 72оС 5 мин. Компоненты реакции: полимераза – смесь 9:1 Taq – полимеразы с Furia – полимеразой (производство «Бигль»), буфер для Taq-полимеразы с сульфатом аммония и 2,5 mM MgCl2 (Fermentas), по 0,4 mM каждого из праймеров и 0,25 mM смеси трифосфатов нуклеотидов (Fermentas). После ПЦР: ПЦР продукт очищали набором для очистки ПЦР продуктов PCR Purification kit QIAquick (QiaGene Cat.No 28106). Концентрация и соответствие предсказанному молекулярному весу проверяли при помощи гель-электрофореза в 1% агарозе (ТАЕ буфер). Полученный ПЦР продукт с рестрикционными сайтами EcoRI и NcoI был использован для дальнейшего конструирования.
Целевой вектор (InvivoGen) и ПЦР продукт обрабатывали рестриктазами EcoRI и NcoI (Fermentas) в течение 1 часа при 37 оС, очищали с помощью PCR Purification kit QIAquick и лигировали, используя 1 U лигазы (Fermentas) по протоколу производителя. Лигазной смесью трансформировали компетентные клетки E.coli Xl10-gold и высевали на среду LB, содержащую зеоцин. Чашки инкубировали в термостате в течение ночи при 37 oC. На следующий день из 20 колоний проверяли на присутствие нужной вставки, для этого часть колонии разводили в 50 мкл воды и кипятили в течение 5 минут. После охлаждения смесь использовали в качестве матрицы в реакции ПЦР. Присутствие вставки проверяли после электрофореза ПЦР продуктов. Из двух колоний, содержащих вставку выделяли плазмидную ДНК и секвенировали на секвенаторе Applied Biosystems 3500 по инструкции производителя, используя праймеры F2(прямой) и FC(обратный).
Сконструированная в результате плазмида, содержащая заявляемую нуклеотидную последовательность, была проверена на отсутствие ошибок при помощи секвенирования с двух праймеров F2 (прямой) и FC (обратный), и показана на Рис. 1.
Пример 2. Продукция гибридного белка.
Для продукции гибридного полипептид-антагониста фактора некроза опухолей TNFR1-hinge-hIgG4_Fc получали стабильную клеточную линию на основе клеток яичников китайских хомячков CHO-K1, адаптированных для производства терапевтических белков. Для получения стабильной клеточной линии использовали прибор Nucleofector 2b (Lonza, Швейцария) и набор Amaxa® Nucleofector® kit T (Lonza, Швейцария) согласно инструкции производителя. Клетки, находившиеся в состоянии 60% конфлюэнтности, снимали с флакона обработкой 0.25% раствором трипсина в изотоническом буфере. Открепившиеся клетки ресуспендировали в 4.5 мл среды DMEM с 10% бычьей фетальной сыворотки и использовали 1 млн. клеток для одной трансфекции. Суспензию клеток центрифугировали 5 мин при 150 g. Полученный клеточный осадок ресуспендировали в свежеприготовленном растворе Nucleofector® Solution (Lonza, Швейцария), добавляли 2 мкг соответствующей линеаризованной плазмиды, переносили в кювету и запускали программу трансфекции U-023 (максимальная эффективность, низкая выживаемость). После чего рассевали в 6-луночные планшеты в ростовой среде без селектирующего антибиотика. Спустя 6 часов прикрепившиеся клетки снимали и рассевали 1 лунку 6-луночного планшета на 24-луночный планшет. Спустя 16 часов после трансфекции клеточная культура подвергалась селекции на антибиотике зеоцин с концентрацией 600 мкг/мл. Для этого ростовую среду заменяли на свежую с антибиотиком по 0.5 мл в лунку. Спустя 3 дня среду меняли на 0.5 мл свежей среды с антибиотиком. Процедуру повторяли каждые 3 дня до достижения конфлюэнтности клеток в лунках. После этого лунки тестировали с целью определения уровня экспрессии гибридного белка. Для скрининга на экспрессию Fc-гибрида одиночные колонии выращивали в 96-луночном планшете (Corning, США) с 80 мкл среды CSFM (полная бессывороточная среда, содержащая 25 мM Hepes, 50 IU/мл пенициллина, инсулин, трансферрин и селениум (Invitrogen, США). На следующий день отбирали среду и содержимое анализировали при помощи стандартного гель-электрофореза в полиакриамидном геле (SDS-PAGE). Секретируемый гибридный белок визуализировали с использованием кроличьих антител против человечьего Fc-домена (Jackson Immunoresearch, США). Отдельные отобранные по уровню экспрессии колонии подвергали трипсинизации и клетки переносили в лунку 12-луночного планшета. Далее выросшие клетки частично замораживали, а частично субклонировали, используя 96-луночный планшет. Субклонирование повторяли до тех пор, пока все одиночные колонии показывали стабильно высокий уровень экспрессии гибридного белка, тогда такую колонию сохраняли для создания банка из клонов-продуцентов. Для продукции гибридного белка размороженные клетки ресуспендировали в 10 мл свежей ростовой среды и высевали в 2 флакона (25 см2). По достижении конфлюэнтности клетки пересевали последовательно последовательно во флаконы большей емкости. Спустя 3 дня среду с сывороткой меняли на бессывороточную среду ProCHO4 (Lonza, Швейцария) с добавками 4 мМ дипептида GlutaMAX (Gibco, США) и смеси антибиотиков. Для очистки гибридного белка культуральную среду, полученную в процессе роста клонов-продуцентов, подвергали фильтрации от клеточного дебриса с использованием фильтрационных модулей 0.45 мкм и 0.22 мкм (Millipore, США). Далее гибридный белок очищали при помощи аффинной хроматографии с использованием Протеин А сефарозы (Millipore, США); элицию с колонки проводили при помощи буфера с низким рН. Полученный гибридный белок тестировали на функциональную активность (связывание и инактивация ФНО) при помощи стандартных методов, таких как метод поверхностного плазмонного резонанса (SPR) и функциональные тесты на активность ФНО.
Несмотря на то, что изобретение описано со ссылкой на раскрываемые варианты воплощения, для специалистов в данной области должно быть очевидно, что конкретные подробно описанные эксперименты приведены лишь в целях иллюстрирования настоящего изобретения, и их не следует рассматривать как каким-либо образом ограничивающие объем изобретения. Должно быть понятно, что возможно осуществление различных модификаций без отступления от сути настоящего изобретения.