Результат интеллектуальной деятельности: ФАРМАЦЕВТИЧЕСКАЯ КОМПОЗИЦИЯ ДЛЯ ИНТРАОПЕРАЦИОННОЙ ВИЗУАЛИЗАЦИИ ЛИМФАТИЧЕСКИХ УЗЛОВ МЕТОДОМ НЕПРЯМОЙ ЦВЕТНОЙ ЛИМФОГРАФИИ
Вид РИД
Изобретение
Изобретение относится к области медицины, связанной с хирургическим лечением злокачественных опухолей, в частности, с интраоперационным определением сторожевых лимфатических узлов в области регионарного лимфоотока от зоны роста злокачественного новообразования.
Ранее для определения сторожевых лимфатических узлов использовалась композиция на основе трифенилметанового красителя натриевой соли 4-{[(4-диэтил-амино)фенил][4-(диэтил-имино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,4-дисуль-фоната в фосфатном буфере. Данная композиция известна под торговым названием «Лимфозурин», производится только в США, и в Российскую Федерацию не поставляется.
Нами было установлено, что изомер трифенилметанового красителя «Лимфозурина» динатриевая соль 4-{[(4-диэтиламино) фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната, известный под торговым названием «Дисульфиновый голубой VN 150» обладает значительно большей лимфотропностью чем «Лимфозурин» однако выход его является незначительным и сопровождается большим количество побочных продуктов.
Так, еще в 1936 году, в СССР, был разработан способ получения синего красителя «Дисульфиновый голубой VN 150» (cas 129-17-9) (А.с. СССР №50850), который получали из толуола, путем сульфирования в среде олеума до толуол-2,4-дисульфокислоты, и после-дующим окислением метальной группы в бензальдегидную. Образующийся бензальдегид-2,4-дисульфокислота в кислой среде конденсировали с диэтиланилином до соответствующего триарилкарбинольного соединения, которое при окислении в кислой среде высаливалось с помощью хлорида натрия в виде соответствующей натриевой соли 4-{[(4-ди-этиламино) фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-или-ден]-метил}бензо-1,3-дисульфоната.
Недостатком данного способа является длительность получения конечного продукта (более 70 часов), поскольку конденсация бензальдегид-2,4-дисульфокислоты с диэтиланилином осуществляется при кипячении в кислой среде в течение 48 часов с относительно небольшим выходом конечного продукта (около 20%, считая на исходные реагенты), а также большое количество побочных продуктов реакции, затрудняющих очистку целевого продукта.
Известен способ получения триарилметановых красителей (А.с. 219725) который получают из толуол-2,4-дисульфокислоты, путем взаимодействия с диэтиланилином с образованием соответствующего триарилкарбинольного соединения с выходом 85% в присутствии гексахлорциклофосфазотриена.
Однако используемый в качестве реакционной среды гексахлорциклофосфазотриен получается с выходом не более 50% и является неустойчивым соединением, что обусловливает низкую технологичность представленного способа.
Известно получение триарилкарбинола (US 2726252 А), в котором конденсацию диэтиланилина и динатриевой соли бензальдегид-2,4-дисульфокислоты, полученной традиционным способом из толуол-2,4-дисульфокислоты, проводят в кипящей ледяной уксусной кислоте в присутствии эквимолярного количества карбамида.
Недостатком данного способа является длительная процедура конденсации исходного дисульфобензальдегида и диэтиланилина и низкий общий выход продукта конденсации (20%), который сопоставим с таковым, получаемом при способе, описанном в первом способе (А.с. СССР №50850).
Наиболее близким решением является способ получения синего изосульфана (американский препарат «Lymphazurin» (US 20120078007 A1), представляющий собой композицию, состоящую из синего красителя натриевой соли 4-{[(4-диэтиламино)фенил] [4-(диэтил-имино)-циклогекса-2,5 диен-1-илиден] -метил} бензо-1,4-дисульфоната в фосфатном буфере (флакон, содержащий 5 мл раствора препарата с концентрацией активного вещества 1 мг/мл, $600).
Однако, выход при синтезе конечного продукта - натриевой соли 4-{[(4-диэтиламино)фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}-бензо-1,4-дисульфоната низкий и составляет всего 8,5% в пересчете от исходного 2-хлор-бензальдегида, что является основной причиной высокой стоимости препарата «Lymphazurin». В экспериментах на животных препарат «Lymphazurin» обладает выраженными лимфотропными свойствами и эффективно прокрашивает лимфатические сосуды и лимфатические узлы в зоне регионарного лимфооттока по отношению к месту введения препарата. В США и других странах, в которых препарат разрешен для клинического применения, препарат «Lymphazurin» эффективно используется для интраоперационной визуализиции сторожевых лимфатических узлов методом непрямой цветной лимфографии у больных злокачественными новообразованиями. Данная процедура выполняется для идентификации и последующего исследования состояния регионарных лимфатических узлов первого уровня лимфооттока с целью уточнения стадии заболевания и индивидуально обоснованного выбора тактики дальнейшего лечения.
В настоящее время препарат «Lymphazurin» и его аналоги не производятся в Российской Федерации и не зарегистрированы в качестве ЛС на территории Российской Федерации.
Таким образом, разработка технологичного способа получения лимфотропного диагностического ЛС, аналогичного по лимфотропным свойствам препарату «Lymphazurin», является насущной потребностью, как для решения задач клинической онкологии, так и с точки зрения вопроса импортозамещения.
Техническим результатом предполагаемого изобретения является разработка отечественного лимфотропного диагностического ЛС - «Лимфотропина» на основе трифенилметанового красителя динатриевой соли 4-{[(4-ди-этила-мино)фенил][4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил }бензо-1,3-дисульфоната, которая превосходит по лимфотропным свойствам краситель на основе 1,4-дисульфоната (Лимфозурин).
Указанный технический результат достигается за счет того, что нами было впервые обнаружено и доказано физико-химическими методами, что основной красящий компонент в трифенилметановом красителе «Дисульфиновый голубой VN 150» является не моно-, а динатриевая соль 4-{[(4-ди-этиламино) фенил][4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната, получающаяся при конденсации динатриевой соли бензальдегид-2,4 дисульфокислоты и диэтиламином в контролируемой конденсации и дополнительной очистке на хроматографической колонне. Предлагаемая нами фармацевтическая композиция, по своим лимфотропным свойствам и доступности превосходит «Лимфозурин» (США), что было нами доказано и продемонстрировано при интраоперационной визуализиции лимфатических узлов методом непрямой цветной лимфографии.
Особенность заявляемого изобретения заключается в том, что в качестве лимфотропного красителя используют смесь синего трифенилметанового красителя - динатриевой соли 4-{[(4-ди-этиламино) фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисульфоната, дигидрофосфата натрия, дигидрофосфата калия в соотношении компонентов в одном миллилитре (мг): 5,0-20,0:6,6:2,7. Концентрация динатриевой соли 4-{[(4-ди-этиламино) фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната в композиции может варьироваться в интервале от 5 мг/мл до 20 мг/мл. Полученная композиция может применяться в виде раствора с вариацией значения рН от 5,0 до 8,0. Оптимальное время регистрации накопления композиции составляет от 5 до 40 минут. Для получения лимфотропного красителя можно использовать доступную п-толуолсульфокислоту. Для получения динатриевой соли 4-{[(4-диэтил-амино) фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисуль-фоната проводят конденсацию динатриевой соли бензальдегид-2,4-дисульфокислоты с диэтиланилином в расплаве карбамида с добавлением хлорида цинка. Для получения динатриевой соли 4-{[(4-диэтил-амино) фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисуль-фоната проводят конденсацию бензальдегид-2,4-дисульфокислоты с диэтиланилином в расплаве смеси пятихлористого фосфора и хлорида аммония. Полученную композицию применяют путем перитуморального внутритканевого введения в виде растворов объемом от 0,5 мл до 2,0 мл.
Изобретение поясняется подробным описанием, клиническими примерами и иллюстрациями, на которых изображено:
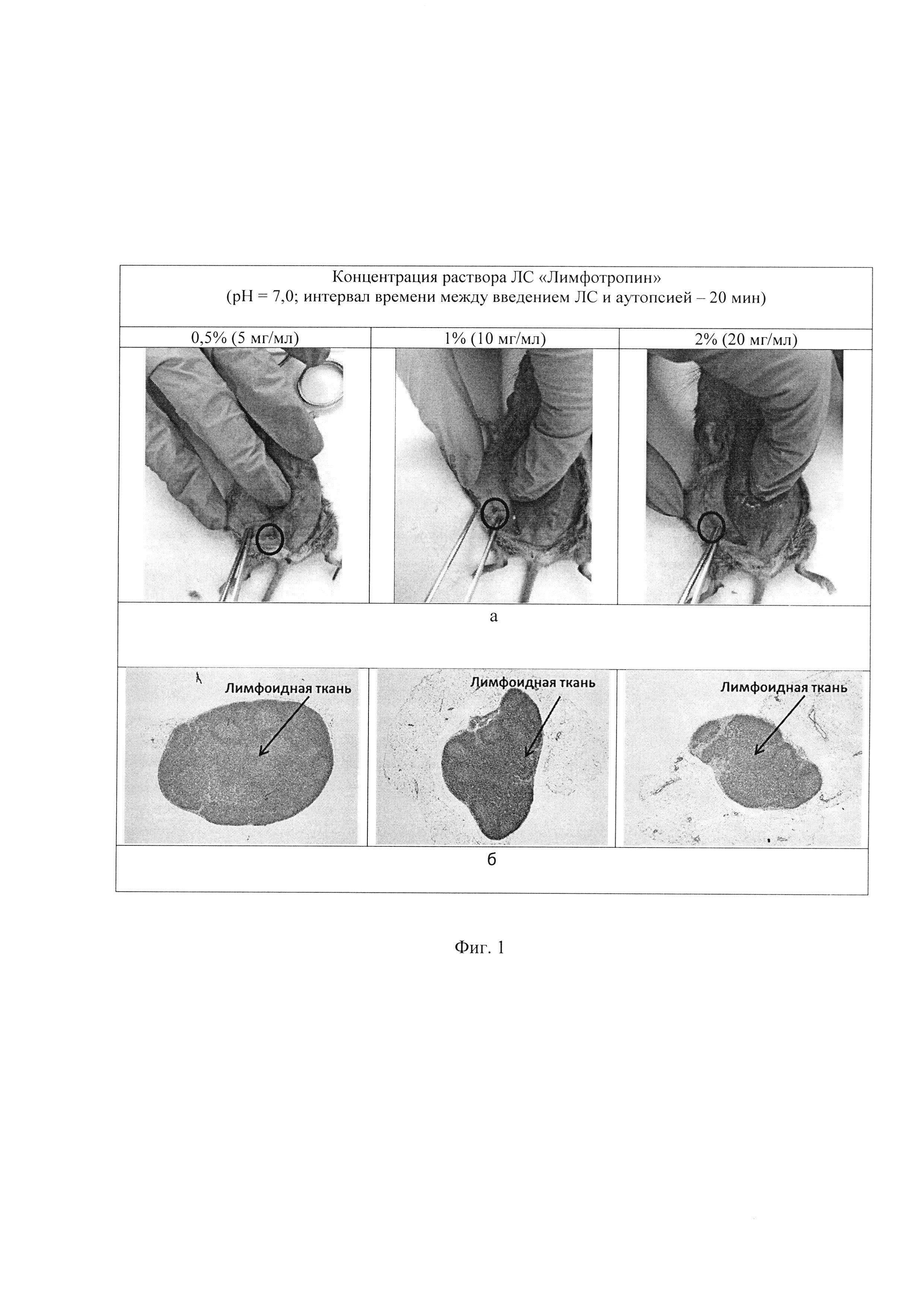
Фиг. 1 - показаны результаты непрямой цветной лимфографии с ЛС «Лимфотропин» у мышей в зависимости от его концентрации; а) макроскопическая оценка, б) гистологическая верификация лимфатического узла (увеличение: 40×)
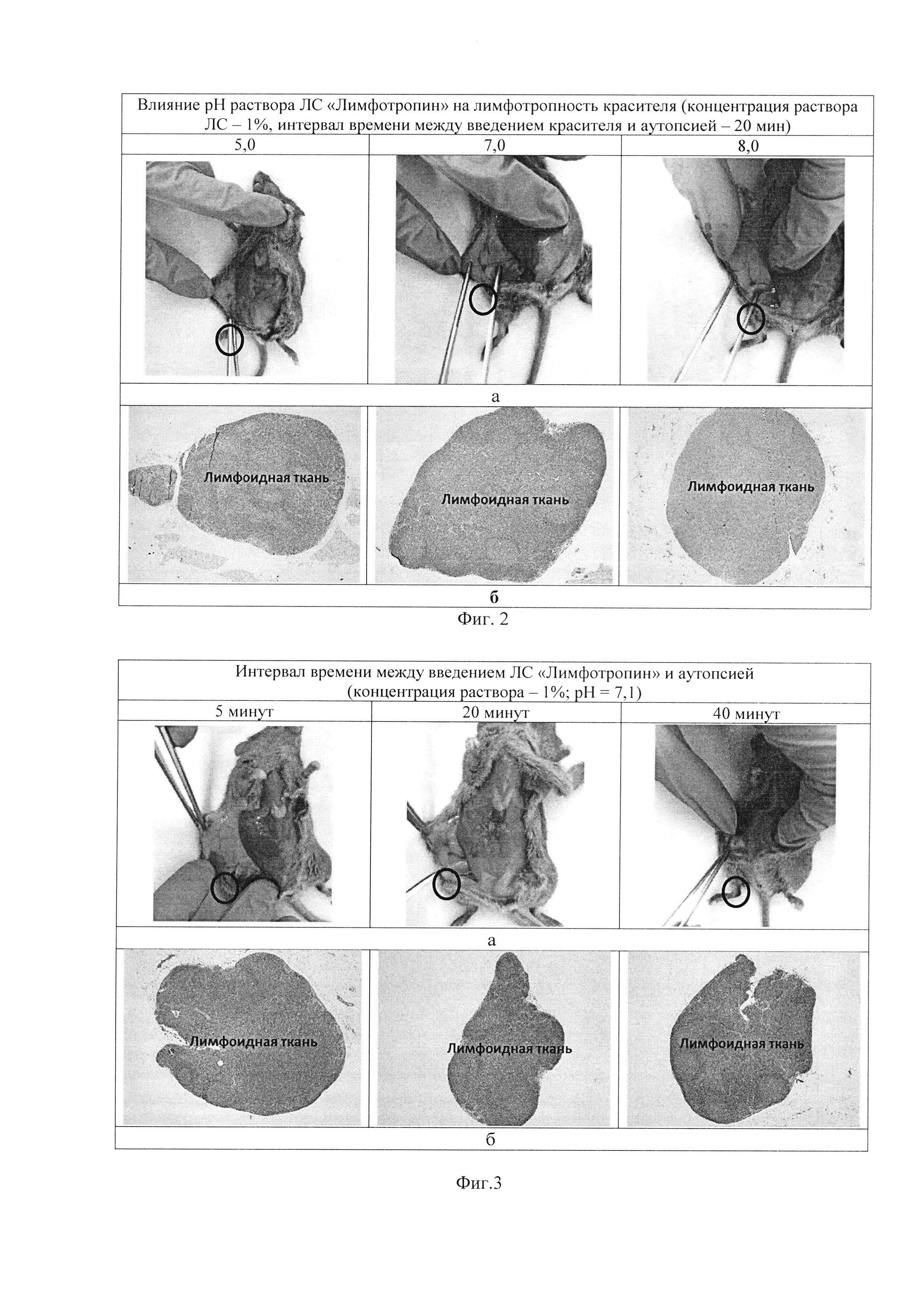
Фиг. 2 - показаны результаты непрямой цветной лимфографии с ЛС «Лимфотропин» у мышей в зависимости от рН раствора ЛС; а) макроскопическая оценка; б) гистологическая верификация лимфатического узла (увеличение: 40×)
Фиг. 3 - показаны результаты непрямой цветной лимфографии с ЛС «Лимфотропин» у мышей в зависимости от интервала времени между введением ЛС и оценкой результата диагностической процедуры; а) макроскопическая оценка; б) гистологическая верификация лимфатического узла (увеличение: 40×).
Фиг. 4 - показаны результаты непрямой цветной лимфографии с ЛС «Лимфотропин» у мышей с саркомой S37, метастазирующей в лимфатические сосуды; а) макроскопическая оценка; б) гистологическая верификация лимфатического узла (увеличение: 100×).
В рамках разработки ЛС для цветной непрямой лимфографии были изучены лимфотропные свойства аналога основного компонента американского препарата «Lymphazurin»(USA) - синего трифенилметанового красителя - динатриевой соли 4-{[(4-диэ-тиламино)фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисульфоната (Дисульфиновый голубой VN 150), который ранее производился в СССР из бензальдегид-2,4-дисульфокислоты, а в настоящее время закупается по импорту. Пилотные исследования лимфотропности Дисульфинового голубого VN 150 в среде фосфатного буфера показали результаты, не уступающие американскому препарату «Lymphazurin». Однако сама субстанция «Дисульфиновый голубой VN 150» не может быть использована в качестве основного компонента медицинского препарата, поскольку состоит из сложной смеси химических соединений. Даже в аналитическом паспорте на импортную субстанцию красителя фирмы «Merck» указывается, что содержание основного компонента субстанции - натриевой соли 4-{[(4-диэтиламино)фенил][4-(ди-этилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисульфоната не превышает 40%.
С помощью метода тонкослойной хроматографии и элементного анализа нами было установлено, что основным красящим лимфотропным соединением в субстанции «Дисульфиновый голубой VN 150» является динатриевая соль 4-{[(4-диэтиламино) фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисульфоната, содержание которой составляет 23-24% от веса исходного красителя. При этом входящие компоненты смеси не позволяют использовать краситель в качестве лимфотропного соединения у больных.
В ходе проведенного исследования была разработана новая высокоэффективная технология синтеза субстанции - динатриевой соли 4-{[(4-диэтиламино) фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил} бензо-1,3-дисульфоната, а также получены характеристики ее физико-химических и биологических параметров.
Предлагаемое лекарственное средство (далее - ЛС) «Лимфотропин» на основе лимфотропного красителя является оригинальным и не имеет аналогов на территории Российской Федерации
Способ осуществляют следующим образом.
В предлагаемом способе в качестве исходного соединения для получения бензальдегид-2,4-дисульфокислоты и последующего синтеза динатриевой соли 4-{[(4-диэтиламино) фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната используют доступную толуол-4-сульфокислоту, которая под действием 20% олеума легко и с высоким выходом образует толуол-2,4-дисульфокислоту. Этот промежуточный продукт без выделения, под действием двуокиси марганца, образует бензальдегид-2,4-дисульфокислоту, которую нейтрализуют и выделяют в виде динатриевой соли бензальдегид-2,4-дисульфокислоты. Общий выход бензальдегид-2,4-дисульфокислоты составляет 70-75%, что существенно выше если использовать непосредственно толуол.
Полученную оригинальным методом динатриевую соль бензальдегид-2,4-дисульфокислоты конденсируют с диэтиланилином до соответствующего триарилкарбинола двумя равнозначными способами.
В первом способе конденсацию бензальдегид-2,4-дисульфокислоты с диэтиланилином проводят в расплаве карбамида с добавлением хлорида цинка.
Во втором способе конденсацию бензальдегид-2,4-дисульфокислоты с диэтиланилином проводят в расплаве смеси пятихлористого фосфора и хлорида аммония.
Обе реакции протекают очень быстро - в течение 1,0-1,5 часов с высоким выходом конечного трифенилкарбинола (75-85%). Полученный триарил-карбинол переводят в соответствующую динатриевую соль 4-{[(4-диэтил-амино)фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисульфоната, используя спиртовой раствор хлористого водорода или водный раствор перекиси водорода. Образовавшуюся динатриевую соль красителя перекристаллизовывают из этанола.
Для доказательства строения динатриевой соли динатриевую соль 4-{[(4-диэтил-амино)фенил][4-(диэтилимино)-циклогекса-2,5-диен-1-илиден]-метил}бензо-1,3-дисуль-фоната использовались следующие физико-химические методы.
Спектры ЯМР образцов динатриевой соли на ядрах 1Н, 13С регистрируют на приборе Bruker Avance II 600 с рабочей частотой 600 МГц при температуре 303К с использованием широкополосного датчика SmartPrope для протонов и ядер 13С.
Масс-спектрометрия высокого разрешения образцов динатриевой соли снималась на приборе Bruker Daltonik с жидкостным хроматографом Agilent 1200.
Элементный анализ образцов производился на приборе Perkin-Elmer 2400.
Осуществление заявленного технического решения демонстрируется следующими примерами.
Пример 1. Получение динатриевой соли бензальдегид-2,4-дисульфокислоты из толуол-4-сульфокислоты.
К 540 г (300 мл) 20% олеума медленно добавляют 86 г (0,5 моля) п-толуол-сульфокислоты. Нагревают 4 часа при 125°С, толуол полностью при этом превращается в дисульфокислоту. Затем к смеси добавляют при постоянном перемешивании небольшими порциями 125 г 80%-ного MnO2. Затем смесь медленно нагревают до 120°С. Смесь оставляют на 12 часов, затем добавляют 2 л воды и Ca(OH)2 до полного исчезновения минеральной кислой реакции. К гипсовой кашице добавляют концентрированный раствор Na2CO3 до тех пор, пока отфильтрованная проба не будет давать осадка при дальнейшем прибавлении раствора Na2CO3. Затем нерастворимые соли отфильтровывают на фильтре, хорошо промывают осадок водой, замешивают его еще раз с водой и фильруют второй раз. Светлый, слабощелочной раствор (рН 7,5-8,0) упаривают в вакууме. Осадок солей растворяют в горячем этаноле (температура 65-70°С), фильтруют и повторно упаривают в вакууме. Выход бензальдегид-2,4-дисульфокислоты динатриевой соли составляет 105 г (79%).
Элементный анализ: Вычислено S,% - 10,84; Na,% - 7,79; C27H32N2Na2S2O6, м.м. 590,66.
Найдено: S,% - 10,91; 10,95; Na,% - 7,71; 7,79.
Пример 2. Получение триарилкарбинола конденсацией в карбамиде.
Образовавшуюся в примере 1 динатриевую соль бензальдегид-2,4-дисульфокислоты смешивают с карбамидом и хлоридом цинка. Смесь нагревают до плавления ингредиентов и при перемешивании добавляют 100 г чистого диэтиланилина. Смесь при перемешивании нагревают до 120-125°С, выдерживают 1-1,5 часа и охлаждают. К реакционной смеси добавляют ацетон, нагревают до кипения (температура 56°С) и отфильтровывают осадок, представляющий из себя триарилкарбинол. Выход готового продукта - триарилкарбинола составляет 152,9 г (80%). Температура плавления 179°С.
Элементный анализ: Вычислено S,% - 10,84; Na,% - 7,79; C27H32N2Na2S2O6, м.м. 590,66
Найдено: S,% - 10,91; 10,95; Na,% - 7,71; 7,79.
Пример 3. Получение триарилкарбинола в смеси пентахлорида фосфора и хлорида аммонии.
Образовавшуюся в примере 1 динатриевую соль бензальдегид-2,4-дисуль-фокислоты добавляют к смеси пентахлорида фосфора и хлорида аммония, перемешивают и добавляют 100 г чистого диэтиланилина. Реакционную смесь нагревают до 110°С, выдерживают 1,0-1,5 часа, охлаждают до 30°С и добавляют ацетон. Образовавшуюся суспензию тщательно перемешивают, фильтруют. Выход готового продукта -динатриевой соли триарилкарбинола составляет 161,6 г (85%).
Элементный анализ: Вычислено S,% - 10,84; Na,% - 7,79; С27Н32N2Nа2S2О6, м.м. 590,66
Найдено: S,% - 10,79; 10,81; Na,% - 7,81; 7,85.
Пример 4. Получение динатриевой соли 4-{[(4-диэтиламино)фенил][4-(диэтил-имино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната.
106 г триарилкарбинола, полученного по методике Примера 2 или по методике Примера 3, медленно добавляют к 200 мл этанола, содержащего 30 г газообразного хлористого водорода, получаемого пропусканием газообразного HCI через этанол. При перемешивании в течение 30 минут реакционная смесь окрашивается в темно-синий цвет. Реакционную массу упаривают в вакууме. Осадок перекристаллизовывают из смеси этанола с изо-пропанолом (в соотношении 1:1).
Выход динатриевой соли 4-{[(4-диэтиламино) фенил][4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната составляет 106 г (100%).
Элементный анализ. Вычислено: S,% - 10,87; Na,% - 7,81; С27Н31N2Nа2О6S2.
Получено: S 11,06±0,07%. Na 7,81±0,17%. Рассчитано: S 10,87%; Na 7,81%.
Анализ спектров ЯМР 1Н, 13С (рис. 2, 3) показал наличие в соединении двух дизамещенных фенильных фрагментов А и В (обозначение фрагментов на рис. 1) (сигналы δН 6.93 (4N), 7.43 (4N), δН 156.8 (2С), 114.6 (4С), 142.0 (4С), 128.5 (2С), тризамещенного фенильного фрагмента С, (сигналы δН 7.18, 7.97, 8.63, δС 140.3, 148.6, 127.3, 148.3, 128.1, 133.1) и четырех этильных групп (сигналы δН 1.29 (12Н), 3.67 (8Н), δС 13.2, 47.0)
ЖХ и МС: [М+] 543 ед.(ТФУ/СН3СN)
ТСХ: Rf=0,67 (ЕАс-ЕtOН)
Пример 5. Получение динатриевой соли 4-{[(4-диэтиламино)фенил][4-(диэтил-имино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната.
106 грамм триарилкарбанола, полученного по методике Примера 2 или по методике Примера 3, растворяют при интенсивном перемешивании в 500 мл 50% этанола. Добавляют при охлаждении до 20°С 30 мл 30% перекиси водорода. Смесь интенсивно окрашивается в темно-синий цвет. Реакционную массу упаривают, осадок перекристаллизовывают из смеси этанол-изопропанол (1:1). Выход динатриевой соли 4-{[(4-диэтиламино) фенил] [4-(диэтилимино)-циклогекса-2,5диен-1-илиден]-метил}бензо-1,3-дисульфоната составляет 106 г (100%).
ЖХ и МС: [М+] 543 ед.(ТФУ/СН3СN)
ТСХ: Rf=0,67 (ЕАс-ЕtOН)
Пример 6. Непрямая цветная лимфография с лекарственным средством «Лимфотропин» у мышей при его использовании в различных концентрациях.
ЛС «Лимфотропин» в виде растворов концентрации 0,5%, 1,0% или 2,0% вводят мышам-гибридам F1, однократно, под кожу бедра задней конечности в объеме 0,1 мл. По истечении 20 минут после введения препарата животных подвергают эвтаназии путем передозировки эфира для наркоза. Далее проводят аутопсию и исследуют область регионарного лимфооттока по отношению к месту введения ЛС. Результаты непрямой лимфографии у мышей с ЛС «Лимфотропин» при использовании красителя в различной концентрации представлены на иллюстрации (Фиг. 1а, б).
После введения мышам под кожу бедра ЛС «Лимфотропин» в концентрациях 0,5%, 1,0% и 2,0% в около паховой области животных на стороне введения наблюдается окрашенное в голубой цвет округлое мягкотканное образование (Фиг. 1а). При гистологическом исследовании окрашенных образований установлена морфологическая картина, характерная для лимфатического узла (Фиг. 1б).
При увеличении концентрации ЛС отмечают усиление интенсивности окраски лимфатического узла. При этом после введения ЛС «Лимфотропин» в концентрации 2,0% у животных наряду с окрашенным паховым лимфатическим узлом наблюдают окрашивание окружающих тканей.
Таким образом, введение ЛС «Лимфотропин» в концентрациях 0,5%, 1,0% и 2,0% под кожу бедра интактным мышам приводит к локальному окрашиванию пахового лимфатического узла в зоне лимфооттока, регионарного по отношению к месту введения ЛС.
Пример 7. Непрямая цветная лимфография с лекарственным средством «Лимфотропин» у мышей при использовании раствора с различными значениями рН.
Растворы ЛС «Лимфотропин» в концентрации 1,0% и рН 5,0, 7,0 или 8,0, вводят мышам-гибридам F1, однократно, под кожу бедра задней конечности в объеме 0,1 мл. По истечении 20 минут после введения препарата животных подвергают эвтаназии путем передозировки эфира для наркоза. Далее проводят аутопсию и исследуют область лимфооттока, регионарного по отношению к месту введения препарата. Результаты непрямой лимфографии у мышей с препаратом «Лимфотропин» при различных рН раствора красителя представлены на иллюстрации (Фиг. 2а, б).
После введения мышам под кожу бедра ЛС «Лимфотропин» в концентрации 1,0% и различных значениях рН раствора (рН=5,0, 7,0 и 8,0), на стороне введения наблюдается окрашивание в голубой цвет пахового лимфатического узла (Фиг. 2а). При использовании всех исследованных растворов препарата интенсивность окраски лимфатического узла одинакова. Результаты гистологической верификации визуализированных красителем лимфатических узлов представлены на Фиг. 2б.
Таким образом, введение под кожу бедра интактным мышам ЛС «Лимфотропин» в концентрации 1,0% независимо от значений рН растворов (рН=5,0, 7,0 и 8,0) приводит к локальному окрашиванию пахового лимфатического узла в зоне лимфооттока, регионарного по отношению к месту введения ЛС.
Пример 8. Непрямая цветная лимфография с ЛС «Лимфотропин» у мышей на различные сроки оценки результата диагностической процедуры.
ЛС «Лимфотропин» в концентрациях 0,5%, 1,0% или 2,0% вводят мышам-гибридам F1, однократно, под кожу бедра задней конечности в объеме 0,1 мл. Через различные интервалы времени после введения - по истечении 5, 20 и 30 минут, животных подвергают эвтаназии путем передозировки эфира для наркоза. Далее проводят аутопсию и исследуют область лимфооттока, регионарного по отношению к месту введения ЛС. Результаты непрямой лимфографии у мышей с ЛС «Лимфотропин» в зависимости от интервала времени между введением красителя и оценкой его накопления в тканях животных, представлены на иллюстрации (Фиг. 3а, б).
На иллюстрации (Фиг. 3а) видно как через 5 мин после введения мышам под кожу бедра ЛС «Лимфотропин» в концентрации 1,0% в околопаховой области животных на стороне введения наблюдается слабо окрашенный с голубым оттенком паховый лимфатический узел. Через 20 и 40 минут после введения лимфотропина окраска лимфатических узлов у мышей становится более выраженной (интенсивный синий цвет). При оценке результата диагностической процедуры отмечено, что через 40 минут после введения красителя у животных на стороне введения имеет место прокрашивание не только лимфатического узла, но и окружающих его тканей. Результаты гистологической верификации визуализированных красителем лимфатических узлов представлены на Фиг. 3б.
Таким образом, после однократного введения под кожу бедра интактным мышам препарата «Лимфотропин" в концентрации 1,0%, прокрашивание регионарного пахового лимфатического узла у животных наблюдают уже через 5 минут после введения препарата.
Пример 9. Непрямая цветная лимфография с ЛС «Лимфотропин» у мышей с саркомой S37, метастазирующей в лимфатические узлы.
Оценку лимфотропных свойств ЛС «Лимфотропин» у животных с метастатическим поражением лимфатических узлов проводят на модели перевиваемой мышиной саркомы S-37. Штамм саркомы S-37 поддерживают в асцитном варианте. Для экспериментов асцитическую жидкость, содержащую опухолевые клетки, прививают мышам-гибридам F1, самкам, под кожу на наружную поверхность бедра, в количестве 1×106 клеток на мышь, в объеме 0,1 мл. Эксперименты выполняют на 5-7 день после инокуляции опухолевых клеток. Размер первичного опухолевого очага на этот срок составляет 50-100 мм3.
ЛС «Лимфотропин» в концентрации 1,0% вводят мышам-опухоленосителям в объеме 0,1 мл однократно под кожу, по периметру опухолевого узла. По истечении 20 минут после введения препарата животных подвергают эвтаназии путем передозировки эфира для наркоза. Далее проводят аутопсию и исследуют регионарный паховый лимфатический узел в области лимфооттока, регионарного по отношению к месту введения ЛС. Результаты непрямой лимфографии с ЛС «Лимфотропин» у мышей с саркомой S37 представлены на иллюстрации (Фиг. 4а, б).
Как видно из иллюстрации (Фиг. 4а), после подкожного перитуморального введения мышам ЛС «Лимфотропин» в концентрации 1,0% наблюдается окрашивание регионарного пахового лимфатического узла в голубой цвет. Результаты гистологической верификации визуализированных красителем лимфатических узлов представлены на Фиг. 4б.
При гистологическом исследовании серийных срезов контрлатеральных паховых лимфатических узлов, а также подмышечных лимфатических узлов животных признаков опухолевого поражения не обнаружено. Наличие микрометастазов у мышей с саркомой, привитой на бедро, только в паховых лимфатических узлах на стороне роста опухоли, свидетельствует в пользу их «сторожевой» анатомической локализации.
Таким образом, ЛС Лимфотропин в концентрации 1,0% при перитуморальном подкожном введении мышам с саркомой S37, привитой на бедро, приводит к локальному окрашиванию сторожевых лимфатических узлов в зоне лимфооттока, регионарного по отношению к опухоли.
Использование предложенной фармацевтической композиции в клинической практике позволяет достигнуть следующих результатов:
- будет введен эффективный метод интраоперационной визуализации лимфотических сосудов без использования дополнительного визуализирующего оборудования;
- у пациента во время удаления первичного опухолевого узла и/или при проведении лимфодиссекции будут контрастированы лимфатические узлы («сторожевые лимфатические узлы») в зоне регионального лимфотока, что позволит с высокой точностью выполнять их прецизионное удаление и тем самым повысить радикальность хирургического лечения.