Результат интеллектуальной деятельности: Флуоресцентный оптический ДНК-сенсор
Вид РИД
Изобретение
Изобретение относится к аналитической химии и касается биосенсорных технологий, в частности, флуоресцентного оптического ДНК-сенсора. Изобретение может быть использовано для изучения различных биомолекул методом люминесценции, для маркирования белков, в качестве клеточного маркера при люминесцентной визуализации клеток и различных их компартментов (митохондрий, клеточных белков и ядер), а также для изучения процессов миграции энергии при моделировании природного фотосинтеза.
Из уровня техники известен Перилен-нановолоконный флуоресцентный сенсор для высокочувствительного и селективного определения аминов (US 8486708 В2), который содержит матрицу из нановолокон перилена. Данный биосенсор заявлен как избирательное и высокочувствительное устройство. Пленка из нановолокон перилена наносится на подложку и после обработки представляется собой пористую структуру, захватывающую молекулы газообразных аминов с их последующей детекцией. При этом, стандартизация нановолокон не описана.
Также известен биосенсор для визуального детектирования (Заявка на выдачу патента на изобретение RU 2015102212), который включает в себя распознающую биомолекулу из перечня, состоящего из антител, пептидов, ферментов, полисахаридов, нуклеиновых кислот (ДНК), аптамеров или пептидно-нуклеиновых кислот; металлические наночастицы из перечня, состоящего из наночастиц золота, наночастиц серебра или наночастиц меди; молекулу-метку и молекулу, специфично связывающуюся с меткой; теплочувствительную бумагу, присоединенную к подложке из перечня, состоящего из стекла, кремния, полистирола, мембран из целлюлозы и ее модификаций. Главными недостатками данного устройства является 1) узкая селективность 2) визуальное определение наличия молекул аналита, что не дает представлений о концентрации анализируемых биомолекул.
Также известен "Флуоресцентный оптический ДНК-биосенсор" (Патент RU 2616879), который содержит биосенсорное устройство с флуоресцентной регистрацией для определения белковых молекул на основе монокристаллического кремния. Недостатком данного устройства является сигнал низкой интенсивности, делающим затруднительным регистрацию биомакромолекул малых концентраций. Заявленный порог детекции белковых молекул составляет 10-15 мг/мл,
Техническим результатом настоящего изобретения является повышение чувствительности флуоресцентного оптического ДНК-биосенсора для детекции биомакромолекул в концентрации менее 10-15 мг/мл.
Технический результат заявленного изобретения достигается за счет того, что оптический ДНК-биосенсор с флуоресцентной регистрацией, содержит подложку и его модификаций сложными оксидами редкоземельных элементов, обладающего возможностью многократного его использования без потери чувствительности, в частности, при определении белковых молекул в малых концентрациях. Технический результат достигается тем, что оптический ДНК-биосенсор флуоресцентной регистрацией состоит из подложки и адсорбированной на подложке тонкой пленки комплекса ДНК-белок - неорганический люминофор, при этом подложка выполнена из оксида цинка размером 18×18 мм, неорганическим люминофором являются сложные оксиды редкоземельных элементов - ванадаты, ренаты, молибдаты, вольфраматы иттрия и гадолиния, содержание ДНК 3 мг/мл, а содержание люминофора в тонкой пленке составляет от 10-8 до 10-14 моль/л.
Изобретение позволяет детектировать белковые молекулы в системе ДНК-белок, сформированной на подложке из оксида цинка, при малых концентрациях белковых молекул, так же существует возможность модификации для увеличения селективности, уменьшении или увеличении чувствительности биосенсорного устройства в зависимости от анализируемых белков или каких-либо других биоорганических молекул и их концентраций.
Сущность способа создания биосенсора заключается в том, что способ состоит из следующих стадий:
а) подготовка подложки
б) приготовление биоспецифичного слоя происходит в несколько этапов:
Навеску ДНК, полученную из тимуса теленка, в количестве 30 мг растворяют в 10 мл 0,1М раствора NaCl, добавляют неорганический люминофор к раствору ДНК в соотношении 1к1, обрабатывают ультразвуком на сонификаторе (частота 42 кГц) в течении 40 минут для полноты растворения и увеличения скорости взаимодействия;
в) нанесение биоспецифичного слоя из приготовленного раствора в количестве 20 мкл методом спинкоатинга (скорость вращения 2000 об/мин)
Пример 1. Определение гемоглобина человека с помощью предложенного сенсора
Использовали материалы: ДНК из тимуса теленка, гемоглобин человека. Навеску ДНК обрабатывали ультразвуком на сонификаторе Branson 1510 (42 кГц) 40 минут в 0,1 моль/л растворе NaCl. Раствор ДНК (0,3 мг/мл) смешивали с раствором белка различных концентраций в 0,1 моль/л NaCl в соотношении 9:1 так, чтобы концентрация белка в растворе для нанесения на подложку составляла от 10-13 до 10-17 моль/л.
Пленку получали методом спинкоатинга на подложках оксида цинка (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
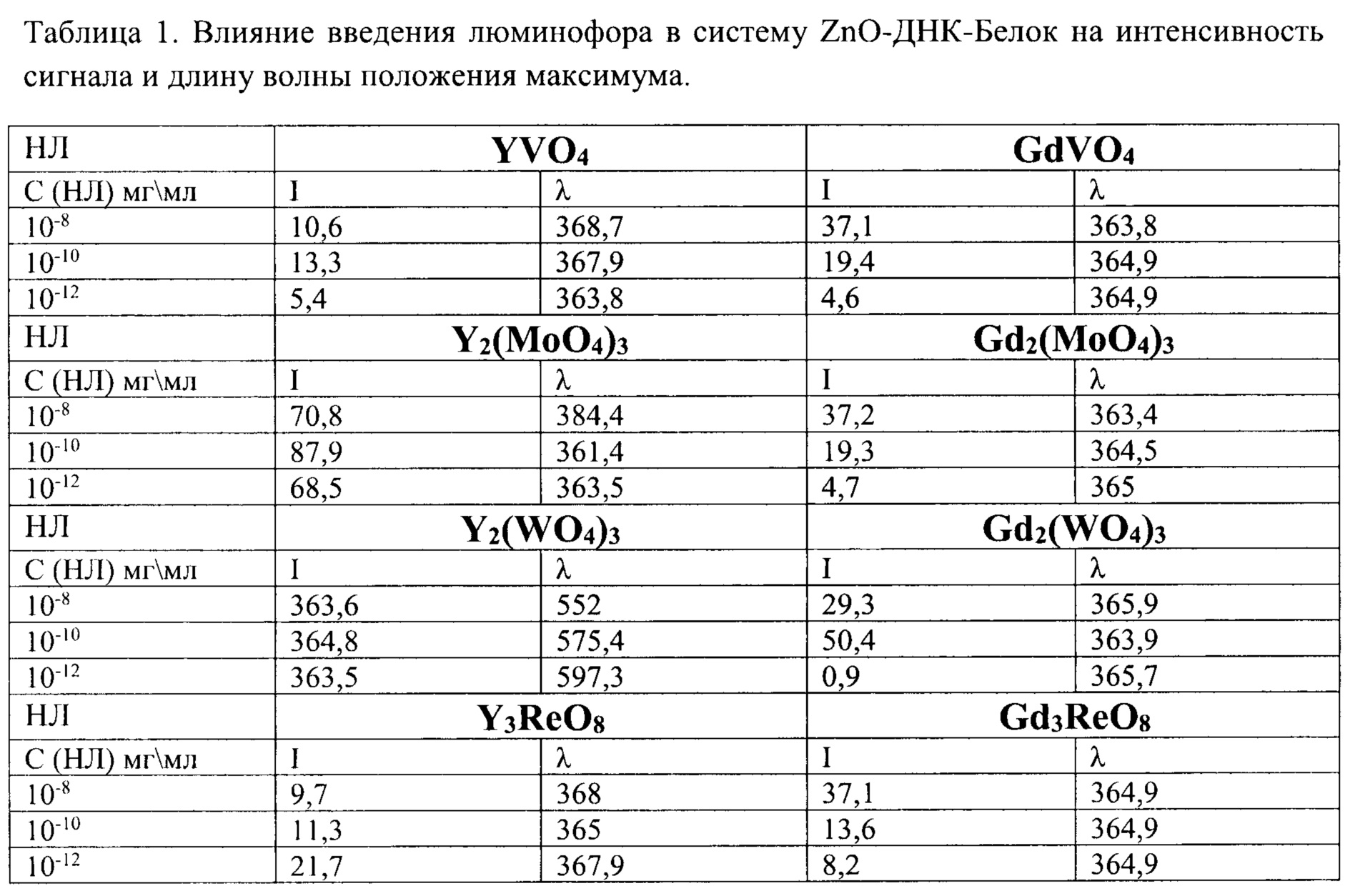
Результаты определения гемоглобина человека с помощью предложенного сенсора представлены на рисунке 1. При определении белка в концентрации 10-17 мг/мл устройством биосенсора величина интенсивности сигнала существенно падает и составляет 9 относительных единиц.
Пример 2. Определение сывороточного альбумина человека с помощью предложенного сенсора
Использовали материалы: ДНК из тимуса теленка, сывороточный альбумин человека. Навеску ДНК обрабатывали ультразвуком на сонификаторе Branson 1510 (42 кГц) 40 минут в 0,1 моль/л растворе NaCl. Раствор ДНК (0,3 мг/мл) смешивали с раствором белка различных концентраций в 0,1 моль/л NaCl в соотношении 9:1 так, чтобы концентрация белка в растворе для нанесения на подложку составляла от 10-13 до 10-17 моль/л.
Пленку получали методом спинкоатинга на подложках оксида цинка (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
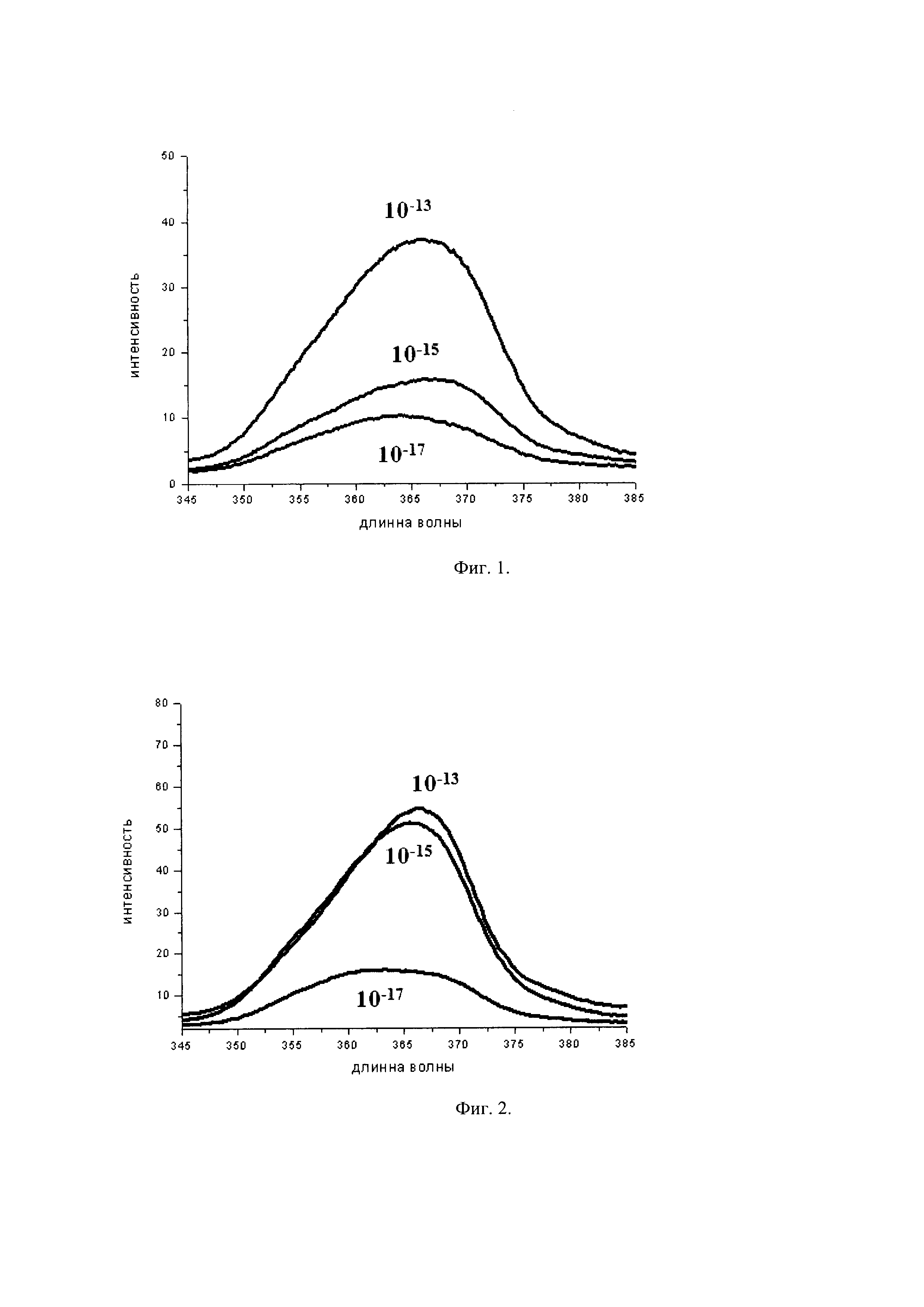
Результаты определения гемоглобина человека с помощью предложенного сенсора представлены на рисунке 2. При определении белка в концентрации 10-17 мг/мл устройством биосенсора величина интенсивности сигнала существенно падает и составляет 16 относительных единиц.
Пример 3. Получение комплекса ДНК-НЛ-Белок
Навеску ДНК обрабатывали ультразвуком на сонификаторе (42 кГц) 40 минут в 0,1 М растворе NaCl. Навеску сложного оксида люминофора (3 мг) добавляли в раствор ДНК-белок (сывороточный альбумин) (3 мг/мл) в 0,1 М NaCl с последующими разбавлениями до различных концентраций так, чтобы концентрация нанокристаллитов люминофора для нанесения на положки составляла от 10-6 до 10-14 М. Избыток люминофора, убирался из раствора путем фильтрации.
Пленки получали методом спинкоатинга на подложках оксида цинка (18×18 мм) на установке на основе центрифуги «Элекон» ЦЛМН-Р 10-02 (Россия) при скорости вращения подложки 2000 об/мин. Объем наносимого раствора - 20 мкл.
Флуоресценцию измеряли на спектрофлуориметре. Регистрацию интенсивности флуоресценции осуществляли с интервалом 0.2 нм при щелях возбуждения 3 и 5 нм соответственно.
В качестве неорганического люминофора используются сложные оксиды иттрия и гадолиния: ванадаты (YVO4, GdVO4), вольфраматы (Y2(WO4)3, Gd2(WO4)3), молибдаты (Y2(MoO4)3, Gd2(MoO4)3) и ренаты (Y3ReO8, Gd3ReO8).
В таблице 1 показана величина сигнала для системы ДНК-Белок-НЛ при различных концентрациях неорганического люминофора и различном составе.