Результат интеллектуальной деятельности: КОМБИНАЦИИ АЦЕТИЛЛЕЙЦИНА ДЛЯ ЛЕЧЕНИЯ ГОЛОВОКРУЖЕНИЯ
Вид РИД
Изобретение
Настоящее изобретение относится к области медицины и фармакологии, а именно, к новым комбинациям ацетиллейцина с, по меньшей мере, одним веществом, выбранным из группы, включающей бетагистин, буспирон, холина альфосцерат и цитиколин, для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии.
Головокружение – часто изнурительное состояние, которое вызывает ощущение потери равновесия и иллюзорных впечатлений от движения тела или окружения больного.
Причины головокружения могут быть отогенными (как в случае синдрома Меньера), т.е. связанными с дисбалансом отовестибулярного аппарата и лабиринта, токсическими (например, вызванными наркотиками или алкоголем), психогенными, неврологическими, гематогенными или связанными с кровообращением, опухолями или зрением (диплопия).
Лечение головокружения, очевидно, зависит от его этиологии, но в настоящее время симптоматическое лечение основано на таких препаратах как дименгидратин, перфеназин и меклозин.
Головокружение наблюдается у 17-30% взрослых лиц общей популяции. Различают вестибулярное (системное, вертиго) и невестибулярное (несистемное) головокружение.
Вестибулярное головокружение
Вестибулярное головокружение в широком смысле может быть обусловлено органическими и функциональными изменениями в центральных и периферических структурах вестибулярного аппарата.
Вестибулярное головокружение – около 24% случаев головокружения (3-10% взрослых лиц общей популяции) – связано с поражением периферического (структуры внутреннего уха) или центрального звена вестибулярного аппарата (ядра и проводящие пути ЦНС).
Распространенность отдельных нозологических форм (в % взрослых лиц общей популяции): доброкачественное позиционное пароксизмальное головокружение, ДППГ – 0,06-0,6% (ряд авторов указывает до 1,6%); болезнь Меньера – 0,12-0,5% ; вестибулярная мигрень – 0,98%; поражения вестибулярных структур ЦНС (моста, среднего мозга, мозжечка) происходят в результате нарушений кровотока вертебробазилярной системы, рассеянного склероза, нейродегенеративных процессов, приема лекарственных препаратов и составляют около 5% случаев вестибулярного головокружения.
Коморбидность вестибулярных и психических (тревога, депрессия) расстройств – около 50%. Вертиго с большей частотой выявляется у лиц женского пола и лиц с мигренью. Наличие вертиго может обуславливать вторичное развитие тревожных расстройств.
При отдельных клинических состояниях, сопровождающихся вестибулярным головокружением, могут применяться/изучаются такие средства как гентамицин (болезнь Меньера); карбамазепин (вестибулярная пароксизмия); ацетазоламид, фампридин (эпизодическая атаксия 2 типа, семейная атаксия).
Медикаментозная терапия имеет симптоматический характер и направлена на купирование головокружения и вестибулярной дисфункции. Основными препаратами выступают вестибулосупрессоры: дименгидринат, метоклопрамид, фенотиазины (фторфеназин, тиэтилперазин, тиоридазин, промазин), транквилизаторы бензодиазепинового ряда (нозепам, диазепам, гидазепам). Из-за рвоты указанные препараты вводят внутримышечно или в виде свечей. Продолжительность их применения диктуется тяжестью головокружения. Обычно она ограничивается 3-мя днями, поскольку данные лекарственные средства тормозят вестибулярную компенсацию.
Невестибулярное головокружение
Невестибулярное (не связано с поражением вестибулярного анализатора) головокружение – около 76% случаев головокружения – представлено главным образом головокружением в связи с нарушением церебрального кровотока и функциональным головокружением (персистирующее постуральное перцептивное головокружение, ранее – хроническое субъективное головокружение, фобическое постуральное головокружение).
Функциональное (психогенное) головокружение – одна из самых частых причин жалоб на головокружение. В общей популяции на долю функционального головокружения приходится около 15-23% [Brandt T., Dieterich M. “Vertigo and dizziness: common complains. 2nd edn. Springer, London: 2013; Obermann M., Bock E., Sabev N. et al. “Long-term outcome of vertigo and dizziness associated disorders following treatment in specialized tertiary care: the Dizziness and Vertigo Registry (DiVeR) Study” // J. Neurol., 2015, 262(9): 2083-2091]. Среди пациентов младше 45 лет функциональное головокружение занимает первое место среди причин жалоб на головокружение: на его долю приходится до 38% случаев головокружения [Замерград М.В. “Возрастные аспекты головокружений” // Неврологический журнал. 2014. Т.19. №3. С.21-28]. В некоторых случаях функциональное головокружение развивается не первично, а вследствие какого-либо органического вестибулярного расстройства. Например, функциональное головокружение – частое осложнение таких распространенных вестибулярных заболеваний как доброкачественное пароксизмальное позиционное головокружение и вестибулярный нейронит.
Функциональное головокружение возникает в результате нарушения взаимодействия между вестибулярной, зрительной и соматосенсорной системами, которые в норме совместно обеспечивают пространственную ориентацию. Головокружение может быть вызвано также физиологической стимуляцией нормально функционирующих сенсорных систем.
Несоответствием между информацией, поступающей от различных сенсорных систем, объясняется укачивание в автомобиле, высотное головокружение и зрительно обусловленное головокружение. Еще один пример функционального головокружения – головокружение, возникающее вследствие слишком активного движения головой в условиях невесомости.
Головокружение, развивающееся в связи с психологическими факторами, определяется также как функциональное головокружение, в противоположность органическому, возникающему на основе структурных изменений органов. Однако функциональным нарушениям нередко предшествуют органические, которые повышают функциональную уязвимость органа в стрессовых ситуациях. Концепция соматоформных расстройств, принятая в современных международных классификациях, предусматривает их диагностику на основе упорных жалоб больных при отсутствии патогенетически обусловленных изменений в органах. По существу, данная концепция лишена сколько-нибудь существенного психопатологического содержания [Вельтищев Д.Ю., Серавина О.Ф. // Психиатрия, 2010, № 4 (55), стр. 48-52].
Функциональное расстройство – это состояние здоровья, которое ухудшает нормальную функцию телесного процесса, но где каждая часть тела выглядит полностью нормальной при исследовании. Это контрастирует со структурным расстройством (в котором можно видеть, что какая-то часть тела функционирует ненормально) или психосоматическим расстройством (в котором симптомы вызваны психологическим или психическим заболеванием). Таким образом, важно отметить, что функциональное головокружение не является психиатрическим заболеванием [Dieterich M., Staab J.P., Brandt T. “Functional (psychogenic) dizziness” // Handbook of Clinical Neurology, Vol. 139, Chapter 37, 2016, pp. 447-468], т.е. не вызвано первичной психиатрической патологией, такой как тревожное расстройство или депрессия, и также не вызвано структурными изменениями ЦНС.
Функциональные вестибулярные расстройства включают, в частности, следующие заболевания, подробно описанные в нейро-отологической литературе: персистирующее постуральное перцептивное головокружение, постуральная фобическая неустойчивость и хроническое субъективное головокружение. Ни у одного из этих расстройств нет патогномонического симптома или проявления, но все они имеют ключевые особенности, которые указывают на их присутствие независимо от того, активны ли другие болезни [Dieterich M., Staab J.P., Brandt T. “Functional (psychogenic) dizziness” // Handbook of Clinical Neurology, Vol. 139, Chapter 37, 2016, pp. 447-468].
Атаксия
Атаксия – это неврологическое проявление, состоящее из отсутствия координации мышечных движений, включая отклонения походки. Атаксия представляет собой неспецифическое клиническое проявление, предполагающее дисфункцию частей нервной системы, которые координируют движение, например, мозжечок. Атаксия может быть ограничена одной стороной тела, которая называется гелиатаксией. Дистаксия является легкой степенью атаксии. Атаксия Фридрейха проявляется в аномалиях походки как наиболее часто встречающийся симптом.
Эффективные варианты лечения дегенеративной атаксии ограничены. Рилузол, амантадин и варениклин имеют лучшие показатели, несмотря на ограничения в их исследованиях.
При этом сообщается о применении ацетил-DL-лейцина для лечения мозжечковой атаксии [Harini Sarva and Vicki Lynn Shanker "Treatment Options in Degenerative Cerebellar Ataxia: A Systematic Review" Movement Disorders Clinical Practice, Volume 1, Issue 4, December 2014, Pages: 291–298] в дозе 5 г в день.
Эпизодическая атаксия (ЭА, семейная периодическая атаксия или наследственная пароксизмальная мозжечковая атаксия) представляет собой редкое наследственное заболевание, наследующееся по аутосомно-доминантному типу. Были выделены, по крайней мере, две группы расстройств: (1) эпизодическая атаксия типа 1 (ЭA-1), которая проявляется без головокружения и связана с миокимией и (2) эпизодическая атаксия 1 типа (ЭA-2), которая часто сопровождается головокружением и связана с нистагмом. ЭA-1 и ЭA-2 были идентифицированы как каналопатии. ЭA-1 обусловлена различными гетерозиготными точечными миссенс-мутациями в гене потенциал-зависимого калиевого канала замедленного выпрямления (KCNA1/Kv1.1) в хромосоме 12p13, тогда как ЭA-2 вызвана мутациями гена альфа 1 субъединицы церебрального кальциевого канала P/Q-типа CACNL1A4, локализованного на хромосоме 19p, который значительно экспрессируется в мозжечке [Brandt T., Strupp M. “Episodic ataxia type 1 and 2 (familial periodic ataxia/vertigo)” // Audiol. Neurootol. 1997, vol. 2(6), pp. 373-83].
Лечение эпизодических атаксий включает вестибулярную реабилитацию (специальные упражнения для адаптации вестибулярного аппарата) и фармакотерапию, направленную на купирование симптомов и достижение вестибулярной компенсации.
В настоящее время основными вариантами лечения эпизодических атаксий являются ацетазоламид и 4-аминопиридин (4-AP).
Было высказано предположение, что механизм действия ацетазоламида заключается в уменьшении рН, который препятствует проникновению ионов через открытые кальциевые каналы. Ацетазоламид может стабилизировать каналы, которые не могут эффективно инактивироваться. Ацетазоламид может не работать во всех случаях, если мутация нарушает область поры кальциевых каналов, изменяя стабилизирующий эффект ионов H+. 4-АР является блокатором калиевых каналов, и его обычно используют, когда ацетазоламид не дает терапевтического эффекта [Yue Q, Jen JC, Nelson SF, Baloh RW. “Progressive ataxia due to a missense mutation in a calcium channel gene” // Am J. Hum. Gen, 1997, vol. 61(5), pp. 1078-87].
Существующие подходы к лечению
Препаратами выбора при вестибулярном головокружении являются вазоактивные (циннаризин, циннаризин и пирацетам, винпоцетин), H1-антигистаминные (дименгидринат) и вестибулотропные (бетагистин) препараты.
Дименгидринат характеризуется седативным эффектом и может оказать негативное влияние на процессы центральной вестибулярной компенсации (с клинических позиций целесообразно применение коротким курсом 3 дня, преимущественно для купирования тошноты и рвоты при острых вестибулопатиях).
Клинические исследования по оценке эффективности медикаментозной терапии при отдельных клинических вариантах периферических и центральных вестибулярных патологических состояний, сопровождающихся головокружением, немногочисленны, что ограничивает возможность представить сравнение по отдельным классам средств/препаратам с позиций доказательной медицины.
Неудовлетворенная потребность обусловлена недостаточным контролем симптомов и достижения долгосрочных целей терапии у пациентов с различными формами периферического и центрального вестибулярного головокружения, так как доступные препараты симптоматической терапии часто замедляют процесс вестибулярной компенсации.
Таким образом, повышение эффективности лекарственных средств, направленных на терапию различных форм головокружения, – одна из острых проблем современной медицины, решение которой крайне необходимо для улучшения общественного здравоохранения.
Ацетиллейцин
Ацетиллейцин (N-ацетил-DL-лейцин, C8H15NO3) представляет собой небольшую молекулу с относительно простой химической структурой. Этот оптически неактивный продукт представляет собой результат N-ацетилирования α-амино-изокапроновой кислоты (C6H13NO2), L-изомер которой лейцин является широко распространенной природной α-аминокислотой.
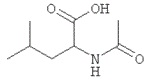
N-ацетил-DL-лейцин
Ацетиллейцин обеспечивает активацию центральных механизмов вестибулярной компенсации при вестибулярном головокружении; не влияет на функционирование нейронов, не вовлеченных в патологический процесс; имеет благоприятный профиль безопасности (в токсикологических экспериментах на животных практически нетоксичен, LD50 для мышей 8 г/кг).
Действие N-ацетил-DL-лейцина на экспериментальной модели головокружения у мышей было обнаружено в 1957 г. С того времени указанное соединение успешно применяли в клинической медицине у людей в качестве симптоматического лекарственного средства при головокружениях.
N-ацетил-DL-лейцин часто назначается врачами, хорошо известен фармацевтам под названием Танганил (Tanganil(R), PierreFabre, раствор для инъекций зарегистрирован в 1957 г, таблетки 1963 г), и его эффективность оценена множеством пациентов, страдающих от головокружения. Фармакологически активной формой является энантиомер N-ацетил-L-лейцин. Однако механизм действия указанного лекарственного средства до сих пор является предметом дискуссий.
Детальное изучение механизма действия препарата на молекулярном и электрофизиологическом уровне проводилось с 1990-х гг. на экспериментальных моделях (крысы, морские свинки, кошки) острого одностороннего разрушения лабиринта (оценка в поведенческих тестах, тестах оценки вестибулярной функции и уровня активности отдельных участков головного мозга по данным позитронно-эмиссионной томографии) и в двойном слепом клиническом исследовании в сравнении с плацебо с участием 60 пациентов, перенесших оперативные вмешательства на структурах лабиринта по поводу болезни Меньера или невриномы слухового нерва. Показано прямое взаимодействие с мембранными фосфолипидами, что может влиять на функцию ионных каналов, а также предполагается возможность модуляции глутаматной системы мозжечка.
В настоящее время препарат изучается в регистрационных клинических исследованиях по показанию мозжечковая атаксия (EudraCT no. 2015–000460–34), предпосылки к которому сформированы по данным 3 наблюдательных клинических исследований.
Ацетиллейцин восстанавливает мембранный потенциал гиперполяризованных и деполяризованных нейронов вестибулярной системы (в частности, на уровне таламуса и мозжечка), не затрагивая при этом нейроны, не вовлеченные в патологический процесс, обеспечивая таким образом процесс вестибулярной компенсации на фоне асимметричной спонтанной активности различных звеньев вестибулярного анализатора при вертиго, поэтому, как полагают авторы настоящего документа, может быть полезен при «каналопатиях», при которых нарушена проводимость кальциевых или калиевых каналов, т.е. при семейной атаксии.
Ацетиллейцин при остром приступе вестибулярного головокружения ускоряет компенсацию преимущественно постуральных симптомов (контроль позы), что ускоряет восстановление способности к нормальному перемещению пациентов и ускоряет дальнейшее восстановление состояния пациентов.
Известно также применение ацетиллейцина для лечения дегенеративной мозжечковой атаксии [Strupp M, Teufel J, Habs M, Feuerecker R, Muth C, van deWarrenburg BP et al Effects of acetyl-DL-leucine in patients with cerebellar ataxia: a case series. J. Neurol. 2013; 260:2556–2561], что может приводить к существенному симптоматическому улучшению в различных формах дегенеративной мозжечковой атаксии (DCA), которые различаются по длительности, тяжести и этиологии симптомов.
С другой стороны, авторы источника [Pelz JO1, Fricke C, Saur D, Classen J. Failure to confirm benefit of acetyl-DL-leucine in degenerative cerebellar ataxia: a case series. J. Neurol. 2015 May; 262(5):1373-5] не смогли подтвердить положительный эффект ацетил-DL-лейцина в сочетании с интенсивной краткосрочной физиотерапией и профессиональной терапией у пациентов с DCA и не рекомендуют ацетил-DL-лейцин для лечения пациентов с мозжечковой атаксией.
Бетагистин
Бетагистин, антагонист Н3 и слабый агонист Н1 гистаминовых рецепторов, усиливает кохлеарный кровоток, влияет на активность вестибулярных нейронов, изменяет продукцию эндолимфы в лабиринте, в связи с чем эффекты препарата можно ожидать преимущественно при головокружении на фоне поражений периферического звена вестибулярного анализатора (ацетиллейцин при вертиго оказывает эффекты на уровне центральных звеньев вестибулярного анализатора).
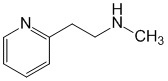
Бетагистин
Так, двойное слепое, перекрестное, плацебо-контролируемое исследование дигидрохлорида бетагистина (12 мг) проводилось у пациентов с головокружением периферического вестибулярного происхождения. Двадцать четыре пациента прошли исследование, которое состояло из двух шестинедельных периодов лечения. Пациенты были диагностированы как страдающие болезнью Меньера (15 пациентов), головокружением из-за других (указанных) причин (пять пациентов) или головокружением неизвестного происхождения (четыре пациента). Пациенты были обследованы в начале исследования и повторно оценивались с интервалом в три недели. Кроме того, пациенты регистрировали характер, частоту и тяжесть своих симптомов в дневнике. Было установлено, что как эпизоды заболевания, так и тяжесть головокружения (преобладающие жалобы) значительно снижаются во время лечения бетагистином (р=0,004). Возникновение тошноты и рвоты также было значительно снижено во время лечения бетагистином (p=0,014 и 0,036 соответственно). Статистически значимых различий в результатах аудиометрических или вестибулометрических тестов между двумя периодами лечения выявлено не было. Общее сравнение двух периодов, проведенное как пациентами, так и исследователем, было в значительной степени благоприятным для бетагистина (p менее 0,001). Все диагностические группы ответили положительно на бетагистин, подтверждая эффективность бетагистина при симптоматическом лечении периферического вестибулярного головокружения [Oosterveld W.J. “Betahistine dihydrochloride in the treatment of vertigo of peripheral vestibular origin. A double-blind placebo-controlled study” // J Laryngol Otol. 1984, vol. 98(1), pp. 37-41].
Буспирон
Буспирон (и его гидрохлорид) является частичным агонистом 5-HT1A рецепторов, который был выведен на рынок более 20 лет назад компанией Bristol-Myers Squibb для перорального лечения тревожных расстройств с сопровождающей депрессией или без нее. В 1990 году буспирон был запущен компанией в сотрудничестве с Menarini для лечения генерализованного тревожного расстройства (GAD). В настоящее время национальный институт рака (NCI) оценивает эффективность препарата в снижении одышки у пациентов, которые проходят химиотерапию для лечения рака. Национальный институт неврологических расстройств и инсульта (NINDS) проводит клинические испытания II фазы в отношении применения буспирона для лечения локализованной эпилепсии. Национальный институт по борьбе со злоупотреблением наркотиками (NIDA) проводит клинические испытания II фазы в отношении применения буспирона для лечения и профилактики кокаиновой зависимости.
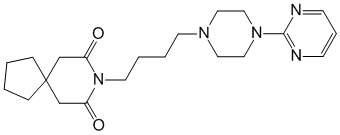
Буспирон
Буспирон – атипичный анксиолитик, высокоэффективный в отношении генерализованного тревожного расстройства [Apter J.T., Allen L.A. “Buspirone: future directions” // J Clin Psychopharmacol. 1999, 19(1):86-93; Flint A.J. “Generalised anxiety disorder in elderly patients: epidemiology, diagnosis and treatment options” // Drugs Aging. 2005; 22(2):101-14; Gale C.K., Millichamp J. “Generalised anxiety disorder in children and adolescents” // BMJ Clin Evid. 2016, 13, 2016. pii: 1002; Goa K.L., Ward A. “Buspirone. A preliminary review of its pharmacological properties and therapeutic efficacy as an anxiolytic” // Drugs. 1986, 32(2):114-29]. Являясь частичным агонистом 5-HT1A рецепторов и антагонистом D2-рецепторов [Loane C., Politis M. “Buspirone: what is it all about?” // Brain Res. 2012, 1461:111-8; Newman-Tancredi A., Gavaudan S., Conte C., et al. “Agonist and antagonist actions of antipsychotic agents at 5-HT1A receptors: a [35S]GTPgammaS binding study” // Eur J Pharmacol. 1998, 355(2-3):245-56; Tunnicliff G. “Molecular basis of buspirone's anxiolytic action” // Pharmacol Toxicol. 1991, 69(3):149-56], буспирон, по-видимому, не замедляет процессы вестибулярной компенсации.
Буспирон (и его гидрохлорид) отличается от типичных бензодиазепиновых анксиолитиков тем, что он не оказывает противосудорожного или миорелаксирующего эффекта. В нем также отсутствует известный седативный эффект, который связан с более типичными анксиолитиками. In vitro буспирон показал высокое сродство к рецепторам серотонина (5-НТ1А). Препарат не имеет существенного сродства к рецепторам бензодиазепина и не влияет на связывание с рецепторами ГАМК in vitro или in vivo при тестировании в доклинических моделях. Он демонстрирует умеренное сродство к дофаминовым рецепторам D2 головного мозга. Некоторые исследования показывают, что буспирон может оказывать косвенное влияние на другие нейромедиаторные системы.
В отличие от бензодиазепинов вероятный анксиолитический механизм действия буспирона остается не до конца выясненным в силу противоречивых анксиолитических эффектов в клинике и на животных моделях [Bauer M.S., Wisniewski S.R., Marangell L.B., et al. “Are antidepressants associated with new-onset suicidality in bipolar disorder? A prospective study of participants in the Systematic Treatment Enhancement Program for Bipolar Disorder (STEP-BD)” // J. Clin Psychiatry. 2006, 67(1):48-55].
Многочисленные работы свидетельствуют о том, что в остром эксперименте применение буспирона на грызунах приводит к анксиолитическому действию в узком и низком диапазоне доз. Это действие значительно варьирует в зависимости от вида животных и используемой модели тревожности. В то же время в широком диапазоне доз при высоких дозах проявляется анксиогенный эффект [Collinson N., Dawson G.R. “On the elevated plus-maze the anxiolytic-like effects of the 5-HT(1A) agonist, 8-OH-DPAT, but not the anxiogenic-like effects of the 5-HT(1A) partial agonist, buspirone, are blocked by the 5-HT1A antagonist, WAY 100635”. Psychopharmacology (Berl). 1997, 132(1):35-43; de Oliveira Citó M.C., da Silva F.C., Silva M.I., et al. “Reversal of cocaine withdrawal-induced anxiety by ondansetron, buspirone and propranolol” // Behav Brain Res. 2012, 231(1):116-23; File S.E., Andrews N. “Low but not high doses of buspirone reduce the anxiogenic effects of diazepam withdrawal” // Psychopharmacology (Berl). 1991, 105(4):578-82; Handley S.L., McBlane J.W. “5HT drugs in animal models of anxiety” // Psychopharmacology (Berl). 1993, 112(1):13-20. Hestermann D., Temel Y., Blokland A., Lim L.W. “Acute serotonergic treatment changes the relation between anxiety and HPA-axis functioning and periaqueductal gray activation” // Behav Brain Res. 2014 Oct 15;273:155-65; Inagaki H, Kiyokawa Y, Takeuchi Y, Mori Y. “The alarm pheromone in male rats as a unique anxiety model: psychopharmacological evidence using anxiolytics” // Pharmacol Biochem Behav. 2010, 94(4):575-9; Moser P.C. “An evaluation of the elevated plus-maze test using the novel anxiolytic buspirone” // Psychopharmacology (Berl). 1989, 99(1):48-53; Paine T.A., Jackman S.L., Olmstead M.C. “Cocaine-induced anxiety: alleviation by diazepam, but not buspirone, dimenhydrinate or diphenhydramine” // Behav Pharmacol. 2002, 13(7):511-23; Shimada T., Matsumoto K., Osanai M., Matsuda H., Terasawa K., Watanabe H. “The modified light/dark transition test in mice: evaluation of classic and putative anxiolytic and anxiogenic drugs” // Gen Pharmacol. 1995, 26(1):205-10; Söderpalm B., Hjorth S., Engel J.A. “Effects of 5-HT1A receptor agonists and L-5-HTP in Montgomery's conflict test” // Pharmacol Biochem Behav. 1989, 32(1):259-65; Varty G.B., Morgan C.A., Cohen-Williams M.E., Coffin V.L., Carey G.J. “The gerbil elevated plus-maze I: behavioral characterization and pharmacological validation” Neuropsychopharmacology. 2002, 27(3):357-70].
Анксиогенный эффект буспирона имеет большую клиническую значимость в связи с тем, что на начальной стадии хронического лечения буспироном может наблюдаться обострение, что требует тщательного контроля за схемой лечения [Chignon J.M., Lepine J.P. “Panic and hypertension associated with single dose of buspirone” Lancet. 1989, 2(8653):46-7; Liegghio N.E., Yeragani V.K., Moore N.C. “Buspirone-induced jitteriness in three patients with panic disorder and one patient with generalized anxiety disorder” // J Clin Psychiatry. 1988, 49(4):165-6; Newton R.E., Marunycz J.D., Alderdice M.T., Napoliello M.J. “Review of the side-effect profile of buspirone” // Am J Med. 1986, 80(3B):17-21].
Сродство буспирона к комплексу рецепторов может лежать в основе его бифазного фармакологического эффекта [Tunnicliff G. “Molecular basis of buspirone's anxiolytic action” // Pharmacol Toxicol. 1991, 69(3):149-56. Review]. Буспирон действует как полный агонист 5-HT1A ауторецепторов, расположенных на поверхности дендритных нейронов ядер шва, снижая возбуждение 5-HT нейронов и снижая таким образом высвобождение серотонина в данной структуре, и активируя тем самым другие мозговые структуры. Данный механизм считается частично отвечающим за анксиолитический эффект буспирона [Carli M., Prontera C., Samanin R. “Evidence that central 5-hydroxytryptaminergic neurones are involved in the anxiolytic activity of buspirone” // Br J Pharmacol. 1989, 96(4):829-36; Adell A., Sarna G.S., Hutson P.H., Curzon G. “An in vivo dialysis and behavioural study of the release of 5-HT by p-chloroamphetamine in reserpine-treated rats” // Br J Pharmacol. 1989, 97(1):206-12; Sharp T., Bramwell S.R., Grahame-Smith D.G. “5-HT1 agonists reduce 5-hydroxytryptamine release in rat hippocampus in vivo as determined by brain microdialysis” // Br J Pharmacol. 1989, 96(2):283-90; Sprouse J.S., Aghajanian G.K. “Electrophysiological responses of serotoninergic dorsal raphe neurons to 5-HT1A and 5-HT1B agonists” // Synapse. 1987, 1(1):3-9].
Однако, буспирон также работает как агонист постсинаптических 5-HT1A рецепторов, снижая тем самым нейрональное возбуждение. Эти противоположные эффекты могут обуславливать бифазный тревожно-модулирующий эффект буспирона [Sillar K.T., Simmers A.J. “Presynaptic inhibition of primary afferent transmitter release by 5-hydroxytryptamine at a mechanosensory synapse in the vertebrate spinal cord” // J Neurosci. 1994, 14(5 Pt 1):2636-47; McNaughton N., Panickar K.S., Logan B. “The pituitary-adrenal axis and the different behavioral effects of buspirone and chlordiazepoxide” // Pharmacol Biochem Behav. 1996, 54(1):51-6; Hodges H., Green S., Glenn B. “Evidence that the amygdala is involved in benzodiazepine and serotonergic effects on punished responding but not on discrimination” // Psychopharmacology (Berl). 1987, 92(4):491-504].
Из уровня техники известно применение буспирона для паллиативного лечения невроза, при котором проявляются симптомы беспокойства (US 4182763, 08.01.1980); при гиперактивности, дефиците внимания (EP 0497314, 01.03.1989); для лечения наркомании и зависимости (US 5185329, 09.02.1993); для лечения тревожных расстройств (WO 2005049041, 02.06.2005; US 7678363, 16.03.2010); психиатрических расстройств (US 7678363, 16.03.2010); депрессии (WO 2007144080, 21.12.2007); неврологических расстройств (WO 2008083204, 10.07.2008).
Известно системное применение буспирона или его производных для лечения патологических состояний, связанных с иммунными ответами (EP0690715, 28.05.2003); для лечения нарушений сексуальной функции и репродукции (US 8052982, 08.11.2011) и сексуальной дисфункции (US 4640921, 03.02.1987); для лечения связанных со сном респираторных заболеваний (WO 2000006163, 10.02.2000). Известно применение буспирона для лечения глаукомы (US 7763619, 27.07.2010), боли, нейропатии (US 6511982, 28.01.2003), зуда (WO 2004084900, 07.10.2004), для лечения, профилактики или облегчения двигательных расстройств, таких как болезнь Паркинсона, дискинезия (US 9186359, 17.11.2015); при травмах спинного мозга, рассеянном склерозе, болезни Паркинсона (WO 2015127558, 03.09.2015); апноэ (EP 0442424, 21.12.1994), а также применение при недержании (WO 1996005817, 29.02.1996), тошноте, рвоте (WO 2008149062, 11.12.2008), приливах (WO 2011064769, 03.06.2011), расстройствах аутистического спектра (US 2012108510, 19.05.2011).
Холина альфосцерат
Холина альфосцерат (Choline alfoscerate) представляет собой производное природного соединения холина, обнаруженного в головном мозге. Является предшественником ацетилхолина (увеличивает уровень ацетилхолина), который может иметь потенциал для лечения болезни Альцгеймера и других деменций. Холина альфосцерат быстро доставляет холин в мозг через гематоэнцефалический барьер и является биосинтетическим предшественником ацетилхолина.
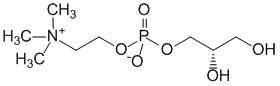
Холина гидроксида (R)-2,3-дигидроксипропилгидрофосфат
Исследования показали эффективность холина альфосцерата для лечения когнитивных расстройств, включая инсульт и болезнь Альцгеймера. В ходе многоцентрового клинического исследования на 2044 пациентах, недавно перенесших инсульт, пациентам давали холина альфосцерат в дозе 1000 мг в день в течение 28 дней и дозе 400 мг три раза в день в течение пяти последующих месяцев. Испытание подтвердило терапевтическую роль холина альфосцерата в когнитивном восстановлении пациентов на основе четырех измерительных шкал, три из которых достигли статистической значимости. Обычно используемые дозы составляют от 300 до 1200 мг в день [Gallelli L. “Choline alphoscerate pharmacology and its role in the treatment of cognitive impairment related to neurological disorders” // Functional Neurology, Vol. XXVI (Suppl.to No.1)].
В некоторых исследованиях сообщалось, что холина альфосцерат, увеличивая выделение ацетилхолина в гиппокампе крысы, способен улучшить память и внимание, а также аффективные и соматические симптомы (усталость, головокружение) у пациентов с сосудистой деменцией. В соответствии с этим экспериментальные исследования подтвердили, что лечение холина альфосцератом предотвращает потерю нервных клеток и глиальную реакцию, главным образом, в подполях CA1 и в зубчатой фасции гиппокампа, тогда как фосфатидилхолин не влиял на гипертензионно-зависимые изменения в микроанатомии гиппокампа [Parnetti L., Mignini F., Tomassoni D., Traini E., Amenta F. “Cholinergic precursors in the treatment of cognitive impairment of vascular origin: ineffective approaches or need for re-evaluation?” // J. Neurol. Sci 2007, 257: 264-269].
Цитиколин
Цитиколин — лекарственное средство, применяемое в качестве ноотропа и психостимулятора. Это промежуточное соединение в образовании фосфатидилхолина из холина. Исследования показывают, что препарат повышает плотность дофаминовых и ацетилхолиновых рецепторов, и предполагается, что он способен предотвращать ухудшение памяти [Teather LA, Wurtman RJ. Dietary CDP-choline supplementation prevents memory impairment caused by impoverished environmental conditions in rats. Learning & Memory, 2005, Vol. 12(1): 39–43]. По предварительным данным, добавки цитиколина помогают улучшить внимание и умственную активность, что может быть полезно при лечении синдрома дефицита внимания и гиперактивности. Также было обнаружено влияние на уровень АКТГ и других гормонов передней доли гипофиза (это может быть полезным для некоторых людей, но не исключены нежелательные последствия при заболеваниях, связанных с гиперсекрецией АКТГ и кортизола). В последнее время цитиколин стал рассматриваться как полезная добавка к пищевому рациону для восстановления и поддержания когнитивной функции у пациентов с впервые перенесенным инсультом, а также для профилактики осложнений у больных с открытоугольной глаукомой [Grieb P., Jünemann F., Rekas M., Rejdak R. Citicoline: A Food Beneficial for Patients Suffering from or Threated with Glaucoma. Frontiers in Aging Neuroscience. 2016, Vol. 8, p. 73].
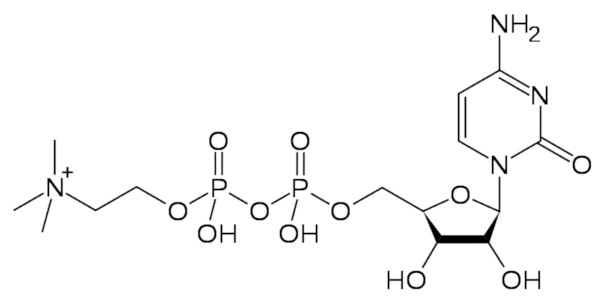
Цитиколин
Известно исследование терапевтической эффективности цитиколина у пациентов с головокружением центрального происхождения и сосудистой этиологии, с недостаточным ответом на стандартное лечение [Petrova D., Maslarov D., Angelov I., and Zekin D. “Analysis of Therapeutic Efficacy of Citicoline in Patients with Vertigo of Central Origin and Vascular Aetiology” // American J. of Neuroprotection and Neuroregeneration, Vol. 4, 1–8, 2012]. В исследование было включено 40 пациентов в среднем возрасте 55,5 ± 4,2 года, разделенных на две группы: пациенты, получавшие Цитиколин в дозировке 2000 мг в день внутривенно, и пациентов, получавших Цитиколин в дозировке 1000 мг в день внутривенно. Полученные результаты дают основание рекомендовать долгосрочное использование цитиколина для комплексного лечения пациентов с головокружением центрального происхождения и сосудистой этиологии.
Из источника [EP2018868, 28.01.2009] известно, что цитиколин является лекарственным средством, которое уже давно используется парентерально для лечения цереброваскулярных расстройств с травматическим или дегенеративным происхож-дением, нарушения сознания, церебрального атеросклероза и осложненных кровотечений, инсультов, тромбоза и болезни Паркинсона. Известны композиции для лечения и профилактики головокружения и шума в ушах, включающие цитиколин и экстракт гинкго билоба.
Цитиколин является важным промежуточным звеном в синтезе фосфолипидов клеточной мембраны, и его образование является лимитирующей стадией синтеза фосфатидилхолина. Он играет несколько важных ролей в физиологии человека, включая усиление структурной целостности клеточных мембран, поддержку синтеза ацетилхолина и синтеза бетаина, метилового донора. Цитиколин обеспечивает мозг источником холина и цитидина, которые эффективно используются в цикле Кеннеди для получения фосфолипидов. Он способен ослаблять образование свободных радикалов в ишемических условиях, а также стимулирует синтез глутатиона и активность глутатионредуктазы. Исследования на животных и людях свидетельствуют о способности цитиколина способствовать улучшению когнитивных нарушений у пациентов с болезнью Альцгеймера и Паркинсона, а также у пациентов с легкой до умеренной стадиями инсульта и церебральной ишемией. Введение цитиколина может также уменьшить продолжительность комы и тяжесть умственного и моторного дефицита, связанного с травмами головы. Фармакокинетические исследования показывают, что цитиколин хорошо всасывается и высоко биодоступен при пероральном введении. Эффективная доза цитиколина на основе данных клинических испытаний составляет от 500 мг до 2000 мг в день. Основываясь на данных нескольких исследований, цитиколин безопасен для использования в детском и взрослом возрасте [Qureshi I., Endres J.R. “Citicoline: A Novel Therapeutic Agent with Neuroprotective, Neuromodulatory, and Neuroregenerative Properties” // Natural Medicine Journal, 2010. Vol. 2 Issue 6].
Ниже приведены определения терминов, которые используются в описании настоящего изобретения.
«Лекарственное средство (препарат)» – вещество (или смесь веществ в виде фармацевтической композиции) в виде таблеток, капсул, инъекций, мазей и др. готовых форм, предназначенное для восстановления, исправления или изменения физиологических функций у человека и животных, а также для лечения и профилактики болезней, диагностики, анестезии, контрацепции, косметологии и прочего.
«Фармацевтическая композиция» обозначает композицию, включающую в себя комбинацию согласно изобретению и, по крайней мере, один из компонентов, выбранных из группы, состоящей из фармацевтически приемлемых и фармакологически совместимых наполнителей, растворителей, разбавителей, носителей, вспомогательных, распределяющих средств, средств доставки, таких как консерванты, стабилизаторы, наполнители, дезинтегрирующие агенты, увлажнители, эмульгаторы, суспендирующие агенты, загустители, подсластители, отдушки, ароматизаторы, антибактериальные агенты, фунгициды, лубриканты, регуляторы пролонгированной доставки, выбор и соотношение которых зависит от их природы, способа введения композиции и дозировки. Примерами суспендирующих агентов являются этоксилированный изостеариловый спирт, полиоксиэтилен, сорбитол и сорбитовый эфир, микрокристаллическая целлюлоза, метагидроксид алюминия, бентонит, агар-агар и трагакант, а также смеси этих веществ. Защита от действия микроорганизмов может быть обеспечена с помощью разнообразных антибактериальных и противогрибковых агентов, например, таких как парабены, хлорбутанол, сорбиновая кислота и подобные им соединения. Композиция может включать также изотонические агенты, например, сахара, хлористый натрий и им подобные. Пролонгированное действие композиции может быть обеспечено с помощью агентов, замедляющих абсорбцию активного начала, например, моностеарат алюминия и желатин. Примерами подходящих носителей, растворителей, разбавителей и средств доставки являются вода, этанол, полиспирты, а также их смеси, растительные масла (такие как оливковое масло) и инъекционные органические сложные эфиры (такие как этилолеат). Примерами наполнителей являются лактоза, молочный сахар, цитрат натрия, карбонат кальция, фосфат кальция и им подобные. Примерами дезинтегрирующих агентов и распределяющих средств являются крахмал, альгиновая кислота и ее соли, силикаты. Примерами лубрикантов являются стеарат магния и кальция, лаурилсульфат натрия, тальк, а также полиэтиленгликоль с высоким молекулярным весом. Фармацевтическая композиция для перорального, сублингвального, трансдермального, внутримышечного, внутривенного, подкожного, местного или ректального введения активного начала, одного или в комбинации с другим активным началом, может быть введена животным и людям в стандартной форме введения, в виде смеси с традиционными фармацевтическими носителями. Пригодные стандартные формы введения включают пероральные формы, такие как таблетки, желатиновые капсулы, пилюли, порошки, гранулы, жевательные резинки и пероральные растворы или суспензии, сублингвальные и трансбуккальные формы введения, аэрозоли, имплантаты, местные, трансдермальные, подкожные, внутримышечные, внутривенные, интраназальные или внутриглазные формы введения и ректальные формы введения.
«Фармацевтически приемлемая соль» означает относительно нетоксичные органические и неорганические соли кислот и оснований, заявленных в настоящем изобретении. Эти соли могут быть получены in situ в процессе синтеза, выделения или очистки соединений или получены специально. В частности, соли оснований могут быть получены специально, исходя из очищенного свободного основания заявленного соединения и подходящей органической или неорганической кислоты. Примерами полученных таким образом солей являются гидрохлориды, гидробромиды, сульфаты, бисульфаты, фосфаты, нитраты, ацетаты, оксалаты, валериаты, олеаты, пальмитаты, стеараты, лаураты, бораты, бензоаты, лактаты, тозилаты, цитраты, фумараты, сукцинаты, тартраты, мезилаты, малонаты, салицилаты, пропионаты, этансульфонаты, бензолсульфонаты, сульфаматы и им подобные, предпочтительно, малеаты (Подробное описание свойств таких солей дано в Berge S.M., et al., “Pharmaceutical Salts” // J. Pharm. Sci. 1977, 66: 1-19). Соли заявленных кислот также могут быть специально получены реакцией очищенной кислоты с подходящим основанием, при этом могут быть синтезированы соли металлов и аминов. К металлическим относятся соли натрия, калия, кальция, бария, цинка, магния, лития и алюминия, наиболее желательными из которых являются соли натрия и калия. Подходящими неорганическими основаниями, из которых могут быть получены соли металлов, являются гидроксид, карбонат, бикарбонат и гидрид натрия, гидроксид и бикарбонат калия, поташ, гидроксид лития, гидроксид кальция, гидроксид магния, гидроксид цинка. В качестве органических оснований, из которых могут быть получены соли заявленных кислот, выбраны амины и аминокислоты, обладающие достаточной основностью, чтобы образовать устойчивую соль, и пригодные для использования в медицинских целях (в частности, они должны обладать низкой токсичностью). К таким аминам относятся аммиак, метиламин, диметиламин, триметиламин, этиламин, диэтиламин, триэтиламин, бензиламин, дибензиламин, дициклогексиламин, пиперазин, этилпиперидин, трис(гидроксиметил)аминометан и подобные им. Кроме того, для солеобразования могут быть использованы гидроокиси тетраалкиламмония, например, такие как холин, тетраметиламмоний, тетраэтиламмоний и им подобные. В качестве аминокислот могут быть использованы основные аминокислоты – лизин, орнитин и аргинин.
Более предпочтительные по настоящему изобретению фармацевтически приемлемые соли цитиколина представляют собой цитиколин натрия, калия; предпочтительная фармацевтически приемлемая соль буспирона представляет собой буспирона гидрохлорид; предпочтительные фармацевтически приемлемые соли бетагистина представляют собой дигидрохлорид, малеат, мезилат, димезилат.
Термин «лечение» обозначает любое лечение заболевания или состояния у субъекта, включающее 1) подавление развития заболевания или состояния, что означает приостановку или подавление развития клинических симптомов, и/или 2) снижение интенсивности симптомов заболевания или состояния, что означает регрессию клинических симптомов.
Термин «терапевтически эффективное количество» означает количество комбинации соединений по настоящему изобретению или любых их производных, которое (1) лечит или предупреждает конкретное заболевание, состояние или расстройство, (2) ослабляет, улучшает или устраняет один или более симптомов конкретного заболевания, состояния или расстройства, или (3) предупреждает или задерживает наступление одного или более симптомов конкретного заболевания, состояния или расстройства, изложенного в данном описании.
Термин «фармацевтически приемлемый» означает, что данное вещество или композиция, в отношении которых применяется этот термин, должны быть совместимы с точки зрения химии и/или токсикологии с другими ингредиентами, входящими в состав препарата, и безопасны для того, кого лечат этим веществом или композицией.
Термины «содержащий», «содержит» означает, что указанные комбинации, композиции и наборы включают перечисленные компоненты, но не исключают включение других компонентов.
Авторы настоящего изобретения обнаружили что применение N-ацетил-DL-лейцина в комбинации с, по меньшей мере, одним веществом, выбранным из группы, состоящей из бетагистина, буспирона, холина альфосцерата и цитиколина, даёт неожиданный синергический эффект в лечении вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной эпизодической атаксии.
Задача настоящего изобретения – создание нового лекарственного средства для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии.
Технические результаты:
- повышение эффективности лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии за счет синергического эффекта для комбинаций ацетиллейцин + бетагистин, ацетиллейцин + буспирон, ацетиллейцин + холина альфосцерат и ацетиллейцин + цитиколин в лечении упомянутых нарушений;
- расширение арсенала средств для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной эпизодической атаксии.
Поставленная задача осуществляется, а технический результат достигается созданием комбинации для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии, содержащая в эффективных количествах (а) ацетиллейцин и (б) по меньшей мере одно вещество, выбранное из группы, включающей бетагистин, буспирон, холина альфосцерат, цитиколин, или их фармацевтически приемлемая соль.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- ацетиллейцин представляет собой N-ацетил-L-лейцин;
- фармацевтически приемлемая соль выбрана из группы, включающей цитиколин натрия, буспирона гидрохлорид и бетагистина дигидрохлорид;
- действующие вещества вводят в предпочтительных суточных дозировках:
ацетиллейцин – 500 – 5000 мг/сут;
бетагистин – 16 – 1440 мг/сут;
буспирон – 5 – 100 мг/сут;
холина альфосцерат – 200 – 3000 мг/сут;
цитиколин – 100 – 2000 мг/сут.
- введение упомянутой комбинации осуществляется инъекционно;
- введение упомянутой комбинации осуществляется перорально.
Поставленная задача решается, а заявленный технический результат также достигается созданием фармацевтической композиции для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии, содержащей в эффективных количествах комбинацию (а) ацетиллейцина и (б) вещества, выбранного из группы, включающей бетагистин, буспирон, холина альфосцерат, цитиколин, или их фармацевтически приемлемых солей, а также по меньшей мере одно вспомогательное вещество и/или по меньшей мере один фармацевтически приемлемый носитель.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- ацетиллейцин представляет собой N-ацетил-L-лейцин;
- действующие вещества находятся в суточных дозировках:
ацетиллейцин – 500-5000 мг/сут;
бетагистин – 16-1440 мг/сут;
буспирон – 5-100 мг/сут;
холина альфосцерат – 200-3000 мг/сут;
цитиколин – 100-2000 мг/сут.
- действующие вещества входят в массовых соотношениях:
ацетиллейцин : бетагистин от 1 : 2,9 до 312,5 : 1;
ацетиллейцин : буспирон от 1 : 0,2 до 1000 : 1;
ацетиллейцин : холина альфосцерат от 1 : 6 до 25 : 1;
ацетиллейцин : цитиколин от 1 : 4 до 50 : 1.
- введение фармацевтической композиции осуществляется инъекционно.
Поставленная задача решается, а заявленный технический результат достигается также созданием набора для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии, который содержит инструкцию по применению и фармацевтическую композицию, содержащую в эффективном количестве ацетиллейцин или его фармацевтически приемлемую соль, вспомогательные вещества и фармацевтически приемлемый носитель, и фармацевтическую композицию, содержащую в эффективном количестве вещество, выбранное из группы, включающей бетагистин, буспирон, холина альфосцерат, цитиколин, или их фармацевтически приемлемые соли, по меньшей мере одно вспомогательное вещество и/или по меньшей мере один фармацевтически приемлемый носитель.
Поставленная задача решается, а заявленный технический результат достигается также применением комбинации или фармацевтической композиции, или набора согласно настоящему изобретению для лечения вестибулярного и невестибулярного головокружения, мозжечковой атаксии, семейной атаксии.
Согласно предпочтительным вариантам реализации указанный технический результат также достигается тем, что:
- действующие вещества вводят в суточных дозировках:
ацетиллейцин – 500-5000 мг/сут,
бетагистин – 16-1440 мг/сут,
буспирон – 5-100 мг/сут,
холина альфосцерат – 200-3000 мг/сут,
цитиколин – 100-2000 мг/сут;
- введение комбинации или фармацевтической композиции, или набора согласно настоящему изобретению осуществляется инъекционно;
- введение комбинации или фармацевтической композиции, или набора согласно настоящему изобретению осуществляется перорально.
Комбинация, композиция или набор по настоящему изобретению могут вводиться перорально или парентерально (например, внутривенно, подкожно, внутрибрюшинно или местно). Клиническая дозировка средства по настоящему изобретению у пациентов может корректироваться в зависимости от терапевтической эффективности и биодоступности активных ингредиентов, скорости их обмена и выведения из организма, а также в зависимости от возраста, пола и стадии заболевания пациента, при этом суточная доза у взрослых обычно составляет 5-5000 мг. Поэтому во время применения комбинации, композиции или набора по настоящему изобретению в виде единиц дозировки необходимо учитывать вышеназванную эффективную дозировку, при этом каждая единица дозировки препарата должна содержать 5-5000 мг действующего вещества. В соответствии с указаниями врача или фармацевта данные препараты могут приниматься несколько раз в течение определенных промежутков времени (предпочтительно – от одного до шести раз).
Далее приводятся примеры осуществления изобретения, которые иллюстрируют, но не охватывают все возможные варианты осуществления изобретения и не ограничивают изобретение.
Пример 1. Оценка эффективности препаратов при вестибулярном головокружении.
Симптомы, аналогичные симптомам вестибулярного головокружения, отмечаются у крыс, утративших вестибулярную функцию в результате односторонней лабиринтэктомии. Утрата вестибулярной функции в таком случае не является полной и необратимой: в норме со временем начинает наблюдаться вестибулярная компенсация.
Крысы: в экспериментах использовались взрослые крысы линии Спрег-Доули, имеющие массу тела 370-400 граммов. Крысы содержались в терморегулируемых боксах (с температурой 21°С) с 12-часовым циклом дня и ночи и достаточным количеством воды и пищи.
Формирование групп исследования: Сто сорок (140) крыс линии Спрег-Доули случайным образом распределяли на двадцать восемь (28) равных по составу групп (N=5), отличающихся типом вводимого препарата и дозировкой. Сформированные группы крыс кратко описаны в таблице 1 ниже.
Вводимые препараты и дозы: Исследование проводилось для 5 препаратов (ацетиллейцин, бетагистин, буспирон, холина альфосцерат, цитиколин), каждый из которых вводился в 3 разных дозах, и для 4 комбинаций (ацетиллейцин+бетагистин, ацетиллейцин+буспирон, ацетиллейцин+холина альфосцерат, ацетиллейцин+цитиколин), каждая из которых также вводилась в трех дозах. Контролем служила группа крыс, получающих только носитель (группа плацебо). Информация по дозировкам приведена в таблице 1 ниже. Все препараты вводились внутривенно (в хвостовую вену) за 30 минут до операции и далее один раз день в течение всего времени исследования. Все дозы приведены в пересчете на человека.
Таблица 1. Группы исследования, сформированные по типам вводимых препаратов и дозировок.
|
Хирургическая операция. Одностороннюю лабиринтэктомию проводили, как описано ранее [Park B.R. Suh J.S., Kim M.S., et al. “Effect of sensory deprivation or electrical stimulation on acute vestibular symptoms following unilateral labyrinthectomy in rabbit” // Acta Otolaryngol. Suppl., 1995, 519:162Y7]. Кратко, крыс анестезировали изофлураном (Sigma), после чего удаляли слуховые косточки в полости среднего уха, чтобы открыть доступ к овальному окну. Вокруг овального окна с помощью хирургического микроскопа было сделано небольшое отверстие. Через это отверстие хирургическим путем удаляли перепончатый лабиринт, используя небольшой прямоугольный крючок. Об успешности операции свидетельствовало появление спонтанных нистагмов, нарушение двигательной способности и координации после восстановления от анестезии.
Оценка двигательной активности проводилась в открытом поле по методу, описанному [Drago F., Nardo L., Rampello L., Raffaele R. “Vestibular compensation in aged rats with unilateral labyrinthectomy treated with dopaminergic drugs” // Pharmacol. Res., 1996, 33(2): 135-40], с небольшими изменениями. Крыс помещали внутрь круглой освещенной платформы (диаметром 20 см, высотой 35 см), дно которой было разделено на 27 зон одинакового размера. За поведением каждого животного наблюдали в течение 3 минут и фиксировали количество зон, в которых животные находились хотя бы передними конечностями (горизонтальная двигательная активность), а также число эпизодов, когда животные вставали на задние лапы (вертикальная двигательная активность с удержанием передних лап на весу).
Оценка координации. Способность координировать и выполнять действия оценивали с помощью теста с вращающимся стержнем. Крыс помещали на цилиндрический стержень (диаметром 7 см), скорость вращения которого увеличивали за время исследования с 4 до 40 оборотов в минуту. Далее в течение 300 секунд для каждого животного регистрировали время до первого падения. В таком формате тест повторяли трижды с интервалом 30 минут. По результатам всех тестов для каждого животного получали единственную оценку – среднее число секунд до падения.
Оценку двигательной активности и координации проводили на 5, 7 и 9 сутки после операции.
Формирование общей оценки для группы. По результатам теста для каждой группы формировалась единая оценка, представляющая собой среднее арифметическое индивидуальных оценок для пяти животных в группе. Таким образом, каждая группа получала набор из 6 оценок: оценка двигательной активности 5, 7 и 9 сутки после операции и оценка координации 5, 7 и 9 сутки после операции. Все данные приведены в таблицах 2-5.
Таблица 2. Влияние ацетиллейцина и бетагистина, применяемых по-отдельности или в комбинации, на двигательную способность и координацию у крыс после одностороннего хирургического разрушения лабиринта.
|
* – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + бетагистин (уровень значимости р<0,05).
Таблица 3. Влияние ацетиллейцина и буспирона, применяемых по-отдельности или в комбинации, на двигательную способность и координацию у крыс после одностороннего хирургического разрушения лабиринта.
|
# – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + буспирон (уровень значимости р<0,05).
Таблица 4. Влияние ацетиллейцина и холина альфосцерата, применяемых по-отдельности или в комбинации, на двигательную способность и координацию у крыс после одностороннего хирургического разрушения лабиринта
|
$ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + холина альфосцерат (уровень значимости р<0,05).
Таблица 5. Влияние ацетиллейцина и цитиколина, применяемых по-отдельности или в комбинации, на двигательную способность и координацию у крыс после одностороннего хирургического разрушения лабиринта
|
^ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + цитиколин (уровень значимости р<0,05)
Статистический анализ. Статистические различия между группами оценивали с помощью парного t-критерия Стьюдента (при уровне значимости p < 0,05).
Результаты.
В целом, функциональное состояние животных, фиксируемое в первую неделю после операции, было лучше в группах, получающих какой-либо препарат, по сравнению с группой плацебо, которой вводили только носитель. Группы, получающие комбинацию препаратов, на 5 и 7 сутки демонстрировали самые высокие показатели восстановления, достоверно отличающиеся от групп моновведения и плацебо. Более того, наблюдаемый эффект был супераддитивным на каждом уровне концентраций.
Выводы: таким образом, был показан синергический эффект для комбинаций ацетиллейцин + бетагистин, ацетиллейцин + буспирон, ацетиллейцин + холина альфосцерат и ацетиллейцин + цитиколин при введении в указанных дозах.
Пример 2. Оценка эффективности препаратов в снижении невестибулярного головокружения.
Невестибулярное головокружение может быть смоделировано для грызунов в условиях вращения в течение заданного периода времени.
Крысы. в исследовании участвовали взрослые крысы линии Спрег-Доули, имеющие массу тела 370-400 граммов. Крысы содержались в терморегулируемых боксах (с температурой 21°С) с 12-часовым циклом дня и ночи и достаточным количеством воды и пищи.
Формирование групп исследования. Сто сорок (140) крыс линии Спрег-Доули случайным образом распределяли на двадцать восемь (28) равных по составу групп (N=5), отличающихся типом вводимого препарата и дозировкой. Сформированные группы крыс кратко описаны в таблице 1 выше.
Вводимые препараты и дозы. Исследование проводилось для 5 препаратов (ацетиллейцин, бетагистин, буспирон, холина альфосцерат, цитиколин), каждый из которых вводился в 3 разных дозах, и для 4 комбинаций (ацетиллейцин+бетагистин, ацетиллейцин+буспирон, ацетиллейцин+холина альфосцерат, ацетиллейцин+цитиколин), каждая из которых также вводилась в трех дозах. Контролем служила группа крыс, получающих только носитель (группа плацебо). Информация по дозировкам приведена в таблице 1 выше. Все препараты вводились внутривенно (в хвостовую вену) ежедневно в течение недели до начала тестирования. Все дозы приведены в пересчете на человека.
Оборудование. Тест основан на удержании равновесия крысами на приподнятой над землей узкой планке (ширина 3 см, длина 1 м). Предварительно в течение 2 минут крыс вращали со скоростью 50 оборотов в минуту в закрытом отсеке, после чего перемещали на узкую планку, ярко освещенную на старте, и наблюдали за движением животных в течение 120 секунд. В таком формате эксперимент повторяли трижды с интервалом 30 минут.
Оценка контроля равновесия животными проводится путем подсчета числа падений с планки и промахов при движении по ней для каждого животного. Далее для группы формируется общая оценка, представляющая собой среднее арифметическое всех индивидуальных оценок.
Статистический анализ. Статистические различия между группами оценивали с помощью парного t-критерия Стьюдента (при уровне значимости p < 0,05).
Результаты
Полученные данные приведены в таблицах 6-9. Комбинация ацетиллейцина с любым заявленным препаратом заметно снижала функциональное головокружение у крыс по сравнению с плацебо и соответствующими группами моновведения. Более того, для тестируемых комбинаций при введении в указанных дозах наблюдался синергический эффект их действия.
Таблица 6. Влияние ацетиллейцина и бетагистина, применяемых по-отдельности или в комбинации, на способность удерживать баланс при моделировании условий возникновения невестибулярного головокружения
|
* – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + бетагистин (уровень значимости р<0,05).
Таблица 7. Влияние ацетиллейцина и буспирона, применяемых по-отдельности или в комбинации, на способность удерживать баланс при моделировании условий возникновения невестибулярного головокружения.
|
# – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + буспирон (уровень значимости р<0,05)
Таблица 8. Влияние ацетиллейцина и холина альфосцерата, применяемых по-отдельности или в комбинации, на способность удерживать баланс при моделировании условий возникновения невестибулярного головокружения
|
$ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + холина альфосцерат (уровень значимости р<0,05)
Таблица 9. Влияние ацетиллейцина и цитиколина, применяемых по-отдельности или в комбинации, на способность удерживать баланс при моделировании условий возникновения невестибулярного головокружения
|
^ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + цитиколин (уровень значимости р<0,05)
Пример 3. Модель атаксии на мышах.
Эффект от введения препаратов исследовали с помощью двух моделей мозжечковой атаксии у мышей. В качестве таких моделей были выбраны мутантные мыши psd, у которых наблюдалась обширная (вплоть до полной) дегенерация клеток Пуркинье коры мозжечка, и мыши weaver с мутацией в калиевом канале внутреннего выпрямления GIRK2.
Мыши. Использовали сто сорок (140) самцов мышей psd и сто сорок (140) самцов weaver мышей, начиная с 14 недели их жизни. На протяжении всего исследования мыши содержались по 5 в клетке при 12-часовом цикле дня и ночи и имели доступ к достаточному количеству воды и пищи.
Формирование групп исследования. Сто сорок (140) самцов мышей psd взвешивали до начала исследования и далее случайным образом распределяли на двадцать восемь (28) равных по составу групп (N=5), отличающихся типом вводимого препарата и дозировкой. Сформированные группы для мышей psd кратко описаны в таблице 10 ниже.
Аналогичная стратификация была проведена для ста сорока (140) мышей weaver. Сформированные группы для мышей weaver кратко описаны в таблице 10 ниже.
Вводимые препараты и дозы. Исследование проводилось для 5 препаратов (ацетиллейцин, бетагистин, буспирон, холина альфосцерат, цитиколин), каждый из которых вводился в 3 разных дозах, и для 4 комбинаций (ацетиллейцин+бетагистин, ацетиллейцин+буспирон, ацетиллейцин+холина альфосцерат, ацетиллейцин+цитиколин), каждая из которых также вводилась в трех дозах. Контролем служила группа мышей, получающих только носитель (группа плацебо). Информация по дозировкам приведена в таблице 10 ниже. Препараты в указанных дозах вводились внутривенно (в хвостовую вену) один раз в три дня на протяжении всего времени исследования и в том же формате за неделю до начала исследования. Все дозы приведены в пересчете на человека.
Таблица 10. Группы исследования для мышей psd и мышей weaver (независимо).
|
Поведенческий тест. Через неделю после каждого введения препарата для каждой мыши во всех группах по шкале от 0 до 3 оценивали четыре показателя: координация, сведение задних конечностей, походка и сгорбленность. Для каждой отдельной мыши эти баллы суммировались, и полученное значение представляло собой индивидуальную оценку функционального состояния животного. Далее рассчитывали среднее арифметическое индивидуальных оценок в каждой группе, которое отражало отклик группы на исследуемый препарат в данный момент времени, и использовалось для статистического сравнения разных групп мышей. Функциональное состояние оценивали на протяжении 25 недель с периодичностью раз в 5 недель. Таким образом, для каждой группы получали набор точек на кривой зависимости функционального состояния группы (выражается средним арифметическим индивидуальных оценок всех животных в группе) от времени. Данные приведены в таблицах 12-15 ниже.
Ниже более подробно описан протокол поведенческого теста с критериями присвоения баллов.
Оценка координации. Вынуть мышь из клетки за хвост и посадить на борт клетки. Слегка подтолкнуть сзади, чтобы она начала перемещаться по борту клетки. В норме мышь какое-то время будет легко перемещаться по краю клетки, а затем без особых трудностей с помощью передних лап спустится обратно в клетку. Таким образом, следует обращать внимание на характер движения мыши и особенности ее перемещения вниз внутрь клетки. Баллы выставляются в соответствии с критериями, приведенными в таблице 11.
Тест на сведение задних конечностей: взять мышь за основание хвоста и поднять над окружающими предметами. В течение 10 секунд следить за положением задних лап. Согласно критериям, изложенным в таблице 11 присвоить животному соответствующий балл.
Оценка походки. Вынуть мышь из клетки и поместить на плоскую поверхность головой в сторону от экспериментатора. Наблюдать за мышью сзади во время ее движения. Оценить характер движений мыши в баллах, согласно критериям, приведенным в таблице 11.
Оценка сгорбленности. Вынуть мышь из клетки, положить на стол и наблюдать за ее движениями. Отмечать наличие или отсутствие при этом характерного горба на спине. В таблице 11 приведены критерии присвоения баллов.
Таблица 11. Критерии присвоения баллов по отдельным показателям приведены в таблице ниже:
|
Статистический анализ. Статистические различия между группами оценивали с помощью парного t-критерия Стьюдента (при уровне значимости p < 0,05).
Результаты
Таблица 12. Влияние ацетиллейцина и бетагистина, применяемых по-отдельности или в комбинации, на состояние мышей с патологией мозжечка
|
* – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + бетагистин (уровень значимости р<0,05).
Таблица 13. Влияние ацетиллейцина и буспирона, применяемых по-отдельности или в комбинации, на состояние мышей с патологией мозжечка
|
# – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + буспирон (уровень значимости р<0,05)
Таблица 14. Влияние ацетиллейцина и цитиколина, применяемых по-отдельности или в комбинации, на состояние мышей с патологией мозжечка
|
$ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + холина альфосцерат (уровень значимости р<0,05)
Таблица 15. Влияние ацетиллейцина и цитиколина, применяемых по-отдельности или в комбинации, на состояние мышей с патологией мозжечка
|
^ – достоверное отличие от ожидаемого (расчётного) аддитивного эффекта комбинации Ацетиллейцин + цитиколин (уровень значимости р<0,05)
В целом, функциональное состояние животных в группах, получающих какой-либо препарат, было лучше (p=0,05) чем в группе плацебо, которой вводили только носитель. В группах, которых лечили комбинацией препаратов, прогрессирование заболевания было выражено слабее всего.
Выводы. На 2 моделях на мышах, являющихся аналогами мозжечковой атаксии у человека, был показан синергический эффект для комбинаций препаратов в любой из введенных доз.
Изобретение может быть использовано в медицине, фармакологии.

