Результат интеллектуальной деятельности: СТАБИЛИЗИРОВАННАЯ АМОРФНАЯ ФОРМА АГОМЕЛАТИНА, СПОСОБ ЕЕ ИЗГОТОВЛЕНИЯ И ФАРМАЦЕВТИЧЕСКИЕ КОМПОЗИЦИИ, ЕЕ СОДЕРЖАЩИЕ
Вид РИД
Изобретение
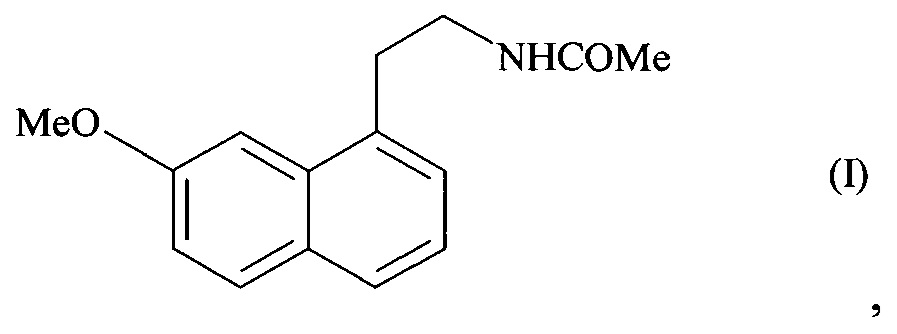
Настоящее изобретение относится к стабилизированной аморфной форме агомелатина, или N-[2-(7-метокси-1-нафтил)этил]ацетамида формулы (I):
 ,
,
к способу ее изготовления, а также к фармацевтическим композициям, ее содержащим.
Агомелатин, или N-[2-(7-метокси-1-нафтил)этил]ацетамид, имеет ценные фармакологические свойства.
В сущности, он имеет двоякую характеристику, являясь, с одной стороны, агонистом рецепторов мелатонинергической системы и, с другой стороны, антагонистом рецептора 5-HT2C. Указанные свойства обеспечивают его активность в центральной нервной системе и, в частности, при лечении большой депрессии, сезонного аффективного расстройства, расстройств сна, патологий сердечно-сосудистой системы, патологий пищеварительной системы, бессонницы и утомления вследствие смены часовых поясов, расстройств аппетита и ожирения.
Агомелатин, его кристаллические формы, его комплексы, его сокристаллы, его соли присоединения с фармацевтически приемлемой кислотой или основанием, его изготовление и его применение в терапии было описано в заявках на получение патента EP 0447285, WO 2005/077887, WO 2007/015003, WO 2007/015002, WO 2007/015004, WO 2010/097052, WO 2010/102554, CN 101955440, WO 2011/050742, CN 102050756, WO 2011/006387, WO 2011/075943, CN 101774937, WO 2011/006387, CN 101870662 и CN 102030673.
Тем не менее, агомелатин представляет собой действующее вещество, недостатком которого является то, что оно имеет очень низкую биологическую доступность и, как следствие, большую вариабельность между пациентами. Указанная низкая биологическая доступность, в частности, связана с растворимостью агомелатина в воде, которая является меньше чем 0,15 мг/мл при температуре 25°C.
Виду фармацевтической ценности указанного соединения и его низкой биологической доступности, аморфная форма представляется возможной стратегией, поскольку является известным, что аморфные формы твердых соединений имеют лучшие характеристики растворения, чем их соответствующие кристаллические формы.
Заявитель в ходе данной работы выявил, что агомелатин имеет аморфное состояние, температура стеклования которого представляет собой -6°C, как было установлено посредством метода сканирующей калориметрии, или ДСК ("Дифференциальная сканирующая калориметрия"). Выше указанной температуры, действующее вещество испытывает переход к кристаллической форме. Сохранение агомелатина в аморфном состоянии при температуре окружающей среды по этой причине является не возможным.
Соответственно, техническая задача состояла в том, чтобы сделать доступной аморфную форму агомелатина в лекарственной форме, которая была бы подходящей для применения в фармацевтической отрасли, в частности с точки зрения стабильности и хранения в обычных условиях.
Решение, известное специалисту в данной области техники, состоит в образовании дисперсии действующего вещества в твердой матрице, которая окружает молекулы и предохраняет их от образования кристаллической решетки. Чем больше разбавлено действующее вещество в пределах матрицы, тем больше аморфное образование. Как следствие, размер таблеток, содержащих аморфное действующее вещество, значительно увеличивается благодаря матрице, что является основным недостатком для пациента, который должен их глотать. Соответственно, другая задача заключается в уменьшении величины применяемой матрицы в пользу действующего вещества, но, предотвращая его при этом от образования кристаллической решетки.
Проводили исследования, пытаясь получить комплексы, применяя агомелатин в циклодекстринах или трегалозе, которые обычно применяют для образования комплексов типа "матрица-примесь", при этом комплекс никогда не возможно было получить таким образом, чтобы он был стабильным с течением времени.
В ходе данной работы заявитель выявил, что является возможным получить стабильную лекарственную форму агомелатина в аморфном виде, воспроизводимым и промышленно осуществимым образом. Указанная новая стабилизированная форма позволяет предусматривать ее применение в фармацевтической отрасли. Более того, указанное позволяет высокие концентрации действующего вещества, что приводит к конечному размеру лекарственной формы, которая является полностью подходящей с точки зрения ее приема пациентом.
Таким образом, настоящее изобретение относится к стабилизированной аморфной форме агомелатина. Под "стабилизированной" понимается то, что аморфная форма агомелатина сохраняется, когда она подвергается условиям температуры и влажности при хранении, изменяющим естественные свойства на протяжении по меньшей мере одной недели. Условия температуры и влажности, изменяющие естественные свойства в соответствии с изобретением, представляют в среднем, например 40°C/75% OB (относительной влажности), 30°C/65% OB, 50°C, 70°C.
В частности, настоящее изобретение состоит из твердой дисперсии агомелатина в органическом полимере, при этом понимается, что агомелатин представляет по меньшей мере 30% от массы дисперсии. Является возможным, в зависимости от выбранного органического полимера, повышать указанное процентное содержание агомелатина по массе. Твердые дисперсии, в которых процентное содержание агомелатина по массе составляет от 30 до 50%, и более предпочтительно от 30 до 40%, являются предпочтительными. Неожиданно, даже при указанном высоком содержании действующего вещества, сохраняется аморфная форма агомелатина - таким образом, он является стабильным в течение длительного времени. Более того, кроме улучшения степени растворения, которое обычно можно было бы ожидать в случае перехода действующего вещества в аморфное состояние, растворимость полученного агомелатина также значительно повышается далеко за пределы растворимости, установленной для кристаллического агомелатина, по меньшей мере в три раза, и в некоторых случаях, в 8 раз. Указанный результат является полностью неожиданным, поскольку, хотя многочисленные публикации в данной области описывают улучшение биофармацевтической активности действующих веществ (растворимости, степени растворения) посредством разработки стабильных твердых дисперсий, указанное относится к содержанию действующего вещества, которое составляет меньше чем 20% (Lin et al., International Journal of Pharmaceutics, 1996, 127, 261-272).
Неожиданно, повышение растворимости действующего вещества поддерживается на протяжении по меньшей мере 4 часов.
Полимер, который применяют в настоящем изобретении, относится в частности к соединениям метакриловой кислоты или к виниловым полимерам или к полимерам на основе целлюлозы.
В частности, полимеры, которые применяют в соответствии с изобретением, относятся к полиметакрилатам или к сополимерам метакриловой кислоты, которые соответствуют полностью полимеризованному сополимеру метакриловой кислоты и сложного акрилового или метакрилового эфира. Указанные полиметакрилаты обычно упоминаются как Eudragit® и могут быть представлены в виде порошка или гранул. Среди различных продуктов Eudragit® на рынке, предпочтительно, в контексте изобретения применяют продукты Eudragit® L., в частности Eudragit® L100 и L100-55, или Eudragit® EPO. Указанные полимеры пригодны в частности для всех уровней содержания агомелатина (% от массы агомелатина).
Виниловые полимеры в соответствии с изобретением относятся в частности к сложным поливиниловым эфирам, таким как, например, поливинилацетатфталат; гомо- или сополимеры на основе поливинилпирролидона, такие как повидоны (Povidone® К30, Plasdone® S630), Kollidon VA64 или также Soluplus®. Повидоны применяют для содержания агомелатина, составляющего меньше 50% от массы.
Среди соединений на основе целлюлозы, которые применяют в соответствии с изобретением, могут быть упомянуты простые эфиры целлюлозы или сложные эфиры, такие как ГПМЦ, и в частности ацетилсукцинат ГПМЦ.
Настоящее изобретение относится также к способу получения стабильной лекарственной формы, которая имеет высокое содержание аморфной формы агомелатина в полимере. Соответственно способу в соответствии с изобретением, соединение формулы (I), полученное любым способом, и присутствующее в любой кристаллической форме, в виде комплексов, сокристаллов, или солей присоединения с фармацевтически приемлемой кислотой или основанием, смешивают с выбранным полимером в одном или большем количестве растворителей, что позволяет получить полное растворение компонентов, и затем растворитель полностью выпаривают при пониженном давлении.
Растворители, которые применяют в соответствии с изобретением, представляют собой растворители, которые способны растворить агомелатин и выбранный полимер; предпочтение отдают полярным протонным или апротонным растворителям, таким как ацетон, спирты, в частности метанол и этанол, а также воде, дихлорметану, этилацетату или смесям указанных растворителей. Растворение проводят с перемешиванием при температуре окружающей среды или посредством нагревания смеси до полного растворения компонентов. Выпаривание растворителей проводят при пониженном давлении при температуре окружающей среды или посредством нагревания до полного выпаривания растворителей.
Предпочтительный вариант осуществления способа изготовления стабильной лекарственной формы, которая имеет высокое содержание аморфной формы агомелатина в полимере, состоит из смешивания и предварительной гомогенизации соединения формулы (I), полученного любым способом, и присутствующего в любой кристаллической форме, в виде комплексов, сокристаллов, или солей присоединения с фармацевтически приемлемой кислотой или основанием, с выбранным полимером, и затем указанную смесь вводят в экструдер, шаг шнека которого и температуру выбирают в зависимости от вязкости смеси, с тем, чтобы получить экструдат, который затем нарезают на куски желательного размера и затем, необязательно, измельчают.
Предпочтительно, вращение шнека необходимо проводить в диапазоне между 50 и 200 об/мин, в частности в диапазоне между 75 и 150 об/мин.
Выбранная температура экструзии будет зависеть от вязкости полученной смеси компонентов и будет находиться в диапазоне между 90°C и 200°C включительно.
В способах получения стабилизированной аморфной формы агомелатина в соответствии с изобретением, могут применять соединение формулы (I), полученное любым способом, и присутствующее в любой кристаллической форме, в виде комплексов, сокристаллов, или солей присоединения с фармацевтически приемлемой кислотой или основанием.
В способах в соответствии с изобретением, содержание агомелатина составляет больше чем или равняется 30% от массы и, в частности варьируется от 30 до 50% от массы, предпочтительно от 30% до 40%.
Полученная таким образом стабилизированная аморфная форма имеет эффективность при лечении расстройств мелатонинергической системы, и показала значительную активность в центральной нервной системе и капиллярном кровообращении, что дает возможность установить ее полезность при лечении стресса, расстройств сна, тревожного расстройства, большой депрессии, сезонного аффективного расстройства, биполярного расстройства, генерализованного тревожного расстройства, патологий сердечно-сосудистой системы, патологий пищеварительной системы, бессонницы и утомления вследствие смены часовых поясов, шизофрении, панических атак, меланхолии, расстройств аппетита, ожирения, бессонницы, боли, психотических расстройств, эпилепсии, диабета, болезни Паркинсона, сенильной деменции, различных расстройств, связанных с нормальным или патологическим старением, мигрени, потери памяти, болезни Альцгеймера, а также расстройств мозгового кровообращения. Является очевидным, что аморфная форма агомелатина может применяться в другом направлении, при лечении половых дисфункций, так как агомелатин имеет ингибирующие овуляцию и иммуномодулирующие свойства, и также может потенциально применяться при лечении злокачественных новообразований.
Стабилизированная аморфная форма агомелатина предпочтительно будет применяться при лечении большой депрессии, сезонного аффективного расстройства, биполярного расстройства, генерализованного тревожного расстройства, расстройств сна, патологий сердечно-сосудистой системы, патологий пищеварительной системы, бессонницы и утомления вследствие смены часовых поясов, расстройств аппетита и ожирения.
Получение стабилизированная аморфная форма агомелатина имеет то преимущество, что делает возможным изготовление биофармацевтических лекарственных форм стойкой и воспроизводимой композиции, которые имеют отличную стабильность в течение длительного времени.
По этой причине, в соответствии с изобретением возможно получить твердые фармацевтические композиции, которые имеют высокое содержание аморфной формы агомелатина, которые, в частности, могут применяться с помощью перорального, буккального, сублингвального, глазного, ректального, вагинального или парентерального способа применения.
Указанные фармацевтические композиции могут быть изготовлены из твердой дисперсии агомелатина в полимере без какой-либо другой операции обработки, кроме упаковки. Если это является желательным, указанные фармацевтические композиции могут, тем не менее, подвергаться обработке посредством измельчения или посредством гранулирования для наполнения в капсулы или для прессования, или они могут подвергаться покрытию.
Фармацевтические композиции в соответствии с изобретением также могут необязательно содержать фармакологически пригодные вспомогательные вещества, выбранные, например, из группы связывающих веществ, веществ для улучшения распадаемости таблеток, разрыхлителей, скользящих веществ, разбавителей, замедлителей окисления, ароматизирующих веществ, красителей, консервантов, подслащивающих веществ и антиадгезивов.
Среди фармацевтических композиций в соответствии с изобретением могут быть в частности упомянуты таблетки или драже, гранулы, сублингвальные таблетки, капсулы, пастилки для рассасывания, суппозитории, кремы, мази, гели для нанесения на кожу, инъекционные препараты, питьевые суспензии и жевательные резинки.
Предпочтительно, фармацевтические композиции в соответствии с изобретением содержат по меньшей мере 25% от массы агомелатина относительно общей массы лекарственной формы.
Применяемая доза может варьироваться в зависимости от природы и серьезности расстройства, способа применения и от возраста и массы пациента. Доза варьируется от 0,1 мг до 1 г агомелатина на день за одно или большее количество применений.
Описание Фигур
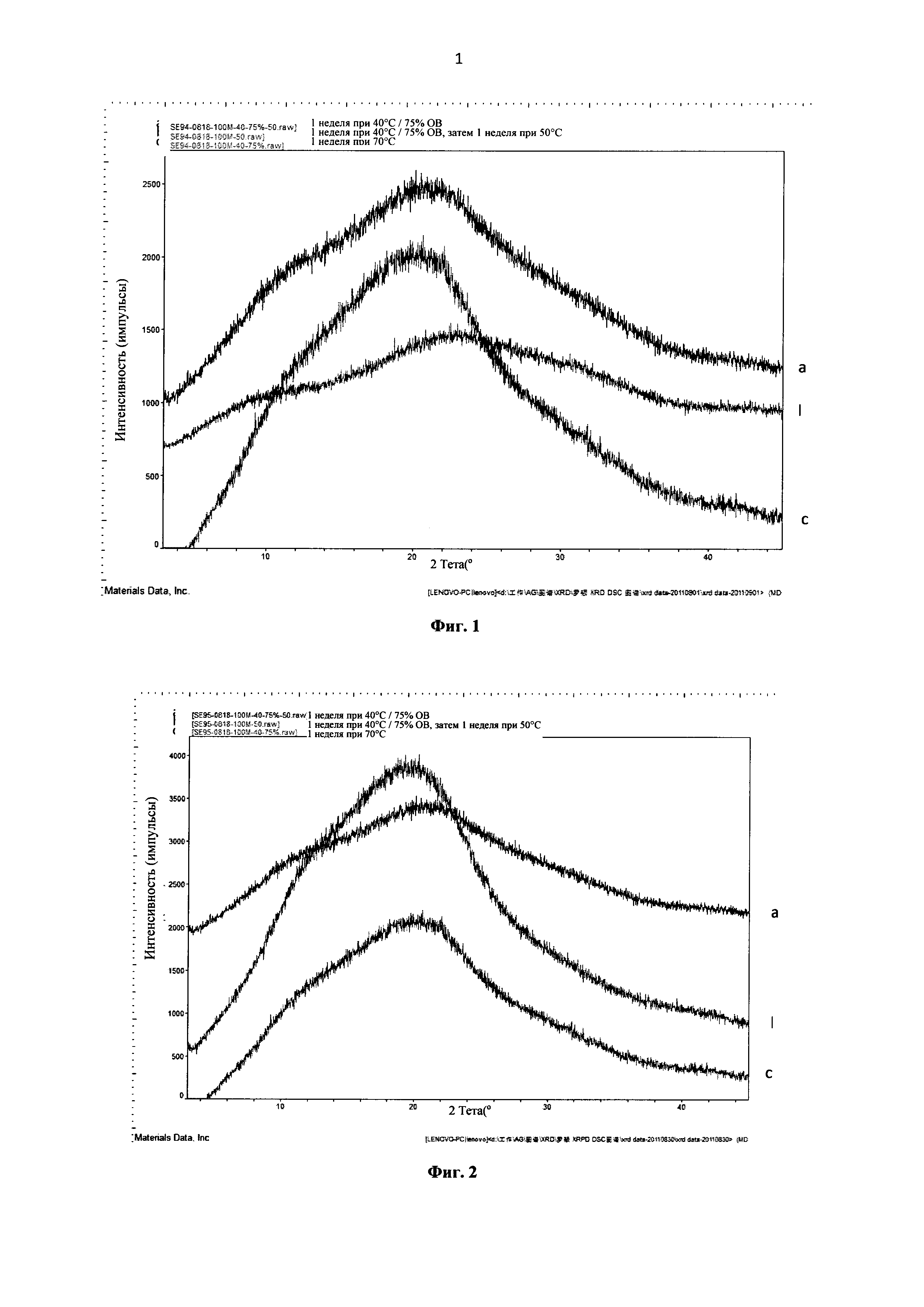
Фиг. 1: диаграммы рентгеновской дифракции аморфной формы Примера 10, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и ОВ 75%, 1 неделя при температуре 40°C/ОВ 75%, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C)
Фиг. 2: диаграммы рентгеновской дифракции аморфной формы Примера 11, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и ОВ 75%, 1 неделя при температуре 40°C/ОВ 75%, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C)
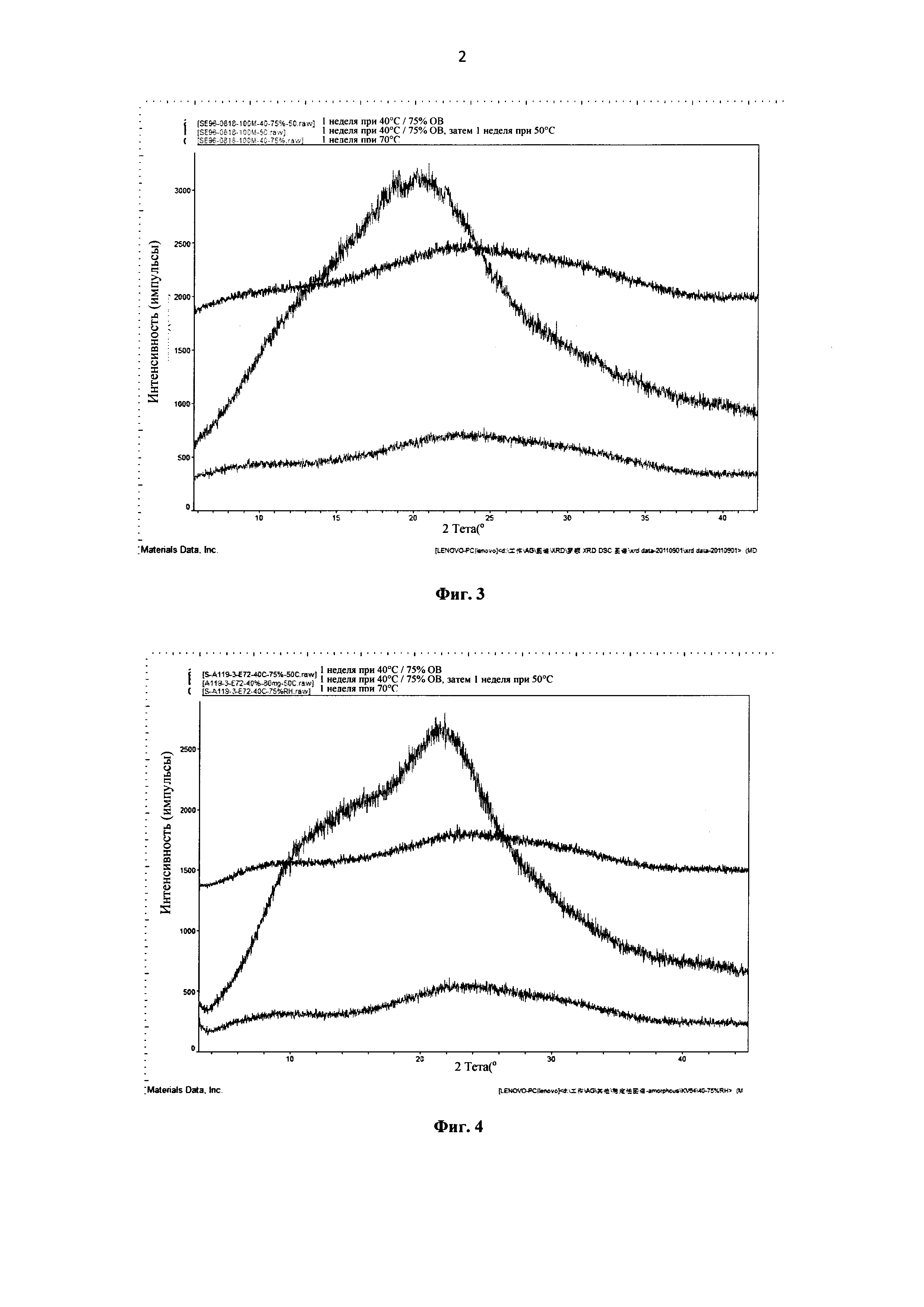
Фиг. 3: диаграммы рентгеновской дифракции аморфной формы Примера 12, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и ОВ 75%, 1 неделя при температуре 40°C/ОВ 75%, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C)
Фиг. 4: диаграммы рентгеновской дифракции аморфной формы Примера 19, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и ОВ 75%, 1 неделя при температуре 40°C/ОВ 75%, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C)
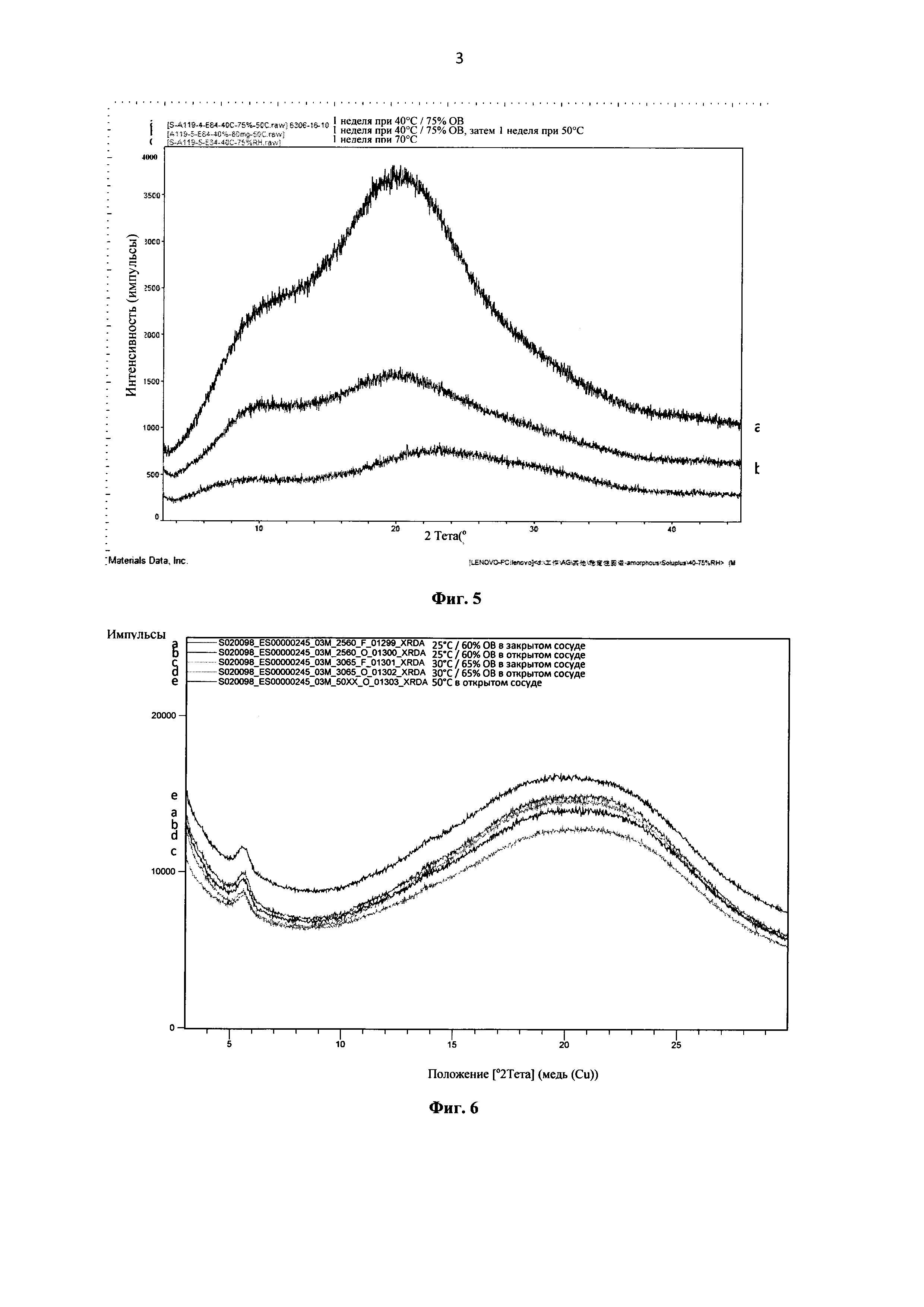
Фиг. 5: диаграммы рентгеновской дифракции аморфной формы Примера 28, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и ОВ 75%, 1 неделя при температуре 40°C/ОВ 75%, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C)
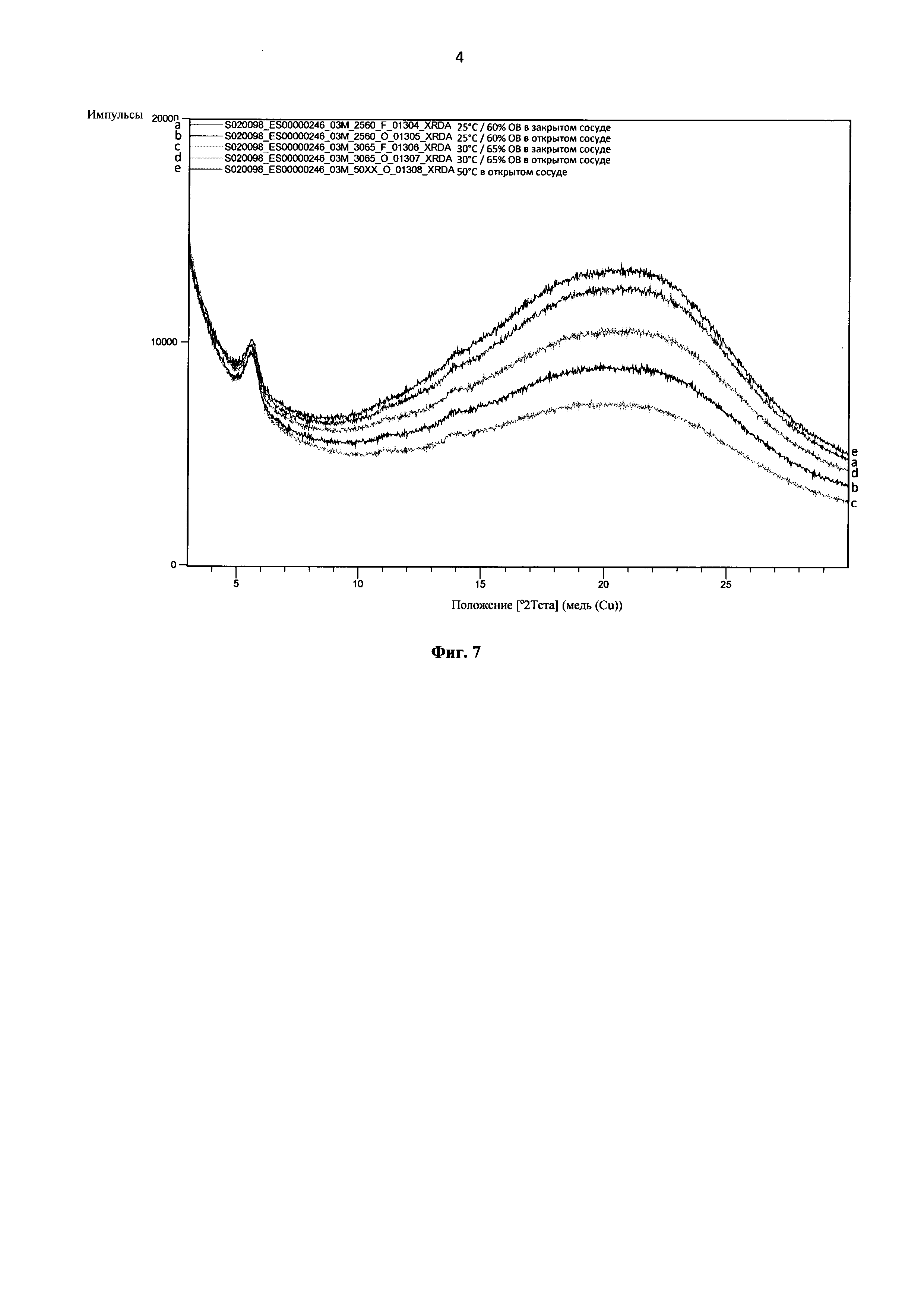
Фиг. 6: диаграммы рентгеновской дифракции аморфной формы Примера 39, записанные в конце 3 месяцев в различных условиях исследования на стабильность (25°C/ОВ 60% в открытом или закрытом сосуде, 30°C/ОВ 65% в открытом или закрытом сосуде, 50°C в открытом сосуде)
Фиг. 7: диаграммы рентгеновской дифракции аморфной формы Примера 40, записанные в конце 3 месяцев в различных условиях исследования на стабильность (25°C/ОВ 60% в открытом или закрытом сосуде, 30°C/ОВ 65% в открытом или закрытом сосуде, 50°C в открытом сосуде).
Примеры здесь и далее иллюстрируют изобретение, но никоим образом не ограничивают его.
А. Общая методика получения стабилизированной аморфной Формы агомелатина посредством растворения-выпаривания
Агомелатин и выбранный полимер помещали в 10-миллиметровый сосуд с 3 мл растворителя(ей). Смесь перемешивали при температуре 40°C на протяжении 30 минут до полного растворения и получения однородного раствора. Растворитель(и) выпаривали при пониженном давлении при температуре 40°C на протяжении 30 минут. Полученный остаток затем сушили в вакууме при температуре окружающей среды (20°C) на протяжении ночи (12 часов) до получения стабилизированной аморфной формы агомелатина. Для каждого исследования, исследовали стабильность аморфной формы в условиях, изменяющих естественные свойства, при температуре 40°C и 75% ОВ, при температуре 40°C и 75% ОВ, а затем при температуре 50°C, а также при температуре 70°C.
Различные Примеры изготовления аморфных форм и полученные результаты изложены в Таблице ниже:


В качестве примера, диаграммы рентгеновской дифракции аморфных форм примеров 10, 11, 12, 19 и 28, записанные в различных условиях исследования на стабильность (1 неделя при температуре 40°C и 75% ОВ, 1 неделя при температуре 40°C/75% ОВ, затем 1 неделя при температуре 50°C, 1 неделя при температуре 70°C), представлены на Фиг. 1, Фиг. 2, Фиг. 3, Фиг. 4 и Фиг. 5 соответственно.
Б. Общий способ получения стабилизированной аморфной формы агомелатина посредством экструзии
Агомелатин и полимер предварительно гомогенизировали в смесителе типа Turbula на протяжении 10 минут. Полученную смесь вручную помещали в конический роторный экструдер (диаметр 5/14 мм) типа HAAKE Minilab II Microcompounder (компания ThermoFisher). Скорость экструзии составляла 100 об/мин.
Стабильность полученной аморфной формы оценивали в условиях различных температур и относительной влажности: 25°C/60% ОВ в открытом или закрытом сосуде, 30°C/65% ОВ в открытом или закрытом сосуде, 50°C в открытом сосуде.
Все примеры аморфных форм, изложенные в Таблице ниже, имели стабильность на протяжении по меньшей мере более, чем 6 недель.

В качестве примера, диаграммы рентгеновской дифракции, записанные в конце 3 месяцев в различных условиях исследования на стабильность (25°C/60% ОВ в открытом или закрытом сосуде, 30°C/65% ОВ в открытом или закрытом сосуде, 50°C в открытом сосуде) для Примеров 39 и 40, представлены на Фиг. 6 и Фиг. 7 соответственно.
В. Растворимость
Исследование растворимости полученных лекарственных форм проводили с использованием оборудования типа Crystal16® в буферном растворе со значением pH 6,8 при температуре 25°C на протяжении периода времени, составляющего 4 часа, со скоростью перемешивания, которая составляла 700 об/мин. Исследовали различные концентрации, и при этом присутствие нерастворимых частиц наблюдали с помощью нефелометрического определения. В качестве контроля, растворимость агомелатина в указанных условиях составляла 0,14 мг/мл.
Полученные результаты изложены в Таблице ниже, где установлена I) максимальная наблюдаемая растворимость и время, при котором указанная максимальная растворимость наблюдается, II) растворимость, наблюдаемая по истечении 4 часов.

Полученные результаты показывают значительное повышение максимальной растворимости. Важным моментом является то, что указанное повышение растворимости продолжается в течение длительного времени: по истечении 4 часов, результаты показывают, что растворимость по меньшей мере умножается на коэффициент в пределах от 1,7 до 8,5, что дает время для поглощения действующего вещества перед тем, как оно снова выпадет в осадок.
Г. Фармацевтические композиции
Пример 42
Состав для изготовления 1000 капсул, каждая из которых содержит 25 мг агомелатина:
|
Экструдат изготавливали в соответствии с Примером 36 и затем нарезали на мини-матрицы, которые вводили в 1 капсулу.
Пример 43
Состав для изготовления 1000 капсул, каждая из которых содержит 25 мг агомелатина:
|
Экструдат изготавливали в соответствии с Примером 38 и затем нарезали на мини-матрицы, которые вводили в 1 капсулу.
Пример 44
Состав для изготовления 1000 таблеток, каждая из которых содержит 25 мг агомелатина:
|