Результат интеллектуальной деятельности: ПИТАТЕЛЬНАЯ СРЕДА ДЛЯ КУЛЬТИВИРОВАНИЯ ПЕРЕВИВАЕМЫХ КЛЕТОЧНЫХ ЛИНИЙ МЛЕКОПИТАЮЩИХ
Вид РИД
Изобретение
Изобретение относится к биотехнологии, вирусологии и может быть использовано при разработке питательной среды для культивирования клеток млекопитающих, в частности, перевиваемых клеточных линий Vero и ВНК, и вирусов, в том числе при получении in vitro биомассы аттенуированного штамма вируса бешенства «Москва 3253».
Известны питательные среды для культивирования клеточных культур определенного химического состава, используемые как с добавлением сыворотки КРС, так и без нее: минимальная среда Игла MEM, основная среда Игла MEM, среда Игла MEM в модификации Дульбекко, среда 199 (среда Хенкса), среда Хэма, среда Мак-Коя, среда Лейбовица [1]. Указанные среды являются коммерчески доступными, их производство существует на территории России, однако они имеют высокую стоимость. Учитывая, что питательная среда должна содержать достаточное количество питательных веществ для поддержания высокой плотности клеток и репликации вируса, оптимальным способом снижения стоимости является использование гидролизатов белков растительного и животного происхождения в качестве основы сред [2, 3], поскольку в их состав входят низкомолекулярные пептиды, микроэлементы и другие биологически активные соединения, обеспечивающие обменные процессы в клетках.
Известен способ получения питательной среды [4] для культивирования клеток млекопитающих, в частности для клеток MDCK и Vero, содержащая сбалансированный солевой раствор, ферментативный гидролизат рисовой муки, аминокислоты и витамины.
Известна питательная среда на основе ферментативного гидролизата белков рыб и отходов рыбного производства [5], которая предлагается для культивирования клеток эукариот.
Известны способы получения и питательные среды для культивирования клеток эукариот, основой для которых являются ферментативные гидролизаты шкур ластоногих и/или шкур крупного рогатого скота (КРС) [6, 7].
Известен способ получения и питательная среда для культивирования клеток эукариот, основой для которой служит ферментативный гидролизат обезжиренной и обезвоженной мозговой ткани КРС, являющейся отходом производства медицинского препарата «Липоцеребрин» [8].
Известны составы питательных сред для суспензионного культивирования клеток млекопитающих на основе ферментативных гидролизатов лактальбумина и мышечных белков [9, 10].
Известна сухая стерильная малосывороточная питательная среда на основе ферментативного гидролизата белков мышц для культивирования клеток млекопитающих, в частности клеток карциномы гортани человека Нер-2 и суспензионной культуры клеток лимфомы Беркита Namalva [11].
Известна питательная среда для выращивания культур клеток животных, основой для которой является ферментативный гидролизат белков молока [12].
Перечисленные среды применяют для культивирования конкретных клеточных линий и для работы с малыми культуральными массами с низкой плотностью.
Использование ценного пищевого сырья для приготовления питательных сред иррационально и экономически неэффективно.
Задачей изобретения является разработка эффективной питательной среды для культивирования перевиваемых клеточных культур млекопитающих на примере клеточных линий Vero и BHK и репродукции вирусов на примере аттенуированного вируса бешенства штамма «Москва 3253» на основе гидролизата белка фибрина крови лошадей, что позволит решить задачу рациональной утилизации отходов производства иммунобиологических препаратов.
Технический результат изобретения заключается в расширении ассортимента питательных сред и обеспечении рациональной утилизации отходов, образующихся при производстве иммунобиологических препаратов. Экономический эффект использования изобретения состоит в снижении стоимости питательных сред при сохранении эффективности наращивания биологического материала.
Указанный технический результат достигается тем, что питательная среда в объеме 1 л содержит компоненты в следующем соотношении, об. %:
|
Сухой ферментативный гидролизат фибрина получают путем выпаривания жидкого ферментативного гидролизата фибрина (содержание аминного азота от 2,6 до 3,0%), который получают по существующему способу: патент RU 2425866 [13].
Концентрирование гидролизата осуществляют методом выпаривания на установке вакуум-выпарной УВВ-50. Высушивание на установке распылительного типа КЯУЛ 101325.002 - методом «псевдокипящего слоя». По агрегатному состоянию ферментативный гидролизат фибрина -мелкодисперсный порошок с нежно-желтым оттенком и белковым запахом. Физико-химические показатели сухого гидролизата: содержание общего азота - (7,5±0,3) %; аминного азота - (2,8±0,2) %; процент расщепления белка - (50,7±1,68) %; содержание пептона (по шкале Дифко) - (53,67±1,53) %; следы белка - отсутствуют; сухой остаток - (10,7±0,2) %; хлориды - (0,2±0,05) %; влажность - (2,4±0,2) %; рН - (6,7±0,2).
Питательную среду для культивирования клеточных культур на основе сухого ферментативного гидролизата фибрина готовят, соблюдая асептические условия, в стерильной посуде, изготовленной из стекла или лабораторной пластмассы. Навеску сухого ферментативного гидролизата фибрина растворяют в стерильном сбалансированном солевом растворе (Эрла или Хенкса) до конечной концентрации 10% и последовательно фильтруют через мембранные фильтры с диаметром пор 0,45 и 0,22 мкм. Полученный концентрат разбавляют стерильным сбалансированным солевым раствором до концентрации от 0,1 до 0,25%. Уровень рН корректируют до значения 7,2±0,2 с помощью раствора гидроксида натрия в концентрации 0,1 моль/л или ацетатного буферного раствора (рН 4,5) в концентрации 0,1 моль/л.
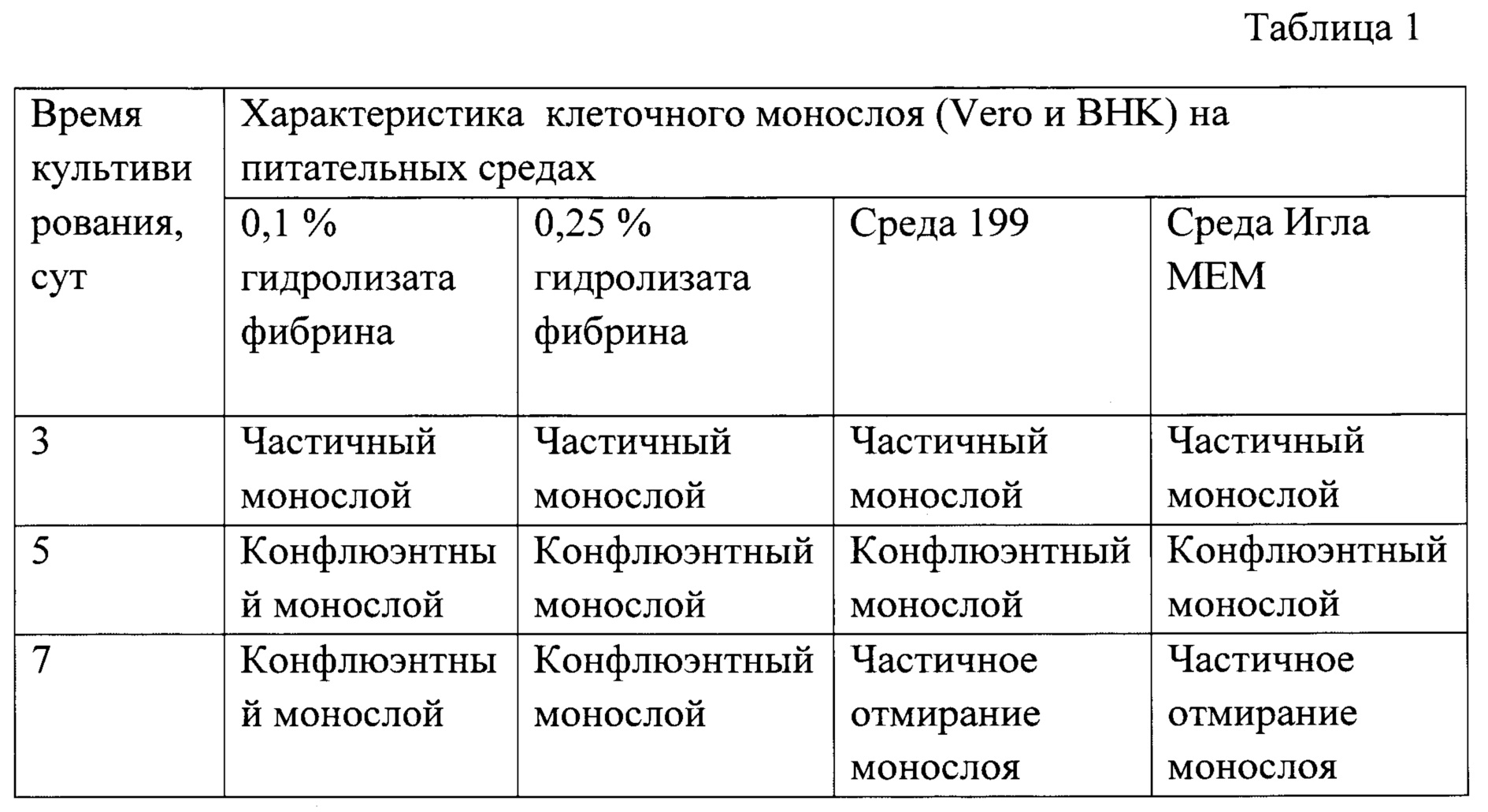
Рабочая концентрация ферментативного гидролизата фибрина в заявляемой питательной среде - от 0,1 до 0,25%. Ростовые свойства питательной среды проверяют при выращивании клеток млекопитающих в течение 3 последовательных пассажей, оценивая рост через 3 и 7 суток [1]. При одинаковой посевной концентрации рост клеток Vero и BHK на заявляемой питательной среде с ферментативным гидролизатом фибрина и среде Игла MEM с содержанием сыворотки КРС 5 или 10%, и среде 199 с содержанием сыворотки КРС 5 или 10% практически одинаков, сроки формирования монослоя и его сохранения одни и те же. Перевиваемые клетки, выращенные на заявляемой питательной среде, сохраняют первоначальную морфологию.
Характеристика роста монослойной культуры перевиваемых линий Vero и BHK при выращивании на различных питательных средах приведена в таблице 1.
Выращенная на питательной среде с ферментативным гидролизатом фибрина клеточная культура Vero, использованная для культивирования аттенуированного вируса бешенства штамма «Москва 3253», сохраняла чувствительность к данному вирусу.
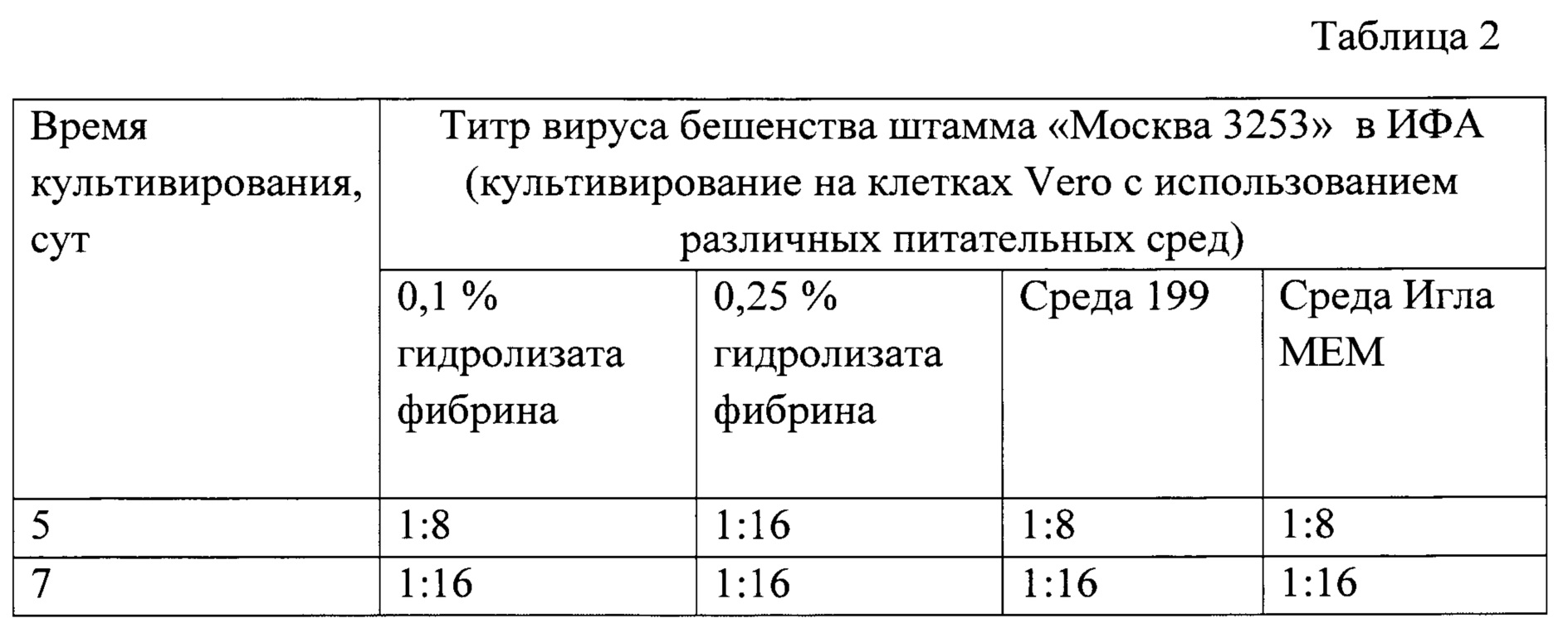
Результаты ИФА по выявлению уровня накопления фиксированного вируса бешенства «Москва 3253» на клетках Vero, выращенных в средах с содержанием фибрина (от 0,1 до 0,25%), Игла MEM и 199 с добавлением 5% сыворотки КРС, приведены в таблице 2.
Заявляемая питательная среда с ферментативным гидролизатом фибрина может быть также использована для многократного пассирования перевиваемых линий клеток.
Использование в заявляемой питательной среде ферментативного гидролизата фибрина решает проблему утилизации отходов производства иммунобиологических препаратов и удешевляет стоимость целевого продукта.
Изготовление питательной среды на основе ферментативного гидролизата фибрина не требует сложного оборудования и может осуществляться на биотехнологических и фармацевтических предприятиях.
Пример 1.
Культивирование клеточной культуры Vero или BHK на среде, содержащей 0,1% ферментативного гидролизата фибрина и 10% сыворотки КРС.
К навеске сухого ферментативного гидролизата фибрина в количестве 0,5 г добавляют до 5 мл стерильного сбалансированного солевого раствора Эрла. Полученный раствор профильтровывают с помощью мембранных фильтров 0,45 мкм и 0,22 мкм. Полученный фильтрат стерильно разводят сбалансированным солевым раствором Эрла в соотношении 1:100 и добавляют сыворотку КРС в концентрации 10%, а также антибиотики (смесь пенициллина и стрептомицина). Манипуляции следует проводить с соблюдением правил асептики.
Подготовленный клеточный монослой (Vero или BHK) отмывают от питательной среды раствором DPBS с последующим удалением жидкой фракции. Добавляют к клеткам раствор трипсина и версена (соотношение 2:1), затем клетки инкубировать при 37°С в атмосфере 5% углекислого газа в течение 3-5 минут. После открепления клеток во флакон добавляют необходимое количество среды на основе ферментативного гидролизата фибрина, а клетки тщательно ресуспендируют с помощью пипетки. После подсчета количества клеток, добавляют необходимое количество клеточной суспензии и указанной среды. Рекомендуемая начальная концентрация клеток составляет 5-10×104 кл./мл. Клетки инкубируют при 37°С в атмосфере 5% углекислого газа в течение 4-5 суток. Питательная среда на основе гидролизата фибрина обеспечивает накопление клеток перевиваемых линий Vero и BHK. Конфлюэнтный монослой сохраняется не менее 2 суток с момента образования. Клетки Vero и BHK, выращенные в экспериментальной среде в течение пятнадцати пассажей, сохраняли форму, характерную для данного вида клеток, с четко выраженными границами, без признаков дегенерации и морфологически не отличались от клеток, выращенных на средах сравнения (199 и Игла MEM).
Культивирование клеточной культуры Vero или BHK на среде, содержащей 0,25% ферментативного гидролизата фибрина и 10% сыворотки КРС проводят аналогично культивированию клеточной культуры Vero или BHK на среде, содержащей 0,1% ферментативного гидролизата фибрина. Результат представлен в таблице 1.
Пример 2.
Накопление фиксированного вируса бешенства «Москва 3253» на клетках Vero, выращенных в среде на основе ферментативного гидролизата фибрина.
Вируссодержащий материал вносят в суспензию клеток Vero, выращенную в экспериментальной среде, приготовленной по Примеру 1. Рекомендуемая заражающая доза составляет от 0,1 до 1,0 lg ИД50/мл. Культивирование вируса на клетках осуществляют при 37°С в атмосфере 5% CO2 в течение от 5 до 7 суток. Рекомендуемая концентрация клеток составляет от 0,5-1,5×106 кл./мл.
Показатели уровня накопления фиксированного вируса бешенства «Москва 3253» на клетках Vero, выращенных в средах с содержанием ферментативного гидролизата фибрина (от 0,1 до 0,25%), Игла MEM и 199 с добавлением 5% сыворотки КРС, сопоставимы друг с другом при исследовании в ИФА. Титр вируса через 7 суток культивирования соответствовал 1:16, что свидетельствует о возможности применения питательной среды с фибрином для накопления вируса бешенства в культуре перевиваемых клеток.
Таким образом, заявляемая питательная среда для культивирования перевиваемых клеточных линий млекопитающих на основе сухого ферментативного гидролизата фибрина расширяет ассортимент питательных сред и обеспечивает рациональную утилизацию отходов, образующихся при производстве иммунобиологических препаратов. Экономический эффект использования изобретения состоит в снижении стоимости питательных сред при сохранении эффективности наращивания биологического материала.
Литература:
1. Фрешни Р.Я. Культура животных клеток: практическое руководство, 2014 г., М.: Бином. 718 с.
2. Телишевская Л.Я. Белковые гидролизаты: Получение, состав, применение, 2000 г., М.: Аграрная наука. 295 с.
3. Богрянцева М.П. Технология изготовления и свойства питательной среды сухой стерильной на основе гидролизатов: диссертация … кандидата биологических наук: 03.00.23., Кольцово, 1999. 30 с.
4. Трошкова Г.П., Сумкина Т.П., Мартынец Л.Д., Мазуркова Н.А. Питательная среда для культивирования клеток млекопитающих. Патент 2377295. Опубл. 27.12.2009. Бюл. 36.
5. Ермишина И.Г., Мейнерт А.Г., Ермолин Г.А., Дудкин С.М. Питательная среда для культивирования клеток эукариотов и способ получения основы питательной среды - протеолитического гидролизата. Патент 2103360. Опубл. 27.01.1998
6. Ермишина И.Г., Мейнерт А.Г., Ермолин Г.А. Способ получения ферментативного гидролизата и питательная среда «Эпидермат-2» для культивирования клеток эукариотов. Патент 2068879. Опубл. 11.10. 1996.
7. Ермишина И.Г., Мейнерт А.Г., Власова Т.Ф. Способ получения ферментативного гидролизата из мышечной ткани ластоногих и питательная среда «Целат» для культивирования клеток эукариотов. Патент 2074249. Опубл. 27.02.1997.
8. Искендеров Р.И., Егоров Б.Б., Ермишина И.Г., Сасунов Н.Ш., Власова Т.Ф., Кирьянова Е.А., Попова Н.А., Джавадов С.А., Эюбов Э., Мирошникова Е.Б., Ермолин Г.А. Способ получения ферментативного гидролизата и питательная среда для культивирования клеток эукариотов. Патент 2020153. Опубл. 30.09.1994.
9. Елисеев А.К., Мельник Н.В., Зенов Н.И., Михеева Г.Ф. Литенкова И.Ю., Шмаленко Т.Г., Красуткин С.Н. Питательная среда для суспензионного культивирования клеток млекопитающих. Патент 2300563 Опубл. 10.06.2007 Бюл. №34.
10. Елисеев А.К. Красуткин С.Н., Зенов Н.И., Литенкова И.Ю., Мельник Н.В., Шмаленко Т.Г., Маслов Е.В., Ельников В.В., Крюкова Е.Н. Питательная среда для суспензионногоо культивирования клеток млекопитающих. Патент 2558253. Опубл. 27.07.2015. Бюл. №21.
11. Трошкова Г.П., Богрянцева М.П., Мазуркова Н.А., Мартынец Л.Д., Кирова Е.В., Юдин А.В. Сухая стерильная малосывороточная питательная среда для культивирования клеток млекопитающих. Патент 2201958 РФ. Опубл. 10.04.2003, Бюл. №10
12. Богрянцева М.П., Трошкова Г.П., Мазуркова Н.А., Ночевный В.Т., Мартынец Л.Д., Сироткина Т.Б. Способ получения жидкой стерильной питательной среды на основе ферментативного гидролизата. Патент 2161649. Опубл. 10.01.2001. Бюл. 1
13. Антонычева М.В., Нижегородцев С.А. Еремин С.А., Аленкина Т.В., Шульгина И.В., Бахрушина Н.И., Белоусов А.Д., Жулидов И.М., Никифоров А.К. Питательная среда для глубинного культивирования холерного вибриона. Патент 2425866. Опубл. 10.08.2011. Бюл. №22.