Результат интеллектуальной деятельности: МЫШИ С ГУМАНИЗИРОВАННОЙ ЛЕГКОЙ ЦЕПЬЮ
Вид РИД
Изобретение
Область техники
Генетически модифицированные отличные от человека фертильные животные, которые экспрессируют вариабельные последовательности λ легкой цепи иммуноглобулина человека, когнатные вариабельным последовательностям тяжелой цепи человека. Описаны генетически модифицированные мыши, клетки, зародыши и ткани, которые содержат последовательность нуклеиновой кислоты, кодирующую ADAM6a, функциональный в локусе ADAM6 мыши, причем мыши, клетки, зародыши и ткани содержат лямбда генные сегменты легкой цепи иммуноглобулина человека, которые способны к реаранжировке для образования функционального вариабельного домена легкой цепи иммуноглобулина. Модификации включают в себя относящиеся к человеку и/или гуманизированные локусы иммуноглобулина. Описаны мыши, которые обладают функцией ADAM6, включая мышей, которые содержат эктопическую последовательность нуклеиновой кислоты, которая кодирует белок ADAM6. Описаны генетически модифицированные самцы мышей, которые содержат генетическую модификацию эндогенного локуса области VH иммуноглобулина мыши и которые дополнительно обладают активностью ADAM6, включая мышей, которые содержат эктопическую последовательность нуклеиновой кислоты, которая восстанавливает фертильность самца мыши.
Предусмотрены генетически модифицированные отличные от человека фертильные животные, которые содержат делецию или модификацию эндогенного гена ADAM6 или его гомолога или ортолога и которые содержат генетическую модификацию, которая полностью или частично восстанавливает функцию ADAM6 (или его гомолога или ортолога), причем отличные от человека животные экспрессируют λ вариабельную последовательность иммуноглобулина человека, ассоциированную с константной последовательностью λ или κ легкой цепи.
Предшествующий уровень техники настоящего изобретения
Фармацевтические применения антител в последних двух десятилетиях активизировали большое количество исследований в области получения антител, подходящих для применений в качестве терапевтических средств для людей. Ранее существующие терапевтические средства на основе антител, основанные на мышиных антителах, не были оптимальными в качестве терапевтических средств для людей, поскольку повторное введение мышиных антител людям приводит к проблемам в отношении иммуногенности, которые могут нарушать схемы длительного лечения. Разрабатывали решения, основанные на гуманизации мышиных антител, чтобы сделать их более похожими на антитела человека и менее похожими на антитела мыши. Придерживались способов экспрессии последовательностей иммуноглобулина человека для применения в антителах, преимущественно основанных на in vitro экспрессии библиотек иммуноглобулина человека в фаге, бактериях или дрожжах. В конце концов, были предприняты попытки создания применимых антител человека из лимфоцитов человека in vitro, в организмах мышей, которым пересадили гематопоэтические клетки человека, и в организмах трансхромосомных или трансгенных мышей с недееспособными эндогенными локусами иммуноглобулина. У трансгенных мышей, было необходимо инактивировать эндогенные гены иммуноглобулина мыши так, чтобы случайным образом интегрированные полностью человеческие трансгены могли бы функционировать в качестве источника последовательностей иммуноглобулина, экспрессированных в организме мыши. Такие мыши могут произовдить антитела человека, подходящие для применения в качестве терапевтических средств для людей, но эти мыши демонстрируют существенные проблемы в отношении их иммунной системы. Эти проблемы (1) делают мышей непригодными для создания разнообразного в достаточной степени набора антител, (2) требуют применения решений для всестороннего переконструирования, (3) обеспечивают субоптимальный процесс селекции клонов, вероятно, вследствие несовместимости между элементами человека и мыши и (4) предоставляют этим мышам ненадежный источник больших и разнообразных популяций вариабельных последовательностей человека, нуждающихся в том, чтобы быть действительно применимыми для получения терапевтических средств для людей.
Трансгенные мыши, которые содержат трансгены полностью человеческих антител, содержат случайным образом вставленные трансгены, которые содержат нереаранжированные вариабельные последовательности тяжелой цепи иммуноглобулина человека (последовательности V, D и J), соединенные с константными последовательностями тяжелой цепи человека, и нереаранжированные вариабельные последовательности легкой цепи иммуноглобулина человека (V и J), соединенные с константными последовательностями легкой цепи человека. Мыши, следовательно, создают реаранжированные гены антитела из локусов, отличных от эндогенных мышиных локусов, причем реаранжированные гены антитела являются полностью человеческими. Как правило, мыши содержат последовательности тяжелой цепи человека и последовательности легкой цепи человека, хотя также сообщалось о мышах по меньшей мере с несколькими последовательностями λ человека. Трансгенные мыши, как правило, содержат поврежденные и нефункциональные эндогенные локусы иммуноглобулина или нокауты эндогенных локусов иммуноглобулина, так чтобы мыши были неспособны к реаранжировке последовательностей антитела человека на эндогенном локусе иммуноглобулина мыши. Изменения у таких трансгенных мышей делают их менее чем оптимальными для создания достаточно разнообразного репертуара антител человека в организме мышей, вероятно, по меньшей мере частично вследствие субоптимального процесса селекции клонов, который обеспечивает контакт молекул полностью человеческих антител в пределах эндогенной системы селекции мыши.
В настоящей области техники остается потребность в получении улучшенных генетически модифицированных отличных от человека животных, которые применимы в создании последовательностей иммуноглобулина, включая последовательности антител человека, и которые применимы в создании достаточно разнообразного набора антител человека. Кроме того, остается необходимость в мышах, которые способны к реаранжировке генных сегментов иммуноглобулина для образования применимых реаранжированных генов иммуноглобулина, включая в себя вариабельные домены тяжелой цепи человека, которые являются когнатными вариабельным доменам λ человека или вариабельным доменам κ человека или которые способны к созданию белков из измененных локусов иммуноглобулина, включая в себя локусы, которые содержат достаточно разнообразную селекцию вариабельных последовательностей λ легкой цепи человека и/или вариабельных последовательностей κ легкой цепи человека. Существует потребность в отличных от человека животных, которые могут создавать вариабельные области антител как из сегментов κ человека, так и сегментов λ человека, причем сегменты κ человека и сегменты λ человека являются когнатными вариабельным доменам тяжелой цепи человека. Также существует необходимость в увеличенной частоте использования последовательностей λ человека у генетически модифицированных животных.
Краткое раскрытие настоящего изобретения
Описаны генетически модифицированные отличные от человека животные, которые содержат модификацию, которая снижает или устраняет активность гена ADAM6 или его гомолога или ортолога, причем модификация приводит к потере фертильности, и животные дополнительно содержат последовательность, которая кодирует активность, взаимодополняющую или восстанавливающую утраченную или сниженную активность ADAM6 (или активность гомолога или ортолога), и отличные от человека животные дополнительно содержат модификации, которые позволяют им экспрессировать вариабельные области тяжелой цепи иммуноглобулина человека, которые являются когнатными вариабельным областям λ легкой цепи иммуноглобулина человека. Согласно различным аспектам экспрессируются вариабельные области λ легкой цепи иммуноглобулина человека, слитые с константными областями λ или κ.
Согласно различным аспектам последовательность, которая кодирует активность ADAM6, является смежной с последовательностью иммуноглобулина человека. Согласно различным аспектам последовательность, которая кодирует активность ADAM6, является смежной с не относящейся к человеку последовательностью иммуноглобулина. Согласно различным аспектам последовательность присутствует на той же хромосоме, что и эндогенный не относящийся к человеку локус тяжелой цепи иммуноглобулина отличного от человека животного. Согласно различным аспектам последовательность присутствует на другой хромосоме, чем локус тяжелой цепи иммуноглобулина отличного от человека животного.
Описаны генетически модифицированные отличные от человека животные, которые содержат модификацию, которая поддерживает активность гена ADAM6 или его гомолога или ортолога, причем модификация включает в себя вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека выше не относящейся к человеку константной области тяжелой цепи иммуноглобулина, и отличные от человека животные дополнительно содержат модификации, которые позволяют им экспрессировать вариабельные области λ легкой цепи иммуноглобулина человека, когнатные вариабельным областям тяжелой цепи иммуноглобулина человека. Согласно различным аспектам экспрессируются вариабельные области λ легкой цепи иммуноглобулина человека, слитые с константными областями λ или κ.
Согласно различным аспектам вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека проводят 3' или ниже гена ADAM6 отличного от человека животного. Согласно различным аспектам вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека проводят таким способом, чтобы ген(ы) ADAM6 отличного от человека животного не был(и) разрушен(ы), удален(ы) и/или функционально выключен(ы) так, чтобы активность ADAM6 отличного от человека животного находилась на таком же или сопоставимом уровне, как у отличного от человека животного, которое не содержит такой вставки. Иллюстративные разрывы, делеции и/или модификации функционального сайленсинга включают в себя любые модификации, которые приводят к снижению, устранению и/или потере активности белка(ов) ADAM6, кодируемого(ых) геном(ами) ADAM6 отличного от человека животного.
Согласно одному аспекту предусмотрены конструкты нуклеиновых кислот, клетки, зародыши, мыши и способы для получения мышей, которые содержат модификацию, которая дает в результате нефункциональный эндогенный белок ADAM6 или ген ADAM6 мыши (например, нокаут или делецию в эндогенном гене ADAM6), причем мыши содержат последовательность нуклеиновой кислоты, которая кодирует белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному аспекту предусмотрены конструкты нуклеиновой кислоты, клетки, зародыши, мыши и способы получения мышей, которые содержат модификацию эндогенного локуса иммуноглобулина мыши, причем мыши содержат белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши. Согласно одному варианту осуществления эндогенный локус иммуноглобулина мыши представляет собой локус тяжелой цепи иммуноглобулина, и модификация снижает или устраняет активность ADAM6 клетки или ткани самца мыши.
Согласно одному аспекту предусмотрены мыши, которые содержат эктопическую нуклеотидную последовательность, кодирующую ADAM6 мыши или его ортолог или гомолог или функциональный фрагмент; также предусмотрены мыши, которые содержат эндогенную нуклеотидную последовательность, кодирующую ADAM6 мыши или его ортолог или гомолог или фрагмент, и по меньшей мере одну генетическую модификацию локуса тяжелой цепи иммуноглобулина.
Согласно одному аспекту предусмотрены способы получения мышей, которые содержат модификацию эндогенного локуса иммуноглобулина мыши, причем мыши содержат белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному аспекту предусмотрены способы получения мышей, которые содержат генетическую модификацию локуса тяжелой цепи иммуноглобулина, причем применение способов дает в результате самцов мышей, которые содержат модифицированный локус тяжелой цепи иммуноглобулина (или его делецию), и самцы мышей способны производить потомство путем спаривания. Согласно одному варианту осуществления самцы мышей способны производить сперму, которая может проходить от матки мыши через яйцевод мыши для оплодотворения яйцеклетки мыши.
Согласно одному аспекту предусмотрены способы получения мышей, которые содержат генетическую модификацию локуса тяжелой цепи иммуноглобулина и локуса легкой цепи иммуноглобулина, причем применение способов модификации локуса тяжелой цепи дает в результате самцов мышей, которые проявляют снижение фертильности, и мыши содержат генетическую модификацию, которая полностью или частично восстанавливает снижение фертильности. Согласно различным вариантам осуществления снижение фертильности характеризуется неспособностью спермы самцов мышей мигрировать от матки мыши через яйцевод мыши для оплодотворения яйцеклетки мыши. Согласно различным вариантам осуществления снижение фертильности характеризуется наличием спермы, которая проявляет in vivo нарушение миграции. Согласно различным вариантам осуществления генетическая модификация, которая полностью или частично восстанавливает снижение фертильности, представляет собой последовательность нуклеиновой кислоты, кодирующую ген ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному варианту осуществления генетическая модификация предусматривает замещение эндогенных вариабельных локусов тяжелой цепи иммуноглобулина вариабельными локусами тяжелой цепи иммуноглобулина другого вида (например, отличного от мыши вида). Согласно одному варианту осуществления генетическая модификация предусматривает вставку ортологичных вариабельных локусов тяжелой цепи иммуноглобулина в эндогенные вариабельные локусы тяжелой цепи иммуноглобулина. Согласно конкретному варианту осуществления вид представляет собой человека. Согласно одному варианту осуществления генетическая модификация предусматривает делецию эндогенного вариабельного локуса тяжелой цепи иммуноглобулина полностью или частично, причем делеция приводит к потере эндогенной функции ADAM6. Согласно конкретному варианту осуществления потеря эндогенной функции ADAM6 связана со снижением фертильности у самцов мышей.
Согласно одному варианту осуществления генетическая модификация предусматривает инактивацию эндогенного не относящегося к человеку вариабельного локуса тяжелой цепи иммуноглобулина полностью или частично, причем инактивация не приводит к потере эндогенной функции ADAM6. Инактивация может включать в себя замещение или делецию одного или нескольких эндогенных не относящихся к человеку генных сегментов, что дает в результате эндогенный не относящийся к человеку локус тяжелой цепи иммуноглобулина, который по существу является неспособным к реаранжировке для кодирования тяжелой цепи антитела, которое содержит эндогенные не относящиеся к человеку генные сегменты. Инактивация может включать в себя другие модификации, которые делают эндогенный локус тяжелой цепи иммуноглобулина неспособным к реаранжировке для кодирования тяжелой цепи антитела, причем модификация не включает в себя замещение или делецию эндогенных генных сегментов. Иллюстративные модификации включают в себя хромосомные вставки и/или транслокации, опосредованные молекулярными техниками, например, с использованием точного размещения сайтов сайт-специфической рекомбинации (например, технологии Cre-lox). Другие иллюстративные модификации включают в себя блокирование функциональной связи между не относящимися к человеку вариабельными генными сегментами иммуноглобулина и не относящимися к человеку константными областями иммуноглобулина.
Согласно одному варианту осуществления генетическая модификация предусматривает вставку в геном отличного от человека животного фрагмента ДНК, содержащего один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека другого вида (например, отличного от мыши вида), функционально связанных с одной или несколькими последовательностями константной области (например, геном IgM и/или IgG). Согласно одному варианту осуществления фрагмент ДНК способен подвергаться реаранжировке в геноме отличного от человека животного для образования последовательности, которая кодирует вариабельный домен тяжелой цепи антитела. Согласно одному варианту осуществления вид представляет собой человека. Согласно одному варианту осуществления генетическая модификация предусматривает вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека ниже или 3' по отношению к эндогенному гену ADAM6 отличного от человека животного так, чтобы активность ADAM6 (например экспрессия и/или функция кодируемого белка) являлась одинаковой или сопоставимой с отличным от человека животным, которое не содержит вставку.
Согласно одному аспекту предусмотрены мыши, которые содержат модификацию, которая снижает или устраняет экспрессию ADAM6 мыши из эндогенного аллеля ADAM6 так, что самец мыши с модификацией проявляет сниженную фертильность (например, сильно сниженную способность производить потомство путем спаривания), или является по существу стерильным вследствие снижения или устранения эндогенной функции ADAM6, причем мыши дополнительно содержат эктопическую последовательность ADAM6 или ее гомолог или ортолог или функциональный фрагмент. Согласно одному аспекту модификация, которая снижает или устраняет экспрессию ADAM6 мыши, представляет собой модификацию (например, вставку, делецию, замещение и т.д.) в локусе иммуноглобулина мыши.
Согласно одному варианту осуществления снижение или потеря функции ADAM6 предусматривает неспособность или существенную неспособность мыши производить сперму, которая может проходить от матки мыши через яйцевод мыши для оплодотворения яйцеклетки мыши. Согласно конкретному варианту осуществления по меньшей мере приблизительно 95%, 96%, 97%, 98% или 99% сперматозоидов, произведенных в объеме эякулята мыши, являются неспособными пройти через яйцевод in vivo после копуляции и оплодотворить яйцеклетку мыши.
Согласно одному варианту осуществления снижение или потеря функции ADAM6 предусматривает неспособность образования или существенную неспособность образования комплекса ADAM2 и/или ADAM3 и/или ADAM6 на поверхности сперматозоида мыши. Согласно одному варианту осуществления потеря функции ADAM6 предусматривает существенную неспособность оплодотворить яйцеклетку мыши путем копуляции с самкой мыши.
Согласно одному аспекту предусмотрена мышь, которая не содержит функциональный эндогенный ген ADAM6, и содержит белок (или эктопическую нуклеотидную последовательность, которая кодирует белок), который предоставляет мыши функциональность ADAM6. Согласно одному варианту осуществления мышь представляет собой самца мыши, и функциональность содержит усиленную фертильность по сравнению с мышью, которая не содержит функциональный эндогенный ген ADAM6.
Согласно одному варианту осуществления белок кодируется геномной последовательностью, расположенной в пределах локуса иммуноглобулина в зародышевой линии мыши. Согласно конкретному варианту осуществления локус иммуноглобулина представляет собой локус тяжелой цепи. Согласно другому конкретному варианту осуществления локус тяжелой цепи содержит по меньшей мере один генный сегмент VH человека, по меньшей мере один генный сегмент DH человека и по меньшей мере один генный сегмент JH человека. Согласно одному варианту осуществления эктопический белок кодируется геномной последовательностью, расположенной в пределах не относящегося к иммуноглобулину локуса в зародышевой линии мыши. Согласно одному варианту осуществления не относящийся к иммуноглобулину локус представляет собой транскрипционно активный локус. Согласно конкретному варианту осуществления транскрипционно активный локус представляет собой локус ROSA26. Согласно конкретному варианту осуществления транскрипционно активный локус ассоциирован с тканеспецифической экспрессией. Согласно одному варианту осуществления тканеспецифическая экспрессия присутствует в репродуктивных тканях. Согласно одному варианту осуществления белок кодируется геномной последовательностью, случайным образом вставленной в зародышевую линию мыши.
Согласно одному варианту осуществления мышь содержит относящуюся к человеку или химерную относящуюся к человеку/мыши или химерную относящуюся к человеку/крысе (например, относящуюся к человеку вариабельную, относящуюся к мыши или крысе константную) легкую цепь и химерную относящуюся к человеку вариабельную/относящуюся к мыши или крысе константную тяжелую цепь. Согласно конкретному варианту осуществления мышь содержит трансген, который содержит химерный ген относящейся к человеку вариабельной/относящейся к крысе или мыши константной легкой цепи, функционально связанный с транскрипционно активным промотором, например, промотором ROSA26. Согласно дополнительному конкретному варианту осуществления химерный трансген относящейся к человеку/мыши или крысы легкой цепи содержит реаранжированную последовательность вариабельной области легкой цепи человека в зародышевой линии мыши.
Согласно одному варианту осуществления эктопическая нуклеотидная последовательность расположена в пределах локуса иммуноглобулина в зародышевой линии мыши. Согласно конкретному варианту осуществления локус иммуноглобулина представляет собой локус тяжелой цепи. Согласно одному варианту осуществления локус тяжелой цепи содержит по меньшей мере один генный сегмент VH человека, по меньшей мере один генный сегмент DH человека и по меньшей мере один генный сегмент JH человека. Согласно одному варианту осуществления эктопическая нуклеотидная последовательность расположена в пределах не относящегося к иммуноглобулину локуса в зародышевой линии мыши. Согласно одному варианту осуществления не относящийся к иммуноглобулину локус представляет собой транскрипционно активный локус. Согласно конкретному варианту осуществления транскрипционно активный локус представляет собой локус ROSA26. Согласно одному варианту осуществления эктопическая нуклеотидная последовательность размещена в виде вставленной случайным образом в зародышевую линию мыши.
Согласно одному аспекту предусмотрена мышь, которая не содержит функциональный эндогенный ген ADAM6, причем мышь содержит эктопическую нуклеотидную последовательность, которая взаимодополняет потерю функции ADAM6 мыши. Согласно одному варианту осуществления эктопическая нуклеотидная последовательность предоставляет мыши способность производить потомство, которое является сопоставимым с таковым у соответствующей мыши дикого типа, которая содержит функциональный эндогенный ген ADAM6. Согласно одному варианту осуществления последовательность предоставляет мыши способность образовывать комплекса ADAM2 и/или ADAM3 и/или ADAM6 на поверхности сперматозоида мыши. Согласно одному варианту осуществления последовательность предоставляет сперматозоиду мыши способность проходить от матки мыши через яйцевод мыши к яйцеклетке мыши для оплодотворения яйцеклетки.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, производит по меньшей мере приблизительно 50%, 60%, 70%, 80% или 90% от числа пометов, которые производит мышь дикого типа мышь того же возраста и линии за шестимесячный период времени.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, производит больше по меньшей мере приблизительно в 1,5 раза, приблизительно в 2 раза, приблизительно в 2,5 раза, приблизительно в 3 раза, приблизительно в 4 раза, приблизительно в 6 раз, приблизительно в 7 раз, приблизительно в 8 раз или приблизительно в 10 раз или более потомства при разведении в течение шестимесячного периода времени, чем мышь такого же возраста и такой же или аналогичной линии, которая не содержит функциональный эндогенный ген ADAM6 и которая не содержит эктопическую нуклеотидную последовательность, которую разводят в течение по существу такого же периода времени и по существу при таких же условиях.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, производит в среднем по меньшей мере приблизительно в 2 раза, в 3 раза или в 4 раза большее число детенышей на помет за 4- или 6-месячный период разведения, чем мышь, которые не содержит функциональный эндогенный ген ADAM6 и которая не содержит эктопическую нуклеотидную последовательность, и которую разводят в течение такого же периода времени.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, представляет собой самца мыши, и самец мыши производит сперму, которая будучи извлеченной из яйцеводов приблизительно через 5-6 часов после копуляции, отражает миграцию в яйцеводе, которая больше по меньшей мере в 10 раз, по меньшей мере в 20 раз, по меньшей мере в 30 раз, по меньшей мере в 40 раз, по меньшей мере в 50 раз, по меньшей мере в 60 раз, по меньшей мере в 70 раз, по меньшей мере в 80 раз, по меньшей мере в 90 раз, в 100 раз, в 110 раз или в 120 раз или выше, чем у мыши, которая не содержит функциональный эндогенный ген ADAM6 и которая не содержит эктопическую нуклеотидную последовательность.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, при копуляции с самкой мыши образует сперму, которая способна к прохождению матки и попаданию и прохождению яйцевода в течение приблизительно 6 часов при результативности, которая приблизительно равна сперме мыши дикого типа.
Согласно одному варианту осуществления мышь, не содержащая функциональный эндогенный ген ADAM6 и содержащая эктопическую нуклеотидную последовательность, производит больше приблизительно в 1,5 раза, приблизительно в 2 раза, приблизительно в 3 раза или приблизительно в 4 раза или более пометов в сопоставимый период времени, чем мышь, которая не содержит функциональный ген ADAM6 и которая не содержит эктопическую нуклеотидную последовательность.
Согласно одному аспекту предусмотрена мышь, содержащая в своей зародышевой линии не относящуюся к мыши последовательность нуклеиновой кислоты, которая кодирует белок иммуноглобулина, причем не относящаяся к мыши последовательность иммуноглобулина содержит вставку гена ADAM6 мыши или его гомолога или ортолога или функционального фрагмента. Согласно одному варианту осуществления не относящаяся к мыши последовательность иммуноглобулина содержит последовательность иммуноглобулина человека. Согласно одному варианту осуществления последовательность содержит последовательность тяжелой цепи иммуноглобулина человека. Согласно одному варианту осуществления последовательность содержит последовательность легкой цепи иммуноглобулина человека. Согласно одному варианту осуществления последовательность содержит один или несколько генных сегментов V, один или несколько генных сегментов D и один или несколько генных сегментов J; согласно одному варианту осуществления последовательность содержит один или несколько генных сегментов V и один или несколько генных сегментов J. Согласно одному варианту осуществления один или несколько генных сегментов V, D и J или один или несколько генных сегментов V и J являются переаранжированными. Согласно одному варианту осуществления один или несколько генных сегментов V, D и J или один или несколько генных сегментов V и J являются реаранжированными. Согласно одному варианту осуществления после реаранжировки одного или нескольких генных сегментов V, D и J или одного или нескольких генных сегментов V и J мышь содержит в своем геноме по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую ген ADAM6 мыши или его гомолог или ортолог или функциональный фрагмент. Согласно одному варианту осуществления после реаранжировки мышь содержит в своем геноме по меньшей мере две последовательности нуклеиновой кислоты, кодирующие ген ADAM6 мыши или его гомолог или ортолог или функциональный фрагмент. Согласно одному варианту осуществления после реаранжировки мышь содержит в своем геноме по меньшей мере одну последовательность нуклеиновой кислоты, кодирующую ген ADAM6 мыши или его гомолог или ортолог или функциональный фрагмент. Согласно одному варианту осуществления мышь содержит ген ADAM6 или его гомолог или ортолог или функциональный фрагмент в В-клетке. Согласно одному варианту осуществления мышь содержит ген ADAM6 или его гомолог или ортолог или функциональный фрагмент в клетке, не относящейся к В-клетке.
Согласно одному аспекту предусмотрены мыши, которые экспрессируют вариабельную область тяжелой цепи иммуноглобулина человека или ее функциональный фрагмент из эндогенного локуса тяжелой цепи иммуноглобулина мыши, причем мыши содержат активность ADAM6, которая является функциональной у самца мыши.
Согласно одному варианту осуществления самцы мышей содержат один немодифицированный эндогенный аллель ADAM6 или его ортолог или гомолог или функциональный фрагмент на эндогенном локусе ADAM6.
Согласно одному варианту осуществления самцы мышей содержат эктопическую последовательность ADAM6 мыши или ее гомолог или ортолог или функциональный фрагмент, который кодирует белок, которые предоставляет функцию ADAM6.
Согласно одному варианту осуществления самцы мышей содержат последовательность ADAM6 или ее гомолог или ортолог или функциональный фрагмент в положении в геноме мыши, которое приблизительно соответствует положению эндогенного аллеля ADAM6 мыши, например, 3' по отношению к последовательности генного сегмента V и 5' по отношению к первому генному сегменту D.
Согласно одному варианту осуществления самцы мышей содержат последовательность ADAM6 или ее гомолог или ортолог или функциональный фрагмент, фланкированный выше, ниже или выше и ниже (относительно направления транскрипции последовательности ADAM6) последовательности нуклеиновой кислоты, кодирующей вариабельный генный сегмент иммуноглобулина. Согласно конкретному варианту осуществления вариабельный генный сегмент иммуноглобулина представляет собой генный сегмент человека. Согласно одному варианту осуществления вариабельный генный сегмент иммуноглобулина представляет собой генный сегмент человека, и последовательность, кодирующая ADAM6 мыши или его ортолог или гомолог или фрагмент, функциональный у мыши, находится между генными сегментами V человека; согласно одному варианту осуществления мышь содержит два или более генных сегментов V человека, и последовательность находится в положении между последним генным сегментом V и предпоследним генным сегментом V; согласно одному варианту осуществления последовательность находится в положении после последнего генного сегмента V и первого генного сегмента D.
Согласно одному варианту осуществления самцы мышей содержат последовательность ADAM6 или ее гомолог или ортолог или функциональный фрагмент, который расположен в положении в эндогенном локусе иммуноглобулина, которое является таким же или по существу таким же, как и у самца мыши дикого типа. Согласно конкретному варианту осуществления эндогенный локус является неспособным кодировать вариабельную область тяжелой цепи антитела, причем вариабельная область содержит или происходит из эндогенного не относящегося к человеку генного сегмента. Согласно конкретному варианту осуществления эндогенный локус размещен в положении в геноме самца мыши, которое делает его неспособным кодировать вариабельную область тяжелой цепи антитела. Согласно различным вариантам осуществления самцы мышей содержат последовательность ADAM6, расположенную на той же хромосоме, что и генные сегменты иммуноглобулина человека, и последовательность ADAM6 кодирует функциональный белок ADAM6.
Согласно одному аспекту предусмотрен самец мыши, который содержит нефункциональный эндогенный ген ADAM6 или делецию эндогенного гена ADAM6, в своей зародышевой линии; причем сперматозоиды мыши способны проходить яйцевод самки мыши и оплодотворять яйцеклетку.
Согласно одному аспекту предусмотрен самец мыши, который содержит функциональный эндогенный ген ADAM6 и модификацию эндогенного локуса иммуноглобулина тяжелой цепи. Согласно одному варианту осуществления модификацию производят ниже, или 3', по отношению к эндогенному гену ADAM6. Согласно одному варианту осуществления модификация представляет собой замещение одного или нескольких эндогенных генных сегментов тяжелой цепи иммуноглобулина одним или несколькими генными сегментами тяжелой цепи иммуноглобулина человека. Согласно одному варианту осуществления модификация представляет собой вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека выше эндогенного гена константной области тяжелой цепи иммуноглобулина.
Согласно одному аспекту предусмотрены мыши, которые содержат генетическую модификацию, которая снижает эндогенную функцию ADAM6 мыши, причем мышь содержит по меньшей мере некоторую функциональность ADAM6, обеспеченную либо эндогенным немодифицированным аллелем, который является функциональным полностью или частично (например, гетерозигота), либо экспрессией из эктопической последовательности, которая кодирует ADAM6 или его ортолог или гомолог или функциональный фрагмент, который является функциональным у самца мыши.
Согласно одному варианту осуществления мыши содержат функцию ADAM6, достаточную для предоставления самцам мышей способности производить потомство путем спаривания по сравнению с самцами мышей, у которых отсутствует функциональный ADAM6. Согласно одному варианту осуществления функция ADAM6 обеспечивается путем присутствия эктопической нуклеотидной последовательности, которая кодирует ADAM6 мыши или его гомолог или ортолог или функциональный фрагмент. Согласно одному варианту осуществления функция ADAM6 обеспечивается эндогенным геном ADAM6, присутствующим в эндогенном локусе иммуноглобулина, причем эндогенный локус иммуноглобулина является неспособным кодировать вариабельную область тяжелой цепи антитела. Гомологи или ортологи ADAM6 или его фрагменты, которые являются функциональными у самца мыши, включают в себя те, которые восстанавливают, полностью или частично, потерю способности производить потомство, наблюдаемую у самца мыши, у которого отсутствует достаточная эндогенная активность ADAM6 мыши, например, потеря способности, наблюдаемая у нокаутной в отношении ADAM6 мыши. В этом смысле нокаутные в отношении ADAM6 мыши включают в себя мышей, которые содержат эндогенный локус или его фрагмент, но который не является функциональным, т.е. который вообще не экспрессирует ADAM6 (ADAM6a и/или ADAM6b) или который экспрессирует ADAM6 (ADAM6a и/или ADAM6b) на уровне, недостаточном для поддержания по существу нормальной способности самца мыши дикого типа производить потомство. Потеря функции может быть обусловлена, например, модификацией в структурном гене локуса (т.е. в кодирующей области ADAM6a или ADAM6b) или в регуляторной области локуса (например, в последовательности 5' по отношению к гену ADAM6a или 3' по отношению к кодирующей области ADAM6a или ADAM6b, причем последовательность контролирует, полностью или частично, транскрипцию гена ADAM6, экспрессию РНК ADAM6 или экспрессию белка ADAM6). Согласно различным вариантам осуществления его ортологи или гомологи или фрагменты, которые являются функциональными у самца мыши, являются такими, которые позволяют сперме самца мыши (или большинству сперматозоидов в эякуляте самца мыши) проходить яйцевод мыши и оплодотворять яйцеклетку мыши.
Согласно одному варианту осуществления самцы мышей, которые экспрессируют вариабельную область иммуноглобулина человека или ее функциональный фрагмент, содержат достаточную активность ADAM6 для предоставления самцам мышей способности производить потомство путем спаривания с самками мышей и согласно одному варианту осуществления самцы мышей проявляют способность производить потомство при спаривании с самками мышей, которое согласно одному варианту осуществления составляет по меньшей мере 25%, согласно одному варианту осуществления по меньшей мере 30%, согласно одному варианту осуществления по меньшей мере 40%, согласно одному варианту осуществления по меньшей мере 50%, согласно одному варианту осуществления по меньшей мере 60%, согласно одному варианту осуществления по меньшей мере 70%, согласно одному варианту осуществления по меньшей мере 80%, согласно одному варианту осуществления по меньшей мере 90% и согласно одному варианту осуществления является приблизительно одинаковым по сравнению с потомством мышей с одним или двумя эндогенными немодифицированными аллелями ADAM6.
Согласно одному варианту осуществления самцы мышей экспрессируют достаточный ADAM6 (или его ортолог или гомолог или функциональный фрагмент) для предоставления сперматозоиду от самцов мышей возможности проходить яйцевод самки мыши и оплодотворять яйцеклетку мыши.
Согласно одному варианту осуществления функциональность ADAM6 обеспечивается последовательностью нуклеиновой кислоты, которая является смежной с хромосомной последовательностью мыши (например, нуклеиновая кислота случайным образом интегрирована в хромосому мыши; или помещена в конкретное положение, например, путем нацеливания нуклеиновой кислоты в конкретное положение, например, с помощью опосредованной сайт-специфической рекомбиназой (например, Cre-опосредованной) вставки или гомологичной рекомбинации). Согласно одному варианту осуществления последовательность ADAM6 присутствует на нуклеиновой кислоте, которая расположена отдельно от хромосомы мыши (например, последовательность ADAM6 присутствует на эписоме, т.е. внехромосомно, например, в конструкте экспрессии, векторе, YAC, трансхромосоме и т.д.).
Согласно одному аспекту предусмотрены генетически модифицированные мыши и клетки, которые содержат модификацию эндогенного локуса тяжелой цепи иммуноглобулина, причем мыши экспрессируют по меньшей мере часть последовательности тяжелой цепи иммуноглобулина, например, по меньшей мере часть последовательности человека, причем мыши содержат активность ADAM6, которая является функциональной у самца мыши. Согласно одному варианту осуществления модификация снижает или устраняет активность ADAM6 мыши. Согласно одному варианту осуществления мышь модифицирована так, что оба аллеля, которые кодируют активность ADAM6, либо отсутствуют, либо экспрессируют ADAM6, который по существу не функционирует для поддержания нормального спаривания у самца мыши. Согласно одному варианту осуществления мышь дополнительно содержит эктопическую последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши или его ортолог или гомолог или функциональный фрагмент. Согласно одному варианту осуществления модификация поддерживает активность ADAM6 мыши и делает эндогенный локус тяжелой цепи иммуноглобулина неспособным кодировать вариабельную область тяжелой цепи антитела. Согласно конкретному варианту осуществления модификация включает в себя хромосомные вставки и/или транслокации, которые делают эндогенные вариабельные генные сегменты тяжелой цепи иммуноглобулина неспособными к реаранжировке для кодирования вариабельной области тяжелой цепи антитела, которая является функционально связанной с константной областью тяжелой цепи.
Согласно одному аспекту предусмотрены генетически модифицированные мыши и клетки, которые содержат модификацию эндогенного локуса тяжелой цепи иммуноглобулина, причем модификация снижает или устраняет активность ADAM6, экспрессированную из последовательности ADAM6 локуса, и причем мыши содержат белок ADAM6 или его ортолог или гомолог или функциональный фрагмент. Согласно различным вариантам осуществления белок ADAM6 или его фрагмент кодируется эктопической последовательностью ADAM6. Согласно различным вариантам осуществления белок ADAM6 или его фрагмент экспрессируется из эндогенного аллеля ADAM6. Согласно различным вариантам осуществления мышь содержит первый аллель тяжелой цепи иммуноглобулина, который содержит первую модификацию, которая снижает или устраняет экспрессию функционального ADAM6 из первого аллеля тяжелой цепи иммуноглобулина, и мышь содержит второй аллель тяжелой цепи иммуноглобулина, который содержит вторую модификацию, которая по существу не снижает или не устраняет экспрессию функционального ADAM6 из второго аллеля тяжелой цепи иммуноглобулина.
Согласно различным вариантам осуществления модификация представляет собой вставку одного или нескольких генных сегментов тяжелой цепи иммуноглобулина человека выше, или 5', по отношению к эндогенному гену константной области тяжелой цепи иммуноглобулина. Согласно различным вариантам осуществления модификация поддерживает эндогенный ген ADAM6, расположенный на эндогенном локусе тяжелой цепи иммуноглобулина.
Согласно одному варианту осуществления вторая модификация расположена 3' (по отношению к направлению транскрипции генного сегмента V мыши) последнего генного сегмента V мыши и расположена 5' (по отношению к направлению транскрипции константной последовательности) относящегося к мыши (или химерного относящегося к человеку/мыши) константного гена тяжелой цепи иммуноглобулина или его фрагмента (например, последовательности нуклеиновой кислоты, кодирующей относящийся к человеку и/или относящийся к мыши: CH1 и/или шарнир и/или CH2 и/или CH3).
Согласно одному варианту осуществления модификация находится на первом аллеле тяжелой цепи иммуноглобулина на первом локусе, который кодирует первый аллель ADAM6, и функция ADAM6 является результатом экспрессии эндогенного ADAM6 на втором аллеле тяжелой цепи иммуноглобулина на втором локусе, который кодирует функциональный ADAM6, причем второй аллель тяжелой цепи иммуноглобулина содержит по меньшей мере одну модификацию генного сегмента V, D и/или J. Согласно конкретному варианту осуществления по меньшей мере одна модификация генного сегмента V, D и/или J представляет собой делецию, замещение генным сегментом V, D и/или J человека, замещение генным сегментом V, D и/или J верблюда, замещение гуманизированным или камелизированным генным сегментом V, D и/или J, замещение последовательности тяжелой цепи последовательностью легкой цепи и их комбинацию. Согласно одному варианту осуществления по меньшей мере одна модификация представляет собой делецию одного или нескольких генных сегментов V, D и/или J тяжелой цепи и замещение одного или нескольких генных сегментов V и/или J легкой цепи (например, генного сегмента V и/или J легкой цепи человека) на локусе тяжелой цепи.
Согласно одному варианту осуществления модификация находится на первом аллеле тяжелой цепи иммуноглобулина на первом локусе и втором аллеле тяжелой цепи иммуноглобулина на втором локусе, и функция ADAM6 является результатом экспрессии эктопического ADAM6 на не относящемся к иммуноглобулину локусе в зародышевой линии мыши. Согласно конкретному варианту осуществления не относящийся к иммуноглобулину локус представляет собой локус ROSA26. Согласно конкретному варианту осуществления не относящийся к иммуноглобулину локус является транскрипционно активным в репродуктивной ткани.
Согласно одному варианту осуществления модификация находится на первом аллеле тяжелой цепи иммуноглобулина на первом локусе и втором аллеле тяжелой цепи иммуноглобулина на втором локусе, и функция ADAM6 является результатом эндогенного гена ADAM6 в зародышевой линии мыши. Согласно конкретному варианту осуществления эндогенный ген ADAM6 находится рядом с генными сегментами иммуноглобулина мыши.
Согласно одному варианту осуществления модификация находится на первом аллеле тяжелой цепи иммуноглобулина на первом локусе и на втором аллеле тяжелой цепи иммуноглобулина на втором локусе, и функция ADAM6 является результатом экспрессии эктопической последовательности ADAM6 на первом аллеле тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления модификация находится на первом аллеле тяжелой цепи иммуноглобулина на первом локусе и на втором аллеле тяжелой цепи иммуноглобулина на втором локусе, и функция или активность ADAM6 является результатом экспрессии эктопического ADAM6 на втором аллеле тяжелой цепи иммуноглобулина.
Согласно одному аспекту предусмотрена мышь, содержащая гетерозиготный или гомозиготный нокаут ADAM6. Согласно одному варианту осуществления мышь дополнительно содержит модифицированную последовательность иммуноглобулина, которая представляет собой относящуюся к человеку или гуманизированную последовательность иммуноглобулина, или относящуюся к верблюду или камелизированную последовательность иммуноглобулина человека или мыши. Согласно одному варианту осуществления модифицированная последовательность иммуноглобулина присутствует на эндогенном локусе тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления модифицированная последовательность иммуноглобулина содержит последовательность вариабельного гена тяжелой цепи человека на эндогенном локусе тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления последовательность вариабельного гена тяжелой цепи человека замещает эндогенную вариабельную последовательность тяжелой цепи на эндогенном локусе тяжелой цепи иммуноглобулина.
Согласно одному аспекту предусмотрена мышь, неспособная к экспрессии функционального эндогенного ADAM6 мыши из эндогенного ADAM6 локуса мыши. Согласно одному варианту осуществления мышь содержит эктопическую последовательность нуклеиновой кислоты, которая кодирует ADAM6 или его функциональный фрагмент, который является функциональным у мыши. Согласно конкретному варианту осуществления эктопическая последовательность нуклеиновой кислоты кодирует белок, который восстанавливает потерю способности производить потомство, проявляемую самцом мыши, который является гомозиготным в отношении нокаута ADAM6. Согласно конкретному варианту осуществления эктопическая последовательность нуклеиновой кислоты кодирует белок ADAM6 мыши.
Согласно одному аспекту предусмотрена мышь, которая не содержит функциональный эндогенный локус ADAM6, и которая содержит эктопическую последовательность нуклеиновой кислоты, которая предоставляет мыши функцию ADAM6. Согласно одному варианту осуществления последовательность нуклеиновой кислоты содержит эндогенную последовательность ADAM6 мыши или ее функциональный фрагмент. Согласно одному варианту осуществления эндогенная последовательность ADAM6 мыши содержит кодирующую ADAM6a и ADAM6b последовательность, расположенную у мыши дикого типа между наиболее 3' генным сегментом V тяжелой цепи (VH) иммуноглобулина мыши и наиболее 5' генный сегмент D тяжелой цепи (DH) иммуноглобулина мыши.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты содержит последовательность, кодирующую ADAM6a мыши или ее функциональный фрагмент и/или последовательность, кодирующую ADAM6b мыши или ее функциональный фрагмент, причем ADAM6a и/или ADAM6b или их функциональный(е) фрагмент(ы) являе(ю)тся функционально связанным(и) с промотором. Согласно одному варианту осуществления промотор представляет собой промотор человека. Согласно одному варианту осуществления промотор представляет собой промотор ADAM6 мыши. Согласно конкретному варианту осуществления промотор ADAM6 содержит последовательность, расположенную между первым кодоном первого гена ADAM6, ближайшего к наиболее 5' генному сегменту DH мыши и сигнальной последовательностью рекомбинации наиболее 5' генного сегмента DH, причем направление 5' указано по отношению к направлению транскрипции генов иммуноглобулина мыши. Согласно одному варианту осуществления промотор представляет собой вирусный промотор. Согласно конкретному варианту осуществления вирусный промотор представляет собой промотор цитомегаловируса (CMV). Согласно одному варианту осуществления промотор представляет собой промотор убиквитина.
Согласно одному варианту осуществления промотор представляет собой индуцируемый промотор. Согласно одному варианту осуществления индуцируемый промотор регулирует экспрессию в нерепродуктивных тканях. Согласно одному варианту осуществления индуцируемый промотор регулирует экспрессию в репродуктивных тканях. Согласно конкретному варианту осуществления экспрессия последовательностей ADAM6a мыши и/или ADAM6b или их функционального(ых) фрагмента(ов) регулируется в зависимости от стадии развития индуцируемым промотором в репродуктивных тканях.
Согласно одному варианту осуществления ADAM6a мыши и/или ADAM6b выбраны из ADAM6a согласно SEQ ID NO: 1 и/или ADAM6b последовательности SEQ ID NO: 2. Согласно одному варианту осуществления промотор ADAM6 мыши представляет собой промотор согласно SEQ ID NO: 3. Согласно конкретному варианту осуществления промотор ADAM6 мыши содержит последовательность нуклеиновой кислоты согласно SEQ ID NO: 3 сразу выше (относительно направления транскрипции ADAM6a) первого кодона ADAM6a и продолжаясь до конца SEQ ID NO: 3 выше кодирующей области ADAM6. Согласно другому конкретному варианту осуществления промотор ADAM6 представляет собой фрагмент, продолжающийся от в пределах приблизительно 5 - приблизительно 20 нуклеотидов выше старт-кодона ADAM6a до приблизительно 0.5 т.п.н., 1 т.п.н., 2 т.п.н. или 3 т.п.н. или более выше старт-кодона ADAM6a.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты содержит SEQ ID NO: 3 или ее фрагмент, который, будучи помещенным в мышь, которая является стерильной или которая характеризуется низкой фертильностью вследствие отсутствия ADAM6, улучшает фертильность или восстанавливает фертильность приблизительно до фертильности дикого типа. Согласно одному варианту осуществления SEQ ID NO: 3 или ее фрагмент предоставляет самцу мыши способность производить сперматозоид, который способен проходить яйцевод самки мыши для оплодотворения яйцеклетки мыши.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты представляет собой любую последовательность, кодирующую ген ADAM6 или его гомолог или ортолог или функциональный фрагмент, который при введении и сохранении у мыши, дает уровень фертильности, который является таким же или сопоставимый с мышью дикого типа. Иллюстративный уровень фертильности может быть продемонстрирован способностью самца мыши производить сперматозоид, который способен проходить яйцевод самки мыши для оплодотворения яйцеклетки мыши.
Согласно одному аспекту предусмотрена мышь, которая содержит делецию эндогенной нуклеотидной последовательности, которая кодирует белок ADAM6, замещение эндогенного генного сегмента VH мыши генным сегментом VH человека и эктопическую нуклеотидную последовательность, которая кодирует белок ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному варианту осуществления мышь содержит локус тяжелой цепи иммуноглобулина, который содержит делецию эндогенной нуклеотидной последовательности локуса иммуноглобулина, которая содержит эндогенный ген ADAM6, содержит нуклеотидную последовательность, кодирующую один или несколько генных сегментов иммуноглобулина человека, и причем эктопическая нуклеотидная последовательность, кодирующая белок ADAM6 мыши находится в пределах или непосредственно прилегает к нуклеотидной последовательности, кодирующей один или несколько генных сегментов иммуноглобулина человека.
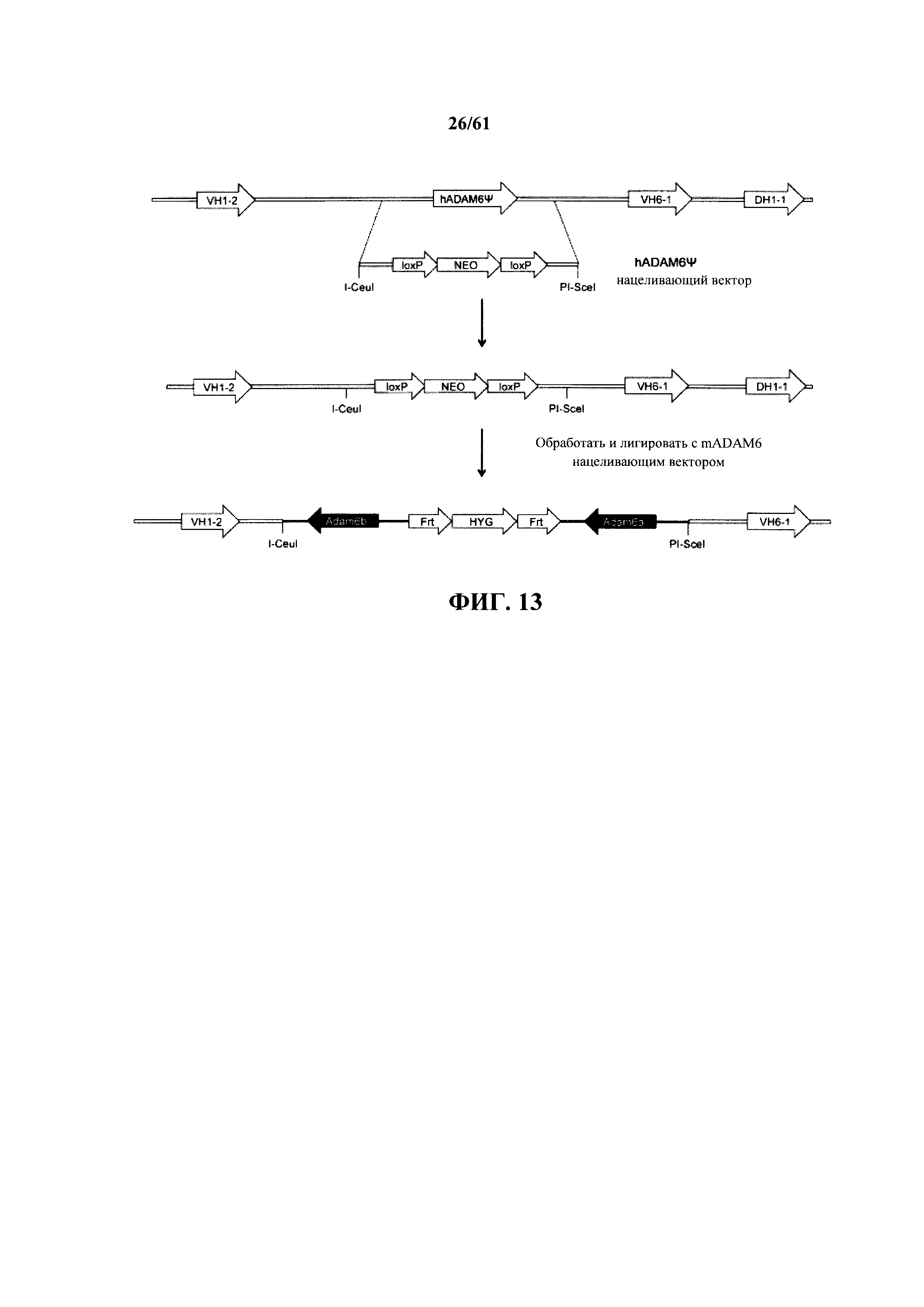
Согласно одному варианту осуществления мышь содержит замещение всех или по существу всех эндогенных генных сегментов VH нуклеотидной последовательностью, кодирующей один или несколько генных сегментов VH человека, и эктопическая нуклеотидная последовательность, кодирующая белок ADAM6 мыши, находится в пределах или непосредственно прилегает к нуклеотидной последовательности, кодирующей один или несколько генных сегментов VH человека. Согласно одному варианту осуществления мышь дополнительно содержит замещение одного или нескольких эндогенных генных сегментов DH одним или несколькими генными сегментами DH человека на эндогенном генном локусе DH. Согласно одному варианту осуществления мышь дополнительно содержит замещение одного или нескольких эндогенных генных сегментов JH одним или несколькими генными сегментами JH человека на эндогенном генном локусе JH. Согласно одному варианту осуществления мышь содержит замещение всех или по существу всех эндогенных генных сегментов VH, DH и JH и замещение на эндогенных генных локусах VH, DH и JH генными сегментами VH, DH и JH человека, причем мышь содержит эктопическую последовательность, кодирующую белок ADAM6 мыши. Согласно одному варианту осуществления мышь содержит вставку генных сегментов VH, DH и JH человека на эндогенном локусе тяжелой цепи иммуноглобулина, причем мышь содержит ген ADAM6, который является функциональным у мыши. Согласно конкретному варианту осуществления эктопическая последовательность, кодирующая мышь белок ADAM6, расположена между предпоследним наиболее 3' генным сегментом VH из присутствующих генных сегментов VH человека и последним 3' генным сегментом VH из присутствующих генных сегментов VH человека. Согласно конкретному варианту осуществления мышь содержит делецию всех или по существу всех генных сегментов VH мыши и замещение всеми или по существу всеми генными сегментами VH человека, и эктопическая нуклеотидная последовательность, кодирующая мышь белок ADAM6, расположена ниже генного сегмента VH1-2 человека и выше генного сегмента VH6-1 человека.
Согласно конкретному варианту осуществления мышь содержит замещение всех или по существу всех эндогенных генных сегментов VH нуклеотидной последовательностью, кодирующей один или несколько генных сегментов VH человека, и эктопическая нуклеотидная последовательность, кодирующая белок ADAM6 мыши, находится в пределах или непосредственно прилегает к нуклеотидной последовательности, кодирующей один или несколько генных сегментов VH человека.
Согласно одному варианту осуществления эктопическая нуклеотидная последовательность, которая кодирует мышь белок ADAM6, присутствует на трансгене в геноме мыши. Согласно одному варианту осуществления эктопическая нуклеотидная последовательность, которая кодирует белок ADAM6 мыши, присутствует внехромосомно у мыши.
Согласно одному аспекту предусмотрена мышь, которая содержит модификацию эндогенного локуса тяжелой цепи иммуноглобулина, причем мышь экспрессирует В-клетку, которая содержит реаранжированную последовательность иммуноглобулина, функционально связанную с последовательностью гена константной области тяжелой цепи, и В-клетка содержит в своем геноме (например, на хромосоме В-клетки) ген, кодирующий ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши. Согласно одному варианту осуществления реаранжированная последовательность иммуноглобулина, функционально связанная с последовательностью гена константной области тяжелой цепи, содержит последовательность V, D и/или J тяжелой цепи человека; последовательность V, D и/или J тяжелой цепи мыши; последовательность V и/или J легкой цепи человека или мыши. Согласно одному варианту осуществления последовательность гена константной области тяжелой цепи содержит последовательность тяжелой цепи человека или мыши, выбранную из группы, состоящей из CH1, шарнира, CH2, CH3 и их комбинации.
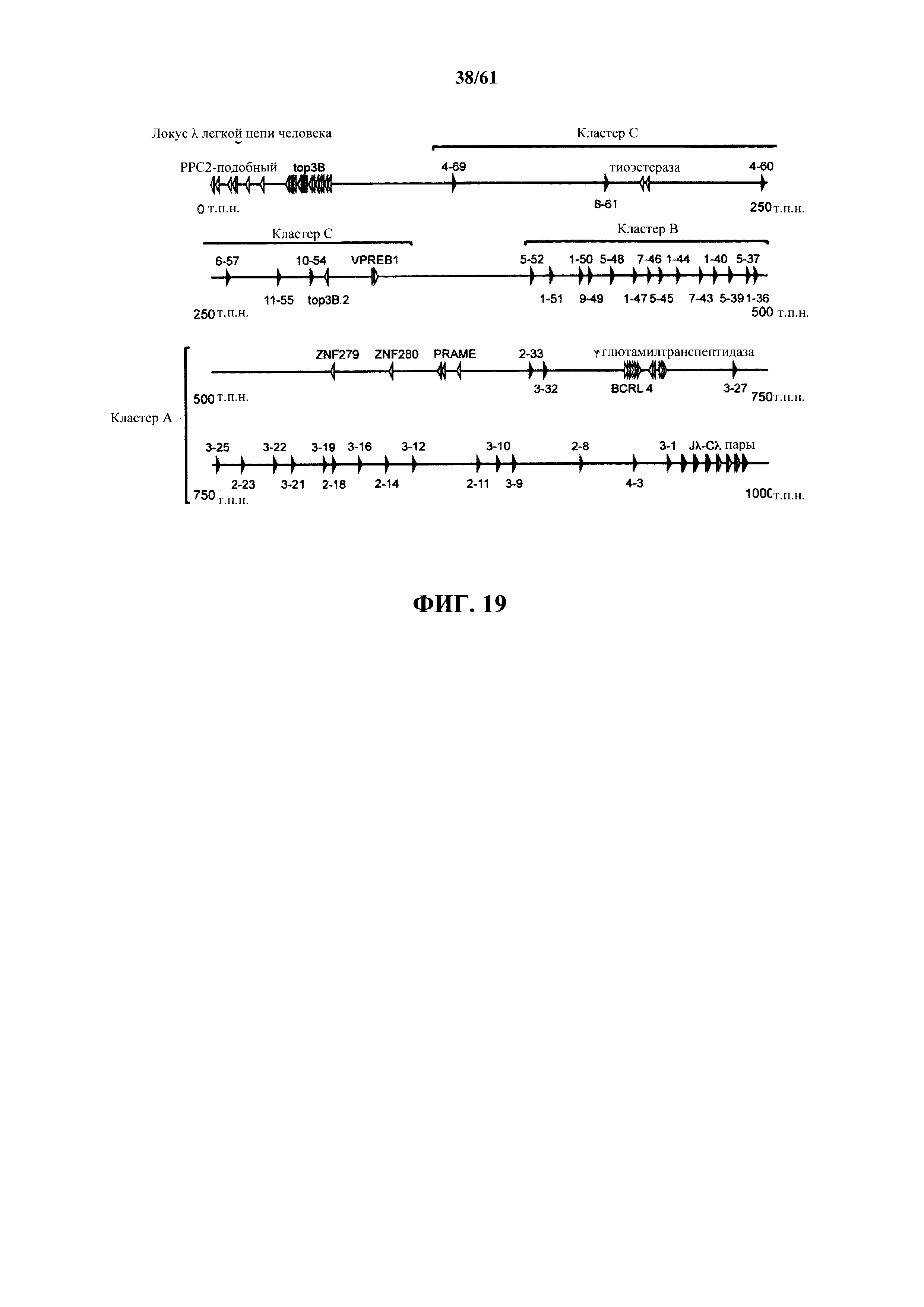
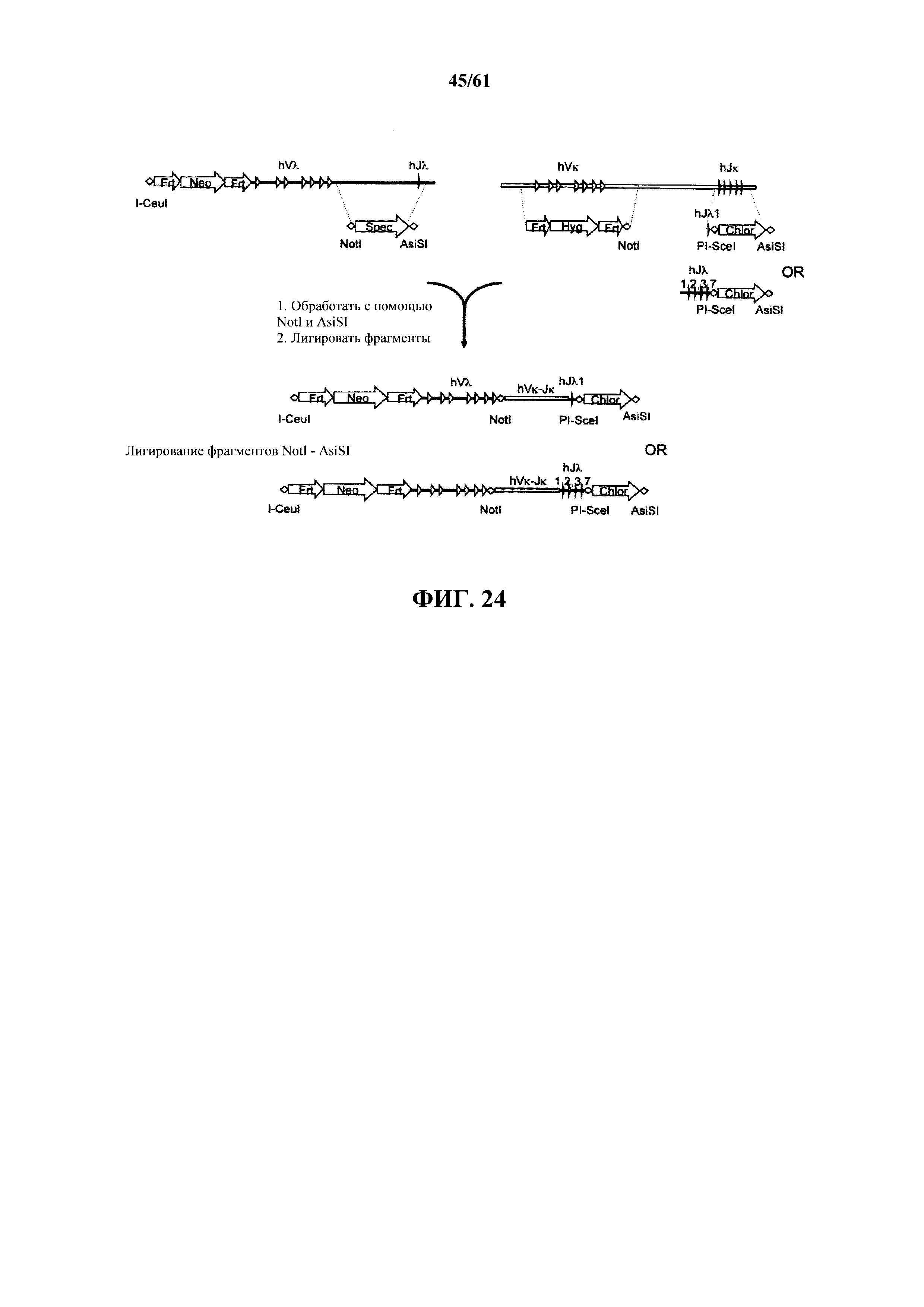
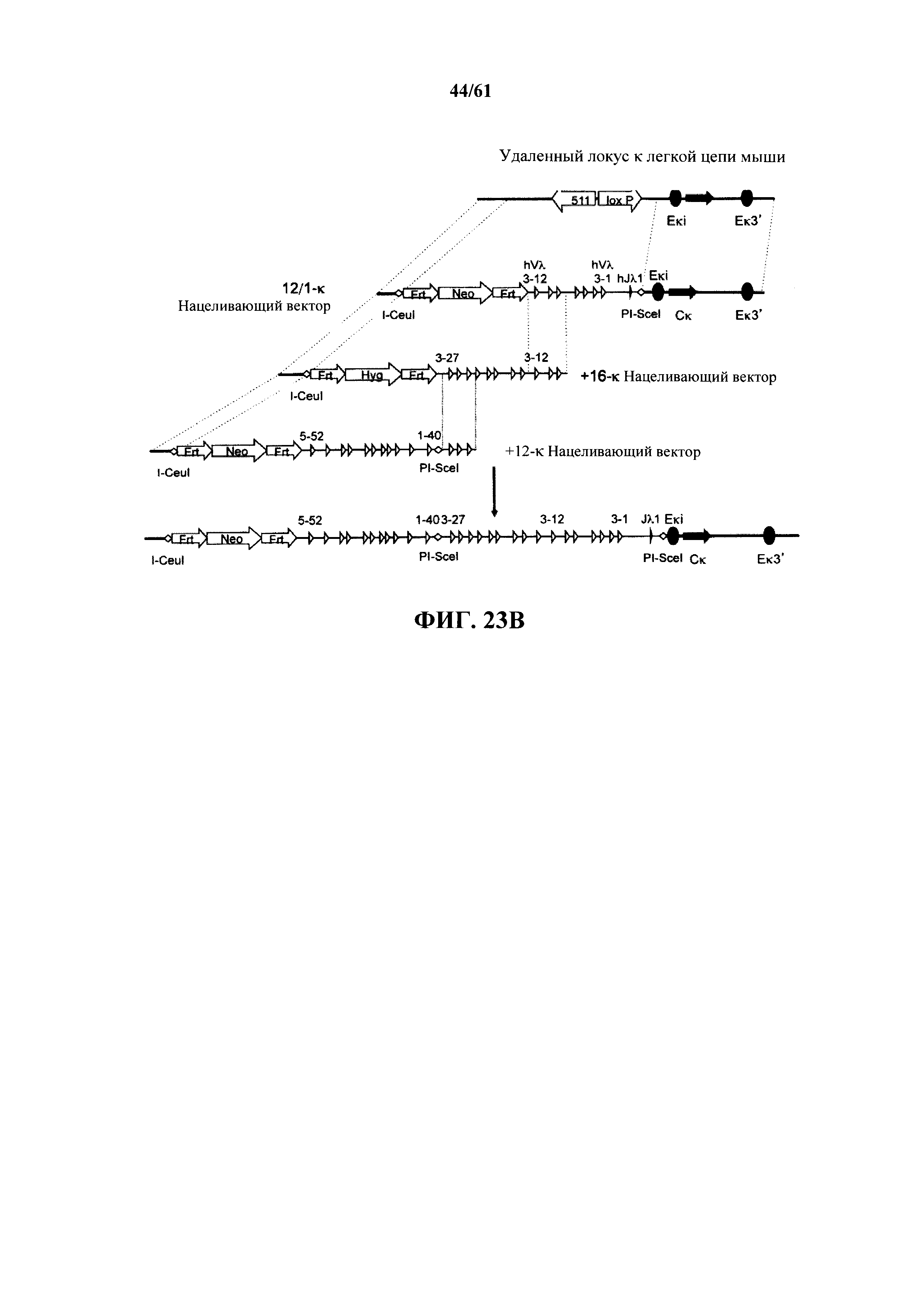
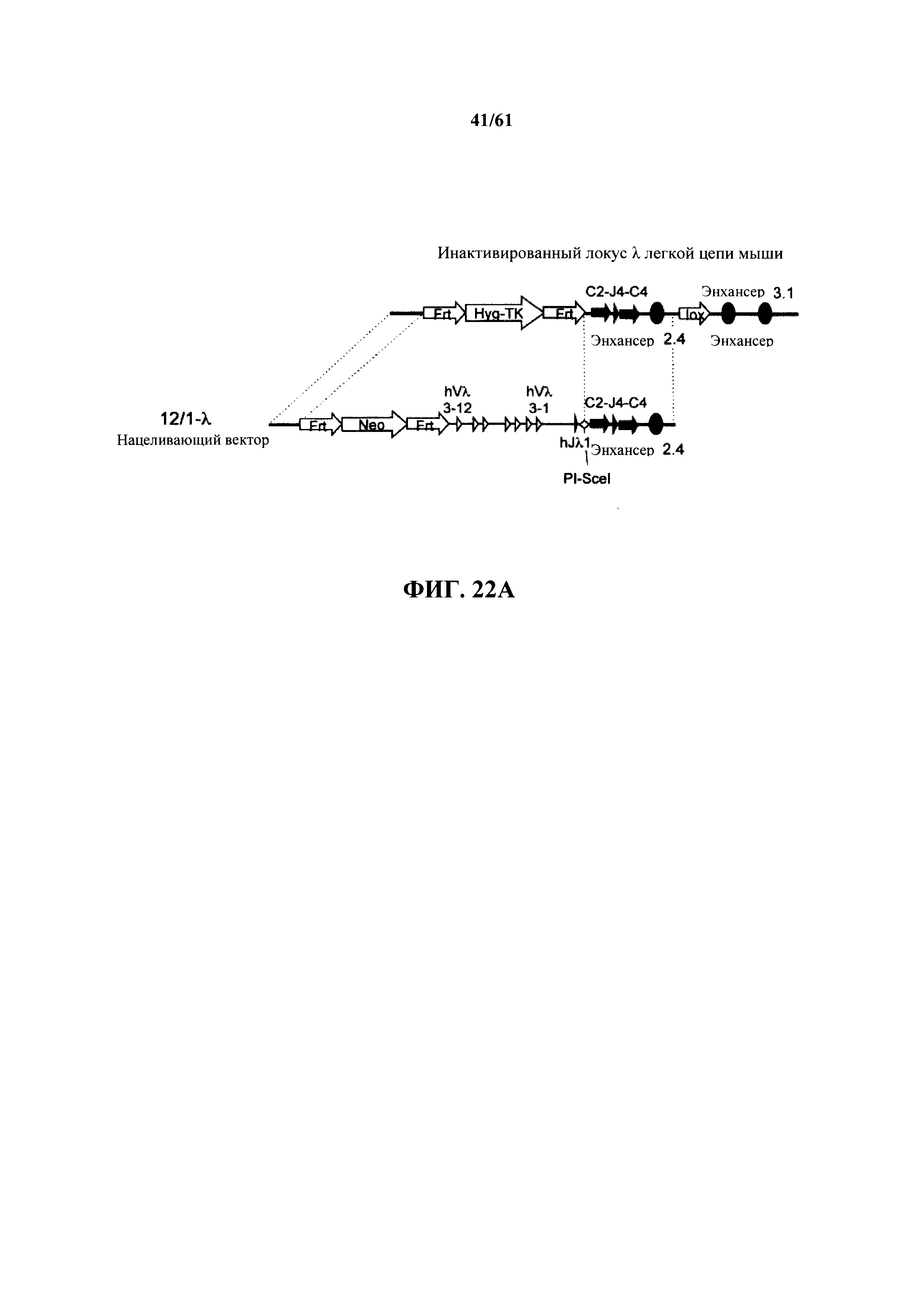
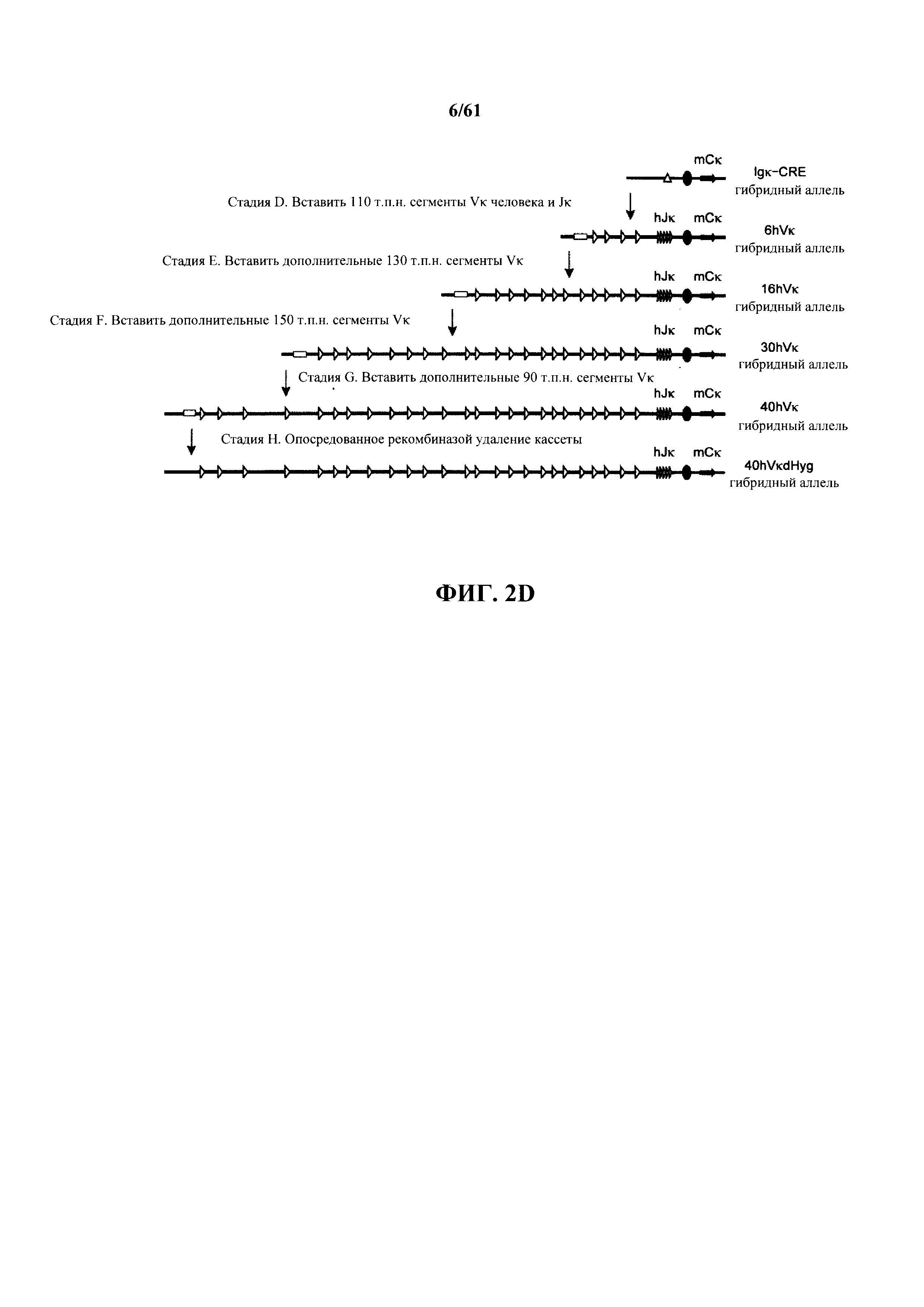
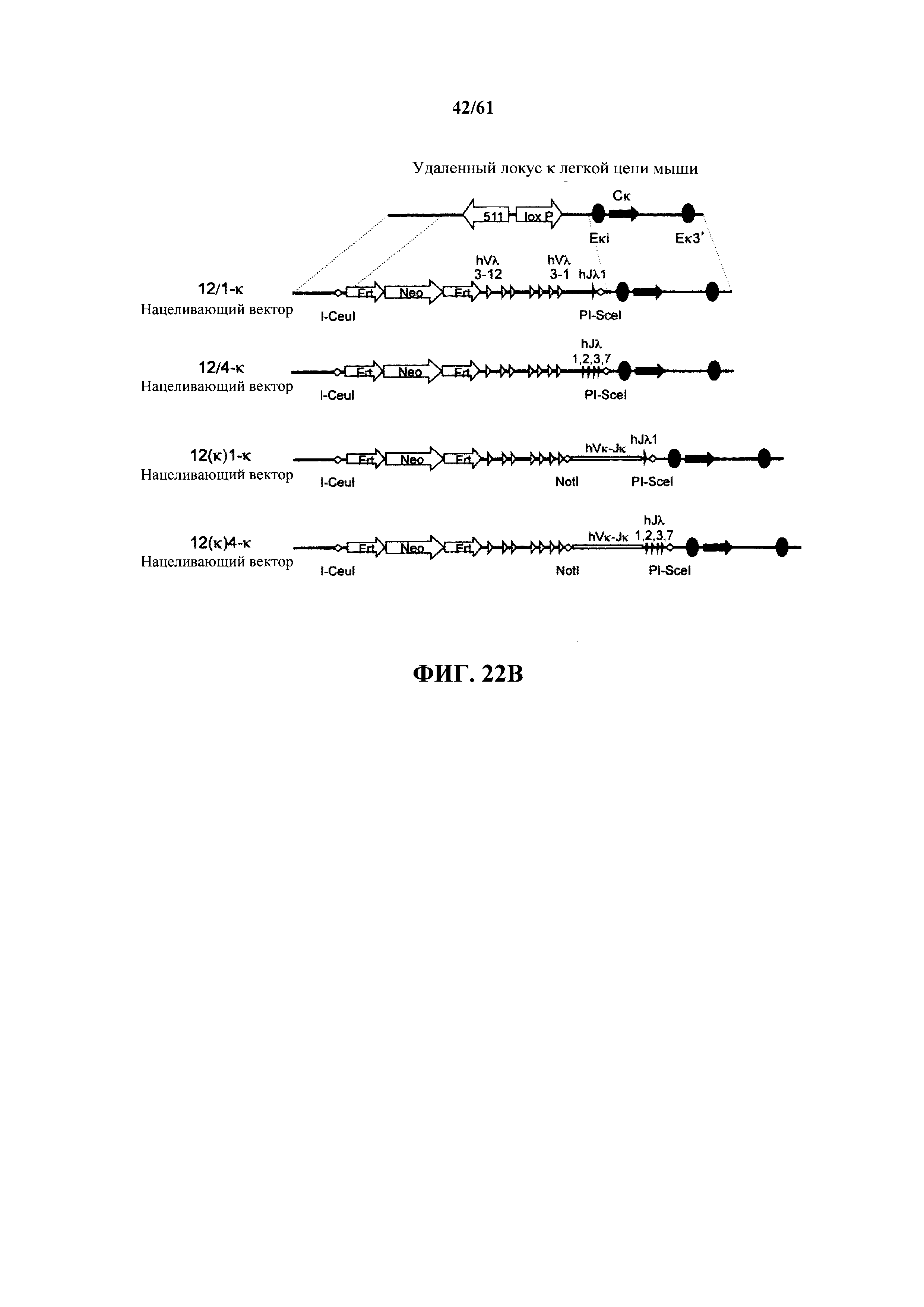
Согласно одному аспекту предусмотрена мышь, которая содержит функционально выключенный эндогенный вариабельный генный локус тяжелой цепи иммуноглобулина, причем функция ADAM6 поддерживается у мыши, и дополнительно содержит вставку одного или нескольких генных сегментов иммуноглобулина человека выше или 5' от одного или нескольких константных областей тяжелой цепи мыши. Согласно одному варианту осуществления один или несколько генных сегментов иммуноглобулина человека включают в себя один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека. Согласно конкретному варианту осуществления мышь дополнительно содержит функционально выключенный эндогенный локус легкой цепи, причем мышь содержит активность ADAM6, которая является такой же или сопоставимой с мышью дикого типа, и дополнительно содержит вставку одного или нескольких генных сегментов λ легкой цепи человека выше или 5' от константной области легкой цепи мыши. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержат 12 генных сегментов Vλ человека и один или несколько генных сегментов Jλ человека. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержат 12 генных сегментов Vλ человека и четыре генных сегмента Jλ человека. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержат 28 генных сегментов Vλ человека и один или несколько генных сегментов Jλ человека. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержит 28 генных сегментов Vλ человека и четыре генных сегмента Jλ человека. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержит 40 генных сегментов Vλ человека и один или несколько генных сегментов Jλ человека. Согласно одному варианту осуществления генные сегменты λ легкой цепи человека содержат 40 генных сегментов Vλ человека и четыре генных сегмента Jλ человека. Согласно различным вариантам осуществления четыре генных сегмента Jλ человека включают в себя Jλ1, Jλ2, Jλ3 и Jλ7. Согласно различным вариантам осуществления константная область легкой цепи мыши представляет собой Сκ мыши или Сλ мыши.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит функционально выключенный ген легкой цепи иммуноглобулина, и дополнительно содержит замещение одного или нескольких эндогенных генных сегментов вариабельная область тяжелой цепи иммуноглобулина одним или несколькими генными сегментами вариабельной области тяжелой цепи иммуноглобулина человека, причем мышь не содержит функциональный эндогенный локус ADAM6, и причем мышь содержит эктопическую нуклеотидную последовательность, которая экспрессирует белок ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному аспекту предусмотрена мышь, которая не содержит функциональный эндогенный локус или последовательность ADAM6 мыши и которая содержит эктопическую нуклеотидную последовательность, кодирующую локус ADAM6 мыши или функциональный фрагмент локуса или последовательности ADAM6 мыши, причем мышь способна спариваться с мышью противоположного пола, чтобы производить потомство, которое содержит эктопический локус или последовательность ADAM6. Согласно одному варианту осуществления мышь представляет собой самца. Согласно одному варианту осуществления мышь представляет собой самку.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит генный сегмент вариабельной области тяжелой цепи иммуноглобулина человека на эндогенном генном локусе вариабельной области тяжелой цепи иммуноглобулина мыши, мышь не содержит эндогенную функциональную последовательность ADAM6 на эндогенном генном локусе вариабельной области тяжелой цепи иммуноглобулина мыши, и причем мышь содержит эктопическую нуклеотидную последовательность, которая экспрессирует белок ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному варианту осуществления эктопическая нуклеотидная последовательность, которая экспрессирует белок ADAM6 мыши, является внехромосомной. Согласно одному варианту осуществления эктопическая нуклеотидная последовательность, которая экспрессирует белок ADAM6 мыши, интегрирована на одном или нескольких локусах в геноме мыши. Согласно конкретному варианту осуществления один или несколько локусов включают в себя локус иммуноглобулина.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует последовательность тяжелой цепи иммуноглобулина из модифицированного эндогенного локуса тяжелой цепи иммуноглобулина мыши, причем тяжелая цепь происходит из генного сегмента V человека, генного сегмента D человека и генного сегмента J человека, причем мышь содержит активность ADAM6, которая является функциональной у мыши.
Согласно одному варианту осуществления мышь содержит множество генных сегментов V человека, множество генных сегментов D и множество генных сегментов J. Согласно одному варианту осуществления генные сегменты D представляют собой генные сегменты D человека. Согласно одному варианту осуществления генные сегменты J представляют собой генные сегменты J человека. Согласно одному варианту осуществления мышь дополнительно содержит гуманизированную последовательность константной области тяжелой цепи, причем гуманизация предусматривает замещение последовательности, выбранной из CH1, шарнира, CH2, CH3 и их комбинации. Согласно конкретному варианту осуществления тяжелая цепь происходит из генного сегмента V человека, генного сегмента D человека, генного сегмента J человека, последовательности CH1 человека, шарнирной последовательности человека или мыши, последовательность CH2 мыши и последовательности CH3 мыши. Согласно другому конкретному варианту осуществления мышь дополнительно содержит константную последовательность легкой цепи человека.
Согласно одному варианту осуществления мышь содержит ген ADAM6, который фланкирован 5' и 3' эндогенными генными сегментами тяжелой цепи иммуноглобулина. Согласно конкретному варианту осуществления эндогенные генные сегменты тяжелой цепи иммуноглобулина являются неспособными кодировать тяжелую цепь антитела. Согласно конкретному варианту осуществления ген ADAM6 мыши находится в положении, которое является таким же, как и у мыши дикого типа, и эндогенные вариабельные генные локусы тяжелой цепи иммуноглобулина мыши являются неспособными к реаранжировке, чтобы кодировать тяжелую цепь антитела.
Согласно одному варианту осуществления генный сегмент V фланкирован 5' (относительно направления транскрипции генного сегмента V) последовательностью, кодирующей активность ADAM6, которая является функциональной у мыши.
Согласно одному варианту осуществления генный сегмент V фланкирован 3' (относительно направления транскрипции генного сегмента V) последовательностью, кодирующей активность ADAM6, которая является функциональной у мыши.
Согласно одному варианту осуществления генный сегмент D фланкирован 5' (относительно направления транскрипции генного сегмента D) последовательностью, кодирующей активность ADAM6, которая является функциональной у мыши.
Согласно одному варианту осуществления активность ADAM6, которая является функциональной у мыши, является результатом экспрессии нуклеотидной последовательности, расположенной 5' по отношению к наиболее 5' генному сегменту D и 3' по отношению к наиболее 3' генному сегменту V (относительно направления транскрипции генного сегмента V) модифицированного эндогенного локуса тяжелой цепи иммуноглобулина мыши.
Согласно одному варианту осуществления активность ADAM6, которая является функциональной у мыши, является результатом экспрессия нуклеотидной последовательности, расположенной между двумя генными сегментами V человека в модифицированном эндогенном локусе тяжелой цепи иммуноглобулина мыши. Согласно одному варианту осуществления два генных сегмента V человека представляют собой генный сегмент VH1-2 человека и генный сегмент VH6-1 человека.
Согласно одному варианту осуществления нуклеотидная последовательность содержит последовательность, выбранную из последовательности ADAM6b мыши или ее функционального фрагмента, последовательности ADAM6a мыши или ее функционального фрагмента и их комбинации.
Согласно одному варианту осуществления нуклеотидная последовательность между двумя генными сегментами V человека расположена в противоположной ориентации транскрипции по отношению к генным сегментам V человека. Согласно конкретному варианту осуществления нуклеотидная последовательность кодирует, в направлении 5'-3' относительно направления транскрипции генов ADAM6, и за последовательностью ADAM6a следует последовательность ADAM6b.
Согласно одному варианту осуществления мышь содержит замещение последовательности псевдогена ADAM6 человека между V генными сегментами VH1-2 и VH6-1 человека последовательностью ADAM6 мыши или ее функциональным фрагментом.
Согласно одному варианту осуществления последовательность, кодирующая активность ADAM6, которая является функциональной у мыши, представляет собой последовательность ADAM6 мыши или ее функциональный фрагмент.
Согласно одному варианту осуществления мышь содержит эндогенный генный сегмент DFL16.1 мыши (например, у мыши, гетерозиготной в отношении модифицированного эндогенного локуса тяжелой цепи иммуноглобулина мыши) или генный сегмент DH1-1 человека. Согласно одному варианту осуществления генный сегмент D тяжелой цепи иммуноглобулина, экспрессированной мышью, происходит из эндогенного генного сегмента DFL16.1 мыши или генного сегмента DH1-1 человека.
Согласно одному аспекту предусмотрена мышь, которая содержит последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) в содержащей ДНК клетке нереаранжированной В-клеточной линии, но не содержит последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) в В-клетке, которая содержат реаранжированные локусы иммуноглобулина, причем последовательность нуклеиновой кислоты, кодирующая ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) находится в геноме в положении, которое отличается от положения, в котором ген ADAM6 мыши встречается у мыши дикого типа. Согласно одному варианту осуществления последовательность нуклеиновой кислоты, кодирующая ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент), присутствует во всех или по существу всех содержащих ДНК клетках, которые не происходят из реаранжированной В-клеточной линии; согласно одному варианту осуществления последовательность нуклеиновой кислоты присутствует в зародышевых клетках мыши, но не в хромосоме реаранжированной В-клетки.
Согласно одному аспекту предусмотрена мышь, которая содержит последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент), во всех или по существу всех содержащих ДНК клетках, включая в себя В-клетки, которые содержат реаранжированные локусы иммуноглобулина, причем последовательность нуклеиновой кислоты, кодирующая ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) находится в геноме в положении, которое отличается от положения, в котором ген ADAM6 мыши встречается у мыши дикого типа. Согласно одному варианту осуществления последовательность нуклеиновой кислоты, кодирующая ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент), находится на нуклеиновой кислоте, которая является смежной с реаранжированным локусом иммуноглобулина. Согласно одному варианту осуществления нуклеиновая кислота, которая является смежной с реаранжированным локусом иммуноглобулина, представляет собой хромосому. Согласно одному варианту осуществления хромосома представляет собой хромосому, которая встречается у мыши дикого типа, и хромосома содержит модификацию локуса иммуноглобулина мыши.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит В-клетку, которая содержит в своем геноме последовательность ADAM6 или ее ортолог или гомолог. Согласно одному варианту осуществления последовательность ADAM6 или ее ортолог или гомолог находится на локусе тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления последовательность ADAM6 или ее ортолог или гомолог находится на локусе, который не является локусом иммуноглобулина. Согласно одному варианту осуществления последовательность ADAM6 находится на трансгене, которым управляет гетерологичный промотор. Согласно конкретному варианту осуществления гетерологичный промотор представляет собой не относящийся к иммуноглобулину промотор. Согласно конкретному варианту осуществления В-клетка экспрессирует белок ADAM6 или его ортолог или гомолог.
Согласно одному варианту осуществления 90% или более В-клеток мыши содержат ген, кодирующий белок ADAM6 или его ортолог или его гомолог или его фрагмент, который является функциональной у мыши. Согласно конкретному варианту осуществления мышь представляет собой самца мыши.
Согласно одному варианту осуществления геном В-клетки содержит первый аллель и второй аллель, содержащий последовательность ADAM6 или ее ортолог или гомолог. Согласно одному варианту осуществления геном В-клетки содержит первый аллель, но не второй аллель, содержащий последовательность ADAM6 или ее ортолог или гомолог.
Согласно одному аспекту предусмотрена мышь, которая содержит модификацию на одном или нескольких эндогенных аллелей тяжелой цепи иммуноглобулина, причем модификация сохраняет один или несколько эндогенных аллелей ADAM6, и мышь дополнительно содержит вставку одного или нескольких генных сегментов Vλ человека и одного или нескольких генных сегментов Jλ человека выше константной области легкой цепи мыши. Согласно различным вариантам осуществления константная область легкой цепи мыши представляет собой Сκ мыши или Сλ мыши.
Согласно одному варианту осуществления модификация делает мышь неспособной экспрессировать функциональную тяжелую цепь, которая содержит реаранжированные эндогенные генные сегменты тяжелой цепи по меньшей мере из одного аллеля тяжелой цепи и сохраняет эндогенный аллель ADAM6, расположенный в пределах по меньшей мере одного эндогенного аллеля тяжелой цепи иммуноглобулина.
Согласно одному варианту осуществления мыши являются неспособными экспрессировать функциональную тяжелую цепь, которая содержит реаранжированные эндогенные генные сегменты тяжелой цепи по меньшей мере из одного из эндогенных аллелей тяжелой цепи иммуноглобулина, и мыши экспрессируют белок ADAM6 из эндогенного аллеля ADAM6. Согласно конкретному варианту осуществления мыши являются неспособными экспрессировать функциональную тяжелую цепь, которая содержит реаранжированные эндогенные генные сегменты тяжелой цепи из двух эндогенных аллелей тяжелой цепи иммуноглобулина, и мыши экспрессируют белок ADAM6 из одного или нескольких эндогенных аллелей ADAM6.
Согласно одному варианту осуществления мыши являются неспособными экспрессировать функциональную тяжелую цепь из каждого эндогенного аллеля тяжелой цепи, и мыши содержат функциональный аллель ADAM6, расположенный в пределах 1, 2, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110 или 120 или более миллионов пар нуклеотидов выше (относительно направления транскрипции локуса тяжелой цепи мыши) последовательности константной области тяжелой цепи иммуноглобулина мыши. Согласно конкретному варианту осуществления функциональный аллель ADAM6 находится на эндогенном локусе тяжелой цепи иммуноглобулина (например, в межгенной V-D области, между двумя генными сегментами V, между генным сегментом V и D, между генным сегментом D и J и т.д.). Согласно конкретному варианту осуществления функциональный аллель ADAM6 расположен в пределах 90-100 т.п.н. межгенной последовательности между последним генным сегментом V мыши и первым генным сегментом D мыши.
Согласно одному аспекту предусмотрена мышь, которая содержит модификацию на одном или нескольких эндогенных аллелях ADAM6.
Согласно одному варианту осуществления модификация делает мышь неспособной экспрессировать функциональный белок ADAM6 по меньшей мере из одного из одного или нескольких эндогенных аллелей ADAM6. Согласно конкретному варианту осуществления мышь является неспособной экспрессировать функциональный белок ADAM6 из каждого из эндогенных аллелей ADAM6.
Согласно одному варианту осуществления мыши являются неспособными экспрессировать функциональный белок ADAM6 из каждого эндогенного аллеля ADAM6, и мыши содержат эктопическую последовательность ADAM6.
Согласно одному варианту осуществления мыши являются неспособными экспрессировать функциональный белок ADAM6 из каждого эндогенного аллеля ADAM6, и мыши содержат эктопическую последовательность ADAM6, расположенную в пределах 1, 2, 3, 4, 5, 10, 20, 30, 40, 50, 60, 70, 80, 90, 100, 110 или 120 или более т.п.н. выше (относительно направления транскрипции локуса тяжелой цепи мыши) последовательности константной области тяжелой цепи иммуноглобулина мыши. Согласно конкретному варианту осуществления эктопическая последовательность ADAM6 находится на эндогенном локусе тяжелой цепи (например, в межгенной области V-D, между двумя генными сегментами V, между генным сегментом V и D, между генным сегментом D и J и т.д.). Согласно конкретному варианту осуществления эктопическая последовательность ADAM6 расположена в пределах 90-100 т.п.н. межгенной последовательности между последним генным сегментом V мыши и первым генным сегментом D мыши. Согласно другому конкретному варианту осуществления эндогенную 90-100 т.п.н. межгенную последовательность V-D удаляют, и эктопическая последовательность ADAM6 расположена между последним генным сегментом V и первым генным сегментом D.
Согласно одному аспекту предусмотрен стерильный самец мыши, причем мышь содержит делецию двух или более эндогенных аллелей ADAM6. Согласно одному аспекту предусмотрена самка мыши, которая представляет собой носителя признака мужской стерильности, причем самка мыши содержит в своей зародышевой линии нефункциональный аллель ADAM6 или нокаут эндогенного аллеля ADAM6.
Согласно одному аспекту предусмотрена мышь, содержащая эндогенный генный сегмент V, D и/или J тяжелой цепи иммуноглобулина, который является неспособным к реаранжировке, чтобы кодировать тяжелую цепь антитела, причем большинство В-клеток мыши содержат функциональный ген ADAM6. Согласно различным вариантам осуществления большинство В-клеток мыши дополнительно содержат один или несколько генных сегментов Vλ человека и один или несколько генных сегментов Jλ человека выше константной области легкой цепи иммуноглобулина мыши. Согласно одному варианту осуществления константная область легкой цепи иммуноглобулина мыши выбрана из Сκ мыши или Cλ мыши.
Согласно одному варианту осуществления мышь содержит интактные эндогенные генные сегменты V, D и J тяжелой цепи иммуноглобулина, которые являются неспособными к реаранжировке, чтобы кодировать функциональную тяжелую цепь антитела. Согласно одному варианту осуществления мышь содержит по меньшей мере один и до 89 генных сегментов V, по меньшей мере один и до 13 генных сегментов D, по меньшей мере один и до четырех генных сегментов J и их комбинацию; причем по меньшей мере один и до 89 генных сегментов V, по меньшей мере один и до 13 генных сегментов D, по меньшей мере один и до четырех генных сегментов J являются неспособными к реаранжировке, чтобы кодировать вариабельную область тяжелой цепи антитела. Согласно конкретному варианту осуществления мышь содержит функциональный ген ADAM6, расположенный в пределах интактных эндогенных генных сегментов V, D и J тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления мышь содержит эндогенный локус тяжелой цепи, который включает в себя эндогенный локус ADAM6, причем эндогенный локус тяжелой цепи содержит 89 генных сегментов V, 13 генных сегментов D и четыре генных сегмента J, причем эндогенные генные сегменты тяжелой цепи являются неспособными к реаранжировке, чтобы кодировать вариабельную область тяжелой цепи антитела, и локус ADAM6 кодирует белок ADAM6, который является функциональным у мыши.
Согласно одному аспекту предусмотрена мышь, которая не содержит эндогенный генный сегмент V, D и J тяжелой цепи иммуноглобулина, причем большинство В-клеток мыши содержат последовательность ADAM6 или ее ортолог или гомолог. Согласно одному варианту осуществления большинство В-клеток мыши экспрессируют легкую цепь иммуноглобулина, содержащую лямбда вариабельный домен человека и эндогенную константную область легкой цепи иммуноглобулина.
Согласно одному варианту осуществления мышь не содержит эндогенные генные сегменты тяжелой цепи иммуноглобулина, выбранные из двух или более генных сегментов V, двух или более генных сегментов D, двух или более генных сегментов J и их комбинации. Согласно одному варианту осуществления мышь не содержит генные сегменты тяжелой цепи иммуноглобулина, выбранные по меньшей мере из одного и до 89 генных сегментов V, по меньшей мере одного и до 13 генных сегментов D, по меньшей мере одного и до четырех генных сегментов J и их комбинации. Согласно одному варианту осуществления мышь не содержит геномный фрагмент ДНК из хромосомы 12, содержащей приблизительно три миллиона пар нуклеотидов эндогенного локуса тяжелой цепи иммуноглобулина. Согласно конкретному варианту осуществления мышь не содержит все функциональные эндогенные генные сегменты V, D и J тяжелой цепи. Согласно конкретному варианту осуществления мышь не содержит 89 генных сегментов VH, 13 генных сегментов DH и четыре генных сегмента JH.
Согласно одному аспекту предусмотрена мышь, причем мышь содержит геном в зародышевой линии, содержащий модификацию локуса тяжелой цепи иммуноглобулина, причем модификация локуса тяжелой цепи иммуноглобулина содержит замещение одной или нескольких последовательностей вариабельной области иммуноглобулина мыши одной или несколькими не относящимися к мыши последовательностями вариабельной области иммуноглобулина, и причем мышь содержит последовательность нуклеиновой кислоты, кодирующую белок ADAM6 мыши. Согласно предпочтительному варианту осуществления последовательности DH и JH и по меньшей мере 3, по меньшей мере 10, по меньшей мере 20, по меньшей мере 40, по меньшей мере 60 или по меньшей мере 80 последовательностей VH локуса тяжелой цепи иммуноглобулина замещают не относящимися к мыши последовательностями вариабельной области иммуноглобулина. Согласно дополнительному предпочтительному варианту осуществления последовательности DH, JH и все последовательности VH локуса тяжелой цепи иммуноглобулина замещают не относящимися к мыши последовательностями вариабельной области иммуноглобулина. Не относящиеся к мыши последовательности вариабельной области иммуноглобулина могут являться переаранжированными. Согласно предпочтительному варианту осуществления не относящиеся к мыши последовательности вариабельной области иммуноглобулина содержат целые нереаранжированные области DH и JH и по меньшей мере 3, по меньшей мере 10, по меньшей мере 20, по меньшей мере 40, по меньшей мере 60 или по меньшей мере 80 нереаранжированных последовательностей VH отличного от мыши вида. Согласно дополнительному предпочтительному варианту осуществления не относящийся к мыши последовательности вариабельной области иммуноглобулина содержат целую вариабельную область, включающую в себя все области VH, DH и JH отличного от мыши вида. Отличный от мыши вид может представлять собой Homo sapiens и не относящиеся к мыши последовательности вариабельной области иммуноглобулина могут представлять собой последовательности человека.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует антитело, которое содержит по меньшей мере один вариабельный домен человека /не относящийся к человеку полипептид константного домена иммуноглобулина, причем мышь экспрессирует белок ADAM6 мыши или его ортолог или гомолог из локуса, отличного от локуса иммуноглобулина.
Согласно одному варианту осуществления белок ADAM6 или его ортолог или гомолог экспрессируется в В-клетке мыши, причем В-клетка содержит реаранжированную последовательность иммуноглобулина, которая содержит вариабельную последовательность человека и не относящуюся к человеку константную последовательность.
Согласно одному варианту осуществления не относящаяся к человеку константная последовательность представляет собой последовательность грызуна. Согласно одному варианту осуществления грызун выбран из мыши, крысы и хомяка.
Согласно одному аспекту предусмотрен способ получения стерильного самца мыши, предусматривающий приведение эндогенного аллеля ADAM6 донорной ES клетки в нефункциональное состояние (или нокаут указанного аллеля), введение донорной ES клетки в зародыш-хозяин, вынашивание зародыша-хозяина в суррогатной матери и предоставление возможности суррогатной матери родить потомство, происходящее полностью или частично из донорной ES клетки. Согласно одному варианту осуществления способ дополнительно предусматривает скрещивание потомства для получения стерильного самца мыши.
Согласно одному аспекту предусмотрен способ получения мыши с представляющей интерес генетической модификацией, причем мышь является стерильной, причем способ предусматривает стадии (а) получения представляющей интерес генетической модификации в геноме; (b) модификации генома для нокаута эндогенного аллеля ADAM6 или приведения эндогенного аллеля ADAM6 в нефункциональное состояние; и (с) использования генома в получении мыши. Согласно различным вариантам осуществления геном происходит из ES клетки или используется в эксперименте ядерного транспорта.
Согласно одному аспекту предусмотрена полученная с использованием нацеливающего вектора мышь, нуклеотидный конструкт или клетка, описанные в настоящем документе.
Согласно одному аспекту предусмотрено потомство скрещивания описанной в настоящем документе мыши со второй мышью, которая представляет собой мышь дикого типа или генетически модифицированную мышь.
Согласно одному аспекту предусмотрен способ поддержания линии мыши, причем линия мыши содержит замещение последовательности тяжелой цепи иммуноглобулина мыши одной или несколькими гетерологичными последовательностями тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления одна или несколько гетерологичных последовательности тяжелой цепи иммуноглобулина представляют собой последовательности тяжелой цепи человека.
Согласно одному варианту осуществления линия мыши содержит делецию одного или нескольких генных сегментов VH, DH и/или JH мыши. Согласно одному варианту осуществления мышь дополнительно содержит один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и/или один или несколько генных сегментов JH человека. Согласно одному варианту осуществления мышь содержит по меньшей мере 3, по меньшей мере 10, по меньшей мере 20, по меньшей мере 40, по меньшей мере 60 или по меньшей мере 80 сегментов VH человека, по меньшей мере 27 человека генных сегментов DH и по меньшей мере шесть генных сегментов JH. Согласно конкретному варианту осуществления мышь содержит по меньшей мере 3, по меньшей мере 10, по меньшей мере 20, по меньшей мере 40, по меньшей мере 60 или по меньшей мере 80 сегментов VH человека, по меньшей мере 27 генных сегментов DH человека и по меньшей мере шесть генных сегментов JH функционально связаны с геном константной области. Согласно одному варианту осуществления ген константной области представляет собой ген константной области мыши. Согласно одному варианту осуществления ген константной области содержит последовательность гена константной области мыши, выбранную из CH1, шарнира, CH2, CH3 и/или CH4 или их комбинации.
Согласно одному варианту осуществления способ предусматривает получение самца мыши, гетерозиготного в отношении замещения последовательности тяжелой цепи иммуноглобулина мыши, и скрещивание гетерозиготного самца мыши с самкой мыши дикого типа или самкой мыши, которая является гомозиготной или гетерозиготной в отношении последовательности тяжелой цепи человека. Согласно одному варианту осуществления способ предусматривает сохранение линии путем повторного скрещивания гетерозиготных самцов с самками, которые являются самками дикого типа или гомозиготными или гетерозиготными в отношении последовательности тяжелой цепи человека.
Согласно одному варианту осуществления способ предусматривает получение клеток от самцов или самок мышей, гомозиготных или гетерозиготных в отношении последовательности тяжелой цепи человека, и использование этих клеток в качестве донорных клеток или ядер из них в качестве донорных ядер и использование клеток или ядер для получения генетически модифицированных животных с использованием клеток-хозяев и/или вынашивания клеток и/или ядер в суррогатных материнских особях.
Согласно одному варианту осуществления только самцов мышей, которые являются гетерозиготными в отношении замещения на локусе тяжелой цепи, скрещивают с самками мышей. Согласно конкретному варианту осуществления самки мышей являются гомозиготными, гетерозиготными или дикого типа по отношению к замещенному локусу тяжелой цепи.
Согласно одному варианту осуществления мышь дополнительно содержит замещение вариабельных последовательностей λ и/или к легкой цепи на эндогенном локусе легкой цепи иммуноглобулина гетерологичными последовательностями легкой цепи иммуноглобулина. Согласно одному варианту осуществления гетерологичные последовательности легкой цепи иммуноглобулина представляют собой вариабельные последовательности λ и/или κ легкой цепи иммуноглобулина человека.
Согласно одному варианту осуществления мышь дополнительно содержит трансген в локусе, отличном от эндогенного локуса иммуноглобулина, причем трансген содержит последовательность, кодирующую реаранжированную или нереаранжированную гетерологичную последовательность λ или κ легкой цепи (например, нереаранжированную VL и нереаранжированную JL или реаранжированную VJ), функционально связанную (для нереаранжированной) или слитую (для реаранжированной) с последовательностью константной области легкой цепи иммуноглобулина. Согласно одному варианту осуществления гетерологичная последовательность λ или κ легкой цепи относится к человеку. Согласно одному варианту осуществления последовательность константной области выбрана из грызуна, человека и отличного от человека примата. Согласно одному варианту осуществления последовательность константной области выбрана из мыши, крысы и хомяка. Согласно одному варианту осуществления трансген содержит не относящийся к иммуноглобулину промотор, который управляет экспрессией последовательностей легкой цепи. Согласно конкретному варианту осуществления промотор представляет собой транскрипционно активный промотор. Согласно конкретному варианту осуществления промотор представляет собой промотор ROSA26.
Согласно одному аспекту предусмотрен конструкт нуклеиновой кислоты, содержащий вышележащее гомологичное плечо и нижележащее гомологичное плечо, причем вышележащее гомологичное плечо содержит последовательность, которая идентична или по существу идентична последовательности вариабельной области тяжелой цепи иммуноглобулина человека, нижележащее гомологичное плечо содержит последовательность, которая идентична или по существу идентична последовательности вариабельной области иммуноглобулина человека или мыши, и между вышележащим и нижележащим гомологичными плечами расположена последовательность, которая содержит нуклеотидную последовательность, кодирующую белок ADAM6 мыши. Согласно конкретному варианту осуществления последовательность, кодирующая ген ADAM6 мыши, функционально связана с промотором мыши, с которым ADAM6 мыши связан у мыши дикого типа.
Согласно одному аспекту предусмотрен нацеливающий вектор, содержащий (а) нуклеотидную последовательность, которая идентична или по существу идентична нуклеотидной последовательности генного сегмента вариабельной области человека; и (b) нуклеотидную последовательность, кодирующую ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у мыши.
Согласно одному варианту осуществления нацеливающий вектор дополнительно содержит промотор, функционально связанный с последовательностью, кодирующей ADAM6 мыши. Согласно конкретному варианту осуществления промотор представляет собой промотор ADAM6 мыши.
Согласно одному аспекту предусмотрен нуклеотидный конструкт для модификации вариабельного локуса тяжелой цепи иммуноглобулина мыши, причем конструкт содержит по меньшей мере один сайт распознавания сайт-специфической рекомбиназы и последовательность, кодирующую белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у мыши.
Согласно одному аспекту предусмотрены клетки мыши и зародыши мыши, включая в себя без ограничения ES клетки, плюрипотентные клетки и индуцированные плюрипотентные клетки, которые содержат описанные в настоящем документе генетические модификации. Предусмотрены клетки, которые представляют собой XX, и клетки, которые представляют собой XY. Также предусмотрены клетки, которые содержат ядро, содержащее модификацию, описанную в настоящем документе, например, модификацию, введенную в клетку путем пронуклеарной инъекции. Также предусмотрены клетки, зародыши и мыши, которые содержат введенный с помощью вируса ген ADAM6, например, клетки, зародыши и мыши, содержащие конструкт трансдукции, содержащий ген ADAM6, который является функциональным у мыши.
Согласно одному аспекту предусмотрена генетически модифицированная клетка мыши, причем клетка не содержит функциональный эндогенный локус ADAM6 мыши и клетка содержит эктопическую нуклеотидную последовательность, которая кодирует белок ADAM6 мыши или его функциональный фрагмент. Согласно одному варианту осуществления клетка дополнительно содержит модификацию эндогенной последовательности вариабельного гена тяжелой цепи иммуноглобулина. Согласно конкретному варианту осуществления модификация эндогенной последовательности вариабельного гена тяжелой цепи иммуноглобулина содержит делецию, выбранную из делеции генного сегмента VH мыши, делеции генного сегмента DH мыши, делеции генного сегмента JH мыши и их комбинации. Согласно конкретному варианту осуществления мышь содержит замещение одной или нескольких последовательностей VH, DH и/или JH иммуноглобулина мыши последовательностью иммуноглобулина человека. Согласно конкретному варианту осуществления последовательность иммуноглобулина человека выбрана из VH человека, VL человека, DH человека, JH человека, JL человека и их комбинации.
Согласно одному варианту осуществления клетка представляет собой тотипотентную клетку, плюрипотентную клетку или индуцированную плюрипотентную клетку. Согласно конкретному варианту осуществления клетка представляет собой ES клетку мыши.
Согласно одному аспекту предусмотрена В-клетка мыши, причем В-клетка мыши содержит реаранжированный ген тяжелой цепи иммуноглобулина, причем В-клетка содержит на хромосоме В-клетки последовательность нуклеиновой кислоты, кодирующую белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши. Согласно одному варианту осуществления В-клетка мыши содержит два аллеля последовательности нуклеиновой кислоты.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на молекуле нуклеиновой кислоты (например, хромосоме В-клетки) которая является смежной с реаранжированным локусом тяжелой цепи иммуноглобулина мыши.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на молекуле нуклеиновой кислоты (например, хромосоме В-клетки), которая находится на расстоянии от молекулы нуклеиновой кислоты, которая содержит реаранжированный локус тяжелой цепи иммуноглобулина мыши.
Согласно одному варианту осуществления В-клетка мыши содержит реаранжированный не относящуюся к мыши последовательность вариабельного гена иммуноглобулина, функционально связанную с геном константной области иммуноглобулина мыши или человека, причем В-клетка содержит последовательность нуклеиновой кислоты, которая кодирует белок ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши.
Согласно одному аспекту предусмотрена соматическая клетка мыши, содержащая хромосому, которая содержит модифицированный локус тяжелой цепи иммуноглобулина и последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши. Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на той же хромосоме, что и модифицированный локус тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления нуклеиновая кислота находится на другой хромосоме, чем модифицированный локус тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления соматическая клетка содержит одну копию последовательности нуклеиновой кислоты. Согласно одному варианту осуществления соматическая клетка содержит по меньшей мере две копии последовательности нуклеиновой кислоты. Согласно конкретному варианту осуществления соматическая клетка представляет собой В-клетку. Согласно конкретному варианту осуществления клетка представляет собой зародышевую клетку. Согласно конкретному варианту осуществления клетка представляет собой стволовую клетку.
Согласно одному аспекту предусмотрена зародышевая клетка мыши, содержащая последовательность нуклеиновой кислоты, кодирующую ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) на хромосоме зародышевой клетки, причем последовательность нуклеиновой кислоты, кодирующая ADAM6 мыши (или его гомолог или ортолог или функциональный фрагмент) находится в положении в хромосоме, которое отличается от положения в хромосоме зародышевой клетки мыши дикого типа. Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на локусе иммуноглобулина мыши. Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на той же хромосоме зародышевой клетки, что и локус иммуноглобулина мыши. Согласно одному варианту осуществления последовательность нуклеиновой кислоты находится на другой хромосоме зародышевой клетки, чем локус иммуноглобулина мыши. Согласно одному варианту осуществления локус иммуноглобулина мыши содержит замещение по меньшей мере одной последовательности иммуноглобулина мыши по меньшей мере одной не относящейся к мыши последовательностью иммуноглобулина. Согласно конкретному варианту осуществления по меньшей мере одна не относящаяся к мыши последовательность иммуноглобулина представляет собой последовательность иммуноглобулина человека.
Согласно одному аспекту предусмотрена плюрипотентная, индуцированная плюрипотентная или тотипотентная клетка, полученная от описанной в настоящем документе мыши. Согласно конкретному варианту осуществления клетка представляет собой эмбриональную стволовую (ES) клетку мыши.
Согласно одному аспекту предусмотрена клетка или ткань, полученная от описанной в настоящем документе мыши. Согласно одному варианту осуществления клетка или ткань получена из селезенки, лимфатического узла или костного мозга мыши, описанной в настоящем документе. Согласно одному варианту осуществления клетка представляет собой В-клетку. Согласно одному варианту осуществления клетка представляет собой эмбриональную стволовую клетку. Согласно одному варианту осуществления клетка представляет собой зародышевую клетку.
Согласно одному варианту осуществления ткань выбрана из соединительной, мышечной, нервной и эпителиальной ткани. Согласно конкретному варианту осуществления ткань представляет собой репродуктивную ткань.
Согласно одному варианту осуществления клетку и/или ткань, полученную от мыши, описанной в настоящем документе, выделяют для применения в одном или нескольких анализах ex vivo. Согласно различным вариантам осуществления один или несколько анализов ex vivo включают в себя измерения физических, термических, электрических, механических или оптических свойств, хирургическую процедуру, измерения взаимодействий различных типов ткани, разработку техник получения изображений или их комбинацию.
Согласно одному аспекту предусмотрено применение клетки или ткани, полученной от описанной в настоящем документе мыши для получения антитела. Согласно одному аспекту предусмотрено применение клетки или ткани, полученной от описанной в настоящем документе мыши для получения гибридомы или квадромы.
Согласно одному аспекту предусмотрена не относящаяся к человеку клетка, содержащая хромосому или ее фрагмент описанного в настоящем документе отличного от человека животного. Согласно одному варианту осуществления не относящаяся к человеку клетка содержит ядро описанного в настоящем документе отличного от человека животного. Согласно одному варианту осуществления не относящаяся к человеку клетка содержит хромосому или ее фрагмент как результат ядерного транспорта.
Согласно одному аспекту предусмотрено ядро, полученное из мыши, описанной в настоящем документе. Согласно одному варианту осуществления ядро происходит из диплоидной клетки, которая не является В-клеткой.
Согласно одному аспекту предусмотрена нуклеотидная последовательность, кодирующая вариабельную область иммуноглобулина, образованного у описанной в настоящем документе мыши.
Согласно одному аспекту предусмотрена аминокислотная последовательность вариабельные область тяжелой цепи иммуноглобулина или легкой цепи иммуноглобулина антитела, образованного у описанного в настоящем документе мыши.
Согласно одному аспекту предусмотрена нуклеотидная последовательность вариабельной области тяжелой цепи иммуноглобулина или легкой цепи иммуноглобулина, кодирующая вариабельную область антитела, образованного у описанной в настоящем документе мыши.
Согласно одному аспекту предусмотрено антитело или его антигенсвязывающий фрагмент (например, Fab, F(ab)2, scFv), образованный у описанной в настоящем документе мыши.
Согласно одному аспекту предусмотрен способ получения генетически модифицированной мыши, предусматривающий замещение одного или нескольких генных сегментов тяжелой цепи иммуноглобулина выше (относительно транскрипции генных сегментов тяжелой цепи иммуноглобулина) эндогенного локуса ADAM6 мыши одним или несколькими генными сегментами тяжелой цепи иммуноглобулина человека, и замещение одного или нескольких генных сегментов иммуноглобулина ниже (относительно транскрипции генных сегментов тяжелой цепи иммуноглобулина) локуса ADAM6 мыши одним или несколькими генными сегментами тяжелой цепи или легкой цепи иммуноглобулина человека. Согласно одному варианту осуществления один или несколько генных сегментов иммуноглобулина человека, замещающие один или несколько эндогенных генных сегментов иммуноглобулина выше эндогенного локуса ADAM6 мыши, включают в себя генные сегменты V. Согласно одному варианту осуществления генные сегменты иммуноглобулина человека, замещающие один или несколько эндогенных генных сегментов иммуноглобулина выше эндогенного локуса ADAM6 мыши, включают в себя генные сегменты V и D. Согласно одному варианту осуществления один или несколько генных сегментов иммуноглобулина человека, замещающие один или несколько эндогенных генных сегментов иммуноглобулина ниже эндогенного локуса ADAM6 мыши, включают в себя генные сегменты J. Согласно одному варианту осуществления один или несколько генных сегментов иммуноглобулина человека, замещающих один или несколько эндогенных генных сегментов иммуноглобулина ниже эндогенного локуса ADAM6 мыши, включают в себя генные сегменты D и J. Согласно одному варианту осуществления один или несколько генных сегментов иммуноглобулина человека, замещающих один или несколько эндогенных генных сегментов иммуноглобулина ниже эндогенного локуса ADAM6 мыши, включают в себя генные сегменты V, D и J.
Согласно одному варианту осуществления один или несколько генных сегментов тяжелой цепи иммуноглобулина выше и/или ниже гена ADAM6 замещают в плюрипотентной, индуцированной плюрипотентной или тотипотентной клетке для получения генетически модифицированной клетки-предшественника; генетически модифицированную клетку-предшественник вводят хозяину; и хозяина, содержащего генетически модифицированную клетку-предшественник, вынашивают для получения мыши, содержащей геном, полученный из генетически модифицированной клетки-предшественника. Согласно одному варианту осуществления хозяин представляет собой зародыш. Согласно конкретному варианту осуществления хозяин выбран из пре-морулы мыши (например, 8- или 4-клеточная стадия), тетраплоидного зародыша, агрегата эмбриональных клеток или бластоцисты.
Согласно одному аспекту предусмотрен способ получения генетически модифицированной мыши, предусматривающий замещение нуклеотидной последовательности мыши, которая содержит нуклеотидную последовательность генного сегмента иммуноглобулина мыши и ADAM6 мыши (или его ортолога или гомолога или фрагмента, функционального у самца мыши) последовательностью, содержащей генный сегмент иммуноглобулина человека для образования первого химерного локуса, затем вставку последовательности, содержащей кодирующую ADAM6 мыши последовательность (или последовательность, кодирующую его ортолог или гомолог или функциональный фрагмент), в последовательность, содержащую генный сегмент иммуноглобулина человека для образования второго химерного локуса.
Согласно одному варианту осуществления второй химерный локус содержит вариабельный генный сегмент тяжелой цепи (VH) иммуноглобулина человека. Согласно одному варианту осуществления второй химерный локус содержит вариабельный генный сегмент легкой цепи (VL) иммуноглобулина человека. Согласно конкретному варианту осуществления второй химерный локус содержит генный сегмент VH человека или генный сегмент VL человека, функционально связанный с генным сегментом DH человека и генным сегментом JH человека. Согласно дополнительному конкретному варианту осуществления второй химерный локус функционально связан с третьим химерным локусом, который содержит последовательность CH1 человека или CH1 человека и шарнирную последовательность человека, слитые с последовательностью CH2+CH3 мыши.
Согласно одному аспекту предусмотрено применение мыши, которая содержит эктопическую нуклеотидную последовательность, содержащую локус или последовательность ADAM6 мыши для получения фертильного самца мыши, причем применение предусматривает спаривание мыши, содержащей эктопическую нуклеотидную последовательность, которая содержит локус или последовательность ADAM6 мыши, с мышью, которая не содержит функциональный эндогенный локус или последовательность ADAM6 мыши, и получение потомства, которое представляет собой самку, способную производить потомство, содержащее эктопический локус или последовательность ADAM6, или которое представляет собой самца, который содержит эктопический локус или последовательность ADAM6, и самец проявляет фертильность, которая является приблизительно такой же, как и фертильность, проявляемая самцом мыши дикого типа.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения нуклеотидной последовательности вариабельной области иммуноглобулина.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения полностью человеческого Fab или полностью человеческого F(ab)2.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения иммортализованной клеточной линии.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения гибридомы или квадромы.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения фаговой библиотеки, содержащей вариабельные области тяжелой цепи человека и вариабельные области легкой цепи человека.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для создания последовательности вариабельной области для получения антитела человека, предусматривающее (а) иммунизацию описанной в настоящем документе мыши представляющим интерес антигеном, (b) выделение лимфоцита из иммунизированной мыши согласно (а), (с) воздействие на лимфоцит одного или нескольких меченых антител, (d) идентификацию лимфоцита, который способен связываться с представляющим интерес антигеном, и (е) амплификацию одной или нескольких последовательностей нуклеиновой кислоты вариабельной области из лимфоцита, тем самым создавая последовательность вариабельной области.
Согласно одному варианту осуществления лимфоцит получен из селезенки мыши. Согласно одному варианту осуществления лимфоцит получен из лимфатического узла мыши. Согласно одному варианту осуществления лимфоцит получен из костного мозга мыши.
Согласно одному варианту осуществления меченое антитело представляет собой конъюгированное с флуорофором антитело. Согласно одному варианту осуществления одно или несколько конъюгированных с флуорофором антител выбраны из IgM, IgG и/или их комбинации.
Согласно одному варианту осуществления лимфоцит представляет собой В-клетку.
Согласно одному варианту осуществления один или несколько последовательность вариабельной области нуклеиновой кислоты содержит последовательность вариабельной области тяжелой цепи. Согласно одному варианту осуществления одна или несколько последовательностей нуклеиновой кислоты вариабельной области содержат последовательность вариабельной области легкой цепи. Согласно конкретному варианту осуществления последовательность вариабельной области легкой цепи представляет собой последовательность вариабельной области κ легкой цепи иммуноглобулина. Согласно одному варианту осуществления один или несколько последовательностей нуклеиновой кислоты вариабельной области содержит последовательность вариабельной области тяжелой цепи и κ легкой цепи.
Согласно одному варианту осуществления предусмотрено применение описанной в настоящем документе мыши для создания последовательности вариабельной области тяжелой и κ легкой цепи для получения антитела человека, предусматривающее (а) иммунизацию описанной в настоящем документе мыши представляющим интерес антигеном, (b) выделение селезенки из иммунизированной мыши согласно (а), (с) воздействие на В-лимфоциты из селезенки одного или нескольких меченых антител, (d) идентификацию В-лимфоцита согласно (с), который способен связываться с представляющим интерес антигеном, и (е) амплификацию последовательности нуклеиновой кислоты вариабельной области тяжелой цепи и последовательности нуклеиновой кислоты вариабельной области легкой цепи из В-лимфоцита, тем самым создавая последовательности вариабельной области тяжелой цепи и κ легкой цепи.
Согласно одному варианту осуществления предусмотрено применение описанной в настоящем документе мыши для создания последовательности вариабельной области тяжелая и κ легкой цепи для получения антитела человека, предусматривающее (а) иммунизацию описанной в настоящем документе мыши представляющим интерес антигеном, (b) выделение одного или нескольких лимфатических узлов из иммунизированной мыши согласно (а), (с) воздействие на В-лимфоциты из одного или нескольких лимфатических узлов одного или нескольких меченых антител, (d) идентификацию В-лимфоцита согласно (с), который способен связываться с представляющим интерес антигеном, и (е) амплификацию последовательности нуклеиновой кислоты вариабельной области тяжелой цепи и последовательности нуклеиновой кислоты вариабельной области κ легкой цепи из В-лимфоцита, тем самым создавая последовательности вариабельной области тяжелой цепи и κ легкой цепи.
Согласно одному варианту осуществления предусмотрено применение описанной в настоящем документе мыши для создания последовательности вариабельной области тяжелой и κ легкой цепи для получения антитела человека, предусматривающее (а) иммунизацию описанной в настоящем документе мыши представляющим интерес антигеном, (b) выделение костного мозга из иммунизированной мыши согласно (а), (с) воздействие на В-лимфоциты из костного мозга одного или нескольких меченых антител, (d) идентификацию В-лимфоцита согласно (с), который способен связываться с представляющим интерес антигеном, и (е) амплификацию последовательности нуклеиновой кислоты вариабельной области тяжелой цепи и последовательности нуклеиновой кислоты вариабельной области κ легкой цепи из В-лимфоцита, тем самым создавая последовательности вариабельной области тяжелой цепи и κ легкой цепи. Согласно различным вариантам осуществления одно или несколько меченых антител выбраны из IgM, IgG и/или их комбинации.
Согласно различным вариантам осуществления предусмотрено применение описанной в настоящем документе мыши для создания последовательности вариабельной области тяжелой и κ легкой цепи для получения антитела человека, дополнительно предусматривающее слияние амплифицированных последовательностей вариабельной области тяжелой и легкой цепи с последовательностями константной области тяжелой и легкой цепи человека, экспрессию слитых последовательностей тяжелой и легкой цепи в клетке и выделение экспрессированных последовательностей тяжелой и легкой цепи, тем самым создавая антитело человека.
Согласно различным вариантам осуществления константные области тяжелой цепи человека выбраны из IgM, IgD, IgA, IgE и IgG. Согласно различным конкретным вариантам осуществления IgG выбран из IgG1, IgG2, IgG3 и IgG4. Согласно различным вариантам осуществления константная область тяжелой цепи человека содержит CH1, шарнир, CH2, CH3, CH4 или их комбинацию. Согласно различным вариантам осуществления константная область легкой цепи представляет собой κ константную область иммуноглобулина. Согласно различным вариантам осуществления клетка выбрана из клетки HeLa, клетки DU145, клетки Lncap, клетки MCF-7, клетки MDA-MB-438, клетки РС3, клетки T47D, клетки ТНР-1, клетки U87, клетки SHSY5Y (нейробластома человека), клетки Saos-2, клетки Vero, клетки СНО, клетки GH3, клетки PC12, ретинальной клетки человека (например, клетки PER.C6™) и клетки МС3Т3. Согласно конкретному варианту осуществления клетка представляет собой клетку СНО.
Согласно одному аспекту предусмотрен способ создания обратного химерного относящегося к грызуну-человеку антитела, специфического к представляющему интерес антигену, предусматривающий стадии иммунизации описанной в настоящем документе мыши антигеном, выделение по меньшей мере одной клетки из мыши, производящей обратное химерное относящееся к мыши - относящееся к человеку антитело, специфическое к антигену, культивирование по меньшей мере одной клетки, производящей обратное химерное относящееся в мыши - относящееся к человеку антитело, специфическое к антигену, и получение указанного антитела.
Согласно одному варианту осуществления обратное химерное относящееся в мыши-человеку антитело содержит вариабельный домен тяжелой цепи человека, слитый с константным геном тяжелой цепи мыши или крысы, и вариабельный домен легкой цепи человека, слитый с константным геном легкой цепи мыши или крысы или человека.
Согласно одному варианту осуществления культивирование по меньшей мере одной клетки, производящей обратное химерное относящееся к грызуну - относящееся к человеку антитело, специфическое к антигену, проводят по меньшей мере на одной гибридомной клетке, созданной по меньшей мере из одной клетки, выделенной из мыши.
Согласно одному аспекту предусмотрен способ создания полностью человеческого антитела, специфического к представляющему интерес антигену, предусматривающий стадии иммунизации описанной в настоящем документе мыши антигеном, выделение по меньшей мере одной клетки из мыши, производящей обратное химерное относящееся к грызуну - относящееся к человеку антитело, специфическое к антигену, создание по меньшей мере одной клетки, производящей полностью человеческое антитело, полученное из обратного химерного относящегося к грызуну - относящегося к человеку антитела, специфического к антигену, и культивирование по меньшей мере одной клетки, производящей полностью человеческое антитело, и получение указанного полностью человеческого антитела.
Согласно различным вариантам осуществления по меньшей мере одна клетка, выделенная из мыши, производящей обратное химерное относящееся к грызуну - относящееся к человеку антитело, специфическое к антигену, представляет собой спленоцит или В-клетку.
Согласно различным вариантам осуществления антитело представляет собой моноклональное антитело.
Согласно различным вариантам осуществления иммунизацию представляющим интерес антигеном проводят с помощью белка, ДНК, комбинации ДНК и белка или клеток, экспрессирущих антиген.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения последовательности нуклеиновой кислоты, кодирующей вариабельную область иммуноглобулина или ее фрагмент. Согласно одному варианту осуществления последовательность нуклеиновой кислоты применяют для получения антитела человека или его антигенсвязывающего фрагмента. Согласно одному варианту осуществления мышь применяют для получения антигенсвязывающего белка, выбранного из антитела, мультиспецифического антитела (например, биспецифического антитела), scFv, биспецифического scFv, диатела, триатела, тетратела, V-NAR, VHH, VL, F(ab), F(ab)2, DVD (т.е. антигенсвязывающего белка с двойным вариабельным доменом), SVD (т.е. антигенсвязывающего белка с одним вариабельным доменом) или биспецифического проводника Т-клеток (BiTE).
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для введения эктопической последовательности ADAM6 в организм мыши, которая не содержит функциональную эндогенную последовательность ADAM6 мыши, причем применение предусматривает спаривание описанной в настоящем документе мыши с мышью, которая не содержит функциональную эндогенную последовательность ADAM6 мыши.
Согласно одному аспекту предусмотрено применение генетического материала из описанной в настоящем документе мыши для получения мыши, содержащей эктопическую последовательность ADAM6. Согласно одному варианту осуществления применение предусматривает ядерный транспорт с использованием ядра клетки описанной в настоящем документе мыши. Согласно одному варианту осуществления применение предусматривает клонирование клетки описанной в настоящем документе мыши для получения животного, полученного из клетки. Согласно одному варианту осуществления применение предусматривает использование спермы или яйцеклетки описанной в настоящем документе мыши с способе получения мыши, содержащей эктопическую последовательность ADAM6.
Согласно одному аспекту предусмотрен способ получения фертильного самца мыши, содержащего модифицированный локус тяжелой цепи иммуноглобулина, предусматривающий оплодотворение первой зародышевой клетки мыши, которая содержит модификацию эндогенного локуса тяжелой цепи иммуноглобулина, второй зародышевой клеткой мыши, которая содержит ген ADAM6 или его ортолог или гомолог или фрагмент, который является функциональным у самца мыши; образование оплодотворенной клетки; предоставление возможности оплодотворенной клетке развиться в зародыш; и вынашивание зародыша в суррогатной матери для получения мыши.
Согласно одному варианту осуществления оплодотворение достигается путем спаривания самца мыши и самки мыши. Согласно одному варианту осуществления самка мыши содержит ген ADAM6 или его ортолог или гомолог или фрагмент. Согласно одному варианту осуществления самец мыши содержит ген ADAM6 или его ортолог или гомолог или фрагмент.
Согласно одному аспекту предусмотрено применение последовательности нуклеиновой кислоты, кодирующей белок ADAM6 мыши или его ортолог или гомолог или функциональный фрагмент соответствующего белка ADAM6, для восстановления или усиления фертильности мыши с геномом, содержащим модификацию локуса тяжелой цепи иммуноглобулина, причем модификация снижает или устраняет эндогенную функцию ADAM6.
Согласно одному варианту осуществления последовательность нуклеиновой кислоты интегрирована в геном мыши в эктопическом положении. Согласно одному варианту осуществления последовательность нуклеиновой кислоты интегрирована в геном мыши на эндогенном локусе иммуноглобулина. Согласно конкретному варианту осуществления эндогенный локус иммуноглобулина представляет собой локус тяжелой цепи. Согласно одному варианту осуществления последовательность нуклеиновой кислоты интегрирована в геном мыши в положении, отличном от эндогенного локуса иммуноглобулина.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе мыши для получения лекарственного средства (например, антигенсвязывающего белка) или для получения последовательности, кодирующей вариабельную последовательность лекарственного средства (например, антигенсвязывающего белка), для лечения заболевания или нарушения человека.
Согласно одному аспекту предусмотрена генетически модифицированная клетка мыши, причем клетка является неспособной экспрессировать тяжелую цепь, содержащую реаранжированные эндогенные генные сегменты тяжелой цепи иммуноглобулина, и клетка содержит функциональный ген ADAM6, который кодирует белок ADAM6 мыши или его функциональный фрагмент. Согласно одному варианту осуществления клетка дополнительно содержит вставку генных сегментов иммуноглобулина человека. Согласно конкретному варианту осуществления генные сегменты иммуноглобулина человека представляют собой генные сегменты тяжелой цепи, которые функционально связаны с константными областями тяжелой цепи мыши так, чтобы при реаранжировке кодировать функциональную тяжелую цепь антитела, которое содержит вариабельную область человека.
Предусмотрены генетически модифицированные отличные от человека животные, зародыши, клетки, ткани, а также конструкты нуклеиновой кислоты для модификации отличных от человека животных и способы и композиции для их получения и применения. Предусмотрены животные и клетки, которые производят лямбда (λ) вариабельные области (относящиеся к человеку или не относящиеся к человеку), ассоциированные с каппа (κ) легкой цепью, причем животные и клетки содержат модификацию локуса тяжелой цепи иммуноглобулина, которая устраняет или снижает активность белка ADAM6 или его гомолога или ортолога, причем животные дополнительно содержат генетическую модификацию, которая полностью или частично восстанавливает активность ADAM6 (или активность его гомолога или ортолога). Предусмотрены мыши, которые являются фертильными и экспрессируют вариабельный домен λ человека, когнатный вариабельному доменому тяжелой цепи человека, причем вариабельный домен λ человека экспрессируется у мыши смежно с константной областью λ или κ, и согласно различным вариантам осуществления вариабельная область λ или κ представляет собой эндогенную (например, относящуюся к мыши или крысе) константную область. Также предусмотрены мыши и клетки, которые образуют λ вариабельные области человека, ассоциированные с κ или λ легкой цепью, например, из эндогенного локуса легкой цепи мыши. Также предусмотрены способы получения антител, которые содержат лямбда вариабельные области. Также предусмотрены способы отбора тяжелых цепей, которые экспрессируются с когнатными лямбда вариабельными областями.
Предусмотрены химерные и относящие к человеку антигенсвязывающие белки (например, антитела) и нуклеиновые кислоты, кодирующие их, которые содержат соматически мутированные вариабельные области, включая в себя антитела, которые содержат легкие цепи, содержащие вариабельный домен, происходящий из генного сегмента Vλ человека и генного сегмента Jλ человека, слитые с константным доменом легкой цепи мыши.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует последовательность λ вариабельной области человека на легкой цепи, которая содержит константную область мыши. Согласно одному аспекту предусмотрена мышь, которая экспрессирует последовательность λ вариабельной области человека на легкой цепи, который содержит константную область κ. Согласно одному аспекту предусмотрена мышь, которая экспрессирует из эндогенного локуса легкой цепи мыши легкую цепь, которая содержит последовательность λ вариабельной области человека. Согласно одному аспекту предусмотрена мышь, которая содержит реаранжированный ген легкой цепи, который содержит λ вариабельную последовательность человека, соединенные с последовательностью константной области мыши; согласно одному варианту осуществления последовательность константной области мыши представляет собой константную последовательность λ; согласно одному варианту осуществления последовательность константной области мыши представляет собой константную последовательность κ.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит нереаранжированный вариабельный генный сегмент λ легкой цепи человека (hVλ) и соединяющий генный сегмент λ человека (hJλ). Согласно одному варианту осуществления нереаранжированный hVλ и hJλ находятся на локусе легкой цепи мыши. Согласно одному варианту осуществления нереаранжированный hVλ и нереаранжированный hJλ находятся на трансгене и функционально связаны с последовательностью константной области человека или мыши. Согласно одному варианту осуществления нереаранжированный hVλ и нереаранжированный hJλ находятся на эписоме. Согласно одному варианту осуществления мышь способна производить иммуноглобулин, который содержит легкую цепь, которые происходит из нереаранжированной последовательности hVλ и последовательности hJλ и последовательности нуклеиновой кислоты константной области легкой цепи мыши (CL). Также предусмотрены способы и композиции для получения и применения генетически модифицированных мышей. Предусмотрены антитела, которые содержат (а) вариабельный домен тяжелой цепи человека (hVH), слитый с константной областью тяжелой цепи мыши, и (b) VL человека, слитый с доменом CL мыши; включая в себя случай, когда один или несколько вариабельных доменов соматически мутированы, например, в ходе отбора антитела или иммунной клетки у мыши согласно настоящему изобретению. Согласно одному варианту осуществления нереаранжированный hVλ и нереаранжированный hJλ функционально связаны с константной областью κ (Сκ) человека или мыши. Согласно одному варианту осуществления нереаранжированный hVλ и нереаранжированный hJλ функционально связаны с константной областью λ (Сλ) человека или мыши.
Согласно одному аспекту предусмотрена мышь, которая содержит в своей зародышевой линии, на эндогенном локусе легкой цепи мыши последовательность вариабельной области λ легкой цепи человека, причем лямбда последовательность вариабельной области человека экспрессируется в легкой цепи, которая содержит последовательность гена константной области иммуноглобулина мыши.
Согласно одному варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус λ. Согласно одному варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус κ.
Согласно одному варианту осуществления мышь не содержит эндогенную вариабельную последовательность легкой цепи на эндогенном локусе легкой цепи мыши.
Согласно одному варианту осуществления все или по существу все эндогенные генные сегменты вариабельной области легкой цепи мыши замещают одним или несколькими генными сегментами вариабельной области λ человека.
Согласно одному варианту осуществления последовательность вариабельной области λ легкой цепи человека содержит последовательность Jλ человека. Согласно одному варианту осуществления последовательность Jλ человека выбрана из группы, состоящей из Jλ1, Jλ2, Jλ3, Jλ7 и их комбинации.
Согласно одному варианту осуществления последовательность вариабельной области λ легкой цепи человека содержит фрагмент кластера A локуса легкой цепи человека. Согласно конкретному варианту осуществления фрагмент кластера A локуса λ легкой цепи человека продолжается от hVλ3-27 до hVλ3-1.
Согласно одному варианту осуществления последовательность вариабельной области λ легкой цепи человека содержит фрагмент кластера В локуса легкой цепи человека. Согласно конкретному варианту осуществления фрагмент кластера В локуса λ легкой цепи человека продолжается от hVλ5-52 до hVλ1-40.
Согласно одному варианту осуществления последовательность вариабельной области λ легкой цепи человека содержит геномный фрагмент кластера A и геномный фрагмент кластера В. Согласно одному варианту осуществления последовательность вариабельной области λ легкой цепи человека содержит по меньшей мере один генный сегмент кластера A и по меньшей мере один генный сегмент кластера В.
Согласно одному варианту осуществления больше 10% нативного репертуара легкой цепи мыши происходит по меньшей мере из двух генных сегментов hVλ, выбранных из 2-8, 2-23, 1-40, 5-45 и 9-49. Согласно одному варианту осуществления больше 20% нативного репертуара легкой цепи мыши происходит по меньшей мере из трех генных сегментов hVλ, выбранных из 2-8, 2-23, 1-40, 5-45 и 9-49. Согласно одному варианту осуществления больше 30% нативного репертуара легкой цепи мыши происходит по меньшей мере из четырех генных сегментов hVλ, выбранных из 2-8, 2-23, 1-40, 5-45 и 9-49.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует легкую цепь иммуноглобулина, которая содержит λ вариабельную последовательность человека, слитую с константной областью мыши, причем мышь проявляет соотношение частоты использования κ к частоте использования λ, составляющее приблизительно 1:1.
Согласно одному варианту осуществления легкая цепь иммуноглобулина экспрессируется из эндогенного локуса легкой цепи мыши.
Согласно одному аспекту предусмотрена мышь, которая содержит последовательность вариабельной области λ легкой цепи (Vλ) и по меньшей мере одну последовательность J (J), смежную с последовательностью константной области легкой цепи мыши.
Согласно одному варианту осуществления мышь не содержит функциональный генный сегмент Vκ мыши и/или генный сегмент Jκ мыши.
Согласно одному варианту осуществления Vλ представляет собой Vλ человека (hVλ) и J представляет собой Jλ человека (hJλ). Согласно одному варианту осуществления hVλ и hJλ представляют собой нереаранжированные генные сегменты.
Согласно одному варианту осуществления мышь содержит множество нереаранжированных генных сегментов hVλ и по меньшей мере один генный сегмент hJλ. Согласно конкретному варианту осуществления множество нереаранжированных генных сегментов hVλ составляет по меньшей мере 12 генных сегментов, по меньшей мере 28 генных сегментов или по меньшей мере 40 генных сегментов.
Согласно одному варианту осуществления по меньшей мере один генный сегмент hJλ выбран из группы, состоящей из Jλ1, Jλ2, Jλ3, Jλ7 и их комбинации.
Согласно одному варианту осуществления эндогенный локус λ легкой цепи мыши удаляют полностью или частично.
Согласно одному варианту осуществления последовательность константной области κ легкой цепи мыши находится на эндогенном локусе легкой цепи мыши.
Согласно одному варианту осуществления приблизительно 10% - приблизительно 45% В-клеток мыши экспрессируют антитело, которое содержит легкую цепь, содержащую вариабельный домен λ легкой цепи (Vλ) человека и константный домен κ легкой цепи мыши (Сκ).
Согласно одному варианту осуществления вариабельный домен λ человека происходит из реаранжированной последовательности hVλ/hJλ, выбранной из группы, состоящей из 3-1/1, 3-1/7, 4-3/1, 4-3/7, 2-8/1, 3-9/1, 3-10/1, 3-10/3, 3-10/7, 2-14/1, 3-19/1, 2-23/1, 3-25/1, 1-40/1, 1-40/2, 1-40/3, 1-40/7, 7-43/1, 7-43/3, 1-44/1, 1-44/7, 5-45/1, 5-45/2, 5-45/7, 7-46/1, 7-46/2, 7-46/7, 9-49/1, 9-49/2, 9-49/7 и 1-51/1.
Согласно одному варианту осуществления мышь дополнительно содержит межгенную область Vκ-Jκ человека из локуса κ легкой цепи человека, причем межгенная область Vκ-Jκ человека является смежной с последовательностью Vλ и последовательностью J. Согласно конкретному варианту осуществления межгенная область Vκ-Jκ человека расположена между последовательностью Vλ и последовательностью J.
Согласно одному аспекту предусмотрена мышь, которая содержит (а) по меньшей мере 12 - по меньшей мере 40 нереаранжированных генных сегментов вариабельной области λ легкой цепи человека и по меньшей мере один генный сегмент Jλ человека на эндогенном локусе легкой цепи мыши; (b) межгенную последовательность Vκ-Jκ человека, расположенную между по меньшей мере 12 - по меньшей мере 40 генными сегментами вариабельной области легкой цепи человека и по меньшей мере одной последовательностью Jλ человека; причем мышь экспрессируют антитело, которое содержит легкую цепь, содержащую домен Vλ человека и домен Сκ мыши.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует антитело, содержащее легкую цепь, которая содержит вариабельную последовательность λ и константную последовательность κ.
Согласно одному варианту осуществления мышь проявляет соотношение частоты использования κ к частоте использования λ, составляющее приблизительно 1:1.
Согласно одному варианту осуществления популяция незрелых В-клеток, полученных из костного мозга мыши, проявляет соотношение частоты использования κ к частоте использования λ, составляющее приблизительно 1:1.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина, функционально связанный с локусом легкой цепи мыши, который содержит ген CL мыши.
Согласно одному варианту осуществления генные сегменты Vλ и/или Jλ представляют собой генные сегменты человека. Согласно одному варианту осуществления генные сегменты Vλ и/или Jλ представляют собой генные сегменты мыши, и CL представляет собой Сκ мыши.
Согласно одному варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус κ легкой цепи. Согласно одному варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус λ легкой цепи.
Согласно одному варианту осуществления нереаранжированные генные сегменты Vλ и Jλ находятся на эндогенном локусе легкой цепи мыши.
Согласно одному варианту осуществления нереаранжированные генные сегменты Vλ и Jλ иммуноглобулина находятся на трансгене.
Согласно одному варианту осуществления мышь дополнительно содержит замещение одного или нескольких генных сегментов V, D и/или J тяжелой цепи одним или несколькими генными сегментами V, D и/или J человека на эндогенном локусе тяжелой цепи иммуноглобулина мыши.
Согласно одному варианту осуществления мышь содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши.
Согласно одному варианту осуществления мышь содержит нереаранжированный вариабельный генный сегмент λ легкой цепи (Vλ) иммуноглобулина человека и λ соединяющий генный сегмент (Jλ) на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши.
Согласно одному варианту осуществления вариабельный генный локус легкой цепи ("локус VL") содержит по меньшей мере один генный сегмент Vλ человека (hVλ). Согласно одному варианту осуществления локус VL содержит по меньшей мере один генный сегмент Jλ человека (hJλ). Согласно другому варианту осуществления локус VL содержит до четырех генных сегментов hJλ. Согласно одному варианту осуществления локус VL содержит смежную последовательность, содержащую геномную последовательность λ человека и геномную последовательность κ человека.
Согласно одному варианту осуществления вариабельный генный локус κ легкой цепи ("локус κ") содержит по меньшей мере один генный сегмент Vλ человека (hVλ). Согласно одному варианту осуществления локус κ содержит по меньшей мере один генный сегмент Jλ человека (hJλ). Согласно одному варианту осуществления локус κ содержит до четырех генных сегментов hJλ. Согласно одному варианту осуществления локус κ содержит по меньшей мере один hVλ и по меньшей мере один hJλ и не содержит или по существу не содержит функциональный генный сегмент Vκ области и не содержит или по существу не содержит функциональный генный сегмент Jκ области. Согласно одному варианту осуществления мышь содержит ни одного функционального генного сегмента Vκ области. Согласно одному варианту осуществления мышь содержит ни одного функционального генного сегмента Jκ области.
Согласно одному варианту осуществления вариабельный генный локус λ легкой цепи ("локус λ") содержит по меньшей мере один генный сегмент hVλ. Согласно одному варианту осуществления локус λ содержит по меньшей мере один генный сегмент Jλ человека (hJλ). Согласно другому варианту осуществления локус λ содержит до четырех генных сегментов hJλ.
Согласно одному варианту осуществления локус VL содержит множество hVλ. Согласно одному варианту осуществления множество hVλ выбирают так, чтобы получить в результате экспрессию репертуара вариабельной области λ легкой цепи, которая отражает приблизительно 10%, приблизительно 20%, приблизительно 30%, приблизительно 40%, приблизительно 50%, приблизительно 60%, приблизительно 70%, приблизительно 80% или приблизительно 90% или более частоты использования Vλ, наблюдаемой у человека. Согласно одному варианту осуществления локус VL содержит генные сегменты hVλ 1-40, 1-44, 2-8, 2-14, 3-21 и их комбинацию.
Согласно одному варианту осуществления hVλ включают в себя 3-1, 4-3, 2-8, 3-9, 3-10, 2-11 и 3-12. Согласно конкретному варианту осуществления локус VL содержит смежную последовательность локус λ легкой цепи человека, которая охватывает от Vλ3-12 до Vλ3-1. Согласно одному варианту осуществления локус VL содержит по меньшей мере 2, 3, 4, 5, 6, 7, 8, 9, 10, 11 или 12 hVλ. Согласно конкретному варианту осуществления hVλ включают в себя 3-1, 4-3, 2-8, 3-9, 3-10, 2-11 и 3-12. Согласно конкретному варианту осуществления локус VL содержит смежную последовательность λ локуса человека, которая охватывает от Vλ3-12 до Vλ3-1. Согласно одному варианту осуществления локус VL находится на эндогенном локусе κ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе κ, и эндогенный локус λ легкой цепи удаляют частично или полностью. Согласно одному варианту осуществления локус VL находится на эндогенном локусе λ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе λ, и эндогенный локус κ удаляют частично или полностью.
Согласно одному варианту осуществления локус VL содержит 13-28 или более hVλ. Согласно конкретному варианту осуществления hVλ включают в себя 2-14, 3-16, 2-18, 3-19, 3-21, 3-22, 2-23, 3-25 и 3-27. Согласно конкретному варианту осуществления локус κ содержит смежную последовательность локуса λ человека, которая охватывает от Vλ3-27 до Vλ3-1. Согласно одному варианту осуществления локус VL находится на эндогенном локусе κ.
Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе κ, и эндогенный локус λ легкой цепи удаляют частично или полностью. Согласно другому варианту осуществления локус VL находится на эндогенном локусе λ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе λ, и эндогенный локус κ удаляют частично или полностью.
Согласно одному варианту осуществления локус VL содержит 29-40 hVλ. Согласно конкретному варианту осуществления локус κ содержит смежную последовательность локуса λ человека, которая охватывает от Vλ3-29 до Vλ3-1, и смежную последовательность локуса λ человека, которая охватывает от Vλ5-52 до Vλ1-40. Согласно конкретному варианту осуществления вся или по существу вся последовательность между hVλ1-40 и hVλ3-29 у генетически модифицированной мыши состоит по существу из последовательности λ человека приблизительно из 959 п.н., встречающейся в природе (например, в человеческой популяции) ниже генного сегмента hVλ1-40 (ниже 3' нетранслируемой части), сайта фермента рестрикции (например, PI-SceI), за которым следует λ последовательность человека приблизительно из 3431 п.н. выше генного сегмента hVλ3-29, встречающегося в природе. Согласно одному варианту осуществления локус VL находится на эндогенном локусе κ мыши. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе κ мыши, и эндогенный локус λ легкой цепи мыши удаляют частично или полностью. Согласно другому варианту осуществления локус VL находится на эндогенном локусе λ мыши. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе λ мыши, и эндогенный локус κ мыши удаляют частично или полностью.
Согласно одному варианту осуществления локус VL содержит по меньшей мере один hJλ. Согласно одному варианту осуществления локус VL содержит множество hJλ. Согласно одному варианту осуществления VL локус содержит по меньшей мере 2, 3, 4, 5, 6 или 7 hJλ. Согласно конкретному варианту осуществления локус VL содержит четыре hJλ. Согласно конкретному варианту осуществления четыре hJλ представляют собой hJλ1, hJλ2, hJλ3 и hJλ7. Согласно одному варианту осуществления локус VL представляет собой локус κ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе κ, и эндогенный локус λ легкой цепи удаляют частично или полностью. Согласно одному варианту осуществления локус VL содержит один hJλ. Согласно конкретному варианту осуществления один hJλ представляет собой hJλ1. Согласно одному варианту осуществления локус VL находится на эндогенном локусе κ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе κ, и эндогенный локус λ легкой цепи удаляют частично или полностью. Согласно другому варианту осуществления локус VL находится на эндогенном локусе λ. Согласно конкретному варианту осуществления локус VL находится на эндогенном локусе λ, и эндогенный локус κ удаляют частично или полностью.
Согласно одному варианту осуществления локус VL содержит по меньшей мере один hVλ, по меньшей мере один hJλ и ген Сκ мыши. Согласно одному варианту осуществления локус VL содержит по меньшей мере один hVλ, по меньшей мере один hJλ и ген Сλ мыши. Согласно конкретному варианту осуществления ген Сλ мыши представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95%, 96%, 97%, 98% или по меньшей мере на 99% идентичен Сλ2 мыши.
Согласно одному варианту осуществления мышь содержит замещение на эндогенном локусе κ мыши эндогенных генных сегментов Vκ мыши одним или несколькими генными сегментами hVλ, причем генные сегменты Vκ функционально связаны с эндогенным геном области Сκ мыши, так что мышь реаранжирует генные сегменты Vλ человека и экспрессирует обратную химерную легкую цепь иммуноглобулина, которая содержит домен Vλ человека и Сκ мыши. Согласно одному варианту осуществления 90-100% нереаранжированных генных сегментов Vκ мыши замещают по меньшей мере одним нереаранжированным генным сегментом hVλ. Согласно конкретному варианту осуществления все или по существу все эндогенные генные сегменты Vκ мыши замещают по меньшей мере одним нереаранжированным генным сегментом hVλ. Согласно одному варианту осуществления замещение происходит с помощью по меньшей мере 12, по меньшей мере 28 или по меньшей мере 40 нереаранжированных генных сегментов hVλ. Согласно одному варианту осуществления замещение происходит с помощью по меньшей мере 7 функциональных нереаранжированных генных сегментов hVλ, по меньшей мере 16 функциональных нереаранжированных генных сегментов hVλ или по меньшей мере 27 функциональных нереаранжированных генных сегментов hVλ. Согласно одному варианту осуществления мышь содержит замещение всех генных сегментов Jκ мыши по меньшей мере одним нереаранжированным генным сегментом hJλ. Согласно одному варианту осуществления по меньшей мере один нереаранжированный генный сегмент Jλ выбран из Jλ1, Jλ2, Jλ3, Jλ4, Jλ5, Jλδ, Jλ7 и их комбинации. Согласно конкретному варианту осуществления один или несколько генных сегментов hVλ выбраны из генного сегмента hVλ 3-1, 4-3, 2-8, 3-9, 3-10, 2-11, 3-12, 2-14, 3-16, 2-18, 3-19, 3-21, 3-22, 2-23, 3-25, 3-27, 1-40, 7-43, 1-44, 5-45, 7-46, 1-47, 5-48, 9-49, 1-50, 1-51, 5-52 и их комбинации. Согласно конкретному варианту осуществления по меньшей мере один нереаранжированный генный сегмент hJλ выбран из Jλ1, Jλ2, Jλ3, Jλ7 и их комбинации.
Согласно одному варианту осуществления мышь содержит замещение эндогенных генных сегментов Vλ мыши на эндогенном локусе λ мыши одним или несколькими генными сегментами Vλ человека на эндогенном локусе λ мыши, причем генные сегменты hVλ функционально связаны с геном области Сλ мыши, так что мышь реаранжирует генные сегменты hVλ и экспрессирует обратную химерную легкую цепь иммуноглобулина, которая содержит домен hVλ и Сλ мыши. Согласно конкретному варианту осуществления ген Сλ мыши представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши. Согласно одному варианту осуществления 90-100% нереаранжированных генных сегментов Vλ мыши замещают по меньшей мере одним нереаранжированным генным сегментом hVλ. Согласно конкретному варианту осуществления все или по существу все эндогенные генные сегменты Vλ мыши замещают по меньшей мере одним нереаранжированным генным сегментом hVλ. Согласно одному варианту осуществления замещение происходит с помощью по меньшей мере 12, по меньшей мере 28 или по меньшей мере 40 нереаранжированных генных сегментов hVλ. Согласно одному варианту осуществления замещение происходит с помощью по меньшей мере 7 функциональных нереаранжированных генных сегментов hVλ, по меньшей мере 16 функциональных нереаранжированных генных сегментов hVλ или по меньшей мере 27 функциональных нереаранжированных генных сегментов hVλ. Согласно одному варианту осуществления мышь содержит замещение всех генных сегментов Jλ мыши по меньшей мере одним нереаранжированным генным сегментом hJλ. Согласно одному варианту осуществления по меньшей мере один нереаранжированный генный сегмент hJλ выбран из Jλ1, Jλ2, Jλ3, Jλ4, Jλ5, Jλ6, Jλ7 и их комбинации. Согласно конкретному варианту осуществления один или несколько генных сегментов hVλ выбраны из генного сегмента hVλ 3-1, 4-3, 2-8, 3-9, 3-10, 2-1 1, 3-12, 2-14, 3-16, 2-18, 3-19, 3-21, 3-22, 2-23, 3-25, 3-27, 1-40, 7-43, 1-44, 5-45, 7-46, 1-47, 5-48, 9-49, 1-50, 1-51, 5-52 и их комбинации. Согласно конкретному варианту осуществления по меньшей мере один нереаранжированный генный сегмент hJλ выбран из Jλ1, Jλ2, Jλ3, Jλ7 и их комбинации.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, которая содержит последовательность межгенной области Vκ-Jκ человека, расположенную на эндогенном локусе κ легкой цепи мыши.
Согласно одному варианту осуществления последовательность межгенной области Vκ-Jκ человека находится на эндогенном локусе κ легкой цепи мыши, который содержит генный сегмент hVλ и Jλ, и последовательность межгенной области Vκ-Jκ человека расположена между генными сегментами hVλ и hJλ. Согласно конкретному варианту осуществления генные сегменты hVλ и hJλ способны к рекомбинации для образования функционального вариабельного домена λ легкой цепи человека у мыши.
Согласно одному варианту осуществления предусмотрена мышь, которая содержит множество hVλ и один или несколько hJλ, и последовательность межгенной области Vκ-Jκ человека расположена, относительно транскрипции, ниже проксимальной или наиболее 3' последовательности hVλ и выше или 5' от первой последовательности hJλ.
Согласно одному варианту осуществления межгенная область Vκ-Jκ человека представляет собой область, расположенную приблизительно 130 п.н. ниже или 3' от генного сегмента Vκ4-1 человека, приблизительно 130 п.н. ниже от 3' нетранслируемой области генного сегмента Vκ4-1 человека, и охватывает приблизительно 600 п.н. выше или 5' от генного сегмента Jκ1 человека. Согласно конкретному варианту осуществления размер межгенной области Vκ-Jκ человека составляет приблизительно 22,8 т.п.н. Согласно одному варианту осуществления межгенная область Vκ-Jκ приблизительно на 90% или более, на 91% или более, на 92% или более, на 93% или более, на 94% или более или приблизительно на 95% или более идентична межгенной области Vκ-Jκ человека, продолжающейся от конца 3' нетранслируемой области генного сегмента Vκ4-1 человека до приблизительно 600 п.н. выше генного сегмента Jκ1 человека. Согласно одному варианту осуществления межгенная область Vκ-Jκ содержит SEQ ID NO: 158. Согласно конкретному варианту осуществления межгенная область Vκ-Jκ содержит функциональный фрагмент SEQ ID NO: 158. Согласно конкретному варианту осуществления межгенная область Vκ-Jκ представляет собой SEQ ID NO: 158.
Согласно одному аспекту предусмотрено отличное от человека животное, не относящаяся к человеку клетка (например, ES клетка или плюрипотентная клетка), не относящийся к человеку зародыш или не относящаяся к человеку ткань, которые содержат указанную последовательность межгенной области Vκ-Jκ человека, причем последовательность межгенная область является эктопической. Согласно конкретному варианту осуществления эктопическая последовательность расположена на гуманизированном эндогенном не относящемся к человеку локусе иммуноглобулина. Согласно одному варианту осуществления отличное от человека животное выбрано из мыши, крысы, хомяка, козы, коровы, овцы и отличного от человека примата.
Согласно одному аспекту предусмотрен выделенный конструкт нуклеиновой кислоты, который содержит указанную последовательность межгенной области Vκ-Jκ человека. Согласно одному варианту осуществления конструкт нуклеиновой кислоты содержит нацеливающие плечи для нацеливания последовательности межгенной области Vκ-Jκ человека на локус легкой цепи мыши. Согласно конкретному варианту осуществления локус легкой цепи мыши представляет собой локус κ. Согласно конкретному варианту осуществления нацеливающие плечи нацеливают межгенную область Vκ-Jκ человека на модифицированный эндогенный локус κ мыши, причем нацеливание происходит в положение между последовательностью hVλ и последовательностью hJλ.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем мышь содержит не более двух аллелей легкой цепи, причем аллели легкой цепи содержат (а) нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина человека на эндогенном локусе легкой цепи мыши, который содержит ген CL мыши; и (b) нереаранжированный генный сегмент VL и JL иммуноглобулина на эндогенном локусе легкой цепи мыши, который содержит ген CL мыши.
Согласно одному варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус κ. Согласно другому варианту осуществления эндогенный локус легкой цепи мыши представляет собой локус λ.
Согласно одному варианту осуществления не более двух аллелей легкой цепи выбраны из аллеля κ и аллеля λ, двух аллелей κ и двух аллелей λ. Согласно конкретному варианту осуществления один из двух аллелей легкой цепи представляет собой аллель λ, который содержит ген Сλ2.
Согласно одному варианту осуществления мышь содержит один функциональный локус легкой цепи иммуноглобулина и один нефункциональный локус легкой цепи, причем функциональный локус легкой цепи содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина человека на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши.
Согласно одному варианту осуществления мышь содержит один функциональный локус легкой цепи иммуноглобулина и один нефункциональный локус легкой цепи, причем функциональный локус легкой цепи содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина человека на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши. Согласно одному варианту осуществления ген Сλ представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному варианту осуществления мышь дополнительно содержит по меньшей мере один аллель тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления по меньшей мере одни аллель тяжелой цепи иммуноглобулина содержит генный сегмент VH человека, генный сегмент DH человека и генный сегмент JH человека на эндогенном локусе тяжелой цепи мыши, который содержит ген тяжелой цепи человека, который экспрессирует относящуюся к человеку/мыши тяжелую цепь. Согласно конкретному варианту осуществления мышь содержит два аллеля тяжелой цепи иммуноглобулина, и мышь экспрессирует относящуюся к человеку/мыши тяжелую цепь.
Согласно одному варианту осуществления мышь содержит первый аллель легкой цепи, который содержит нереаранжированный hVλ и нереаранжированный hJλ, на эндогенном локусе κ мыши, который содержит эндогенный ген Сκ; и второй аллель легкой цепи, который содержит нереаранжированный hVλ и нереаранжированный hJλ, на эндогенном локусе κ мыши, который содержит эндогенный ген Сκ. Согласно конкретному варианту осуществления первый и второй аллели легкой цепи представляют собой только функциональные аллели легкой цепи генетически модифицированной мыши. Согласно конкретному варианту осуществления мышь содержит нефункциональный локус λ. Согласно одному варианту осуществления генетически модифицированная мышь не экспрессирует легкую цепь, которая содержит константную область λ.
Согласно одному варианту осуществления мышь содержит первый аллель легкой цепи, который содержит нереаранжированный hVλ и нереаранжированный hJλ, на эндогенном локусе κ мыши, который содержит эндогенный ген Сκ; и второй аллель легкой цепи, который содержит нереаранжированный hVλ и нереаранжированный hJλ, на эндогенном локусе λ мыши, который содержит эндогенный ген Сλ. Согласно конкретному варианту осуществления первый и второй аллели легкой цепи представляют собой только функциональные аллели легкой цепи генетически модифицированной мыши. Согласно одному варианту осуществления эндогенный ген Сλ представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному варианту осуществления мышь содержит шесть аллелей иммуноглобулина, причем первый аллель содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши, второй содержит нереаранжированный генный сегмент Vκ и Jκ иммуноглобулина на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши, третий содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши, каждый из четвертого и пятого независимо содержат нереаранжированный генный сегмент VH и DH и JH на эндогенном локусе тяжелой цепи мыши, который содержит ген тяжелой цепи мыши, и шестой содержит или (а) нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши, (b) локус λ, который является нефункциональным, или (с) полную или частичную делецию локуса λ.
Согласно одному варианту осуществления первый аллель содержит нереаранжированный hVλ и hJλ. Согласно одному варианту осуществления второй аллель содержит нереаранжированный hVκ и hJκ. Согласно одному варианту осуществления третий аллель содержит нереаранжированный hVλ и hJλ. Согласно одному варианту осуществления каждый из четвертого и пятого независимо содержат нереаранжированный hVH и hDH и hJH. Согласно одному варианту осуществления шестой аллель содержит эндогенный локус λ мыши, который полностью или частично удаляют.
Согласно одному варианту осуществления мышь содержит шесть аллелей иммуноглобулина, причем первый аллель содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши, второй содержит нереаранжированный генный сегмент Vλ и Jλ иммуноглобулина на эндогенном локусе λ легкой цепи мыши, который содержит ген Сλ мыши, третий содержит нереаранжированный генный сегмент Vκ и Jκ иммуноглобулина на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши, каждый из четвертого и пятого независимо содержат нереаранжированный генный сегмент VH и DH и JH на эндогенном локусе тяжелой цепи мыши, который содержит ген тяжелой цепи мыши, и шестой содержит или (а) нереаранжированный генный сегмент Vκ и Jκ иммуноглобулина на эндогенном локусе κ легкой цепи мыши, который содержит ген Сκ мыши, (b) локус κ, который является нефункциональным, или (с) делецию одного или нескольких элементов локуса κ.
Согласно одному варианту осуществления первый аллель содержит нереаранжированный генный сегмент hVλ и hJλ. Согласно одному варианту осуществления второй аллель содержит нереаранжированный генный сегмент hVλ и hJλ. Согласно одному варианту осуществления третий аллель содержит нереаранжированный генный сегмент hVκ и hJκ. Согласно одному варианту осуществления каждый из четвертого и пятого независимо содержат нереаранжированный генный сегмент hVH и hDH и hJH. Согласно одному варианту осуществления шестой аллель содержит эндогенный локус κ мыши, который является функционально выключенным.
Согласно одному варианту осуществления генетически модифицированная мышь содержит В-клетку, которая содержит реаранжированный ген антитела, содержащий реаранжированный домен hVλ, функционально связанный с доменом CL мыши. Согласно одному варианту осуществления домен CL мыши выбран из домена Сκ мыши и домена Сλ мыши. Согласно конкретному варианту осуществления домен Сλ мыши происходит из гена Сλ2. Согласно конкретному варианту осуществления домен Сλ мыши происходит из домена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, которая экспрессирует область Vλ на CL, которая представляет собой Сκ. Согласно одному аспекту предусмотрена генетически модифицированная мышь, которая экспрессирует область hVλ на CL, выбранной из Сκ человека, Сλ человека или Сκ мыши. Согласно одному аспекту предусмотрена генетически модифицированная мышь, которая экспрессирует область hVλ на Сκ мыши.
Согласно одному варианту осуществления приблизительно 10-50% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 9-28% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно конкретному варианту осуществления приблизительно 23-34% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 9-11% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно конкретному варианту осуществления приблизительно 19-31% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), которых 9-17% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно конкретному варианту осуществления приблизительно 21-38% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 24-27% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно конкретному варианту осуществления приблизительно 10-14% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 9-13% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно конкретному варианту осуществления приблизительно 31-48% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 15-21% из них экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши. Согласно конкретному варианту осуществления приблизительно 30-38% спленоцитов мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 33-48% экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно одному варианту осуществления приблизительно 52-70% клеток костного мозга мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 31-47% незрелых В-клеток (т.е. CD19-положительных/В220-промежуточных положительных/IgM-положительных) экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно одному варианту осуществления приблизительно 60% клеток костного мозга мыши представляют собой В-клетки (т.е. CD19-положительные), из которых приблизительно 38,3% незрелых В-клеток (т.е. CD19-положительных/В220-промежуточных положительных/IgM-положительных) экспрессируют легкую цепь иммуноглобулина, содержащую домен hVλ, слитый с доменом Сκ мыши.
Согласно одному варианту осуществления мышь экспрессирует антитело, содержащее легкую цепь, которая содержит вариабельный домен, происходящий из генного сегмента V человека и J человека, и константный домен, происходящий из гена константной области мыши. Согласно одному варианту осуществления ген константной области мыши представляет собой ген Сκ. Согласно другому варианту осуществления ген константной области мыши представляет собой ген Сλ. Согласно конкретному варианту осуществления область Сλ представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши. Согласно конкретному варианту осуществления антитело дополнительно содержит тяжелую цепь, содержащую вариабельный домен, происходящий из генного сегмента V человека, D человека и J человека, и константный домен тяжелой цепи, происходящий из гена константной области тяжелой цепи мыши. Согласно одному варианту осуществления ген константной области тяжелой цепи мыши содержит последовательность шарнир-CH2-CH3 константного домена тяжелой цепи. Согласно другому варианту осуществления ген константной области тяжелой цепи мыши содержит последовательность CH1-шарнир-CH2-CH3 константного домена тяжелой цепи. Согласно другому варианту осуществления ген константной области тяжелой цепи мыши содержит последовательность CH1-CH2-CH3-CH4 константного домена тяжелой цепи. Согласно другому варианту осуществления ген константной области тяжелой цепи мыши содержит последовательность CH2-CH3-CH4 константного домена тяжелой цепи.
Согласно одному варианту осуществления мышь экспрессирует антитело, содержащее легкую цепь, которая содержит реаранжированную последовательность Vλ-Jλ человека и последовательность Сκ мыши. Согласно одному варианту осуществления реаранжированная последовательность Vλ-Jλ человека происходит из реаранжировки генных сегментов hVλ, выбранных из генного сегмента 3-1, 4-3, 2-8, 3-9, 3-10, 2-14, 3-19, 2-23, 3-25, 1-40, 7-43, 1-44, 5-45, 7-46, 1-47, 9-49 и 1-51. Согласно одному варианту осуществления реаранжированная последовательность Vλ-Jλ человека происходит из реаранжировки генных сегментов hJλ, выбранных из генного сегмента Jλ1, Jλ2, Jλ3 и Jλ7.
Согласно одному варианту осуществления мышь экспрессирует антитело, содержащее легкую цепь, которая содержит реаранжированную вариабельную область λ легкой цепи иммуноглобулина, содержащую последовательность Vλ/Jλ человека выбранная из 3-1/1, 3-1/7, 4-3/1, 4-3/7, 2-8/1, 3-9/1, 3-10/1, 3-10/3, 3-10/7, 2-14/1, 3-19/1, 2-23/1, 3-25/1, 1-40/1, 1-40/2, 1-40/3, 1-40/7, 7-43/1, 7-43/3, 1-44/1, 1-44/7, 5-45/1, 5-45/2, 5-45/7, 7-46/1, 7-46/2, 7-46/7, 9-49/1, 9-49/2, 9-49/7 и 1-51/1. Согласно конкретному варианту осуществления В-клетка экспрессирует антитело, содержащее вариабельный домен тяжелой цепи иммуноглобулина человека, слитый с константным доменом тяжелой цепь мыши, и вариабельный домен λ легкой цепи иммуноглобулина человека, слитый с константным доменом κ легкой цепи мыши.
Согласно одному аспекту предусмотрена мышь, которая экспрессирует антитело, содержащее (а) тяжелую цепь, содержащую вариабельный домен тяжелой цепи, происходящий из нереаранжированного генного сегмента вариабельной области тяжелой цепи человека, причем вариабельный домен тяжелой цепи слит с константной (CH) областью тяжелой цепи мыши; и (b) легкую цепь, содержащую вариабельный домен легкой цепи, происходящий из нереаранжированного hVλ и hJλ, причем вариабельный домен легкой цепи слит с областью CL мыши.
Согласно одному варианту осуществления мышь содержит (i) локус тяжелой цепи, который содержит замещение всех или по существу всех функциональных эндогенных генных сегментов V, D и J мыши всеми или по существу всеми функциональными генными сегментами V, D и J человека, ген CH мыши, (ii) первый локус κ легкой цепи, содержащий замещение всех или по существу всех функциональных эндогенных генных сегментов Vκ и Jκ мыши всеми, по существу всеми или множеством функциональных генных сегментов hVλ и hJλ, и ген CL мыши, (iii) второй локус κ легкой цепи, содержащий замещение всех или по существу всех функциональных эндогенных генных сегментов Vκ и Jκ мыши всеми, по существу всеми или множеством функциональных генных сегментов hVκ и hJκ, и ген Сκ мыши. Согласно одному варианту осуществления мышь не экспрессирует антитело, которое содержит область Сλ. Согласно одному варианту осуществления мышь содержит делецию гена Сλ и/или генного сегмента Vλ и/или Jλ. Согласно одному варианту осуществления мышь содержит нефункциональный локус λ легкой цепи. Согласно конкретному варианту осуществления локус λ легкой цепи удаляют полностью или частично.
Согласно одному варианту осуществления мышь содержит (i) локус тяжелой цепи, который содержит замещение всех или по существу всех функциональных эндогенных генных сегментов V, D и J мыши всеми или по существу всеми функциональными генными сегментами V, D и J человека, ген CH мыши, (ii) первый локус λ легкой цепи, содержащий замещение всех или по существу всех функциональных эндогенных генных сегментов Vλ и Jλ мыши всеми, по существу всеми или множеством функциональных генных сегментов hVλ и hJλ, и ген Сλ мыши, (iii) второй локус λ легкой цепи, содержащий замещение всех или по существу всех функциональных эндогенных генных сегментов Vλ и Jλ мыши всеми, по существу всеми или множеством функциональных генных сегментов hVλ и hJλ, и ген Сλ мыши. Согласно конкретному варианту осуществления ген Сλ мыши представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному варианту осуществления мышь содержит делецию гена Сκ и/или генного сегмента Vκ и/или Jκ. Согласно одному варианту осуществления мышь содержит нефункциональный локус κ легкой цепи.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, которая экспрессирует антитело, причем больше чем 10%, больше чем 15%, больше чем 20%, больше чем 25%, больше чем 30%, больше чем 35%, больше чем 40%, больше чем 60%, больше чем 70%, больше чем 80% или более чем 90% от общего количества производимых мышью антител IgG содержит происходящий из λ вариабельный домен, и причем мышь экспрессирует антитела, содержащие происходящий из κ вариабельный домен, слитый с областью Сκ мыши. Согласно конкретным вариантам осуществления приблизительно 15-40%, 20-40%, 25-40%, 30-40% или 35-40% от общего количества производимого мышью антитела содержит происходящий из λ вариабельный домен.
Согласно одному варианту осуществления происходящий из λ вариабельный домен происходит из hVλ и hJλ. Согласно одному варианту осуществления происходящий из λ вариабельный домен находится в легкой цепи, которая содержит область Сκ мыши. Согласно конкретному варианту осуществления происходящий из λ вариабельные область находится в легкой цепи, которая содержит область Сλ мыши. Согласно другому конкретному варианту осуществления область Сλ представляет собой область Сλ2. Согласно одному варианту осуществления происходящий из κ вариабельный домен происходит из hVκ и hJκ, и согласно конкретному варианту осуществления находится в легкой цепи, которая содержит область Сκ мыши.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, который содержит вышележащее гомологичное плечо и нижележащее гомологичное плечо, причем вышележащее и нижележащее гомологичные плечи нацеливают конструкт на κ локус мыши, и конструкт содержит функциональный нереаранжированный сегмент hVλ и функциональный нереаранжированный сегмент hJλ, и селективную или маркерную последовательность.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания последовательности λ мыши выше Vλ2 мыши, кассету селекции, фланкированной 5' и 3' сайтами распознавания рекомбиназы, и нацеливающее плечо для нацеливания последовательности λ мыши 3' по отношению к Jλ2 мыши. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную Frt кассету Hyg-TK. Согласно одному варианту осуществления 3' нацеливающие плечо содержит Сλ2, Jλ4, Сλ4 мыши, и энхансер 2.4 мыши.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающие плечо для нацеливания локуса λ мыши 5' по отношению к Vλ1, кассету селекции, фланкированной 5' и 3' сайтами распознавания рекомбиназы, и 3' нацеливающие плечо для нацеливания последовательности λ мыши 3' по отношению к мыши Сλ1. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную lox кассету неомицина. Согласно одному варианту осуществления 3' нацеливающее плечо содержит энхансер λ 3' мыши и λ 3' энхансер 3.1 мыши.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий в направлении 5'-3' относительно направления транскрипции нацеливающее плечо для нацеливания локуса λ мыши 5' по отношению к Vλ2, кассету селекции, фланкированной 5' и 3' сайтами распознавания рекомбиназы, и 3' нацеливающее плечо для нацеливания последовательности λ мыши 3' по отношению к Jλ2 мыши и 5' по отношению к Сλ2 мыши. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную Frt кассету гигромицина-TK. Согласно одному варианту осуществления 3' нацеливающее плечо содержит генные сегменты Cλ2-Jλ4-Cλ4 мыши и λ энхансер 2.4 мыши.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания локуса λ мыши 5' по отношению к Vλ2, кассету селекции, фланкированную 5' и 3' сайтами распознавания рекомбиназы, геномный фрагмент человека, содержащий смежную область локуса λ легкой цепи человека из hVλ3-12 ниже по отношению к концу hJλ1 и 3' нацеливающее плечо для нацеливания последовательности λ мыши 3' по отношению к Jλ2 мыши. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную Frt кассету неомицина. Согласно одному варианту осуществления 3' нацеливающее плечо содержит генные сегменты Cλ2-Jλ4-Сλ4 мыши и λ энхансер 2.4 мыши.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий смежную область локуса λ легкой цепи человека из hVλ3-12 ниже по отношению к концу hλJ1.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания локуса λ мыши 5' по отношению к Vλ2, кассету селекции, фланкированную 5' и 3' сайтами распознавания рекомбиназы, и геномный фрагмент человека, содержащий смежную область локуса λ легкой цепи человека из hVλ3-27 ниже по отношению к концу hVλ2-8. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную Frt кассету гигромицина. Согласно одному варианту осуществления геномный фрагмент человека содержит 3' нацеливающее плечо. Согласно конкретному варианту осуществления 3' нацеливающее плечо содержит приблизительно 53 т.п.н. локуса λ легкой цепи человека из hVλ3-12 ниже по отношению к концу hVλ2-8.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий смежную область локуса λ легкой цепи человека из hVλ3-27 ниже по отношению к концу hVλ3-12.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания локуса λ мыши 5' по отношению к Vλ2, кассету селекции, фланкированную 5' и 3' сайтами распознавания рекомбиназы, первый геномный фрагмент человека, содержащий смежную область локуса λ легкой цепи человека из hVλ5-52 ниже по отношению к концу hVλ1-40, сайт фермента рестрикции и второй геномный фрагмент человека, содержащий смежную область локуса λ легкой цепи человека из hVλ3-29 ниже по отношению к концу hVλ82K. Согласно одному варианту осуществления кассета селекции представляет собой фланкированную Frt кассету неомицина. Согласно одному варианту осуществления сайт фермента рестрикции представляет собой сайт хоминг-эндонуклеазы. Согласно конкретному варианту осуществления хоминг-эндонуклеаза представляет собой PI-SceI. Согласно одному варианту осуществления второй геномный фрагмент человека представляет собой 3' нацеливающее плечо. Согласно конкретному варианту осуществления 3' нацеливающее плечо содержит приблизительно 27 т.п.н. локуса λ легкой цепи человека из hVλ3-29 ниже по отношению к концу hVλ82K.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий смежную область локуса λ легкой цепи человека из hVλ5-52 ниже по отношению к концу hVλ1-40.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания локуса κ мыши 5' по отношению к эндогенным генным сегментам Vκ, два расположенных рядом сайта распознавания рекомбиназы, кассету селекции 3' по отношению к расположенным рядом сайтам распознавания рекомбиназы и 3' нацеливающее плечо для нацеливания последовательности κ мыши 5' по отношению к вариабельным генным сегментам κ легкой цепи. Согласно одному варианту осуществления расположенные рядом сайты распознавания рекомбиназы находятся в противоположной ориентации по отношению друг к другу. Согласно конкретному варианту осуществления сайты распознавания рекомбиназы являются различными. Согласно другому конкретному варианту осуществления сайты распознавания рекомбиназы представляет собой сайт loxP и сайт lox511. Согласно одному варианту осуществления кассета селекции представляет собой кассету неомицина.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, нацеливающее плечо для нацеливания локуса κ мыши 5' по отношению к генным сегментам Jκ мыши, кассету селекции, сайт распознавания рекомбиназы 3' по отношению к кассете селекции и 3' нацеливающее плечо для нацеливания последовательности κ мыши 3' по отношению к генным сегментам Jκ мыши и 5' по отношению к интронному энхансеру κ мыши. Согласно одному варианту осуществления кассета селекции представляет собой кассету гигромицина-TK. Согласно одному варианту осуществления сайт распознавания рекомбиназы расположен в том же направлении относительно транскрипции, что и кассета селекции. Согласно конкретному варианту осуществления сайт распознавания рекомбиназы представляет собой сайт loxP.
Согласно одному аспекту предусмотрен выделенный конструкт ДНК, содержащий, в направлении 5'-3' относительно направления транскрипции, первый геномный фрагмент мыши, содержащий последовательность 5' от эндогенных генных сегментов Vκ мыши, первый сайт распознавания рекомбиназы, второй сайт распознавания рекомбиназы и второй геномный фрагмент мыши, содержащий последовательность 3' от эндогенных генных сегментов Jκ мыши и 5' от интронного энхансера κ мыши.
Согласно одному аспекту предусмотрена генетически модифицированная мышь, причем генетическая модификация предусматривает модификацию с помощью одного или нескольких описанных выше или в настоящем документе конструктов ДНК.
Согласно одному аспекту предусмотрено применение выделенного конструкта ДНК для получения описанной в настоящем документе мыши. Согласно одному аспекту предусмотрено применение описанного в настоящем документе выделенного конструкта ДНК в способе получения антигенсвязывающего белка.
Согласно одному аспекту предусмотрена не относящаяся к человеку стволовая клетка, которая содержит нацеливающий вектор, который содержит описанный выше и в настоящем документе ДНК конструкт. Согласно одному аспекту предусмотрена не относящаяся к человеку стволовая клетка, причем не относящаяся к человеку стволовая клетка происходит от описанной в настоящем документе мыши.
Согласно одному варианту осуществления не относящаяся к человеку стволовая клетка представляет собой эмбриональную стволовую (ES) клетку. Согласно конкретному варианту осуществления ES клетка представляет собой ES клетку мыши.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе не относящейся к человеку стволовой клетки для получения описанной в настоящем документе мыши. Согласно одному аспекту предусмотрено применение описанной в настоящем документе не относящейся к человеку стволовой клетки для получения антигенсвязывающего белка.
Согласно одному аспекту предусмотрен зародыш мыши, причем зародыш мыши содержит предусмотренную в настоящем документе генетическую модификацию. Согласно одному варианту осуществления предусмотрен зародыш мыши-хозяин, который содержит донорную ES клетку, причем донорная ES клетка содержит описанную в настоящем документе генетическую модификацию. Согласно одному варианту осуществления зародыш мыши представляет собой зародыш на стадии пре-морулы. Согласно конкретному варианту осуществления зародыш на стадии пре-морулы представляет собой зародыш на стадии 4 клеток или зародыш на стадии 8 клеток. Согласно другому конкретному варианту осуществления зародыш мыши представляет собой бластоцисту.
Согласно одному аспекту предусмотрено применение описанного в настоящем документе зародыша мыши для получения описанной в настоящем документе мыши. Согласно одному аспекту предусмотрено применение описанного в настоящем документе зародыша мыши для получения антигенсвязывающего белка.
Согласно одному аспекту предусмотрена не относящаяся к человеку клетка, причем не относящаяся к человеку клетка содержит реаранжированную последовательность гена легкой цепи иммуноглобулина, происходящую от описанной в настоящем документе генетически модифицированной мыши. Согласно одному варианту осуществления клетка представляет собой В-клетку. Согласно одному варианту осуществления клетка представляет собой гибридому. Согласно одному варианту осуществления клетка кодирует вариабельный домен легкой цепи иммуноглобулина и/или вариабельный домен тяжелой цепи иммуноглобулина, который является соматически мутированным.
Согласно одному аспекту предусмотрена не относящаяся к человеку клетка, причем не относящаяся к человеку клетка содержит реаранжированную последовательность гена легкой цепи иммуноглобулина, происходящую от описанной в настоящем документе генетически модифицированной мыши. Согласно одному варианту осуществления клетка представляет собой В-клетку. Согласно одному варианту осуществления клетка представляет собой гибридому. Согласно одному варианту осуществления клетка кодирует вариабельный домен легкой цепи иммуноглобулина и/или вариабельный домен тяжелой цепи иммуноглобулина, который является соматически мутированным.
Согласно одному аспекту предусмотрено применение описанной в настоящем документе не относящейся к человеку клетки для получения описанного в настоящем документе отличного от человека животного. Согласно одному аспекту предусмотрено применение описанной в настоящем документе не относящейся к человеку клетки для получения антигенсвязывающего белка. Согласно одному варианту осуществления отличное от человека животное выбрано из мыши, крысы, хомяка, овцы, козы, коровы и отличного от человека примата.
Согласно одному аспекту предусмотрена В-клетка мыши, которая экспрессирует легкую цепь иммуноглобулина, которая содержит (а) вариабельную область, происходящую из генного сегмента hVλ и генного сегмента hJλ; и (b) ген CL мыши. Согласно одному варианту осуществления ген CL мыши выбран из гена Сκ и Сλ. Согласно конкретному варианту осуществления ген Сλ представляет собой Сλ2. Согласно конкретному варианту осуществления ген Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши. Согласно одному варианту осуществления В-клетка мыши дополнительно экспрессирует когнатную тяжелую цепь, которая содержит (с) вариабельную область, происходящую из hVH, hDH и (d) сегмент hJH. Согласно одному варианту осуществления В-клетка не содержит реаранжированный ген λ. Согласно другому варианту осуществления В-клетка не содержит реаранжированный ген κ.
Согласно одному аспекту предусмотрен способ получения антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированное отличное от человека животное антигена, причем животное содержит геном, содержащий по меньшей мере один hVλ и по меньшей мере один hJλ на эндогенном локусе легкой цепи, причем эндогенный локус легкой цепи содержит не относящийся к человеку ген CL; (b) предоставление возможности генетически модифицированному животному развивать иммунный ответ на антиген; и (с) выделение из животного согласно (b) антитела, которое специфически распознает антиген, или выделение из животного согласно (b) клетки, содержащей домен иммуноглобулина, который специфически распознает антиген, причем антитело содержит легкую цепь, происходящую из hVλ, hJλ и гена CL животного. Согласно конкретному варианту осуществления не относящийся к человеку ген CL представляет собой ген Сκ мыши. Согласно одному варианту осуществления отличное от человека животное выбрано из мыши, крысы, хомяка, кролика, овцы, козы, коровы и отличного от человека примата.
Согласно одному варианту осуществления предусмотрен способ получения антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированного животного антигена, причем животное содержит геном, содержащий по меньшей мере один hVλ на эндогенном локусе κ и по меньшей мере один hJλ на локусе κ, причем локус κ содержит не относящийся к человеку ген Сκ; (b) предоставление возможности генетически модифицированному животному развивать иммунный ответ на антиген; и (с) выделение из животного согласно (b) антитела, которое специфически распознает антиген, или выделение из мыши согласно (b) клетки, содержащей домен иммуноглобулина, который специфически распознает антиген, причем антитело содержит легкую цепь, происходящую из hVλ, hJλ и не относящегося к человеку гена Сκ.
Согласно одному варианту осуществления константный ген κ легкой цепи выбран из гена Сκ человека и гена Сκ мыши.
Согласно одному варианту осуществления предусмотрен способ получения антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированного отличного от человека животного антигена, причем животное содержит геном, содержащий по меньшей мере один hVλ на локусе λ легкой цепи и по меньшей мере один Jλ на локусе λ легкой цепи, причем локус λ легкой цепи содержит не относящийся к человеку ген Сλ; (b) предоставление возможности генетически модифицированному животному развивать иммунный ответ на антиген; и (с) выделение из животного согласно (b) антитела, которое специфически распознает антиген, или выделение из животного согласно (b) клетки, содержащей домен иммуноглобулина, который специфически распознает антиген, или идентификацию в животном согласно (b) последовательности нуклеиновой кислоты, кодирующей вариабельный домен тяжелой и/или легкой цепи, который связывает антиген, причем антитело содержит легкую цепь, происходящую из hVλ, hJλ и не относящегося к человеку гена Сλ. Согласно одному варианту осуществления отличное от человека животное выбрано из мыши, крысы, хомяка, овцы, козы, коровы и отличного от человека примата.
Согласно одному варианту осуществления константный ген λ легкой цепи выбран из гена Сλ человека и не относящегося к человеку гена Сλ. Согласно одному варианту осуществления константный ген λ легкой цепи представляет собой ген Сλ человека. Согласно конкретному варианту осуществления ген Сλ человека выбран из Сλ1, Сλ2, Сλ3 и Сλ7. Согласно одному варианту осуществления константный ген λ легкой цепи представляет собой ген Сλ мыши или крысы. Согласно конкретному варианту осуществления ген Сλ мыши выбран из Сλ1, Сλ2 и Сλ3. Согласно более конкретному варианту осуществления ген Сλ мыши представляет собой Сλ2. Согласно другому конкретному варианту осуществления ген Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному аспекту предусмотрен способ получения реаранжированного гена антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированное отличное от человека животное антигена, причем генетическая модификация предусматривает hVλ и hJλ на эндогенном локусе легкой цепи, причем эндогенный локус легкой цепи содержит не относящийся к человеку ген CL или его функциональный фрагмент; и (b) идентификацию реаранжированного гена иммуноглобулина у указанного отличного от человека животного, причем реаранжированный ген иммуноглобулина содержит генный сегмент вариабельной области λ легкой цепи и ген CL или его функциональный фрагмент.
Согласно одному варианту осуществления способ дополнительно предусматривает клонирование последовательности нуклеиновой кислоты, кодирующей вариабельную область тяжелой и/или легкой цепи из животного, причем вариабельная область тяжелой и/или легкой цепи происходит из антитела, которое содержит Vλ человека и CL мыши.
Согласно одному варианту осуществления ген CL мыши или его функциональный фрагмент выбран из гена CL человека и гена CL мыши или его функционального фрагмента.
Согласно одному варианту осуществления предусмотрен способ получения реаранжированного гена антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированное отличное от человека животное антигена, причем генетическая модификация предусматривает hVλ и hJλ на локусе κ легкой цепи, причем локус κ легкой цепи содержит не относящийся к человеку ген Сκ или его функциональный фрагмент; и (b) идентификацию реаранжированного гена иммуноглобулина у указанного животного, причем реаранжированный ген иммуноглобулина содержит генный сегмент вариабельной области λ легкой цепи и ген Сκ или его функциональный фрагмент.
Согласно одному варианту осуществления константный ген κ легкой цепи или его функциональный фрагмент выбран из гена Сκ человека и не относящегося к человеку (например, относящегося к мыши или крысе) гена Сκ или его функционального фрагмента.
Согласно одному варианту осуществления способ дополнительно предусматривает клонирование последовательности нуклеиновой кислоты, кодирующей вариабельную область тяжелой и/или легкой цепи из животного, причем вариабельная область тяжелой и/или легкой цепи происходит из антитела, которое содержит Vλ человека и не относящийся к человеку (например, относящийся мыши или крысе) Сκ.
Согласно одному варианту осуществления предусмотрен способ получения реаранжированного гена антитела в генетически модифицированном отличном от человека животном, предусматривающий: (а) воздействие на генетически модифицированное отличное от человека животное антигена, причем генетическая модификация предусматривает hVλ и hJλ на не относящемся к человеку локусе λ легкой цепи, причем локус λ легкой цепи содержит не относящийся к человеку ген Сλ или его функциональный фрагмент; и (b) идентификацию реаранжированного гена иммуноглобулина у указанного животного, причем реаранжированный ген иммуноглобулина содержит генный сегмент вариабельной области λ легкой цепи и Сλ ген или его функциональный фрагмент.
Согласно одному варианту осуществления константный ген λ легкой цепи или его функциональный фрагмент выбран из гена Сλ человека и гена Сλ мыши или крысы, или его функционального фрагмента. Согласно конкретному варианту осуществления константный ген λ легкой цепи представляет собой ген Сλ мыши или крысы или его функциональный фрагмент.
Согласно одному варианту осуществления способ дополнительно предусматривает клонирование кодирующей вариабельную область тяжелой и/или легкой цепи последовательности нуклеиновой кислоты из животного, причем вариабельная область тяжелой и/или легкой цепи происходит из антитела, которое содержит Vλ человека и не относящийся к человеку (например, относящийся к мыши или крысе) Сκ.
Согласно одному аспекту предусмотрен способ получения антитела, предусматривающий воздействие на описанное в настоящем документе отличное от человека животное антигена, предоставление возможности животному развить иммунный ответ, который включает в себя создание антитела, которое специфически связывает антиген, идентификацию реаранжированной последовательности нуклеиновой кислоты у животного, которая кодирует тяжелую цепь, и реаранжированной последовательности нуклеиновой кислоты у животного, которая кодирует когнатную последовательность вариабельного домена легкой цепи антитела, причем антитело специфически связывает антиген, и применение последовательностей нуклеиновой кислоты вариабельных доменов тяжелой и легкой цепи, слитых с константными доменами человека для получения требуемого антитела, причем требуемое антитело содержит легкую цепь, которая содержит домен Vλ, слитый с домен CL. Согласно одному варианту осуществления домен Vλ представляет собой домен человека и домен CL представляет собой домен Сλ человека или мыши или крысы. Согласно одному варианту осуществления домен Vλ представляет собой домен мыши или крысы и домен CL представляет собой домен Сκ человека или мыши.
Согласно одному варианту осуществления предусмотрен способ получения антитела, предусматривающий воздействие на описанное в настоящем документе отличное от человека животное антигена, предоставление возможности животному развить иммунный ответ, который предусматривает образование антитела, которое специфически связывает антиген, идентификацию реаранжированной последовательности нуклеиновой кислоты у мыши, которая кодирует тяжелую цепи, и реаранжированной последовательности нуклеиновой кислоты у животного, которая кодирует когнатную последовательность вариабельного домена легкой цепи антитела, причем антитело специфически связывает антиген, и использование последовательностей нуклеиновой кислоты вариабельных доменов тяжелой и легкой цепи, слитых с последовательностями нуклеиновой кислоты константных доменов человека, для получения требуемого антитела, причем требуемое антитело содержит легкую цепь, которая содержит домен Vλ, слитый с доменом Сκ.
Согласно одному варианту осуществления предусмотрен способ получения антитела, предусматривающий воздействие на описанное в настоящем документе отличное от человека животное антигена, предоставление возможности животному развить иммунный ответ, который предусматривает образование антитела, которое специфически связывает антиген, идентификацию реаранжированной последовательности нуклеиновой кислоты у животного, которая кодирует вариабельный домен тяжелой цепи, и реаранжированной последовательности нуклеиновой кислоты, которая кодирует когнатную последовательность вариабельного домена легкой цепи антитела, причем антитело специфически связывает антиген, и использование последовательностей нуклеиновой кислоты, слитых с последовательностями нуклеиновой кислоты, которые кодируют константный домен тяжелой цепи человека и константный домен легкой цепи человека, для получения антитела, происходящего из последовательностей человека, причем антитело, которое специфически связывает антиген, содержит легкую цепь, которая содержит домен Vλ человека, слитый с не относящейся к человеку (например, относящейся к мыши или крысе) областью Cλ.
Согласно одному варианту осуществления область Сλ относится к мыши и согласно одному варианту осуществления выбрана из Сλ1, Сλ2 и Сλ3. Согласно конкретному варианту осуществления область Сλ мыши представляет собой Сλ2.
Согласно одному аспекту предусмотрен способ получения реаранжированной последовательности гена вариабельной области легкой цепи антитела, предусматривающий (а) воздействие на описанное в настоящем документе отличное от человека животное антигена; (b) предоставление возможности животному развить иммунный ответ; (с) идентификацию клетки у животного, которая содержит последовательность нуклеиновой кислоты, которая кодирует реаранжированную последовательность домена Vλ человека, слитую с не относящимся к человеку доменом CL, причем клетка также кодирует когнатную тяжелую цепь, содержащую домен VH человека и не относящийся к человеку домен CH, и причем клетка экспрессирует антитело, которое связывает антиген; (d) клонирование из клетки последовательности нуклеиновой кислоты, кодирующей домен Vλ человека и последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека; и (е) применение клонированной последовательности нуклеиновой кислоты, кодирующей домен Vλ человека, и клонированной последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека, для получения полностью человеческого антитела. Согласно одному варианту осуществления отличное от человека животное и не относящиеся к человеку домены выбраны из доменов мыши и крысы.
Согласно одному варианту осуществления предусмотрен способ получения реаранжированной последовательность гена вариабельной области легкой цепи антитела, предусматривающий (а) воздействие на описанное в настоящем раскрытии отличное от человека животное антигена; (b) предоставление возможности животному развить иммунный ответ; (с) идентификацию клетки у животного, которая содержит последовательность нуклеиновой кислоты, которая кодирует реаранжированную последовательность домена Vλ человека, смежную на той же молекуле нуклеиновой кислоты с последовательность нуклеиновой кислоты, кодирующей домен Сλ отличного от человека животного, причем клетка также кодирует когнатную тяжелую цепь, содержащую домен VH человека и домен CH отличного от человека животного, и причем клетка экспрессирует антитело, которое связывает антиген; (d) клонирование из клетки последовательности нуклеиновой кислоты, кодирующей домен Vλ человека, и последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека; и (е) применение клонированной последовательности нуклеиновой кислоты, кодирующей домен Vλ человека, и клонированной последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека, для получения полностью человеческого антитела.
Согласно одному варианту осуществления предусмотрен способ получения реаранжированной последовательности гена вариабельной области легкой цепи антитела, предусматривающий (а) воздействие на описанное в настоящем документе отличное от человека животное антигена; (b) предоставление возможности животному развить иммунный ответ на антиген; (с) идентификацию клетки у животного, которая содержит ДНК, которая кодирует реаранжированную последовательность домена Vλ человека, слитую с не относящимся к человеку доменом Сλ животного, причем клетка также кодирует когнатную тяжелую цепь, содержащую домен VH человека и не относящийся к человеку домен Сλ животного, и причем клетка экспрессирует антитело, которое связывает антиген; (d) клонирование из клетки последовательности нуклеиновой кислоты, кодирующей реаранжированный домен Vλ человека, и последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека; и (е) применение клонированной последовательности нуклеиновой кислоты, кодирующей домен Vλ человека, и клонированной последовательности нуклеиновой кислоты, кодирующей когнатный домен VH человека, для получения полностью человеческого антитела. Согласно одному варианту осуществления отличное от человека животное представляет собой мышь, и Сλ домен представляет собой Сλ2 мыши. Согласно конкретному варианту осуществления домен Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному аспекту предусмотрено генетически модифицированное отличное от человека животное, которое экспрессирует происходящую из λ легкую цепь человека, слитую с эндогенной константной областью легкой цепи (CL), причем животное, при иммунизации антигеном, производит антитело, содержащее домен Vλ человека, слитый с не относящимся к человеку доменом CL животного. Согласно одному варианту осуществления не относящийся к человеку домен CL выбран из домена Сκ и домена Сλ. Согласно одному варианту осуществления домен CL представляет собой домен Сκ. Согласно одному варианту осуществления животное представляет собой мышь. Согласно одному варианту осуществления домен CL мыши представляет собой домен Сλ. Согласно конкретному варианту осуществления домен Сλ представляет собой Сλ2. Согласно конкретному варианту осуществления домен Сλ мыши происходит из гена Сλ, который по меньшей мере на 60%, по меньшей мере на 70%, по меньшей мере на 80%, по меньшей мере на 90%, по меньшей мере на 95% или по меньшей мере на 98% идентичен Сλ2 мыши.
Согласно одному аспекту предусмотрено генетически модифицированное отличное от человека животное, содержащее описанный в настоящем документе модифицированный эндогенный локус κ или λ легкой цепи, которое экспрессирует множество λ легких цепей иммуноглобулина, связанных с множеством тяжелых цепей иммуноглобулина. Согласно одному варианту осуществления тяжелая цепь содержит последовательность человека. Согласно различным вариантам осуществления последовательность человека выбрана из вариабельной последовательности, CH1, шарнира, CH2, CH3 и их комбинации. Согласно одному варианту осуществления множество λ легких цепей иммуноглобулина содержит последовательность человека. Согласно различным вариантам осуществления последовательность человека выбрана из вариабельной последовательности, константной последовательности и их комбинации. Согласно одному варианту осуществления животное содержит недееспособный эндогенный локус иммуноглобулина и экспрессирует тяжелую цепь и/или λ легкую цепь из трансгена или внехромосомной эписомы. Согласно одному варианту осуществления животное содержит замещение на эндогенном (не относящемся к человеку) локусе некоторых или всех эндогенных не относящихся к человеку генных сегментов тяжелой цепи (т.е. V, D, J), и/или некоторых или всех эндогенных не относящихся к человеку константных последовательностей тяжелой цепи (например, CH1, шарнира, CH2, CH3 или их комбинации), и/или некоторых или всех эндогенных не относящихся к человеку последовательностей легкой цепи (например, V, J, константной или их комбинации) одной или несколькими последовательностями иммуноглобулина человека. Согласно одному варианту осуществления отличное от человека животное представляет собой мышь.
Согласно одному аспекту предусмотрено отличное от человека животное, подходящие для получения антител, которые содержат происходящую из λ легкую цепь человека, причем все или по существу все антитела, произведенные в отличном от человека животном, экспрессируются с происходящей из λ легкой цепью человека. Согласно одному варианту осуществления происходящая из λ легкая цепь человека экспрессируется из эндогенного локуса легкой цепи. Согласно одному варианту осуществления эндогенный локус легкой цепи представляет собой локус κ легкой цепи. Согласно конкретному варианту осуществления животное представляет собой мышь, и локус κ легкой цепи представляет собой локус κ легкой цепи мыши.
Согласно одному аспекту предусмотрен способ получения происходящей из λ легкой цепи для антитела человека, предусматривающий получение от описанного в настоящем документе отличного от человека животного последовательности легкой цепи и последовательности тяжелой цепи, и применение последовательности легкой цепи и последовательности тяжелой цепи в получении антитела человека.
Согласно одному аспекту предусмотрен способ получения антигенсвязывающего белка, предусматривающий воздействие на описанное в настоящем документе отличное от человека животное антигена; предоставление возможности отличному от человека животному развить иммунный ответ; и получение от отличного от человека животного антигенсвязывающего белка, который связывает антиген, или получение от отличного от человека животного последовательности, подлежащей использованию в получении антигенсвязывающего белка, который связывает антиген.
Согласно одному аспекту предусмотрена клетка, происходящая из описанного в настоящем документе отличного от человека животного (например, мыши или крысы). Согласно одному варианту осуществления клетка выбрана из эмбриональной стволовой клетки, плюрипотентной клетки, индуцированной плюрипотентной клетки, В-клетки и гибридомы.
Согласно одному аспекту предусмотрена клетка, которая содержит описанную в настоящем документе генетическую модификацию. Согласно одному варианту осуществления клетка представляет собой клетку мыши. Согласно одному варианту осуществления клетка выбрана из гибридомы и квадромы. Согласно одному варианту осуществления клетка экспрессирует легкую цепь иммуноглобулина, которая содержит вариабельную последовательность λ человека, слитую с константной последовательностью мыши. Согласно конкретному варианту осуществления константная последовательность мыши представляет собой константную последовательность κ мыши.
Согласно одному аспекту предусмотрена ткань, полученная от описанного в настоящем документе отличного от человека животного.
Согласно одному аспекту предусмотрено применение отличного от человека животного или клетки, описанных в настоящем документе, для получения антигенсвязывающего белка. Согласно одному варианту осуществления антигенсвязывающий белок представляет собой белок человека. Согласно одному варианту осуществления белок человека представляет собой антитело человека.
Согласно одному аспекту предусмотрен антигенсвязывающий белок, произведенный отличным от человека животным, клеткой, тканью или способом, описанными в настоящем документе. Согласно одному варианту осуществления антигенсвязывающий белок представляет собой белок человека. Согласно одному варианту осуществления белок человека представляет собой антитело человека.
Любой из описанных в настоящем документе вариантов осуществления и аспектов может использоваться в сочетании друг с другом, если иное не указано или не очевидно из контекста. Другие варианты осуществления станут очевидными специалистам в настоящей области техники при рассмотрении последующего описания
Краткое описание фигур
На фиг. 1А показано общее изображение, без соблюдения масштаба, прямого геномного замещения приблизительно трех миллионов пар нуклеотидов (Mb) вариабельного генного локуса тяжелой цепи иммуноглобулина мыши (закрашенные обозначения) приблизительно одним миллионом пар нуклеотидов (Mb) вариабельного генного локуса тяжелой цепи иммуноглобулина человека (незакрашенные обозначения).
На фиг. 1В показано общее изображение, без соблюдения масштаба, прямого геномного замещения приблизительно трех миллионов пар нуклеотидов (Mb) вариабельного генного локуса κ легкой цепи иммуноглобулина мыши (закрашенные обозначения) приблизительно 0,5 миллиона пар нуклеотидов (Mb) первым, или проксимальным, из двух почти идентичных повторов вариабельного генного локуса κ легкой цепи иммуноглобулина человека (незакрашенные обозначения).
На фиг. 2А показано подробное изображение, без соблюдения масштаба, трех начальных стадий (А-С) прямого геномного замещения вариабельного генного локуса тяжелой цепи иммуноглобулина мыши, которое приводит к делеции всех генных сегментов VH, DH и JH мыши и замещению тремя генными сегментами VH человека, всеми генными сегментами DH и JH человека. Нацеливающий вектор для первой вставки генных сегментов тяжелой цепи иммуноглобулина человека показан (3hVH BACvec) с 67 т.п.н. 5' гомологичным плечом мыши, кассетой селекции (незакрашенный прямоугольник), сайтом сайт-специфической рекомбинации (незакрашенный треугольник), 145 т.п.н. геномным фрагментом человека и 8 т.п.н. 3' гомологичным плечом мыши. Показаны генные сегменты иммуноглобулина человека (незакрашенные обозначения) и мыши (закрашенные обозначения), дополнительные кассеты селекции (незакрашенные прямоугольники) и сайты сайт-специфической рекомбинации (незакрашенные треугольники), вставленные из последующих нацеливающих векторов.
На фиг. 2В показано подробное изображение, без соблюдения масштаба, шести дополнительных стадий (D-I) прямого геномного замещения вариабельного генного локуса тяжелой цепи иммуноглобулина мыши, которое приводит к вставке 77 дополнительных генных сегментов VH человека и удалению последней кассеты селекции. Нацеливающий вектор для вставки дополнительных генных сегментов VH человека (18hVH BACvec) в начальную вставку генных сегментов тяжелой цепи человека (гибридный аллель 3hVH-CRE) показан с 20 т.п.н. 5' гомологичным плечом мыши, кассетой селекции (незакрашенный прямоугольник), 196 т.п.н. геномным фрагментом человека и 62 т.п.н. гомологичным плечом человека, которое перекрывается с 5' концом начальной вставки генных сегментов тяжелой цепи человека, которая показана с сайтом сайт-специфической рекомбинации (незакрашенный треугольник), расположенном 5' по отношению к генным сегментам человека. Показаны генные сегменты иммуноглобулина человека (незакрашенные обозначения) и мыши (закрашенные обозначения) и дополнительные кассеты селекции (незакрашенные прямоугольники), вставленные с помощью последующих нацеливающих векторов.
На фиг. 2С показано подробное изображение, без соблюдения масштаба, трех начальных стадий (А-С) прямого геномного замещения вариабельного генного локуса κ легкой цепи иммуноглобулина мыши, которое приводит к делеции всех генных сегментов Vκ и Jκ мыши (гибридный аллель Igκ-CRE). Показаны кассеты селекции (незакрашенные прямоугольники) и сайты сайт-специфической рекомбинации (незакрашенные треугольники), вставленные из нацеливающих векторов.
На фиг. 2D показано подробное изображение, без соблюдения масштаба, пяти дополнительных стадий (D-H) прямого геномного замещения вариабельного генного локуса κ легкой цепи иммуноглобулина мыши, которое приводит к вставке всех генных сегментов Vκ и Jκ человека в проксимальный повтор и делеции последней кассеты селекции (гибридный аллель 40hVκdHyg). Показаны генные сегменты иммуноглобулина человека (незакрашенные обозначения) и мыши (закрашенные обозначения) и дополнительные кассеты селекции (незакрашенные прямоугольники), вставленные последующими нацеливающими векторами.
На фиг. 3А показано общее изображение, без соблюдения масштаба, стратегии скрининга, включающей в себя положения праймеров/зондов количественной ПЦР (кПЦР) в отношении вставки генных последовательностей тяжелой цепи человека и потери генных последовательностей тяжелой цепи мыши в нацеленных эмбриональных стволовых (ES) клетках. Стратегия скрининга в ES клетках и мышах в отношении первой вставки гена тяжелой области человека показана с наборами праймеров/зондов кПЦР для удаленной области (зонды "потери" С и D), вставленной области (зонды "hIgH" G и Н) и фланкирующих областей (зонды "удерживания" A, В, Е и F) на немодифицированной мышиной хромосоме (вверху) и точно нацеленной хромосоме (внизу).
На фиг. 3В показан репрезентативный расчет наблюдаемого числа копий зонда в родительских и модифицированных ES клетках для первой вставки генных сегментов тяжелой цепи иммуноглобулина человека. Наблюдаемое число копий зонда для зондов A-F рассчитывали как 2/2ΔΔCt. ΔΔCt рассчитывают как ave[ΔCt(образец) - medΔCt(контроль)], где ΔCt представляет собой разницу в Ct между исследуемым и эталонным зондами (между 4 и 6 эталонными зондами в зависимости от анализа). Термин medΔCt(контроль) представляет собой срединное значение ΔCt многочисленных (>60) ненацеленных образцов ДНК из родительских ES клеток. Каждый клон модифицированных ES клеток анализировали в шести параллельных испытаниях. Для расчета значений числа копий IgH зондов G и Н в родительских ES клетках принимали, что эти зонды характеризуются числом копий, равным 1 в модифицированных ES клетках, и максимальный Ct, равный 35, использовали, даже если не наблюдалось никакой амплификации
На фиг. 3С показан репрезентативный расчет значений числа копий для четырех мышей каждого генотипа, рассчитанный аналогичным образом, используя только зонды D и Н. Мыши дикого типа: WT мыши; мыши, гетерозиготные в отношении первой вставки генных сегментов иммуноглобулина человека: НЕТ мыши; мыши, гомозиготные в отношении первой вставки генных сегментов иммуноглобулина человека: Homo мыши.
На фиг. 4А показано подробное изображение, без соблюдения масштаба, трех стадий, используемых для конструкции 3hVH BACvec с помощью бактериальная гомологичной рекомбинации (BHR). Показаны генные сегменты иммуноглобулина человека (незакрашенные обозначения) и мыши (закрашенные обозначения), кассеты селекции (незакрашенные прямоугольники) и сайты сайт-специфической рекомбинации (незакрашенные треугольники), вставленные из нацеливающих векторов.
На фиг. 4В показан гель-электрофорез в пульсирующем поле (PFGE) трех клонов ВАС (B1, В2 и В3) после обработки NotI. Маркеры M1, М2 и М3 представляют собой маркеры низкого диапазона, среднего диапазона и лямбда лэддера PFG, соответственно (New England BioLabs, Ипсвич, Массачусетс).
На фиг. 5А показано схематическое изображение, без соблюдения масштаба, последовательных модификаций локуса тяжелой цепи иммуноглобулина мыши с помощью возрастающих количеств генных сегментов тяжелой цепи иммуноглобулина человека. Гомозиготных мышей получали из каждой из трех различных стадий гуманизации тяжелой цепи. Незакрашенные обозначения отображают последовательность человека; закрашенные обозначения отображают последовательность мыши.
На фиг. 5В показано схематическое изображение, без соблюдения масштаба, последовательных модификаций локуса κ легкой цепи иммуноглобулина мыши с помощью возрастающих количеств генных сегментов κ легкой цепи иммуноглобулина человека. Гомозиготных мышей получали из каждой из трех различных стадий гуманизации κ легкой цепи. Незакрашенные обозначения отображают последовательность человека; закрашенные обозначения отображают последовательность мыши.
На фиг. 6 показаны точечные диаграммы FACS популяций В-клеток у мышей дикого типа и гуманизированных мышей VELOCIMMUNE®. Клетки из селезенки (верхний ряд, третий ряд сверху и нижний ряд) или пахового лимфатического узла (второй ряд сверху) мышей дикого типа (wt) или VELOCIMMUNE® 1 (V1), VELOCIMMUNE® 2 (V2) или VELOCIMMUNE® 3 (V3) окрашивали в отношении экспрессирующих поверхностный IgM В-клеток (верхний ряд, и второй ряд сверху), поверхностный иммуноглобулин, содержащий или κ или λ легкие цепи (третий ряд сверху) или поверхностный IgM специфических гаплотипов (нижний ряд), и популяции разделяли с помощью FACS.
На фиг. 7А показаны репрезентативные последовательности CDR3 тяжелой цепи выбранных произвольно антител VELOCIMMUNE® около участка соединения VH-DH-JH (CDR3), демонстрирующие множественность сегментов J и нуклеотидные вставки. Последовательности CDR3 тяжелой цепи группируются согласно частоте использования генного сегмента DH, зародышевая линия которого приведена над каждой группой жирным шрифтом. Генные сегменты VH для каждой последовательности CDR3 тяжелой цепи указаны в скобках на 5' конце каждой последовательности (например, 3-72 представляет собой VH3-72 человека). Генные сегменты JH для каждой CDR3 тяжелой цепи указаны в скобках на 3' конце каждой последовательности (например, 3 представляет собой JH3 человека). SEQ ID NO для каждой представленной последовательности являются следующими, приведенными сверху вниз: SEQ ID NO: 21; SEQ ID NO: 22; SEQ ID NO: 23; SEQ ID NO: 24; SEQ ID NO: 25; SEQ ID NO: 26; SEQ ID NO: 27; SEQ ID NO: 28; SEQ ID NO: 29; SEQ ID NO: 30; SEQ ID NO: 31; SEQ ID NO: 32; SEQ ID NO: 33; SEQ ID NO: 34; SEQ ID NO: 35; SEQ ID NO: 36; SEQ ID NO: 37; SEQ ID NO: 38; SEQ ID NO: 39.
На фиг. 7B показаны репрезентативные последовательности CDR3 легкой цепи выбранных произвольно антител VELOCIMMUNE® около участка соединения Vκ-Jκ (CDR3), демонстрирующие множественность сегментов J и нуклеотидные вставки. Генные сегменты Vκ для каждой последовательности CDR3 легкой цепи указаны в скобках на 5' конце каждой последовательности (например, 1-6 представляет собой Vκ1-6 человека). Генные сегменты Jκ для каждой CDR3 легкой цепи указаны в скобках на 3' конце каждой последовательности (например, 1 представляет собой Jκ1 человека). SEQ ID NO для каждой представленной последовательности являются следующими, приведенными сверху вниз: SEQ ID NO: 40; SEQ ID NO: 41; SEQ ID NO: 42; SEQ ID NO: 43; SEQ ID NO: 44; SEQ ID NO: 45; SEQ ID NO: 46; SEQ ID NO: 47; SEQ ID NO: 48; SEQ ID NO: 49; SEQ ID NO: 50; SEQ ID NO: 51; SEQ ID NO: 52; SEQ ID NO: 53; SEQ ID NO: 54; SEQ ID NO: 55; SEQ ID NO: 56; SEQ ID NO: 57; SEQ ID NO: 58.
На фиг. 8 показаны частоты соматических гипермутаций тяжелых и легких цепей антител VELOCIMMUNE®, подсчитанные (после выравнивания с совпадающими зародышевыми последовательностями) как процент измененных последовательностей на каждом нуклеотидном (NT; левая колонка) или аминокислотном положении (АА; правая колонка) среди наборов из 38 (неиммунизированный IgM), 28 (неиммунизированный IgG), 32 (неиммунизированная Igκ из IgG), 36 (иммунизированный IgG) или 36 (иммунизированная Igκ из IgG) последовательностей. Заштрихованные столбики указывают на положения CDR.
На фиг. 9А показаны уровни иммуноглобулина в сыворотке для изотипов IgM и IgG у мышей дикого типа (белые столбики) или VELOCIMMUNE® (окрашенные столбики).
На фиг. 9В показаны уровни иммуноглобулина в сыворотке для изотипа IgA у мышей дикого типа (белые столбики) или VELOCIMMUNE® (окрашенные столбики).
На фиг. 9С показаны уровни иммуноглобулина в сыворотке для изотипа IgE у мышей дикого типа (белые столбики) или VELOCIMMUNE® (окрашенные столбики).
На фиг. 10А показаны титры антигенспецифических IgG к рецептору интерлейкина-6 в сыворотке семи мышей VELOCIMMUNE® (VI) и пяти мышей дикого типа (WT) после двух (кровопускание 1) или трех (кровопускание 2) циклов иммунизации с помощью эктодомена рецептора IL-6R.
На фиг. 10В показаны титры специфических изотипов IgG, специфических к рецептору IL-6R от семи мышей VELOCIMMUNE® (VI) и пяти мышей дикого типа (WT).
На фиг. 11А показано распределение аффинности моноклональных антител к рецептору интерлейкина-6, образованных у мышей VELOCIMMUNE®.
На фиг. 11В показано антиген-специфическое блокирование моноклональных антител к рецептору интерлейкина-6, образованных у мышей VELOCIMMUNE® (VI) и мышей дикого типа (WT).
На фиг. 12 показано схематическое изображение, без соблюдения масштаба, генов ADAM6a и ADAM6b мыши на локусе тяжелой цепи иммуноглобулина мыши. Нацеливающий вектор (нацеливающий вектор mADAM6), используемый для вставки ADAM6a и ADAM6b мыши в гуманизированный эндогенный локус тяжелой цепи, показан с кассетой селекции (HYG: гигромицин), фланкированной сайтами сайт-специфической рекомбинации (Frt), включающих в себя сконструированные сайты рестрикции на 5' и 3' концах.
На фиг. 13 показано схематическое изображение, без соблюдения масштаба, псевдогена ADAM6 человека (hADAM6Ψ), расположенного между вариабельными генными сегментами 1-2 (VH1-2) и 6-1 (VH6-1) тяжелой цепи человека. Нацеливающий вектор для бактериальной гомологичной рекомбинации нацеливающий вектор (hADAM6Ψ) для делеции псевдогена ADAM6 человека и вставки уникальных сайтов рестрикции на локус тяжелой цепи человека показан с кассетой селекции (NEO: неомицин), фланкированной сайтами сайт-специфической рекомбинации (loxP), включающих в себя сконструированные сайты рестрикции на 5' и 3' концах. Показано изображение, без соблюдения масштаба, полученного нацеленного гуманизированного локуса тяжелой цепи, содержащего геномный фрагмент, который кодирует гены ADAM6a и ADAM6b мыши, включающего в себя кассету селекции, фланкированную сайтами сайт-специфической рекомбинации.
На фиг. 14А показаны контурные графики FACS лимфоцитов, дающих сигнал выше порогового значения на синглетах в отношении поверхностной экспрессии IgM и В220 в костном мозге мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и к легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепей человека, содержащих вставленный геномный фрагмент мыши, содержащий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение незрелых (B220intIgM+) и зрелых (B220highIgM+) В-клеток указано на каждом контурном графике.
На фиг. 14В показано общее количество незрелых (B220intIgM+) и зрелых (B220highIgM+) В-клеток в костном мозге, выделенном из бедренных костей мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+ A6resκ+/+).
На фиг. 15А показаны контурные графики FACS дающих сигнал CD19+ выше порогового значения В-клеток в отношении поверхностной экспрессии c-kit и CD43 в костном мозге мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+), и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение про-В (CD19+CD43+ckit+) и пре-В (CD19+CD43-ckit-) клеток указано в верхнем правом и нижнем левом квадрантах, соответственно, каждого контурного графика.
На фиг. 15В показано общее количество про-В-клеток (CD19+CD43+ckit+) и пре-В-клеток (CD19+CD43-ckit-) в костном мозге, выделенном из бедренных костей мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический мыши геномный фрагмент мыши, содержащий гены ADAM6 мыши (Н+/+A6resκ+/+).
На фиг. 16А показаны контурные графики FACS лимфоцитов гейтированных по синглетам в отношении поверхностной экспрессии CD19 и CD43 в костном мозге мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение незрелых В (CD19+CD43-), пре-В (CD19+CD43int) и про-В (CD19+CD43+) клеток указано на каждом контурном графике.
На фиг. 16В показаны гистограммы незрелых В (CD19+CD43-) и пре-В (CD19+CD43int) клеток в костном мозге мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+).
На фиг. 17А показаны контурные графики FACS лимфоцитов гейтированных по синглетам в отношении поверхностной экспрессии CD19 и CD3 в спленоцитах мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека (H+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение В (CD19+CD3-) и Т (CD19-CD3+) клеток указано на каждом контурном графике.
На фиг. 17В показаны контурные графики FACS гейтированных по CD19+ В-клеток в отношении поверхностной экспрессии Igλ и Igκ легких цепей в селезенке мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение Igλ+ (верхний левый квадрант) и Igκ+ (нижний правый квадрант) В-клеток указан на каждом контурном графике.
На фиг. 17С показано общее количество CD19+ В-клеток в селезенке мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+).
На фиг. 18А показаны контурные графики FACs дающих сигнал CD19+ выше порогового значения В-клеток в отношении поверхностной экспрессии IgD и IgM в селезенке мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека (H+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+). Процентное отношение зрелых В-клеток (CD19+IgDhighIgMint) указано на каждом контурном графике. Стрелка на правом контурном графике иллюстрирует процесс созревания В-клеток по отношению к поверхностной экспрессии IgM и IgD.
На фиг. 18В показано общее количество В-клеток в селезенке мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека (Н+/+/κ+/+) и мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6 мыши (Н+/+A6resκ+/+) в ходе созревания от CD19+IgMhighIgDint до CD19+IgMintIgDhigh.
На фиг. 19 показано подробное изображение, без соблюдения масштаба, локуса λ легкой цепи человека, включающего в себя кластеры генных сегментов Vλ (A, В и С) и пары областей Jλ и Сλ (пары J-C).
На фиг. 20 показано общее изображение, без соблюдения масштаба, стратегии нацеливания, используемой для инактивации эндогенного локуса λ легкой цепи мыши.
На фиг. 21 показано общее изображение, без соблюдения масштаба, стратегии нацеливания, используемой для инактивации эндогенного локуса κ легкой цепи мыши.
На фиг. 22А показано общее изображение, без соблюдения масштаба, исходного нацеливающего вектора для нацеливания на эндогенный локус λ легкой цепи мыши с последовательностями λ легкой цепи человека, включая в себя 12 генных сегментов hVλ и 1 генный сегмент hJλ (нацеливающие вектор 12/1-λ).
На фиг. 22В показано общее изображение, без соблюдения масштаба, четырех исходных нацеливающих векторов для нацеливания на эндогенный локус κ легкой цепи мыши с последовательностями λ легкой цепи человека, включая в себя 12 генных сегментов hVλ и 1 генный сегмент hJλ (12/1-κ нацеливающий вектор), 12 генных сегментов hVλ и 1, 2, 3 и 7 генных сегментов hJλ (12/4-κ нацеливающий вектор), 12 генных сегментов hVλ, геномную последовательность Vκ-Jκ человека и 1 генный сегмент hJλ (12(κ)1-κ нацеливающий вектор) и 12 генных сегментов hVλ, геномную последовательность Vκ-Jκ человека и 1, 2, 3 и 7 генных сегментов hJλ (12(κ)4-κ нацеливающий вектор).
На фиг. 23А показано общее изображение, без соблюдения масштаба, стратегии нацеливания для поэтапной вставки 40 генных сегментов hVλ и одного генного сегмента hJλ в локус λ легкой цепи мыши.
На фиг. 23В показано общее изображение, без соблюдения масштаба, стратегии нацеливания для поэтапной вставки 40 генных сегментов hVλ и одного генного сегмента hJλ в локус κ мыши.
На фиг. 24 показано общее изображение, без соблюдения масштаба, стадий нацеливания и молекулярного конструирования, используемых для получения уникальных человека λ-κ гибридных нацеливающих векторов для конструирования гибридного локуса легкой цепи, содержащего κ межгенную последовательность человека, множественные генные сегменты hJλ или и то и другое.
На фиг. 25А показано общее изображение, без соблюдения масштаба, структуры локуса для модифицированого локуса λ легкой цепи мыши, содержащего 40 генных сегментов hVλ и один генный сегмент hJλ, функционально связанный с эндогенным геном Сλ2.
На фиг. 25В показано общее изображение, без соблюдения масштаба, структуры локуса для четырех независимых модифицированных локусов κ легкой цепи мыши, содержащих 40 генных сегментов hVλ и или один, или четыре генных сегментов hJλ со или смежной геномной последовательностью Vκ-Jκ человека или без нее, функционально связанной с эндогенным геном Сκ.
На фиг. 26А показаны контурные графики Igλ+ и Igκ+ спленоцитов, гейтированных по CD19+ из мыши дикого типа (WT), мыши, гомозиготной в отношении 12 hVλ и четырех hJλ генных сегментов, включая в себя геномная последовательность Vκ-Jκ человека (12hVλ-VκJκ-4hJλ), и мыши, гомозиготной в отношении 40 hVλ и одного hJλ генного сегмента (40hVλ-1hJλ).
На фиг. 26В показано общее количество CD19+ В-клеток в собранных селезенках от мышей дикого типа (WT), мышей, гомозиготных в отношении 12 hVλ и четырех генных сегментов hJλ, включая в себя геномную последовательность человека Vκ-Jκ (12hVλ-VκJκ-4hJλ и мышей, гомозиготный в отношении 40 hVλ и одного hJλ генного сегмента (40hVλ-1hJλ).
На фиг. 27A, на верхней панели, показаны контурные графики спленоцитов, гейтированных по синглетам и окрашенных в отношении В- и Т-клеток (CD19+ и CD3+, соответственно) от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ). На нижней панели показаны контурные графики спленоцитов, гейтированных по CD19+ и окрашенных в отношении экспрессии Igλ+ и Igκ+ от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 27В показано общее количество CD19+, CD19Igκ+ и CD19+Igλ+ В-клеток в собранных селезенках от мышей дикого типа (WT) и мышей, гомозиготных в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 27С показаны контурные графики спленоцитов, гейтированных по CD19+ и окрашенных в отношении иммуноглобулина D (IgD) и иммуноглобулина М (IgM) от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ). Зрелые В-клетки (72 для WT, 51 для 40hVλ-VκJκ-4hJλ) и переходные В-клетки (13 для WT, 22 для 40hVλ-VκJκ-4hJλ) отмечали на каждом контурном графике.
На фиг. 27D показано общее количество CD19+ В-клеток, переходных В-клеток (CD19IgMhiIgDlo) и зрелых В-клеток (CD19+IgMloIgDhi) в собранных селезенках от мышей дикого типа (WT) и мышей, гомозиготных в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 28A, на верхней панели, показаны контурные графики костного мозга, окрашенного в отношении В- и Т-клеток (CD19+ и CD3+, соответственно) от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ). На нижней панели показаны контурные графики костного мозга, гейтированного по CD19+ и окрашенного в отношении ckit+ и CD43+ от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ). Про- и пре-В-клетки отмечены на контурных графиках на нижней панели.
На фиг. 28В показано количество про-(CD19+CD43+ckit+) и пре-(CD19+CD43-ckit-) В-клеток в костном мозге, собранном из бедренных костей мышей дикого типа (WT) и мышей, гомозиготных в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 28С показаны контурные графики костного мозга, гейтированного по синглетам, окрашенного в отношении иммуноглобулина М (IgM) и В220 от мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ). Незрелые, зрелые и про/пре-В-клетки отмечены на каждом из контурных графиков.
На фиг. 28D показано общее количество незрелых (B220intIgM+) и зрелых (B220hiIgM+) В-клеток в костном мозге, выделенном из бедренных костей мышей дикого типа (WT) и мышей, гомозиготных в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 28Е показаны контурные графики костного мозга, гейтированного по незрелым (B220intIgM+) и зрелым (B220hiIgM+) В-клеткам, окрашенного в отношении экспрессия Igλ и Igκ, выделенного из бедренных костей мыши дикого типа (WT) и мыши, гомозиготной в отношении 40 hVλ и четырех Jλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека (40hVλ-VκJκ-4hJλ).
На фиг. 29 показано выравнивание нуклеотидных последовательностей участка соединения Vλ-Jλ-Cκ 18 независимых клонов ОТ-ПЦР, амплифицированных из РНК спленоцита мышей, содержащих генные последовательности λ легкой цепи человека на эндогенном локусе κ легкой цепи мыши. А6 = SEQ ID NO: 115; В6 = SEQ ID NO: 116; F6 = SEQ ID NO: 117; B7 = SEQ ID NO: 118; E7 = SEQ ID NO: 119; F7 = SEQ ID NO: 120; C8 = SEQ ID NO: 121; E12 = SEQ ID NO: 122; 1-4 = SEQ ID NO: 123; 1-20 = SEQ ID NO: 124; 3B43 = SEQ ID NO: 125; 5-8 = SEQ ID NO: 126; 5-19 = SEQ ID NO: 127; 1010 = SEQ ID NO: 128; 11A1 = SEQ ID NO: 129; 7A8 = SEQ ID NO: 130; 3A3 = SEQ ID NO: 131; 2-7 = SEQ ID NO: 132. Обозначенные строчными буквами основания обозначают не относящиеся к зародышевой линии основания, являющиеся результатом или мутации, и/или N-вставки в ходе рекомбинации. Консенсусные аминокислоты в пределах каркасной области 4 (FWR4), кодируемой нуклеотидной последовательностью 1 hJλ и Сκ мыши, отмечены внизу выравнивания последовательностей.
На фиг. 30 показано выравнивание нуклеотидных последовательностей участка соединения Vλ-Jλ-Cκ 12 независимых клонов ОТ-ПЦР, амплифицированных из РНК спленоцитов мышей, содержащих генные последовательности λ легкой цепи человека, включая в себя смежную геномную последовательность Vκ-Jκ человека, на эндогенном локусе κ легкой цепи мыши. 5-2 = SEQ ID NO: 145; 2-5 = SEQ ID NO: 146; 1-3 = SEQ ID NO: 147; 4B-1 = SEQ ID NO: 148; 3B-5 = SEQ ID NO: 149; 7A-1 = SEQ ID NO: 150; 5-1 = SEQ ID NO: 151; 4A-1 = SEQ ID NO: 152; 11A-1 = SEQ ID NO: 153; 5-7 = SEQ ID NO: 154; 5-4 = SEQ ID NO: 155; 2-3 = SEQ ID NO: 156. Обозначенные строчными буквами основания обозначают не относящиеся к зародышевой линии основания, являющиеся результатом или мутации, и/или N-вставки в ходе рекомбинации. Консенсусные аминокислоты в пределах каркасной области 4 (FWR4), кодируемой нуклеотидной последовательностью каждого Jλ человека и Сκ мыши, отмечены внизу выравнивания последовательностей.
На фиг. 31 показано выравнивание нуклеотидных последовательностей участка соединения Vλ-Jλ-Сκ 3 независимых клонов ОТ-ПЦР, амплифицированных из РНК спленоцитов мышей, содержащих генные последовательности λ легкой цепи человека на эндогенном локусе λ легкой цепи мыши. 2D1 = SEQ ID N0. 159; 2D9 = SEQ ID NO: 160; 3E15 = SEQ ID NO: 161. Обозначенные строчными буквами основания обозначают не относящиеся к зародышевой линии основания, являющиеся результатом или мутации, и/или N-вставки в ходе рекомбинации. Консенсусные аминокислоты в пределах каркасной области 4 (FWR4), кодируемой нуклеотидной последовательностью 1 hJλ и Сλ2 мыши, отмечены внизу выравнивания последовательностей.
Подробное раскрытие настоящего изобретения
Настоящее изобретение не ограничивается конкретными способами и описанными экспериментальными условиями, поскольку такие способы и условия могут варьировать. Кроме того, следует понимать, что используемая в настоящем документе терминология предназначена только для цели описания конкретных вариантов осуществления и не предусматривается для ограничения, поскольку объем настоящего изобретения определяется его формулой.
Если не указано иное, все используемые в настоящем документе термины и фразы, включают в себя те значения, которые подразумеваются под терминами и фразами в настоящей области техники, если иное прямо не указано или явно не следует из контекста, в котором используется термин или фраза. Хотя любые способы и материалы, подобные или эквивалентные описанным в настоящем документе, могут быть использованы на практике или при испытании настоящего изобретения, теперь будут описаны конкретные способы и материалы. Все упомянутые публикации включены в настоящий документ посредством ссылки.
Фраза "существенный" или "по существу" при использовании для обозначения количества генных сегментов (например, "по существу все" генные сегменты V) включает в себя как функциональные, так и нефункциональные генные сегменты и включает в себя, согласно различным вариантам осуществления, например, 80% или более, 85% или более, 90% или более, 95% или более 96% или более, 97% или более, 98% или более, или 99% или более всех генных сегментов; согласно различным вариантам осуществления фраза "по существу все" генные сегменты включает в себя, например, по меньшей мере 95%, 96%, 97%, 98% или 99% функциональных (т.е. не относящихся к псевдогенам) генных сегментов.
Термин "замещение" включает в себя помещение последовательности ДНК в геном клетки таким образом, чтобы заменить последовательность в пределах генома гетерологичной последовательностью (например, последовательностью человека у мыши) на локусе геномной последовательности. Помещенная таким образом последовательность ДНК может включать в себя одну или несколько регуляторных последовательностей, которые представляют собой часть исходной ДНК, используемой для получения помещенной таким образом последовательности (например, промоторы, энхансеры, 5'- или 3'-нетранслируемые области, соответствующие последовательности сигналов рекомбинации и т.д.). Например, согласно различным вариантам осуществления замещение представляет собой замену эндогенной последовательности гетерологичной последовательностью, что приводит к производству генного продукта из помещенной таким образом последовательности ДНК (содержащей гетерологичную последовательность), но не экспрессии эндогенной последовательности; замещение эндогенной геномной последовательности последовательностью ДНК, которая кодирует белок, который характеризуется аналогичной функцией, что и белок, кодируемый эндогенной геномной последовательностью (например, эндогенная геномная последовательность кодирует ген или домен иммуноглобулина, и фрагмент ДНК кодирует один или несколько генов или доменов иммуноглобулина человека). Согласно различным вариантам осуществления эндогенный ген или его фрагмент заменяют соответствующим геном человека или его фрагментом. Соответствующий ген человека или его фрагмент представляет собой ген человека или фрагмент, который представляет собой ортолог, гомолог или по существу идентичный или такой же по структуре и/или функции, как эндогенный ген или его фрагмент, который заменен.
Термин "смежный" включает в себя ссылку на расположение на одной молекуле нуклеиновой кислоты, например, две последовательности нуклеиновой кислоты являются "смежными", если они располагаются на одной молекуле нуклеиновой кислоты, но прерываются другой последовательностью нуклеиновой кислоты. Например, реаранжированная последовательность V(D)J является "смежной" с генной последовательностью константной области, хотя за последним кодоном последовательности V(D)J не сразу следует первый кодон последовательности константной области. Согласно другому пример, две последовательности генного сегмента V являются "смежными", если они находятся на одном геномном фрагменте, хотя они могут быть разделены последовательностью, которая не кодирует кодон области V, например, они могут быть разделены регуляторной последовательностью, например, промотором или другой некодирующей последовательностью. Согласно одному варианту осуществления смежная последовательность включает в себя геномный фрагмент, который содержит геномные последовательности, расположенные так, как они встречаются в геноме дикого типа.
Фраза "происходящий из" при использовании в отношении вариабельной области, "происходящей из" указанного гена или генного сегмента, включает в себя способность установить для последовательность конкретный нереаранжированный генный сегмент или генные сегменты, которые были реаранжированы для образования гена, который экспрессирует вариабельный домен (учитывая при необходимости отличия в отношении сплайсинга и соматические мутации).
Фраза "функциональный" при использовании в отношении генного сегмента вариабельной области или соединяющего генного сегмента относится в частоте использования в экспрессируемом репертуаре антитела; например, у людей генные сегменты Vλ 3-1, 4-3, 2-8 и т.д. являются функциональными, тогда как генные сегменты Vλ 3-2, 3-4, 2-5 и т.д. являются нефункциональными.
"Локус тяжелой цепи" включает в себя положение на хромосоме, например, хромосоме мыши, в котором у мыши дикого типа встречаются последовательности ДНК вариабельной области тяжелой цепи (VH), дополнительной области тяжелой цепи (DH), соединяющей области тяжелой цепи (JH) и константной области тяжелой цепи (CH).
"Локус κ" включает в себя положение на хромосоме, например, хромосоме мыши, в котором у мыши дикого типа встречаются последовательности ДНК κ вариабельной (Vκ), κ соединяющей (Jκ) и κ константной (Сκ) области.
"Локус λ" включает в себя положение на хромосоме, например, хромосоме мыши, в котором у мыши дикого типа встречаются последовательности ДНК λ вариабельной (Vλ), λ соединяющей (Jλ) и λ константной (Сλ) области.
Термин "клетка" при использовании в отношении экспрессии последовательности включает в себя любую клетку, которая является подходящей для экспрессии рекомбинантной последовательности нуклеиновой кислоты. Клетки включают в себя клетки прокариот и эукариот (одноклеточных или многоклеточных), бактериальные клетки (например, штаммы Е. coli, Bacillus spp., Streptomyces spp. и т.д.), клетки микобактерий, клетки грибов, дрожжевые клетки (например, S. cerevisiae, S. pombe, P. pastoris, P. methanolica и т.д.), растительные клетки, клетки насекомых (например, SF-9, SF-21, инфицированные бакуловирусом клетки насекомых, Trichoplusia ni и т.д.), клетки отличных от человека животных, клетки человека или такие слияния клеток, как, например, гибридомы или квадромы. Согласно некоторым вариантам осуществления клетка представляет собой клетку человека, мартышки, человекообразной обезьяны, хомяка, крысы или мыши. Согласно некоторым вариантам осуществления клетка является эукариотической и выбрана из следующих клеток: СНО (например, СНО K1, DXB-11 СНО, Veggie-CHO), COS (например, COS-7), ретинальная клетка, Vero, CV1, почечная клетка (например, HEK293, 293 EBNA, MSR 293, MDCK, HaK, BHK), HeLa, HepG2, VVI38, MRC 5, Colo205, HB 8065, HL-60, (например, BHK21), Jurkat, Daudi, A431 (эпидермальная), CV-1, U937, 3Т3, клетка L, клетка С127, SP2/0, NS-O, MMT 060562, клетка Сертоли, клетка BRL 3A, клетка НТ1080, клетка миеломы, опухолевая клетка и клеточная линия, происходящая из вышеупомянутой клетки. Согласно некоторым вариантам осуществления клетка содержит один или несколько вирусных генов, например, ретинальная клетка, которая экспрессирует вирусный ген (например, клетка PER.C6™).
Фраза "определяющая комплементарность область", или термин "CDR", включает в себя аминокислотную последовательность, кодируемую последовательностью нуклеиновой кислоты генов иммуноглобулина организма, которая в норме (т.е. у животного дикого типа) находится между двумя каркасными областями в вариабельной области легкой или тяжелой цепи молекулы иммуноглобулина (например, антитела или Т-клеточного рецептора). CDR может кодироваться, например, зародышевой последовательностью или реаранжированной или нереаранжированной последовательностью, и, например, наивной или зрелой В-клеткой или Т-клеткой. В некоторых обстоятельствах (например, для CDR3), CDR могут кодироваться двумя или более последовательностями (например, зародышевыми последовательностями), которые не являются смежными (например, в нереаранжированной последовательности нуклеиновой кислоты), но являются смежными в последовательности нуклеиновой кислоты В-клетки, например, в результате сплайсинга или соединения последовательностей (например, V-D-J рекомбинации для образования CDR3 тяжелой цепи).
Фраза "генный сегмент" или "сегмент" включает в себя ссылку на генный сегмент иммуноглобулина V (легкий или тяжелый) или D или J (легкий или тяжелый), который включает в себя нереаранжированные последовательности на локусах иммуноглобулина (например, у людей и мышей), которые могут участвовать в реаранжировке (опосредованной, например, эндогенными рекомбиназами) для образования реаранжированной последовательности V/J или V/D/J. Если не указано иное, сегменты V, D и J содержат сигнальный последовательности рекомбинации (RSS), которые обеспечивают рекомбинацию V/J или рекомбинацию V/D/J согласно правилу 12/23. Если не указано иное, сегменты дополнительно содержат последовательности, с которыми они связаны в природе, или их функциональные эквиваленты (например, для V сегментов промотор(ы) и лидер(ы)).
Термин "нереаранжированный" включает в себя состояние локуса иммуноглобулина, при котором генные сегменты V и генные сегменты J (для тяжелых цепей, а также генные сегменты D) сохраняются отдельно, но они способны быть объединенными для образования реаранжированного гена V(D)J, который содержит один V,(D),J из репертуара V(D)J.
Фраза "микромолярный диапазон" подразумевает 1-999 микромоль; фраза "наномолярный диапазон" подразумевает 1-999 наномоль; фраза "пикомолярный диапазон" подразумевает 1-999 пикомоль.
Подразумевается, что термин "отличные от человека животные" включает в себя любые отличные от человека животные, такие как круглоротые, костные рыбы, такие хрящевые рыбы, как акулы и ромбовые скаты, амфибии, рептилии, млекопитающие и птицы. Подходящие отличные от человека животные включают в себя млекопитающих. Подходящие млекопитающие включают в себя отличных от человека приматов, коз, овец, свиней, собак, коров и грызунов. Подходящие отличные от человека животные выбраны из семейства грызунов, включающего в себя крысу и мышь. Согласно одному варианту осуществления отличные от человека животные представляют собой мышей.
Мышь в качестве генетической модели была значительно усовершенствована с помощью трансгенных технологий и технологий нокаута, которые предоставили возможность для изучения эффектов направленной избыточной экспрессии или делеции специфических генов. Несмотря на все свои преимущества, мышь все еще демонстрирует генетические затруднения, которые делают ее несовершенной моделью для заболеваний человека и несовершенной платформой для испытания или получения терапевтических средств для людей. Во-первых, несмотря на то, что приблизительно 99% генов человека имеют мышиный гомолог (Waterston, R.H., et al. (2002). Initial sequencing and comparative analysis of the mouse genome. Nature 420, 520-562.), потенциальные терапевтические средства зачастую не дают перекрестной реакции или дают неадекватную перекрестную реакцию с мышиными ортологами предполагаемых мишеней человека. Для устранения этой проблемы выбранные целевые гены могут быть "гуманизированы", то есть ген мыши может быть устранен и замещен соответствующей ортологичной генной последовательностью человека (например, патенты США №№6586251, 6596541 и 7105348, включенные в настоящий документ посредством ссылки). Изначально, попытки гуманизировать мышиные гены с помощью стратегии "генный нокаут вместе с трансгенной гуманизацией" предусматривали скрещивание мыши, несущей делецию (т.е., нокаут) эндогенного гена, с мышью, несущей интегрированный в произвольном порядке трансген человека (смотрите, например, Bril, W.S., et al. (2006). Tolerance to factor VIII in a transgenic mouse expressing human factor VIII cDNA carrying an Arg(593) to Cys substitution. Thromb Haemost 95, 341-347; Homanics, G.E., et al. (2006). Production and characterization of murine models of classic and intermediate maple syrup urine disease. BMC Med Genet 7, 33; Jamsai, D., et al. (2006). A humanized ВАС transgenic/knockout mouse model for HbE/beta-thalassemia. Genomics 88(3):309-15; Pan, Q., et al. (2006). Different role for mouse and human CD3delta/epsilon heterodimer in preT cell receptor (preTCR) function: human CD3delta/epsilon heterodimer restores the defective preTCR function in CD3gamma- and CD3gammadelta-deficient mice. Mol Immunol 43, 1741-1750). Но эти попытки затруднялись ограничениями в размере; традиционные технологии генного нокаута были недостаточными для прямого замещения больших мышиных генов их большими геномными эквивалентами человека. Простой подход прямого гомологичного замещения, при котором эндогенный мышиный ген напрямую замещается эквивалентным геном человека в том же точном генетическом положении гена меши (т.е., на эндогенном мышином локусе), редко предпринимался вследствие технических сложностей. До настоящего времени попытки прямого замещения предусматривали усложненные и трудные процедуры, таким образом, ограничивая длину генетического материала, с который могли быть произведены манипуляции, и точность, с которой эти манипуляции могли быть произведены.
Экзогенно введенные трансгены иммуноглобулина человека перестраиваются в предшественниках В-клеток у мышей (Alt, F.W., Blackwell, Т.K., and Yancopoulos, G.D. (1985). Immunoglobulin genes in transgenic mice. Trends Genet 1, 231-236). Это открытие использовалось в конструировании мышей с использованием генного нокаута вместе с трансгенным подходом для экспрессии антител человека (Green, L.L. et al. (1994). Antigen-specific human monoclonal antibodies from mice engineered with human Ig heavy and light chain YACs. Nat Genet 7, 13-21; Lonberg, N. (2005). Human antibodies from transgenic animals. Nat Biotechnol 23, 1117-1125; Lonberg, N., et al. (1994). Antigen-specific human antibodies from mice comprising four distinct genetic modifications. Nature 368, 856-859; Jakobovits, A., et al. (2007). From XenoMouse technology to panitumumab, the first fully human antibody product from transgenic mice. Nat Biotechnol 25, 1134-1143). Эндогенные локусы тяжелой цепи и к легкой цепи иммуноглобулина мыши инактивировали у этих мышей путем направленной делеции небольших, но критически важных частей каждого эндогенного локуса с последующим введением генных локусов иммуноглобулина человека в виде описанных выше случайным образом интегрированных больших трансгенов или минихромосом (Tomizuka, K., et al. (2000). Double trans-chromosomic mice: maintenance of two individual human chromosome fragments containing Ig heavy and kappa loci and expression of fully human antibodies. Proc Natl Acad Sci USA 97, 722-727). Такие мыши представляли важное преимущество в генной инженерии; выделенные из них полностью человеческие моноклональные антитела давали в результате перспективные терапевтические средства для лечения различных заболеваний человека (Gibson, Т.В., et al. (2006). Randomized phase III trial results of panitumumab, a fully human anti-epidermal growth factor receptor monoclonal antibody, in metastatic colorectal cancer. Clin Colorectal Cancer 6, 29-31; Jakobovits et al., 2007; Kim, Y.H., et al. (2007). Clinical efficacy of zanolimumab (HuMax-CD4): two Phase II studies in refractory cutaneous T-cell lymphoma. Blood 109(11):4655-62; Lonberg, 2005; Maker, A.V., et al. (2005). Tumor regression and autoimmunity in patients treated with cytotoxic T lymphocyte-associated antigen 4 blockade and interleukin 2: a phase I/II study. Ann Surg Oncol 12, 1005-1016; McClung, M.R., Lewiecki, E.M. et al. (2006). Denosumab in postmenopausal women with low bone mineral density. N Engl J Med 354, 821-831). Но, как обсуждалось выше, эти мыши проявляют нарушенное развитие В-клеток и иммунологические дефициты по сравнению с мышами дикого типа. Такие проблемы потенциально ограничивают способность мышей обеспечивать сильный гуморальный ответ и, следовательно, образовывать полностью человеческие антитела к некоторым антигенам. Недостаточности могут быть обусловлены следующим: (1) неэффективная функциональность вследствие введения случайным образом трансгенов иммуноглобулина человека и полученная в результате неправильная экспрессия вследствие отсутствия контролирующих элементов против хода транскрипции и по ее ходу (Garrett, F.E., et al. (2005). Chromatin architecture near a potential 3' end of the igh locus involves modular regulation of histone modifications during B-Cell development and in vivo occupancy at CTCF sites. Mol Cell Biol 25, 1511-1525; Manis, J.P., et al. (2003). Elucidation of a downstream boundary of the 3' IgH regulatory region. Mol Immunol 39, 753-760; Pawlitzky, I., et al. (2006). Identification of a candidate regulatory element within the 5' flanking region of the mouse Igh locus defined by pro-B cell-specific hypersensitivity associated with binding of PU.1, Pax5, and E2A. J Immunol 176, 6839-6851); (2) неэффективные межвидовые взаимодействия между константными доменами человека и мышиными компонентами В-клеточного рецепторного сигнального комплекса на клеточной поверхности, которые могут ослаблять сигнальные процессы, необходимые для нормального созревания, пролиферации и выживания В-клеток (Hombach, J., et al. (1990). Molecular components of the B-cell antigen receptor complex of the IgM class. Nature 343, 760-762); и (3) неэффективные межвидовые взаимодействия между растворимыми иммуноглобулинами человека и мышиными Fc рецепторами, которые могут снижать аффинную селекцию (Rao, S.P., et al. (2002). Differential expression of the inhibitory IgG Fc receptor FcgammaRIIB on germinal center cells: implications for selection of high-affinity В cells. J Immunol 169, 1859-1868) и концентрации иммуноглобулинов в сыворотке (Brambell, F.W., et al. (1964). A Theoretical Model of Gamma-Globulin Catabolism. Nature 203, 1352-1354; Junghans, R.P., and Anderson, C.L. (1996). The protection receptor for IgG catabolism is the beta2-microglobulin-containing neonatal intestinal transport receptor. Proc Natl Acad Sci USA 93, 5512-5516; Rao et al., 2002; Hjelm, F., et al. (2006). Antibody-mediated regulation of the immune response. Scand J Immunol 64, 177-184; Nimmerjahn, F., and Ravetch, J.V. (2007). Fc-receptors as regulators of immunity. Adv Immunol 96, 179-204). Эти дефициты можно корректировать с помощью гуманизации in situ только вариабельных областей локусов иммуноглобулина мыши в пределах их естественных положений на эндогенных локусах тяжелых и легких цепей. Это будет действительно давать в результате мышей, которые образуют обратные химерные антитела (т.е. V человека: С мыши), которые будут способны к нормальным взаимодействиям и селекции в мышином окружении на основании сохранения константных областей мыши. Более того, такие обратные химерные антитела легко реформатируются в полностью человеческие антитела для терапевтических целей.
Генетически модифицированные животные, которые содержат замещение на эндогенном локусе тяжелой цепи иммуноглобулина гетерологичными (например, от другого вида) последовательностями иммуноглобулина, могут быть получены в сочетании с замещениями на эндогенных локусах легкой цепи иммуноглобулина или в сочетании с трансгенами легкой цепи иммуноглобулина (например, химерными трансгенами легкой цепи иммуноглобулина или полностью человеческими полностью мышиными и т.д.). Вид, из которого происходят гетерологичные последовательности тяжелой цепи иммуноглобулина, может изменяться в широком диапазоне; как и в случае последовательностей легкой цепи иммуноглобулина, используемых в замещениях последовательности легкой цепи иммуноглобулина или трансгенов легкой цепи иммуноглобулина.
Последовательности нуклеиновой кислоты вариабельной области иммуноглобулина, например, сегменты V, D и/или J согласно различным вариантам осуществления получены от человека или отличного от человека животного. Отличные от человека животные, подходящие для предоставления сегментов V, D и/или J, включают в себя, например, костных рыб, таких хрящевых рыб, как акулы и ромбовидные скаты, амфибий, рептилий, млекопитающих, птиц (например, куриц). Отличные от человека животные включают в себя, например, млекопитающих. Млекопитающие включают в себя, например, отличных от человека приматов, коз, овец, свиней, собак, крупный рогатый скот (например, корову, быка, буйвола), оленя, верблюдов, хорьков и грызунов и отличных от человека приматов (например, шимпанзе, орангутанов, горилл, игрунок, макак-резусов, бабуинов). Подходящие отличные от человека животные выбраны из семейства грызунов, включающего в себя крыс, мышей и хомяков. Согласно одному варианту осуществления отличные от человека животные представляют собой мышей. Из контекста ясно, что различные отличные от человека животные могут быть использованы в качестве источника вариабельных доменов или генных сегментов вариабельной области (например, акулы, ромбовидные скаты, млекопитающие (например, верблюды, такие грызуны, как мыши и крысы).
Согласно контексту отличные от человека животные также используются в качестве источника последовательностей константной области для применения вместе с вариабельными последовательностями или сегментами, например, константные последовательности грызуна могут использоваться в трансгенах, функционально связанных с относящимися к человеку или не относящимися к человеку вариабельными последовательностями (например, вариабельные последовательности человека или отличного от человека примата, функционально связанные, например, с константными последовательностями грызуна, например, мыши или крысы или хомяка). Таким образом, согласно различным вариантам осуществления сегменты V, D и/или J человека функционально связаны с генными последовательностями константной области грызуна (например, мыши или крысы или хомяка). Согласно некоторым вариантам осуществления сегменты V, D и/или J человека (или одного или нескольких реаранжированных генов VDJ или VJ) функционально связаны или слиты с генной последовательностью константной области мыши, крыса или хомяка, например, в трансгене, интегрированном в локус, который не является эндогенным локусом иммуноглобулина.
Согласно конкретному варианту осуществления предусмотрена мышь, которая содержит замещение генных сегментов VH, DH, и JH на эндогенном локусе тяжелой цепи иммуноглобулина одним или несколькими сегментами VH, DH и JH человека, причем один или несколько сегментов VH, DH и JH человека функционально связаны с эндогенным константным геном тяжелой цепи иммуноглобулина; причем мышь содержит трансген на локусе, отличном от эндогенного локуса иммуноглобулина, причем трансген содержит нереаранжированный или реаранжированный сегмент VL человека и JL человека, функционально связанный с константной областью мыши или крысы или человека.
Согласно конкретному варианту осуществления предусмотрена мышь, которая содержит вставку одного или нескольких генных сегментов VH, DH и JH человека на эндогенном локусе тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления вставка находится выше эндогенного константного гена тяжелой цепи иммуноглобулина; согласно одному варианту осуществления вставка находится ниже эндогенного вариабельного (V) генного сегмента; согласно одному варианту осуществления вставка находится ниже эндогенного дополнительного (D) генного сегмента; согласно одному варианту осуществления вставка находится ниже эндогенного соединяющего (J) генного сегмента. Согласно различным вариантам осуществления вставка находится так, что один или несколько генных сегментов VH, DH и JH человека расположены в функциональной связи с одним или несколькими эндогенными константными генами тяжелой цепи.
Описан способ для большого генетического замещения in situ зародышевых вариабельных генных локусов иммуноглобулина мыши зародышевыми вариабельными генными локусами иммуноглобулина человека при сохранении способности мышей производить потомство. В частности, описано точное замещение шести миллионов пар нуклеотидов вариабельных генных локусов как тяжелой цепи, так и κ легкой цепи иммуноглобулина мыши их эквивалентами человека при сохранении константных областей мыши интактными. В результате были образованы мыши, которые содержат точное замещение их полного зародышевого репертуара вариабельной области иммуноглобулина эквивалентными зародышевыми последовательностями вариабельной области иммуноглобулина человека при сохранении константных областей мыши. Вариабельные области человека соединяют с константными областями мыши для образования химерных человеческо-мышиных иммуноглобулиновых локусов, которые перестраиваются и экспрессируются на физиологически приемлемых уровнях. Экспрессированные антитела представляют собой "обратные химеры", т.е. они содержат последовательности вариабельной области человека и последовательности константной области мыши. Эти мыши, характеризующиеся гуманизированными вариабельными областями иммуноглобулина, которые экспрессируют антитела, содержащие вариабельные области человека и константные области мыши, имею название мыши VELCOIMMUNE®.
Гуманизированные мыши VELOCIMMUNE® проявляют полностью функциональную гуморальную иммунную систему, которая по существу неотличима от таковой у мышей дикого типа. Они проявляют нормальные клеточные популяции на всех стадиях развития В-клеток. Они проявляют нормальную морфологию лимфоидных органов. Последовательности антител мышей VELOCIMMUNE® проявляют нормальную реаранжировку V(D)J и нормальные показатели частоты соматической гипермутации. Популяции антител у этих мышей отражает распределения изотипов, которые являются результатом нормального переключения класса (например, нормального цис-переключения изотипа). Иммунизация мышей VELOCIMMUNE® приводит к устойчивым гуморальным иммунным ответам, которые образуют большие, разнообразные репертуары антител, содержащих вариабельные домены иммуноглобулина человека, подходящие в качестве кандидатов терапевтических средств. Эта платформа предоставляет обильный источник последовательностей вариабельной области иммуноглобулина человека естественным образом созревшей аффинности для получения фармацевтически приемлемых антител и других связывающих антиген белков.
Это представляет собой точное замещение последовательностей вариабельной области иммуноглобулина мыши последовательностями вариабельной области иммуноглобулина человека, которое обеспечивает возможность получения мышей VELOCIMMUNE®. Даже точное замещение эндогенных последовательностей иммуноглобулина мыши на локусах тяжелых и легких цепей эквивалентными последовательностями иммуноглобулина человека с помощью последовательной рекомбинационной инженерии очень больших интервалов последовательностей иммуноглобулина человека может представлять определенные проблемы вследствие дивергентной эволюции локусов иммуноглобулина между мышью и человеком. Например, межгенные последовательности, разбросанные в пределах локусов иммуноглобулина, не идентичны между мышами и людьми и в некоторых обстоятельствах могут не быть функционально эквивалентными. Различия между мышами и людьми в их локусах иммуноглобулина может все еще приводить к аномалиям у гуманизированных мышей, в частности, при гуманизации или манипуляции с определенными частями эндогенных локусов тяжелой цепи иммуноглобулина мыши. Некоторые модификации на локусах тяжелой цепи иммуноглобулина мыши являются вредными. Вредные модификации могут включать в себя, например, потерю способности модифицированных мышей спариваться и производить потомство. Согласно различным вариантам осуществления конструирование последовательностей иммуноглобулина человека в геноме мыши включает в себя способы, которые сохраняют эндогенные последовательности, которые при отсутствии у модифицированных линий мышей являются вредными. Иллюстративные неблагоприятные эффекты могут включать в себя неспособность воспроизводить модифицированные линии, потерю функции жизненно важных генов, неспособность экспрессировать полипептиды и т.д. Такие неблагоприятные эффекты могут быть напрямую или косвенно связаны с модификацией, разработанной в геноме мыши.
Проводили точное, крупномасштабное замещение in situ шести миллионов пар нуклеотидов вариабельных областей локусов тяжелых и легких цепей иммуноглобулина мыши (VH-DH-JH и Vκ-Jκ) соответствующими геномными последовательностями человека, составляющими 1,4 миллиона пар нуклеотидов при сохранении фланкирующих последовательностей мыши интактными и функциональными в пределах гибридных локусов, включающих в себя все гены константной цепи мыши и области транскрипционного контроля локуса (фиг. 1А и фиг. 1В). В частности, генные последовательности VH, DH, JH, Vκ и Jκ человека вводили посредством поэтапной вставки 13 химерных основанных на ВАС нацеливающих векторов, несущих перекрывающиеся фрагменты зародышевых вариабельных локусов человека, в мышиные ES клетки с использованием технологии генетической инженерии VELOCIGENE® (смотрите, например, патент США №6586251 и Valenzuela, D.M. et al. (2003). High-throughput engineering of the mouse genome coupled with high-resolution expression analysis. Nat Biotechnol 21, 652-659).
Гуманизация генов иммуноглобулина мыши представляет наибольшую генетическую модификацию мышиного генома к настоящему времени. Наряду с тем что предыдущие попытки с интегрированными случайным образом трансгенами иммуноглобулина человека оказались в некоторой степени успешными (как обсуждалось выше), прямое замещение генов иммуноглобулина мыши их эквивалентами человека значительно увеличивает результативность, с которой полностью человеческие антитела могут быть эффективно образованы у нормальных в других отношениях мышей. Кроме того, такие мыши проявляют значительно увеличенное разнообразие полностью человеческих антител, которые могут быть получены после иммунизации фактически любым антигеном, по сравнению с мышами, несущими недееспособные эндогенные локусы и трансгены полностью человеческих антител. Многочисленные варианты замещенных, гуманизированных локусов проявляют полностью нормальные уровни зрелых и незрелых В-клеток, в отличие от мышей с интегрированными случайным образом трансгенами человека, которые проявляют значительно уменьшенные популяции В-клеток на различных стадиях дифференциации. Наряду с тем что попытки по увеличению числа генных сегментов человека у гуманизированных трансгенных мышей снизили такие дефекты, расширенные иммуноглобулиновые репертуары не скорректировали в общей сложности снижения в популяциях В-клеток по сравнению с мышами дикого типа.
Несмотря на то, что близкая к дикому типу гуморальная иммунная функция, наблюдаемая у мышей с замещенными локусами иммуноглобулина (т.е. у мышей VELOCIMMUNE®), существуют другие обнаруживаемые при использовании прямого замещения иммуноглобулина сложности, которые не встречаются в некоторых подходах, которые используют интегрированные случайным образом трансгены. Различия в генетическом составе иммуноглобулиновых локусов между мышами и людьми привело к открытию последовательностей, преимущественных для размножения мышей с замещенными иммуноглобулиновыми генными сегментами. В частности, гены ADAM мыши, расположенные в пределах эндогенного локуса иммуноглобулина, оптимально присутствуют у мышей с замещенными иммуноглобулиновыми локусами вследствие их роли в фертильности.
Положение в геноме и функция ADAM6 мыши
Самцы мышей, у которых отсутствует способность экспрессировать какой-либо функциональный белок ADAM6, неожиданно проявляют дефект в способности мышей спариваться и давать потомство. Мыши утрачивают способность экспрессировать функциональный белок ADAM6 посредством замещения всех или по существу всех генных сегментов вариабельной области иммуноглобулина мыши генными сегментами вариабельной области человека. Потеря функции ADAM6 происходит, поскольку локус ADAM6 расположен в пределах области эндогенного генного локуса вариабельной области тяжелой цепи иммуноглобулина мыши, проксимального к 3' концу локуса генного сегмента VH, который находится выше генных сегментов DH. Разведение мышей, являющихся гомозиготными в отношении замещения всех или по существу всех эндогенных вариабельных генных сегментов тяжелой цепи мыши генными сегментами вариабельной области тяжелой цепи человека, как правило, представляет собой трудоемкий подход для спаривания самцов и самок, каждый из которых являются гомозиготными в отношении замещения, и ожидания продуктивного спаривания. Частота и размер успешных пометов являются низкими. Вместо этого, самцы, гетерозиготные в отношении замещения, использовались для спаривания с самками, гомозиготными в отношении замещения, для получения потомства, которое является гетерозиготным в отношении замещения, затем выводя из него гомозиготную мышь. Авторы настоящего изобретения показали, что вероятной причиной потери фертильности у самцов мышей является отсутствие у гомозиготных самцов мышей функционального белка ADAM6.
Согласно различным аспектам самцы мышей, которые содержат поврежденный (т.е. нефункциональный или незначительно функциональный) ген ADAM6, проявляют снижение или устранение фертильности. Поскольку у мышей (и других грызунов) ген ADAM6 расположен в локусе тяжелой цепи иммуноглобулина, авторы настоящего изобретения определили, что для того чтобы воспроизвести мышей или создать и поддержать линию мышей, которые содержат замещенный локус тяжелой цепи иммуноглобулина, использовали различные модифицированные схемы скрещивания или размножения. Низкая фертильность, или стерильность, самцов мышей, гомозиготных в отношении замещения эндогенного вариабельного генного локуса тяжелой цепи иммуноглобулина затрудняет поддержание такой модификации в линии мыши. Согласно различным вариантам осуществления сохранение линии предусматривает устранение проблем со стерильностью, которые проявляют самцы мышей, гомозиготные в отношении замещения.
Согласно одному аспекту предусмотрен способ поддержания линии описанной в настоящем документе мыши. Линия мыши может не содержать эктопическую последовательность ADAM6, и согласно различным вариантам осуществления линия мыши является гомозиготным или гетерозиготным в отношении нокаута (например, функционального нокаута) ADAM6.
Линия мыши содержит модификацию эндогенного локуса тяжелой цепи иммуноглобулина, которая приводит к снижению или потере фертильности у самца мыши. Согласно одному варианту осуществления модификация предусматривает делецию регуляторной области и/или кодирующей области гена ADAM6. Согласно конкретному варианту осуществления модификация предусматривает модификацию эндогенного гена ADAM6 (регуляторной и/или кодирующей области), которая снижает или устраняет фертильность самца мыши, который содержит модификацию; согласно конкретному варианту осуществления модификация снижает или устраняет фертильность самца мыши, который является гомозиготным в отношении модификации.
Согласно одному варианту осуществления линия мыши является гомозиготным или гетерозиготным в отношении нокаута (например, функционального нокаута) или делеции гена ADAM6.
Согласно одному варианту осуществления линию мыши поддерживают путем выделения из мыши, которая является гомозиготной или гетерозиготной в отношении модификации, клетки, и использование донорной клетки в зародыше-хозяине и вынашивание зародыша-хозяина и донорной клетки в суррогатной матери и получение от суррогатной матери потомства, которое содержит генетическую модификацию. Согласно одному варианту осуществления донорная клетка представляет собой ES клетку. Согласно одному варианту осуществления донорная клетка представляет собой плюрипотентную клетку, например, индуцированную плюрипотентную клетку.
Согласно одному варианту осуществления линию мыши поддерживают путем выделения из мыши, которая является гомозиготной или гетерозиготной в отношении модификации, последовательности нуклеиновой кислоты, содержащей модификацию, и введение последовательности нуклеиновой кислоты в ядро-хозяина и вынашивание клетки, содержащей последовательность нуклеиновой кислоты и ядро-хозяин в подходящем животном. Согласно одному варианту осуществления последовательность нуклеиновой кислоты вводят в зародыш из ооцита-хозяина.
Согласно одному варианту осуществления линию мыши поддерживают путем выделения из мыши, которая является гомозиготной или гетерозиготной в отношении модификации, ядра и введение ядра в клетку-хозяин, и вынашивание ядра и клетки-хозяина в подходящем животном для получения потомства, которое является гомозиготным или гетерозиготным в отношении модификации.
Согласно одному варианту осуществления линию мыши поддерживают путем использования оплодотворения in vitro (IVF) самки мыши (дикого типа, гомозиготной в отношении модификации или гетерозиготной в отношении модификации), используя сперму от самца мыши, содержащего генетическую модификацию. Согласно одному варианту осуществления самец мыши является гетерозиготным в отношении генетической модификации. Согласно одному варианту осуществления самец мыши является гомозиготным в отношении генетической модификации.
Согласно одному варианту осуществления линию мыши поддерживают путем скрещивания самца мыши, который является гетерозиготным в отношении генетической модификации, с самкой мыши для получения потомства, которое содержит генетическую модификацию, идентификации мужского и женского потомства, содержащего генетическую модификацию, и использования самца, который является гетерозиготным в отношении генетической модификации, в скрещивании с самкой, которая относится к дикому типу, является гомозиготной или гетерозиготной в отношении генетической модификации, для получения потомства, содержащего генетическую модификацию. Согласно одному варианту осуществления стадию скрещивания самца, гетерозиготного в отношении генетической модификации, с самкой дикого типа, самкой, гетерозиготной в отношении генетической модификации, или самкой, гомозиготной в отношении генетической модификации, повторяют для поддержания генетической модификации в линии мыши.
Согласно одному аспекту предусмотрен способ поддержания линии мыши, который предусматривает замещение эндогенного вариабельного генного локуса тяжелой цепи иммуноглобулина одним или несколькими последовательностями тяжелой цепи иммуноглобулина человека, предусматривая скрещивание линии мыши так, чтобы создать гетерозиготных самцов мышей, причем гетерозиготных самцов мышей скрещивают для поддержания генетической модификации в линии. Согласно конкретному варианту осуществления линию не поддерживают путем какого-либо скрещивания гомозиготного самца с самкой дикого типа или самкой, гомозиготной или гетерозиготной в отношении генетической модификации.
Белок ADAM6 представляет собой представителя семейства ADAM белков, где ADAM представляет собой сокращение англ. A Disintegrin And Metalloprotease (дизинтегрин и металлопротеаза). Семейство белков ADAM является большим и разнообразным, с различными функциями, включая в себя клеточную адгезию. Некоторые представители семейства ADAM вовлечены в сперматогенез и оплодотворение. Например, ADAM2 кодирует субъединицу белка фертилина, который вовлечен во взаимодействия сперматозоидов и яйцеклетки. ADAM3, или циритестин, оказывается необходимым для связывания сперматозоида с вителлиновым слоем. Отсутствие или ADAM2, или ADAM3 приводит к стерильности. Предположили, что ADAM2, ADAM3 и ADAM6 формируют комплекс на поверхности мышиных сперматозоидов.
Ген ADAM6 человека, в норме встречающийся между VH генными сегментами VH1-2 и VH6-1 человека, по-видимому, является псевдогеном (фигура 12). У мышей существует два гена ADAM6 - ADAM6a и ADAM6b - которые встречаются в межгенной области между генными сегментами VH и DH мыши, и у мыши ADAM6a и ADAM6b гены ориентированы в транскрипционной ориентации, противоположной ориентации транскрипции окружающих иммуноглобулиновых генных сегментов (фиг. 12). У мышей функциональный локус ADAM6 очевидно необходим для нормального оплодотворения. Функциональный локус или последовательность ADAM6, затем относится к локусу или последовательности ADAM6, которая может дополнить или восстановить резко сниженное оплодотворение, демонстрируемое самцами мышей с утраченными или нефункциональными эндогенными локусами ADAM6.
Положение межгенной последовательности у мышей, которая кодирует ADAM6a и ADAM6b, делает межгенную последовательность подверженной модификации при модификации эндогенной тяжелой цепи мыши. Когда генные сегменты VH подвергаются делеции или замещаются или когда генные сегменты DH подвергаются делеции или замещаются, существует высокая вероятность того, что полученная мышь будет проявлять тяжелую недостаточность фертильности. Для компенсации этой недостаточности мышь модифицируют, чтобы включить в нее нуклеотидную последовательность, которая кодирует белок, который будет дополнять потерю активности ADAM6 вследствие модификации эндогенного локуса ADAM6 мыши. Согласно различным вариантам осуществления дополняющая нуклеотидная последовательность представляет собой такую, которая кодирует мышиный ADAM6a, мышиный ADAM6b или его гомолог или ортолог или функциональный фрагмент, который восстанавливает недостаточность фертильности. Альтернативно, могут использоваться подходящие способы для сохранения эндогенного локуса ADAM6, при это делая эндогенные последовательности тяжелой цепи иммуноглобулина, фланкирующие локус ADAM6 мыши, неспособными к реаранжировке, чтобы кодировать функциональную эндогенную вариабельную область тяжелой цепи. Иллюстративные альтернативные способы включают в себя манипуляцию с большими частями хромосом мыши, которые располагают эндогенные локусы вариабельной области тяжелой цепи иммуноглобулина таким образом, что они являются неспособными к реаранжировке, чтобы кодировать функциональную вариабельную область тяжелой цепи, которая функционально связана с эндогенным константным геном тяжелой цепи. Согласно различным вариантам осуществления способы предусматривают вставки и/или транслокации хромосомных фрагментов мыши, содержащих эндогенные генные сегменты тяжелой цепи иммуноглобулина.
Нуклеотидная последовательность, которая восстанавливает фертильность, может быть расположена в любом подходящем положении. Она может быть расположена в межгенной области или в любом подходящем положении в геноме (т.е. эктопически). Согласно одному варианту осуществления нуклеотидная последовательность может быть введена в трансген, который случайным образом интегрирован в геном мыши. Согласно одному варианту осуществления последовательность может храниться эписомно, то есть на отдельной нуклеиновой кислоте, а не на хромосоме мыши. Подходящие положения предусматривают положения, которые являются транскрипционно пермиссивными или активными, например, локус ROSA26 (Zambrowicz et at., 1997, PNAS USA 94:3789-3794), локус BT-5 (Michael et al., 1999, Mech. Dev. 85:35-47), или локус Oct4 (Wallace et al., 2000, Nucleic Acids Res. 28:1455-1464). Нацеливание нуклеотидных последовательностей на транскрипционно активные локусы описаны, например, в патенте США №7473557, включенный посредством ссылки в настоящий документ.
Альтернативно нуклеотидная последовательность, которая восстанавливает фертильность, может быть соединена с индуцируемым промотором так, чтобы облегчать оптимальную экспрессию в соответствующих клетках и/или тканях, например, репродуктивных тканях. Иллюстративные индуцируемые промоторы включают в себя промоторы, активируемые физическими (например, промотор теплового шока) и/или химическими средствами (например, IPTG или тетрациклином).
Кроме того, экспрессия нуклеотидной последовательности может быть ассоциирована с другими генами так, чтобы достичь экспрессии на конкретной стадии развития или в специфических тканях. Такая экспрессия может быть достигнута путем помещения нуклеотидной последовательности в функциональной связи с промотором гена, экспрессируемого на конкретной стадии развития. Например, последовательности иммуноглобулина от одного вида, сконструированные в геноме вида-хозяина, помещают в функциональной связи с промоторной последовательностью гена CD19 (специфический для В-клеток ген) от вида-хозяина. Достигается специфическая для В-клеток экспрессия на точно определенных стадиях развития при экспрессии иммуноглобулинов.
Еще один способ достижения устойчивой экспрессии вставленной нуклеотидной последовательности предусматривает использование конститутивного промотора. Иллюстративные конститутивные промоторы включают в себя SV40, CV, UBC, EF1A, PGK и CAGG. Аналогичным образом, требуемая нуклеотидная последовательность располагают в функциональной связи с выбранным конститутивным промотором, что обеспечивает высокий уровень экспрессии белка(ов), кодируемого(ых) нуклеотидной последовательностью.
Предусматривается, что термин "эктопический" включает в себя перемещение или размещение в положении, которое в норме не встречается в природе (например, размещение последовательности нуклеиновой кислоты в положении, которое не является аналогичным положением, в котором последовательность нуклеиновой кислоты встречается у мыши дикого типа). Термин согласно различным вариантам осуществления используется в том смысле, что его объект находится за пределами его нормального, или правильного, положения. Например, фраза "эктопическая нуклеотидная последовательность, кодирующая…" относится к нуклеотидной последовательности, которая находится в положении, в котором она не встречается в норме у мыши. Например, в случае эктопической нуклеотидной последовательности, кодирующей белок ADAM6 мыши (или ее ортолога или гомолога или фрагмента, который обеспечивает такое же или сходное улучшение фертильности у самцов мышей), последовательность может быть расположена в положении в геноме мыши, которое отличается от встречающегося в норме у мыши дикого типа. В таких случаях, новые участки соединения последовательности для последовательности мыши будут создаваться путем помещения последовательности в положение в геноме мыши, отличное от такового у мыши дикого типа. Функциональный гомолог или ортолог ADAM6 мыши представляет собой последовательность, которая обеспечивает восстановление потери фертильности (например, потери способности самца мыши давать потомство путем спаривания), которая наблюдается у мыши ADAM6-/-. Функциональные гомологи или ортологи предусматривают белки, которые характеризуются по меньшей мере приблизительно 89% идентичности или более, например, до 99% идентичности, с аминокислотной последовательностью ADAM6a и/или с аминокислотной последовательностью ADAM6b, и которые могут дополнять или восстанавливать способность успешно спариваться у мыши, характеризующейся фенотипом, который содержит делецию или нокаут ADAM6a и/или ADAM6b.
Эктопическое положение может находиться где-либо (например, как в случае случайной вставки трансгена, содержащего последовательность ADAM6 мыши), или может находиться, например, в положении, которое приблизительно соответствует (но не является точно таким же как) его расположение у мыши дикого типа (например, в модифицированном эндогенном локусе иммуноглобулина мыши, но или выше, или ниже в отношении хода транскрипции от его естественного положения, например, в пределах модифицированного локуса иммуноглобулина, но между различными генными сегментами, или в другом положении в V-D межгенной последовательности мыши). Один пример эктопического размещения представляет собой поддержание положения, встречающегося в норме у мышей дикого типа в пределах эндогенного локуса тяжелой цепи иммуноглобулина, при этом делая окружающие эндогенные генные сегменты тяжелой цепи неспособными к реаранжировке, чтобы кодировать функциональную тяжелую цепь, содержащую эндогенную константную область тяжелой цепи. Согласно описанному примеру, это можно осуществить путем инверсии хромосомного фрагмента, содержащего эндогенные вариабельные локусы тяжелой цепи иммуноглобулина, например с использованием сконструированных сайтов сайт-специфической рекомбинации, помещенных в положениях, фланкирующих локус вариабельной области. Таким образом, при рекомбинации эндогенные локусы вариабельной области тяжелой цепи помещаются на большом расстоянии от эндогенных генов константной области тяжелой цепи, тем самым предотвращая реаранжировку для кодирования функциональной тяжелой цепи, содержащей эндогенную константную область тяжелой цепи. Другие иллюстративные способы для достижения функционального сайленсинга эндогенного вариабельного генного локуса тяжелой цепи иммуноглобулина при сохранении функционального локуса ADAM6 будут очевидными специалистам в настоящей области техники при прочтении настоящего раскрытия и/или в комбинации со способами, известными в настоящей области техники. При таком размещении эндогенного локуса тяжелой цепи эндогенные гены ADAM6 сохраняются, и эндогенный локус тяжелой цепи иммуноглобулина является функционально выключенным.
Другой пример эктопического размещения представляет собой размещение в пределах гуманизированного локуса тяжелой цепи иммуноглобулина. Например, мышь, содержащая замещение одного или нескольких эндогенных генных сегментов VH генными сегментами VH человека, причем замещение удаляет эндогенную последовательность ADAM6, может быть сконструирована так, чтобы содержать последовательность ADAM6 мыши, расположенную в пределах последовательности, которая содержит генные сегменты VH человека. Полученная модификация будет образовывать (эктопическую) последовательность ADAM6 мыши в пределах генной последовательности человека, и (эктопическое) размещение последовательности ADAM6 мыши в пределах генной последовательности человека может приблизительно соответствовать положению псевдогена ADAM6 человека (т.е., между двумя сегментами V) или может приблизительно соответствовать положению последовательности ADAM6 мыши (т.е. в пределах V-D межгенной области). Полученные участки соединения последовательности, созданные соединением (эктопической) последовательности ADAM6 мыши в пределах или рядом с генной последовательностью человека (например, генной последовательностью иммуноглобулина) в зародышевой линии мыши, будут новыми по сравнению с таким же или аналогичным положением в геноме мыши дикого типа.
Согласно различным вариантам осуществления предусмотрены отличные от человека животные, у которых отсутствует ADAM6 или его ортолог или гомолог, причем отсутствие делает отличного от человека животного стерильным или по существу снижает фертильность отличного от человека животного. Согласно различным вариантам осуществления отсутствие ADAM6 или его ортолога или гомолога обусловлено модификацией эндогенного локуса тяжелой цепи иммуноглобулина. Существенное снижение фертильности, например, представляет собой снижение фертильности (например, частоты скрещивания, количества детенышей на помет, количества пометов в год и т.д.) приблизительно на 50%, 60%, 70%, 80%, 90% или 95% или больше. Согласно различным вариантам осуществления отличным от человека животным добавляют ген ADAM6 мыши или его ортолог или гомолог или функциональный фрагмент, который является функциональным у самца отличного от человека животного, причем добавленный ген ADAM6 или его ортолог или гомолог или функциональный фрагмент восстанавливает снижение фертильности полностью или существенную ее часть. Восстановление существенной части фертильности представляет собой, например, такое восстановление фертильности, что отличное от человека животное проявляет фертильность, которая составляет по меньшей мере 70%, 80% или 90% или больше по сравнению с немодифицированным (т.е. животное без модификации гена ADAM6 или его ортолога или гомолога) локусом тяжелой цепи.
Последовательность, которая обеспечивает генетически модифицированное животное (т.е. животное, которое не содержит функциональный ADAM6 или его ортолог или гомолог, вследствие, например, модификации локуса тяжелой цепи иммуноглобулина), согласно различным вариантам осуществления выбрана из гена ADAM6 или его ортолога или гомолога. Например, у мыши потеря функции ADAM6 восстанавливается путем добавления согласно одному варианту осуществления гена ADAM6 мыши. Согласно одному варианту осуществления потеря функции ADAM6 у мыши восстанавливается путем добавления ортолога или гомолога близкородственных видов по отношению к мыши, например, грызуна, например, мыши другой линии или вида, крысы любого вида, грызуна; причем добавление мыши ортолога или гомолога восстанавливает потерю фертильности вследствие потери функции ADAM6 или потери гена ADAM6. Ортологи и гомологи из других видов согласно различным вариантам осуществления выбраны из филогенетически родственного вида и согласно различным вариантам осуществления проявляют процентную идентичность по отношению к эндогенному ADAM6 (или ортологу), которая составляет приблизительно 80% или более, 85% или более, 90% или более, 95% или более, 96% или более, или 97% или более; и которые восстанавливают связанную с ADAM6 или (у не относящихся к мыши) связанную с ортологом ADAM6 потерю фертильности. Например, у генетически модифицированного самца крысы, у которого отсутствует функция ADAM6 (например, крыса с эндогенной вариабельной областью тяжелой цепи иммуноглобулина, замещенной вариабельной областью тяжелой цепи иммуноглобулина человека, или нокаут у крысы области тяжелой цепи иммуноглобулина), потеря фертильности у крысы восстанавливается путем добавления ADAM6 крысы или согласно некоторым вариантам осуществления ортолога ADAM6 крысы (например, ортолога ADAM6 от другой линии или вида крысы или согласно одному варианту осуществления от мыши).
Таким образом, согласно различным вариантам осуществления генетически модифицированные животные, которые не проявляют фертильности или снижение фертильности вследствие модификации последовательности нуклеиновой кислоты, кодирующей белок ADAM6 (или его ортолог или гомолог) или регуляторной области, функционально связанной с последовательностью нуклеиновой кислоты, содержат последовательность нуклеиновой кислоты, которая взаимодополняет или восстанавливает потерю фертильности, если последовательность нуклеиновой кислоты, которая взаимодополняет или восстанавливает потерю фертильности, происходит от другой линии того же вида или из филогенетически родственного вида. Согласно различным вариантам осуществления взаимодополняющая последовательность нуклеиновой кислоты представляет собой ADAM6, его ортолог или гомолог или функциональный фрагмент. Согласно различным вариантам осуществления взаимодополняющий ортолог ADAM6 или его гомолог или функциональный фрагмент происходит от отличного от человека животного, которое является близкородственным генетически модифицированному животному с нарушением фертильности. Например, если генетически модифицированное животное представляет собой мышь конкретной линии, ортолог ADAM6 или его гомолог или функциональный фрагмент может быть получен от мыши другой линии или мыши родственного вида. Согласно одному варианту осуществления если генетически модифицированное животное, содержащее нарушение фертильности, происходит из отряда Rodentia, то ортолог ADAM6 или его гомолог или функциональный фрагмент происходит от другого животного отряда Rodentia. Согласно одному варианту осуществления генетически модифицированное животное, содержащее нарушение фертильности, происходит из подотряда Myomoropha (например, тушканчики, полутушканчики, мышевидные хомяки, хомяки, крысы и мыши Нового Света, полевки, истинные мыши и крысы, карликовые песчанки, иглистые мыши, косматые хомяки, рипидомисы, скалистые хомячки, белохвостые крысы, мадагаскарские крысы и мыши, колючие соневидные хомяки, слепыши, бамбуковые крысы, цокоры), и ортолог ADAM6 или его гомолог или функциональный фрагмент выбран из животного отряда Rodentia или подотряда Myomorpha.
Согласно одному варианту осуществления генетически модифицированное животное происходит из надсемейство Dipodoidea, и ортолог ADAM6 или его гомолог или функциональный фрагмент происходит из надсемейства Muroidea. Согласно одному варианту осуществления генетически модифицированное животное происходит из надсемейство Muroidea, и ортолог ADAM6 или его гомолог или функциональный фрагмент происходит из надсемейства Dipodoidea.
Согласно одному варианту осуществления генетически модифицированное животное представляет собой грызуна. Согласно одному варианту осуществления грызун выбран из надсемейства Muroidea, и ортолог или гомолог ADAM6 происходит от другого вида в пределах надсемейства Muroidea. Согласно одному варианту осуществления генетически модифицированное животное происходит из семейства, выбранного из Calomyscidae (например, мышевидные хомяки), Cricetidae (например, хомяк, крысы и мыши Нового Света, полевки), Muridae (настоящие мыши и крысы, карликовые песчанки, иглистые мыши, косматые хомяки), Nesomyidae (рипидомисы, скалистые хомячки, белохвостые крысы, мадагаскарские крысы и мыши), Platacanthomyidae (например, колючие соневидные хомяки), и Spalacidae (например, слепыши, бамбуковые крысы и цокоры); и ортолог или гомолог ADAM6 выбран из другого вида того же семейства. Согласно конкретному варианту осуществления генетически модифицированный грызун выбран из настоящей мыши или крысы (семейство Muridae), и ортолог или гомолог ADAM6 происходит от вида, выбранного из карликовой песчанки, иглистой мыши, косматого хомяка. Согласно одному варианту осуществления генетически модифицированная мышь происходит из представителя семейства Muridae, и ортолог или гомолог ADAM6 происходит от другого вида семейства Muridae. Согласно конкретному варианту осуществления генетически модифицированный грызун представляет собой мышь семейства Muridae, и ортолог или гомолог ADAM6 происходит от крысы, карликовой песчанки, иглистой мыши, косматого хомяка семейства Muridae.
Согласно различным вариантам осуществления один или несколько ортологов ADAM6 грызуна или их гомологов или функциональных фрагментов грызуна в семействе восстанавливает фертильность генетически модифицированного грызуна того же семейства, который не содержит ортолог или гомолог ADAM6 (например, Cricetidae (например, хомяки, крысы и мыши Нового Света, полевки); Muridae (например, настоящие мыши и крысы, карликовые песчанки, иглистые мыши, косматые хомяки)).
Согласно различным вариантам осуществления ортологи ADAM6, их гомологи и фрагменты оценивают в отношении функциональности путем определения того, восстанавливает ли ортолог, гомолог или фрагмент фертильность генетически модифицированного самца отличного от человека животного, у которого отсутствует активность ADAM6 (например, грызуна, например, мыши или крысы, которая содержит нокаут ADAM6 или его ортолога). Согласно различным вариантам осуществления функциональность определяют как способность спермы генетически модифицированного животного, у которого отсутствует эндогенный ADAM6 или его ортолог или гомолог, проходить яйцевод и оплодотворять яйцеклетку того же вида генетически модифицированного животного.
Согласно различным аспектам могут быть получены мыши, которые содержат делеции или замещения эндогенного локуса вариабельной области тяжелой цепи или его частей, которые содержат эктопическую нуклеотидную последовательность, кодирующую белок, обеспечивающий сходные улучшения фертильности ADAM6 мыши (например, его ортолог или гомолог или фрагмент, который является функциональным у самца мыши). Эктопическая нуклеотидная последовательность может содержать нуклеотидную последовательность, кодирующую белок, который представляет собой гомолог или ортолог ADAM6 (или их фрагмент) другой линии или другого вида, например, другого вида грызунов, и которая обеспечивает улучшение фертильности, например, увеличенное количество пометов в течение определенного периода времени и/или увеличенное количество детенышей на помет и/или способность сперматозоида самца мыши проходить через яйцевод мыши для оплодотворения яйцеклетки мыши.
Согласно одному варианту осуществления ADAM6 представляет собой гомолог или ортолог, которые по меньшей мере на 89%-99% идентичен белку ADAM6 мыши (например, по меньшей мере на 89%-99% идентичен ADAM6a мыши или ADAM6b мыши). Согласно одному варианту осуществления эктопическая нуклеотидная последовательность кодирует один или несколько белков, независимо выбранных из белка, по меньшей мере на 89% идентичного ADAM6a мыши, белка, по меньшей мере на 89% идентичного ADAM6b мыши, и их комбинации. Согласно одному варианту осуществления гомолог или ортолог представляет собой белок крысы, хомяка, мыши или морской свинки, который является или модифицирован, чтобы быть приблизительно на 89% или более идентичным ADAM6a мыши и/или ADAM6b мыши. Согласно одному варианту осуществления гомолог или ортолог является или по меньшей мере на 90%, 91%, 92%, 93%, 94%, 95%, 96%, 97%, 98% или 99% идентичен ADAM6a мыши и/или ADAM6b мыши.
Согласно одному аспекту предусмотрены отличные от человека животные, причем отличные от человека животные содержат (а) вставку одного или нескольких генных сегментов Vλ и Jλ человека выше не относящейся к человеку константной области легкой цепи иммуноглобулина, (b) вставку одного или нескольких генных сегментов VH человека, одного или нескольких генных сегментов DH человека и одного или нескольких генных сегментов JH человека выше не относящейся к человеку константной области тяжелой цепи иммуноглобулина, и (с) нуклеотидную последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент. Согласно одному варианту осуществления не относящиеся к человеку константные области тяжелой и/или легкой цепи представляют собой константные области грызун (например, выбранные из константных областей мыши, крысы или хомяка). Согласно одному варианту осуществления не относящаяся к человеку константная область легкой цепи представляет собой константную область грызуна. Согласно конкретному варианту осуществления константная область легкой цепи представляет собой область Сκ мыши или область Сκ крысы. Согласно конкретному варианту осуществления константная область легкой цепи представляет собой область Сλ мыши или область Сκ крысы. Подходящие отличные от человека животные включают в себя грызунов, например, мышей, крыс и хомяков. Согласно одному варианту осуществления грызун представляет собой мышь или крысу.
Согласно одному варианту осуществления отличное от человека животное содержит по меньшей мере 12 - по меньшей мере 40 генных сегментов Vλ человека и по меньшей мере один генный сегмент Jλ человека. Согласно конкретному варианту осуществления отличное от человека животное содержит 12 генных сегментов Vλ человека и по меньшей мере один генный сегмент Jλ человека. Согласно конкретному варианту осуществления отличное от человека животное содержит 28 генных сегментов Vλ человека и по меньшей мере один генный сегмент Jλ человека. Согласно одному варианту осуществления отличное от человека животное содержит 40 генных сегментов Vλ человека и по меньшей мере один генный сегмент Jλ человека. Согласно различным вариантам осуществления по меньшей мере один генный сегмент Jλ человека выбран из Jλ1, Jλ2, Jλ3 и Jλ7. Согласно конкретному варианту осуществления отличное от человека животное содержит по меньшей мере четыре генных сегмента Jλ человека. Согласно одному варианту осуществления по меньшей мере четыре генных сегмента Jλ человека содержат по меньшей мере Jλ1, Jλ2, Jλ3 и Jλ7.
Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент, является эктопической у отличного от человека животного. Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент (который является функциональным у отличного от человека животного), присутствует в том же положении по сравнению с не относящимся к человеку локусом ADAM6 дикого типа. Согласно одному варианту осуществления отличное от человека животное представляет собой мышь, и нуклеотидная последовательность кодирует белок ADAM6 мыши или его функциональный фрагмент и присутствует в эктопическом положении в геноме отличного от человека животного. Согласно одному варианту осуществления отличное от человека животное представляет собой мышь, и нуклеотидная последовательность кодирует белок ADAM6 мыши или его функциональный фрагмент и присутствует в пределах генных сегментов иммуноглобулина. Согласно конкретному варианту осуществления генные сегменты иммуноглобулина представляют собой генные сегменты тяжелой цепи. Согласно одному варианту осуществления генные сегменты тяжелой цепи относятся к человеку. Согласно одному варианту осуществления генные сегменты тяжелой цепи представляют собой эндогенные генные сегменты тяжелой цепи отличного от человека животного. Согласно одному варианту осуществления мышь содержит эктопическую смежную последовательность, содержащую один или несколько эндогенных нереаранжированных генных сегментов тяжелой цепи, и последовательность ADAM6 находится в пределах эктопической смежной последовательности.
Согласно одному варианту осуществления отличное от человека животное не содержит эндогенный генный сегмент VL и/или JL иммуноглобулина на эндогенном локусе легкой цепи иммуноглобулина. Согласно одному варианту осуществления отличное от человека животное содержит эндогенные генные сегменты VL и/или JL иммуноглобулина, которые являются неспособными к реаранжировке для образования домена VL иммуноглобулина у отличного от человека животного. Согласно одному варианту осуществления все или по существу все эндогенные генные сегменты Vκ и Jκ иммуноглобулина замещают одним или несколькими генными сегментами Vλ и Jλ человека. Согласно одному варианту осуществления все или по существу все эндогенные генные сегменты Vλ и Jλ иммуноглобулина замещают одним или несколькими генными сегментами Vλ и Jλ человека. Согласно одному варианту осуществления все или по существу все эндогенные генные сегменты VL и JL иммуноглобулина являются интактнымим у отличного от человека животного, и отличное от человека животное содержит один или несколько генных сегментов Vλ человека и один или несколько генных сегментов Jλ человека, вставленных между эндогенными генными сегментами VL и/или JL иммуноглобулина и эндогенной константной областью легкой цепи иммуноглобулина. Согласно конкретному варианту осуществления интактные эндогенные генные сегменты VL и JL иммуноглобулина становятся неспособными к реаранжировке для образования домена VL антитела у отличного от человека животного. Согласно различным вариантам осуществления эндогенный локус легкой цепи иммуноглобулина отличного от человека животного представляет собой локус κ легкой цепи иммуноглобулина. Согласно различным вариантам осуществления эндогенный локус легкой цепи иммуноглобулина отличного от человека животного представляет собой локус λ легкой цепи иммуноглобулина. Согласно различным вариантам осуществления эндогенные генные сегменты VL и JL иммуноглобулина представляют собой генные сегменты Vκ и Jκ. Согласно различным вариантам осуществления эндогенные генные сегменты VL и JL иммуноглобулина представляют собой генные сегменты Vλ и Jλ.
Согласно одному варианту осуществления отличное от человека животное дополнительно содержит межгенную область Vκ-Jκ человека из локуса κ легкой цепи человека, причем межгенная область Vκ-Jκ человека является смежной с одним или несколькими генными сегментами Vλ и Jλ человека. Согласно конкретному варианту осуществления межгенная область Vκ-Jκ человека расположена между генным сегментом Vλ человека и генным сегментом Jλ человека.
Согласно одному аспекту предусмотрены клетки и/или ткани, происходящий из отличных от человека животных, описанных в настоящем документе, причем клетки и/или ткани содержат (а) вставку одного или нескольких генных сегментов Vλ и Jλ человека выше не относящейся к человеку константной области легкой цепи иммуноглобулина, (b) вставку одного или нескольких генных сегментов VH человека, одного или нескольких генных сегментов DH человека и одного или нескольких генных сегментов JH человека выше не относящейся к человеку константной области тяжелой цепи иммуноглобулина, и (с) нуклеотидную последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент. Согласно одному варианту осуществления не относящиеся к человеку константные области тяжелой и/или легкой цепи представляют собой константный области мыши. Согласно одному варианту осуществления не относящиеся к человеку константные области тяжелой и/или легкой цепи представляют собой константные области крысы. Согласно одному варианту осуществления не относящиеся к человеку константные области тяжелой и/или легкой цепи представляют собой константные области хомяка.
Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент, является эктопической в клетке и/или ткани. Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент, присутствует в таком же положение по сравнению с не относящимся к человеку локусом ADAM6 дикого типа. Согласно одному варианту осуществления не относящаяся к человеку клетка и/или ткань происходит от мыши, и нуклеотидная последовательность кодирует белок ADAM6 мыши или его функциональный фрагмент и присутствует в эктопическом положении. Согласно одному варианту осуществления не относящаяся к человеку клетка и/или ткань происходит от мыши, и нуклеотидная последовательность кодирует белок ADAM6 мыши или его функциональный фрагмент и присутствует в пределах генных сегментов иммуноглобулина. Согласно конкретному варианту осуществления генные сегменты иммуноглобулина представляют собой генные сегменты тяжелой цепи. Согласно одному варианту осуществления смежная последовательность эндогенных генных сегментов тяжелой цепи размещена эктопически у отличного от человека животного, причем смежная последовательность эктопически размещенных эндогенных генных сегментов тяжелой цепи содержит ген ADAM6, который является функциональным у мыши (например, у самца мыши).
Согласно одному аспекту предусмотрено применение описанного в настоящем документе отличного от человека животного для получения антигенсвязывающего белка, причем отличное от человека животное экспрессирует (а) антитело, которое содержит (i) легкую цепь иммуноглобулина, которая содержит домен Vλ человека и не относящуюся к человеку константную область легкой цепи и (ii) тяжелую цепь иммуноглобулина, которая содержит домен VH человека и не относящуюся к человеку константную область; и (b) белок ADAM6 или его функциональный фрагмент. Согласно одному варианту осуществления антигенсвязывающий белок является относящимся к человеку. Согласно одному варианту осуществления отличное от человека животное представляет собой грызуна, и не относящиеся к человеку константные области представляют собой константные области грызуна. Согласно конкретному варианту осуществления грызун представляет собой мышь.
Согласно одному аспекту предусмотрена не относящаяся к человеку клетка или ткань, происходящая от описанного в настоящем документе отличного от человека животного. Согласно одному варианту осуществления не относящаяся к человеку клетка или ткань содержит один или несколько генных сегментов Vλ иммуноглобулина человека и по меньшей мере один генный сегмент Jλ иммуноглобулина человека, смежный с не относящимся к человеку геном константной области легкой цепи иммуноглобулина, и один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека, смежных с не относящимся к человеку геном константной области тяжелой цепи иммуноглобулина, причем клетка или ткань экспрессирует белок ADAM6 или его функциональный фрагмент. Согласно одному варианту осуществления не относящийся к человеку ген константной области легкой цепи представляет собой Сκ мыши или Сλ мыши.
Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент, является эктопической. Согласно одному варианту осуществления нуклеотидная последовательность, которая кодирует ADAM6 белок или ее функциональный фрагмент, расположена в положении, которое является таким же, как и в не относящейся к человеку клетке дикого типа. Согласно различным вариантам осуществления не относящаяся к человеку клетка представляет собой В-клетку мыши. Согласно различным вариантам осуществления не относящаяся к человеку клетка представляет собой эмбриональную стволовую клетку.
Согласно одному варианту осуществления ткань происходит из селезенки, костного мозга или лимфатического узла отличного от человека животного.
Согласно одному аспекту предусмотрено применение клетки или ткани, происходящей от описанного в настоящем документе отличного от человека животного для получения гибридомы или квадромы.
Согласно одному аспекту предусмотрена не относящаяся к человеку клетка, содержащая описанный в настоящем документе модифицированный геном, причем не относящаяся к человеку клетка представляет собой ооцит, зародыш-хозяин или слияние клетки от описанного в настоящем документе отличного от человека животного и клетки от другого отличного от человека животного.
Согласно одному аспекту предусмотрено применение клетки или ткани, происходящей от описанного в настоящем документе отличного от человека животного для получения полностью человеческого антитела. Согласно одному варианту осуществления полностью человеческое антитело содержит домен VH человека и домен Vλ человека, выделенный из описанного в настоящем документе отличного от человека животного.
Согласно одному аспекту предусмотрен способ получения антитела, которое связывается с представляющим интерес антигеном, причем способ предусматривает (а) воздействие на описанное в настоящем документе отличное от человека животное представляющего интерес антигена, (b) выделение одного или нескольких В-лимфоцитов отличного от человека животного, причем один или несколько В-лимфоцитов экспрессируют антитело, которые связывает представляющий интерес антиген, и (с) идентификацию последовательности нуклеиновой кислоты, которая кодирует легкую цепь иммуноглобулина антитела, которое связывает рассматриваемый представляющий интерес антиген, причем легкая цепь иммуноглобулина содержит домен Vλ человека и не относящийся к человеку константный домен легкой цепи, и (d) использование последовательности нуклеиновой кислоты согласно (с) с последовательностью нуклеиновой кислоты константной области легкой цепи иммуноглобулина человека для получения антитела человека, которое связывает представляющий интерес антиген.
Согласно одному варианту осуществления не относящийся к человеку константная домен легкой цепи представляет собой Сκ мыши. Согласно одному варианту осуществления не относящийся к человеку константный домен легкой цепи представляет собой Сλ мыши. Согласно одному варианту осуществления отличное от человека животное представляет собой мышь.
Согласно одному аспекту предусмотрен фертильный самец мыши, содержащий модификацию на локусе тяжелой цепи иммуноглобулина, причем фертильный самец мыши содержит эктопическую последовательность ADAM6, которая является функциональной у самца мыши.
Эктопический ADAM6 у мышей с гуманизированной тяжелой цепью
Разработки в области нацеленного воздействия на гены, например, разработка бактериальных искусственных хромосом (ВАС), в настоящее время обеспечивают возможность рекомбинации относительно больших геномных фрагментов. Конструирование ВАС предоставила возможность получения больших делеций и больших вставок в ES клетки мыши.
Мыши, которые производят человеческие антитела, были доступны уже в течение определенного времени. Хотя они представляют собой важный прогресс в разработке человеческих терапевтических антител, эти мыши проявляют ряд значительных нарушений, которые ограничивают их применимость. Например, они проявляют нарушенное развитие В-клеток. Нарушенное развитие может быть обусловлено разнообразными различиями между трансгенными мышами и мышами дикого типа.
Существует вероятность, что человеческие антитела не взаимодействуют оптимально с рецепторами пре-В-клеток или В-клеток мыши на поверхности клеток мыши, которые передают сигнал к созреванию, пролиферации или выживанию в ходе клональной селекции. Полностью человеческие антитела могут не взаимодействовать оптимально с Fc рецепторной системой мыши; мыши экспрессируют Fc рецепторы, которые не проявляют соответствия один к одному с Fc рецепторами человека. В конце концов, различные мыши, которые производят полностью человеческие антитела, не включают в себя все истинные мышиные последовательности, например, нижележащие энхансерные элементы и другие контролирующие элементы локуса, которые могут быть необходимы для развития В-клеток дикого типа.
Мыши, которые производят полностью человеческие антитела, как правило, содержат эндогенные локусы иммуноглобулина, которые являются некоторым образом недееспособными, и человеческие трансгены, которые содержат вариабельные и константные генные сегменты иммуноглобулина, вводят в случайное положение в геноме мыши. При условии, что эндогенный локус является достаточно недееспособным, так чтобы не реаранжировать генные сегменты для образования функционального гена иммуноглобулина, цель получения полностью человеческих антител в такой мыши может быть достигнута, хотя и с нарушенным развитием В-клеток.
Несмотря на принуждение производить полностью человеческие антитела из человеческого трансгенного локуса, образование человеческих антител у мыши является очевидно затрудненным процессом. У некоторых мышей процесс является настолько затрудненным, что приводит к формированию химерных человеческих вариабельных/мышиных константных тяжелых цепей (но не легких цепей) посредством механизма транс-переключения. С помощью этого механизм, транскрипты, которые кодируют полностью человеческие антитела, подвергаются переключению изотипа в транс-конфигурации из изотипа человека на изотип мыши. Процесс происходит в транс-конфигурации, поскольку полностью человеческий трансген расположен в отдалении от эндогенного локуса, который сохраняет неповрежденную копию генной константной области тяжелой цепи мыши. Хотя у таких мышей транс-переключение очевидно выражено, явление остается недостаточным для восстановления развития В-клеток, которое остается фактически нарушенным. В любом случае, транс-переключенные антитела, произведенные у таких мышей, сохраняют полностью человеческие легкие цепи, поскольку явление транс-переключения, очевидно, не происходит в отношении легких цепей; транс-переключение, вероятно, основано на переключении последовательностей в используемых эндогенных локусах (хотя и по-другому) в переключении нормального изотипа в цис-конфигурации. Таким образом, даже когда мыши, сконструированные для получения полностью человеческих антител, выбирают механизм транс-переключения для образования антител с константными областями мыши, стратегия остается все еще недостаточной для восстановления нормального развития В-клеток.
Первоочередной задачей в получении основанных на антителах терапевтических средств для людей состоит в получении достаточно большого разнообразия последовательностей вариабельной области иммуноглобулина человека для выявления применимых вариабельных доменов, которые специфически распознают конкретные эпитопы и связывают их с необходимой аффинностью, как правило, но не всегда, с высокой аффинностью. Перед разработкой мышей VELOCIMMUNE® (описанных в настоящем документе), не существовало ни одного указания на то, что мыши, экспрессирующие вариабельные области человека с константными областями мыши, будут проявлять какие-либо значительные отличия от мышей, которые образуют человеческие антитела из трансгена. Это предположение, тем не менее, было неправильным.
Гуманизированные мыши VELOCIMMUNE®, которые содержат точное замещение вариабельных областей иммуноглобулина мыши вариабельными областями иммуноглобулина человека на эндогенных локусах мыши, проявляют удивительное и существенное сходство с мышами дикого типа по отношению к развитию В-клеток. В удивительном и замечательном развитии мыши VELOCIMMUNE® проявили по существу нормальный ответ дикого типа на иммунизацию, который отличался только в одном существенном аспекте от мышей дикого типа мыши - вариабельные области, образованные в ответ на иммунизацию, являются полностью человеческими.
Мыши VELOCIMMUNE® содержат точное, крупномасштабное замещение зародышевых вариабельных областей тяжелой цепи иммуноглобулина мыши (IgH) и легкой цепи иммуноглобулина (например, к легкой цепи, Igκ) соответствующими вариабельными областями иммуноглобулина человека на эндогенных локусах. В общем, приблизительно шесть миллионов пар нуклеотидов мышиных локусов замещают приблизительно 1,5 миллиона пар нуклеотидов геномной последовательности человека. Это точное замещение дает в результате мышь с гибридными локусами иммуноглобулина, которая образует тяжелые и легкие цепи, которые содержатся вариабельные области человека и константную область мыши. Точное замещение сегментов VH-DH-JH и Vκ-Jκ мыши оставляет фланкирующие мышиные последовательности интактнымии функциональными на гибридных локусах иммуноглобулина. Гуморальная иммунная система мыши функционирует как система у мыши дикого типа. Развитие В-клеток не затруднено каким-либо существенным образом, и у мыши при антигенной сенсибилизации образуется богатое разнообразие вариабельных областей человека.
Мыши VELOCIMMUNE® являются возможными, поскольку иммуноглобулиновые генные сегменты тяжелых и к легких цепей реаранжируются подобным образом у людей и мышей, что не означает, что их локусы являются одинаковыми или даже приблизительно таковы - ясно, что они не такие. Тем не менее, локусы являются достаточно сходными, чтобы гуманизация вариабельного генного локуса тяжелой цепи могла осуществиться путем замещения приблизительно трех миллионов пар нуклеотидов смежной мышиной последовательности, которая содержит все генные сегменты VH, DH и JH, приблизительно одним миллионом оснований смежной геномной последовательности человека, охватывающей, в сущности, эквивалентную последовательность из локуса иммуноглобулина человека.
Согласно некоторым вариантам осуществления дополнительное замещение определенных генных последовательностей константной области мыши генными последовательностями человека (например, замещение последовательности CH1 мыши последовательностью CH1 человека и замещение последовательность CL мыши последовательностью CL человека) дает в результате мышей с гибридными локусами иммуноглобулина, которые образуют антитела, содержащие вариабельные области человека и частично константные области человека, подходящие, например, для образования полностью человеческих фрагментов антител, например, полностью человеческих Fab. Мыши с гибридными локусами иммуноглобулина проявляют нормальную реаранжировку вариабельных генных сегментов, нормальную соматическую гипермутацию и нормальное переключение класса. Эти мыши проявляют гуморальную иммунную систему, которая неотличима от мышей дикого типа, и демонстрируют нормальные клеточные популяции на всех стадиях развития В-клеток и нормальные структуры лимфомных органов - даже когда если у мышей отсутствует полный репертуар вариабельных генных сегментов человека. Иммунизация указанных мышей приводит к устойчивым гуморальным ответам, которые проявляют широкое разнообразие использования вариабельных генных сегментов.
Точное замещение зародышевых генных сегментов вариабельной области мыши обеспечивают получение мышей, которые содержат частично человеческие локусы иммуноглобулина. Поскольку частично человеческие локусы иммуноглобулина нормально реаранжируются, гипермутируют и подвергаются переключению класса, частично человеческие локусы иммуноглобулина образуют у мыши антитела, которые содержат вариабельные области человека. Нуклеотидные последовательности, которые кодируют вариабельные области, могут быть установлены и клонированы, затем слиты (например, в системе in vitro) с любыми предпочтительными последовательностями, например, любым изотипом иммуноглобулина, подходящим для конкретного применения, давая в результате антитело или антигенсвязывающий белок, происходящий полностью из последовательностей человека.
Крупномасштабную гуманизацию с помощью способов рекомбинационный инженерии использовали для модификации мышиных эмбриональных стволовых (ES) клеток для точного замещения до трех миллионов пар нуклеотидов локуса тяжелой цепи иммуноглобулина мыши, который содержал по существу все генные сегменты VH, DH и JH мыши, эквивалентными генными сегментами человека, составляющими до одного миллиона пар нуклеотидов геномной последовательности человека, содержащей несколько или по существу все генные сегменты VH, DH и JH человека. Составляющий до 0,5 миллиона пар нуклеотидов сегмент генома человека, содержащий один из двух повторов, кодирующих по существу все генные сегменты Vκ и Jκ человека использовали для замещения сегмента локуса κ легкой цепи иммуноглобулина мыши размером 3 миллиона пар нуклеотидов, содержащего по существу все генные сегменты Vκ и Jκ мыши.
Мыши с такими замещенными иммуноглобулиновыми локусами могут содержать разрыв или делецию эндогенного локуса ADAM6 мыши, который в норме встречается между расположенным наиболее 3' генным сегментом VH и наиболее 5' генным сегментом DH на локусе тяжелой цепи иммуноглобулина мыши. Разрыв в этой области может привести к снижению или подавлению функциональности эндогенного локуса ADAM6 мыши. Если наиболее 3' генные сегменты VH репертуара тяжелой цепи человека используют в замещении, межгенная область, содержащая псевдоген, который, по-видимому, является псевдоген ADAM6 человека, присутствует между этими генными сегментами VH, т.е. между VH1-2 и VH1-6 человека. Тем не менее самцы мышей, которые содержат эту межгенную последовательность человека, проявляют снижение фертильности.
Описываются мыши, которые содержат описанные выше замещенные локусы, и которые также содержат эктопическую последовательность нуклеиновой кислоты, кодирующую мышиный ADAM6, причем мыши проявляют по существу нормальную фертильность. Согласно одному варианту осуществления эктопическая последовательность нуклеиновой кислоты содержит последовательность ADAM6a мыши и/или ADAM6b мыши или ее функциональные фрагменты, расположенные между генным сегментом VH1-2 человека и генным сегментом VH6-1 человека на модифицированном эндогенном локусе тяжелой цепи. Согласно одному варианту осуществления эктопическая последовательность нуклеиновой кислоты представляет собой SEQ ID NO: 3, расположенную между VH1-2 и VH1-6 человека на модифицированном эндогенном локусе тяжелой цепи. Направление транскрипции генов ADAM6 SEQ ID NO: 3 является противоположным по отношению к направлению транскрипции окружающих генных сегментов VH человека. Хотя примеры в настоящем документе демонстрируют восстановление фертильности путем размещения эктопической последовательности между указанными генными сегментами VH человека, специалистам в настоящей области будет понятно, что размещение эктопической последовательности на любом подходящем транскрипционно пермиссивном локусе в мышином геноме (или даже внехромосомно), как предполагается, приведет к подобному восстановлению фертильности у самца мыши.
Явление дополнения у мыши, у которой отсутствует функциональный локус ADAM6, с помощью эктопической последовательности, которая содержит ген ADAM6 мыши или его ортолог или гомолог или функциональный фрагмент, представляет собой общий способ, который является применимым для восстановления любых мышей с нефункциональными или минимально функциональными эндогенными локусами ADAM6. Таким образом, фертильность большого количества мышей, которые содержат разрушающую ADAM6 модификацию локуса тяжелой цепи иммуноглобулина, может быть восстановлена с помощью композиций и способов по настоящему изобретению. Соответственно, настоящее изобретение предусматривает мышей с широким разнообразием модификаций локусов тяжелой цепи иммуноглобулина, которые нарушают функцию эндогенного ADAM6. Некоторые (не ограничивающие) примеры представлены в настоящем описании. В дополнение к описанным мышам VELOCIMMUNE® относящиеся к ADAM6 композиции и способы могут использоваться в многочисленных применениях, например, при модификации локуса тяжелой цепи разнообразными путями.
Согласно одному аспекту предусматривается мышь, которая содержит эктопическую последовательность ADAM6, которая кодирует функциональный белок ADAM6 (или его ортолог или гомолог или функциональный фрагмент), замещение всех или по существу всех VH генных сегментов мыши одним или несколькими VH генными сегментами человека, замещение всех или по существу всех генных сегментов DH и генных сегментов JH мыши генными сегментами DH человека и генными сегментами JH человека; причем у мыши отсутствует CH1 и/или шарнирная область. Согласно одному варианту осуществления мышь производит связывающий один вариабельный домен белок, который представляет собой димер иммуноглобулиновых цепей, выбранный из следующего: (a) VH человека -CH1 мыши -CH2 мыши -CH3 мыши; (b) VH человека -шарнир мыши -CH2 мыши -CH3 мыши; и, (с) VH человека -CH2 мыши -CH3 мыши.
Согласно одному аспекту нуклеотидная последовательность, которая восстанавливает фертильность, расположена в пределах последовательности вариабельной области тяжелой цепи иммуноглобулина человека (например, между генными сегментами VH1-2 и VH1-6 человека) у мыши, которая содержит замещение одного или нескольких вариабельных генных сегментов тяжелой цепи иммуноглобулина мыши (mVH, mDH и/или mJH) одним или несколькими вариабельными генными сегментами тяжелой цепи иммуноглобулина человека (hVH, hDH и/или hJH), и мышь дополнительно содержит замещение одного или нескольких вариабельных генных сегментов κ легкой цепи иммуноглобулина мыши (mVκ, mJκ) одним или несколькими вариабельными генными сегментами κ легкой цепи иммуноглобулина человека (hVκ и/или hJκ). Согласно одному варианту осуществления нуклеотидная последовательность расположена между генным сегментом VH1-2 человека и генным сегментом VH1-6 человека у мыши VELOCIMMUNE® (патенты США №6596541 и 7105348, включенные в настоящий документ посредством ссылки). Согласно одному варианту осуществления модифицированная таким образом мышь VELOCIMMUNE® содержит замещение всеми или по существу всеми вариабельными генными сегментами тяжелой цепи иммуноглобулина человека (всеми hVH, hDH и hJH) и всеми или по существу всеми вариабельными генными сегментами κ легкой цепи иммуноглобулина человека (hVκ и hJκ).
Согласно одному варианту осуществления один или несколько вариабельных генных сегментов тяжелой цепи иммуноглобулина мыши содержат приблизительно три миллиона пар нуклеотидов локуса тяжелой цепи иммуноглобулина мыши. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов тяжелой цепи иммуноглобулина мыши содержат по меньшей мере 89 генных сегментов VH, по меньшей мере 13 генных сегментов DH, по меньшей мере четыре генных сегмента JH или их комбинацию локуса тяжелой цепи иммуноглобулина мыши. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов тяжелой цепи иммуноглобулина человека содержат приблизительно один миллион пар нуклеотидов локуса тяжелой цепи иммуноглобулина человека. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов тяжелой цепи иммуноглобулина человека содержат по меньшей мере 80 генных сегментов VH, по меньшей мере 27 генных сегментов DH, по меньшей мере шесть генных сегментов JH или их комбинацию локуса тяжелой цепи иммуноглобулина человека.
Согласно одному варианту осуществления один или несколько вариабельных генных сегментов κ легкой цепи иммуноглобулина мыши содержат приблизительно три миллиона пар нуклеотидов локуса κ легкой цепи иммуноглобулина мыши. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов κ легкой цепи иммуноглобулина мыши содержат по меньшей мере 137 генных сегментов Vκ, по меньшей мере пять генных сегментов Jκ или их комбинацию локуса κ легкой цепи иммуноглобулина мыши. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов κ легкой цепи иммуноглобулина человека содержат приблизительно 0,5 миллиона пар нуклеотидов локуса κ легкой цепи иммуноглобулина человека. Согласно конкретному варианту осуществления один или несколько вариабельных генных сегментов κ легкой цепи иммуноглобулина человека содержат проксимальный повтор (по отношению к константной области κ иммуноглобулина) локуса κ легкой цепи иммуноглобулина человека. Согласно одному варианту осуществления один или несколько вариабельных генных сегментов κ легкой цепи иммуноглобулина человека содержат по меньшей мере 40 генных сегментов Vκ, по меньшей мере пять генных сегментов Jκ или их комбинацию локуса κ легкой цепи иммуноглобулина человека.
Согласно одному варианту осуществления нуклеотидная последовательность расположена между двумя генными сегментами иммуноглобулина человека. Согласно конкретному варианту осуществления два генных сегмента иммуноглобулина человека представляют собой генные сегменты тяжелой цепи.
Согласно одному аспекту функциональный локус ADAM6 мыши (или его ортолог или гомолог или функциональный фрагмент) присутствует в окружении генных сегментов мыши, которые присутствуют на эндогенном локусе вариабельной области тяжелой цепи мыши, причем указанный локус является неспособным к реаранжировке, чтобы кодировать функциональную тяжелую цепь, содержащую эндогенную константную область тяжелой цепи. Согласно одному варианту осуществления эндогенный локус тяжелой цепи мыши содержит по меньшей мере один и до 89 генных сегментов VH, по меньшей мере один и до 13 генных сегментов DH, по меньшей мере один и до четырех генных сегментов JH и их комбинацию. Согласно различным вариантам осуществления функциональный локус ADAM6 мыши (или его ортолог или гомолог или функциональный фрагмент) кодирует один или несколько белков ADAM6, которые являются функциональными у мыши, причем один или несколько белков ADAM6 содержат SEQ ID NO: 1, SEQ ID NO: 2 и/или их комбинацию.
Согласно одному аспекту функциональный локус ADAM6 мыши (или его ортолог или гомолог или функциональный фрагмент) присутствует в окружении генных сегментов VH человека, которые замещают эндогенные генные сегменты VH мыши. Согласно одному варианту осуществления по меньшей мере 89 генных сегментов VH мыши удаляют и замещают одним или несколькими генными сегментами VH человека, и локус ADAM6 мыши присутствует непосредственно рядом с 3' концом генных сегментов VH человека, или между двумя генными сегментами VH человека. Согласно конкретному варианту осуществления локус ADAM6 мыши присутствует между двумя генными сегментами VH в пределах приблизительно 20 тысяч пар нуклеотидов (т.п.н., или kb) - приблизительно 40 тысяч пар нуклеотидов (т.п.н.) от 3'-конца вставленных генных сегментов VH человека. Согласно конкретному варианту осуществления локус ADAM6 мыши присутствует между двумя генными сегментами VH в пределах приблизительно 29 т.п.н. - приблизительно 31 т.п.н. от 3' конца вставленных генных сегментов VH человека. Согласно конкретному варианту осуществления локус ADAM6 мыши присутствует в пределах приблизительно 30 т.п.н. от 3'-конца вставленных человека VH генные сегменты. Согласно конкретному варианту осуществления локус ADAM6 мыши присутствует в пределах приблизительно 30184 п.н. от 3' конца вставленных генных сегментов VH человека. Согласно конкретному варианту осуществления замещение включает в себя генные сегменты VH человека VH1-2 и VH6-1, и локус ADAM6 мыши присутствует ниже генного сегмента VH1-2 и выше генного сегмента VH6-1. Согласно конкретному варианту осуществления локус ADAM6 мыши присутствует между генным сегментом VH1-2 человека и генным сегментом VH6-1 человека, причем 5' - конец локуса ADAM6 мыши расположен приблизительно на 13848 п.н. от 3' конца генного сегмента VH1-2 человека, и 3' - конец локуса ADAM6 расположен приблизительно на 29737 п.н. 5' от генного сегмента VH6-1 человека. Согласно конкретному варианту осуществления локус ADAM6 мыши содержит SEQ ID NO: 3 или его фрагмент, который обеспечивает функцию ADAM6 в клетках мыши. Согласно конкретному варианту осуществления расположение генных сегментов VH человека после этого является следующим (сверху вниз относительно направления транскрипции генных сегментов VH человека): VH1-2 человека - локус ADAM6 мыши - VH6-1 человека. Согласно конкретному варианту осуществления псевдоген ADAM6 между VH1-2 человека и VH6-1 человека замещен локусом ADAM6 мыши. Согласно одному варианту осуществления ориентация одного или нескольких из мышиного ADAM6a и мышиного ADAM6b локуса ADAM6 мыши является противоположной относительно направления транскрипции по сравнению с ориентацией генных сегментов VH человека. Альтернативно, локус ADAM6 мыши расположен в межгенной области между наиболее 3' генным сегментом VH человека и наиболее 5' генным сегментом DH. Это может иметь место независимо от того, является ли наиболее 5' сегмент DH мышиным или человеческим.
Аналогично, мышь, модифицированная с помощью одного или нескольких генных сегментов VL человека (например, сегментов Vκ или Vλ), замещающих все или по существу все эндогенные VH генные сегменты мыши, может быть модифицирована так, чтобы или сохранять эндогенный локус ADAM6 мыши, как описано выше, например, путем использования нацеливающего вектора, характеризующегося расположенным ниже гомологичным плечом, которое содержит локус ADAM6 мыши или его функциональный фрагмент, или замещать поврежденный локус ADAM6 мыши эктопической последовательностью, расположенной между двумя генными сегментами VL человека или между генными сегментами VL человека и генным сегментом DH (либо человека, либо мыши, например, Vλ+m/hDH), или генным сегментом J (либо человека, либо мыши, например, Vκ+JH). Согласно одному варианту осуществления замещение предусматривает два или более генных сегментов VL человека, и локус ADAM6 мыши или его функциональный фрагмент расположен между двумя наиболее 3' генными сегментами VL. Согласно конкретному варианту осуществления расположение генных сегментов VL человека после этого является следующим (сверху вниз относительно направления транскрипции генных сегментов человека): VL3'-1 человека - локус ADAM6 мыши -VL3' человека. Согласно одному варианту осуществления ориентация одного или нескольких из мышиного ADAM6a и мышиного ADAM6b локуса ADAM6 мыши является противоположной относительно направления транскрипции по сравнению с ориентацией VL генных сегментов человека. Альтернативно, локус ADAM6 мыши расположен в межгенной области между наиболее 3' генным сегментом VL человека и наиболее 5' генным сегментом DH. Это может иметь место независимо от того, является ли наиболее 5' сегмент DH мышиным или человеческим.
Согласно одному аспекту предусматривается мышь с замещением одного или нескольких эндогенных генных сегментов VH мыши, и которая содержит по меньшей мере один эндогенный генный сегмент DH мыши. У такой мыши модификация эндогенных генных сегментов VH мыши может содержать модификацию одного или нескольких из наиболее 3' генных сегментов VH, но не наиболее 5' генный сегмент DH, причем нужно быть внимательным, чтобы модификация одного или нескольких наиболее 3' VH генных сегментов не разрушила эндогенный локус ADAM6 мыши или не сделала его нефункциональным. Например, согласно одному варианту осуществления мышь содержит замещение всех или по существу всех эндогенных VH генных сегментов мыши одним или несколькими генными сегментами VH человека, и мышь содержит один или несколько эндогенных генных сегментов DH и функциональный эндогенный локус ADAM6 мыши.
Согласно другому варианту осуществления мышь содержит модификацию эндогенных наиболее 3' генных сегментов VH мыши, и модификацию одного или нескольких эндогенных генных сегментов DH мыши, и модификацию проводят так, чтобы сохранить целостность эндогенного локуса ADAM6 мыши до такой степени, чтобы эндогенный ADAM6 локус оставался функциональным. Согласно одному примеру такую модификацию выполняют в две стадии: (1) замещение наиболее 3' эндогенных генных сегментов VH мыши одним или несколькими генными сегментами VH человека с использованием нацеливающего вектора с вышележащим гомологичным плечом и нижележащим гомологичным плечом, причем нижележащее гомологичное плечо содержит весь или часть функционального локуса ADAM6 мыши; (2) затем замещение и эндогенного генного сегмента DH мыши с помощью нацеливающего вектора, содержащего вышележащее гомологичное плечо, которое содержит весь или функциональную часть локуса ADAM6 мыши.
Согласно различным аспектам использование мышей, которые содержат эктопическую последовательность, которая кодирует белок ADAM6 мыши или его ортолог или гомолог или функциональные гомолог, является применимым, если модификации нарушают функцию эндогенного ADAM6 мыши. Вероятность разрушения функции эндогенного ADAM6 мыши является высокой при осуществлении модификаций в отношении локусов иммуноглобулина мыши, в частности, при модификации вариабельных областей тяжелой цепи иммуноглобулина мыши и окружающих последовательностей. Следовательно, такие мыши представляют конкретное преимущество при получении мышей с локусами тяжелой цепи иммуноглобулина, которые подвергнуты делеции полностью или частично, которые являются гуманизированными полностью или частично или замещенными (например, Vκ или Vλ последовательностями) полностью или частично. Способы получения генетических модификаций, описанных для мышей, описанных ниже, известны специалистам в настоящей области техники.
Мыши, содержащие эктопическую последовательность, кодирующую белок ADAM6 мыши или по существу идентичный или сходный белок, который обеспечивает улучшения фертильности белка ADAM6 мыши, являются особенно применимыми в связи с модификациями относительно вариабельной генного локуса тяжелой цепи иммуноглобулина мыши, которые разрушают или подвергают делеции эндогенную последовательность ADAM6 мыши. Несмотря на то, что изначально описаны в связи с мышами, которые экспрессируют антитела с вариабельными областями человека и константными областями мыши, такие мыши применимы в отношении любых генетических модификаций, которые нарушают эндогенные гены ADAM6 мыши. Специалистам в настоящей области понятно, что это охватывает широкое разнообразие генетически модифицированных мышей, которые содержат модификации вариабельных генных локусов тяжелой цепи иммуноглобулина мыши. Они предусматривают, например, мышей с делецией или замещением всех или части генных сегментов тяжелой цепи иммуноглобулина мыши, независимо от других модификаций. Не ограничивающие примеры описаны ниже.
Согласно некоторым аспектам предусматриваются генетически модифицированные мыши, которые содержат эктопический ген ADAM6 мыши, грызуна или другого животного (или ортолог или гомолог или фрагмент), функциональный у мыши, и один или несколько генных сегментов вариабельной и/или константной области иммуноглобулина человека. Согласно различным вариантам осуществления другие ортологи или гомологи или фрагменты гена ADAM6, функциональные у мыши, могут включать в себя последовательности от коров, собак, примата, кролика или другие не относящиеся к человеку последовательности.
Согласно одному аспекту предусматривается мышь, которая содержит эктопическую последовательность ADAM6, которая кодирует функциональный белок ADAM6, замещение всех или по существу всех генных сегментов VH мыши одним или несколькими VH генными сегментами человека; замещение всех или по существу всех генных сегментов DH мыши одним или несколькими генными сегментами DH человека; и замещение всех или по существу всех генных сегментов JH мыши одним или несколькими генными сегментами JH человека.
Согласно одному варианту осуществления мышь дополнительно содержит замещение нуклеотидной последовательности CH1 мыши нуклеотидной последовательностью CH1 человека. Согласно одному варианту осуществления мышь дополнительно содержит замещение шарнирной нуклеотидной последовательности мыши шарнирной нуклеотидной последовательностью человека. Согласно одному варианту осуществления мышь дополнительно содержит замещение вариабельного локуса легкой цепи иммуноглобулина (VL и JL) вариабельным локусом легкой цепи иммуноглобулина человека. Согласно одному варианту осуществления мышь дополнительно содержит замещение нуклеотидной последовательности константной области легкой цепи иммуноглобулина мыши нуклеотидной последовательностью константной области легкой цепи иммуноглобулина человека. Согласно конкретному варианту осуществления VL, JL и CL представляют собой последовательности κ легкой цепи иммуноглобулина. Согласно конкретному варианту осуществления мышь содержит последовательность константной области иммуноглобулина CH2 мыши и CH3 мыши, слитую с шарнирной последовательностью человека и последовательностью CH1 человека, так что локусы иммуноглобулина мыши реаранжируются для образования гена, который кодирует связывающий белок, содержащий (а) тяжелую цепь, которая содержит вариабельную область человека, область CH1 человека, шарнирную область человека и область CH2 мыши и область CH3 мыши; и (b) ген, который кодирует легкую цепь иммуноглобулина, которая содержит вариабельный домен человека и константную область человека.
Согласно одному аспекту предусматривается мышь, которая содержит эктопическую последовательность ADAM6, которая кодирует функциональный белок ADAM6, замещение всех или по существу всех генных сегментов VH мыши одним или несколькими генными сегментами VL человека, и необязательно замещение всех или по существу всех генных сегментов DH и/или генных сегментов JH одним или несколькими генными сегментами DH человека и/или генными сегментами JH человека, или необязательно замещение всех или по существу всех генных сегментов DH и генных сегментов JH одним или несколькими генными сегментами JL человека.
Согласно одному варианту осуществления мышь содержит замещение всех или по существу всех генных сегментов VH, DH и JH мыши одним или несколькими VL, одним или несколькими DH и одним или несколькими генными сегментами J (например, Jκ или Jλ), причем генные сегменты функционально связаны с эндогенной шарнирной областью мыши, причем мышь образует реаранжированный ген цепи иммуноглобулина, который содержит, от 5' к 3' в направлении транскрипции, VL человека -DH человека или мыши -J человека или мыши -шарнир мыши -CH2 мыши -CH3 мыши. Согласно одному варианту осуществления J область представляет собой Jκ область человека. Согласно одному варианту осуществления J область представляет собой JH область человека. Согласно одному варианту осуществления J область представляет собой Jλ область человека. Согласно одному варианту осуществления VL область человека выбрана из Vλ области человека и Vκ области человека.
Согласно конкретным вариантам осуществления мышь экспрессирует антитело с одним вариабельным доменом, содержащее константную область мыши или человека и вариабельную область, происходящую из Vκ человека, DH человека и Jκ человека; Vκ человека, DH человека и JH человека; Vλ человека, DH человека и Jλ человека; Vλ человека, DH человека и JH человека; Vκ человека, DH человека и Jλ человека; Vλ человека, DH человека и Jκ человека. Согласно конкретному варианту осуществления, последовательности распознавания рекомбинации модифицируют так, чтобы обеспечить осуществление продуктивных реаранжировок между указанными генными сегментами V, D и J или между указанными генными сегментами V и J.
Согласно одному аспекту предусматривается мышь, которая содержит эктопическую последовательность ADAM6, которая кодирует функциональный белок ADAM6 (или его ортолог или гомолог или функциональный фрагмент), замещение всех или по существу всех генных сегментов VH мыши одним или несколькими VL генными сегментами человека, замещение всех или по существу всех генных сегментов DH и генных сегментов JH мыши генными сегментами JL человека; причем у мыши отсутствует CH1 и/или шарнирная область.
Согласно одному варианту осуществления у мыши отсутствует последовательность, кодирующая домен CH1. Согласно одному варианту осуществления у мыши отсутствует последовательность, кодирующая шарнирную область. Согласно одному варианту осуществления у мыши отсутствует последовательность, кодирующая домен CH1 и шарнирную область.
Согласно конкретному варианту осуществления мышь экспрессирует связывающий белок, который содержит вариабельный домен легкой цепи (λ или κ) иммуноглобулина человека, слитый с доменом CH2 мыши, который прикреплен к домену CH3 мыши.
Согласно одному аспекту предусматривается мышь, которая содержит эктопическую последовательность ADAM6, которая кодирует функциональный белок ADAM6 (или его ортолог или гомолог или функциональный фрагмент), замещение всех или по существу всех генных сегментов VH мыши одним или несколькими генными сегментами VL человека, замещение всех или по существу всех генных сегментов DH и JH мыши генными сегментами JL человека.
Согласно одному варианту осуществления мышь содержит делецию генной последовательности константной области тяжелой цепи иммуноглобулина, кодирующей область CH1, шарнирную область, CH1 и шарнирную область или область CH1 и шарнирную область и область CH2.
Согласно одному варианту осуществления мышь образует связывающий один вариабельный домен белок, содержащий гомодимер, выбранный из следующего: (a) VL человека - CH1 мыши - CH2 мыши - CH3 мыши; (b) VL человека - шарнир мыши - CH2 мыши - CH3 мыши; (с) VL человека - CH2 мыши - CH3 мыши.
Согласно одному аспекту предусматривается мышь с недееспособным эндогенным локусом тяжелой цепи иммуноглобулина, содержащая недееспособный или удаленный эндогенный локус ADAM6 мыши, причем мышь содержит последовательность нуклеиновой кислоты, которая экспрессирует химерное антитело человека или мыши или человеческое/мышиное или другое химерное антитело. Согласно одному варианту осуществления последовательность нуклеиновой кислоты присутствует на интегрированном трансгене, который интегрирован случайным образом в геном мыши.
Согласно одному варианту осуществления мышь дополнительно содержит недееспособный эндогенный локус легкой цепи иммуноглобулина. Согласно конкретному варианту осуществления эндогенный локус легкой цепи иммуноглобулина выбран из локуса каппа (κ) и лямбда (λ) легкой цепи. Согласно конкретному варианту осуществления мышь содержит недееспособный эндогенный локус κ легкой цепи и недееспособный локус λ легкой цепи, причем мышь экспрессирует антитело, которое содержит вариабельный домен тяжелой цепи иммуноглобулина человека и домен легкой цепи иммуноглобулина человека. Согласно одному варианту осуществления домен легкой цепи иммуноглобулина человека выбран из домена κ легкой цепи человека и домена λ легкой цепи человека. Согласно конкретному варианту осуществления мышь содержит недееспособный эндогенный локус κ легкой цепи, причем мышь экспрессирует антитело, которое содержит относящуюся к человеку/мыши (т.е. относящуюся к человеку вариабельную/относящуюся к мыши константную) тяжелую цепь иммуноглобулина и относящуюся к человеку/мыши легкую цепь иммуноглобулина, содержащую домен Vλ человека. Согласно одному варианту осуществления относящаяся к человеку/мыши легкая цепь иммуноглобулина содержит Сκ мыши. Согласно одному варианту осуществления относящаяся к человеку/мыши легкая цепь иммуноглобулина содержит Сλ мыши. Согласно конкретному варианту осуществления Сλ мыши представляет собой Сλ2.
Согласно одному аспекту предусмотрено генетически модифицированное животное, которое экспрессирует химерное антитело и экспрессирует белок ADAM6 или его ортолог или гомолог, который является функциональным у генетически модифицированного животного.
Согласно одному варианту осуществления генетически модифицированное животное выбрано из мыши и крысы. Согласно одному варианту осуществления генетически модифицированное животное представляет собой мышь, и белок ADAM6 или его ортолог или гомолог происходит от линии мыши, которая представляет собой линию, отличную от генетически модифицированного животного. Согласно одному варианту осуществления генетически модифицированное животное представляет собой грызуна семейства Cricetidae (например, хомяк, крыса или мышь Нового Света, полевка), и ортолог или гомолог белка ADAM6 происходит от грызуна семейства Muridae (например, настоящая мышь или крыса, карликовая песчанка, иглистая мышь, косматый хомяк). Согласно одному варианту осуществления генетически модифицированное животное представляет собой грызуна семейства Muridae, и ортолог или гомолог белка ADAM6 происходит от грызуна семейства Cricetidae.
Согласно одному варианту осуществления химерное антитело содержит вариабельный домен человека и последовательность константной области грызуна. Согласно одному варианту осуществления грызун выбран из грызуна семейства Cricetidae и грызуна семейства Muridae, согласно конкретному варианту осуществления грызун семейства Cricetidae и семейство Muridae представляет собой мышь. Согласно конкретному варианту осуществления грызун семейства Cricetidae и семейства Muridae представляет собой крысу. Согласно одному варианту осуществления химерный антитело содержит вариабельный домен человека и константный домен от животного, выбранного из мыши или крысы; согласно конкретному варианту осуществления мышь или крыса выбрана из семейства Cricetidae и семейства Muridae. Согласно одному варианту осуществления химерное антитело содержит вариабельный домен тяжелой цепи человека, вариабельный домен легкой цепи человека и последовательность константной области, происходящую от грызуна, выбранного из мыши и крысы, причем вариабельный домен тяжелой цепи человека и легкая цепь человека являются когнатными. Согласно конкретному варианту осуществления когнатный предусматривает, что вариабельные домены тяжелой цепи человека и легкой цепи человека происходят из одной В-клетки, которая экспрессирует вариабельный домен легкой цепи человека и вариабельный домен тяжелой цепи человека вместе, и вариабельные домены представляются вместе на поверхности отдельной В-клетки.
Согласно одному варианту осуществления химерное антитело экспрессируется из локуса иммуноглобулина. Согласно одному варианту осуществления вариабельный домен тяжелой цепи химерного антитела экспрессируется из реаранжированного эндогенного локуса тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления вариабельный домен легкой цепи химерного антитела экспрессируется из реаранжированного эндогенного локуса легкой цепи иммуноглобулина. Согласно одному варианту осуществления вариабельный домен тяжелой цепи химерного антитела и/или вариабельный домен легкой цепи химерного антитела экспрессируется из реаранжированного трансгена (например, реаранжированной последовательности нуклеиновой кислоты, происходящей из нереаранжированной последовательности нуклеиновой кислоты, интегрированной в геном животного в локус, отличный от эндогенного локуса иммуноглобулина). Согласно одному варианту осуществления вариабельный домен легкой цепи химерного антитела экспрессируется из реаранжированного трансгена (например, реаранжированной последовательности нуклеиновой кислоты, происходящей из нереаранжированной последовательности нуклеиновой кислоты, интегрированной в геном животного в локус, отличный от эндогенного локуса иммуноглобулина).
Согласно конкретному варианту осуществления трансген экспрессируется из транскрипционно активного локуса, например, локуса ROSA26, например, мышиного (например, относящегося к мыши) локуса ROSA26.
Согласно одному аспекту предусмотрено отличное от человека животное, содержащее гуманизированный локус тяжелой цепи иммуноглобулина, причем гуманизированный локус тяжелой цепи иммуноглобулина содержит не относящуюся к человеку последовательность ADAM6 или ее ортолог или гомолог.
Согласно одному варианту осуществления отличное от человека животное представляет собой грызуна, выбранного из мыши, крысы и хомяка.
Согласно одному варианту осуществления не относящийся к человеку ортолог или гомолог ADAM6 представляет собой последовательность, которая является ортологичной и/или гомологичной последовательности ADAM6 мыши, причем ортолог или гомолог является функциональным у отличного от человека животного.
Согласно одному варианту осуществления отличное от человека животное выбрано из мыши, крысы и хомяка, и ортолог или гомолог ADAM6 происходит от отличного от человека животного, выбранного из мыши, крысы и хомяка. Согласно конкретному варианту осуществления отличное от человека животное представляет собой мышь, и ортолог или гомолог ADAM6 происходит от животного, которое выбрано из другого вида мыши, крысы и хомяка. Согласно конкретному варианту осуществления отличное от человека животное представляет собой крысу, и ортолог или гомолог ADAM6 происходит от грызуна, который выбран из другого вида крысы, мыши и хомяка. Согласно конкретному варианту осуществления отличное от человека животное представляет собой хомяка, и ортолог или гомолог ADAM6 происходит от грызуна, который выбран из другого вида хомяка, мыши и крысы.
Согласно конкретному варианту осуществления отличное от человека животное происходит из подотряда Myomorpha, и последовательность ADAM6 происходит от животного, выбранного из грызуна надсемейства Dipodoidea и грызуна надсемейства Muroidea. Согласно конкретному варианту осуществления грызун представляет собой мышь надсемейства Muroidea, и ортолог или гомолог ADAM6 происходит от мыши или крысы или хомяка надсемейства Muroidea.
Согласно одному варианту осуществления гуманизированный локус тяжелой цепи содержит один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека. Согласно конкретному варианту осуществления один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека функционально связаны с одним или несколькими генами константной области человека, являющихся химерными и/или относящихся к грызуну (например, мыши или крысе). Согласно одному варианту осуществления гены константной области являются относящимися к мыши. Согласно одному варианту осуществления гены константной области являются относящимися к крысе. Согласно одному варианту осуществления гены константной области являются относящимися к хомяку. Согласно одному варианту осуществления гены константной области содержат последовательность, выбранную из шарнира, CH2, CH3 и их комбинации. Согласно конкретному варианту осуществления гены константной области содержат шарнир, последовательность CH2 и CH3.
Согласно одному варианту осуществления не относящаяся к человеку последовательность ADAM6 является смежной с последовательностью тяжелой цепи иммуноглобулина человека. Согласно одному варианту осуществления не относящаяся к человеку последовательность ADAM6 расположена в пределах последовательности тяжелой цепи иммуноглобулина человека. Согласно конкретному варианту осуществления последовательность тяжелой цепи иммуноглобулина человека содержит генный сегмент V, D и/или J.
Согласно одному варианту осуществления не относящаяся к человеку последовательность ADAM6 расположена рядом с генным сегментом V. Согласно одному варианту осуществления не относящаяся к человеку последовательность ADAM6 расположена между двумя генными сегментами V. Согласно одному варианту осуществления не относящаяся к человеку последовательность ADAM6 расположена рядом между генным сегментом V и генным сегментом D. Согласно одному варианту осуществления последовательность ADAM6 мыши расположена между генным сегментом V и генным сегментом J. Согласно одному варианту осуществления последовательность ADAM6 мыши расположена рядом между генным сегментом D и генным сегментом J.
Согласно одному аспекту предусмотрено генетически модифицированное отличное от человека животное, содержащее В-клетку, которая экспрессирует домен VH человека, когнатный домену VL человека из локуса иммуноглобулина, причем отличное от человека животное экспрессирует не относящийся к иммуноглобулину не относящийся к человеку белок из локуса иммуноглобулина. Согласно одному варианту осуществления не относящийся к иммуноглобулину не относящийся к человеку белок представляет собой белок ADAM. Согласно конкретному варианту осуществления белок ADAM представляет собой белок ADAM6 или его гомолог или ортолог или функциональный фрагмент.
Согласно одному варианту осуществления отличное от человека животное представляет собой грызуна (например, мышь или крысу). Согласно одному варианту осуществления грызун происходит из семейства Muridae. Согласно одному варианту осуществления грызун происходит из подсемейства Murinae. Согласно конкретному варианту осуществления грызун подсемейства Murinae выбран из мыши и крысы.
Согласно одному варианту осуществления не относящийся к иммуноглобулину не относящийся к человеку белок представляет собой белок грызуна. Согласно одному варианту осуществления грызун происходит из семейства Muridae. Согласно одному варианту осуществления грызун происходит из подсемейства Murinae. Согласно конкретному варианту осуществления грызун выбран из мыши, крысы и хомяка.
Согласно одному варианту осуществления домены VH и VL человека прикреплены напрямую или через линкер к последовательности константного домена иммуноглобулина. Согласно конкретному варианту осуществления последовательность константного домена содержит последовательность, выбранную из шарнира, CH2, CH3 и их комбинации. Согласно конкретному варианту осуществления домен VL человека выбран из домена Vκ или Vλ.
Согласно одному аспекту предусмотрено генетически модифицированное отличное от человека животное, содержащее в своей зародышевой линии последовательность иммуноглобулина человека, причем сперма самца отличного от человека животного характеризуется нарушением миграции in vivo. Согласно одному варианту осуществления нарушение миграции in vivo предусматривает неспособность спермы самца отличного от человека животного мигрировать из матки через яйцевод самки отличного от человека животного того же вида. Согласно одному варианту осуществления отличное от человека животное не содержит нуклеотидную последовательность, которая кодирует белок ADAM6 или его функциональный фрагмент. Согласно конкретному варианту осуществления белок ADAM6 или его функциональный фрагмент включает в себя белок ADAM6a и/или ADAM6b или его функциональный фрагменты. Согласно одному варианту осуществления отличное от человека животное представляет собой грызуна. Согласно конкретному варианту осуществления грызун выбран из мыши, крысы и хомяка.
Согласно одному аспекту предусмотрено отличное от человека животное, содержащее последовательность иммуноглобулина человека, смежную с не относящейся к человеку последовательностью, которая кодирует белок ADAM6 или его ортолог или гомолог или функциональный фрагмент. Согласно одному варианту осуществления отличное от человека животное представляет собой грызуна. Согласно конкретному варианту осуществления грызун выбран из мыши, крысы и хомяка.
Согласно одному варианту осуществления последовательность иммуноглобулина человека представляет собой последовательность тяжелой цепи иммуноглобулина. Согласно одному варианту осуществления последовательность иммуноглобулина содержит один или несколько генных сегментов VH. Согласно одному варианту осуществления последовательность иммуноглобулина человека содержит один или несколько генных сегментов DH. Согласно одному варианту осуществления последовательность иммуноглобулина человека содержит один или несколько генных сегментов JH. Согласно одному варианту осуществления последовательность иммуноглобулина человека содержит один или несколько генных сегментов VH, один или несколько генных сегментов DH и один или несколько генных сегментов JH.
Согласно одному варианту осуществления последовательность иммуноглобулина содержит один или несколько генных сегментов VH, которые характеризуются высокой частотой встречаемости в природных репертуарах человека. Согласно конкретному варианту осуществления один или несколько генных сегментов VH содержат не более двух генных сегментов VH, не более трех генных сегментов VH, не более четырех генных сегментов VH, не более пяти генных сегментов VH, не более шести генных сегментов VH, не более семи генных сегментов VH, не более восьми генных сегментов VH, не более девяти генных сегментов VH, не более 10 генных сегментов VH, не более 11 генных сегментов VH, не более 12 генных сегментов VH, не более 13 генных сегментов VH, не более 14 генных сегментов VH, не более 15 генных сегментов VH, не более 16 генных сегментов VH, не более 17 генных сегментов VH, не более 18 генных сегментов VH, не более 19 генных сегментов VH, не более 20 генных сегментов VH, не более 21 генных сегментов VH, не более 22 генных сегментов VH или не более 23 генных сегментов VH.
Согласно конкретному варианту осуществления один или несколько генных сегментов VH содержат пять генных сегментов VH. Согласно конкретному варианту осуществления один или несколько генных сегментов VH содержат 10 генных сегментов VH. Согласно конкретному варианту осуществления один или несколько генных сегментов VH содержат 15 генных сегментов VH. Согласно конкретному варианту осуществления один или несколько генных сегментов VH содержат 20 генных сегментов VH.
Согласно различным вариантам осуществления генные сегменты VH выбраны из VH6-1, VH1-2, VH1-3, VH2-5, VH3-7, VH1-8, VH3-9, VH3-11, VH3-13, VH3-15, VH3-16, VH1-18, VH3-20, VH3-21, VH3-23, VH1-24, VH2-26, VH4-28, VH3-30, VH4-31, VH3-33, VH4-34, VH3-35, VH3-38, VH4-39, VH3-43, VH1-45, VH1-46, VH3-48, VH3-49, VH5-51, VH3-53, VH1-58, VH4-59, VH4-61, VH3-64, VH3-66, VH1-69, VH2-70, VH3-72, VH3-73 и VH3-74. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-2, VH1-8, VH1-18, VH1-46, VH1-69, VH3-7, VH3-9, VH3-11, VH3-13, VH3-15, VH3-21, VH3-23, VH3-30, VH3-33, VH3-43, VH3-48, VH4-31, VH4-34, VH4-39, VH4-59, VH5-51 и VH6-1. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-18, VH1-46, VH1-69, VH3-7, VH3-11, VH3-15, VH3-21, VH3-23, VH3-30, VH3-33, VH3-48, VH4-34, VH4-39, VH4-59 и VH5-51. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-18, VH1-69, VH3-7, VH3-11, VH3-15, VH3-21, VH3-23, VH3-30, VH3-43, VH3-48, VH4-39, VH4-59 и VH5-51. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-18, VH3-11, VH3-21, VH3-23, VH3-30, VH4-39 и VH4-59. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-18, VH3-21, VH3-23, VH3-30 и VH4-39. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH1-18, VH3-23 и VH4-39. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH3-21, VH3-23 и VH3-30. Согласно различным вариантам осуществления генные сегменты VH выбраны из VH3-23, VH3-30 и VH4-39.
Согласно конкретному варианту осуществления последовательность иммуноглобулина человека содержит по меньшей мере 18 генных сегментов VH, 27 генных сегментов DH и шесть генных сегментов JH. Согласно конкретному варианту осуществления последовательность иммуноглобулина человека содержит по меньшей мере 39 генных сегментов VH, 27 генных сегментов DH и шесть генных сегментов JH. Согласно конкретному варианту осуществления последовательность иммуноглобулина человека содержит по меньшей мере 80 генных сегментов VH, 27 генных сегментов DH и шесть генных сегментов JH.
Согласно одному варианту осуществления отличное от человека животное представляет собой мышь, и мышь содержит замещение эндогенных мыши генных сегментов VH одним или несколькими генными сегментами VH человека, причем генные сегменты VH человека функционально связаны с геном области CH мыши так, что мышь реаранжирует генные сегменты VH человека и экспрессирует обратную химерную тяжелую цепь иммуноглобулина, которая содержит домен VH человека и CH мыши. Согласно одному варианту осуществления 90-100% нереаранжированных генных сегментов VH мыши замещают по меньшей мере одним нереаранжированным генным сегментом VH человека. Согласно конкретному варианту осуществления все или по существу все эндогенные генные сегменты VH мыши замещают по меньшей мере одним нереаранжированным генным сегментом VH человека. Согласно одному варианту осуществления замещение проводят с помощью по меньшей мере 19, по меньшей мере 39 или по меньшей мере 80 или 81 нереаранжированного генного сегмента VH человека. Согласно одному варианту осуществления замещение проводят с помощью по меньшей мере 12 функциональных нереаранжированных генных сегментов VH человека, по меньшей мере 25 функциональных нереаранжированных генных сегментов VH человека или по меньшей мере 43 функциональных нереаранжированных генных сегментов VH человека. Согласно одному варианту осуществления мышь содержит замещение всех сегментов DH и JH мыши по меньшей мере одним нереаранжированным сегментом DH человека и по меньшей мере одним нереаранжированным сегментом JH человека. Согласно одному варианту осуществления по меньшей мере один нереаранжированный сегмент DH человека выбран из 1-1, 1-7, 1-26, 2-8, 2-15, 3-3, 3-10, 3-16, 3-22, 5-5, 5-12, 6-6, 6-13, 7-27 и их комбинации. Согласно одному варианту осуществления по меньшей мере один нереаранжированный сегмент JH человека выбран из 1, 2, 3, 4, 5, 6 и их комбинации. Согласно конкретному варианту осуществления один или несколько генных сегментов VH человека выбраны из генного сегмента VH человека 1-2, 1-8, 1-24, 1-69, 2-5, 3-7, 3-9, 3-11, 3-13, 3-15, 3-20, 3-23, 3-30, 3-33, 3-48, 3-53, 4-31, 4-39, 4-59, 5-51, 6-1 и их комбинации.
Согласно различным вариантам осуществления последовательность иммуноглобулина человека находится в функциональной связи с константной областью в зародышевой линии отличного от человека животного (например, грызуна, например, мыши, крысы или хомяка). Согласно одному варианту осуществления константная область представляет собой константную область человека, химерную относящуюся к человеку/мыши или химерную относящуюся к человеку/крысе или химерную относящуюся к человеку/хомяку константную область, константную область мыши, крысы или хомяка. Согласно одному варианту осуществления константная область представляет собой константную область грызуна (например, мыши или крысы или хомяка). Согласно конкретному варианту осуществления грызун представляет собой мышь или крысу. Согласно различным вариантам осуществления константная область содержит по меньшей мере домен CH2 и домен CH3.
Согласно одному варианту осуществления последовательность иммуноглобулина человека тяжелой цепи расположена на локусе тяжелой цепи иммуноглобулина в зародышевой линии отличного от человека животного (например, грызуна, например, мыши или крысы или хомяка). Согласно одному варианту осуществления последовательность иммуноглобулина человека тяжелой цепи расположена на не относящемся к тяжелой цепи иммуноглобулина локусе в зародышевой линии отличного от человека животного, причем не относящийся к тяжелой цепи иммуноглобулина локус представляет собой транскрипционно активный локус. Согласно конкретному варианту осуществления не относящийся к тяжелой цепи иммуноглобулина локус представляет собой локус ROSA26.
Согласно различным аспектам отличное от человека животное дополнительно содержит последовательность легкой цепи иммуноглобулина человека (например, одну или несколько нереаранжированных последовательностей легкой цепи V и J, или одну или несколько реаранжированных последовательностей VJ) в зародышевой линии отличного от человека животного. Согласно конкретному варианту осуществления последовательность иммуноглобулина легкой цепи представляет собой последовательность λ легкой цепи иммуноглобулина. Согласно одному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит один или несколько генных сегментов Vλ. Согласно одному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит один или несколько генных сегментов Jλ. Согласно одному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит один или несколько генных сегментов Vλ и один или несколько генных сегментов Jλ.
Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 12 генных сегментов Vλ и один генный сегмент Jλ. Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 12 генных сегментов Vλ и четыре генных сегмента Jλ.
Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 28 генных сегментов Vλ и один генный сегмент Jλ. Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 28 генных сегментов Vλ и четыре генных сегмента Jλ.
Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 40 генных сегментов Vλ и один генный сегмент Jλ. Согласно конкретному варианту осуществления последовательность легкой цепи иммуноглобулина человека содержит по меньшей мере 40 генных сегментов V и четыре генных сегмента Jλ.
Согласно различным вариантам осуществления последовательность легкой цепи иммуноглобулина человека находится в функциональной связи с константной областью в зародышевой линии отличного от человека животного (например, грызуна, например, мыши или крысы или хомяка). Согласно одному варианту осуществления константная область представляет собой константную область человека, химерную относящуюся к человеку/грызуну, константную область мыши, крысы или хомяка. Согласно конкретному варианту осуществления константная область представляет собой константную область мыши или крысы. Согласно конкретному варианту осуществления константная область представляет собой константную область κ мыши (mCκ) или κ константную область крысы (rCκ). Согласно конкретному варианту осуществления константная область представляет собой λ константную область мыши (mCλ) область или константную область λ крысы (rCλ). Согласно одному варианту осуществления область Сλ2 мыши представляет собой область Сλ мыши.
Согласно одному варианту осуществления последовательность легкой цепи иммуноглобулина человека расположена на локусе легкой цепи иммуноглобулина в зародышевой линии отличного от человека животного. Согласно конкретному варианту осуществления локус легкой цепи иммуноглобулина в зародышевой линии отличного от человека животного представляет собой локус κ легкой цепи иммуноглобулина. Согласно конкретному варианту осуществления локус легкой цепи иммуноглобулина в зародышевой линии отличного от человека животного представляет собой локус λ легкой цепи иммуноглобулина. Согласно одному варианту осуществления последовательность легкой цепи иммуноглобулина человека расположена на не относящемся к легкой цепи иммуноглобулина локусе в зародышевой линии отличного от человека животного, который является транскрипционно активным. Согласно конкретному варианту осуществления не относящийся к иммуноглобулину локус представляет собой локус ROSA26.
Согласно одному аспекту предусмотрен способ получения антитела человека, причем антитело человека содержит вариабельные домены, происходящие из одной или нескольких последовательностей нуклеиновой кислоты вариабельной области, кодируемых в клетке описанного в настоящем документе отличного от человека животного.
Согласно одному аспекту предусмотрена фармацевтическая композиция, содержащая полипептид, который содержит антитело или фрагмент антитела, который происходит из одной или нескольких последовательностей нуклеиновой кислоты вариабельной области, выделенных из описанного в настоящем документе отличного от человека животного. Согласно одному варианту осуществления полипептид представляет собой антитело. Согласно одному варианту осуществления полипептид представляет собой только тяжелую цепь антитела. Согласно одному варианту осуществления полипептид представляет собой одноцепочечный вариабельный фрагмент (например, scFv).
Согласно одному аспекту предусмотрено применение описанного в настоящем документе отличного от человека животного для получения антитела. Согласно различным вариантам осуществления антитело содержит один или несколько вариабельных доменов, которые происходят из одной или нескольких последовательностей нуклеиновой кислоты вариабельной области, выделенных из отличного от человека животного. Согласно конкретному варианту осуществления последовательности нуклеиновой кислоты вариабельной области содержат генные сегменты тяжелой цепи иммуноглобулина. Согласно конкретному варианту осуществления последовательности нуклеиновой кислоты вариабельной области содержат генные сегменты легкой цепи иммуноглобулина.
Мыши, экспрессирующие вариабельные домены λ человека
Генетически модифицированных отличных от человека животных (например, мыши, крысы и т.д.), содержащих модификацию, которая снижает фертильность вследствие потери активности белка ADAM (например, зависимой от ADAM6) могут скрещивать с описанными в настоящем документе не относящимися к человеку животными, которые содержат вариабельные последовательности λ человека на эндогенных не относящихся к человеку или относящихся к человеку (например, трансгенных) генов константной области легкой цепи. Например, такие отличные от человека животные, как мыши или крысы, которые содержат поврежденный ген ADAM6 (или удаленный ген ADAM6), например, животные с гуманизированными локусами тяжелой цепи иммуноглобулина, комбинируют с мышами, которые содержат локус легкой цепи (эндогенный или трансгенный), который содержит сегменты λ человека и сегменты JL, соединенные с генами константной области легкой цепи человека или не относящимися к человеку (например, эндогенными относящимися к мыши или крысе) генами константной области легкой цепи, причем отличные от человека животные содержат активность, которая восстанавливает зависимую от ADAM фертильность. Генетическая модификация, которая восстанавливает зависимую ADAM фертильность, может находиться либо у отличного от человека животного, например, у мыши с гуманизированной тяжелой цепью, либо у мыши с гуманизированными λ вариабельными сегментами. Потомство содержит гены, которые происходят из гуманизированной тяжелой цепи (т.е. приводят к экспрессии вариабельного домена тяжелой цепи человека) и гуманизированного локуса легкой цепи (т.е. приводят к экспрессии вариабельного домена λ легкой цепи человека, слитого с относящейся к человеку или не относящейся к человеку областью λ или κ), причем животные проявляют фертильность, которая является повышенной по сравнению с мышью, которая не содержит активность ADAM6 или активность ортолога или гомолога ADAM6.
Генетически сконструированные мыши VELOCIMMUNE® содержат замещение нереаранжированных генных сегментов V(D)J на эндогенных локусах мыши генными сегментами V(D)J человека. Мыши VELOCIMMUNE® экспрессируют химерные антитела с вариабельными доменами человека и константными доменами мыши (смотрите, например, патент США №7605237). Большинство других работ относятся к мышам, которые экспрессируют полностью человеческие антитела из полностью человеческих трансгенов у мышей, которых содержат недееспособные эндогенные локусы иммуноглобулина.
Легкие цепи антител кодируются одним из двух отдельных локусов: каппа (κ) и лямбда (λ). Легкие цепи антител мыши преимущественно относятся к типу κ. Мыши, которые образуют мышиные антитела, и модифицированные мыши, которые образуют полностью человеческие или химерные относящиеся к человеку-мыши антитела, проявляют смещение в частоте использования легкой цепи. Для людей также характерно смещение частоты использования легких цепей, но не такая выраженная, чем у мышей; соотношение κ легких цепей к λ легким цепям у мышей составляет приблизительно 95:5, тогда как у людей соотношение составляет приблизительно 60:40. Как полагают, более выраженное смещение у мышей не оказывает существенного влияния на разнообразие антител, поскольку, во-первых, у мышей вариабельный локус λ не является настолько разнообразным. Это не характерно для людей. Локус λ легкой цепи человека является очень разнообразным.
Локус λ легкой цепи человека охватывает свыше 1000 т.п.н. и содержит свыше 80 генов, которые кодируют вариабельные (V) или соединяющие (J) сегменты (фиг. 19). В пределах локуса λ легкой цепи человека свыше половины всех наблюдаемых доменов Vλ кодируются генными сегментами 1-40, 1-44, 2-8, 2-14 и 3-21. В общем, полагают, что приблизительно 30 или около этого из генных сегментов Vλ человека являются функциональными. Существуют семь генных сегментов Jλ, только четыре из которых рассматривают в качестве функциональных генных сегментов Jλ - Jλ1, Jλ2, Jλ3 и Jλ7.
Локус λ легкой цепи у людей аналогичен по структуре локусу λ как мышей, так и людей в том, что локус λ легкой цепи человека содержит несколько генных сегментов вариабельной области, которые способны к рекомбинации для образования функционального белка легкой цепи. Локус λ легкой цепи человека содержит приблизительно 70 генных сегментов Vλ и 7 пар генных сегментов Jλ-Сλ. Только четыре из этих пар генных сегментов Jλ-Сλ оказываются функциональными. В некоторых аллелях пятая пара генных сегментов Jλ-Сλ, по имеющимся данным, представляет собой псевдоген (Сλ6). По-видимому, 70 генных сегментов Vλ содержат 38 функциональных генных сегментов. 70 последовательностей Vλ организованы в три кластера, все из которых содержат различных представителей отдельных групп генного семейства V (кластеры A, В и С; фиг. 19). Это представляет собой потенциально богатый источник относительно неиспользованного разнообразия для создания антител с областями V человека у отличных от человека животных.
В разительно контрасте от вышеизложенного, локус λ легкой цепи мыши содержит только два или три (в зависимости от линии) генных сегмента Vλ области мыши (фиг. 20). По меньшей мере по этой причине, сильное смещение к κ у мышей, как полагают, не причиняет особенного ущерба общему разнообразию антител.
Согласно опубликованным картам локуса λ легкой цепи мыши, локус состоит по существу из двух кластеров генных сегментов в пределах отрезка, составляющего приблизительно 200 т.п.н. (фиг. 20). Два кластера содержат два набора генов V, J и С, которые способны к независимой реаранжировке: Vλ2-Jλ2-Cλ2-Jλ4-Cλ4 и Vλ1-Jλ3-Cλ3-Jλ1-Сλ1. Хотя было обнаружено, что Vλ2 рекомбинируется со всеми генными сегментами Jλ, оказывается, что исключительно Vλ1 рекомбинируется с Сλ1. Полагают, что Сλ4 представляет собой псевдоген с дефектными сайтами сплайсинга.
Локус к легкой цепи мыши разительно отличается от вышеизложенного. Структура и количество генных сегментов, которые участвуют в событиях рекомбинации, приводящих к образованию функционального белка легкой цепи из локуса κ мыши, являются намного более сложными (фиг. 21). Таким образом, легкие цепи λ мыши не вносят большой вклад в разнообразие популяции антител у типичной мыши.
Использование богатого разнообразия локуса λ легкой цепи человека у мышей, вероятно, даст в результате, среди прочего, источник более полного репертуара человека доменов V легкой цепи. В предыдущих попытках освоить это разнообразие использовали трансгены человека, содержащие большие количества локусов λ легкой цепи человека, случайным образом встроенных в геном мыши (смотрите, например, патенты США №№6998514 и 7435871). Сообщают, что мыши, содержащие эти случайным образом интегрированные трансгены, экспрессируют полностью человеческие λ легкие цепи, тем не менее, в некоторых случаях, один или оба эндогенных локусов легкой цепи остаются интактными. Эта ситуация является нежелательной, поскольку последовательности легкой цепи человека конкурируют с легкой цепью (κ или λ) мыши в экспрессируемом репертуаре антител мыши.
Напротив, авторы настоящего изобретения описывают генетически модифицированных мышей, которые способны экспрессировать одну или несколько последовательности нуклеиновой кислоты λ легкой цепи напрямую из локуса легкой цепи мыши, включая в себя использование замещения на эндогенном локусе легкой цепи мыши. Генетически модифицированных мышей, способных экспрессировать последовательности λ легкой цепи человека из эндогенного локуса, могут дополнительно скрестить с мышами, которые содержат локус тяжелой цепи человека и, таким образом, использовать для экспрессии антител, содержащих области V (тяжелые и легкие), которые являются полностью человеческими. Согласно различным вариантам осуществления области V экспрессируются с константными областями мышей. Согласно различным вариантам осуществления эндогенные генные сегменты иммуноглобулина мыши отсутствуют, и области V экспрессируются с константными областями человека. Эти антитела нашли бы применимыми в многочисленных применениях, как диагностических, так и терапевтических.
Многие преимущества могут быть достигнуты для различных вариантов осуществления экспрессии связывающих белков, происходящих из генных сегментов Vλ и Jλ человека у мышей. Преимущества могут осуществляться путем помещения последовательностей λ человека на эндогенный локус легкой цепи, например, локус κ или λ мыши. Антитела, полученные от таких мышей, могут содержать легкие цепи, которые содержат домены Vλ человека, слитые с областью CL мыши, в частности, областью Сκ или Сλ мыши. Мыши также будут экспрессировать домены Vλ человека, которые являются подходящими для идентификации и клонирования для применения с областями CL человека, в частности, областями Сκ или Сλ. Поскольку развитие В-клеток у таких мышей является в остальном нормальным, возможно создать совместимые домены Vλ (включающие в себя соматически мутированные домены Vλ), ассоциированные или с Сλ, или с Сκ областями.
Описаны генетически модифицированные мыши, которые содержат нереаранжированный генный сегмент Vλ на локусе κ или λ легкой цепи иммуноглобулина. Описаны мыши, которые экспрессируют антитела, которые содержат легкую цепь с доменом Vλ человека, слитым с областью Сκ или Сλ.
Согласно одному аспекту описано генетически модифицированное отличное от человека животное, которое содержит (1) один или несколько нереаранжированных генных сегментов Vλ человека и один или несколько нереаранжированных генных сегментов Jλ человека на эндогенном локусе легкой цепи иммуноглобулина отличного от человека животного, (2) один или несколько генных сегментов VH человека, один или несколько генных сегментов DH человека и один или несколько генных сегментов JH человека на эндогенном локусе тяжелой цепи иммуноглобулина отличного от человека животного, причем отличное от человека животное способно экспрессировать белок ADAM6 или его функциональный фрагмент, причем белок ADAM6 является функциональным у самца отличного от человека животного. Согласно одному аспекту описано генетически модифицированное отличное от человека животное, которое экспрессирует антитела, содержащие тяжелые цепи, которые содержат домены VH человека и не относящиеся к человеку константные области тяжелой цепи и легкие цепи, которые содержат домены Vλ человека и не относящиеся к человеку константные области легкой цепи, причем отличные от человека животные способны экспрессировать белок ADAM6 или его функциональный фрагмент. Согласно различным вариантам осуществления отличное от человека животное представляет собой грызуна. Согласно одному варианту осуществления грызун представляет собой мышь или крысу.
Согласно одному варианту осуществления не относящийся к человеку константный домен легкой цепи представляет собой домен Сκ или Сλ. Согласно одному варианту осуществления белок ADAM6 или его функциональный фрагмент кодируется эктопической последовательностью в зародышевой линии мыши. Согласно одному варианту осуществления белок ADAM6 или его функциональный фрагмент кодируется эндогенной последовательностью отличного от человека животного.
Согласно одному варианту осуществления эндогенный локус легкой цепи отличного от человека животного представляет собой локус λ легкой цепи иммуноглобулина. Согласно одному варианту осуществления эндогенный локус легкой цепи отличного от человека животного представляет собой локус κ легкой цепи иммуноглобулина.
Согласно одному варианту осуществления отличное от человека животное не содержит эндогенный генный сегмент VL и/или JL на эндогенном локусе легкой цепи. Согласно конкретному варианту осуществления генный сегмент VL и/или JL представляют собой генный сегмент Vκ и/или Jκ. Согласно конкретному варианту осуществления генный сегмент VL и/или JL представляют собой генный сегмент Vλ и/или Jλ.
Согласно одному варианту осуществления генные сегменты VL и JL отличного от человека животного замещают одним или несколькими генными сегментами Vλ человека и одним или несколькими генными сегментами Jλ человека. Согласно конкретному варианту осуществления генные сегменты VL и JL отличного от человека животного представляют собой генные сегменты κ. Согласно конкретному варианту осуществления генные сегменты VL и JL отличного от человека животного представляют собой генные сегменты λ.
Согласно одному варианту осуществления один или несколько генных сегментов Vλ человека происходят из фрагмента кластера A локуса λ легкой цепи иммуноглобулина человека. Согласно конкретному варианту осуществления фрагмент кластера A расположен от Vλ3-27 человека до Vλ3-1 человека. Согласно конкретному варианту осуществления фрагмент кластера A продолжается от Vλ3-12 человека до Jλ1 человека. Согласно одному варианту осуществления один или несколько генных сегментов Vλ человека происходят из фрагмента кластера В локуса λ легкой цепи иммуноглобулина человека. Согласно конкретному варианту осуществления фрагмент кластера В продолжается от Vλ5-52 человека до Vλ1-40 человека. Согласно конкретному варианту осуществления один или несколько генных сегментов Vλ человека происходят из фрагмента кластера A и из фрагмента кластера В описанного в настоящем документе локуса λ легкой цепи иммуноглобулина человека.
Согласно одному варианту осуществления отличное от человека животное содержит по меньшей мере 12 генных сегментов Vλ человека. Согласно одному варианту осуществления отличное от человека животное содержит по меньшей мере 28 генных сегментов Vλ человека. Согласно одному варианту осуществления отличное от человека животное содержит по меньшей мере 40 генных сегментов Vλ человека.
Согласно одному варианту осуществления по меньшей мере один генный сегмент Jλ человека выбран из группы, состоящей из Jλ1, Jλ2, Jλ3, Jλ7 и их комбинации.
Согласно одному аспекту предусмотрен самец фертильного отличного от человека животного, причем фертильное отличное от человека животное экспрессирует (1) легкую цепь иммуноглобулина, содержащую домен Vλ человека или домен Vκ человека, и (2) тяжелую цепь иммуноглобулина, содержащую домен VH человека, причем самец отличного от человека животного содержит модифицированный локус вариабельной области тяжелой цепи и эктопический ген ADAM6, который является функциональным у самца отличного от человека животного. Согласно одному варианту осуществления самец отличное от человека животное представляет собой мышь.
Согласно одному аспекту предусмотрено применение описанного в настоящем документе отличного от человека животного для получения антигенсвязывающего белка. Согласно одному варианту осуществления антигенсвязывающий белок является относящимся к человеку. Согласно одному варианту осуществления антигенсвязывающий белок представляет собой антитело. Согласно одному варианту осуществления антигенсвязывающий белок содержит домен VH человека и/или домен Vλ человека, происходящий от описанного в настоящем документе отличного от человека животного.
Согласно одному аспекту предусмотрена клетка или ткань, происходящая от описанного в настоящем документе отличного от человека животного. Согласно одному варианту осуществления ткань происходит из селезенки, костного мозга или лимфатического узла. Согласно одному варианту осуществления клетка представляет собой В-клетку. Согласно одному варианту осуществления клетка представляет собой эмбриональную стволовую (ES) клетку. Согласно одному варианту осуществления клетка представляет собой зародышевую клетку.
Согласно одному аспекту предусмотрен ооцит, содержащий диплоидный геном описанного в настоящем документе генетически модифицированного отличного от человека животного.
Стерильные транскрипты локуса κ легкой цепи иммуноглобулина
Вариации на тему экспрессии последовательностей λ иммуноглобулина человека у мышей отражены в различных вариантах осуществления генетически модифицированных мышей, способных к такой экспрессии. Таким образом, согласно некоторым вариантам осуществления генетически модифицированные мыши содержат определенную(ые) некодирующую(ие) последовательность(и) из локуса человека. Согласно одному варианту осуществления генетически модифицированная мышь содержит генные сегменты Vλ и Jλ человека на эндогенном локусе κ легкой цепи, и дополнительно содержит геномный фрагмент κ легкой цепи человека. Согласно конкретному варианту осуществления геномный фрагмент κ легкой цепи человека представляет собой некодирующую последовательность, встречающуюся в природе между генным сегментом Vκ человека и генным сегментом Jκ человека.
Локусы κ легкой цепи человека и мышь содержат последовательности, которые кодируют стерильные транскрипты, у которых отсутствуют либо старт-кодон, либо открытая рамка считывания, и которые рассматривают в качестве элементов, которые регулируют транскрипцию локусов κ легкой цепи. Эти стерильные транскрипты происходят из межгенной последовательности, расположенной ниже или 3' от наиболее проксимального генного сегмента Vκ и выше или 5' от интронного энхансера κ легкой цепи (Eκi), который расположен выше гена константной области κ легкой цепи (Сκ). Стерильные транскрипты происходят из реаранжировки межгенной последовательности для образования сегмента VκJκ1, слитого с Сκ.
Замещение локуса к легкой цепи выше гена Сκ будет удалять межгенную область, кодирующую стерильные транскрипты. Следовательно, согласно различным вариантам осуществления замещение последовательности κ легкой цепи мыши выше гена Сκ мыши генными сегментами λ легкой цепи человека будет давать в результате гуманизированный локус κ легкой цепи мыши, который содержит генные сегменты Vλ и Jλ человека, но не межгенную область κ легкой цепи, которая кодирует стерильные транскрипты.
Как описано в настоящем документе, гуманизация эндогенного локуса κ легкой цепи мыши генными сегментами λ легкой цепи человека, причем гуманизация удаляет межгенную область, приводит к сильному снижению в частоте использования локуса κ легкой цепи наряду со значительным повышением частоты использования λ легкой цепи. Следовательно, хотя гуманизированная мышь, у которой отсутствует межгенная область, является применимой в том, что она может производить антитела с вариабельными доменами легкой цепи человека (например, доменами λ или κ человека), частота использования из локуса снижается.
Кроме того, описана гуманизация эндогенного локуса κ легкой цепи мыши с помощью генных сегментов Vλ и Jλ человека совместно со вставкой межгенной области κ человека для создания локуса Vλ, который содержит, относительно транскрипции, между последним генным сегментом Vλ человека и первым генным сегментом Jλ человека, межгенную область κ; которая проявляет популяцию В-клеток с повышенной экспрессией по сравнению с локусом, который не содержит межгенную область κ. Это наблюдение согласуется с гипотезой о том, что межгенная область - напрямую через стерильный транскрипт или опосредованно - подавляет частоту использования из эндогенного локуса λ легкой цепи. В свете этой гипотезы, введение межгенной области будет приводить к снижению частоты использования эндогенного локуса λ легкой цепи, оставляя мыши ограниченный выбор использовать модифицированный (λ в κ) локус для образования антител.
Согласно различным вариантам осуществления замещение последовательности κ легкой цепи мыши выше гена Сκ мыши последовательностью λ легкой цепи человека дополнительно содержит межгенную область κ легкой цепи человека, расположенную, относительно транскрипции, между 3' - нетранслируемой областью от наиболее 3' генного сегмента Vλ и 5' по отношению к первому генному сегменту Jλ человека. Альтернативно, такая межгенная область может быть исключена из замещенного эндогенного локуса κ легкой цепи (выше гена Сκ мыши) путем введения делеции в эндогенный локус λ легкой цепи. Аналогично, согласно настоящему варианту осуществления мышь образует антитела из эндогенного локуса κ легкой цепи, содержащего последовательности λ легкой цепи человека.
Подходы к конструированию мышей для экспрессии доменов Vλ человека
Описаны различные подходы для получения генетически модифицированных мышей, которые образуют антитела, содержащие легкую цепь, которая содержит домен Vλ человека, слитый с эндогенной областью CL (например Сκ или Сλ). Описаны генетические модификации, которые согласно различным вариантам осуществления содержат делецию одного или обоих эндогенных локусов легкой цепи. Например, для удаления λ легких цепей мыши из репертуара эндогенных антител может быть произведена делеция первого генного кластера Vλ-Jλ-Cλ и замещение, полностью или частично, генных сегментов Vλ-Jλ второго генного кластера генными сегментами Vλ-Jλ человека. Также предусмотрены генетически модифицированные зародыши мыши, клетки и нацеливающие конструкты для получения мышей, зародышей мышей и клеток.
Делеция одного эндогенного генного кластера Vλ-Jλ-Cλ и замещение генных сегментов Vλ-Jλ другого эндогенного генного кластера Vλ-Jλ-Cλ использует относительно минимальное нарушение природной ассоциации и функции константной области антитела у животного согласно различным вариантам осуществления, поскольку эндогенные гены Сλ остаются интактными и, следовательно, сохраняют нормальную функциональность и способность ассоциироваться с константной областью эндогенной тяжелой цепи. Таким образом, согласно таким вариантам осуществления модификация не оказывает воздействия на другие эндогенные константные области тяжелой цепи, находящиеся в зависимости от функциональных константных областей легкой цепи для сборки функциональной молекулы антитела, содержащей две тяжелые цепи и две легкие цепи. Кроме того, согласно различным вариантам осуществления модификация не оказывает воздействия на сборку функциональной мембраносвязанной молекулы антитела, включающей в себя эндогенную тяжелую цепь и легкую цепь, например, домен hVλ, соединенный с областью Сλ мыши. Поскольку по меньшей мере один функциональный ген Сλ сохраняется на эндогенном локусе, животные, содержащие замещение генных сегментов Vλ-Jλ эндогенного генного кластера Vλ-Jλ-Cλ генными сегментами Vλ-Jλ человека, должны быть способными получить нормальные λ легкие цепи, которые способны связывать антиген в ходе иммунного ответа посредством генных сегментов Vλ-Jλ человека, присутствующих в экспрессированном репертуаре антител животного.
Схематическое изображение (без соблюдения масштаба) удаленного эндогенного генного кластера Vλ-Jλ-Cλ мыши представлено на фиг. 20. Как показано, локус λ легкой цепи мыши организован в два генных кластера, оба из которых содержат функциональные генные сегменты, способные рекомбинироваться для образования функциональной λ легкой цепи мыши. Эндогенный генный кластер Vλ1-Jλ3-Cλ3-Jλ1-Cλ1 мыши удаляют с помощью нацеливающего конструкта (нацеливающий вектор 1) с неомициновой кассетой, фланкированной сайтами рекомбинации. Другой эндогенный генный кластер (Vλ2-Vλ3-Jλ2-Cλ2-Jλ4-Cλ4) удаляют частично с помощью нацеливающего конструкта (нацеливающий вектор 2) с кассетой гигромицина-тимидинкиназы, фланкированной сайтами рекомбинации. В этом втором событии нацеленного воздействия сохраняют эндогенные генные сегменты Cλ2-Jλ4-Cλ4. Второй нацеливающий конструкт (нацеливающий вектор 2) конструируют с использованием сайтов рекомбинации, которые отличаются от таковых в первом нацеливающем конструкте (нацеливающий вектор 1), тем самым предоставляя возможность для селективной делеции кассеты селекции после достижения успешного нацеленного воздействия. Полученный дважды нацеленный локус является функционально выключенным в том, что эндогенная λ легкая цепь не может быть произведена. Этот модифицированный локус может использоваться для вставки генных сегментов Vλ и Jλ человека для создания эндогенного локуса λ мыши, содержащего генные сегменты Vλ и Jλ человека, посредством чего при рекомбинации на модифицированном локусе животное производит λ легкие цепи, содержащие реаранжированные генные сегменты Vλ и Jλ человека, соединенные с эндогенным генным сегментом Сλ мыши.
Генетически модифицируя мышь для того, чтобы сделать эндогенные генные сегменты λ нефункциональными согласно различным вариантам осуществления приводит в результате к мыши, которая проявляет исключительно κ легкие цепи в своем репертуаре антител, делая мышь применимой для оценки роли λ легких цепей в иммунном ответе, и применимой для получения репертуара антител, содержащих домены Vκ, но не домены Vλ.
Генетически модифицированная мышь, которая экспрессирует hVλ, соединенный с геном Сλ мыши, рекомбинирующийся на эндогенном локусе λ легкой цепи мыши, может быть получена любым способом, известным в настоящей области техники. Схематическое изображение (без соблюдения масштаба) замещения эндогенных генных сегментов Vλ2-Vλ3-Jλ2 мыши генными сегментами Vλ и Jλ человека представлено на фиг. 22А. Как показано, эндогенный локус λ легкой цепи мыши, который был сделан нефункциональным, замещают с помощью нацеливающего конструкта (12/1-λ нацеливающего вектора), который включает в себя кассету неомицина, фланкированную сайтами рекомбинации. Генные сегменты Vλ2-Vλ3-Jλ2 замещают геномным фрагментом, содержащим последовательность λ человека, которая включает в себя 12 генных сегментов hVλ и один генный сегмент hJλ.
Таким образом, этот первый подход помещает один или несколько генных сегментов hVλ на эндогенный локус λ легкой цепи смежно с одним генным сегментом Jλ (фиг. 22А).
Дополнительные модификации в модифицированном эндогенном локусе λ легкой цепи могут быть достигнуты с использованием аналогичных техник, чтобы вставить больше генных сегментов hVλ. Например, схематические изображения двух дополнительных нацеливающих конструктов (+16-λ и +12-λ нацеливающие векторы), используемых для последовательной вставки дополнительных генных сегментов hVλ человека представлены на фиг. 23А. Как показано, дополнительные геномные фрагменты, содержащие конкретные генные сегменты hVλ человека, вставляют в модифицированный эндогенный локус λ легкой цепи в течение последовательных стадий с использованием гомологии, обеспеченной предыдущей вставкой последовательностей λ легкой человека цепи. При рекомбинации с каждым проиллюстрированным нацеливающим конструктом последовательным образом 28 дополнительных генных сегментов hVλ вставляют в модифицированный эндогенный локус λ легкой цепи. Это создает химерный локус, который производит белок λ легкой цепи, который содержит генные сегменты Vλ-Jλ человека, соединенные с геном Сλ мыши.
Описанные выше подходы для вставки генных сегментов λ легкой цепи человека на локус λ мыши сохраняют энхансеры, расположенные ниже генных сегментов Cλ2-Jλ4-Cλ4 (обозначенные Энхансер 2.4, Энхансер и Энхансер 3.1 на фиг. 22А и фиг. 23А). Этот подход дает в результате один модифицированный аллель на эндогенном локусе λ легкой цепи мыши (фиг. 25А).
Предусмотрены композиции и способы получения мыши, которая экспрессирует легкую цепь, содержащую генные сегменты hVλ и Jλ, функционально связанные с генным сегментом мыши Сλ, включая в себя композиции и способ получения мыши, которая экспрессирует такие гены из эндогенного локуса λ легкой цепи мыши. Способы включают в себя селективное приведение одного эндогенного генного кластера Vλ-Jλ-Cλ мыши в нефункциональное состояние (например, путем нацеленной делеции), и использование генных сегментов hVλ и Jλ на эндогенном локусе λ легкой цепи мыши для экспрессии домена hVλ у мыши.
Альтернативно, во втором подходе генные сегменты λ легкой цепи человека могут быть расположены на эндогенном локусе κ легкой цепи. Генетическая модификация согласно различным вариантам осуществления содержит делецию эндогенного локуса κ легкой цепи. Например, для удаления κ легких цепей мыши из эндогенного репертуара антител может быть произведена делеция генных сегментов Vκ и Jκ мыши. Также предусмотрены генетически модифицированные зародыши мыши, клетки и нацеливающие конструкты для получения мышей, зародышей мышей и клеток.
Для указанных выше целей делеция генных сегментов Vκ и Jκ мыши использует относительно минимальное нарушение. Схематическое изображение (без соблюдения масштаба) удаленных генных сегментов Vκ и Jκ мыши представлено на фиг. 21. Эндогенные генные сегменты Vκ и Jκ мыши удаляют посредством опосредованной рекомбиназой делеции положения последовательностей мышей, между двумя точно расположенными нацеливающими векторами, каждый из которых использует сайты сайт-специфической рекомбинации. Первый нацеливающий вектор (Jκ нацеливающий вектор) используют в первом событии нацеленного воздействия для удаления генных сегментов Jκ мыши. Второй нацеливающий вектор (Vκ нацеливающий вектор) используют во втором последующем событии нацеленного воздействия для удаления последовательности, расположенной 5' от наиболее дистального генного сегмента Vκ мыши. Оба нацеливающих вектора содержат сайты сайт-специфической рекомбинации, тем самым предоставляя возможность для селективной делеции обеих кассет селекции и всех промежуточных последовательностей κ легкой цепи мыши после достижения успешного нацеленного воздействия. Полученный удаленный локус является функционально выключенным в том, что не может быть произведена никакая эндогенная κ легкая цепь. Этот модифицированный локус может использоваться для вставки генных сегментов hVλ и Jλ для создания эндогенного локуса к мыши, содержащего генные сегменты hVλ и Jλ, посредством чего при рекомбинации на модифицированном локусе животное производит λ легкие цепи, содержащие реаранжированные генные сегменты hVλ и Jλ, функционально связанные с эндогенным генным сегментом Сκ мыши. Различные нацеливающие векторы, содержащие последовательности λ легкой цепи человека могут использоваться в сочетании с этим удаленным локусом κ мыши для создания гибридного локуса легкой цепи, содержащего генные сегменты λ человека, функционально связанные с областью Сκ мыши.
Таким образом, второй подход помещает один или несколько генных сегментов Vλ человека на локус κ легкой цепи мыши смежно с одним генным сегментом Jλ человека (12/1-κ нацеливающий вектор, фиг. 22В).
Согласно различным вариантам осуществления могут быть произведены модификации в этом подходе для добавления генных сегментов и/или регуляторных последовательностей для оптимизации частоты использования последовательностей λ легкой цепи человека из локуса κ мыши в репертуаре антител мыши.
Согласно третьему подходу один или несколько генных сегментов hVλ размещают на локусе κ легкой цепи мыши смежно с четырьмя генными последовательностями hJλ (12/4-κ нацеливающий вектор на фиг. 22В).
Согласно третьему подходу один или несколько генных сегментов hVλ размещают на локусе κ легкой цепи мыши смежно с межгенной последовательностью κ человека и одной генной последовательностью hJλ (12(κ)1-κ нацеливающий вектор, фиг. 22В).
Согласно четвертому подходу один или несколько генных сегментов hVλ размещают на локусе κ легкой цепи мыши смежно с межгенной последовательностью κ человека и четырьмя генными последовательностями hJλ (12(κ)4-κ нацеливающий вектор фиг. 22В).
Все описанные выше подходы для вставки генных сегментов λ легкой цепи человека на локус κ мыши сохраняют интронный энхансерный элемент κ выше гена Сκ (обозначенный как Еκi, фиг. 22В и фиг. 23В) и 3' к энхансер ниже гена Сκ (обозначенный как Еκ3', фиг. 22В и фиг. 23В). Подходы дают в результате четыре отдельных модифицированных аллеля на эндогенном локусе κ легкой цепи мыши (фиг. 25В).
Согласно различным вариантам осуществления генетически модифицированная мышь содержит нокаут эндогенного локуса λ легкой цепи мыши. Согласно одному варианту осуществления локус λ легкой цепи нокаутируют с помощью стратегии, которая удаляет область, расположенную от Vλ2 до Jλ2, и область, расположенную от Vλ1 до Сλ1 (фиг. 20). Любая стратегия, которая снижает или устраняет способность эндогенного локуса λ легкой цепи экспрессировать эндогенные λ домены, является подходящей для применения в соответствии с вариантами осуществления настоящего раскрытия.
Антитела с лямбда-доменом от генетически модифицированных мышей
Мыши, содержащие последовательности λ человека либо на локусе κ легкой цепи мыши, либо на локусе λ легкой цепи мыши, будут экспрессировать легкую цепь, которая содержит область hVλ, слитую с областью CL мыши (Сκ или Сλ). Их предпочтительно скрещивают с мышами, которые (а) содержат функционально выключенный локус легкой цепи (например, нокаут эндогенного локуса κ или λ легкой цепи); мыши (b) содержат эндогенный локус λ легкой цепи мыши, который содержит генные сегменты hVλ и hJλ, функционально связанные с эндогенным геном Сλ мыши; (с) содержат эндогенный локус κ легкой цепи мыши, который содержит генные сегменты hVκ и hVκ, функционально связанные с эндогенным геном Сκ мыши; и, (d) мышью, у которой один аллель κ содержит hVκ и hVκ; другой аллель κ, содержащий hVλ и hVλ; один аллель λ, содержащий hVλ и hVλ и один аллель λ, выключенный или нокаутированный, или оба аллеля λ, содержащие hVλ и hJλ; и два аллеля тяжелой цепи, каждый из которых содержат hVH, hDH и hJH.
Антитела, которые содержат домены hVλ, экспрессированные в ассоциации либо с Сκ, либо с Сλ, использовали для получения полностью человеческих антител путем клонирования нуклеиновых кислот, кодирующих домены hVλ в конструкты экспрессии, которые несут гены, кодирующие Сλ человека. Полученные конструкты экспрессии трансфектируют в подходящие клетки-хозяева для экспрессии антител, которые проявляют полный домен hVλ, слитый с hCλ.
ПРИМЕРЫ
Следующие примеры предусмотрены для описания получения и применения способов и композиций согласно настоящему изобретению, и не предусмотрены для ограничения объема того, что авторы настоящего изобретения рассматривают как свое изобретение. Если не указано иное, температура указана в градусах Цельсия и давление равно или близко атмосферному.
Пример 1. Гуманизация генов иммуноглобулина мыши
Бактериальные искусственные хромосомы (ВАС) человека и мыши использовали для конструирования 13 различных основанных на ВАС нацеливающих векторов (BACvec) для гуманизации локусов тяжелой цепи и κ легкой цепи иммуноглобулина мыши. На таблицах 1 и 2 представлены подробные описания стадий, проведенных для конструкции всех BACvec, используемых для гуманизации локусов тяжелой цепи и κ легкой цепи иммуноглобулина мыши, соответственно.
Определение ВАС человека и мыши. ВАС мыши, которые охватывают 5' и 3' концы локусов тяжелой цепи и κ легкой цепи иммуноглобулина, определяли путем гибридизации фильтров, на которые точечно наносили библиотеку ВАС, или путем скрининга с помощью ПЦР пулов ДНК библиотеки ВАС мыши. Фильтры гибридизировали при стандартных условиях с использованием зондов, которые соответствовали представляющим интерес областям. Пулы библиотеки подвергали скринингу путем ПЦР с использованием пар уникальных праймеров, которые фланкируют целевую представляющую интерес область. Дополнительную ПЦР с использованием тех же праймеров проводили для деконволюции данной лунки и выделения соответствующей представляющей интерес ВАС. Как фильтры ВАС, так и пулы библиотеки создавали из ES клеток 129 SvJ мыши (Incyte Genomics/Invitrogen). ВАС человека, которые охватывают все целые локусы тяжелой цепи и κ легкой цепи иммуноглобулина определяли или с помощью гибридизации фильтров, на которые точечно наносили библиотеку ВАС (библиотеки Caltech В, С или D и библиотека RPCI-11, Research Genetics/Invitrogen) посредством скрининга пулов библиотеки ВАС человека (библиотека Caltech, Invitrogen) с помощью основанного на ПЦР способа или с использованием баз данных концевых последовательностей ВАС (библиотека Caltech D, TIGR).
Конструкция BACvec с помощью бактериальной гомологичной рекомбинации и лигирования. Бактериальную гомологичную рекомбинацию (BHR) проводили, как описано (Valenzuela et al., 2003; Zhang, Y., Buchholz, F., Muyrers, J.P., and Stewart, A.F. (1998). A new logic for DNA engineering using recombination in Escherichia coli. Nat Genet 20, 123-128). В большинстве случаев линейные фрагменты создавали путем лигирования полученных с помощью ПЦР гомологичных фрагментов с клонированными кассетами с последующим выделением с использованием геля продуктов лигирования и электропорации в BHR-компетентные бактерии, содержащие целевую ВАС. После селекции на чашках Петри с соответствующим антибиотиком, правильно рекомбинированные ВАС определяли с помощью ПЦР в обоих новых участках соединения с последующим рестрикционным анализом на гелях в пульсирующем поле (Schwartz, D.C., and Cantor, C.R. (1984) Separation of yeast chromosome-sized DNAs by pulsed field gradient gel electrophoresis. Cell 37, 67-75) и выборочной проверкой с помощью ПЦР с использованием праймеров, распределенных в последовательностях человека.
3hVH BACvec конструировали с использованием трех последовательных стадий BHR для начальной стадии гуманизации локуса тяжелой цепи иммуноглобулина (фиг. 4А и таблица 1). На первой стадии (стадия 1) кассету вводили в родительскую ВАС человека выше против хода транскрипции от генного сегмента VH1-3 человека, который содержит область гомологии с локусом тяжелой цепи иммуноглобулина мыши (НВ1), ген, который обеспечивает устойчивость к канамицину у бактерий и устойчивость к G418 у клеток животных (kanR) и сайт сайт-специфической рекомбинации (например, loxP). На второй стадии (стадия 2), вторую кассету вводили сразу ниже по ходу транскрипции от последнего JH сегмента, который содержит вторую область гомологии с локусом тяжелой цепи иммуноглобулина мыши (НВ2) и ген, который обеспечивает устойчивость бактерий к спектиномицину (specR). Эта вторая стадия предусматривала делецию последовательностей локуса тяжелой цепи иммуноглобулина человека ниже по ходу транскрипции от JH6 и ген устойчивости к хлорамфениколу из вектора ВАС (cmR). На третьей стадии (стадия 3) дважды модифицированную ВАС человека (В1) затем линеаризировали с использованием сайтов ICeuI, которые добавляли в ходе первых двух стадий и интегрировали в ВАС мыши (В2) с помощью BHR через две области гомологии (НВ1 и НВ2). Отборы по чувствительности к лекарственным средствам для первой (cm/kan), второй (spec/kan) и третьей (cm/kan) стадий разрабатывали так, чтобы они были специфическими для необходимых продуктов. Модифицированные клоны ВАС анализировала с помощью гель-электрофореза в пульсирующем поле (PFGE) после обработки рестрикционных ферментов для определения приемлемой конструкции (фиг. 4В).
Аналогичным образом, 12 дополнительных BACvec сконструировали для гуманизации локусов тяжелой цепи и κ легкой цепи. В некоторых случаях лигирование ВАС проводили вместо BHR для сочетания двух больших ВАС посредством введения редких сайтов рестрикции в оба родительских BACvec с помощью BHR наряду с точным размещением селектируемых маркеров. Это обеспечивает выживание необходимого продукта лигирования при селекции с помощью маркерных комбинаций специфических лекарственных средств. Рекомбинантные ВАС, полученные путем лигирования после обработки с помощью редких рестрикционных ферментов, определяли и подвергали скринингу способом, аналогичным для ВАС, полученных с помощью BHR (как описано выше).
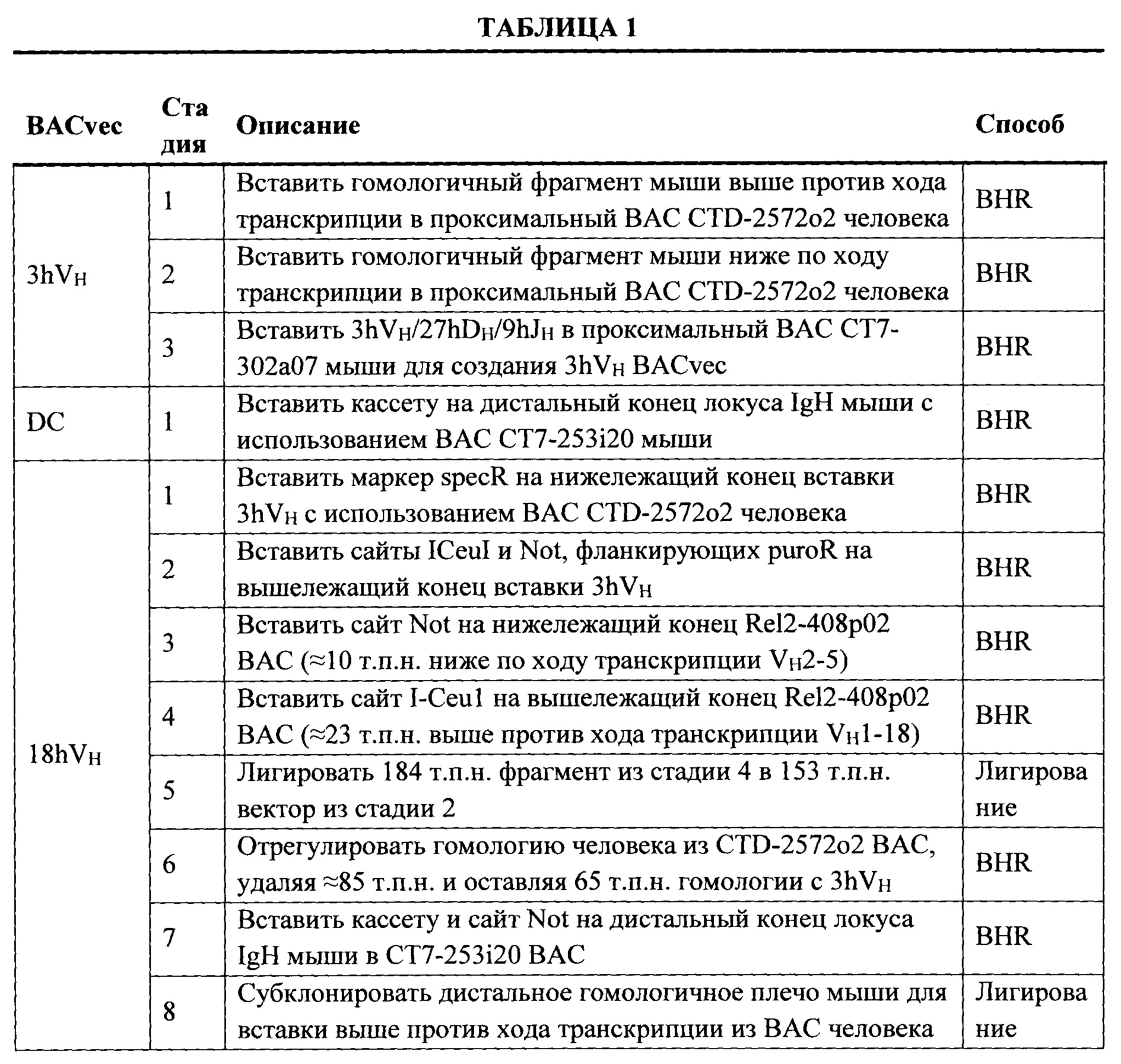
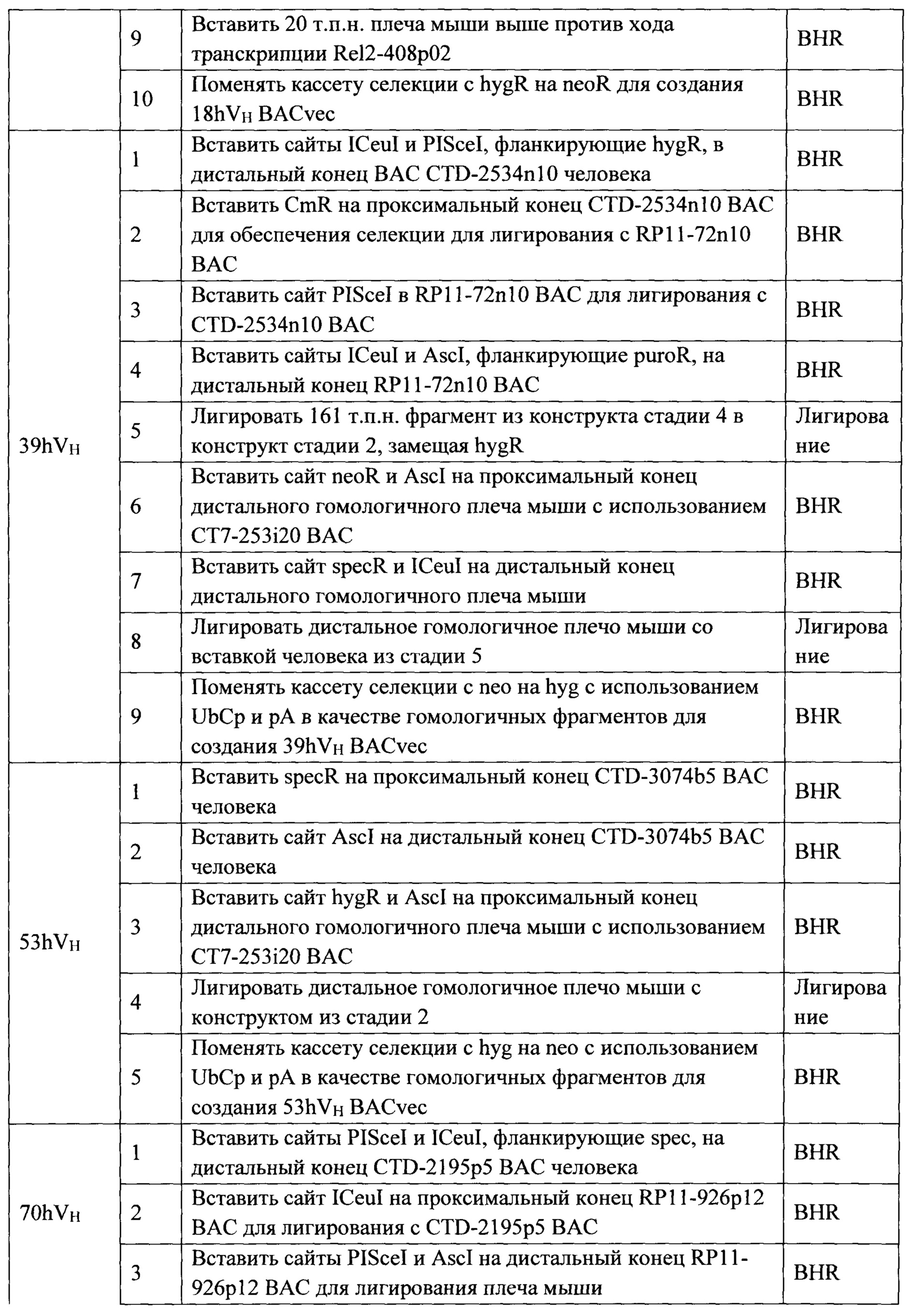

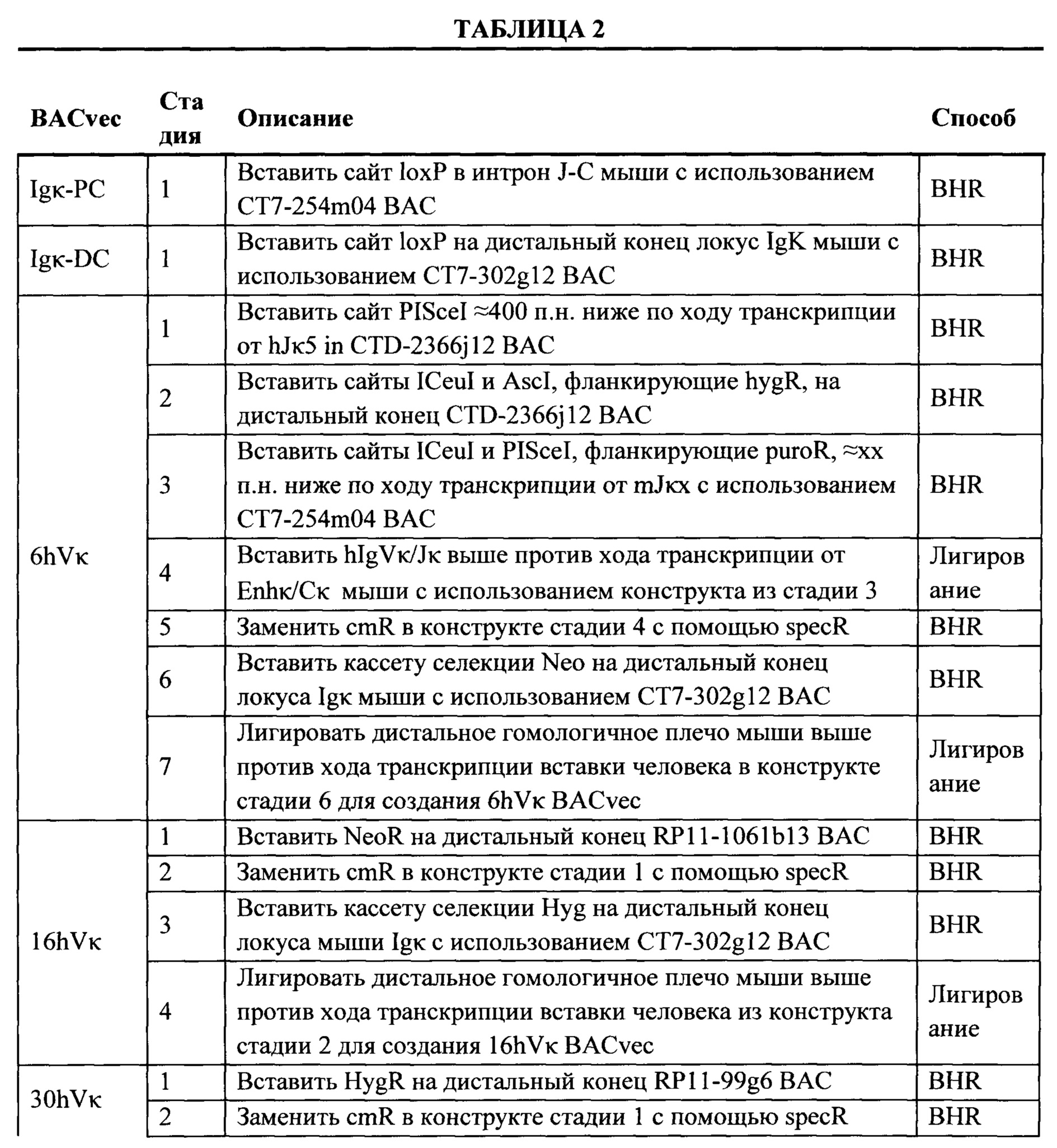

Модификация эмбриональных стволовых (ES) клеток и создание мышей. Нацеленное воздействие на ES клетки (F1H4) проводили с использованием способа генной инженерии VELOCIGENE®, как описано (Valenzuela et al., 2003). Получение мышей из модифицированных ES клеток либо с помощью инъекции бластоцисты (Valenzuela et al., 2003), либо инъекции 8 клеток (Poueymirou et al., 2007) соответствовало описанному. Нацеленные ES клетки и мышей подтверждали с помощью скрининга ДНК из ES клеток или мышей с помощью уникальных наборов зондов и праймеров в основанном на ПЦР анализе (например, фиг. 3A, 3В и 3С). Все исследования на мышах проводились под наблюдением и были одобрены Институциональным комитетом по содержанию и использованию животных Regeneron (IACUC).
Анализ кариотипа и флуоресцентная гибридизация in situ (FISH). Анализ кариотипа проводили с помощью Coriell Cell Repositories (Coriell Institute for Medical Research, Камден, Нью-Джерси). FISH проводили на нацеленных ES клетках, как описано (Valenzuela et al., 2003). Зонды, соответствующие либо ДНК ВАС мыши, либо ДНК ВАС человека, метили с помощью ник-трансляции (Invitrogen) с помощью флуоресцентно меченых dUTP нуклеотидов оранжевого или зеленого спектра (Vysis).
Вариабельный генный локус тяжелой цепи иммуноглобулина. Гуманизацию вариабельной области локуса тяжелой цепи выполняли за девять последовательных стадий путем прямого замещения приблизительно трех миллионов пар нуклеотидов (Mb) смежной геномной последовательности мыши, содержащей все генные сегменты VH, DH и JH, приблизительно одной Mb смежной геномной последовательности человека, содержащей эквивалентные генные сегменты человека (фиг. 1А и таблица 1) с использованием VELOCIGENE® технология генной инженерии (смотрите, например, патент США №6586251 и Valenzuela et al., 2003).
Интрон между генными сегментами JH и генами константной области (интрон J-C) содержит транскрипционный энхансер (Neuberger, M.S. (1983) Expression and regulation of immunoglobulin heavy chain gene transfected into lymphoid cells. Embo J 2, 1373-1378), за которым следует область простых повторов, необходимых для рекомбинации в ходе переключения изотипа (Kataoka, Т, Kawakami, Т., Takahashi, N., and Honjo, Т. (1980). Rearrangement of immunoglobulin gamma 1-chain gene and mechanism for heavy-chain class switch. Proc Natl Acad Sci USA 77, 919-923). Участок соединения между областью VH-DH-JH человека и CH областью мыши (проксимальный участок соединения) выбирали для сохранения интронного энхансера тяжелой цепи мыши и переключения домена для сохранения как эффективной экспрессии, так и переключения класса гуманизированного локуса тяжелой цепи у мыши. Определение точного положения нуклеотидов этого и последующих участков соединения во всех замещениях было возможным путем использования способа генной инженерии VELOCIGENE® (ранее), который использовал бактериальную гомологичную рекомбинацию, управляемую синтезированными олигонуклеотидами. Таким образом, проксимальный участок соединения располагали приблизительно на 200 п.н. ниже по ходу транскрипции от последнего генного сегмента JH и дистальный участок соединения располагали на несколько сотен выше против хода транскрипции от наиболее 5' генного сегмента VH локуса человека и приблизительно на 9 т.п.н. ниже по ходу транскрипции от генного сегмента VH1-86 мыши, также известного как J558.55. Генный сегмент VH1-86 (J558.55) мыши представляет собой наиболее дистальный вариабельный генный сегмент тяжелой цепи, который, как сообщается, представляет собой псевдоген у C57BL/6 мышей, но является потенциально активным, хотя и со слабой последовательностью RSS, в нацеленном 129 аллеле. Дистальный конец локуса тяжелой цепи мыши, как сообщается, может содержать контрольные элементы, которые регулируют экспрессию и/или реаранжировку локуса (Pawlitzky et al., 2006).
Первую вставку последовательности ДНК иммуноглобулина человека в мышь осуществляли с использованием 144 т.п.н. проксимального конца локуса тяжелой цепи человека, содержащего 3 VH, все 27 DH и 9 JH генных сегментов человека, вставленных в проксимальный конец локус IgH мыши, с сопутствующей 16,6 т.п.н. делецией геномной последовательности мыши с использованием приблизительно 75 т.п.н. гомологичных плечей мыши (стадия A, фиг. 2А; таблицы 1 и 3, 3hVH). Эту большую 144 т.п.н. вставку и сопутствующую 16,6 т.п.н. делецию проводили в одной стадии (стадия А), которая происходила с частотой, составляющей 0,2% (таблица 3). Правильно нацеленные ES клетки подсчитывали с помощью анализа потери нативного аллеля (LONA) (Valenzuela et al., 2003) с использованием зондов в пределах удаленной последовательности мыши и фланкирующих ее и в пределах вставленной последовательности человека, и целостность большой вставки человека подтверждали с использованием множественных зондов, охватывающих всю вставку (фиг. 3A, 3В и 3С). Поскольку предполагали много циклов последовательного нацеленного воздействия на ES клетки, нацеленные ES клеточные клоны на этой и всех последующих стадиях подвергали кариотипическому анализу (ранее) и только те клоны, которые показывали нормальные кариотипы меньшей мере в 17 из 20 выборок использовали для последующих стадий.
Нацеленные ES клетки из стадии A подвергали повторному нацеленному воздействию с помощью BACvec, который производил 19 т.п.н. делецию на дистальном конце локуса тяжелой цепи (стадия В, фиг. 2А). BACvec стадии В содержал ген устойчивости к гигромицину (hyg) в отличие от гена устойчивости к неомицину (neo), содержащегося на BACvec стадии А. Гены устойчивости из двух BACvec разработали так, чтобы при успешном нацеленном воздействии на одну и ту же хромосому, приблизительно три Mb вариабельного генного локуса тяжелой цепи мыши, содержащего все генные сегменты VH мыши, отличные от VH1-86 и все генные сегменты DH, отличные от DQ52, а также два гена устойчивости, фланкировали с помощью сайтов loxP; DQ52 и все генные сегменты JH цепи мыши удаляли на стадии A. ES клеточные клоны, дважды нацеленные на одну и ту же хромосому, определяли, приводя проксимальную кассету 3hVH к гомозиготности в клетках с высоким содержанием G418 (Mortensen, R.M. et al. (1992) Production of homozygous mutant ES cells with a single targeting construct. Mol Cell Biol 12:2391-239) и следуя направлению дистальной кассеты hyg. Сегменты мыши размером до четырех Mb, модифицированные таким образом, чтобы фланкироваться сайтами loxP, успешно удаляли в ES клетках путем временной экспрессии CRE рекомбиназы с высокими показателями результативности (до ≈11%) даже при отсутствии селекции по чувствительности к лекарственным средствам (Zheng, В., et al. (2000). Engineering mouse chromosomes with Cre-loxP: range, efficiency, and somatic applications. Mol Cell Biol 20:648-655). Сходным образом, авторы настоящего изобретения осуществили трех Mb делецию у 8% ES клеточных клонов после временной экспрессии CRE (стадия С, фиг. 2А; таблица 3). Делецию оценивали с помощью анализа LONA с использованием зондов на любом конце удаленной последовательности мыши, а также потерю neo и hyg и появление продукта ПЦР в точке делеции, содержащей единственный оставшийся сайт loxP. Более того, делецию подтверждали путем флуоресцентной гибридизации in situ (данные не показаны).
Остаток вариабельной области тяжелой цепи человека добавляли к аллелю 3hVH в серии из 5 стадий с использованием способа генной инженерии VELOCIGENE® (стадии Е-Н, фиг. 2В), причем каждая стадия включала в себя точную вставку до 210 т.п.н. генных последовательностей человека. Для каждой стадии проксимальный конец каждого нового BACvec разрабатывали так, чтобы он перекрывал наиболее дистальные последовательности человека предыдущей стадии и дистальный конец каждого нового BACvec содержал такую же дистальную область гомологии мыши, как использовалась на стадии A. BACvec из стадий D, F и Н содержали кассеты селекции neo, тогда как BACvec из стадий Е и G содержали кассеты селекции hyg, таким образом, селекции чередовали между G418 и гигромицином. Нацеленное воздействие на стадии D анализировали с помощью потери уникального продукта ПЦР в дистальном сайте loxP гибридного аллеля 3hVH. Нацеленное воздействие для стадий Е-I анализировали с помощью потери предыдущей кассеты селекции. На конечной стадии (стадия I, фиг. 2В) кассету селекции neo, фланкированную сайтами Frt (McLeod, М. et al. (1986) Identification of the crossover site during FLP-mediated recombination in the Saccharomyces cerevisiae plasmid 2 microns circle. Mol Cell Biol 6, 3357-3367), удаляли с помощью временной экспрессии FLPe (Buchholz, F. et al. (1998) Improved properties of FLP recombinase evolved by cycling mutagenesis. Nat Biotechnol 16, 657-662). Последовательности человека из BACvec для стадий D, Е и G получали из двух родительских ВАС человека каждый, тогда как таковые из стадий F и Н были из одних ВАС. Сохранение последовательностей человека подтверждали на каждой стадии с использованием множественных зондов, охватывающих вставленные последовательности человека (как описано выше, например, фиг. 3A, 3В и 3С). Только клоны с нормальным кариотипы и зародышевый потенциал переносили далее в каждой стадии. ES клетки из конечной стадии все еще были способны вносить вклад в зародышевую линию после девяти последовательных манипуляций (таблица 3). Мыши, гомозиготные в отношении каждого из аллелей тяжелой цепи были жизнеспособны, казались здоровыми и демонстрировали по существу гуморальную иммунную систему дикого типа (смотрите пример 3).
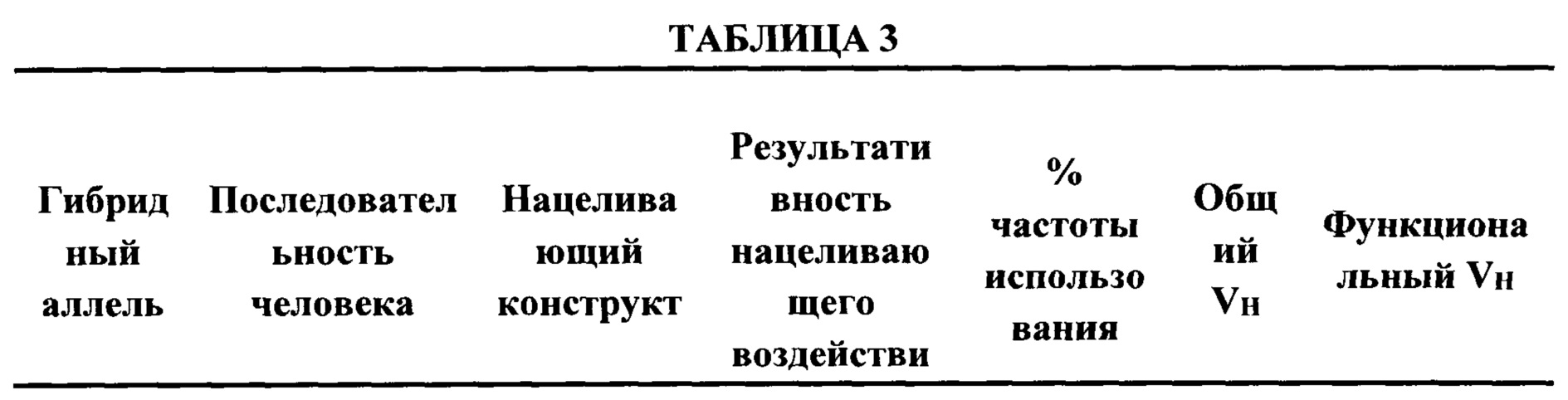
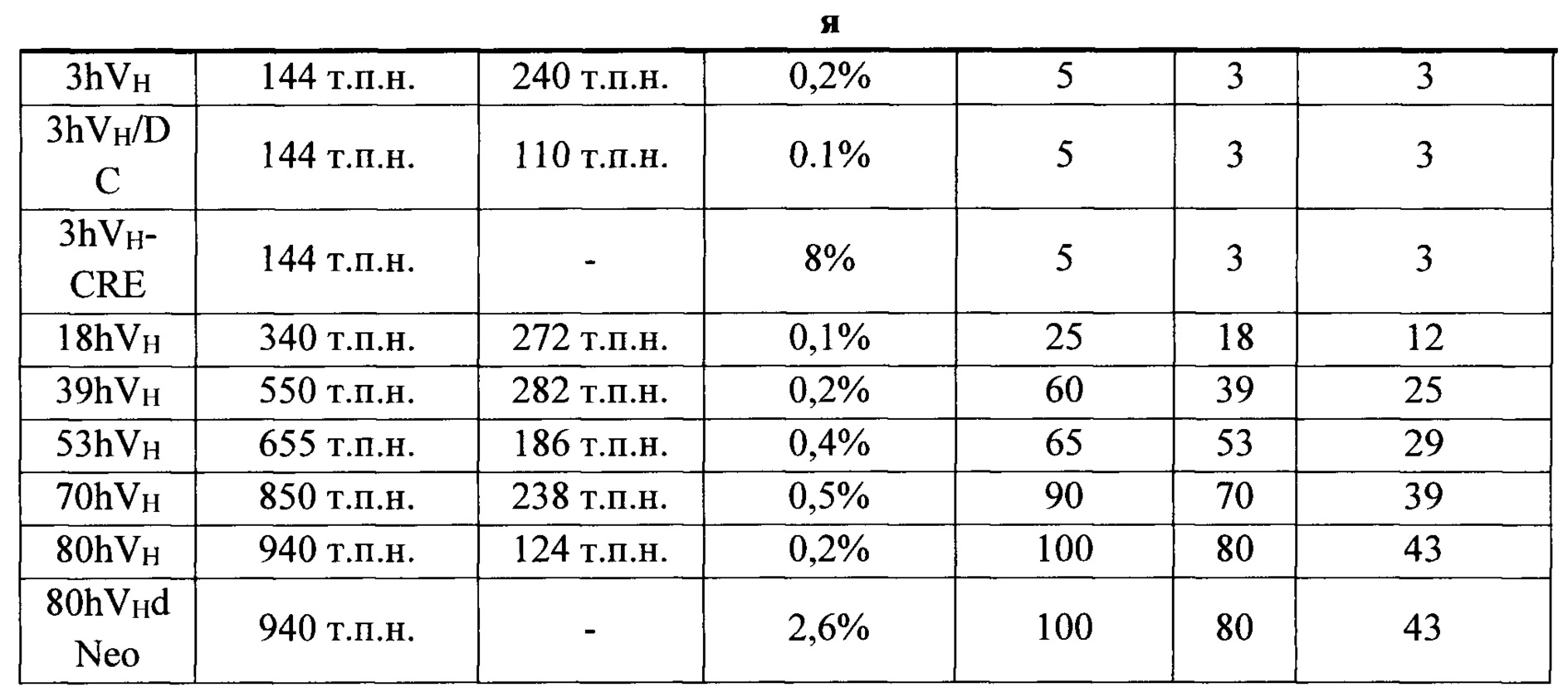
Вариабельный генный локус κ легкой цепи иммуноглобулина. Вариабельную область κ легкой цепи гуманизировали в ходе восьми последовательных стадий путем прямого замещения приблизительно трех Mb последовательности мыши, содержащей все генные сегменты Vκ и Jκ приблизительно 0,5 Mb последовательности человека, содержащей проксимальные генные сегменты Vκ и Jκ человека способом, сходным с таковым для тяжелой цепи (фиг. 1В; таблицы 2 и 4).
Вариабельная область локуса κ легкой цепи человека содержит два почти идентичных 400 т.п.н. повтора, разделенных 800 т.п.н. спейсером (Weichhold, G.M. et al. (1993) The human immunoglobulin kappa locus consists of two copies that are organized in opposite polarity, Genomics 16:503-511). Поскольку повторы являются настолько сходными, почти все разнообразие локусов может быть воспроизведено у мышей путем использования проксимального повтора. Кроме того, сообщалось об естественном аллеле человека локуса κ легкой цепи, утратившем дистальный повтор (Schaible, G. et al. (1993) The immunoglobulin kappa locus: polymorphism and haplotypes of Caucasoid and non-Caucasoid individuals, Hum Genet 91:261-267). Авторы настоящего изобретения заместили приблизительно три Mb вариабельной генной последовательности κ легкой цепи мыши приблизительно 0,5 Mb вариабельной генной последовательности κ легкой цепи человека для эффективного замещения всех генных сегментов Vκ и Jκ мыши проксимальными Vκ человека и всеми генными сегментами Jκ человека (фиг. 2С и 2D; таблицы 2 и 4). В отличие от описанного в примере 1 для локуса тяжелой цепи способа целую генную область Vκ мыши, содержащую все генные сегменты Vκ и Jκ, удаляли с помощью трехстадийного способа перед добавлением какой-либо последовательности человека. Вначале, кассету neo вводили на проксимальный конец вариабельной области (стадия A, фиг. 2С). Далее, кассету hyg вставляли на дистальный конец κ локуса (стадия В, фиг. 2С). Сайты loxP снова размещали в пределах каждой кассета селекции так, чтобы обработка CRE вызывала делецию оставшихся 3 Mb области Vκ мыши вместе с обоими генами устойчивости (стадия С, фиг. 2С).
Геномный фрагмент человека размером приблизительно 480 т.п.н., содержащий целую вариабельную область κ легкой цепи иммуноглобулина, вставляли в ходе четырех последовательных стадий (фиг. 2D; таблицы 2 и 4), причем до 150 т.п.н. последовательности κ легкой цепи иммуноглобулина человека вставляли за одну стадию с использованием способов, сходных в таковыми, используемыми для тяжелой цепи (смотрите пример 1). Последний ген устойчивости к гигромицину удаляли с помощью временной экспрессии FLPe. Как и в случае тяжелой цепи, нацеленные ES клеточные клоны оценивали в отношении целостности полной вставки человека, нормального кариотипа и зародышевого потенциала после каждой стадии. Получали мышей, гомозиготных в отношении каждого из аллелей κ легкой цепи, и было обнаружено, что они являлись здоровыми и имели нормальный внешний вид.
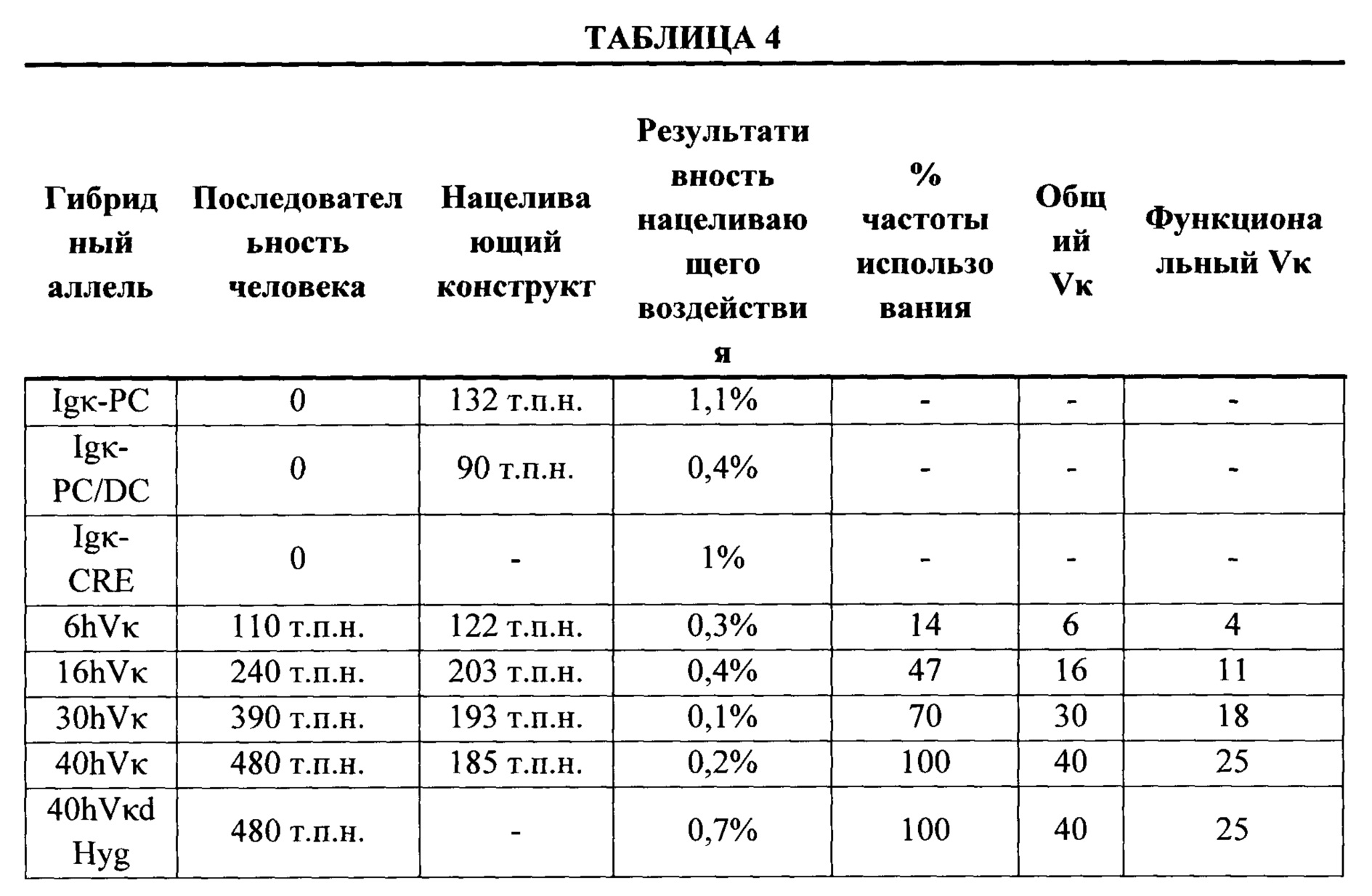
Пример 2. Получение полностью гуманизированных мышей с помощью комбинации множественных гуманизированных аллелей иммуноглобулина
В нескольких местах ES клетки, несущие часть вариабельных репертуаров тяжелой цепи или κ легкой цепи иммуноглобулина человека, как описано в примере 1, подвергали микроинъекции и полученных мышей скрещивали для получения множественных вариантов мышей VELOCIMMUNE® с возрастающим количеством фракций зародышевых репертуаров иммуноглобулина человека (таблица 5; фиг. 5A и 5В). Мыши VELOCIMMUNE® 1 (V1) обладают 18 генными сегментами VH человека и всеми генными сегментами DH и JH человека, комбинированными с 16 человек генными сегментами Vκ и всеми генными сегментами Jκ человека. Мыши VELOCIMMUNE® 2 (V2) и VELOCIMMUNE® (V3) характеризуются увеличенными вариабельными репертуарами, включая в себя в общем 39 VH и 30 Vκ, и 80 VH и 40 Vκ, соответственно. Поскольку геномные области, кодирующие генные сегменты VH, DH и JH мыши, и генные сегменты Vκ и Jκ, полностью замещали, антитела, производимые любым вариантом мышей VELOCIMMUNE®, содержат вариабельные области человека, связанные с константными областями мыши. Локусы λ легкой цепи мыши остаются интактными во всех вариантах мышей VELOCIMMUNE® и служат в качестве средства сравнения результативности экспрессии различных гуманизированных локусов κ легкой цепи VELOCIMMUNE®.
Мышей, дважды гомозиготных в отношении обеих гуманизаций тяжелой цепи и κ легкой цепи иммуноглобулина, получали из подгруппы описанных в примере 1 аллелей. Все генотипы, наблюдаемые в течение курса скрещивания для получения дважды гомозиготных мышей, возникали приблизительно в менделевских пропорциях. Мужское потомство, гомозиготное в отношении каждого из аллелей тяжелой цепи человека, показало сниженную фертильность. Сниженная фертильность являлась результатом потери активности ADAM6 мыши. Вариабельный генный локус тяжелой цепи мыши содержит два включенных в него функциональных гена ADAM6 (ADAM6a и ADAM6b). В ходе гуманизации вариабельного генного локуса тяжелой цепи мыши вставленная геномная последовательность человека содержала псевдоген ADAM6. ADAM6 мыши может быть необходимым для фертильности, и, таким образом, отсутствие генов ADAM6 мыши в гуманизированных вариабельных генных локусах тяжелой цепи может привести в сниженной фертильности у этих мышей, несмотря на присутствие псевдогена человека. В примерах 7-9 описано точное замещение удаленных генов ADAM6 мыши обратно в гуманизированный вариабельный генный локус тяжелой цепи, и восстановление уровня фертильности дикого типа у мышей с гуманизированным локусом тяжелой цепи иммуноглобулина.
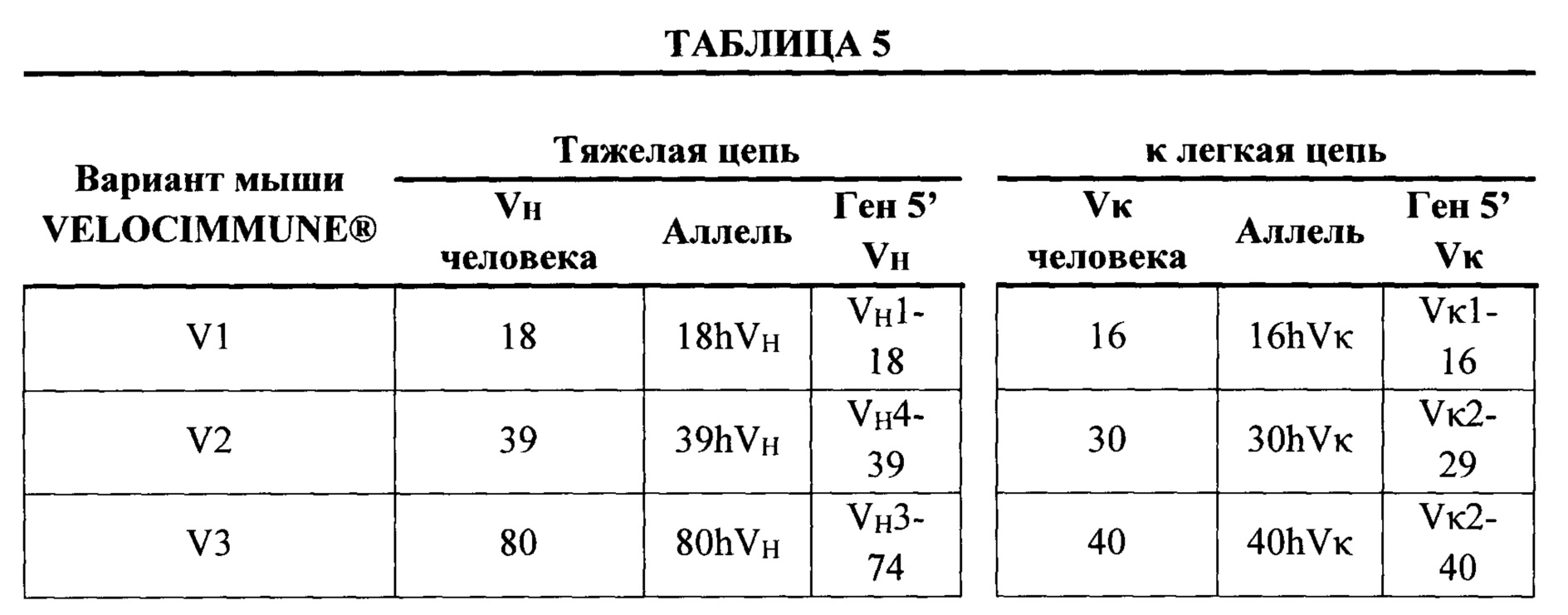
Пример 3. Популяции лимфоцитов у мышей с гуманизированными генами иммуноглобулина
Популяции зрелых В-клеток у трех различных вариантов мышей VELOCIMMUNE® оценивали с помощью проточной цитометрии.
Кратко, клеточные суспензии из костного мозга, селезенки и тимуса получали с использованием стандартных способов. Клетки ресуспендировали в концентрации 5×105 клеток/мл в буфере для окрашивания для FACS BD Pharmingen, блокировали с помощью антитела к CD16/32 мыши (BD Pharmingen), окрашивали с помощью пригодного коктейля антител и фиксировали с помощью BD Cytofix™, все согласно инструкциям производителей. Последние клеточные осадки ресуспендировали в 0,5 мл буфера для окрашивания и анализировали с использованием программного обеспечения BD FACSCALIBUR™ и BD CELLQUEST PRO™. Все антитела (BD Pharmingen) получали в массовом разведении/коктейле и добавляли до конечной концентрации 0,5 мг/105 клеток. Коктейли антител для окрашивания костного мозга (A-D) были следующими: А: антитело к IgMb-FITC мыши, антитело к IgMa-PE мыши, антитело к CD45R(B220)-APC мыши; В: антитело к CD43(S7)-PE мыши, антитело к CD45R(B220)-APC мыши; С: антитело к CD24(HSA)-PE мыши; антитело к CD45R(B220)-APC мыши; D: антитело к ВР-1-РЕ мыши, антитело к CD45R(B220)-APC мыши. Коктейли антител для окрашивания селезенки и паховых лимфатических узлов (Е-Н) были следующими: Е: антитело к IgMb-FITC мыши, антитело к IgMa-PE мыши, антитело к CD45R(B220)-APC мыши; F: антитело к Ig, λ1, λ2, λ3 легкая цепь-FITC мыши, антитело к Igκ легкая цепь-РЕ мыши, антитело к CD45R(B220)-АРС мыши; G: антитело к Ly6G/C-FITC мыши, антитело к CD49b(DX5)-PE мыши, антитело к CD11b-APC мыши; Н: антитело к CD4(L3T4)-FITC мыши, антитело к CD45R(B220)-PE мыши, антитело к CD8a-APC мыши. Результаты показаны на фиг. 6.
Лимфоциты, выделенные из селезенки или лимфатического узла гомозиготных мышей VELOCIMMUNE®, окрашивали в отношении поверхностной экспрессии маркеров В220 и IgM и анализировали с использованием проточной цитометрии (фиг. 6). Размеры популяций В220+ IgM+ зрелых В-клеток во всех вариантах исследованных мышей VELOCIMMUNE® были фактически идентичны таковым у мышей дикого типа, независимо от числа генных сегментов VH, которые они содержали. Кроме того, мыши, содержащие гомозиготные гибридные гуманизированные локусы тяжелой цепи иммуноглобулина, даже таковые только с 3 VH генными сегментами, но нормальными локусами κ легкой цепи иммуноглобулина мыши или мыши, содержащие гомозиготные гибридные гуманизированные локусы κ легкой цепи с нормальными локусами тяжелой цепи иммуноглобулина мыши также содержали нормальные количества клеток В220+ IgM+ в их периферических компартментах (не показано). Эти результаты показывают, что химерные локусы с вариабельными генными сегментами человека и константными областями мыши могут полностью заполнить компартмент зрелых В-клеток. Кроме того, число вариабельных генных сегментов на локусах или тяжелой цепи, или κ легкой цепи и, таким образом, теоретическое разнообразие репертуара антител, не коррелирует со способностью создавать популяции дикого типа зрелых В-клеток. Напротив, мыши с интегрированными случайным образом полностью человеческими иммуноглобулиновыми трансгенами и инактивированными локусами иммуноглобулина мыши характеризуются сниженными количествами В-клеток в этих компартментах, причем тяжесть дефицита зависит от числа включенных в трансген вариабельных генных сегментов (Green, L.L., and Jakobovits, А. (1998) Regulation of В cell development by variable gene complexity in mice reconstituted with human immunoglobulin yeast artificial chromosomes, J Exp Med 188:483-495). Это показывает, что стратегия "in situ генетической гуманизации" приводит к функциональному результату, фундаментально отличному от интегрированных случайным образом трансгенов, полученных с помощью "генного нокаута вместе с трансгенным подходом".
Исключение аллеля и выбор локуса. Способность сохранять исключение аллеля исследовали у мышей, гетерозиготных в отношении различные вариантов гуманизированного локуса тяжелой цепи иммуноглобулина.
Гуманизацию локусов иммуноглобулина проводили в ES линии F1 (F1H4 (Valenzuela et al., 2003)), происходящей из гетерозиготных эмбрионов 129S6/SvEvTac и C57BL/6NTac. Зародышевые генные последовательности вариабельной области тяжелой цепи человек подвергают нацеленному воздействию на 129S6 аллель, который несет гаплотип IgMa, тогда как немодифицированный аллель C576BL/6N мыши несет гаплотип IgMb. Эти аллельные формы IgM могут быть дифференцированы с помощью проточной цитометрии с использованием антител, специфических к полиморфизмам, обнаруженным в аллелях IgMa или IgMb. Как показано на фиг. 6 (нижний ряд), В-клетки, определенные у мышей, гетерозиготных в отношении каждого варианта гуманизированного локуса тяжелой цепи, экспрессируют только один аллель, или IgMa (гуманизированный аллель), или IgMb (аллель дикого типа). Это показывает, что механизмы, вовлеченные в исключение аллеля, являются интактными у мышей VELOCIMMUNE®. Кроме того, относительное количество В-клеток, положительных в отношении гуманизированного аллеля (IgMa) приблизительно пропорционально числу присутствующих генных сегментов VH. Гуманизированный локус иммуноглобулина экспрессируется приблизительно в 30% В-клеток у гетерозиготных мышей VELOCIMMUNE® 1, которые содержат 18 генных сегментов VH человека, и в 50% В-клеток у гетерозиготных мышей VELOCIMMUNE® 2 и 3 (не показано), с 39 и 80 генными сегментами VH человека, соответственно. В частности, отношение клеток, экспрессирующих гуманизированный аллель мыши, к аллелю дикого типа (0,5 для мышей VELOCIMMUNE® 1 и 0,9 для мышей VELOCIMMUNE® 2) является больше, чем отношение числа вариабельных генных сегментов, содержащихся в гуманизированных локусах, к локусам дикого типа (0,2 для мышей VELOCIMMUNE® 1 и 0,4 для мышей VELOCIMMUNE® 2). Это может показывать, что вероятность выбора аллеля является промежуточной между случайным выбором одной или другой хромосомы и случайным выбором RSS любого конкретного V сегмента. Кроме того, может иметь место фракция В-клеток, но не все, в которой один аллель становится доступным для рекомбинации, завершает процесс и прекращает рекомбинацию до того, как другой аллель становится доступным. Кроме того, даже распределение клеток, которые содержат поверхностный IgM (sIgM), происходящий или из гибридного гуманизированного локуса тяжелой цепи, или локуса тяжелой цепи мыши дикого типа, является доказательством того, что гибридный локус функционирует на нормальном уровне. В отличие от этого, интегрированные случайным образом трансгены иммуноглобулина человека слабо конкурируют с локусами иммуноглобулина мыши дикого типа (Bruggemann, М., et al. (1989) A repertoire of monoclonal antibodies with human heavy chains from transgenic mice. PNAS 86, 6709-6713; Green et al. (1994); Tuaillon, N. et al. (1993) Human immunoglobulin heavy-chain minilocus recombination in transgenic mice: gene-segment use in mu and gamma transcripts, Proc Natl Acad Sci USA 90:3720-3724). Это дополнительно демонстрирует, что произведенные мышами VELOCIMMUNE® иммуноглобулины являются функционально отличными от таковых, произведенных интегрированными случайным образом трансгенами у мышей, полученных с помощью "генного нокаута вместе с трансгенным подходом".
Полиморфизмы областей Сκ являются недоступными в 129S6 или C57BL/6N для исследования исключения аллеля гуманизированных локусов κ легкой цепи по сравнению с негуманизированными локусами. Тем не менее, все мыши VELOCIMMUNE® обладают локусами λ легкой цепи мыши дикого типа, следовательно, возможно наблюдать, может ли реаранжировка и экспрессия гуманизированных локусов κ легкой цепи предотвратить экспрессию λ легкой цепи мыши. Отношение числа клеток, экспрессирующих гуманизированную κ легкую цепь, к числу клеток, экспрессирующих λ легкую цепь мыши, было относительно неизменным у мышей VELOCIMMUNE® по сравнению с мышами дикого типа, независимо от числа генных сегментов Vκ человека, вставленных на локус κ легкой цепи (фиг. 6, третий ряд сверху). Кроме того, не наблюдалось увеличение числа дважды положительных (κ и λ) клеток, указывая на то, что продуктивная рекомбинация в гибридных локусах κ легкой цепи приводит к соответствующему подавлению рекомбинации локусов λ легкой цепи мыши. В отличие от этого, мыши, содержащие интегрированные случайным образом трансгены κ легкой цепи с инактивированными локусами κ легкой цепи мыши - но локусами λ легкой цепи мыши дикого типа - проявляют сильно увеличенные соотношения λ/κ (Jakobovits, 1998), косвенно указывая на то, что введенные трансгены κ легкой цепи не функционируют правильным образом у таких мышей. Это дополнительно демонстрирует другой функциональный результат, наблюдаемый в иммуноглобулинах, произведенных мышами VELOCIMMUNE® по сравнению с таковыми, произведенными мышами, полученными с помощью "генного нокаута вместе с трансгенным подходом".
Развитие В-клеток. Поскольку популяции зрелых В-клеток у мышей VELOCIMMUNE® сходны с таковыми у мышей дикого типа (описано выше), возможно, что дефекты в ранней дифференциации В-клеток компенсируются путем распространения популяций зрелых В-клеток. Различные стадии дифференциации В-клеток исследовали путем анализа популяций В-клеток с использованием проточной цитометрии. На таблице 6 представлено отношение фракции клеток в каждой В-клеточной родословной, определенной с помощью FACs, с использованием специфических маркеров клеточной поверхности, у мышей VELOCIMMUNE® по сравнению с однопометными животными дикого типа.
Развитие ранних В-клеток происходит в костном мозге, и различные стадии дифференциации В-клеток характеризуются изменениями в типах и уровнях экспрессии маркеров клеточной поверхности. Эти различия в поверхностной экспрессии коррелируют с молекулярными изменениями, происходящими на локусах иммуноглобулина внутри клетки. Для перехода от про-В к пре-В-клетке необходима успешная реаранжировка и экспрессия функционального белка тяжелой цепи, наряду с тем, что переход от пре-В к стадии зрелых В-клеток регулируется правильной реаранжировкой и экспрессией κ или λ легкой цепи. Таким образом, неэффективный переход между стадиями В-клеточной дифференциации можно обнаружить с помощью изменений в относительных популяциях В-клеток на данной стадии.
Не наблюдалось никаких значительных дефектов в В-клеточной дифференциации у любой из мышей VELOCIMMUNE®. По-видимому, введение генных сегментов тяжелой цепи человека не оказывает воздействия на переход от про-В к пре-В, и введение генных сегментов κ легкой цепи человека не оказывает воздействия на переход от пре-В к В-клеткам у мышей VELOCIMMUNE®. Это демонстрирует, что "обратные химерные" молекулы иммуноглобулина, содержащие вариабельные области человека и константные области мыши, функционируют нормально в контексте передачи сигналов В-клетками и корецепторных молекул, приводя к подходящей В-клеточной дифференциации в мышином окружении. В отличие от этого, баланс между различными популяциями в ходе В-клеточной дифференциации нарушается до определенной степени у мышей, которые содержат интегрированный случайным образом трансгены иммуноглобулина и инактивированные эндогенные локусы тяжелой цепи или κ легкой цепи (Green and Jakobovits, 1998).
Пример 4. Репертуар вариабельных генов у мышей с гуманизированным иммуноглобулином
Частоту использования вариабельных генных сегментов человека в репертуаре гуманизированных антител мышей VELOCIMMUNE® анализировали с помощью полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР) вариабельных областей человека из множественных источников, включающих в себя спленоциты и клетки гибридомы. Определяли последовательность вариабельной области, частота использования генного сегмента, соматическая гипермутация и множественность сегментов J реаранжированных генных сегментов вариабельной области.
Кратко, общую РНК экстрагировали из 1×107 - 2×107 спленоцитов или приблизительно 104-105 гибридомных клеток с использованием TRIZOL™ (Invitrogen) или мининабора Qiagen RNEASY™ (Qiagen) и примировали с помощью специфических маркеров константной области мыши с использованием SUPERSCRIPT™ III системы одностадийной ОТ-ПЦР (Invitrogen). Реакции проводили с 2-5 мкл РНК из каждого образца с использованием вышеупомянутых 3' специфических маркеров константной области, спаренных с объединенными лидерными праймерами для каждого семейства вариабельных областей человека как для тяжелой цепи, так и для κ легкой цепи, отдельно. Объемы реагентов и праймеров и условия ОТ-ПЦР/ПЦР обеспечивали согласно инструкциям производителя. Последовательности праймеров были основаны на множественных источниках (Wang, X. and Stollar, B.D. (2000) Human immunoglobulin variable region gene analysis by single cell RT-PCR, J Immunol Methods 244:217-225; наборы Ig-праймеров, Novagen). В соответствующих случаях вложенные вторичные ПЦР реакции проводили с объединенными специфическими в отношении семейства каркасными праймерами и таким же 3' специфическим праймером константной области иммуноглобулина мыши, используемым в первичной реакции. Аликвоты (5 мкл) из каждой реакции анализировали с помощью электрофореза в агарозном геле и продукты реакции очищали от агарозы с использованием набора для экстракции из геля MONTAGE™ (Millipore). Очищенные продукты клонировали с использованием ТОРО™ ТА клонирующей системы (Invitrogen) и трансформировали в клетки DH10β E. coli путем электропорации. Отдельные клоны выбирали из каждой реакции трансформации и выращивали в 2 мл бульонных культур Лурия-Бертани с селекцией по чувствительности к антибиотику в течение ночи при 37°С. Плазмидную ДНК очищали от бактериальных культур с помощью основанного на использовании набора подхода (Qiagen).
Частота использования вариабельных генов иммуноглобулина. Плазмидную ДНК клонов как тяжелой цепи, так и κ легкой цепи секвенировали или с Т7, или с М13 обратными праймерами на генетическом анализаторе ABI 3100 (Applied Biosystems). Необработанные данные о последовательностях вносили в SEQUENCHER™ (версия 4.5, Gene Codes). Каждую последовательность собирали в контиги и выравнивали с последовательностями иммуноглобулина человека с использованием IMGT V-Quest (Brochet, X, Lefranc, М.Р., and Giudicelli, V. (2008). IMGT/V-QUEST: the highly customized and integrated system for IG and TR standardized V-J and V-D-J sequence analysis. Nucleic Acids Res 36, W503-508) поисковой функции для определения частоты использования сегментов VH, DH, JH и Vκ, Jκ человека. Последовательности сравнивали с зародышевыми последовательностями для анализа соматической гипермутации и рекомбинации участков соединения.
Мышей получали из ES клеток, содержащих начальную модификацию тяжелой цепи (гибридный аллель 3hVH-CRE, нижняя часть фиг. 2А) с помощью RAG комплементации (Chen, J. et al. (1993) RAG-2-deficient blastocyst complementation: an assay of gene function in lymphocyte development, Proc Natl Acad Sci USA 90:4528-4532), и кДНК получали из РНК спленоцита. кДНК амплифицировали с использованием наборов праймеров (описанных выше), специфических к предсказанной мРНК химерной тяжелой цепи, которая будет возникать путем V(D)J рекомбинации в пределах вставленных генных сегментов человек и последующего сплайсинга с константными доменами либо IgM, либо IgG мыши. Последовательности, происходящие из этих клонов кДНК (не показаны), демонстрировали, что правильная V(D)J рекомбинация происходила в пределах генных последовательностей вариабельной области человека, что реаранжированные генные сегменты V(D)J человека правильно сплайсировались в рамке считывания с константными доменами мыши и что произошла рекомбинация переключения класса. Проводили дополнительный анализ последовательности продуктов мРНК последующих гибридных локусов иммуноглобулина
В сходном эксперименте В-клетки из неиммунизированных мышей дикого типа и мышей VELOCIMMUNE® разделяли с помощью проточной цитометрии на основании поверхностной экспрессии В220 и IgM или IgG. Клетки В220+ IgM+ или поверхностный IgG+ (sIgG+) объединяли и получали последовательности VH и Vκ на основании ОТ-ПЦР амплификации и клонирования (описано выше). Регистрировали частоту использования репрезентативных генов в наборе амплифицированных с помощью ОТ-ПЦР кДНК из неиммунизированных мышей VELOCIMMUNE® 1 (таблица 7) и мышей VELOCIMMUNE® 3 (таблица 8) (* дефектная RSS;  отсутствие или псевдоген).
отсутствие или псевдоген).
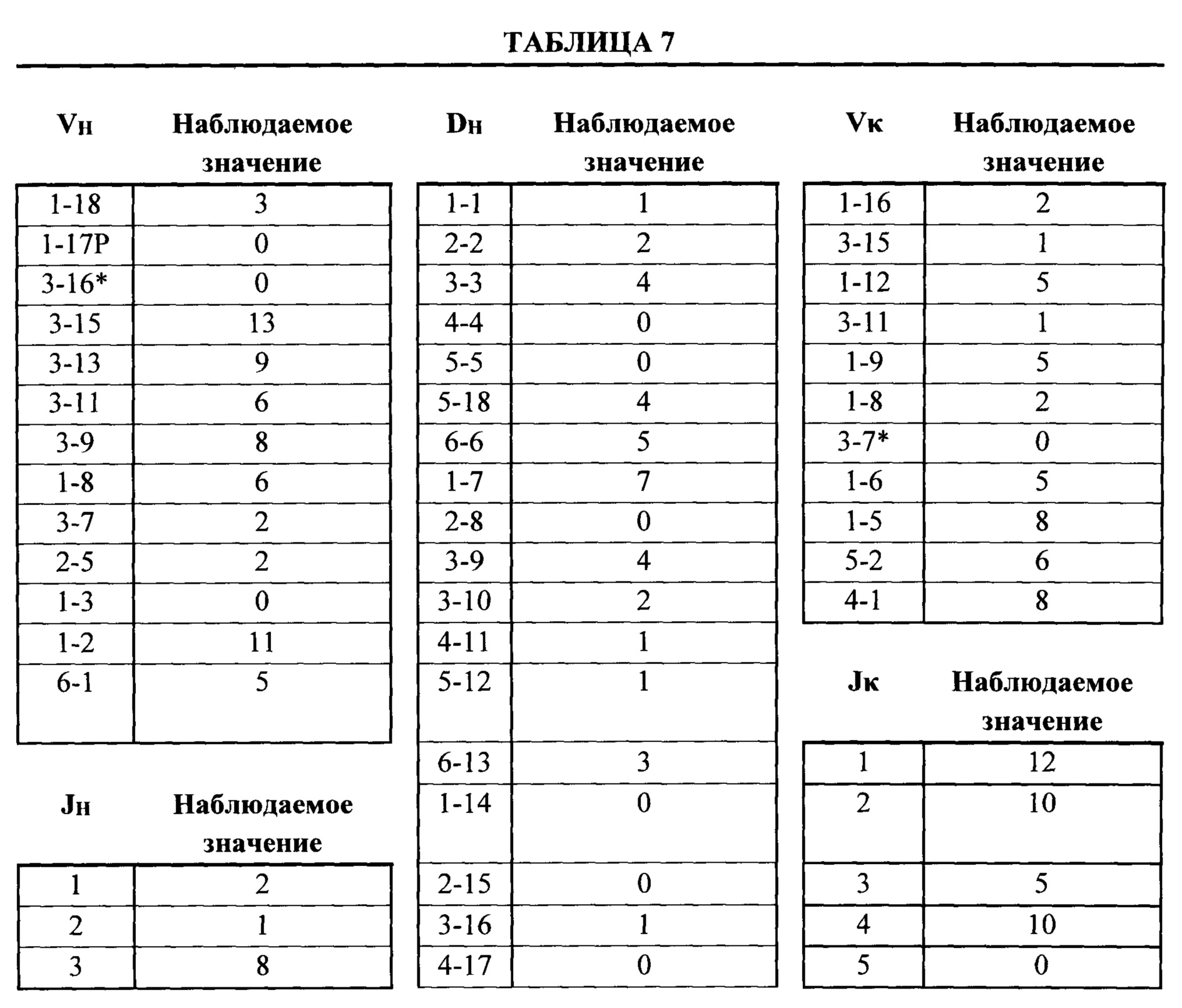
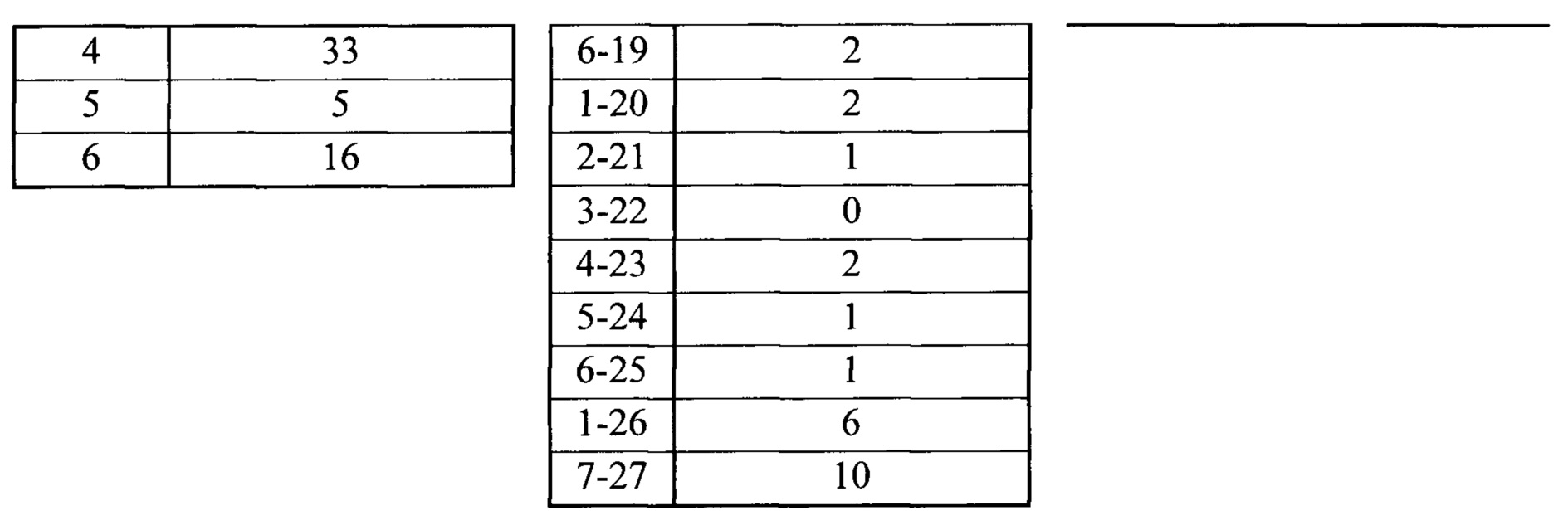
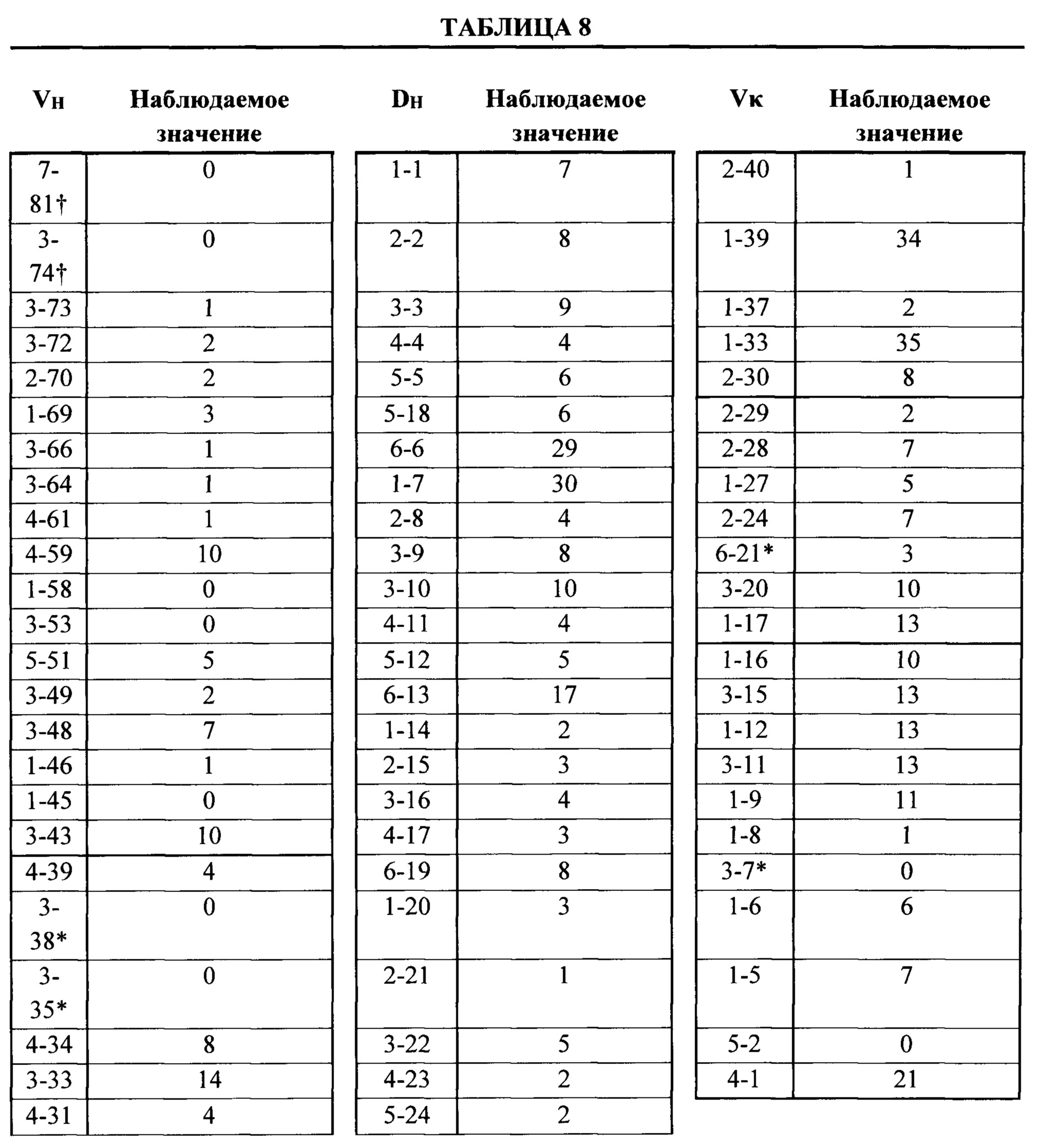
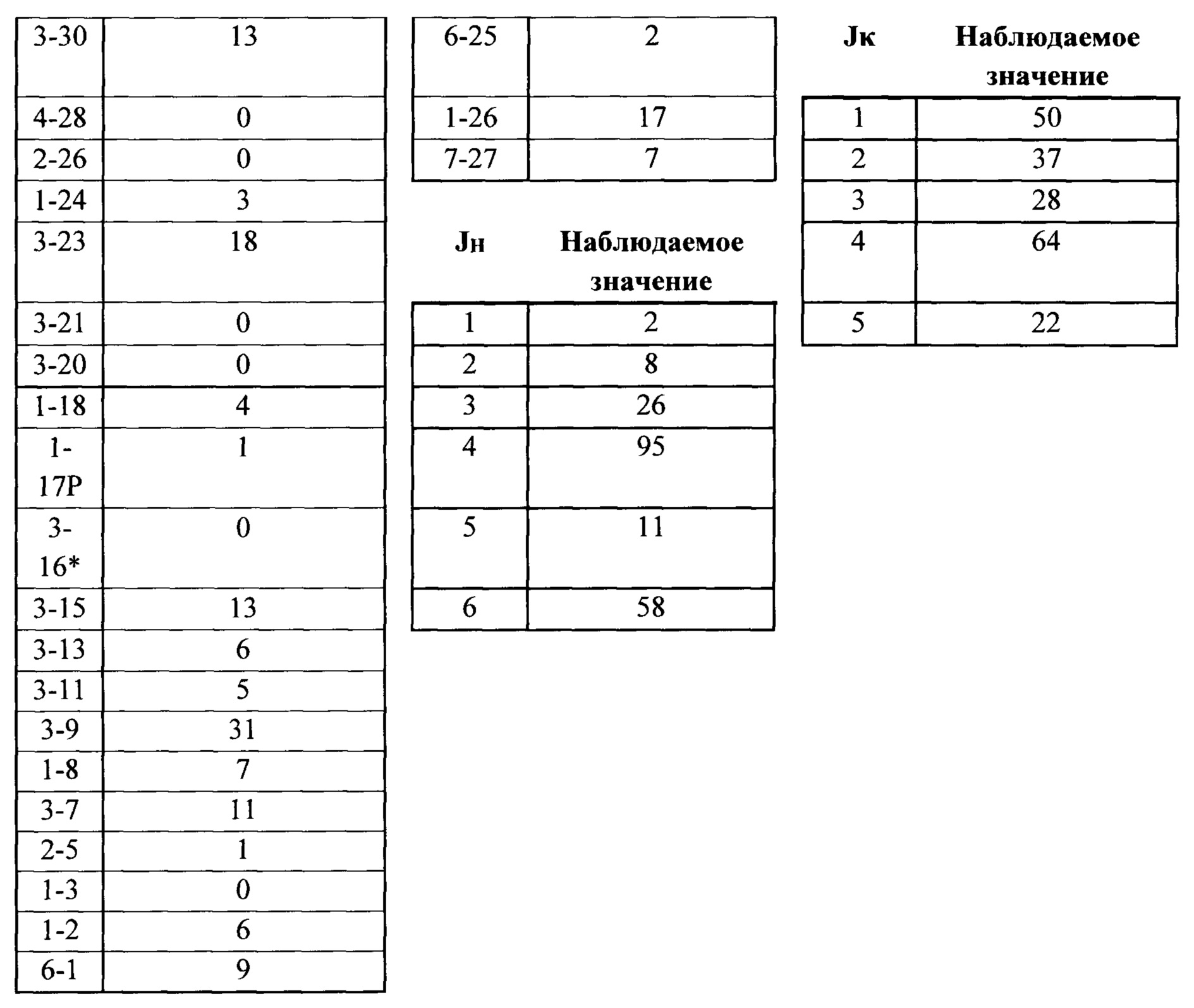
Как показано в таблицах 7 и 8, используются почти все функциональные генные сегменты VH, DH, JH, Vκ и Jκ человека. Из функциональных вариабельных генных сегментов, описанных, но не обнаруженных у мышей VELOCIMMUNE® в настоящем эксперименте, сообщалось, что некоторые содержат дефектные сигнальные последовательности рекомбинации (RSS) и, таким образом, как предполагают, не будут экспрессироваться (Feeney, A.J. (2000) Factors that influence formation of В cell repertoire. Immunol Res 21:195-202). Анализ некоторых других наборов последовательностей иммуноглобулина из различных мышей VELOCIMMUNE®, выделенных как из нативных, так иммунизированных репертуаров, показал использование этих генных сегментов, хотя и с более низкими показателями частоты (данные не показаны). Сводные данные о частоте использования генов показали, что все функциональные генные сегменты VH, DH, JH, Vκ и Jκ человека, содержащиеся у мышей VELOCIMMUNE®, наблюдались как в нативных, так и в иммунизированных репертуарах (данные не показаны). Хотя генный сегмент VH7-81 человека определили в анализе последовательностей локуса тяжелой цепи человека (Matsuda, F. et al. (1998) The complete nucleotide sequence of the human immunoglobulin heavy chain variable region locus, J Exp Med 188:2151-2162), он не присутствует у мышей VELOCIMMUNE®, что подтверждается путем повторного секвенирования полного генома мыши VELOCIMMUNE® 3.
Известно, что последовательности тяжелых и легких цепей антител демонстрируют исключительную вариабельность, особенно в коротких полипептидных сегментах в пределах реаранжированного вариабельного домена. Эти области, известные как гипервариабельные области или определяющие комплементарность области (CDR) образуют сайт связывания для антигена в структуре молекулы антитела. Промежуточные полипептидные последовательности называются каркасные области (FR). Существуют три CDR (CDR1, CDR2, CDR3) и 4 FR (FR1, FR2, FR3, FR4) как в тяжелых, так и легких цепях. Одна CDR, CDR3, является уникальной в том, что эта CDR образуется путем рекомбинации как генных сегментов VH, DH и JH, так и Vκ и Jκ и создает значительное количество разнообразия репертуаров до того, как встретиться антиген. Это соединение является неточным вследствие как нуклеотидных делеций посредством экзонуклеазной активности, так и не кодируемых матрицей вставок посредством терминальной дезоксинуклеотидилтрансферазы (TdT) и, таким образом, обеспечивает возможность появления новых последовательностей в результате процесса рекомбинации. Хотя FR могут демонстрировать существенную соматическую мутацию вследствие высокой частоты мутирования вариабельной области целиком, вариабельность, тем не менее, не распределена равномерно по вариабельной области. CDR представляют собой сконцентрированные и локализованные области высокой вариабельности на поверхности молекулы антитела, которые обеспечивают связывание антигена. Последовательности тяжелой цепи и легкой цепи выбранных антител из мышей VELOCIMMUNE® около участка соединения CDR3, демонстрирующего множественность сегментов J, показаны на фиг. 7A и 7В, соответственно.
Как показано на фиг. 7A, не кодируемые матрицей нуклеотидные вставки (N-вставки) наблюдаются как на соединении VH-DH, так и DH-JH в антителах из мышей VELOCIMMUNE®, указывая на полноценную функцию TdT с сегментами человека. Концы сегментов VH, DH и JH относительно их зародышевых эквивалентов показывают, что также имела место экзонуклеазная активность. В отличие от локуса тяжелой цепи, реаранжировки κ легкой цепи человека проявляют немного или отсутствие вставок TdT на CDR3, которая сформирована путем рекомбинации сегментов Vκ и Jκ (фиг. 7В). Это предполагают вследствие отсутствия экспрессии TdT у мышей в ходе реаранжировок легкой цепи на переходе от пре-В к В-клетке. Разнообразие, наблюдаемое в CDR3 реаранжированных областей Vκ человека, вводится преимущественно посредством экзонуклеазной активности в ходе события рекомбинации.
Соматическая гипермутация. Дополнительное разнообразие добавляют к вариабельным областям реаранжированных генов иммуноглобулина в ходе реакции в зародышевом центре с помощью процесса, имеющего название соматическая гипермутация. В-клетки, экспрессирующие соматически мутированные вариабельные области, конкурируют с другими В-клетками за доступ к антигену, представленному фоликулярными дендритными клетками. В-клетки с более высокой аффинностью к антигену будут продолжать развиваться и будут подвергаться переключению класса перед выходом на периферию. Таким образом, В-клетки, экспрессирующие переключенные изотипы, как правило, встретились с антигеном и подверглись реакциям в зародышевом центре и будут характеризоваться увеличенными количествами мутаций относительно наивных В-клеток. Более того, предполагают, что последовательности вариабельной области из преимущественно наивных sIgM+ В-клеток будут характеризоваться относительно меньшим количеством мутаций, чем вариабельные последовательности из sIgG+ В-клеток, которые подверглись антигензависимой селекции.
Последовательности из случайных клонов VH или Vκ из sIgM+ или sIgG+ В-клеток из неиммунизированных мышей VELOCIMMUNE® или sIgG+ В-клеток из иммунизированных мышей сравнивали с их зародышевыми вариабельными генными сегментами и комментировали изменения относительно зародышевой последовательности. Полученные нуклеотидные последовательности подвергали трансляции in silico и также комментировали мутации, приводящие к изменениям аминокислот. Данные собирали от всех вариабельных областей и рассчитывали процентное изменение в данном положении (фиг. 8).
Как показано на фиг. 8, вариабельные области тяжелой цепи человека, происходящие из sIgG+ В-клеток из неиммунизированных мышей VELOCIMMUNE®, проявляют намного больше нуклеотидов относительно sIgM+ В-клеток из тех же пулов спленоцитов, и вариабельные области тяжелой цепи, происходящие из иммунизированных мышей, проявляют даже больше изменений. Число изменений увеличивается в определяющих комплементарность областях (CDR) по отношению к каркасным областям, что указывает на антигензависимую селекцию. Соответствующие аминокислотные последовательности из вариабельных областей тяжелой цепи человека также проявляют значительно большие количества мутаций в IgG по сравнению с IgM и даже больше в иммунизированном IgG. Эти мутации вновь оказываются более частыми в CDR по сравнению с каркасными последовательностями, указывая на то, что антитела были антигензависимыми in vivo. Сходное увеличение числа нуклеотидных и аминокислотных мутаций наблюдают в последовательностях Vκ, происходящих из IgG+ В-клеток из иммунизированных мышей.
Частота использования гена и соматическая гипермутация, наблюдаемые у мышей VELOCIMMUNE®, показывают, что по существу все присутствующие генные сегменты способны к реаранжировке для образования полностью функциональных обратных химерных антител у этих мышей. Более того, антитела VELOCIMMUNE® участвуют в полной мере в иммунной системе мыши, подвергаясь аффинной селекции и созреванию для создания полностью зрелых человеческих антител, которые могут эффективно нейтрализовать их целевой антиген. Мыши VELOCIMMUNE® способны развивать устойчивые иммунные ответы на многочисленные классы антигенов, что приводит к использованию широкого диапазона человеческих антител, которые характеризуются высокой аффинностью, а также являются подходящими для терапевтического применения (данные не показаны).
Пример 5. Анализ лимфоидной структуры и сывороточных изотипов
Макроструктуры селезенки, паховых лимфатических узлов, пейеровых бляшек и тимуса тканевых образцов из мышей дикого типа или мышей VELOCIMMUNE®, окрашенные с помощью Н&Е, исследовали с помощью световой микроскопии. Уровни изотипов иммуноглобулина в сыворотке, собранной от мышей дикого типа и мышей VELOCIMMUNE®, анализировали с использованием технологии LUMINEX™.
Структура лимфоидных органов. Структура и функция лимфоидных тканей частично зависит от правильного развития гематопоэтических клеток. Нарушение развития или функции В-клеток могут проявляться в виде изменения в структуре лимфоидных тканей. При анализе окрашенных тканевых срезов не установили никакого значительного различия во внешнем виде вторичных лимфоидных органов между мышами дикого типа и мышами VELOCIMMUNE® (данные не показаны).
Уровни иммуноглобулина в сыворотке. Уровень экспрессии каждого изотипа является сходным у мышей дикого типа и мышей VELOCIMMUNE® (фиг. 9A, 9В и 9С). Это демонстрирует, что гуманизация вариабельных генных сегментов не оказывала какого-либо очевидного неблагоприятного действия на переключение класса или экспрессию и секрецию иммуноглобулина и, следовательно, очевидно сохраняет все эндогенные последовательности мыши, необходимые для этих функций.
Пример 6. Иммунизация и продукция антител у мышей с гуманизированными иммуноглобулинами
Различные варианты мышей VELOCIMMUNE® иммунизировали антигеном для исследования гуморального ответ на сенсибилизацию чужеродным антигеном.
Иммунизация и развитие гибридомы. Мышей VELOCIMMUNE® и мышей дикого типа можно иммунизировать антигеном в форме белка, ДНК, комбинации ДНК и белка или клеток, экспрессирующих антиген. Животным, как правило, проводят повторную иммунизацию каждые три недели, в общем, в течение двух-трех раз. После каждой повторной иммунизации антигеном образцы сыворотки от каждого животного собирают и анализируют в отношении ответов антигенспецифических антител с помощью определения сывороточного титра. Перед слиянием мыши получали конечный дозу предшествующей слиянию повторной иммунизации 5 мкг белка или ДНК, при необходимости, посредством интраперитонеальной и/или внутривенной инъекций. Спленоциты собирают и проводят их слияние с Ag8.653 миеломными клетками в камере электрослияния согласно рекомендуемому производителем протоколу (Cyto Pulse Sciences Inc., Глен-Бурни, Мериленд). Через десять дней культивации гибридомы подвергают скринингу относительно антигенной специфичности с использованием анализа ELISA (Harlow, Е. and Lane, D. (1988) Antibodies: A Laboratory Manual. Cold Spring Harbor Press, New York). Альтернативно, антигенспецифические В-клетки выделяют непосредственно из иммунизированных мышей VELOCIMMUNE® и подвергают скринингу с использованием стандартных техник, включающих в себя описанные в настоящем документе, для получения человеческих антител, специфических к представляющему интерес антигену.
Определения сывороточного титра. Для мониторинга ответа сыворотки животного на антиген образцы сыворотки собирают через приблизительно 10 дней после каждой повторной иммунизации и титры определяют с использованием антиген-специфического анализа ELISA. Кратко, Nunc MAXISORP™ 96-луночные планшеты покрывают 2 мкг/мл антигена в течение ночи при 4°С и блокируют с помощью бычьего сывороточного альбумина (Sigma, Сент-Луис, Миссури). Обеспечивают связывание образцов сыворотки в серийных 3-кратных разведениях с планшетами в течение одного часа при комнатной температуре. Планшеты затем отмывают с помощью PBS, содержащего 0,05% Tween-20 и связанный IgG определяют с использованием конъюгированного с HRP козьего антитела к Fc мыши (Jackson Immuno Research Laboratories, Inc., Вест Гров, Пенсильвания) для общего титра IgG, или меченных биотином специфических к изотипу или специфических к легким цепям поликлональных антител (SouthernBiotech Inc.) для специфических к изотипу титров, соответственно. Для меченных биотином антител после отмывки планшета добавляют конъюгированный с HRP стрептавидин (Pierce, Рокфорд, Иллинойс). Все планшеты проявляют с использованием таких колориметрических субстратов, как BD OPTEIA™ (BD Biosciences Pharmingen, Сан-Диего, Калифорния). После остановки реакции с помощью 1 М фосфорной кислоты, регистрируют показатели оптического поглощения при 450 нм и данные анализируют с использованием программного обеспечения PRISM™ от Graph Pad. Разведения, необходимые для получения сигнала, превышающего в два раза фоновый уровень, определяют как титр.
Согласно одному эксперименту мышей VELOCIMMUNE® иммунизировали рецептором интерлейкина-6 человека (hIL-6R). Репрезентативный набор сывороточных титров для мышей VELOCIMMUNE® и мышей дикого типа, иммунизированных hIL-6R, показан на фиг. 10А и 10В.
Мыши VELOCIMMUNE® и мыши дикого типа развивали сильные ответы в отношении IL-6R со сходными диапазонами титров (фиг. 10A). Некоторые мыши из когорт мышей VELOCIMMUNE® и мышей дикого типа достигали максимального ответа после оной иммунизации антигена. Эти результаты показывают, что сила иммунного ответа и кинетические параметры в отношении этого антигена были сходными у мышей VELOCIMMUNE® и мышей дикого типа. Эти ответы антигенспецифических антител дополнительно анализировали для исследования конкретных изотипов антигенспецифических антител, обнаруженных в сыворотках. Как группы мышей VELOCIMMUNE®, так и группы дикого типа преимущественно развивают ответ IgG1 (фиг. 10В), указывая на то, что переключение класса в ходе гуморального ответа является сходным у мышей каждого типа.
Определение аффинности связывания антитела с антигеном в растворе. Основанный на ELISA анализ конкуренции в растворе, как правило, разрабатывают для определения аффинность связывания антитела с антигеном.
Кратко, антитела в кондиционированной среде предварительно смешивают с серийными разведениями антигенного белка в диапазоне от 0-10 мг/мл. Растворы смеси антитела и антигена затем инкубируют в течение двух-четырех часов при комнатной температуре для достижения равновесных состояний связывания. Количества свободного антитела в смесях затем измеряют с использованием количественного сэндвич-анализа ELISA. 96-луночные планшеты MAXISORB™ (VWR, Вест-Честер, Пенсильвания) покрывают 1 мкг/мл антигенного белка в растворе PBS в течение ночи при 4°С с последующим BSA неспецифическим блокированием. Растворы смеси антител с антигенами затем переносят на эти планшеты с последующей часовой инкубацией. Планшеты затем отмывают буфером отмывки и связанные с планшетом антитела обнаруживают с помощью реагента конъюгированного с HRP козьего поликлонального антитела к IgG мыши (Jackson Immuno Research Lab) и проявляли с использованием таких колориметрических субстратов, как BD OPTEIA™ (BD Biosciences Pharmingen, Сан-Диего, Калифорния). После остановки реакции с помощью 1 М фосфорной кислоты, регистрируют показатели оптического поглощения при 450 нм и данные анализируют с использованием программного обеспечения PRISM™ от Graph Pad. Зависимость сигналов от концентраций антигена в растворе анализируют с помощью анализа согласия в отношении 4 параметров и выражали как IC50, концентрация антигена, необходимая для достижения 50% снижения сигнала от образцов антител без присутствия антигена в растворе.
Согласно одному эксперименту мышей VELOCIMMUNE® иммунизировали с помощью hIL-6R (как описано выше). На фиг. 11А и 11В показан репрезентативный набор измерений аффинности для антител к hIL6R из мышей VELOCIMMUNE® и мышей дикого типа.
После получения иммунизированными мышами третьей повторной иммунизации антигеном сывороточные титры определяют с помощью ELISA. Спленоциты выделяют из выбранных когорт мышей дикого типа и мышей VELOCIMMUNE® и проводили слияние с Ag8.653 миеломными клетками для образования гибридом и выращивали при условиях селекции (как описано выше). Обнаружили, что из 671 образованных анти-IL-6R гибридом 236 экспрессируют антиген-специфические антитела. Среды, собранные из положительных в отношении антигена лунок, использовали для определения аффинности антител в отношении связывания с антигеном с использованием анализа конкуренции в растворе ELISA. Антитела, полученные из мышей VELOCIMMUNE®, проявляют широкий диапазон аффинности в связывании с антигеном в растворе (фиг. 11А). Более того, обнаружили, что 49 из 236 анти-IL-6R гибридом препятствуют связыванию IL-6 с рецептором в биологическом анализе in vitro (данные не показаны). Более того, эти 49 анти-IL-6R блокирующие антитела проявляли диапазон высоких аффинностей в растворе, сходный с таковым у блокирующих антител, полученных в параллельной иммунизации мышей дикого типа (фиг. 11В)
Пример 7. Конструкция нацеливающего вектора ADAM6 мыши
Нацеливающий вектор для вставки генов ADAM6a и ADAM6b мыши в гуманизированный локус тяжелой цепи конструировали с использованием технология генной инженерии VELOCIGENE® (ранее) для модификации бактериальной искусственной хромосомы (ВАС) 929d24, полученной от Dr. Fred Alt (Гарвардский университет). ДНК 929d24 ВАС конструировали так, чтобы она содержала геномные фрагменты, содержащие гены ADAM6a и ADAM6b мыши и кассету гигромицина для направленной делеции псевдогена ADAM6 человека (hADAM6Ψ), расположенного между генными сегментами VH1-2 и VH6-1 человека гуманизированного локуса тяжелой цепи (фиг. 12).
Во-первых, геномный фрагмент, содержащий ген ADAM6b мыши, ~800 п.н. последовательности против хода транскрипции (5') и ~4800 п.н. последовательности по ходу транскрипции (3'), субклонировали из клона 929d24 ВАС. Второй геномный фрагмент, содержащий ген ADAM6a мыши, ~300 п.н. последовательности против хода транскрипции (5') и ~3400 п.н. последовательности по ходу транскрипции (3'), отдельно субклонировали из клона 929d24 ВАС. Два геномных фрагмента, содержащие гены ADAM6b и ADAM6a мыши, лигировали с кассетой гигромицина, фланкированной Frt сайтами рекомбинации для создания нацеливающего вектора (нацеливающий вектор ADAM6 мыши, фигура 20; SEQ ID NO: 3). Различные сайты рестрикционных ферментов конструировали на 5' конце нацеливающего вектора после гена ADAM6b мыши и на 3' конце после гена ADAM6a мыши (фиг. 12, снизу) для лигирования в гуманизированный локус тяжелой цепи.
Отдельную модификацию проводили в отношении ВАС - клона, содержащего замещение локуса тяжелой цепи мыши локусом тяжелой цепи человек, содержащим псевдоген ADAM6 человек, расположенный между генными сегментами VH1-2 и VH6-1 человека гуманизированного локуса для последующего лигирования нацеливающего вектора ADAM6 мыши (фиг. 13).
Кратко, кассету неомицина, фланкированную сайтами рекомбинации loxP, конструировали так, чтобы она содержала гомологичные плечи, содержащие геномную последовательность человека в положениях 3' от генного сегмента VH1-2 человека (5' по отношению к hADAM6Ψ) и 5' от генного сегмента VH6-1 человека (3' по отношению к hADAM6Ψ; смотрите среднюю часть фиг. 13). Расположение сайта вставки этого нацеливающего конструкта находилось приблизительно 1,3 т.п.н. 5' и ~350 п.н. 3' от псевдогена ADAM6 человек. Нацеливающий конструкт также содержал такие же сайты рестрикции, как нацеливающий вектор ADAM6 мыши для обеспечения последующего ВАС - лигирования между модифицированными ВАС - клоном, содержащим делецию псевдогена ADAM6 человека и нацеливающего вектора ADAM6 мыши.
После обработки ВАС - ДНК, полученной из обоих конструктов, геномные фрагменты лигировали вместе для конструирования сконструированного ВАС - клона, содержащего гуманизированный локус тяжелой цепи, содержащий эктопически расположенную геномную последовательность, содержащую нуклеотидные последовательности ADAM6a и ADAM6b мыши. Конечный нацеливающий конструкт для делеции гена ADAM6 человека в пределах гуманизированного локуса тяжелой цепи и вставки последовательностей ADAM6a и ADAM6b мыши в ES клетки, содержащие, в направлении 5'-3', 5' геномный фрагмент, содержащий ~13 т.п.н. геномной последовательности человека 3' от генного сегмента VH1-2 человек, ~800 п.н. геномной последовательности мыши ниже по ходу транскрипции от гена ADAM6b мыши, ген ADAM6b мыши, ~4800 п.н. геномной последовательности выше против хода транскрипции от гена ADAM6b мыши, 5' сайт Frt, кассету гигромицина, сайт 3' Frt, ~300 п.н. геномной последовательности мыши ниже по ходу транскрипции от гена ADAM6a мыши, ген ADAM6a мыши, ~3400 п.н. геномной последовательности мыши выше против хода транскрипции от гена ADAM6a мыши и 3' геномный фрагмент, содержащий ~30 т.п.н. геномной последовательности человека 5' от генного сегмента VH6-1 человека (нижняя часть фиг. 13).
Сконструированный ВАС - клон (описанный выше) использовали для электропорации ES клеток мыши, которые содержали гуманизированный локус тяжелой цепи для создания модифицированных ES клеток, содержащих геномную последовательность мыши, расположенную эктопически, которая содержит последовательности ADAM6a и ADAM6b мыши в пределах гуманизированного локуса тяжелой цепи. Положительные ES клетки, содержащие эктопический геномный фрагмент мыши в пределах гуманизированного локуса тяжелой цепи определяли с помощью анализа количественной ПЦР с использованием зондов TAQMAN™ (Lie, Y.S. and Petropoulos, C.J. (1998) Advances in quantitative PCR technology: 5'nuclease assays. Curr Opin Biotechnol 9(1):43-48). Вышележащие и нижележащие области за пределами модифицированной части гуманизированного локуса тяжелой цепи подтверждали с помощью ПЦР с использованием праймеров и зондов, расположенных в пределах модифицированной области для подтверждения присутствия эктопической геномной последовательности мыши в пределах гуманизированного локуса тяжелой цепи, а также кассеты гигромицина. Нуклеотидная последовательность в вышележащей точке вставки включала в себя следующее, что показывает геномную последовательность тяжелой цепи человека, расположенная выше против хода транскрипции от точки вставки, и сайт рестрикционный I-Ceu I (содержащийся в скобках ниже), смежно соединенные с геномной последовательностью мыши, присутствующей в точке вставки: (CCAGCTTCAT TAGTAATCGT TCATCTGTGG TAAAAAGGCA GGATTTGAAG CGATGGAAGA TGGGAGTACG GGGCGTTGGA AGACAAAGTG CCACACAGCG CAGCCTTCGT CTAGACCCCC GGGCTAACTA TAACGGTCCT AAGGTAGCGA G) GGGATGACAG ATTCTCTGTT CAGTGCACTC AGGGTCTGCC TCCACGAGAA TCACCATGCC CTTTCTCAAG ACTGTGTTCT GTGCAGTGCC CTGTCAGTGG (SEQ ID NO: 4). Нуклеотидная последовательность в нижележащей точке вставки на 3' конце нацеленной области включала в себя следующее, что показывает геномную последовательность мыши и сайт рестрикции PI-Sce I (содержащийся в скобка ниже), смежно соединенные с геномной последовательностью тяжелой цепи человека ниже по ходу транскрипции от точки вставки: (AGGGGTCGAG GGGGAATTTT ACAAAGAACA AAGAAGCGGG CATCTGCTGA CATGAGGGCC GAAGTCAGGC TCCAGGCAGC GGGAGCTCCA CCGCGGTGGC GCCATTTCAT TACCTCTTTC TCCGCACCCG ACATAGATAAAGCTT) АТСССССАСС AAGCAAATCC CCCTACCTGG GGCCGAGCTT CCCGTATGTG GGAAAATGAA TCCCTGAGGT CGATTGCTGC ATGCAATGAA ATTCAACTAG (SEQ ID NO: 5).
Описанные выше нацеленные ES клетки использовали в качестве донорных ES клеток и вводили в эмбрион мыши на стадии 8 клеток с помощью способа генной инженерии мыши VELOCIMOUSE® (смотрите, например, патенты США №№76598442, 7576259, 7294754). Мышей, несущих гуманизированный локус тяжелой цепи, содержащий эктопическую геномную последовательность мыши, содержащую последовательности ADAM6a и ADAM6b мыши, определяли путем генотипирования с использованием модификации анализа аллелей (Valenzuela et al., 2003), в котором обнаруживали присутствие генов ADAM6a и ADAM6b мыши в гуманизированном локусе тяжелой цепи.
Мышей, несущих гуманизированный локус тяжелой цепи, который содержит гены ADAM6a и ADAM6b мыши, скрещивали с FLPe делеторным штаммом мышей (смотрите, например,  , C.I. et al. (2000) High-efficiency deleter mice show that FLPe is an alternative to Cre-loxP. Nature Genetics 25:139-140) для удаления любой фланкированной Frt кассеты гигромицина, введенной с помощью нацеливающего вектора, которые е удаляют, например, на стадии ES клетки или в эмбрионе. Необязательно, кассету гигромицина оставляют у мышей.
, C.I. et al. (2000) High-efficiency deleter mice show that FLPe is an alternative to Cre-loxP. Nature Genetics 25:139-140) для удаления любой фланкированной Frt кассеты гигромицина, введенной с помощью нацеливающего вектора, которые е удаляют, например, на стадии ES клетки или в эмбрионе. Необязательно, кассету гигромицина оставляют у мышей.
Детенышей генотипируют и детеныша, гетерозиготного в отношении гуманизированного локуса тяжелой цепи, содержащего эктопический геномный фрагмент мыши, который содержит последовательности ADAM6a и ADAM6b мыши, выбирают для определения характеристик экспрессии и фертильности гена ADAM6 мыши.
Пример 8. Определение хараткеристик мышей с восстановленным ADAM6
Проточная цитометрия. Трех мышей в возрасте 25 недель, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и κ легкой цепи человека (Н/κ), и трех мышей в возрасте 18-20 недель, гомозиготных в отношении тяжелой цепи человека и κ легкой цепи человека, содержащих эктопический геномный фрагмент мыши, кодирующий гены ADAM6a и ADAM6b мыши в обоих аллелях локуса тяжелой цепи человека (Н/κ-A6), умерщвляли для определения и анализа клеточных популяций лимфоцитов с помощью FACs на BD LSR II системе (BD Bioscience). Лимфоциты выделяли путем гейтирования в отношении специфических клеточных родословных и анализировали в отношении прохождения через различные стадии развития В-клеток. Собранные от животных ткани предусматривали кровь, селезенку и костный мозг. Кровь собирали в пробирки BD microtainer с EDTA (BD Biosciences). Костный мозг собирали из бедренных костей с помощью промывки полной средой RPMI, дополненной фетальной телячьей сывороткой, пируватом натрия, HEPES, 2-меркаптоэтанолом, заменимыми аминокислотами и гентамицином. Эритроциты из препаратов крови, селезенки и костного мозга лизировали с помощью лизирующего буфера на основе хлорида аммония (например, лизирующий буфер ACK) с последующей отмывкой полной средой RPMI.
Для окрашивания клеточных популяций 1×106 клеток из различных источников ткани инкубировали с антителом к CD16/CD32 мыши (2,4G2, BD Biosciences) на льду в течение 10 минут с последующим мечением одним или комбинацией следующих коктейлей антител в течение 30 мин на льду.
Костный мозг: антитело к FITC-CD43 мыши (1В11, BioLegend), PE-ckit (2В8, BioLegend), РеСу7-IgM (II/41, eBioscience), PerCP-Cу5,5-IgD (11-26c,2a, BioLegend), APC-eFluor780-B220 (RA3-6B2, eBioscience), A700-CD19 (1D3, BD Biosciences).
Периферическая кровь и селезенка: антитело к FITC-κ мыши (187.1, BD Biosciences), РЕ-λ (RML-42, BioLegend), РеСу7-IgM (II/41, eBioscience), PerCP-Cу5.5-IgD (11-26с.2а, BioLegend), APC-CD3 (145-2С11, BD), A700-CD19 (1D3, BD), APC-eFluor780-B220 (RA3-6B2, eBioscience). После инкубация с мечеными антителами клетки отмывали и фиксировали в 2% формальдегиде. Сбор данных проводили на проточном цитометре LSRII и анализировали с помощью FlowJo. Результаты от репрезентативной Н/κ и Н/κ-А6 мыши показаны на фигурах 14-18.
Результаты показывают, что В-клетки Н/κ-А6 мышей проходят через стадии развития В-клеток аналогично Н/κ мышам в костном мозге и периферических компартментах, и показывают нормальные паттерны созревания, как только они поступают на периферию. Н/κ-А6 мыши демонстрировали увеличенную CD43intCD19+ клеточную популяцию по сравнению с Н/κ мышами (фиг. 16В). Это может указывать на ускоренную экспрессию IgM из гуманизированного локуса тяжелой цепи, содержащего эктопический геномный фрагмент мыши, содержащий последовательности ADAM6a и ADAM6b мыши у Н/κ-А6 мышей. На периферии В- и Т-клеточные популяции Н/κ-А6 мышей оказываются нормальными и сходными с Н/κ мышами.
Морфология семенников и определение характеристик сперматозоидов. Для определения того, является ли стерильность у мышей, характеризующихся гуманизированными вариабельными локусами тяжелой цепи иммуноглобулина вследствие нарушений семенников и/или продукции сперматозоидов, исследовали морфологию яичек и содержание сперматозоидов в придатке семенника.
Кратко, семенники от двух групп из пяти мышей на группу (группа 1: мыши, гомозиготные в отношении вариабельных генных локусов тяжелой и κ легкой цепи человека, mADAM6-/-; группа 2: мыши, гетерозиготная в отношении вариабельных генных локусов тяжелой цепи человека и гомозиготные в отношении вариабельных генных локусовκ легкой цепи, mADAM6+/-) вырезали с интактным придатком семенника и взвешивали. Образцы затем фиксировали, погружали в парафин, делали срезы и окрашивали с помощью гематоксилинового и эозинового (НЕ) красителя. Срезы семенника (2 семенника от каждой мыши, общим количеством 20) исследовали в отношении нарушений в морфологии и данных о продукции сперматозоидов, тогда как срезы придатка семенника исследовали в отношении присутствия сперматозоидов.
Согласно настоящему эксперименту не наблюдали различий в весе или морфологии семенников между mADAM6-/- мышами и mADAM6+/- мышами. Сперму наблюдали во всех генотипах, как в семенниках, так и в придатке семенника. Эти результаты доказывают, что отсутствие генов ADAM6a и ADAM6b мыши не приводит к обнаруживаемым изменениям в морфологии семенника, и что сперматозоиды производятся у мышей в присутствии и при отсутствии этих двух генов. Нарушения в фертильности самцов ADAM6-/- мышей, следовательно, вероятно, не обусловлены низкой продукцией сперматозоидов.
Подвижность и миграция сперматозоидов. Мыши, у которых отсутствуют другие представители семейства генов ADAM, являются стерильными вследствие нарушений в подвижности и миграции сперматозоидов. Миграцию сперматозоидов определяют как способность спермы проходить от матки в яйцевод, и в норме необходима для оплодотворения у мышей. Для определения того, влияет ли делеция мышиных ADAM6a и ADAM6b на этот процесс, миграцию сперматозоидов оценивали у mADAM6-/- мышей. Также исследовали подвижность сперматозоидов.
Кратко, сперму получали из семенников (1) мышей, гетерозиготных в отношении вариабельных генных локусов тяжелой цепи человек и гомозиготных в отношении вариабельных генных локусов κ легкой цепи человека (ADAM6+/-); (2) мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и гомозиготных в отношении вариабельных генных локусов κ легкой цепи человека (ADAM6-/-); (3) мышей, гомозиготных в отношении вариабельных генных локусов тяжелой цепи человека и гомозиготных в отношении κ легкой цепи дикого типа (ADAM6-/-mκ); и, (4) С57 BL/6 мышей дикого типа (WT). Не наблюдали никаких значительных аномалий в количество сперматозоидов или общую подвижность сперматозоидов путем осмотра. Для всех мышей наблюдали дисперсию кумулюса, указывая на то, что каждый образец спермы был способен проникать в клетки кумулюса и связываться с виттелиновым слоем in vitro. Эти результаты показывают, что ADAM6-/- мыши характеризуются спермой, которая способна к проникновению в кумулюс и связыванию с виттелиновым слоем.
Оплодотворение яйцеклеток мыши in vitro (IVF) проводили с использованием спермы от мышей, как описано выше. Несколько меньшее число нерасщепленных эмбрионов присутствовало для ADAM6-/- на следующих день после IVF, а также сниженное количество сперматозоидов, связанных с яйцеклетками. Эти результаты показывают, что сперма от ADAM6-/- мышей, при взаимодействии с яйцеклеткой, способна к проникновению в кумулюс и связыванию с виттелиновым слоем.
Согласно другому эксперименту способность спермы от ADAM6-/- мышей мигрировать из матки и через яйцевод определяли в анализе миграции сперматозоидов.
Кратко, первую группу из пяти подвергнутых суперовуляции самок мышей спаривали с пятью ADAM6-/- самцами. Вторую группу из пяти подвергнутых суперовуляции самок мышей спаривали с пятью ADAM6+/- самцами. Семейные пары подвергали наблюдению в отношении копуляции, и через пять-шесть часов после копуляции матку и прикрепленный яйцевод из всех самок удаляли и промывали для анализа. Промывочные растворы проверяли в отношении яйцеклеток для подтверждения овуляции и подсчета количества сперматозоидов. Миграцию сперматозоидов оценивали двумя различными путями. Согласно первому способу оба яйцевода удаляли из матки, промывали солевым раствором и любые обнаруженные сперматозоиды подсчитывали. Присутствие яйцеклеток также отмечали как доказательство овуляции. Согласно второму способу яйцеводы оставляли прикрепленными к матке и обе ткани фиксировали, погружали в парафин, делали срезы и окрашивали (как описано выше). Срезы исследовали в отношении присутствия сперматозоидов, как в матке, так и в обоих яйцеводах.
Для пяти самок, спаренных с пятью ADAM6-/- самцами, очень небольшое количество спермы обнаружили в промывочном растворе из яйцевода. Промывочные растворы из яйцеводов пяти самок, спаренных с пятью ADAM6+/- самцами, демонстрировали содержание сперматозоидов, приблизительно в 25-30 раз выше (среднее, n=10 яйцеводов), чем присутствующее в промывочных растворах из яйцеводов пяти самок, спаренных с пятью ADAM6-/- самцами.
Получали гистологические срезы матки и яйцевода. Срезы исследовали в отношении присутствия сперматозоидов в матке и яйцеводе (colliculus tubarius). Осмотр гистологических срезов яйцевода и матки выявил, что для самок мышей, спаренных с ADAM6-/- мышами, сперму обнаружили в матке, но не в яйцеводе. Более того, срезы от самок, спаренных с ADAM6-/- мышами выявили, что сперму не обнаружили в маточно-трубном сочленении (UTJ). В срезах от самок, спаренных с ADAM6+/- мышами сперму обнаружили в UTJ и в яйцеводе.
Эти результаты показывают, что мыши, не содержащие гены ADAM6a и ADAM6b, производят сперму, которая проявляет in vivo нарушение миграции. Во всех случаях сперму обнаружили в матке, что указывает на то, что копуляция и высвобождение спермы, вероятно, происходит в норме, но небольшое количество сперматозоидов или их отсутствие наблюдали в яйцеводах после копуляции, что измеряли или с помощью определения количества сперматозоидов, или с помощью гистологического наблюдения. Эти результаты показывают, что мыши с отсутствием генов ADAM6a и ADAM6b производят сперматозоиды, которые проявляют неспособность мигрировать из матки в яйцевод. Это нарушение, вероятно, приводит к стерильности, поскольку сперматозоиды не способны пересечь маточно-трубное сочленение в яйцеводе, где оплодотворяются яйцеклетки. Взятые вместе, все эти результаты сходятся к подтверждению гипотезы о том, что гены ADAM6 мыши способствуют в направлении сперматозоидов с нормальной подвижностью мигрировать из матки, через маточно-трубное сочленение и яйцевод и, таким образом, достигать яйцеклетки для осуществления события оплодотворения. Механизм, которым ADAM6 достигает этого, может быть прямым путем действия белков ADAM6 или посредством координированной экспрессии с другими белками, например, другими белками ADAM, в сперматозоиде, как описано ниже.
Экспрессия семейства генов ADAM. Известно, что комплекс белков ADAM присутствует в виде комплекса на поверхности созревающих сперматозоидов. Мыши, не содержащие других представителей семейства генов ADAM, теряют этот комплекс, как только сперматозоиды созревают, и проявляют снижение множественных белков ADAM в зрелых сперматозоидах. Для определения того, влияет ли отсутствие генов ADAM6a и ADAM6b на другие белки ADAM сходным образом, вестерн-блоты белковых экстрактов из семенника (незрелые сперматозоиды) и придатка семенника (созревающие сперматозоиды) анализировали для определения уровней экспрессии других представителей семейства генов ADAM.
Согласно настоящему эксперименту анализировали белковые экстракты от четырех ADAM6-/- и четырех ADAM6+/- мышей. Результаты показали, что экспрессия ADAM2 и ADAM3 не подверглась воздействию в экстрактах семенников. Тем не менее, как ADAM2, так и ADAM3 были сильно снижены в экстрактах придатка семенника. Это демонстрирует, что отсутствие ADAM6a и ADAM6b в сперматозоидах ADAM6-/- мышей может напрямую воздействовать на экспрессию и, возможно, функцию других белков ADAM, когда сперматозоиды созревают (например, ADAM2 и ADAM3). Это указывает на то, что ADAM6a и ADAM6b являются частью белкового комплекса ADAM на поверхности сперматозоидов, который может быть критически важным для правильной миграции сперматозоидов.
Пример 9. Частота использования вариабельных генов тяжелой цепи человека у мышей с восстановленным ADAM6
Частоту использования выбранных вариабельных генов тяжелой цепи человека определяли у мышей, гомозиготных в отношении вариабельных генных локусов тяжелой и κ легкой цепи человека, либо не содержащих гены ADAM6a и ADAM6b мыши (mADAM6-/-), либо содержащих эктопический геномный фрагмент, кодирующий гены ADAM6a и ADAM6b мыши (ADAM6+/+; смотрите пример 1) с помощью анализа количественной ПЦР с использованием зондов TAQMAN™ (как описано выше).
Кратко, очищали CD19+ В-клетки из селезенок mADAM6-/- и ADAM6+/+ мышей с использованием мышиных CD19 Microbeads (Miltenyi Biotec) и общую РНК очищали с использованием мининабора RNEASY™ (Qiagen). Геномную РНК удаляли с использованием обработки не содержащей РНазу ДНКазой на колонке (Qiagen). Приблизительно 200 нг мРНК обратно транскрибировали в кДНК с использованием набора First Stand cDNA Synthesis (Invitrogen) и затем амплифицировали с использованием универсального мастер-микса для ПЦР TAQMAN™ (Applied Biosystems) с использованием системы обнаружения последовательности ABI 7900 (Applied Biosystems). Относительную экспрессию каждого гена нормировали к κ константной области мыши (mCκ). На таблице 9 представлены комбинации смысловых/антисмысловых/TAQMAN™ MGB зондов, используемых в настоящем эксперименте.

Согласно настоящему эксперименту экспрессию всех четырех генов VH человека наблюдали в анализируемых образцах. Более того, уровни экспрессии были сопоставимыми между mADAM6-/- и ADAM6+/+ мышами. Эти результаты показывают, что все гены VH человека, которые являлись как дистальными по отношению к сайту модификации (VH3-23 и VH1-69), так и проксимальными по отношению к сайту модификации (VH1-2 и VH6-1), были способны рекомбинироваться для образования функционально экспрессируемой тяжелой цепи человека. Эти результаты показывают, что эктопический геномный фрагмент, содержащий последовательности ADAM6a и ADAM6b мыши, вставленные в геномную последовательность тяжелой цепи человека, не оказывают влияния на V(D)J рекомбинацию генных сегментов тяжелой цепи человека в пределах локуса, и эти мыши способны к рекомбинации генных сегментов тяжелой цепи человека нормальным способом для получения функциональных иммуноглобулиновых белков тяжелой цепи.
Пример 10. Делеция локусов легкой цепи иммуноглобулина мыши
Различные нацеливающие конструкты получали с использованием технологии VELOCIGENE® (смотрите, например, патент США №6586251 и Valenzuela et al. (2003) High-throughput engineering of the mouse genome coupled with high-resolution expression analysis, Nature Biotech. 21(6):652-659) для модификации библиотек геномных бактериальных искусственных хромосом (ВАС) мыши для инактивации локусов κ и λ легкой цепи мыши.
Делеция локуса λ легкой цепи мыши. ДНК из клона ВАС RP23-135k15 (Invitrogen) мыши модифицировали гомологичной рекомбинацией для инактивации эндогенного локуса λ легкой цепи мыши посредством нацеленной делеции генных кластеров Vλ-Jλ-Cλ (фиг. 20).
Кратко, целый проксимальный кластер, содержащий генные сегменты Vλ1-Jλ3-CλJ1-Cλ1 удаляли в течение одного события нацеленного воздействия с использованием нацеливающего вектора, содержащего кассету неомицина, фланкированную сайтами loxP с 5' гомологичным плечом мыши, содержащим последовательность 5' от генного сегмента Vλ1, и 3' гомологичным плечом мыши, содержащим последовательность 3' от генного сегмента Сλ1 (фиг. 20, нацеливающий вектор 1).
Второй нацеливающий конструкт получали для точного удаления дистального эндогенного λ генного кластера мыши, содержащего Vλ2-Jλ2-Cλ2-Jλ4-Cλ4 за исключением того, что нацеливающий конструкт содержал 5' гомологичное плечо мыши, которое содержало последовательность 5' от генного сегмента Vλ2, и 3' гомологичное плечо мыши, которое содержало последовательность 5' по отношению к эндогенному генному сегменту Сλ2 (фиг. 20, нацеливающий вектор 2). Таким образом, второй нацеливающий конструкт точно удалял Vλ2-Jλ2, сохраняя при этом Cλ2-Jλ4-Cλ4 интактным на эндогенном локусе λ мыши. ES клетки, содержащие инактивированный эндогенный локус λ (описанный выше), подтверждали с помощью способов кариотипирования и скрининга (например, TAQMAN®), известных в настоящей области техники. Затем ДНК выделяли из модифицированных ES клеток и подвергали обработке с помощью CRE рекомбиназы, тем самым опосредуя делецию проксимальной нацеливающей кассеты, содержащей маркерный ген неомицина, сохраняя только один сайт loxP в точке делеции (фиг. 20, нижняя часть).
Делеция локуса κ легкой цепи мыши. Несколько нацеливающий конструктов получали с использованием аналогичных способов, описанных выше для модификации ДНК из клонов ВАС RP23-302g12 и RP23-254m04 мыши (Invitrogen) путем гомологичной рекомбинации для инактивации локуса к легкой цепи мыши в двухстадийном процессе (фиг. 21).
Кратко, генные сегменты Jκ (1-5) эндогенного локуса κ легкой цепи мыши удаляли за одно событие нацеленного воздействия с использованием нацеливающего вектора, содержащего кассету гигромицина-тимидинкиназы (hyg-TK), содержащую один сайт loxP 3' по отношению к кассете hyg-TK (фиг. 21, Jκ нацеливающий вектор). Гомологичные плечи, используемые для получения этого нацеливающего вектора, содержали геномную последовательность мыши 5' и 3' от эндогенных генных сегментов Jκ мыши. Во втором событии нацеленного воздействия второй нацеливающий вектор получали для удаления части геномной последовательности мыши выше (5') по отношению к наиболее дистальному эндогенному генному сегменту Vκ мыши (фиг. 21, Vκ нацеливающий вектор). Этот нацеливающий вектор содержал инвертированный сайт lox511, сайт loxP и кассету неомицина. Гомологичные плечи, используемые для получения этого нацеливающего вектора, содержали геномную последовательность мыши выше наиболее дистального генного сегмента Vκ мыши. Нацеливающие векторы использовали последовательно (т.е. Jκ, затем Vκ) для нацеливания ДНК в ES клетках. ES, несущие дважды нацеленную хромосому (т.е. один эндогенный локус κ мыши, нацеленный с помощью обоих нацеливающих векторов), подтверждали с помощью способов кариотипирования и скрининга (например, TAQMAN™), известных в настоящей области техники. Затем ДНК выделяли из модифицированных ES клеток и подвергали обработке Cre рекомбиназой, тем самым опосредуя делецию эндогенных генных сегментов Vκ мыши и обеих кассет селекции, при этом сохраняя два расположенных рядом сайтов lox в противоположной ориентации по отношению друг к другу (фиг. 21, нижняя часть; SEQ ID NO: 59).
Таким образом, два модифицированных эндогенных локуса (κ и λ) легкой цепи, содержащие интактный энхансер и константные области, создавали для поэтапной вставки нереаранжированных зародышевых генных сегментов λ человека точным образом с использованием описанных ниже нацеливающих векторов.
Пример 11. Замещение локусов легкой цепи мыши мини-локусом λ легкой цепи человека
Многочисленные нацеливающие векторы конструировали для поэтапной вставки генных сегментов λ человека в эндогенные локусы κ и λ легкой цепи мыши с использованием аналогичных способов, описанных выше. Многочисленные независимые исходные модификации производили в эндогенных локусах легкой цепи, каждая из которых производила химерный локус легкой цепи, содержащий генные сегменты hVλ и Jλ, функционально связанные с константными генами и энхансерами легкой цепи мыши.
Мини-локус λ человека, содержащий 12 генных сегментов Vλ человека и один генный сегмент Jλ человека. Серию исходных нацеливающих векторов конструировали, чтобы они содержали первые 12 последовательных генных сегментов Vλ человека из кластера A и генный сегмент hJλ1 или четыре генных сегмента hJλ с использованием ВАС клона человека с названием RP11-729g4 (Invitrogen). На фигурах 22А и 22В показаны нацеливающие векторы, которые сконструированы для получения исходной вставки генных сегментов λ легкой цепи человека на локусы λ и κ легкой цепи мыши, соответственно.
Для первого набора исходных нацеливающих векторов фрагмент ДНК длиной 124125 п.н. из 729g4 ВАС клона, содержащий 12 генных сегментов hVλ и 1 генный сегмент hJλ конструировали, чтобы он содержал сайт PI-SceI на 996 п.н. ниже (3') от генного сегмента hJλ1 для лигирования 3' гомологичного плеча мыши. Два различных набора гомологичных плечей использовали для лигирования с этим фрагментом человека; один набор гомологичных плечей содержал эндогенные последовательности λ мыши из 135k15 ВАС клона (фиг. 22А), и другой набор содержал эндогенную последовательность κ 5' и 3' от генных сегментов Vκ и Jκ мыши из ВАС клонов мыши RP23-302g12 и RP23-254m04, соответственно (фиг. 22В).
Для 12/1-λ нацеливающего вектора (фиг. 22А) сайт PI-SceI конструировали на 5' - конце от 27847 п.н. фрагмента ДНК, содержащего Cλ2-Jλ4-Cλ4 мыши и энхансер 2.4 модифицированного локуса λ мыши, описанного в примере 10. Фрагмент ~28 т.п.н. мыши использовали в качестве 3' гомологичного плеча путем лигирования с ~124 т.п.н. λ фрагментом человека, что создавало 3' участок соединения, содержащий, в направлении 5'-3', генный сегмент hJλ1, 996 п.н. последовательности λ человека 3' от генного сегмента hJλ1, 1229 п.н. последовательности λ мыши 5' по отношению к гену Сλ2 мыши, ген Сλ2 мыши и оставшуюся часть ~28 т.п.н. фрагмента мыши. Выше (5') от генного сегмента Vλ3-12 человека размещали дополнительные 1456 п.н. последовательности λ человека до начала 5' гомологичного плеча мыши, которое содержало 23792 п.н. геномной ДНК мыши, соответствующей последовательности 5' от эндогенного локуса λ мыши. Между 5' гомологичным плечом и началом последовательности λ человека находилась кассета неомицина, фланкированная сайтами Frt.
Таким образом, 12/1-λ нацеливающий вектор включал в себя, в направлении 5'-3', 5' гомологичное плечо, содержащее ~24 т.п.н. геномной последовательности λ мыши 5' от эндогенного λ локуса, 5' сайт Frt, кассету неомицина, сайт 3' Frt, ~123 т.п.н. геномной последовательности λ человека, содержащей первые 12 последовательных генных сегментов hVλ и генный сегмент hJλ1, сайт PI-SceI, и 3' гомологичное плечо, содержащее ~28 т.п.н. геномной последовательности мыши, включая в себя эндогенные генные сегменты Cλ2-Jλ4-Cλ4, последовательность энхансера 2.4 мыши и дополнительные геномные последовательности мыши ниже (3') энхансера 2.4 (фиг. 22А).
Аналогичным образом, в 12/1-κ нацеливающий вектор (фиг. 22В) использовали такой же ~124 фрагмент λ человека за исключением того, что гомологичные плечи мыши, содержащие последовательность κ мыши, использовали так, чтобы нацеливание на эндогенный локус κ могло быть достигнуто путем гомологичной рекомбинации. Таким образом, 12/1-κ нацеливающий вектор включал в себя, в направлении 5'-3', 5' гомологичное плечо, содержащее ~23 т.п.н. геномной последовательности мыши 5' от эндогенного локуса κ, сайт I-CeuI, 5' сайт Frt, кассету неомицина, 3' сайт Frt, ~124 т.п.н. геномной последовательности λ человека, содержащей первые 12 последовательных генных сегментов hVλ и генный сегмент hJλ1, сайт PI-SceI, и 3' гомологичное плечо, содержащее ~28 т.п.н. геномной последовательности мыши, включая в себя эндогенный ген Сκ мыши, Еκi и Еκ3' и дополнительную геномную последовательность мыши ниже (3') Еκ3' (фиг. 22В, 12/1-κ нацеливающий вектор).
Гомологичная рекомбинация с любым из этих двух исходных нацеливающих векторов создавала модифицированный локус легкой цепи (κ или λ) мыши, содержащий 12 генных сегментов hVλ и генный сегмент hJλ, функционально связанные с эндогенным константным геном легкой цепи и энхансерами мыши (Сκ или С λ2 и Eκi/Еκ3' или Enh 2.4/Enh 3.1), который при рекомбинации приводит в образованию химерной λ легкой цепи.
Мини-локус λ человека с 12 генными сегментами Vλ человека и четырьмя генными сегментами Jλ человека. Согласно другому подходу для добавления разнообразия в химерный локус λ легкой цепи третий исходный нацеливающий вектор конструировали для вставки первых 12 последовательных генных сегментов человека Vλ из кластера A и hJλ1, 2, 3 и 7 генных сегментов в локус κ легкой цепи мыши (фиг. 22В, 12/4-κ нацеливающий вектор). Сегмент ДНК, содержащий генные сегменты hJλ1, Jλ2, Jλ3 и Jλ7, получали с помощью de novo синтеза ДНК (Integrated ДНК Technologies), включая в себя каждый генный сегмент Jλ и геномную последовательность человека, содержащую ~100 п.н. из обеих ближайших 5' и 3' областей каждого генного сегмента Jλ. Сайт PI-SceI конструировали в 3' конец этого ~1 т.п.н. фрагмента ДНК и лигировали с кассетой хлорамфеникола. Гомологичные плечи амплифицировали с помощью ПЦР из λ последовательности человека в 5' и 3' положениях по отношению к генному сегменту hJλ1 ВАС клона 729g4 человека. Гомологичную рекомбинацию с этим промежуточным нацеливающим вектором проводили на модифицированном ВАС клоне729g4, который предварительно нацеливали выше (5') от генного сегмента NA.3-12 человека с кассетой неомицина, фланкированной сайтами Frt, который также содержал сайт I-CeuI 5' по отношению к 5' сайте Frt. Дважды нацеленный 729g4 ВАС клон включал в себя в направлении 5'-3' сайт I-CeuI, 5' сайт Frt, кассету неомицина, 3' сайт Frt, ~123 т.п.н. фрагмент, содержащий первые 12 генных сегментов hVλ, ~1 т.п.н. фрагмент, содержащий генные сегменты Jλ1, 2, 3 и 7 человека, сайт PI-SceI и кассету хлорамфеникол. Этот промежуточный нацеливающий вектор обрабатывали вместе с I-CeuI и PI-SceI и впоследствии лигировали в модифицированный ВАС клон мыши (описанный выше) для создания третьего нацеливающего вектора.
Это лигирование давало в результате третий нацеливающий вектор для вставки последовательностей λ человека в эндогенный локус κ легкой цепи, который включал в себя, в направлении 5'-3', 5' гомологичное плечо мыши, содержащее ~23 т.п.н. геномной последовательности 5' от эндогенного локуса κ мыши, сайт I-CeuI, 5' сайт Frt, кассету неомицина, 3' сайт Frt, -123 т.п.н. фрагмент, содержащий первые 12 генных сегментов hVλ, ~1 т.п.н. фрагмент, содержащий генные сегменты hJλ1, 2, 3 и 7, сайт PI-SceI и 3' гомологичное плечо, содержащее ~28 т.п.н. геномной последовательности мыши, включая в себя эндогенный ген Сκ мыши, Eκi и Еκ3' и дополнительную геномную последовательность мыши ниже (3') от Еκ3' (фиг. 22В, 12/4-κ нацеливающий вектор). Гомологичная рекомбинация с этим третьим нацеливающим вектором создавала модифицированный локус κ легкой цепи мыши, содержащий 12 генных сегментов hVλ и четыре генных сегмента hJλ, функционально связанных с эндогенным геном Сκ мыши, который при рекомбинации приводит к образованию химерной относящейся к человеку λ/ относящейся к мыши κ легкой цепи.
Мини-локус λ человека с интегрированной последовательностью κ легкой цепи человека. Аналогичным образом, два дополнительных нацеливающих вектора, аналогичных векторам, сконструированным для получения исходной вставки генных сегментов λ человека в эндогенный локус κ легкой цепи (фиг. 22В, 12/1-κ и 12/4-κ нацеливающие векторы), конструировали для поэтапной вставки генных сегментов λ легкой цепи человека с использованием уникально сконструированных нацеливающих векторов, содержащих смежные геномные последовательности λ и κ человека. Эти нацеливающие векторы конструировали, чтобы включать в себя ~23 т.п.н. геномную последовательность κ человека, расположенную в естественных условиях между генными сегментами Vκ4-1 и Jκ1 человека. Эту геномную последовательность κ человека специально помещали в этих двух дополнительных нацеливающих векторах между генными сегментами Vλ и Jλ человека (фиг. 22В, 12(κ)1-κ и 12(κ)4-κ нацеливающие векторы).
Оба нацеливающих вектора, содержащих геномную последовательность κ человека, получали с использованием описанного выше модифицированного RP11-729g4 ВАС клона (фиг. 24). Этот модифицированный ВАС клон нацеливали с помощью кассеты селекции спектиномицина, фланкированной сайтами рестрикции NotI и AsiSI (фиг. 24, вверху слева). Гомологичная рекомбинация с кассетой спектиномицина давала в результате дважды нацеленный 729g4 ВАС клон, который включал в себя, в направлении 5'-3', сайт I-CeuI, 5' сайт Frt, кассету неомицина, 3' сайт Frt, ~123 т.п.н. фрагмент, содержащий первые 12 генные сегменты hVλ, сайт NotI приблизительно 200 п.н. ниже (3') от нонамерной последовательности hVλ3-1 генного сегмента, кассету спектиномицина и сайт AsiSI. Отдельный ВАС клон человека, содержащий κ последовательность человека (CTD-2366j12), нацеливали два независимых раза для конструирования сайтов рестрикции в положениях между генными сегментами hVκ4-1 и hJκ1 для обеспечения последующего клонирования ~23 т.п.н. фрагмента для лигирования с генными сегментами hVλ, содержащимися в дважды нацеленном модифицированном 729g4 ВАС клоне (фиг. 24, вверху справа).
Кратко, размер 2366j12 ВАС клона составляет приблизительно 132 т.п.н. и он содержит генные сегменты hVκ 1-6, 1-5, 2-4, 7-3, 5-2, 4-1, геномную последовательность человека ниже от генных сегментов Vκ, генные сегменты hJκ1-5, hCκ и приблизительно 20 т.п.н. дополнительной геномной последовательности локуса κ человека. Этот клон вначале нацеливали с помощью нацеливающего вектора, содержащего кассету гигромицина, фланкированную сайтами Frt и сайтом NotI ниже (3') от 3' сайта Frt. Гомологичные плечи для этого нацеливающего вектора содержали геномную последовательность человека 5' и 3' от генных сегментов Vκ в пределах ВАС клона так, чтобы при гомологичной рекомбинации с этим нацеливающим вектором удалить генные сегменты Vκ, и сайт NotI конструировали ~133 п.н. ниже от hVκ4-1 генного сегмента (фиг. 24, вверху справа). Этот модифицированный 2366j12 ВАС клон нацеливали независимо двумя нацеливающими векторами на 3' -конце для удаления генных сегментов hJλ с помощью кассеты хлорамфеникола, которая также содержала или генный сегмент hJλ1, сайт PI-SceI и сайт AsiSI, или геномный фрагмент λ человека, содержащий четыре генных сегмента hJλ (выше), сайт PI-SceI и сайт AsiSI (фиг. 24, вверху справа). Гомологичные плечи для этих двух аналогичных нацеливающих векторов содержали последовательность 5' и 3' от генных сегментов hJλ. Гомологичная рекомбинация с этими вторыми нацеливающими векторами и модифицированным 2366j12 ВАС клоном давала в результате дважды нацеленный 2366j12 клон, который включал в себя, в направлении 5'-3', 5' сайт Frt, кассету гигромицина, 3' сайт Frt, сайт NotI, 22800 п.н. геномный фрагмент локуса κ человека, содержащий межгенную область между генными сегментами Vκ4-1 и Jκ1, или генный сегмент hJλ1, или геномный фрагмент λ человека, содержащий hJλ1, Jλ2, Jλ3 и Jλ7, сайт PI-SceI и кассету хлорамфеникола (фиг. 24, вверху справа). Два последних нацеливающих вектора для получения двух дополнительных модификаций получали с помощью двух стадий лигирования с использованием дважды нацеленных клонов 729g4 и 2366j12.
Дважды нацеленные клоны 729g4 и 2366j12 обрабатывали с помощью NotI и AsiSI, получая в результате один фрагмент, содержащий кассету неомицина и генные сегменты hVλ, и другой фрагмент, содержащий ~23 т.п.н. геномный фрагмент локуса κ человека, содержащий межгенную область между генными сегментами Vκ4-1 и Jκ1, или генный сегмент hJλ1, или геномный фрагмент, содержащий генные сегменты hJλ1, Jλ2, Jλ3 и Jλ7, сайт PI-SceI и кассету хлорамфеникола, соответственно. Лигирование этих фрагментов создавало два уникальных ВАС клона, содержащих в направлении 5'-3' генные сегменты hVλ, геномную последовательность κ человека между генными сегментами Vκ4-1 и Jκ1, или генный сегмент hJλ1, или геномный фрагмент, содержащий генные сегменты hJλ1, Jλ2, Jλ3 и Jλ7, сайт PI-SceI и кассету хлорамфеникола (фиг. 24, нижняя часть). Эти новые ВАС клоны затем обрабатывали с помощью I-CeuI и PI-SceI для высвобождения уникальных фрагментов, содержащих вышележащую кассету неомицина и смежные λ и κ последовательности человека, и лигировали в модифицированный ВАС клон 302g12 мыши, который содержал в направлении 5'-3' геномную последовательность мыши 5' от эндогенного κ локуса, сайт I-CeuI, 5' сайт Frt, кассету неомицина, 3' сайт Frt, генные сегменты hVλ (3-12 до 3-1), сайт NotI ~200 п.н. ниже от Vλ3-1, ~23 т.п.н. последовательности κ человека, встречающейся в природе между генными сегментами Vκ4-1 и Jκ1 человека, или генный сегмент hJλ1, или геномный фрагмент, содержащий генные сегменты hJλ1, Jλ2, Jλ3 и Jλ7, Еκi мыши, ген Сκ мыши и Еκ3' (фиг. 22, 12hVλ-VκJκ-hJλ1 и 12hVλ-VκJκ-4hJλ нацеливающие векторы). Гомологичная рекомбинация с обоими из этих нацеливающих векторов создавала два отдельных модифицированных локуса κ легкой цепи мыши, содержащих 12 генных сегментов hVλ, геномную последовательность κ человека, и или один, или четыре генных сегмента hJλ, функционально связанных с эндогенным геном Сκ мыши, который при рекомбинации приводит к образованию химерной относящейся к человеку λ/ относящейся к мыши κ легкой цепи.
Пример 12. Конструирование дополнительных генных сегментов Vλ человека в мини-локус λ легкой цепи человека
Дополнительные генные сегменты hVλ добавляли независимо в каждую из исходных модификаций, описанных в примере 11 с использованием аналогичных нацеливающих векторов и способов (фиг. 23A, +16-λ нацеливающий вектор и фиг. 23В, +16-κ нацеливающий вектор).
Введение 16 дополнительных генных сегментов Vλ человека. Вышележащие (5') гомологичные плечи, используемые в конструировании нацеливающих векторов для добавления 16 дополнительных генных сегментов hVλ в модифицированные локусы легкой цепи, описанные в примере 11, содержали геномную последовательность мыши 5' от или эндогенного локуса κ легкой цепи, или эндогенного локуса λ легкой цепи. 3' гомологичные плечи были одинаковыми для всех нацеливающих векторов и содержали геномную последовательность человека, перекрывающуюся с 5' концом λ последовательности человека описанных в примере 11 модификаций.
Кратко, два нацеливающих вектора конструировали для введения 16 дополнительных генных сегментов hVλ в описанные в примере 11 модифицированные локусы легкой цепи мыши (фиг. 23А и 5В, +16-λ или +16-κ нацеливающий вектор). ~172 т.п.н. фрагмент ДНК из ВАС клона RP11-761113 человека (Invitrogen), содержащий 21 последовательный генный сегмент hVλ из кластера A, конструировали с 5' гомологичным плечом, содержащим геномную последовательность мыши 5' по отношению или к эндогенному локусу κ, или эндогенному локусу λ легкой цепи и 3' гомологичным плечом, содержащим геномную последовательность λ человека. 5' κ или λ гомологичные плечи мыши, используемые в этих нацеливающих конструктах, были такими же 5' гомологичными плечами, описанными в примере 11 (фиг. 23А и 23В). 3' гомологичное плечо включало в себя 53057 п.н. область наложения геномной λ последовательности человека, соответствующей эквивалентному 5' концу ~123 т.п.н. фрагмента геномной последовательности λ человека, описанной в примере 11. Эти два нацеливающих вектора включали в себя, в направлении 5'-3', 5' гомологичное плечо мыши, содержащее или ~23 т.п.н. геномной последовательности 5' эндогенного локуса κ легкой цепи мыши или ~24 т.п.н. геномной последовательности мыши 5' от эндогенного локуса λ легкой цепи, 5' сайт Frt, кассету гигромицина, 3' сайт Frt и 171457 п.н. геномной последовательности λ человека, содержащей 21 последовательный генный сегмент hVλ, ~53 т.п.н. которой перекрываются с 5' -концом последовательности λ человека, описанной в примере 12, и служит в качестве 3' гомологичного плеча для этого нацеливающего конструкта (фиг. 23A и 23В, +16-λ или +16-κ нацеливающие векторы). Гомологичная рекомбинация с этими нацеливающими векторами создавала независимо модифицированные локусы κ и λ легкой цепи мыши, каждый из которых содержал 28 генных сегментов hVλ и генный сегмент hJλ1, функционально связанный с эндогенными константными генами мыши (Сκ или Сλ2), которые при рекомбинации приводят к образованию химерной легкой цепи.
Аналогичным образом, +16-κ нацеливающий вектор также использовали для введения 16 дополнительных генных сегментов hVλ в другие исходные модификации, описанные в примере 11, которые встраивали многочисленные генные сегменты hJλ с интегрированной κ последовательностью человека и без нее (фиг. 22В). Гомологичная рекомбинация с этим нацеливающим вектором на эндогенном локусе κ мыши, содержащем другие исходные модификации, создавала локусы κ легкой цепи мыши, содержащие 28 генных сегментов hVλ и генные сегменты hJλ1, 2, 3 и 7 с геномной последовательностью Vκ-Jκ человека и без нее, функционально связанной с эндогенным геном Сκ мыши, который при рекомбинации приводит к образованию химерной λ-κ легкой цепи.
Введение 12 дополнительных генных сегментов Vλ человека. Дополнительные генные сегменты hVλ добавляли независимо к каждой из описанных выше модификаций с использованием аналогичных нацеливающих векторов и способов. Конечная структура локуса, полученного из гомологичной рекомбинации с нацеливающими векторами, содержащими дополнительные генные сегменты hVλ, показана на фиг. 25А и 25В.
Кратко, нацеливающий вектор конструировали для введения 12 дополнительных генных сегментов hVλ в описанный выше модифицированные локусы κ и λ легкой цепи мыши (фиг. 23А и 23В, +12-λ или 12-κ нацеливающие векторы). 93,674 п.н. фрагмент ДНК из ВАС клона RP11-22118 человека (Invitrogen), содержащий 12 последовательных генных сегментов hVλ из кластера В, конструировали с 5' гомологичным плечом, содержащим геномную последовательность мыши 5' по отношению или к эндогенному локусу κ легкой цепи, или локусу λ легкой цепи мыши, и 3' гомологичное плечо, содержащее геномную последовательность λ человека. 5' гомологичные плечи, используемые в этом нацеливающем конструкте, были такими же 5' гомологичными плечами, используемыми для добавления описанных выше 16 генных сегментов hVλ (фиг. 23А и 23В). 3' гомологичное плечо получали путем конструирования сайта PI-SceI ~3431 п.н. 5' по отношению к генному сегменту Vλ3-29P человека, содержащемуся в 27468 п.н. геномном фрагменте последовательности λ человека из ВАС клона RP11-761113. Этот сайт PI-SceI служил в качестве точки лигирования для соединения ~94 т.п.н. фрагмента дополнительной последовательности λ человека с ~27 т.п.н. фрагментом последовательности λ человека, который перекрывается с 5' концом последовательности λ человека в предыдущей модификации с использованием +16-λ или +16-κ нацеливающих векторов (фиг. 23А и 23В). Эти два нацеливающих вектора включали в себя, в направлении 5'-3', 5' гомологичное плечо, содержащее или ~23 т.п.н. геномной последовательности мыши 5' от эндогенного локуса κ легкой цепи, или ~24 т.п.н. геномной последовательности мыши 5' от эндогенного локуса λ легкой цепи, 5' сайт Frt, кассету неомицина, 3' сайт Frt и 121188 п.н. геномной последовательности λ человека, содержащей 16 генных сегментов hVλ и сайт PI-SceI, ~27 т.п.н. из которых перекрывается с 5' концом последовательности λ человека из вставки 16 добавленных генных сегментов hVλ и служит в качестве 3' гомологичного плеча для этого нацеливающего конструкта (фиг. 23А и 23В, +12-λ или 12-κ нацеливающие векторы). Гомологичная рекомбинация с этими нацеливающими векторами независимо создавала модифицированные локусы κ и λ легкой цепи мыши, содержащие 40 генных сегментов hVλ и hJλ1 человека, функционально связанный с эндогенными константными генами мыши (Сκ или Сλ2) которые при рекомбинации приводили к образованию химерной легкой цепи (нижняя часть фиг. 23А и 23В).
Аналогичным образом, +12-κ нацеливающий вектор также использовали для введения 12 дополнительных генных сегментов hVλ в другие исходные модификации, которые встраивали многочисленные генные сегменты hJλ с интегрированной последовательностью κ человека и без нее (фиг. 22В). Гомологичная рекомбинация м этим нацеливающим вектором на эндогенном локусе κ мыши, содержащем другие модификации, создавала локус κ легкой цепи мыши, содержащий 40 генные сегменты hVλ и генные сегменты hJλ1, 2, 3 и 7 с и без геномной последовательности Vκ-Jκ человека, функционально связанной с эндогенным геном Сκ мыши, который при рекомбинации приводит к образованию химерной λ-κ легкой цепи.
Пример 13. Идентификация нацеленных ES клеток, несущих генные сегменты λ легкой цепи человека
Нацеленную ВАС ДНК, полученную согласно предыдущим примерам, использовали для электропорации ES клеток мыши для создания модифицированных ES клеток для создания химерных мышей, которые экспрессируют генные сегменты λ легкой цепи человека. ES клетки, содержащие вставку нереаранжированных генных сегментов λ легкой цепи человека, идентифицировали с помощью количественного анализа TAQMAN®. Наборы специфических праймеров и зонды разрабатывали для вставки последовательностей λ человека и ассоциированных кассет селекции (приобретение аллеля, GOA), потери эндогенных последовательностей мыши и любых кассет селекции (потеря аллеля, LOA) и удержания фланкирующих последовательностей мыши (удержание аллеля, AR). Для каждой дополнительной вставки последовательностей λ человека дополнительные наборы праймеров и зонды использовали для подтверждения присутствия дополнительных последовательностей λ человека, а также предыдущие наборы праймеров и зонды использовали для подтверждения удержания ранее нацеленных последовательностей человека. На таблице 10 представлены праймеры и ассоциированные зонды, используемые в анализах количественной ПЦР. На таблице 11 представлены комбинации, используемые для подтверждения вставки каждого отдела генных сегментов λ легкой цепи человека в клоны ES клеток.
ES клетки, несущие генные сегменты λ легкой цепи человека необязательно трансфектировали с помощью конструкта, который экспрессирует FLP, для удаления фланкированной Frt кассеты неомицина, введенной путем вставки нацеливающего конструкта, содержащего генные сегменты Vλ5-52 - Vλ1-40 человека (фиг. 23А и 23В). Кассету неомицина могут необязательно удалить скрещиванием с мышами, которые экспрессируют рекомбиназу FLP (например, патент США №6774279). Необязательно, кассету неомицина у мышей сохраняют.
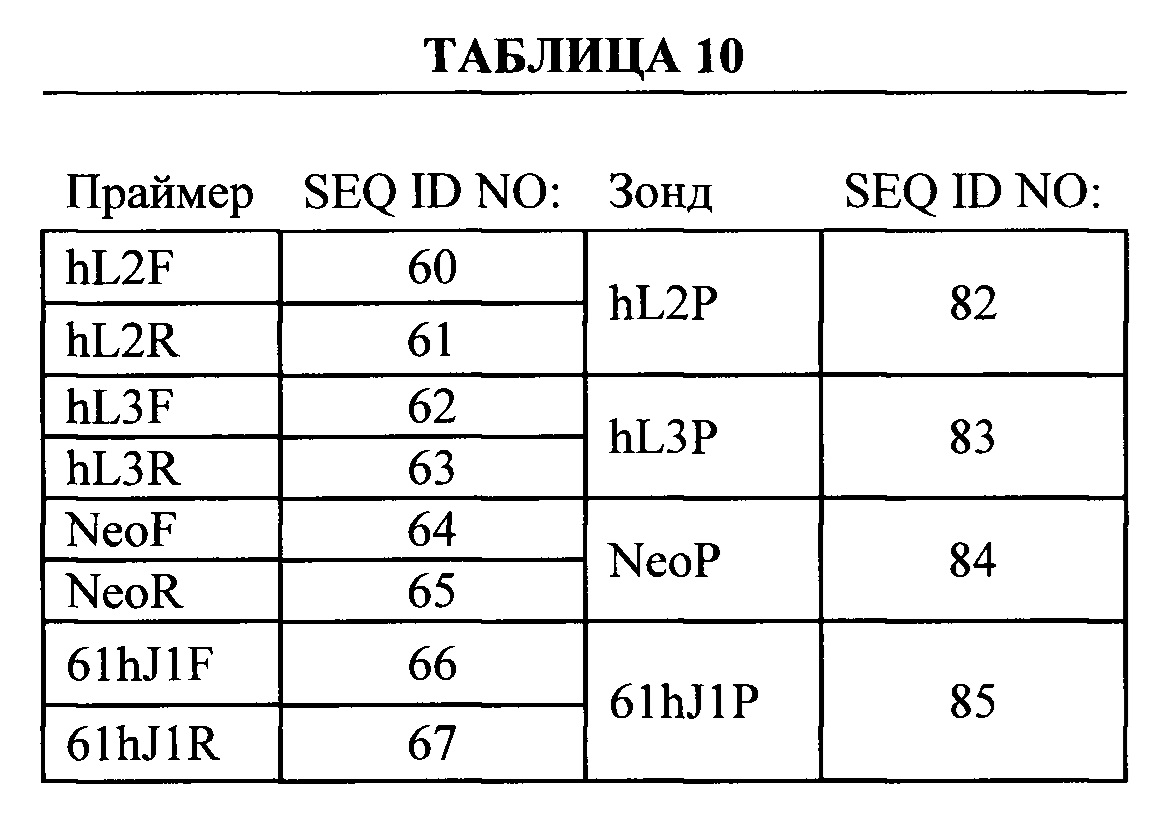
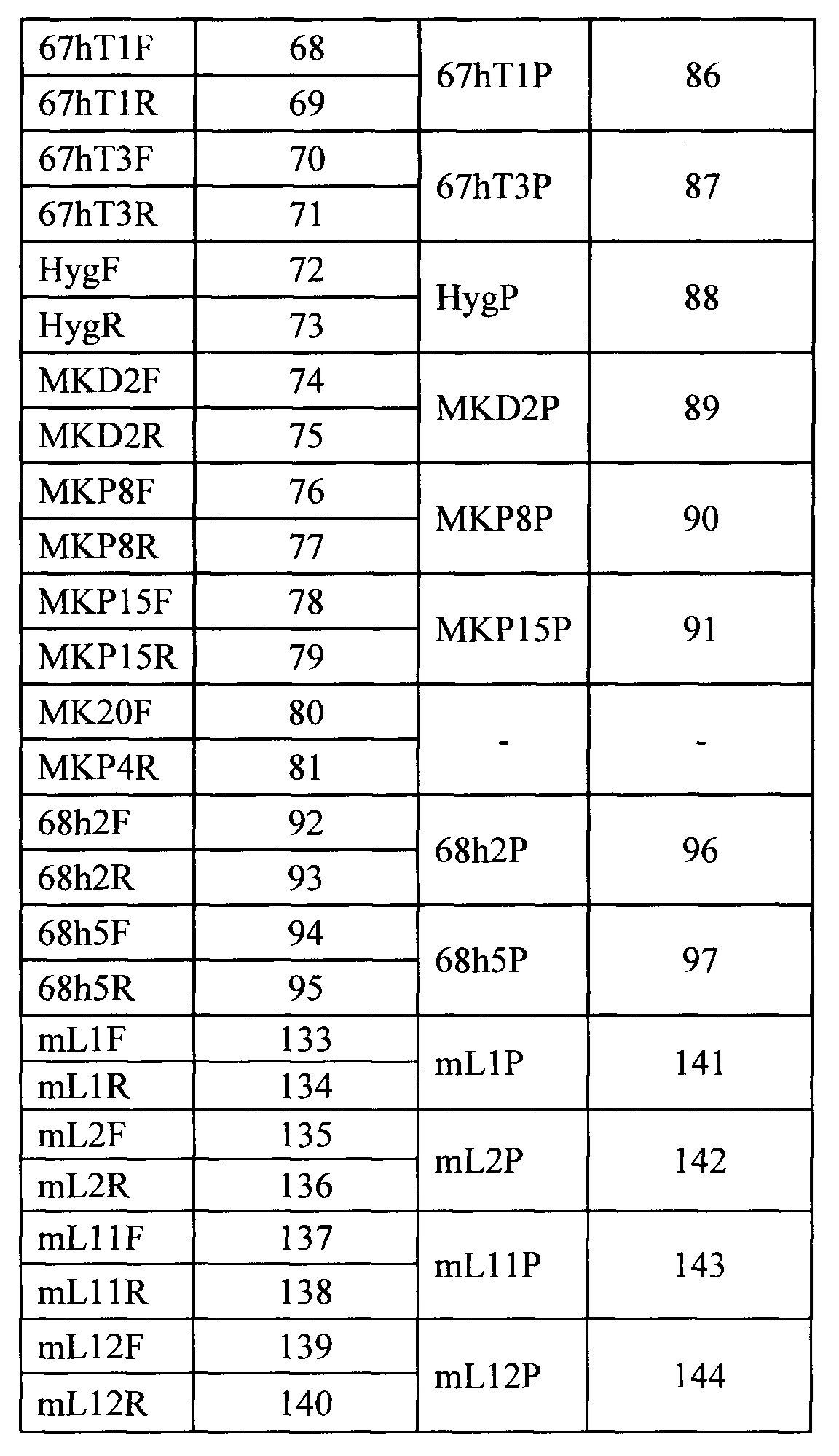
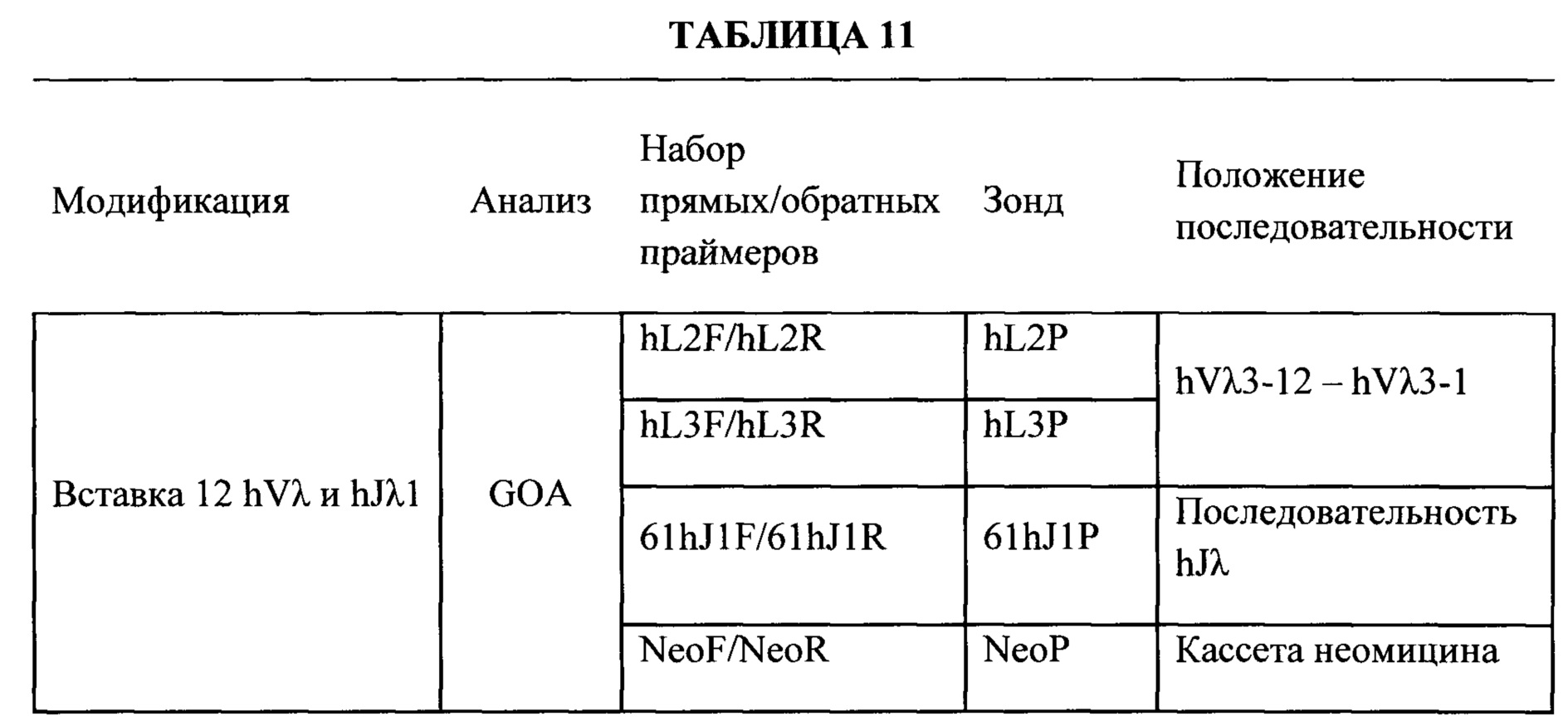
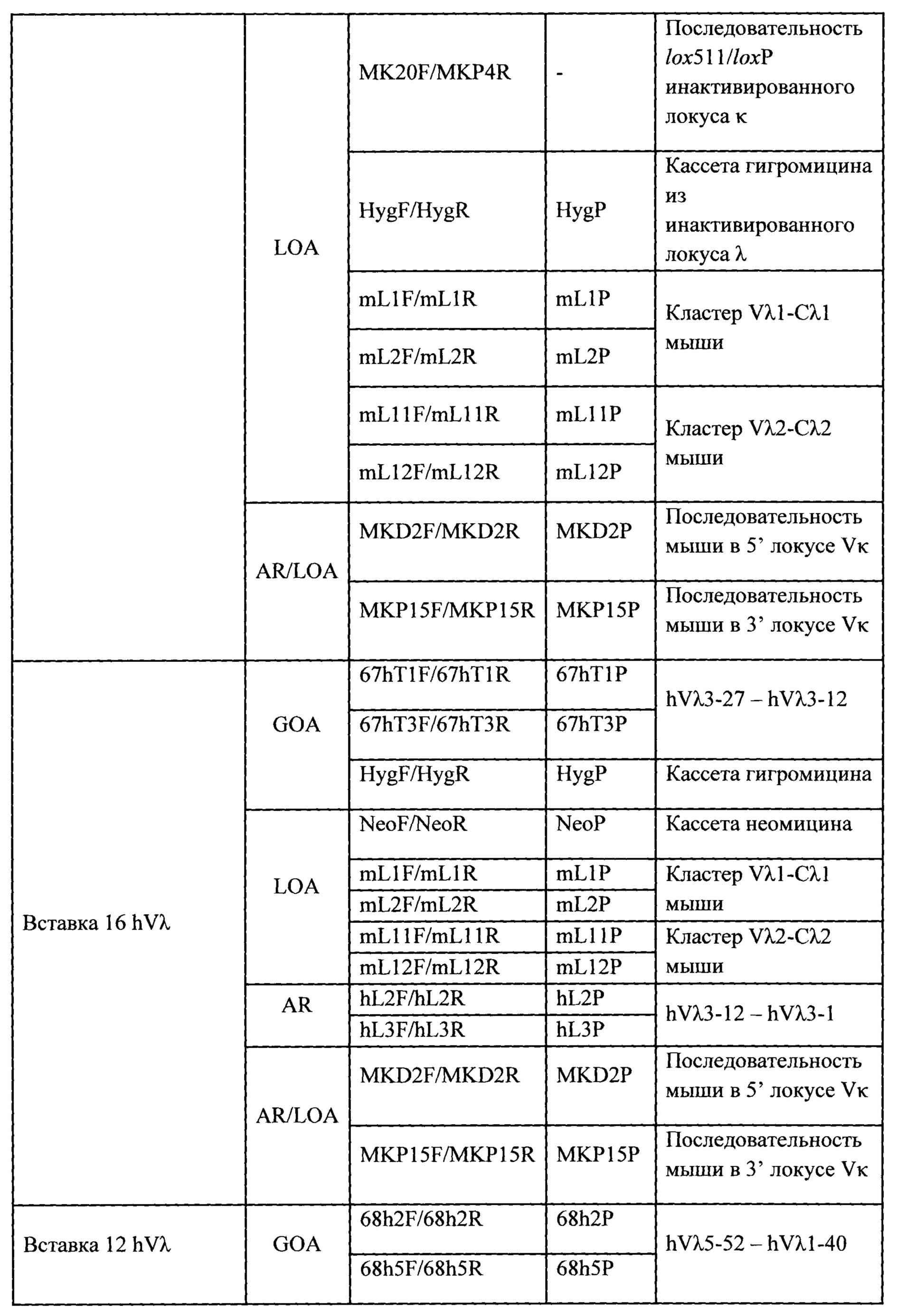
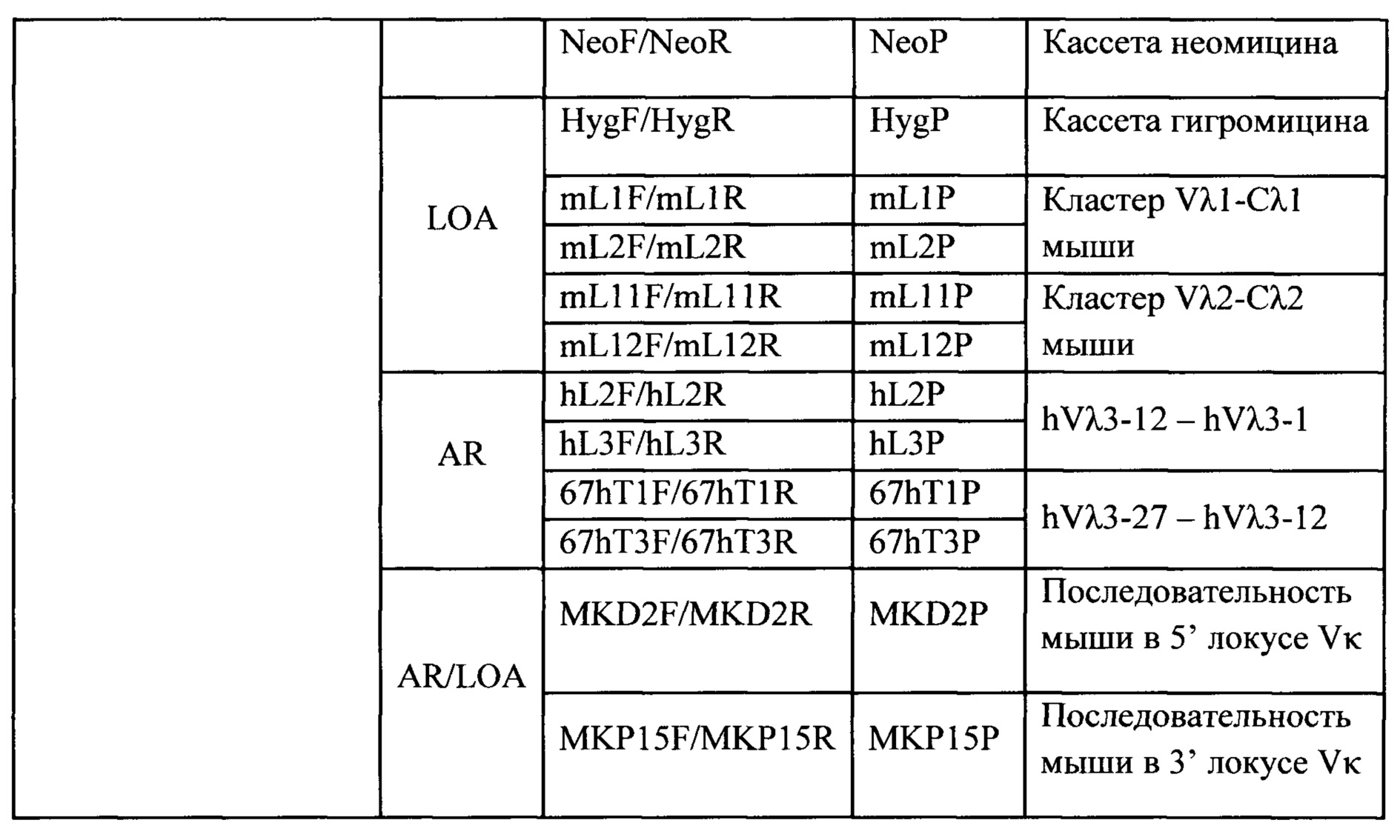
Пример 14. Получение мышей, экспрессирующих λ легкую цепь человека из эндогенного локуса легкой цепи
Описанные выше нацеленные ES клетки использовали в качестве донорных ES клеток и вводили в зародыш мыши на стадии 8 клеток и с помощью способа VELOCIMOUSE® (смотрите, например, патент США №7294754 и Poueymirou et al. (2007) F0 generation mice that are essentially fully derived from the donor gene-targeted ES cells allowing immediate phenotypic analyses Nature Biotech. 25(1):91-99. VELOCIMICE® (F0 мышей, полностью происходящих из донорной ES клетки), независимо несущих генные сегменты λ человека, идентифицировали путем генотипирования с использованием модификации аллельного анализа (Valenzuela et al., выше), который обнаруживает присутствие уникальных генных сегментов λ человека (выше).
Частота использования κ:λ легкой цепи мышей, несущих генные сегменты λ легкой цепи человека. Мышей, гомозиготных в отношении каждой из трех успешных вставок генных сегментов hVλ с одним генным сегментом hJλ (фиг. 23В), и мышей, гомозиготных в отношении первой вставки генных сегментов hVλ или с одним генным сегментом hJλ, или с четырьмя генными сегментами Jλ человека, включая в себя геномную последовательность Vκ-Jκ человека (фиг. 22В), анализировали в отношении экспрессии κ и λ легкой цепи в спленоцитах с использованием проточной цитометрии.
Кратко, селезенки собирали от групп мышей (в диапазоне от трех до семи животных на группу) и измельчали с использованием предметных стекол. После лизиса эритроцитов (RBC) с помощью лизирующего буфера ACK (Lonza Walkersville) спленоциты окрашивали с помощью конъюгированных с флуоресцентным красителем антител, специфических к CD19 мыши (клон 1 D3; BD Biosciences), CD3 мыши (17А2; Biolegend), Igκ мыши (187.1; BD Biosciences) и Igλ мыши (RML-42; Biolegend). Данные получали с использованием проточного цитометра BD™ LSR II (BD Biosciences) и анализировали с использованием программного обеспечения FLOVVJO™ (Tree Star, Inc.). На таблице 12 представлены средние значения в процентах для В-клеток (CD19+), экспрессии κ легкой цепи (CD19+Igκ+Igλ-) и λ легкой цепи (CD19+Igκ-Igλ+), наблюдаемой в спленоцитах из групп животных, несущих каждую генетическую модификацию.
В сходном эксперименте содержание В-клеток компартмента селезенки из мышей, гомозиготных в отношении первой вставки 12 hVλ и четырех hJλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека, функционально связанную с геном Сκ мыши (нижняя часть фиг. 22В), и мышей, гомозиготных в отношении 40 hVλ и одного генного сегмента hJλ (нижняя часть фиг. 23В или верхняя часть фиг. 25В), анализировали в отношении экспрессия Igκ и Igλ с использованием проточной цитометрии (как описано выше). На фиг. 26А показана экспрессия Igλ и Igκ в CD19+ В-клетках для репрезентативной мыши из каждой группы. Количество CD19+ В-клеток на селезенку также регистрировали для каждой мыши (фиг. 26В).
Согласно другому эксперимент содержание В-клеток компартментов селезенки и костного мозга из мышей, гомозиготных в отношении 40 hVλ и четырех hJλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека, функционально связанную с геном Сκ мыши (нижняя часть фиг. 26В), анализировали в отношении хода развития В-клеток с использованием проточной цитометрии различных маркеров клеточной поверхности.
Кратко, две группы (N=3 каждая, самцы и самки возрастом 9-12 недель) дикого типа и мышей, гомозиготных в отношении 40 hVλ и четырех hJλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека, функционально связанную с геном Сκ мыши, умерщвляли и собирали селезенки и костный мозг. Костный мозг собирали из бедренных костей путем промывания с помощью полной среды RPMI (среда RPMI, дополненная фетальной телячьей сывороткой, пируватом натрия, Hepes, 2-меркаптоэтанолом, заменимыми аминокислотами и гентамицином). Эритроциты из препаратов селезенки и костного мозга лизировали с помощью лизирующего буфера ACK (Lonza Walkersville), после чего отмывали полной средой RPMI. 1×106 клеток инкубировали с антителами к CD16/CD32 мыши (2.4G2, BD Biosciences) на льду в течение 10 минут, после чего метили с помощью выбранной панели антител в течение 30 мин. на льду.
Панель для костного мозга: антитело к FITC-CD43 мыши (1В11, BioLegend), PE-ckit (2В8, BioLegend), РеСу7-lgM (11/41, eBioscience), PerCP-Cу5.5-lgD (11-26c.2a, BioLegend), APC-B220 (RA3-6B2, eBioscience), APC-H7-CD19 (ID3, BD) и Pacific Blue-CD3 (17A2, BioLegend).
Панель для костного мозга и селезенки: антитело к FITC-lgic мыши (187.1, BD), РЕ-lgX (RML-42, BioLegend), РеСу7-lgM (11/41, eBioscience), PerCP-Cу5.5-lgD (11-26c.2a, BioLegend), Pacific Blue-CD3 (17A2, BioLegend), APC-B220 (RA3-6B2, eBioscience), APC-H7-CD19 (ID3, BD).
После окрашивания клетки отмывали и фиксировали в 2% формальдегиде. Сбор данных проводили на проточном цитометре FACSCANTOII™ (BD Biosciences) и данные анализировали с помощью программного обеспечения FLOWJO™ (Tree Star, Inc.). На фигурах 27А-27D показаны результаты компартмента селезенки одной репрезентативной мыши из каждой группы. На фигурах 28А-28Е показаны результаты для компартмента костного мозга одной репрезентативной мыши из каждой группы. На таблице 13 представлены средние значения в процентах для В-клеток (CD19+), экспрессии κ легкой цепи (CD19+Igκ+Igλ-) и λ легкой цепи (CD19+Igκ-Igλ+), наблюдаемой в спленоцитах от групп животных, несущих различные генетические модификации. На Таблице 14 представлены средние значения в процентах для В-клеток (CD19+), зрелых В-клеток (B220hiIgM+), незрелых В-клеток (B220intIgM+), незрелых В-клеток, экспрессирующих κ легкую цепь (B220intIgM+Igκ+) и незрелых В-клеток, экспрессирующих λ легкую цепь (B220intIgM+Igλ+), наблюдаемых в костном мозге мышей дикого типа и мышей, гомозиготных в отношении 40 hVλ и четырех hJλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека, функционально связанную с геном Сκ мыши. Этот эксперимент повторяли с дополнительными группами описанных выше мышей и показали сходные результаты (данные не показаны).

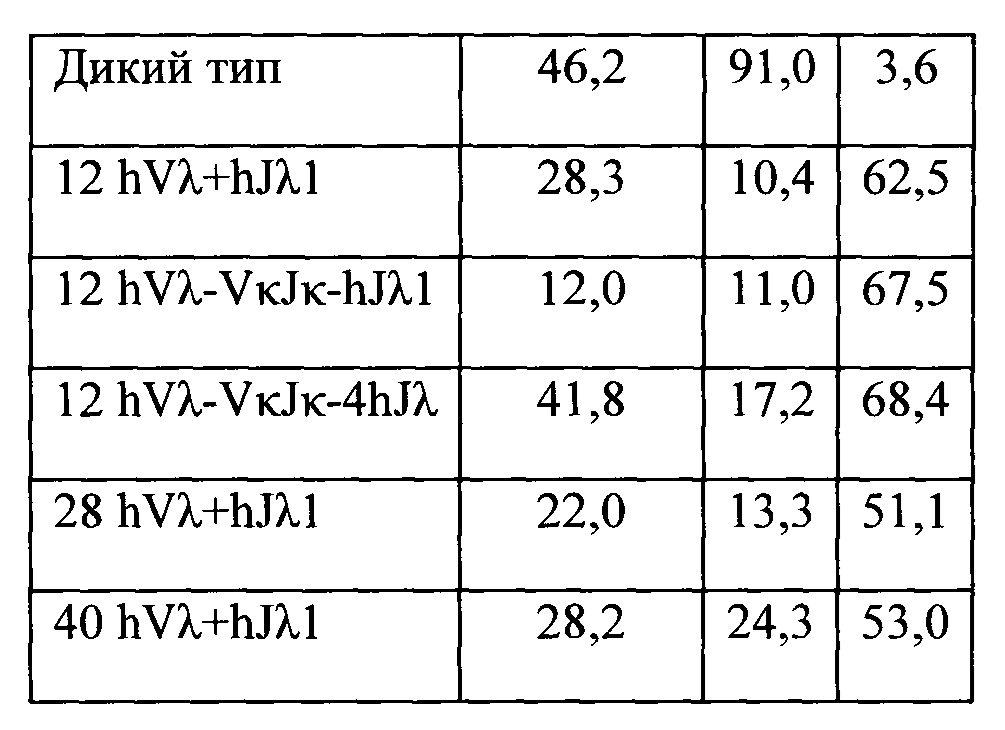

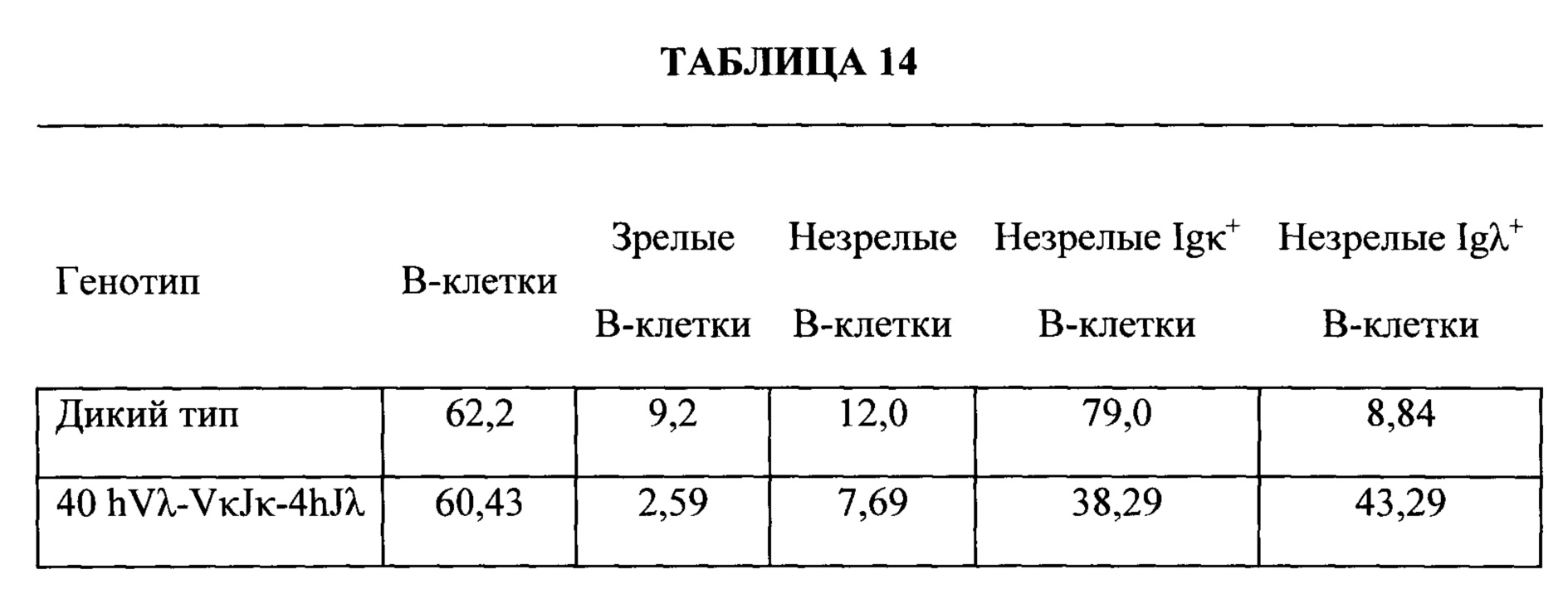
Частота использования гена Vλ человека у мышей, несущих генные сегменты λ легкой цепи человека. Мышей, гетерозиготных в отношении первой вставки λ последовательностей человека (hVλ3-12-hVλ3-1 и hJλ1, фиг. 23В), и гомозиготных в отношении третьей вставки λ последовательностей человека (hVλ5-52-hVλ3-1 и hJλ1, фиг. 23В), анализировали в отношении частоты использования гена λ легкой цепи человека с помощью полимеразной цепной реакции с обратной транскриптазой (ОТ-ПЦР) с использованием РНК, выделенной из спленоцитов.
Кратко, селезенки собирали и промывали с помощью 10 мл RPMI-1640 (Sigma) с 5% HI-FBS в стерильных одноразовых пакетах. Каждый пакет, содержащий одну селезенку, затем помещали в STOMACHER™ (Seward) и гомогенизировали при средней скорости в течение 30 секунд. Гомогенизированные селезенки фильтровали с использованием 0,7 мкм клеточного фильтра и затем осаждали с помощью центрифуги (1000 об/мин в течение 10 минут) и RBC лизировали в BD PHARM LYSE™ (BD Biosciences) в течение трех минут. Спленоциты разбавляли в RPMI-1640 и центрифугировали снова, после чего ресуспендировали в 1 мл PBS (Irvine Scientific). РНК выделяли из осажденных спленоцитов с использованием известных в настоящей области техники стандартных техник.
ОТ-ПЦР проводили на РНК спленоцитов с использованием праймеров, специфических для генных сегментов hVλ человека и гена Сκ мыши (таблица 15). Продукты ПЦР очищали с применением геля и клонировали в вектор pCR2.1-TOPO ТА (Invitrogen) и секвенировали с праймерами: прямой М13 (GTAAAACGAC GGCCAG; SEQ ID NO: 113) и обратный М13 (CAGGAAACAG CTATGAC; SEQ ID NO: 114), расположенными в пределах вектора в положениях, фланкирующих сайт клонирования. Клоны общим количество 84, происходящие из первой и третьей вставок λ последовательностей человека, секвенировали для определения частоты использования гена hVλ (таблица 16). Нуклеотидная последовательность участка соединения hVλ-hJλ1-mCκ для выбранных клонов ОТ-ПЦР показана на фиг. 29.
Аналогичным образом, мышей, гомозиготных в отношении третьей вставки генных последовательностей λ легкой цепи человека (т.е. 40 генных сегментов hVλ и четырех генных сегментов hJλ, включая в себя геномную последовательность Vκ-Jκ человека, нижняя часть фиг. 25В), функционально связанных с эндогенным геном Сκ мыши, анализировали в отношении частота использования гена λ легкой цепи человека с помощью ОТ-ПЦР с использованием РНК, выделенной из спленоциты (как описано выше). Частота использования генных сегментов λ легкой цепи человека для 26 выбранных клонов ОТ-ПЦР показана в таблице 17. Нуклеотидная последовательность участок соединения hVλ-hJλ-mCK для выбранных клонов ОТ-ПЦР показана на фиг. 30.
Аналогичным образом, мышей, гомозиготных в отношении первой вставки генных сегментов λ легкой цепи человека (12 генных сегментов hVλ и hJλ1, фиг. 22А и фиг. 23А), функционально связанных с эндогенным геном Сλ2 мыши, анализировали в отношении частоты использования гена λ легкой цепи человека с помощью ОТ-ПЦР с использованием РНК, выделенной из спленоцитов (как описано выше). Праймеры, специфические для генных сегментов hVλ (таблица 15) использовали с паре с одним из двух праймеров, специфических для гена Сλ2 мыши; Сλ2-1 (SEQ ID NO: 162) или Сλ2-2 (SEQ ID NO: 163).
Многочисленные генные сегменты hVλ, реаранжированные до hλ1, наблюдали из клонов ОТ-ПЦР от мышей, несущих генные сегменты λ легкой цепи человека на эндогенном локусе λ легкой цепи мыши. Нуклеотидная последовательность участка соединения hVλ-hJλ-mCλ2 для выбранных клонов ОТ-ПЦР показана на фиг. 31.
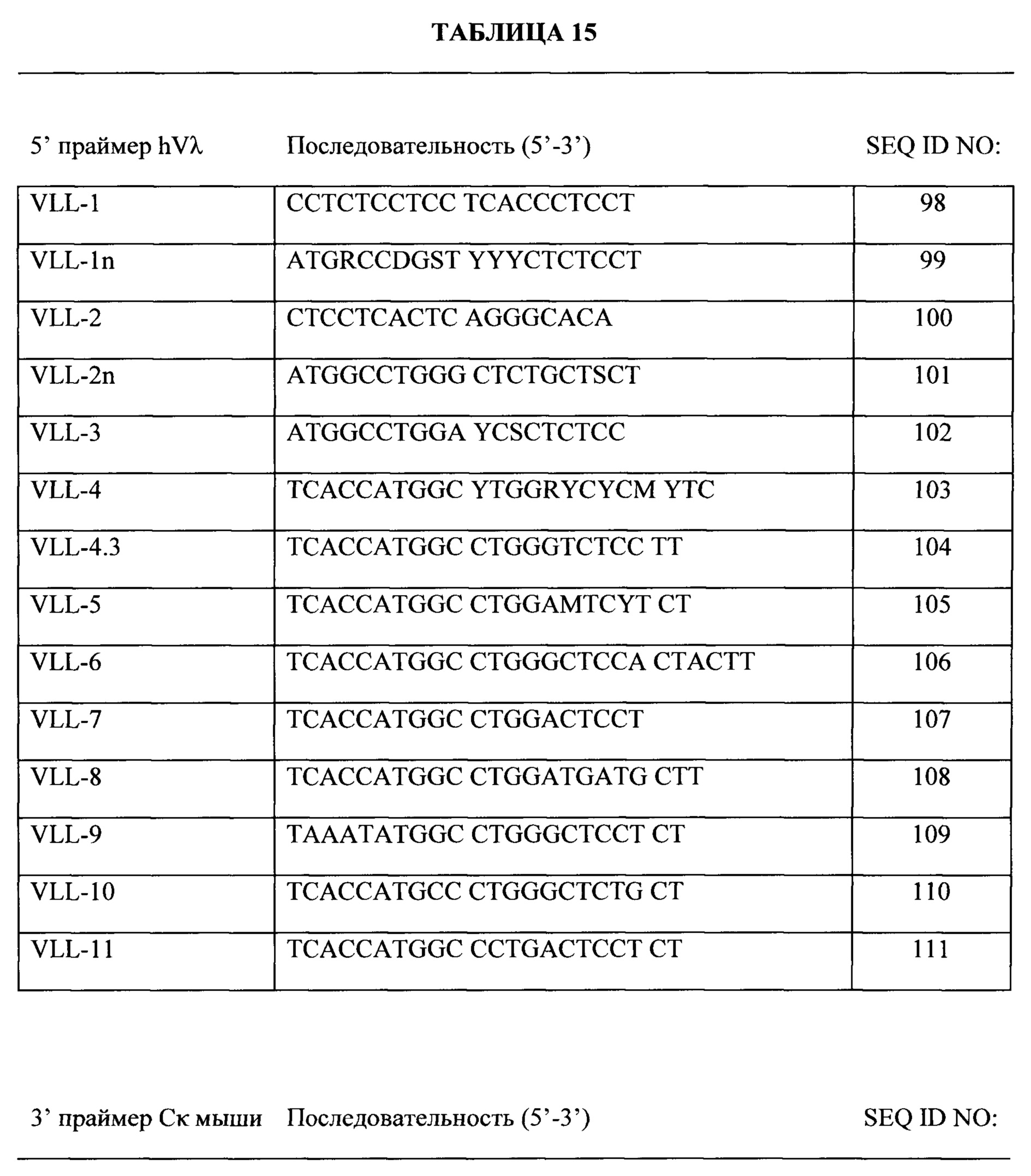
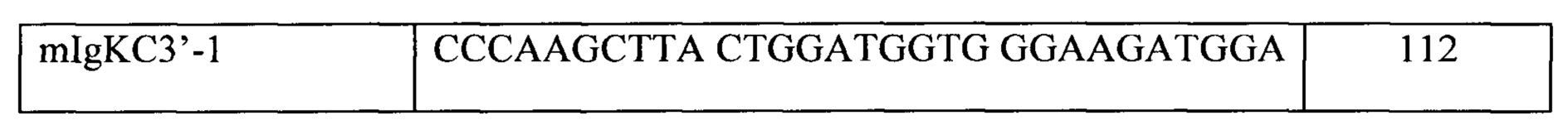
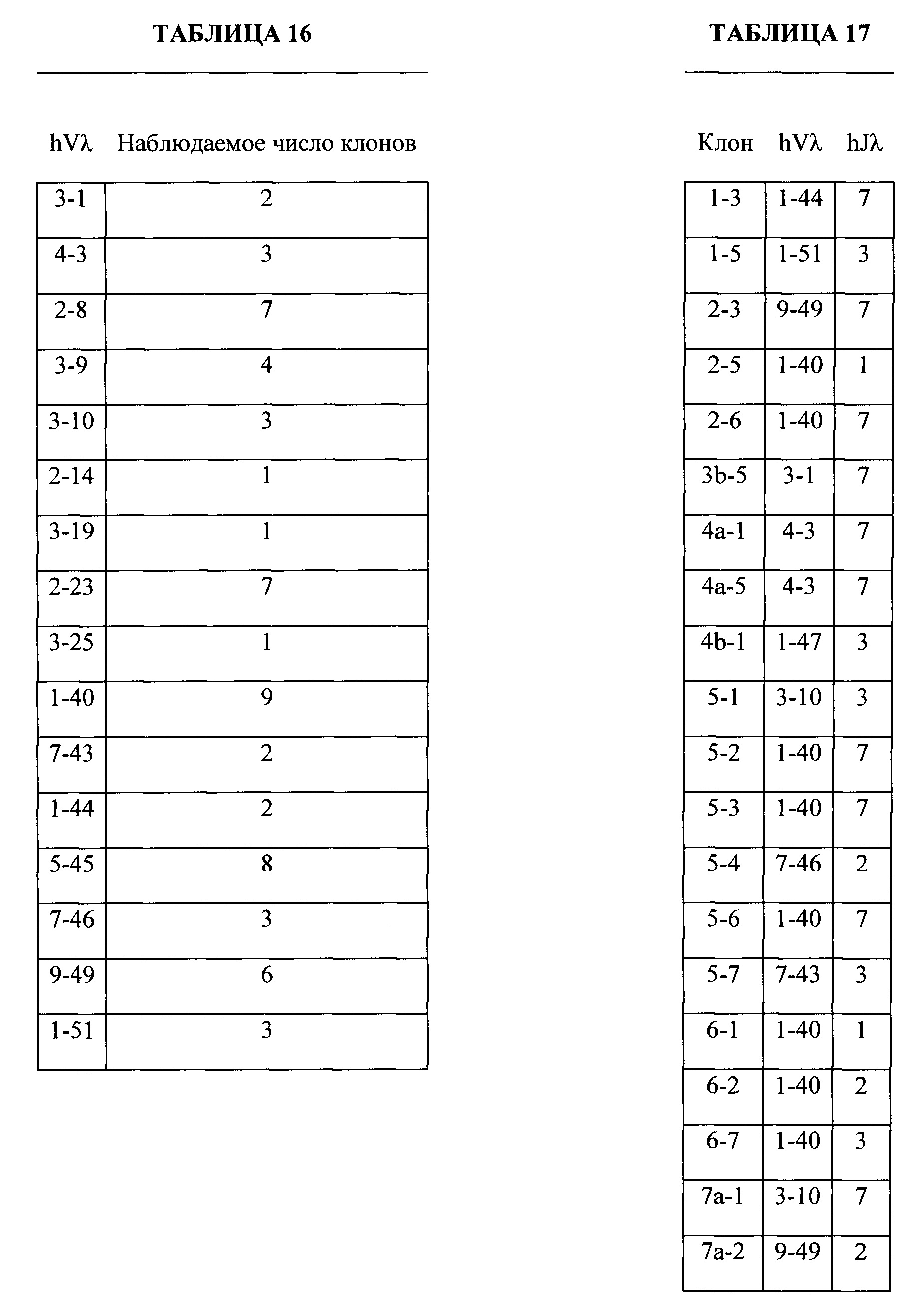

На фиг. 29 показана последовательность участка соединения hVλ-hJλ1-mCκ для клонов ОТ-ПЦР от мышей, несущих первую и третью вставку генных сегментов hVλ с одним генным сегментом hJλ. Последовательности, показанные на фиг. 29, иллюстрируют уникальные реаранжировки, в которые вовлечены различные генные сегменты hVλ с hJλ1, рекомбинированные с геном Сκ мыши. Как гетерозиготные мыши, несущие один модифицированный эндогенный локус κ, содержащий 12 генных сегментов hVλ и hJλ1, так и гомозиготные мыши, несущие два модифицированных эндогенных κ локуса, содержащие 40 генных сегментов hVλ и hJλ1, были способны производить генные сегменты λ человека, функционально связанные с геном Сκ мыши и производить В-клетки, которые экспрессировали λ легкие цепи человека. Эти реаранжировки демонстрируют, что химерные локусы были способны независимо реаранжировать генные сегменты λ человека в многочисленных независимых В-клетках у этих мышей. Кроме того, эти модификации в эндогенном локусе κ легкой цепи не делали какой-либо из генных сегментов hVλ неработоспособным или не предотвращали в химерном локусе рекомбинацию многочисленных генных сегментов hVλ и hJλ (Jλ1) в ходе развития В-клеток, о чем свидетельствуют 16 различных генных сегментов hVλ, которые, как показывают наблюдения, реаранжируются с hJλ1 (таблица 16). Кроме того, эти мыши производили функциональные антитела, содержащие реаранжированные генные сегменты Vλ-Jλ человека, функционально связанные с генами Сκ мыши, как часть эндогенного репертуара легких цепей иммуноглобулина.
На фиг. 30 показана последовательность участка соединения hVλ-hJλ-mCκ для выбранных клонов ОТ-ПЦР от мышей, гомозиготных в отношении 40 hVλ и четырех hJλ генных сегментов, включая в себя геномную последовательность Vκ-Jκ человека. Последовательности, показанные на фиг. 30, иллюстрируют дополнительные уникальные реаранжировки, включающие в себя многочисленные различные генные сегменты hVλ, охватывающие целый химерный локус, с многочисленными различными генными сегментами hJλ, реаранжированными и функционально связанными с геном Сκ мыши. Гомозиготные мыши, несущие модифицированные эндогенные κ локусы, содержащие 40 hVλ и четыре hJλ генных сегмента, также были способны производить генные сегменты λ человека, функционально связанные с геном Сκ мыши, и производить В-клетки, которые экспрессировали λ легкие цепи человека. Эти реаранжировки дополнительно демонстрируют, что все стадии химерных локусов были способны независимо реаранжировать генные сегменты λ человека в многочисленных независимых В-клетках у этих мышей. Кроме того, эти дополнительные модификации в эндогенном локусе κ легкой цепи демонстрируют, что каждая вставка генных сегментов λ человека не делала какой-либо из генных сегментов hVλ и/или Jλ неработоспособным или не предотвращала в химерном локусе рекомбинацию многочисленных генных сегментов hVλ и hJλ в ходе развития В-клеток, о чем свидетельствуют 12 различных генных сегментов hVλ, которые, как показывают наблюдения, реаранжируются со всеми четырьмя генными сегментами hJλ (таблица 17) из 26 выбранных клонов ОТ-ПЦР. Кроме того, эти мыши также производили функциональные антитела, содержащие генные сегменты Vλ-Jλ человека, функционально связанные с областями Сκ мыши, как часть эндогенного репертуара легких цепей иммуноглобулина.
На фиг. 31 показана последовательность участка соединения hVλ-hJλ-mCλ2 для трех отдельных клонов ОТ-ПЦР от мышей, гомозиготных в отношении 12 генных сегментов hVλ и hJλ1. Последовательности, показанные на фиг. 31, иллюстрируют дополнительные уникальные реаранжировки, включающие в себя различные генные сегменты hVλ, охватывающие длину первой вставки, с hJλ1, реаранжированным и функционально связанным с геном Сλ2 мыши (2D1 = Vλ2-8Jλ1; 2D9 = Vλ3-10Jλ1; 3Е15 = Vλ3-1Jλ1). Один клон продемонстрировал непродуктивную реаранжировку вследствие N добавлений на участке соединения hVλ-hJλ (2D1, фиг. 31). Это не редко происходит при V(D)J рекомбинации, поскольку было показано, что соединение генных сегментов в ходе рекомбинации, является неточным. Хотя этот клон представляет собой непродуктивный рекомбинант, присутствующий в репертуаре легких цепей этих мышей, он демонстрирует, что генетический механизм, который вносит вклад в разнообразие J-сегментов среди генов антител, нормально работает у этих мышей и дает в результате репертуар антител, содержащих легкие цепи с большим разнообразием.
Гомозиготные мыши, несущие модифицированные эндогенные λ локусы, содержащие 12 генных сегментов hVλ и hJλ1, также были способны производить генные сегменты λ человека, функционально связанные с эндогенным геном Сλ мыши и производить В-клетки, которые экспрессировали обратные химерные λ легкие цепи, содержащие области hVλ, соединенные с областями Сλ мыши. Эти реаранжировки дополнительно демонстрируют, что генные сегменты λ легкой цепи человека, помещенные на другой локус легкой цепи (т.е. локус λ), были способны независимо реаранжировать генные сегменты λ человека в многочисленных независимых В-клетках у этих мышей. Кроме того, модификации в эндогенном локусе λ легкой цепи демонстрируют, что вставка генных сегментов λ человека не делал какой-либо из генных сегментов hVλ и/или hJλ1 или не предотвращала в химерном локусе рекомбинацию многочисленных генных сегментов hVλ и hJλ1 в ходе развития В-клеток. Кроме того, эти мыши также производили функциональные антитела, содержащие генные сегменты Vλ-Jλ человека, функционально связанные с областью Сλ мыши, как часть эндогенного репертуара легких цепей иммуноглобулина.
Как показано в настоящем примере, мыши, несущие генные сегменты λ легкой цепи человека на эндогенных локусах κ и λ легкой цепи, способны к реаранжировке генных сегментов λ легкой цепи человека и их экспрессии в ассоциации с областью Сκ и/или Сλ мыши, как часть нормального репертуара антител мыши, поскольку функциональная легкая цепь необходима во многих ключевых моментах развития В-клеток как в селезенке, так и в костном мозге. Кроме того, ранние подклассы В-клеток (например, пре-, про- и переходные В-клетки) демонстрируют нормальный фенотип у этих мышей по сравнению с однопометными животными дикого типа (фигуры 27D, 28А и 28В). Наблюдался небольшой дефицит у популяциях В-клеток в костном мозге и периферических популяциях В-клеток, что может быть обусловлено делецией подкласса аутореактивный незрелых В-клеток и/или субоптимальной ассоциацией λ легкой цепи человека с тяжелой цепью мыши. Тем не менее частота использования Igκ/Igλ, наблюдаемая у этих мышей, демонстрирует ситуацию, которая больше напоминает экспрессию легких цепей человека, чем таковую, наблюдаемую у мышей.
Пример 15. Сκрещивание мышей, экспрессирующих λ легкие цепи человека из эндогенного локуса легкой цепи
Для оптимизации частоты использования генных сегментов λ человека на эндогенном локусе легкой цепи мыши, мышей, несущих нереаранжированные генные сегменты λ человека, скрещивают с другой мышью, содержащей делецию в противоположном эндогенном локусе легкой цепи (или κ, или λ). Например, генные сегменты λ человека, расположенные на эндогенном локусе κ, будут единственными функциональными генными сегментами легкой цепи, присутствующими у мыши, которая также несет делецию в эндогенном локусе λ легкой цепи. Таким образом, полученное потомство будет экспрессировать только λ легкие цепи человека, как описано в предыдущих примерах. Скрещивание проводят стандартными техниками, признанными в настоящей области техники, и, альтернативно, с помощью коммерческих компаний, например, The Jackson Laboratory. Линии мышей, несущих генные сегменты λ легкой цепи человека на эндогенном локусе κ и делецию эндогенного локуса λ легкой цепи, подвергают скринингу в отношении присутствия уникальных обратных химерных (относящихся к человеку-мыши) λ легких цепей и отсутствия эндогенных λ легких цепей мыши.
Мышей, несущих нереаранжированный локус λ легкой цепи человека, также скрещивали с мышами, которые содержат замещение эндогенного вариабельного генного локуса тяжелой цепи мыши вариабельным генным локусом тяжелой цепи человека (смотрите патент США №6596541, Regeneron Pharmaceuticals, генетически сконструированная мышь VELOCIMMUNE®). Мышь VELOCIMMUNE® включает в себя, частично, геном, содержащий вариабельные области тяжелой цепи человека, функционально связанные с эндогенными локусами константной области мыши так, чтобы мышь производила антитела, содержащие вариабельную область тяжелой цепи человека и константную область тяжелой цепи мыши в ответ на антигенную стимуляцию. ДНК, кодирующая вариабельные области тяжелых цепей антител, могут выделить и функционально связать с ДНК, кодирующей константные области тяжелой цепи человека. Затем ДНК могут экспрессировать в клетку, способную экспрессировать полностью человеческую тяжелую цепь антитела. При подходящей схеме скрещивания получают мышей, несущих замещение эндогенного локуса тяжелой цепи мыши локусом тяжелой цепи человека и нереаранжированным локусом λ легкой цепи человека на эндогенном локусе κ легкой цепи. Антитела, содержащие соматически мутированные вариабельные области тяжелой цепи человека и вариабельные области λ легкой цепи человека, могут выделять при иммунизации с помощью представляющего интерес антигена.
Пример 16. Получение антител от мышей, экспрессирующих тяжелые цепи человека и λ легкие цепи человека
После скрещивания мышей, которые содержат нереаранжированный локус λ легкой цепи человека, с различными требуемыми линиями, содержащими модификации и делеции других эндогенных локусов Ig (описанных выше), выбранных мышей иммунизировали представляющим интерес антигеном.
В общем, мышь VELOCIMMUNE®, содержащая одну из отдельных реаранжированных зародышевых областей легкой цепи человека, сенсибилизировали антигеном, и лимфатические клетки (такие как В-клетки) выделяли из сыворотки животных, лимфатические клетки могут быть слитыми с клеточной линией миеломы для получения бессмертных гибридомных клеточных линий, и такие гибридомные клеточные линии подвергают скринингу и отбору для идентификации гибридомных клеточных линий, которые производят антитела, содержащие тяжелую цепь человека и λ легкую цепь человека, которые являются специфическими к используемому для иммунизации антигену. ДНК, кодирующую вариабельные области тяжелых цепей и λ легких цепей, могут выделять и соединять с требуемыми изотипическими константными областями тяжелой цепи и легкой цепи. Вследствие присутствия дополнительных генных сегментов hVλ по сравнению с эндогенным локусом λ мыши, разнообразие репертуара легких цепей сильно увеличивается и предоставляет повышенное разнообразие антигенспецифическому репертуару при иммунизации. Полученные клонированные последовательности антител могут впоследствии получать в такой клетке, как клетка СНО. Альтернативно, ДНК, кодирующую антигенспецифические химерные антитела или вариабельные домены легких и тяжелых цепей, могут выделять непосредственно из антигенспецифических лимфоцитов (например, В-клеток).
Вначале, выделяют высокоаффинные химерные антитела с вариабельной областью человека и константной областью мыши. Как описано выше, определяют характеристики антител и проводят селекцию в отношении требуемых характеристик, включая в себя аффинность, селективность, эпитоп и т.д. Константные области мыши замещают требуемой константной областью человека для получения полностью человеческого антитела, содержащего соматически мутированную тяжелую цепь человека и λ легкую цепь человека, происходящую из нереаранжированного локуса λ легкой цепи человека согласно настоящему изобретению. Подходящие константные области человека включают в себя, например, относящиеся к дикому типу или модифицированные IgG1, IgG2, IgG3 или IgG4.
Пример 17. Скрещивание содержащих ADAM6 мышей и содержащих вариабельный сегмент λ человека мышей
Любую из описанных в настоящем документе мышей, которая содержит модификацию эндогенного гена ADAM6 или его ортолога или гомолога и дополнительно содержит ген, которые предоставляет мыши функцию ADAM6, скрещивают с мышью, содержащей модификацию, которая содержит вариабельный сегмент λ человека (например, сегмент V и J), функционально связанный с константным геном λ или κ человека или мыши. Мышь, содержащая вариабельный сегмент λ человека, может содержать вариабельный сегмент, присутствующий на модифицированном эндогенном локусе λ или κ или на трансгене. Мышей скрещивают и потомство дополнительно скрещивают между собой при необходимости и потомство подвергают скринингу в отношении фертильных мышей, которые проявляют функцию ADAM6 и которые также экспрессируют последовательность λ человека, ассоциированную с константной областью λ или κ человека или мыши, в зависимости от конкретного случая.
Мышь, содержащую гуманизированный вариабельный локус тяжелой цепи (сегменты V, D и J человека, замещающие все или по существу все сегменты V, D и J мыши), которая дополнительно содержит эктопическую последовательность ADAM6 (или последовательность ортолога или гомолога ADAM6, которая предоставляет мыши функцию ADAM6), скрещивают с мышью, которая содержит замещение всех или по существу всех сегментов V и J легкой цепи сегментом V и J λ легкой цепи человека на локусе λ мыши и/или локусе κ мыши. Потомство дополнительно скрещивают при необходимости и идентифицируют мышей, которые экспрессируют антитело, содержащее VH человека, слитый с константной последовательностью тяжелой цепи, и когнатный λ VL человека, слитый с константной последовательностью λ или κ легкой цепи.
Мышей подвергают воздействию представляющего интерес антигена и позволяют им развить иммунный ответ. Антитела, специфические к представляющему интерес антигену, идентифицируют и последовательности VH человека и вариабельные последовательности λ человека (включая в себя вариабельные последовательности λ человека, соединенные с константными областями κ мыши) идентифицируют и используют для получения антитела человека путем конструирования последовательностей вариабельного домена в комбинации с генами константной области человека.
В одном случае путем скрещивания получают мышь, которая содержит замещение всех или по существу всех сегментов V, D и J тяжелой цепи мыши сегментами V, D и J человека на эндогенном локусе тяжелой цепи мыши, и которая содержит аллель легкой цепи, который содержит замещение всех или по существу всех вариабельных последовательностей λ легкой цепи одной или несколькими вариабельными последовательностями λ человека на эндогенном локусе λ мыши, функционально связанными с константной последовательностью λ, и которая содержит аллель легкой цепи, который содержит замещение всех или по существу всех вариабельных последовательностей κ легкой цепи на эндогенном локусе κ одной или несколькими вариабельными последовательностями λ человека. Животное подвергают воздействию представляющего интерес антигена и позволяют развить иммунный ответ. Идентифицируют антитела, которые связывают представляющий интерес антиген, которые содержат вариабельные домены тяжелой цепи человека, когнатные вариабельным доменам λ человека на константной области λ мыши или κ мыши. Последовательности нуклеиновой кислоты, кодирующие вариабельные домены используют для получения полностью человеческого антитела путем конструирования вариабельных последовательностей в комбинации с последовательностями константной области человека.
Описанные в настоящем примере мыши содержат одну или несколько межгенных областей Vκ-Jκ, описанных в тексте описания и на фигурах в настоящем документе.