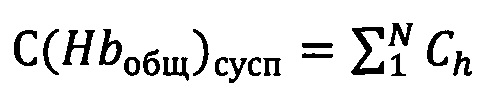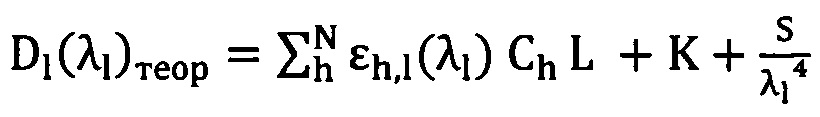Результат интеллектуальной деятельности: Способ определения концентраций гемоглобина и его производных в крови
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Настоящее изобретение относится к медицине, а именно к физическим методам анализа крови путем измерения интенсивности спектральных линий непосредственно в самом спектре, и может быть использовано для определения концентраций гемоглобина (Hb) и его производных в крови человека.
Определение концентрации Hb является одним из наиболее важных и распространенных исследований в клинической лабораторной диагностике. Оно проводится при различных заболеваниях, а также при контроле за лечением всех видов анемий, связанных с кровопотерей, с нарушением кровообращения, с повышенным кроверазрушением, при первичных и вторичных эритроцитозах, эритремии, полицитемии и других заболеваниях.
Уровень техники
В настоящее время известны несколько биофизических методов определения концентрации Hb и его производных без использования дополнительных специальных химических агентов.
Известен способ определения концентраций производных Hb без добавления в раствор специальных химических агентов, основанный на аппроксимации экспериментальной кривой теоретической с учетом молярных показателей поглощения различных производных Hb. (Bellavia, L. DuMond, J.F. Perlegas, A. Bruce King, S. Kim-Shapiro, D.B. Nitroxyl accelerates the oxidation of oxyhemoglobin by nitrite. Nitric Oxide 31, 38-47 (2013). Однако при использовании данного способа измеряют спектр свободного Hb, полученного в результате гемолиза эритроцитов в воде, а не нативного Hb в цельных клетках, что может привести к искажению результатов измерения концентраций производных Hb.
Известен также ряд зарубежных патентов, включающих возможность определения концентрации общего Hb без добавления в кровь дополнительных химических агентов. К ним относятся способы оценки концентрации Hb, основанные на сравнении данных, измеренных спектрофотометрически на двух длинах волн при пропускании света через слой цельной крови (US 20150029492 А1. Measurement of total hemoglobin in whole blood, 2012; WO 2003056327 A1. Method for quantitative hemoglobin determination in undiluted unhemolyzed whole blood, 2001). Однако эти методы не учитывают при расчетах физические закономерности рассеяния света при его распространении в слое крови. Также эти методы не позволяют определить концентрации производных Hb, в частности их процентное содержание в крови. В соответствии с патентом US 20070259436 А1 Blood Hemolysis Analyzer, 2006 авторы изучают поглощение света Hb, находящимся внутри клетки, и свободным Hb вне клетки. Измерения проводят на двух или нескольких длинах волн, причем только в области длин волн 400-430 нм. При этом в расчетах возникает необходимость учитывать индивидуальные пики поглощения различных производных Hb, отличающиеся лишь на 5-15 нм, что снижает точность оценки из-за мультиколлинеарности молярных показателей поглощения различных производных Hb. В расчетах не учитывают закономерности рассеяния света на разных длинах волн и на разных по размерам неоднородностях. К тому же, у свободного Hb постепенно изменяется соотношение концентраций производных Hb, что также приводит к искажению оценки действительных показателей.
Наиболее близким к заявляемому способу по совокупности существенных признаков является способ измерения концентраций производных Hb и общего Hb в крови (Elena Kozlova, Aleksandr Chernysha, Victor Moroz, Victoria Sergunova, Anna Zavialova, Artem Kuzovlev/ Nanoparticles of perfluorocarbon emulsion contribute to the reduction of methemoglobin to oxyhemoglobin // International Journal of Pharmaceutics 497 (2016) 88-95], основанный на измерении спектра поглощения Dl(λl)экспер раствора Hb в дистиллированной воде с помощью цифрового спектрофотометра в диапазоне длин волн λ=500-700 нм, с точностью 0,5 нм и на последующей математической обработке данного спектра, а именно на подборе методом нелинейной регрессии таких параметров теоретической кривой Ch (неизвестных концентраций производных Hb), которые наилучшим способом аппроксимируют этот эмпирический спектр. Теоретическая кривая при этом базируется на законе поглощения Бугера - Ламберта - Бэра, с учетом зависимости оптической плотности от концентраций производных Hb и молярных показателей поглощения:
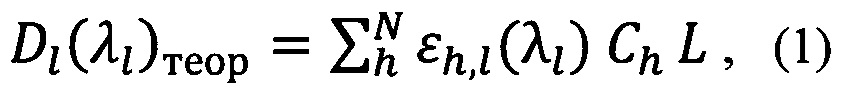
где λl - длина волны излучения;
Dl(λl) - оптическая плотность раствора на длине волны λl;
h - номер производной Hb в растворе;
N - общее число производных Hb в растворе;
εh,l(λl) - молярный показатель поглощения соответствующей производной Hbh на данной длине волны λl;
Ch - концентрация соответствующей производной Hbh в растворе;
L - толщина слоя раствора;
Индекс l означает номер длины волны, например λ1=500 нм, λ2=500,5 нм, и т.д.
Величины εh,l(λl) являются собственными стандартными характеристиками вещества, их значения приведены в литературе, в частности в работе (Bellavia, L. DuMond, J.F. Perlegas, A. Bruce King, S. Kim-Shapiro, D.B. Nitroxyl accelerates the oxidation of oxyhemoglobin by nitrite. Nitric Oxide 31, 38-47 (2013)).
Принят в качестве прототипа.
Однако использование в лабораторной практике способа-прототипа не позволяет достичь технических результатов заявляемого изобретения по следующим причинам. При использовании способа-прототипа перед измерением оптической плотности эритроциты помещают в дистиллированную воду. При этом неизбежно происходит их гемолиз, то есть эритроциты лопаются и их содержимое, в том числе и молекулы Hb, а также молекулы всех его производных, оказываются в водном растворе. Тем самым внутриклеточный Hb превращается в свободный Hb. Известно, что свободный Hb способен окисляться, тем самым смещая соотношение концентраций производных Hb. Таким образом, результат измерения не будет соответствовать тем концентрациям производных Hb, которые были в исходном образце.
Другим недостатком данного метода является то, что при определении концентраций Hb и его производных авторы не учитывают наличие в воде теней эритроцитов и других рассеивающих центров, например неоднородностей мембран клеток, конгломератов Hb, белковых кластеров, что вносит нежелательный вклад в результаты расчетов.
Заявляемое изобретение направлено на решение задачи измерения концентраций производных Hb, а также общего (суммарного) Hb в крови.
Использование в клинической практике заявляемого способа позволяет достичь нескольких технических результатов:
- приближение исследуемого препарата к нативным условиям существования и функционирования Hb в эритроцитах за счет использования буфера в качестве среды;
- повышение точности проводимых исследований за счет учета эффекта рассеяния света на частицах в суспензии;
- повышение точности проводимых исследований за счет исключения фактора влияния лекарственного препарата, имеющегося в крови пациента и способного исказить картину наличия производных Hb;
- возможность определения процентного содержания как каждого из производных Hb, так и его общего количества;
Указанные технические результаты при осуществлении изобретения достигаются за счет того, что, так же как в известном способе, определяют спектр поглощения Dl(λl)экспер гемоглобиносодержащего раствора с помощью цифрового спектрофотометра в диапазоне длин волн λ=500-700 нм, с точностью 0,5 нм, затем аппроксимируют эмпирическую кривую теоретической кривой Dl(λl)теор.
Особенность заявляемого способа заключается в том, что спектр поглощения Hb измеряют в суспензии эритроцитов, полученной с использованием буфера PBS рН 7,4 в качестве среды, при аппроксимации учитывают поглощение света производными Hb, а также величины рэлеевского рассеяния света и рассеяния света на эритроцитах. Расчет осуществляют в соответствии с формулой:
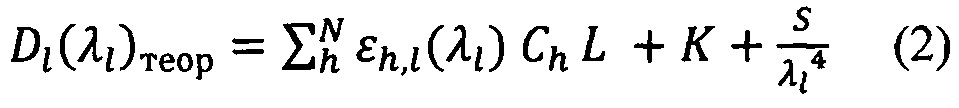
где λl - длина волны излучения;
Dl(λl) - оптическая плотность суспензии эритроцитов в буфере на длине волны λl;
h - номер производной Hb в суспензии эритроцитов (Hbh);
N - общее число производных Hb в суспензии эритроцитов;
εh,l(λl) - молярный показатель поглощения соответствующей производной Hbh на данной длине волны λl;
Ch - концентрация соответствующей производной Hbh суспензии эритроцитов;
L - толщина слоя раствора;
S - коэффициент, учитывающий рэлеевское рассеяние света на частицах размером D<<λ; то есть на неоднородностях мембран клеток, на белковых конгломератах и кластерах;
K - коэффициент, учитывающий рассеяние света на частицах размером D≥λ, то есть учитывает рассеяние на клетках.
Раскрытие сущности изобретения
Для приближения к нативным условиям существования и функционирования Hb в эритроцитах спектр поглощения Hb измеряют в суспензии эритроцитов в буфере (используют стандартный для крови буфер PBS рН 7,4) с помощью цифрового спектрофотометра в диапазоне длин волн λ=500-700 нм, с точностью 0,5 нм. Замена дистиллированной воды в качестве среды буферным раствором позволяет избежать гемолиза эритроцитов, в результате которого изменяется процентное содержание производных Hb по сравнению с исходным. Таким образом, исследованию подвергают не раствор Hb, а суспензию цельных эритроцитов в буфере.
При этом имеет место эффект рассеяния света на частицах в суспензии, что необходимо учитывать для повышения точности результатов исследования. Авторы аппроксимируют эмпирический спектр теоретической кривой, которая наилучшим способом вписывается в экспериментальную кривую. Для повышения точности аппроксимации необходимо учитывать, что ослабление света обусловлено истинным его поглощением производными Hb и одновременно рассеянием света на частицах в суспензии - рэлеевское рассеяние света на частицах размером D<<λ (коэффициент S) и рассеяние света на частицах размером D≥λ (коэффициент K):
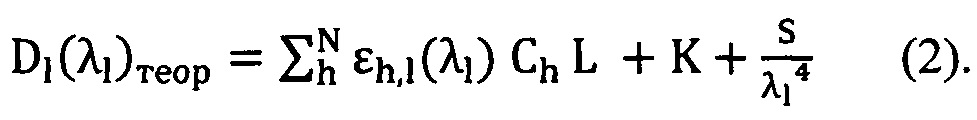
Формула записана в соответствии с физическими закономерностями, изложенными в работе Ремизова А.Н., Максиной А.Г., Потапенко А.Я. «Медицинская и биологическая физика», Издательство "ДРОФА", 2003; Дисперсные системы / Т.А. Савицкая, М.Б. Черепенников, М.П. Шевелева. - Минск: БГУ, 2012. - 200 с. ISBN 978-985-518-795-1.
Теоретическую кривую Dl(λl)теор подбирают так, чтобы она оптимально вписывалась в экспериментальные данные Dl(λl)экспер. При построении аппроксимирующей кривой Dl(λl)теор стандартным методом нелинейной регрессии статус зависимой переменной присваивают искомой функции Dl(λl)экспер, независимыми переменными являются молярные показатели поглощения для каждой производной Hbh на заданных длинах волн εh,l. Неизвестными величинами являются концентрации производных Hb Ch. Неизвестные коэффициенты K и S являются параметрами модели, и их подбирают так, чтобы теоретическая кривая Dl(λl)теор описывала бы экспериментальные данные Dl(λl)экспер наилучшим образом (R-square > 0,98). При аппроксимации должно быть выполнено условие Ci≥0. Именно величины Ch являются результатом расчетов стандартной статистической программы - искомыми концентрациями производных Hb.
Для трех основных производных Hb: HbO2 (оксигемоглобин), Hb (дезоксигемоглобин), MetHb (метгемоглобин) уравнение (2) записывается в следующем виде:
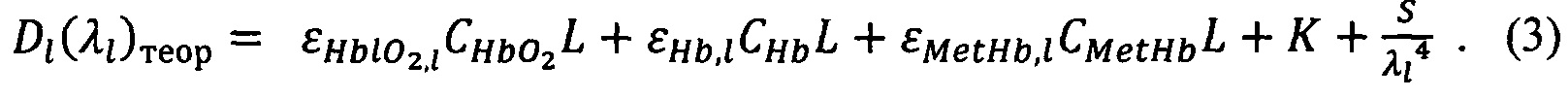
Данное уравнение может быть скорректировано для любого количества производных Hbh, которые необходимо принять во внимание.
Концентрацию общего Hb рассчитывают по формуле:
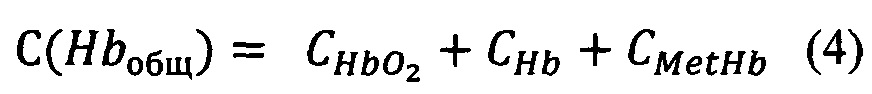
Правомерность предлагаемого авторами способа измерения концентрации Hb и его производных в крови была подтверждена результатами эксперимента, в котором были созданы условия, моделирующие изменения концентраций производных Hb. В соответствии с заявляемым способом было определено процентное содержание метгемоглобина и других производных Hb после воздействия нитрита натрия NaNO2 в различных концентрациях на кровь in vitro.
У пациента взяли цельную кровь в ходе профилактического осмотра, поместили в 3 микроветты с ЭДТА. В каждую микроветту капнули по 10 мкл раствора NaNO2 различной концентрации:
вариант 1 - 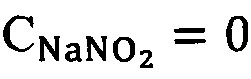 , вариант 2 -
, вариант 2 - 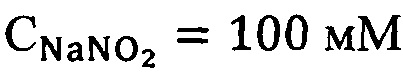 , вариант 3 -
, вариант 3 - 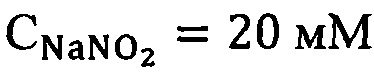 .
.
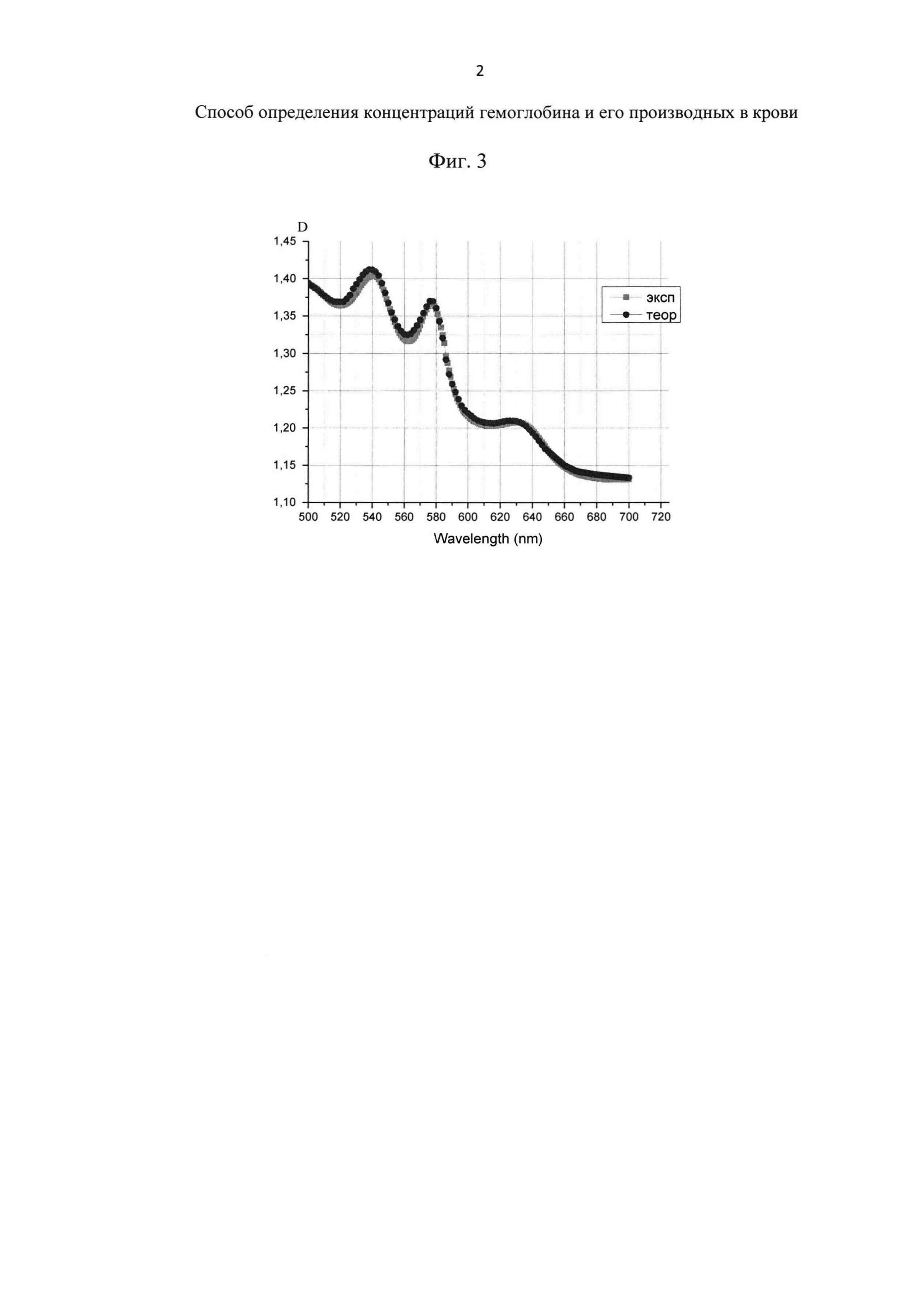
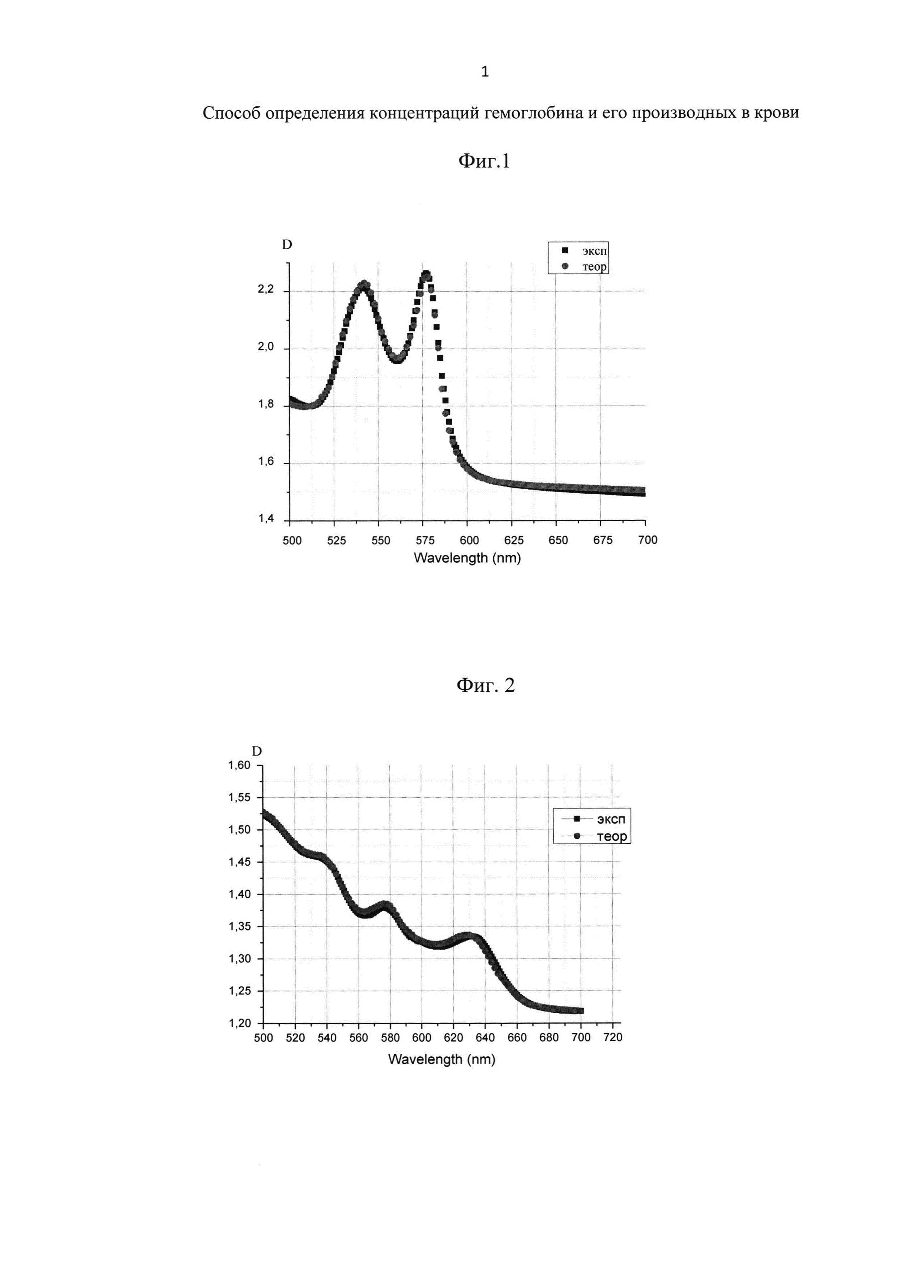
Затем 3 раза промыли суспензии в микроветтах буфером с помощью центрифуги (число оборотов 1500 мин-1, время центрифугирования 5 мин). Затем 15 мкл крови из одной микроветты капнули в измерительную кювету для спектрофотометра с буфером объемом Vбуфера=2,4 мл (PBS рН 7,4). В этом случае коэффициент разбавления составил 160. С помощью цифрового спектрофотометра Unico 2800 (USA) измерили спектр поглощения суспензии эритроцитов Dl(λl)экспер в диапазоне длин волн λ=500-700 нм, с точностью 1 нм. Процесс повторили для каждой из трех микроветт отдельно. На фиг. 1-3 приведены экспериментальные данные и соответствующие теоретические кривые, наилучшим способом аппроксимирующие опытные результаты. Как видно на представленных чертежах, спектры имеют разную форму, что обусловлено различным содержанием метгемоглобина, образующегося при воздействии NaNO2 различных концентраций. Концентрации производных Hbh, рассчитанные на основе оптимальной аппроксимации, и концентрация общего 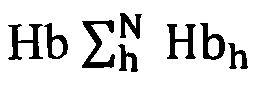 представлены в таблицах 1-3.
представлены в таблицах 1-3.
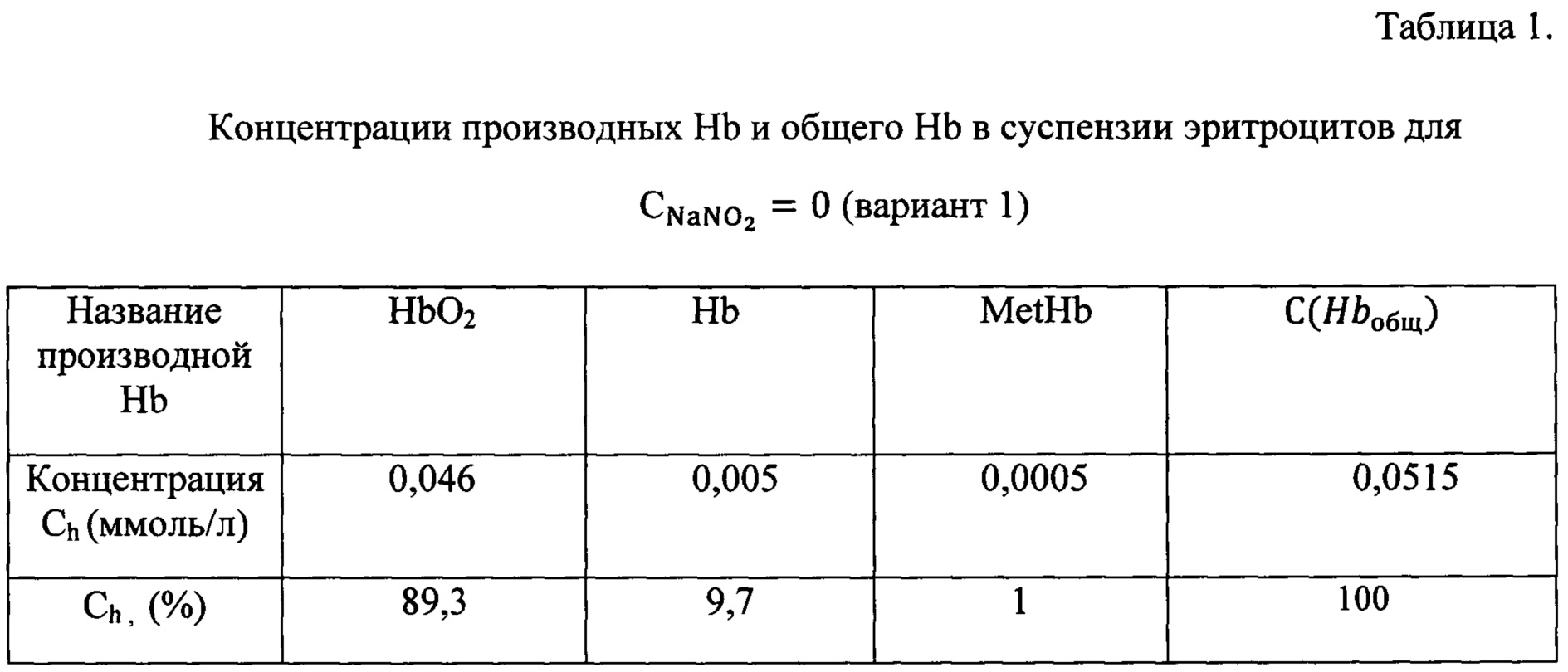
Как следует из данных, приведенных в таблице, концентрация общего Hb в крови составляет 0,0515 ммоль/л, что соответствует 133 г/л. Определенная в соответствии с заявляемым способом данная величина очень хорошо согласуется с результатами содержания Hb, измеренного на гематологическом анализаторе (132 г/л). Практически отсутствие метгемоглобина в крови также свидетельствует о соответствии результатов, полученных заявляемым способом, содержанию метгемоглобина в крови при физиологических условиях.
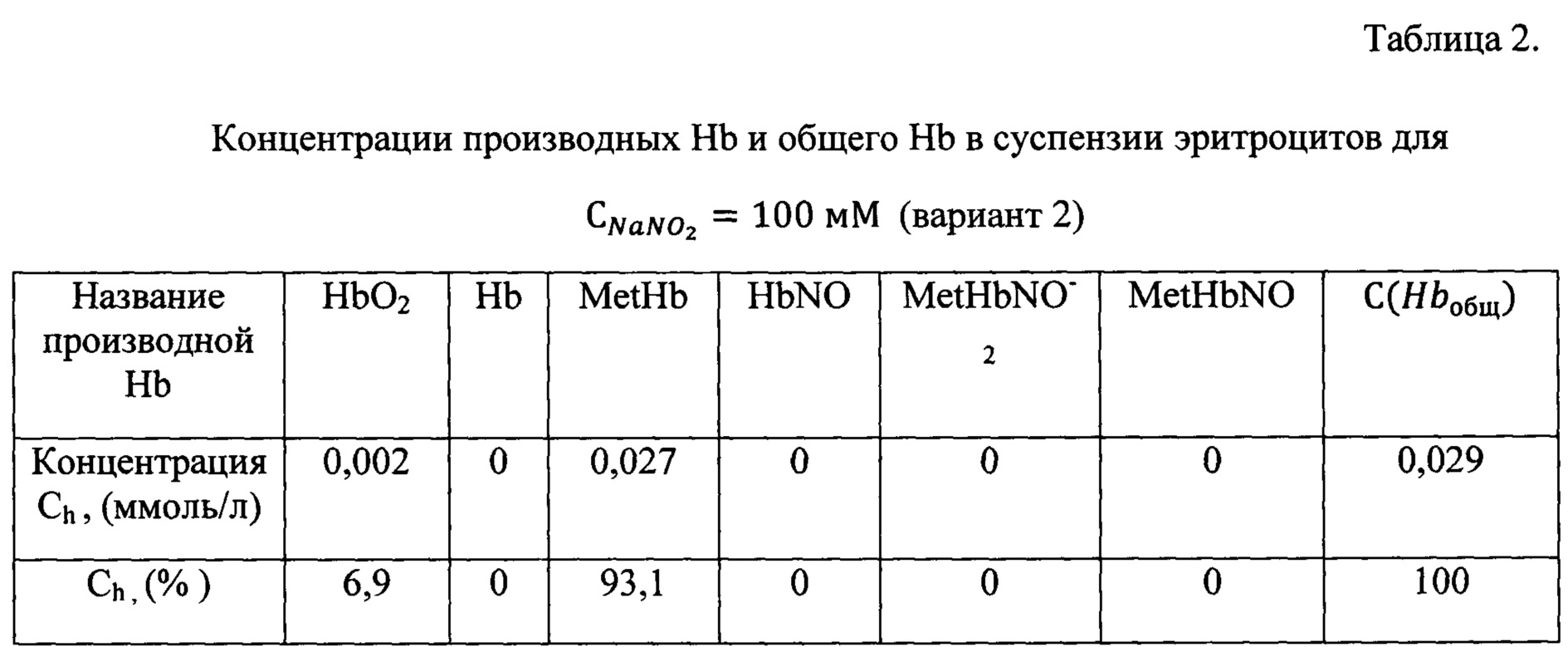
Известно, что при действии NaNO2 высокой концентрации почти весь Hb превращается в метгемоглобин. Кровь становится коричневой, Hb из двухвалентного превращается в трехвалентный и не присоединяет кислород. Как следует из данных таблицы 2, результаты, полученные предлагаемым способом, свидетельствуют о том, что в исследуемом образце присутствует почти 93% метгемоглобина. Это полностью соответствуют состоянию крови при таком сильно окислении Hb.
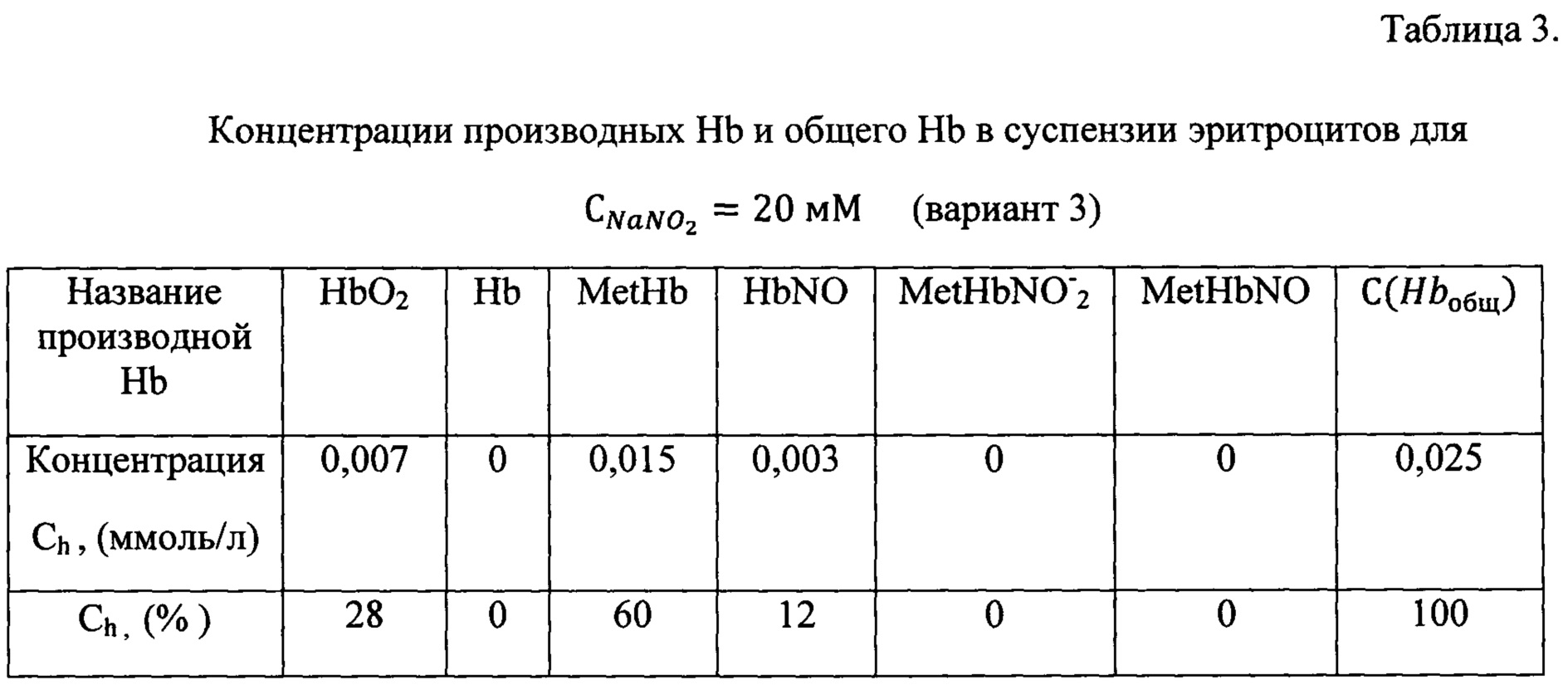
Как следует из данных таблицы 3, расчеты, выполненные на основе предлагаемого способа, свидетельствуют, что в этом случае происходит частичное превращение оксигемоглобина в метгемоглобин. При уменьшении концентрации NaNO2 в крови концентрация метгемоглобина уменьшается, а концентрация оксигемоглобина увеличивается по сравнению с вариантом 2. Это адекватно условиям и результатам биофизического эксперимента.
Таким образом, экспериментальные данные моделирования изменения состава крови, в частности изменения процентного содержания производных Hb, полностью подтверждают возможность и целесообразность использования заявляемого способа в лабораторной практике.
Заявляемый способ может быть с успехом использован при исследовании содержания других производных Hb, в частности при диагностике патологических состояний, например при отравлении нитритами, нитратами и др.
Имеется еще один нежелательный факт, связанный с гемолизом эритроцитов в воде. В крови могут присутствовать лекарственные препараты, вводимые пациенту во время лечения. Их действие на внутриклеточный Hb и свободный Hb в воде разное. Они способны окислить свободный Hb, что приведет к ложным результатам измерения производных Hb в крови у данного пациента. Поэтому для повышения точности результатов необходимо эритроциты при измерении спектра помещать в буфер. При этом необходимо использовать стандартный буфер для работы с кровью PBS 7,4. Таким образом, использование заявляемого способа в процессе лабораторной диагностики позволяет оценить динамику изменения концентраций производных Hb и общего Hb в процессе лечения, исключив фактор влияния лекарственного препарата, имеющегося в крови пациента и способного исказить картину наличия производных, на результаты измерений
С целью подтверждения необходимости учета эффекта рассеяния света на частицах в суспензии для повышения точности результатов исследования авторами заявляемого способа было проведено сравнение результатов оценки концентраций производных Hb с учетом рассеяния и без него для одного и того же контрольного образца крови (кровь здорового человека).
1. Экстраполяция экспериментальных данных проведена с учетом эффектов рассеяния по формуле:
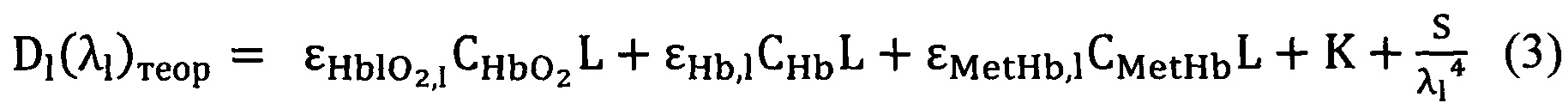
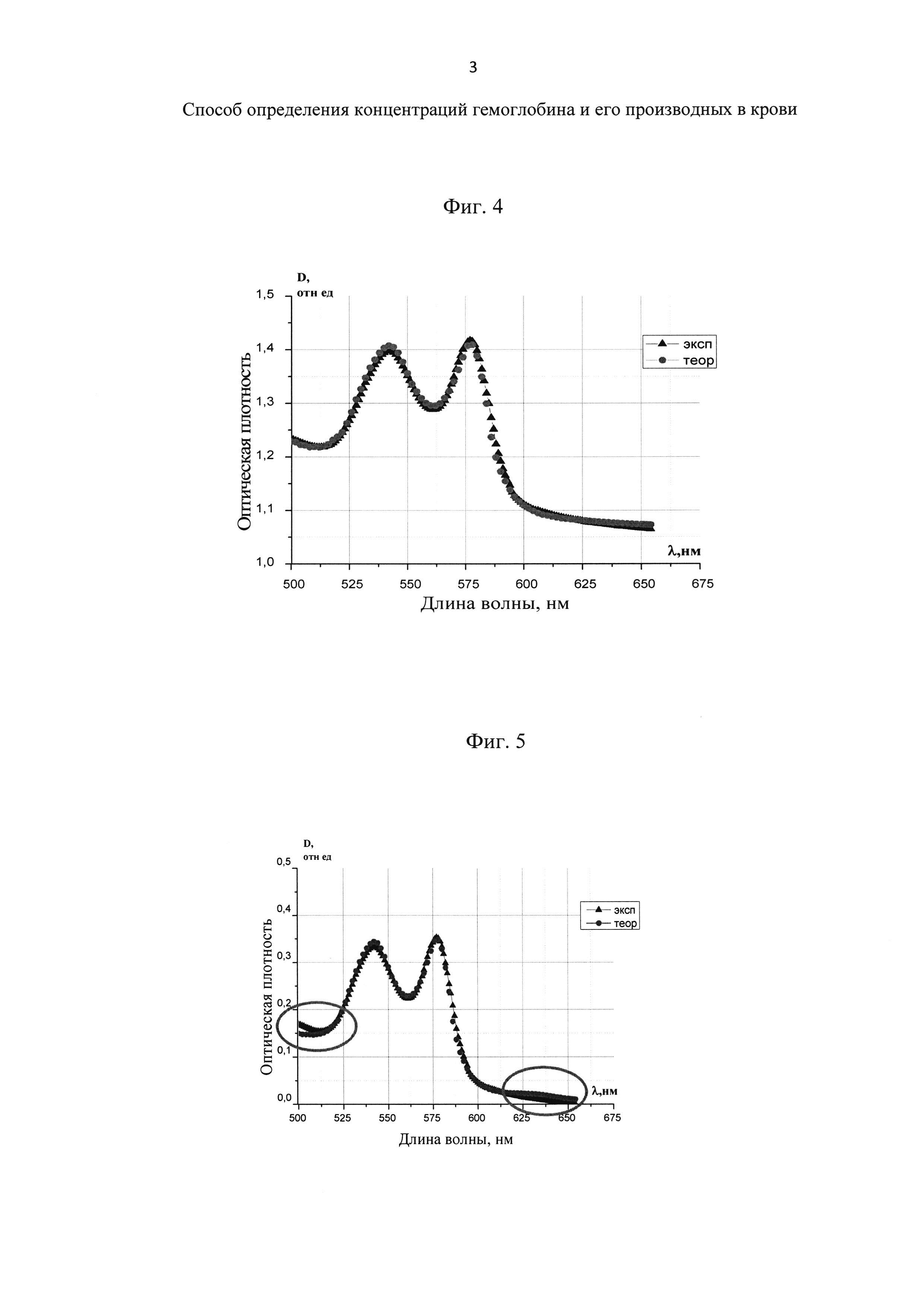
На фиг. 4 представлены результаты измерений Dl(λl)экспер (обозначены треугольниками) и Dl(λl)теор (обозначены кружками). Наблюдается очень хорошее совпадение теоретических и экспериментальных данных. Процентное содержание метгемоглобина составило 1,1%. Это полностью соответствует процентному содержанию метгемоглобина у человека в норме (0,2-1%). Полученные результаты также подтверждаются данными таблицы 4.

2. Экстраполяция тех же самых экспериментальных данных (вариант 1) проведена без учета эффектов рассеяния (коэффициент S=0) по формуле:
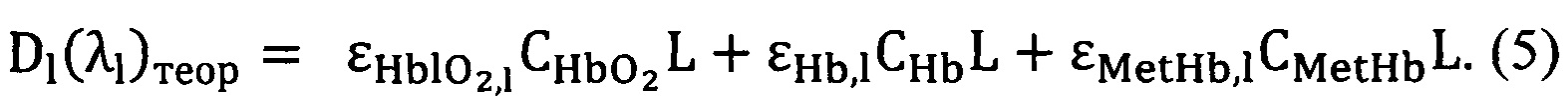
На фиг. 5 представлены результаты измерений Dl(λl)экспер (обозначены треугольниками) и Dl(λl)теор (обозначены кружками), отражающие существенное несовпадение теоретических и экспериментальных данных в ряде диапазонов длин волн. Рассчитанное процентное содержание метгемоглобина составило 12,3%. Это не соответствует содержанию метгемоглобина у человека в норме, а именно, превышает в 10 раз. Полученные результаты также подтверждаются данными таблицы 5.

Таким образом, учет эффекта рассеяния при аппроксимации экспериментальных данных позволяет повысить точность оценки процентного содержания производных Hb в крови здорового и больного человека. Получение достоверных результатов, адекватных действительности, позволяет проводить диагностику заболеваний на основе измерения концентраций производных Hb, в том числе метгемоглобина.
Краткое описание чертежей
На Фиг. 1 изображен спектр поглощения суспензии эритроцитов при 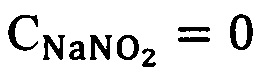 . Представлены экспериментальные данные и аппроксимирующая кривая.
. Представлены экспериментальные данные и аппроксимирующая кривая.
На Фиг. 2 изображен спектр поглощения суспензии эритроцитов при 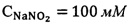 . Представлены экспериментальные данные и аппроксимирующая кривая.
. Представлены экспериментальные данные и аппроксимирующая кривая.
На Фиг. 3 изображен спектр поглощения суспензии эритроцитов при 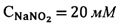 . Представлены экспериментальные данные и аппроксимирующая кривая.
. Представлены экспериментальные данные и аппроксимирующая кривая.
На Фиг. 4 изображен спектр поглощения суспензии эритроцитов (треугольники) и расчетный спектр аппроксимации (кружки) с учетом рассеяния.
На Фиг. 5 изображен спектр поглощения суспензии эритроцитов (треугольники) и расчетный спектр аппроксимации (кружки) без учета рассеяния. Кругами показаны области, где экспериментальные данные не совпадают с теоретическими.
Способ осуществляют следующим образом.
У пациента делают забор крови. Затем порцию крови объемом Vкрови=10-15 мкл капают в стандартную измерительную кювету для спектрофотометра с буфером объемом Vбуфера=2,4-3,0 мл (PBS рН 7,4). С помощью цифрового спектрофотометра измеряют спектр поглощения суспензии эритроцитов D(λ)эспер в диапазоне длин волн λ=500-700 нм, с точностью 0,5 нм. В спектре проявляются и эффекты поглощения и эффекты рассеяния света. Далее, используя стандартные программы статистической обработки экспериментальных данных (например, Origin Pro9 (USA)), эмпирический спектр аппроксимируют теоретической кривой, которая наилучшим способом вписывается в экспериментальную кривую. При этом учитывают поглощение света разными производными Hb, а также рэлеевское рассеяние света на частицах размером D<<λ (коэффициент S) и рассеяние света на частицах размером D≥λ (коэффициент K):
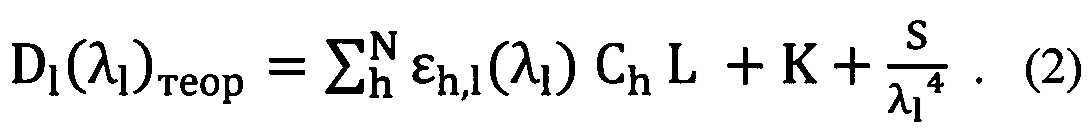
Теоретическую кривую Dl(λl)теор подбирают так, чтобы она оптимально вписывалась в экспериментальные данные Dl(λl)экспер. При построении аппроксимирующей кривой Dl(λl)теор стандартным методом нелинейной регрессии статус зависимой переменной присваивают искомой функции Dl(λl)экспер, независимыми переменными являются молярные показатели поглощения для каждой производной Hb на заданных длинах волн εh,l. Неизвестными являются концентрации Ch, коэффициентами K и S являются параметры модели и их подбирают так, чтобы теоретическая кривая Dl(λl)теор описывала бы экспериментальные данные Dl(λl)экспер наилучшим образом (R-square > 0,98). При аппроксимации должно быть выполнено условие Ci≥0.
Концентрации каждого из производных Hb Ch и концентрацию общего Hb в измеряемой суспензии С(Hbобщ) в ммол/л определяют по формуле:
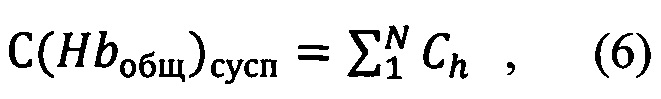
где С(Hbобщ)сусп - концентрация общего Hb в суспензии;
Ch - концентрация каждой производной гемоглобина;
N - количество производных Hb.
Концентрацию общего Hb в крови определяют по формуле:
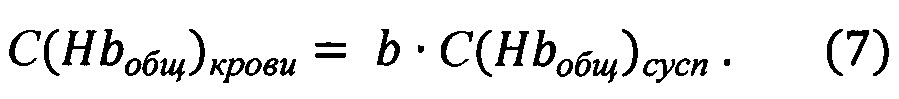
где С(Hbобщ)сусп - концентрация общего Hb в суспензии;
С(Hbобщ)крови - концентрация общего Hb в крови;
b=(Vкрови+Vбуфера)/Vкрови. - коэффициент разбавления суспензии;
Vкрови - объем крови в спектрофотометрической кювете;
Vбуфера - объем буфера в спектрофотометрической кювете при измерении спектра.
Для пересчета в единицы СИ (г/л) делят полученное значение в ммол/л на стандартный коэффициент пересчета 0,621 и умножают на 10 по формуле:
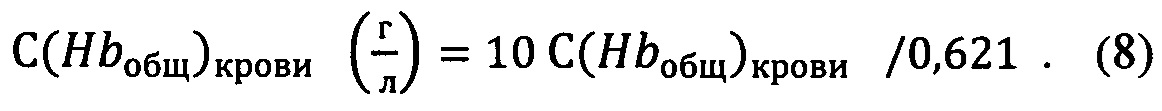
Находят процентное содержание каждой производной Hb по формуле:
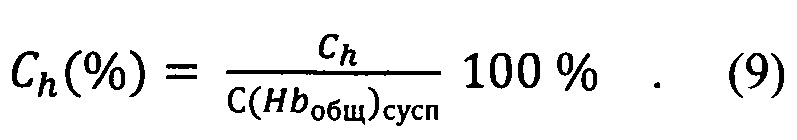
Примеры выполнения
1. Пациент А.
В ходе профилактического осмотра порцию цельной крови Vкрови=15 мкл поместили в измерительную кювету для спектрофотометра с буфером объемом Vбуфера=2,4 мл (PBS рН 7,4). С помощью цифрового спектрофотометра Unico 2800 (USA) измерили спектр поглощения суспензии эритроцитов D(λ)эспер в диапазоне длин волн λ=500-700 нм, с точностью 1 нм (фиг. 6).
Провели аппроксимацию экспериментальных данных теоретической кривой по формуле (3), оптимальная аппроксимация оказалась возможной при определенных концентрациях трех производных Hb и соответственно общего Hb (таблица 6).
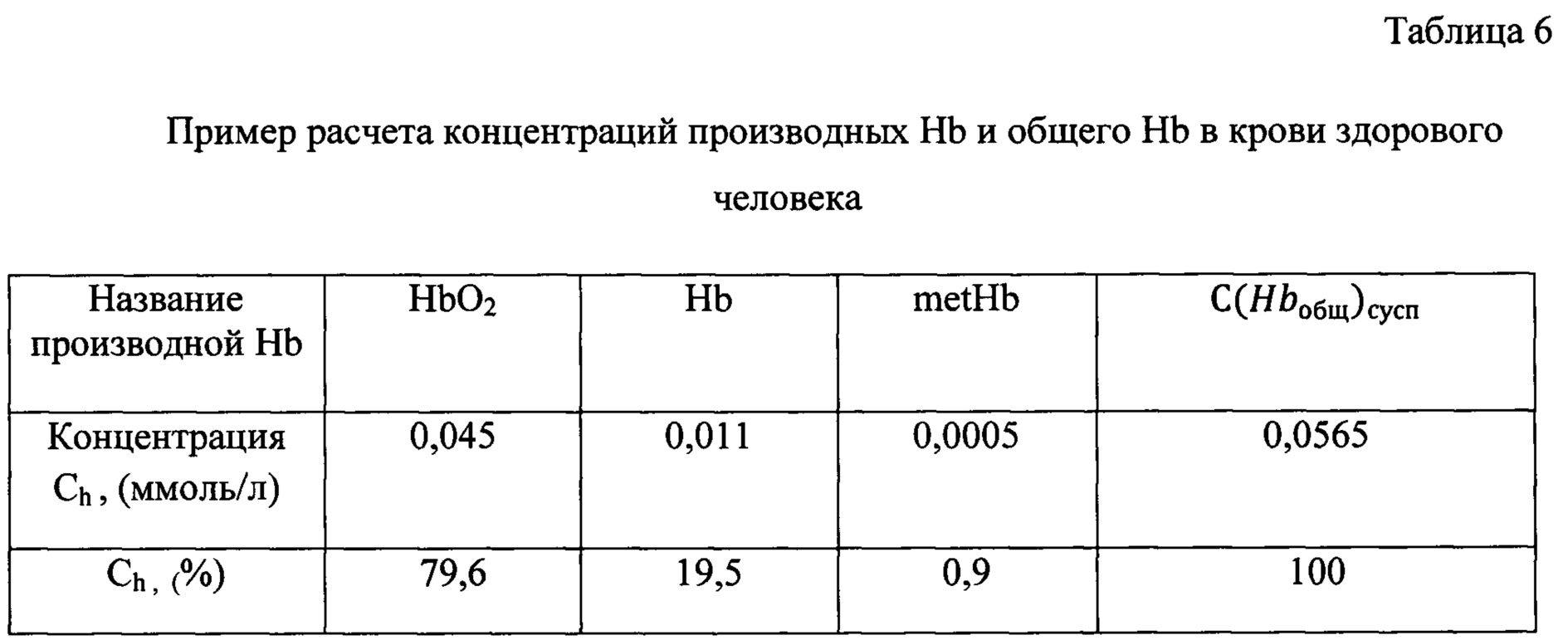
Из таблицы следует, что концентрация общего Hb в измеряемой суспензии составляет 0,0565 ммол/л. Коэффициент разбавления b=161. Концентрация общего Hb в крови с учетом формул (7, 8) равна 146 г/л.
Была измерена концентрация общего Hb на гематологическом анализаторе Advia 60 - СТ (Bayer, Germany) - 144 г/л. Относительная разность этих двух методов составила 1,5%.
Было рассчитано процентное содержание производных Hb в данном образце крови (по формуле 9), результаты представлены в таблице 6. Процентное содержание метгемоглобина в крови составило 0,9%, что очень хорошо согласуется с общепринятыми физиологическими данными.
2. Пациент В.
В ходе профилактического осмотра порцию цельной крови пациента Vкрови=15 мкл поместили в измерительную кювету для спектрофотометра с буфером объемом Vбуфера=2,4 мл (PBS рН 7,4). С помощью цифрового спектрофотометра Unico 2800 (USA) измерили спектр поглощения суспензии эритроцитов D(λ)эспер в диапазоне длин волн λ=500-700 нм, с точностью 1 нм.
Провели аппроксимацию экспериментальных данных теоретической кривой по формуле (3), оптимальная аппроксимация оказалась возможной при определенных концентрациях трех производных Hb и соответственно общего Hb (таблица 7).
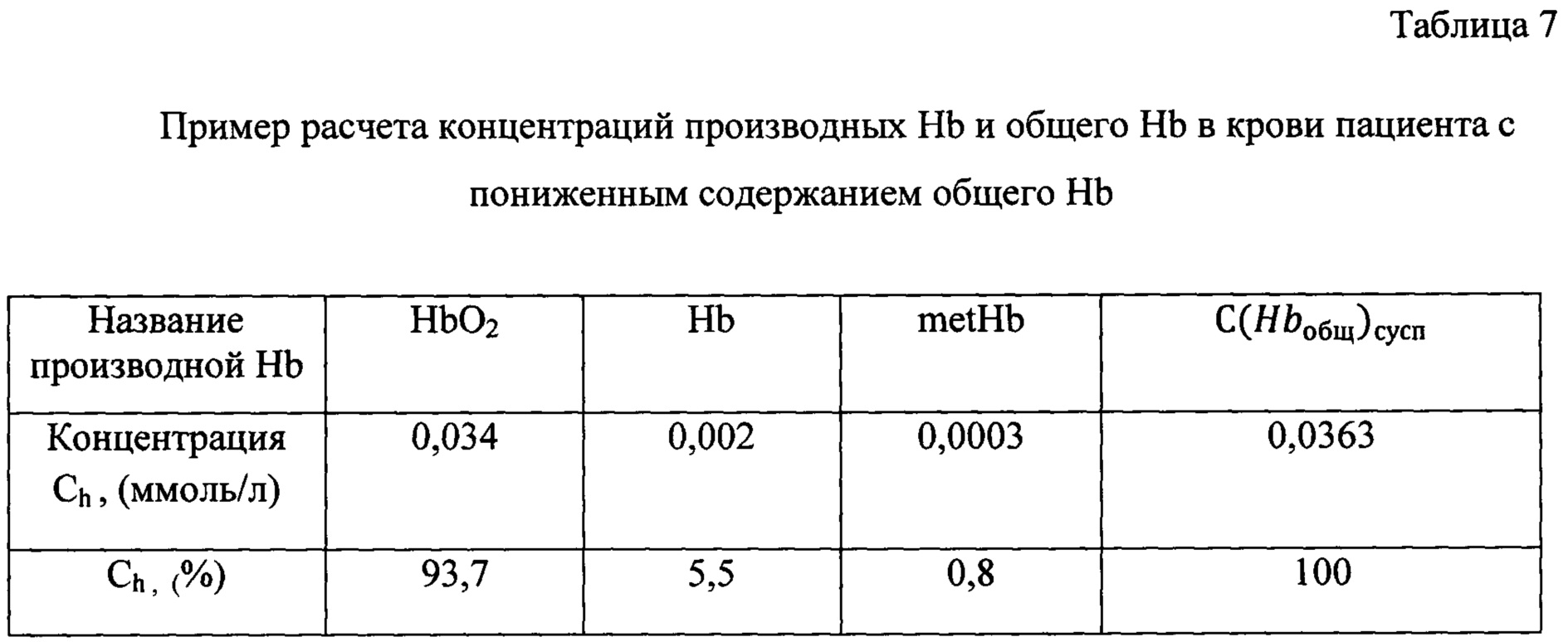
Из таблицы следует, что концентрация общего Hb в измеряемой суспензии составляет 0,0363 ммол/л. Коэффициент разбавления b=161. Концентрация общего Hb в крови с учетом формул (7, 8) равна 94 г/л.
Была измерена концентрация общего Hb на гематологическом анализаторе Advia 60 - СТ (Bayer, Germany) - 96 г/л. Относительная разность этих двух методов составила 1,5%.
Было рассчитано процентное содержание производных Hb в данном образце крови (по формуле 9), результаты представлены в таблице 6. Процентное содержание метгемоглобина в крови составило 0,8%, что очень хорошо согласуется с общепринятыми физиологическими данными.
Таким образом, заявляемый способ определения концентраций Hb и его производных в крови отвечает критериям охраноспособности и может найти широкое применение в лабораторной практике.