Результат интеллектуальной деятельности: Способ получения лиофилизата бортезомиба и фармацевтическая композиция, содержащая бортезомиб в форме стабильного лиофилизованного продукта, полученная указанным способом
Вид РИД
Изобретение
Настоящее изобретение касается способа получения лиофилизата бортезомиба и лиофилизата бортезомиба, в частности полученного вышеупомянутым способом, а также фармацевтической композиции, включающей этот лиофилизат.
Бортезомиб является модифицированной дипептидилбороновой кислотой с химическим названием [(1R)-3-метил-1-([((2S)-3-фенил-2[(пиразин-2-илкарбонил)амино]пропаноил]амино)бутил]бороновая кислота, также известной в данной области под названием "N-(2-пиразин)карбонил-L-фенилаланин-L-лейцин бороновая кислота". Бортезомиб имеет следующую структурную формулу
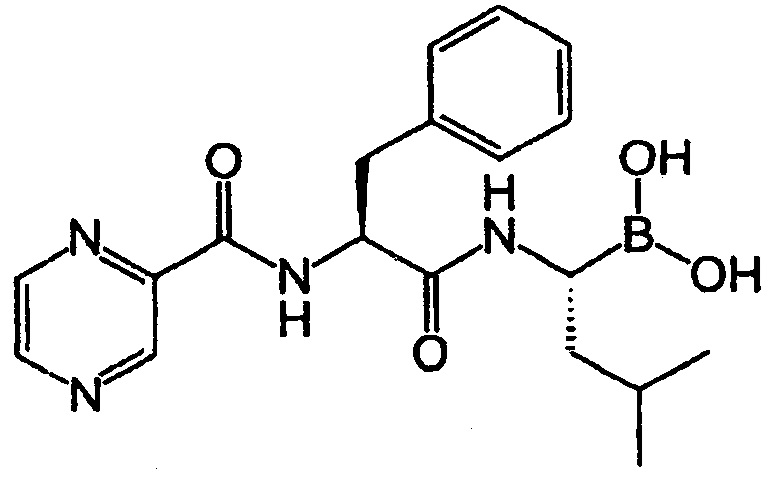
Известно, что бортезомиб обладает растворимостью ниже, чем 1 мг/мл в 0,9% (мас./об.) хлорида натрия. Он реализуется на рынке под торговым названием Velcade® для инъекций. Он используется в лиофилизированной форме, которая после восстановления влагосодержания образует раствор, состоящий из сложного эфира маннита в равновесии с бортезомибом. Как известно, бортезомиб является первым терапевтическим ингибитором протеазы, в частности, обратимым ингибитором сходной с химотрипсином активности 26S протеасомы в клетках млекопитающих. Он утвержден в США для лечения рецидивной множественной миеломы и лимфомы из клеток зоны мантии.
Фармацевтические композиции соединений бороновой кислоты, получаемые путем лиофилизации водной смеси, включающей соединение бороновой кислоты и соединение, включающее, по меньшей мере, две гидроксильных группы, раскрываются в документах WO 2002/059130 А1 и WO 2002/059131 А1. В документе WO 2010/039762 А2, очевидно, раскрываются устойчивые бессахарные фармацевтические композиции бортезомиба.
Для обеспечения достаточного растворения бортезомиба для лиофилизации в документе WO 2002/059130 А1 применяют воду и приблизительно 40% трет-бутанола в качестве сорастворителя. Однако применение большого количества дорогих органических сорастворителей, которые в торговой сети можно приобрести с ограниченной степенью очищения, например, приблизительно до 99,9%, невыгодно. Как правило, в лиофилизированном продукте остаются примеси сорастворителя, а также значительное количество остаточного сорастворителя. К тому же, применение большого количества растворителей невыгодно из-за того, что удаление растворителя в вакууме во время лиофилизации требует большого количества времени и энергии.
Как описывается в документах WO 2010/089768 А2, 12/08/2010, и WO 2010/039762 А2, 08.04.2010 А2, рецептирование бортезомиба связано со значительными проблемами, касающимися устойчивости и растворимости, в частности, из-за низкой растворимости бортезомиба в воде или 0,9% (объем/объем) растворе хлорида натрия.
Итак, существующая технология приготовления лиофилизата бортезомиба включает в себя растворение субстанции в трет-бутаноле. После растворения субстанции в раствор прибавляется вода и маннит. Трет-бутанол выбирается из соображений последующей лиофилизации раствора и как растворитель для субстанции (US 2002188100, 12.12.2002).
Также было установлено, что в субстанции бортезомиба одновременно могут присутствовать несколько ее кристаллических форм, в результате при растворении в водном манните, часть субстанции не растворяется, и визуально раствор может оставаться мутным, несмотря на увеличение температуры раствора и рН.
Тем не менее, есть способы перевести такую субстанцию в удобную для растворения форму.
Для этого, можно, например, подобрать растворитель для кристаллизации субстанции бортезомиба, из которого выкристаллизовывается нужная нам водорастворимая форма, например, метанол, другой вариант включает в себя растворение субстанции в хлористом метилене, и, упаривание раствора на роторном испарителе, после чего получается водорастворимая аморфная форма бортезомиба.
Бортезомиб, как было установлено, имеет рН зависимое растворение в воде, гораздо легче растворяясь при высоких значениях рН.
Такой подход реализован, например, в патенте WO 2010/089768 А2, 12.08.2010, где растворение субстанции бортезомиба проводят в среде с рН от 6,8 до 8,4, предпочтительно, от 7,9 до 8,1. Однако оказалось, что увеличение рН раствора более 6,5-6,7 приводит впоследствии к значительному увеличению примесей в лекарственной форме.
В патентной заявке WO 2010/089768, А2, при приготовлении раствора субстанции бортезомиба, для улучшения растворимости, проводят нагрев до 40-50°.
В этом документе WO 2010/089768 для преодоления этой проблемы с устойчивостью приготовление композиций включает бортезомиб и трометамин, с регулированием уровня рН в диапазоне от 6,8 до 8,4. Композицию получают путем смешивания бортезомиба и трометамина и добавления воды при непрерывном перемешивании. Раствор нагревают, обычно, до 45°C-50°C, для образования прозрачного раствора. Описывается, что полученный лиофилизат восстанавливает влагосодержание за 48 сек. Однако нагревание бортезомиба, который, согласно описанию, обладают низкой химической устойчивостью, невыгодно, поскольку нагревание обычно увеличивает скорость распада. К тому же, восстановление влагосодержания полученного лиофилизата не является предпочтительным.
В документе WO 2011/110286 также указывается на проблему собственной неустойчивости бортезомиба, в частности, его водных растворов. Для преодоления проблемы устойчивости растворов бортезомиба предлагаются, по существу, неводные жидкие композиции или композиции, в которых бортезомиб рецептирован с гетеро-бифункциональным основанием по Льюису в качестве донорного соединения. Однако неводные композиции невыгодны для получения фармацевтических композиций, в частности, для инъекций.
В другом патентном источнике ЕА 021179, 30.04.2015, раскрыт способ получения лиофилизата бортезомиба или его соли, или производной, который включает этапы:
a) приготовления водного раствора, включающего соединение, содержащее, по меньшей мере, две гидроксильных группы, разделенные, по меньшей мере, двумя соединительными атомами в цепи или кольце, или соединение, включающее гидроксильную группу и аминогруппу, разделенные, по меньшей мере, двумя соединительными атомами в цепи или кольце, причем система растворителя состоит из воды;
b) растворения бортезомиба или его соли, или производной в водном растворе, полученном на этапе а);
с) лиофилизации водного раствора, полученного на этапе b), необязательно после разбавления вышеупомянутого раствора водой.
Бортезомиб или его соль или производная (в дальнейшем - "бортезомиб"), применяемый в соответствии со способом настоящего изобретения, известен специалистам в данной области. Синтез бортезомиба описывается, например, в документах US 6617317 или WO 2005/097809 А2.
Соединение, имеющее по меньшей мере две гидроксильных группы, разделенные по меньшей мере двумя соединительными атомами в цепи или кольце, в контексте данного описания также называемое "дигидроксильным соединением", означает любое соединение, имеющее две или более гидроксильных групп, в котором две гидроксильных группы разделены по меньшей мере двумя соединительными атомами. Соединение, имеющее гидроксильную группу и аминогруппу, разделенные по меньшей мере двумя соединительными атомами в цепи или кольце, в контексте данного описания также называемое "аминогидроксильным соединением", означает любое соединение, имеющее по меньшей мере одну гидроксильную группу и по меньшей мере одну аминогруппу, разделенную по меньшей мере двумя соединительными атомами. Соединительные атомы дигидроксильного соединения или аминогидроксильного соединения могут быть в цепи или кольце, и цепь или кольцо могут включать атомы углерода и, необязательно, один или несколько гетероатомов, например, N, S или О. Примерами дигидроксильных соединений являются сахара, пинандиол, пинакол, перфторопинакол, этиленгликоль, диэтиленгликоль, катехол, 1,2-циклогександиол, 2,3-бутандиол, 1,2-бутандиол и глицерин. В предпочтительном варианте дигидроксильными соединениями являются сахара, более предпочтительно - моносахариды или дисахариды. Примерами подходящих сахаров являются глюкоза, сахароза, фруктоза, трегалоза, маннит и сорбит. В предпочтительном варианте применяемый сахар является восстановленным сахаром, общеизвестным как сахарный спирт такой, как маннит, сорбит, эритрит или пентаэритрит, наиболее предпочтительно - D-маннит.
Примерами аминогидроксильных соединений являются гидроксильные аминокислоты, аминоспирты и аминогидроксильные тиолы, в предпочтительном варианте - 2-аминоэтанол, серии, 2-амино-1,3-пропандиол, трометамин, цистеин или цистеинол (2-амино-3-гидрокси-пропан-1-тиол). В предпочтительном варианте аминогидроксильным соединением является 2-аминоэтанол, 2-амино-1,3-пропандиол, цистеин или цистеинол.
Система растворителя, применяемая для приготовления водного раствора дигидроксильного соединения или аминогидроксильного соединения на этапе а), является водной системой растворителя, включающей воду в качестве растворителя. Предполагается, что в системе растворителя также могут применяться до 10 мас.% сорастворителя, например, органического сорастворителя, или до 5 мас.%, или до 1 мас.% сорастворителя. Согласно известному изобретению, система растворителя по существу состоит из воды, то есть в системе растворителя присутствуют только до 0,1 мас.%, более предпочтительно - до 0,05 мас.%, в частности до 0,01 мас.% или менее, отличных от воды веществ. Как правило, применяют очищенную воду, в предпочтительном варианте - высокоочищенную воду (согласно Ph. Eur.). Таким образом, за исключением воды, другие сорастворители в системе растворителя присутствуют в малых количествах.
Согласно известному способу получения лиофилизата бортезомиба или его соли или производной, водный раствор дигидроксильного соединения или аминогидроксильного соединения в воде приготавливают на этапе а), в предпочтительном варианте - до полного растворения дигидроксильного соединения или аминогидроксильного соединения. Как правило, концентрация дигидроксильного соединения или аминогидроксильного соединения в водном растворе, приготовленном на этапе а), составляет, по меньшей мере, приблизительно 10 мг/мл, в предпочтительном варианте - по меньшей мере приблизительно 20 мг/мл, более предпочтительно - по меньшей мере приблизительно 25 мг/мл, в частности, по меньшей мере приблизительно 30 мг/мл, например, по меньшей мере приблизительно 50 мг/мл. Верхний предел концентрации дигидроксильного соединения или аминогидроксильного соединения может достигать предела растворимости соответствующего соединения в воде, как правило, до приблизительно 200 мг/мл, в предпочтительном варианте - до приблизительно 150 мг/мл, в частности, до приблизительно 100 мг/мл. Типичный диапазон концентрации дигидроксильного соединения или аминогидроксильного соединения в растворе, приготовленном на этапе а), составляет от приблизительно 10 до приблизительно 200 мг/мл, в предпочтительном варианте - от приблизительно 15 до приблизительно 180 мг/мл, более предпочтительно - от приблизительно 20 до приблизительно 150 мг/мл, в частности от приблизительно 25 до приблизительно 100 мг/мл, например от приблизительно 50 до приблизительно 100 мг/мл.
Согласно известному способу получения лиофилизата бортезомиба или его соли или производной, на этапе b) бортезомиб или его соль или производную, в частности, свободную кислоту бортезомиба, растворяют в водном растворе, полученном на этапе а). В предпочтительном варианте раствор бортезомиба растворяют в водном растворе, полученном на этапе а), при температуре ниже, чем приблизительно 30°C, в предпочтительном варианте - при комнатной температуре, то есть приблизительно 20°C, или ниже, более предпочтительно - приблизительно 15°C или ниже, в частности, приблизительно 10°C или ниже, например, приблизительно 5°C. В предпочтительном варианте раствор, полученный на этапе а), охлаждают до соответствующей температуры перед добавлением бортезомиба. Бортезомиб может применяться в твердой форме для растворения. В одном предпочтительном варианте осуществления бортезомиб суспендируют в воде, как правило, в массовом соотношении воды с бортезомибом от 10:1 до 1:1, в предпочтительном варианте - от 2:1 до 1:1, и суспензию добавляют к раствору, полученному на этапе а). Количество бортезомиба в растворе на этапе b) в предпочтительном варианте таково, что молярное соотношение дигидроксильного соединения или аминогидроксильного соединения с бортезомибом составляет от приблизительно 0,5:1 до приблизительно 100:1, более предпочтительно - от приблизительно 5:1 до приблизительно 100:1, в частности от приблизительно 10:1 до приблизительно 100:1, например приблизительно от 10:1 до 20:1.
Количество бортезомиба в растворе на этапе b) в предпочтительном варианте таково, что массовое соотношение дигидроксильного соединения или аминогидроксильного соединения с бортезомибом составляет от приблизительно 0,5:1 до приблизительно 100:1, более предпочтительно - от приблизительно 5:1 до приблизительно 100:1, в частности от приблизительно 10:1 до приблизительно 100:1, например приблизительно от 10:1 до 20:1.
В одном варианте осуществления известного способа раствор перед лиофилизацией может включать один или несколько фармацевтически приемлемых формообразующих, носителей, растворителей, наполнителей, солей, буферов, стабилизаторов или солюбилизаторов, как известно специалистам в данной области. В предпочтительном варианте при лиофилизации раствора ни один из дополнительных формообразующих или адъювантов не присутствует в водном растворе, за исключением бортезомиба и дигидроксильного соединения.
Этап лиофилизации с) осуществляют известным специалистам в данной области способом. Как правило, раствор, подлежащий лиофилизации, приготавливают для достижения полного растворения. После этого этапа осуществляют второй этап, на котором температуру значительно снижают, например, до уровня от приблизительно -80 до -20°C, в предпочтительном варианте - до уровня приблизительно от -40 до -15°C, и подают вакуум, как правило, приблизительно 100-200 мТорр. Сниженную температуру и вакуум, как правило, поддерживают от приблизительно 5 до приблизительно 24 часов.
После этого температуру, как правило, повышают до уровня от приблизительно 10 до приблизительно 25°C, например приблизительно 20°C, при поддержании или повышении вакуума, например до 20-50 мТорр, как правило, до существенного удаления остаточного растворителя.
В одном варианте осуществления известного способа раствор бортезомиба, включающий дигидроксильное соединение или аминогидроксильное соединение, полученный на этапе b), применяют на этапе лиофилизации с) без дальнейшего разбавления, то есть, без добавления дополнительной воды перед лиофилизацией. Таким образом, в этом варианте осуществления раствор, подвергаемый лиофилизации, имеет такую же концентрацию дигидроксильного соединения или аминогидроксильного соединения, как и на этапе а), как указано выше. В предпочтительном варианте осуществления перед подверганием раствора, полученного на этапе b), лиофилизации, вышеупомянутый раствор разбавляют путем добавления воды. В предпочтительном варианте достаточное количество воды добавляют для снижения концентрации дигидроксильного соединения или аминогидроксильного соединения до приблизительно 20 мг/мл или ниже, в предпочтительном варианте - приблизительно 15 мг/мл или ниже, в частности приблизительно 10 мг/мл или ниже, перед подверганием разбавленного раствора лиофилизации на этапе с).
Известное изобретение также касается лиофилизата, получаемого способом согласно данному изобретению. Полученный лиофилизат характеризуется низким количеством примесей, в частности деградантов бортезомиба, и быстрым восстановлением влагосодержания.
Кроме того, известное изобретение касается лиофилизата бортезомиба или его соли или производной, которые свободны от примесей от сорастворителя и не содержат сррастворителя.
Известное изобретение описывает также и фармацевтическую композицию, включающую лиофилизат согласно настоящему изобретению, в частности, лиофилизат, получаемый известным способом. Фармацевтическая композиция также может включать соответствующие формообразующие и адъюванты, известные специалистам в данной области.
Данное известное техническое решение по ЕА 021179 может быть выбрано в качестве ближайшего аналога (прототипа) заявленного изобретения.
Технической задачей заявленного изобретения является создание нового способа получения лиофилизата соединения бороновой кислоты бортезомиба либо его соли или производного, обеспечивающего получение более устойчивого (стабильного) и высокоочищенного целевого продукта - лиофилизата бортезомиба и обеспечивающего осуществление возможности контроля над проведением всех стадий процесса и условий их осуществления.
Таким образом, в соответствии с поставленной технической задачей достигаемый технический результат заключается в контролируемом процессе получения стабильного и высокоочищенного конечного целевого продукта - лиофилизата бортезомиба, и повышенной эффективности его при использовании в фармацевтической композиции в качестве активного действующего вещества. При этом при получении его способом по заявленному изобретению совершенно не используются органические растворители; при получении лиофилизата бортезомиба (субстанции бортезомиба) заявленным способом в качестве растворителя при получении растворов маннита, при растворении бортезомиба используют только воду. Исключение органического растворителя при растворении маннита, бортезомиба является одним из существенных преимуществ заявленного способа по сравнению с вышеуказанным патентом ЕА 021179, в котором предусмотрено использование органического растворителя, что уменьшает безопасность проведения процесса получения лиофилизата бортезомиба, а также способствует увеличению ненужных примесей.
Как указывалось выше, при описании уровня техники, является известным, что растворение бортезомиба в воде и, в частности, в водном растворе маннита, осуществляется легче и быстрее при высоких значениях рН от 6,8 до 8,4.
В заявленном в данном изобретении техническом решении задачи поддерживают рН на стадиях растворения маннита в воде и бортезомиба в водном растворе маннита, соответственно, рН в диапазоне от 4,0 до 5,0 и рН от 5,0 до 6,5.
Полученный заявленным способом бортезомиб (лиофилизат бортезомиба) характеризуется очень низким содержанием примесей, в частности, деградантов бортезомиба и быстрым восстановлением влагосодержания в водном растворе, например, в водном растворе хлорида натрия, в частности, 0,9-1,0%-ном растворе хлорида натрия (физиологический раствор).
Итак, поставленная техническая задача и полученный технический результат достигаются заявленным способом получения лиофилизата бортезомиба, включающим следующие стадии:
(a) приготовление водного раствора маннита до полного его растворения с концентрацией его в растворе 10-20 мг/мл при 0-60°С в течение 0,5-5,0 ч и поддержанием рН от 4,0 до 5,0.
(b) растворение субстанции бортезомиба в полученном водном растворе маннита в течение от 1,0 до 5,0 ч с получением концентрации бортезомиба в полученном растворе 1,0-2,5 мг/мл при 15-30°С при поддержании рН раствора в диапазоне рН в диапазоне от 5,0 до 6,5;
(c) стерилизующую фильтрацию раствора со стадии (б) с использованием фильтрации под вакуумом или фильтрации под давлением 0,1-0,6 МПа и дозирование его во флаконы;
(d) проведение лиофильной сушки продукта со стадии (с) в камере лиофильной сушки в несколько этапов в течение 24-72 ч, при этом осуществляют сначала первичную сушку в интервале температур (-30°C)-(-20°C), повышая температуру на полке в камере через каждые 30-60 мин на 0,5-5,0°C/ч, осуществляя таким образом циклы постепенного подъема температуры и выдержки при заданной температуре до достижения температуры (-5°C)-(-2°C),
- затем осуществляют выдержку при этой температуре в течение 0,5-5,0 ч, устанавливают далее температуру сушки в интервале от 0 до (-1°C), выдерживают при этой температуре 5-30 ч для удаления около 90 мас.% воды из продукта;
- затем проводят плавное повышение температуры со скоростью подъема 0,5-5,0°C/ч до достижения температуры полок камеры лиофильной сушки до 25-30°C в течение 5-25 ч и вакууме 1-150 м/Торр;
(f) заполнение камеры лиофильной сушки инертным газом, укупоривание флаконов и закатку их колпачками.
При этом, регулирование и контроль значений рН растворов на стадиях (а) и (b) при осуществлении способа по изобретению осуществляют с помощью гидроксида щелочного металла NaOH (гидроксида натрия) или КОН (гидроксида калия), например, путем дробного добавления раствора щелочи.
При получении лиофилизата бортезомиба используют субстанцию бортезомиба, представляющую собой свободную кислоту бортезомиба, или ее соль, или производную ее (в дальнейшем и «бортезомиб»).
В результате проведения многочисленных экспериментов было установлено влияние на достижение поставленного технического результата трех параметров при осуществлении способа, таких как время, температура и значение рН. За 1-5 ч, и в основном за 3 ч, происходит растворение бортезомиба в водном растворе маннита при рН от 5,0 до 6,5. Идеальное значение рН 5,7-6,0, чем выше рН тем лучше и быстрее происходит растворение бортезомиба в водном растворе маннита, но нами, в ходе работ, была выявлена зависимость при рН выше 6,5 в процессе хранения немного интенсивнее идет образование примесей бортезомиба в лекарственной форме (лиофилизате). Коррекцию и поддержание рН проводили путем дробного добавления раствора NaOH до достижения заданного значение показателя рН. Также известна зависимость растворения бортезомиба в растворе маннита и, в частности, чем выше температура, тем лучше и быстрее проходит его растворение, но при этом известно, что при повышении температуры также немного интенсивнее идет деградация бортезомиба с образованием примесей, поэтому весь процесс целесообразно проводить при температуре не выше 25°C, в среднем около 22-23°C. Растворение бортезомиба в растворе маннита проводилось в среде инертного газа - азоте.
Другим изобретением, заявленным в данной заявке, входящим в заявленную группу изобретений, является фармацевтическая композиция, содержащая бортезомиб в форме лиофилизованного продукта (лиофилизата), полученного способом, описанным выше, являющимся одним из изобретений заявленной группы, в терапевтически эффективных количествах и фармацевтически приемлемые носители.
При этом предпочтительно фармацевтическая композиция содержит лиофилизат полностью водорастворимой кристаллической формы субстанции бортезомиба.
Заявленная фармацевтическая композиция в качестве фармацевтически приемлемых носителей содержит воду очищенную, физиологический раствор (0,9-1,0%-ный водный раствор хлористого натрия).
Заявленная фармацевтическая композиция дополнительно может содержать различные вспомогательные целевые добавки, такие как буферы (лимонная кислота, уксусная кислота, винная кислота), антиоксиданты (например, бутилированный гидрокситолуол, бутилированный гидроксианизол, пропилгаллат, α-токоферол), гидрофильные антиоксиданты (натриевая ЭДТА, тиоглицерин, консерванты (фенол, тримерозал, хлорбутанол и др., например, в концентрации от 0,001 мас.% и до менее чем 5% масс./масс. от общей композиции) и другие общепринятые известные специалистам вспомогательные добавки (наполнители, криопротекторы, липопротекторы (например, аминокислоты), полимеры (желатин, альбумин) или смеси их в приемлемых количествах.
Полученный заявленным способом лиофизилат бортезомиба обладает повышенной стабильностью в течение продолжительного периода времени (по меньшей мере, 2-36 мес).
Заявленная фармацевтическая композиция может быть использована в терапевтически эффективных количествах для получения (или использована) при лечении злокачественных опухолей, (онкологических заболеваний).
Действующий активный фармацевтический ингрединет - Бортезомиб представляет собой высокоселективный обратимый ингибитор активности протеасомы 26S, представляет собой модифицированную бороновую кислоту.
Протеасома 26S присутствует в ядре и цитозоле всех эукариотических клеток и является ключевым компонентом, катализирующим расщепление основных белков, участвующих в управлении жизненным циклом клеток. Бортезомиб ингибирует химотрипсиноподобное действие протеасомы, вызывает торможение протеолиза и приводит к апоптозу.
Миеломные клетки почти в 1000 раз более восприимчивы к апоптозу, вызванному бортезомибом, чем нормальные клетки плазмы.
Основным фактором, объясняющим способность ингибитора протеасомы бортезомиба уничтожать клетки миеломы, является его способность блокировать активацию NF-kB. В нормальных клетках NF-kB (который существует как димер р50-р65) связан с ингибирующим белком LkB, который удерживает его в неактивной форме в цитозоли. Некоторые опухоли содержат активированные формы NF-kB, и протеасома играет важную роль в этом активировании, т.к. она катализирует протеолитическую генерацию подгруппы NF-kB р50 из неактивного предшественника р150 и разрушение ингибирующего белка LkB. Активированный NF-kB, проникая в ядро, помогает клетке выжить и пролиферировать. Ингибируя протеасому и, следовательно, тормозя активацию NF-kB, бортезомиб способствует уменьшению количества антиапоптозных факторов, воспалительных молекул, молекул клеточной адгезии (которые позволяют соединительным клеткам прикрепляться к клеткам костного мозга) и цитокинов (которые стимулируют рост клеток миеломы).
Бортезомиб вызывает замедление роста человеческих опухолей на многих экспериментальных моделях, включая множественную миелому.
Заявленный способ получения лиофилизата бортезомиба позволяет получить лиофилизат бортезомиба, который имеет чистоту, приблизительно, 99,80-99,85 мас.%.
Фармацевтическую композицию используют в виде раствора для инфузий или инъекций (после восстановления).
Полученный заявленным способом лиофилизат бортезомиба содержится в фармацевтической композиции в количестве, приблизительно от 0,01 до 99,0 мас.% от общей массы композиции.
Ниже приведены для иллюстрации заявленного изобретения примеры, не ограничивающие заявленное изобретение.
Пример 1.
Приготовление раствора лиофилизата субстанции бортезомиба на 1000 флаконов.
В приготовленную воду (очищенную воду) для инъекций (≈2000 г) в стеклянном реакторе при перемешивании добавляют маннит (≈35 г) до его полного растворения с получением концентрации маннита в растворе 10 мг/мл при 0°C в течение 4-5 ч и рН раствора в диапазоне рН=4-5.
Далее добавляют к полученному раствору маннита (с концентрацией 10 мг/мл) субстанцию бортезомиба (далее «бортезомиб») и проводят растворение его в течение 1 ч с получением раствора бортезомиба с концентрацией в растворе 1,0 мг/мл при 15°C и при поддержании рН раствора в диапазоне от 5,0 до 6,5 в среде иертного газа азота с получением концентрации бортезомиба 1,0 мг/мл.
Осуществляют стерилизующую фильтрацию полученного раствора бортезомиба в водном растворе маннита (под вакуумом) и последующую дозировку раствора по флаконам.
Далее осуществляют лиофильную сушку полученного раствора бортезомиба в камере лиофильной сушки в несколько этапов в течение 24 ч, при соблюдении следующих условий лиофильной сушки на каждом этапе:
- сначала проводят первичную сушку раствора при -20°C, повышая температуру на полках камеры лиофильной сушки через каждые 30-35 мин на 2,0°C/ч, осуществляя таким образом попеременные циклы постепенного подъема температуры и выдержки при этой температуре до достижения температуры до (-2°C).
Осуществляют выдержку при этой температуре в течение 3 ч. Далее устанавливают температуру сушки на полках камеры 0°C, выдерживают при этой температуре 30 ч для удаления около 90 мас.% воды из продукта.
Далее плавно повышают температуру сушки до достижения температуры на полках камеры лиофильной сушки до 25°C со скоростью подъема температуры 5°C/ч в течение 5 ч и вакууме 1-10 м/торр.
Заполняют камеру лиофильной сушки инертным газом (азотом), закупоривают флаконы и закатывают их колпачками.
Получают лиофилизат бортезомиба с чистотой продукта ≈99,80 мас.%.
Пример 2.
Процесс получения лиофилизата бортезомиба осуществляют аналогично примеру 1, но при варьировании условий осуществления процесса в пределах диапазонов температуры, времени и других условий, приведенных в формуле изобретения:
- готовят водный раствор маннита до полного растворения его с концентрацией раствора 20 мг/мл (при 60°C в течение 0,5 ч при рН=5,0);
- растворяют субстанцию бортезомина в полученном водном растворе маннита в течение 3,0-5,0 ч с получением раствора с концентрацией бортезомиба в нем 2,5 мг/мл при 23-25°C, рН раствора в диапазоне от 5,7 до 6,5 и в среде инертного газа азота;
- осуществляют стерилизационную фильтрацию раствора под давлением 0,1-0,6 МПа и дозирование его во флаконы.
При этом поддержание рН в указанных диапазонах осуществляют путем добавления, при необходимости, NaOH или KOH.
Проводят лиофильную сушку полученного раствора бортезомиба в течение 72 ч при соблюдении следующих условий:
- первоначальная сушка при (-30°С) при повышении температуры через каждые 60 мин на 5°С/ч до достижения температуры (-5°С);
- выдержка при этой температуре 0,5 ч;
- устанавливают температуру на полках камеры 0°С и выдерживают при этой температуре 0,5 часов до удаления около 90 мас.% воды из продукта.
Плавно повышают температуру до 30°С в течение 25 ч (со скоростью подъема температуры 0,5°С /ч в течение 25 ч в вакууме 150 м/Торр (или возможно 100 м/Торр). Заполняют камеру инертным газом (азотом); укупоривают флаконы и закатывают их колпачками.
Получают лиофилизат бортезомиба с чистотой 99,85 мас. %.
Лиофилизат бортезомиба восстанавливает влагосодержание быстро за 10-15 с после смешения его с водным раствором, в частности, 0,9% мас раствором хлорида натрия (физиологический раствор) при комнатной температуре, приблизительно при 20-23°C, получаю, по существу, фармкомпозицию на основе лиофилизата бортезомиба.
Фармкомпозиция может дополнительно содержать различные вспомогательные добавки (антиоксиданты, консерваторы, буферы и т.д., а также их смеси в приемлемых количествах, известных специалистам).
Таким образом, заявленный способ позволяет получить лиофилизат бортезомиба с высокой степенью чистоты, обладающий повышенной стабильностью с концентрацией бортезомиба в лиофилизате 1,0-2,5 мг/мл, что в итоге обеспечивает получение фармацевтической композиции, содержащей лиофилизат бортезомиба с повышенной устойчивостью и эффективностью при использовании ее.

