Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ РЕБАУДИОЗИДА M С ИСПОЛЬЗОВАНИЕМ ФЕРМЕНТАТИВНОГО СПОСОБА
Вид РИД
Изобретение
Область техники
Настоящее изобретение относится к способу получения ребаудиозида M и в частности к биологическому способу получения ребаудиозида M.
Предшествующий уровень техники
Подсластители представляют собой класс пищевых добавок, которые находят широкое применение в производстве пищевых продуктов, напитков и конфет. Их можно добавлять в способе получения пищевого продукта или альтернативно их можно использовать путем соответствующего разбавления в качестве заменителя сахарозы во время домашней выпечки. Подсластители включают натуральные подсластители, например сахарозу, кукурузный сироп с высоким содержанием фруктозы, мед и т.д., и искусственные подсластители, например аспартам, сахарин и т.д. Стевиозиды представляют собой класс натуральных подсластителей, экстрагируемых из растения Stevia rebaudkma и в настоящее время широко используются в пищевых продуктах и напитках. Экстракт Stevia rebaudkma содержит ряд стевиозидов, включая ребаудиозид. Экстрагируемые естественным образом стевиозиды характеризуются большим различием ингредиентов в различных партиях, и нуждаются в последующей очистке. Коммерчески производимый в настоящее время продукт ребаудиозид A содержит некоторые другие стевиозиды, например ребаудиозиды C, D и F, и т.д. Стевиозид, получаемый способ экстракции, как правило, дополнительно содержит некоторые примеси, смешанные с ним, которые оказывают определенное влияние на область его применения. Ребаудиозид M обладает преимуществами по сравнению с ребаудиозидом A, но его содержание в листьях Stevia rebaudkma является очень низким и его детектируют только в растении Stevia rebaudkma Morita (2010, J. Appl. Glycosci., 57, 199-209). В настоящее время не существует какого-либо промышленного производства ребаудиозида M.
Сущность изобретения
Техническая проблема, подлежащая решению в настоящем изобретении, заключается в предоставлении способа получения ребаудиозида M ферментативным способом для устранения недостатков известного уровня техники. Этим способом можно получать продукт ребаудиозида M высокой степени чистоты при более низких затратах за более короткий период времени.
Для решения указанной выше технической проблемы в настоящем изобретении применяют следующее техническое решение: способ получения ребаудиозида M ферментативным способом. В способе в качестве субстрата используют ребаудиозид A или ребаудиозид D; и в присутствии донора глюкозила ребаудиозид M получают путем взаимодействия субстрата при катализе UDP-глюкозилтрансферазы и/или рекомбинантных клеток, содержащих UDP-глюкозилтрансферазу.
По настоящему изобретению донор глюкозила может представлять собой UDP-глюкозу или систему регенерации UDP-глюкозы, состоящую из сахарозы, сахарозосинтетазы и UDP (2007, FEBS Letters, 581, 2562-2566), и предпочтительно систему регенерации UDP-глюкозы, состоящую из сахарозы, сахарозосинтетазы и UDP. UDP-глюкоза является более дорогостоящей, и применение системы регенерации UDP-глюкозы может значительно снижать затраты.
По настоящему изобретению UDP-глюкозилтрансфераза (т.е. уридиндифосфоглюкозилтрансфераза, сокращенно обозначаемая как UGT) является известной. Предпочтительно UDP-глюкозилтрансфераза, применяемая в настоящем изобретении, представляет собой UGT-A из Stevia rebaudkma и/или UGT-B из Oryza sativa.
Аминокислотная последовательность UGT-A может обладать по меньшей мере 60% идентичностью с последовательностью 2. Предпочтительно аминокислотная последовательность UGT-A обладает по меньшей мере 70% идентичностью с последовательностью 2. Кроме того, предпочтительно аминокислотная последовательность UGT-A обладает по меньшей мере 80% идентичностью с последовательностью 2. Наиболее предпочтительно аминокислотная последовательность UGT-A обладает по меньшей мере 90% идентичностью с последовательностью 2. По одному конкретному аспекту аминокислотная последовательность UGT-A является полностью идентичной последовательности 2.
Аминокислотная последовательность UGT-B может обладать по меньшей мере 60% идентичностью с последовательностью 4. Более предпочтительно аминокислотная последовательность UGT-B обладает по меньшей мере 70% идентичностью с последовательностью 4. Кроме того, предпочтительно аминокислотная последовательность UGT-B обладает по меньшей мере 80% идентичностью с последовательностью 4. Наиболее предпочтительно аминокислотная последовательность UGT-B обладает по меньшей мере 90% идентичностью с последовательностью 4. По одному конкретному аспекту аминокислотная последовательность UGT-B является полностью идентичной последовательности 4.
По настоящему изобретению реакцию можно проводить в водно-фазной системе при температуре от 4 до 50°C и значении pH от 5,0 до 9,0. Предпочтительно реакцию проводят в водно-фазной системе при температуре от 25 до 35°C и значении pH от 6,5 до 7,5.
Более предпочтительно реакцию проводят при температуре 30°C.
Более предпочтительно реакцию проводят при значении pH 7,0.
По одному конкретному предпочтительному аспекту реакцию проводят в фосфатном буфере при pH 7.
По настоящему изобретению, когда катализ проводят с применением рекомбинантных клеток, содержащих UDP-глюкозилтрансферазу, реакцию можно проводить в присутствии средств, способствующих проникновению в клетки. Предпочтительно средство, способствующее проникновению в клетки, представляет собой толуол в концентрации, которая может составлять от 1% до 3% по объемному отношению во всей реакционной смеси. Более предпочтительно концентрация толуола составляет 2% по объемному отношению.
По настоящему изобретению рекомбинантные клетки могут представлять собой и предпочтительно представляют собой клетки микроорганизмов, где микроорганизмы могут представлять собой и предпочтительно представляют собой Escherichia coli, Saccharomyces cerevisiae или Pichia pastoris и т.п.
По одному конкретному и предпочтительному аспекту способ получения проводят так, как указано ниже: все исходные вещества, применяемые в реакции, добавляют в реакционный котел, перемешивают до однородного состояния, затем помещают при указанной температуре и перемешивают для начала реакции. После завершения реакции можно получать продукт ребаудиозида Μ, соответствующий требованиям использования, путем обработки очисткой. В одном конкретном способе очистки можно получать продукт ребаудиозида Μ с чистотой до 95% в соответствии со способом очистки посредством дополнительной обработки, включающей разделение смолой.
По одному конкретному аспекту настоящего изобретения субстрат представляет собой ребаудиозид A, и UDP-глюкозилтрансфераза представляет собой смесь UGT-A из Stevia rebaudkma и UGT-B из Oryza sativa, где аминокислотная последовательность UGT-A из Stevia rebaudkma обладает по меньшей мере 80% идентичностью с последовательностью 2, и аминокислотная последовательность UGT-B из Oryza sativa обладает по меньшей мере 80% идентичностью с последовательностью 4. Предпочтительно массовое отношение в смеси UGT-A из Stevia rebaudkma и UGT-B из Oryza sativa составляет 1: от 0,8 до 1,2, например оно может составлять 1:1.
По одному другому конкретному аспекту настоящего изобретения субстрат представляет собой ребаудиозид D, и UDP-глюкозилтрансфераза представляет собой UGT-A из Stevia rebaudkma, где аминокислотная последовательность UGT-A из Stevia rebaudkma обладает по меньшей мере 80% идентичностью с последовательностью 2.
В результате реализация указанных выше технических решений настоящее изобретение обладает следующими ниже преимуществами по сравнению с известным уровнем техники.
Способ получения ребаудиозида M ферментативным способом, предоставленным в настоящем изобретении, имеет важное прикладное значение. Вследствие того, что скорость роста микроорганизмов является значительно выше чем скорость роста растений, способом получения по настоящему изобретению можно значительно снижать производственные затраты, можно сокращать цикл производства и можно значительно увеличивать конкурентоспособность продукта. Кроме того, стевиозид характеризуется низким содержанием в растениях и содержит относительно много стевиозидов с различными структурами таким образом, что экстракция более чистых продуктов является крайне затруднительной. В свою очередь применение способа синтеза с использованием ферментативного способа по настоящему изобретению способно обеспечивать продукты более высокой степени чистоты, что дополнительно расширит его область применения. По сравнению со способом экстракции ребаудиозида M из листьев Stevia rebaudkma способ по настоящему изобретению характеризуется значительно более коротким циклом производства, улучшенной производительностью, более низкими затратами и может обеспечивать продукты с более высокой степенью чистоты и таким образом его можно использовать с меньшими затратами в пищевой промышленности и промышленности напитков.
Краткое описание чертежей
Фиг. 1 представляет собой диаграмму протонного магнитного спектра продукта, получаемого в примере 5 по настоящему изобретению.
Подробное описание предпочтительных вариантов осуществления
Следующие ниже ребаудиозид A, ребаудиозид D и ребаудиозид M сокращенно обозначают соответственно как Reb A, Reb D и Reb M, где структурные формулы соответственно относятся к формулам I, II и III.
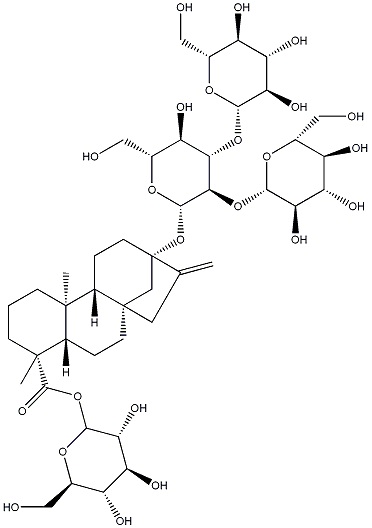 I;
I; 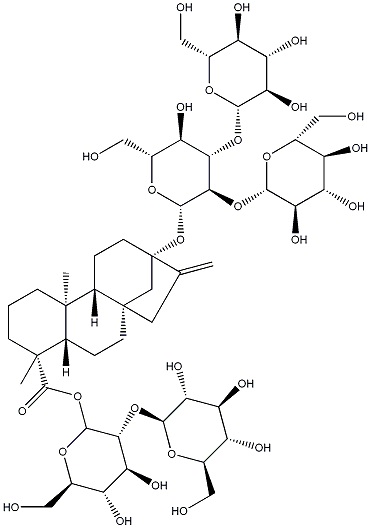 II;
II;
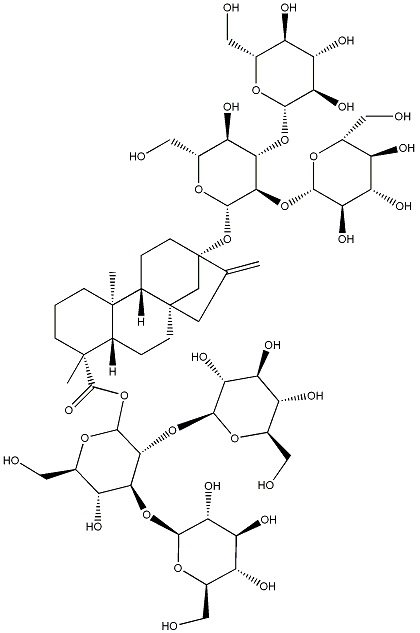 III.
III.
Настоящее изобретение относится в основном к четырем путям синтеза Reb M:
Способ 1:
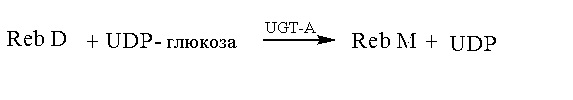
Способ 2:
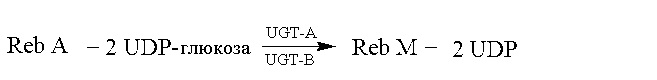
Способ 3:
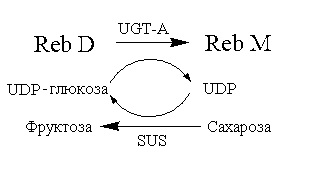
Способ 4:
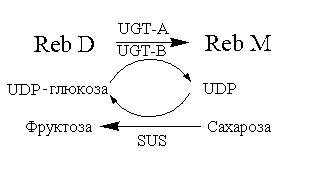 .
.
По настоящему изобретению применяемые UGT-A или UGT-B могут находиться в форме порошка лиофилизированного фермента или содержаться в рекомбинантных клетках.
UGT-A или UGT-B получают способом так, как указано ниже:
Рекомбинантные штаммы Escherichia coli (или других бактериальных клеток), экспрессирующие UGT-A или UGT-B, получают с использованием техник молекулярного клонирования и техник генетической инженерии. Затем рекомбинантные Escherichia coli подвергают ферментации для получения рекомбинантных клеток, содержащих UGT-A или UGT-B, или для получения лиофилизированных порошков UGT-A или UGT-B.
Все указанные выше техники молекулярного клонирования и техники генетической инженерии хорошо известны. Техники молекулярного клонирования можно найти в Molecular Cloing A Laboratory Manual. 3rd Edition, J. Shambrook, 2005.
Этапы экспрессии для конструирования рекомбинантных штаммов по настоящему изобретению с применением способа генетической инженерии являются такими, как указано ниже:
(1) (в соответствии с последовательностью 1 и последовательностью 2 или в соответствии с последовательностью 3 и последовательностью 4) генетически синтезируют необходимые фрагменты гена, лигируют в них векторы pUC57 и на оба конца добавляют участки рестрикции ферментов NdeI и BamHI соответственно;
(2) путем двойного ферментативного расщепления и лигирования каждый из фрагментов гена вводят в соответствующие участки ферментов рестрикции экспрессирующего вектора pET30a, чтобы обеспечивать возможность того, что каждый из генов находится под контролем промотора T7, и
(3) рекомбинантыми плазмидами трансформируют Escherichia coli BL21 (DE3) и индуцируют экспрессию целевых белков с использованием IPTG так, чтобы получать рекомбинантные штаммы Escherichia coli, экспрессирующие UGT-A или UGT-B.
Рекомбинантные клетки, содержащие UGT-A или UGT-B, или лиофилизированные порошки of UGT-A или UGT-B получают с использованием рекомбинантных экспрессионных штаммов Escherichia coli, содержащих UGT-A или UGT-B, посредством следующих ниже этапов.
Рекомбинантные экспрессионные штаммы Escherichia coli, содержащие UGT-A или UGT-B, инокулируют в 4 мл жидкой среды LB в количественном соотношении 1% и встряхивают (200 об/мин) при 37°C при культивировании в течение ночи. Культуру, которую культивировали в течение ночи, переносят в 50 мл жидкой среды LB при размере инокулята 1%. Среду для культивирования встряхивают (200 об./мин) при 37°C при культивировании до значения OD600 0,6-0,8. Затем добавляют IPTG в конечной концентрации 0,4 мМ и встряхивают смесь при 20°C при культивировании в течение ночи. После завершения индукции клетки собирают центрифугированием (8000 об/мин, 10 мин). Клетки ресуспендируют с использованием 5 мл 2 ммоль/л фосфатного буфера (pH 7,0) с получением рекомбинантных клеток или дополнительно разрушают с использованием ультразвука на ледяной бане с получением лиофилизированного порошка центрифугированием жидкости, подвергаемой обработке ультразвуком (8000 об/мин, 10 мин), сбором супернатант и лиофилизацией в течение 24 часов.
Настоящее изобретение более подробно описано ниже в сочетании с конкретными примерами.
Пример 1: получение рекомбинантных клеток Escherichia coli , содержащих UGT-A
В соответствии с последовательностью 1 и последовательностью 2 фрагменты гена UGT-A получали генетическим синтезом, к обоим концам добавляли участки ферментов рестрикции NdeI и BamHI соответственно и лигировали в них векторы pUC57 (Suzhou Genewiz Biotech Co., Ltd.). Фрагменты гена UGT подвергали ферментативному расщеплению рестрикционными эндонуклеазами NdeI и BamHI. Выделяли очищенные фрагменты. Добавляли к ним лигазу T4 и лигировали фрагменты в соответствующие участки ферментов рестрикции pET30a для трансформации штаммов BL21 (DE3).
Штаммы UGT инокулировали в 4 мл жидкой среды LB в количественном отношении 1% и встряхивали (200 об/мин) при 37°C при культивировании в течение ночи. Культуру, которую культивировали в течение ночи, переносили в 50 мл жидкой среды LB при размере инокулята 1%. Среду для культивирования встряхивали (200 об/мин) при 37°C при культивировании до значения OD600 0,6-0,8. Добавляли в нее IPTG в конечной концентрации 0,4 мМ и встряхивали смесь при 20°C при культивировании в течение ночи. После завершения индукции клетки собирали центрифугированием (8000 об/мин, 10 мин). Клетки ресуспендировали с использованием 5 мл 2 ммоль/л фосфатного буфера (pH 7,0) с получением рекомбинантных клеток, содержащих UGT-A для применения в катализе.
Пример 2: получение лиофилизированного порошка UGT-A
Рекомбинантные клетки UGT-A, получаемые в примере 1, разрушали с использованием ультразвука на ледяной бане с получением лиофилизированного порошка UGT-A центрифугированием жидкости, подвергаемой обработке ультразвуком (8000 об/мин, 10 мин), сбором супернатанта и лиофилизацией в течение 24 часов.
Пример 3: получение рекомбинантных клеток Escherichia coli , содержащих UGT-B
В соответствии с последовательностью 3 и последовательностью 4 фрагменты ген UGT-B получали генетическим синтезом, к обоим концам добавляли участки ферментов рестрикции NdeI и BamHI соответственно и лигировали в них векторы pUC57 (Suzhou Genewiz Biotech Co., Ltd.). Фрагменты гена UGT подвергали ферментативному расщеплению рестрикционными эндонуклеазами NdeI и BamHI. Выделяли очищенные фрагменты. Добавляли к ним лигазу T4 и лигировали фрагменты в соответствующие участки ферментов рестрикции pET30a для трансформации штаммов BL21 (DE3).
Штаммы UGT инокулировали в 4 мл жидкой среды LB в количественном отношении 1% и встряхивали (200 об/мин) при 37°C при культивировании в течение ночи. Культуру, которую культивировали в течение ночи, переносили в 50 мл жидкой среды LB при размере иноулята 1%. Среду для культивирования встряхивали (200 об/мин) при 37°C при культивировании до значения OD600 0,6-0,8. Добавляли к ним IPTG в конечной концентрации 0,4 мМ и встряхивали смесь при 20°C при культивировании в течение ночи. После завершения индукции клетки собирали центрифугированием (8000 об/мин, 10 мин). Клетки ресуспендировали с использованием 5 мл 2 ммоль/л фосфатного буфера (pH 7,0) с получением рекомбинантных клеток, содержащих UGT-B, для применения в катализе.
Пример 4: получение лиофилизированного порошка UGT-B
Рекомбинантные клетки UGT-B, получаемые в примере 3, разрушали с использованием ультразвука на ледяной бане с получением лиофилизированного порошка UGT-B центрифугированием жидкости, подвергаемой обработке ультразвуком (8000 об/мин, 10 мин), сбором супернатанта и лиофилизацией в течение 24 часов.
Пример 5: синтез Reb M ферментативным способом с Reb D в качестве субстрата (способ 1)
В этом примере в каталитическом синтезе Reb M использовали лиофилизированный порошок UGT-A, получаемый способом в примере 2.
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,255 г UDP-глюкозы, 0,17 г Reb D и 1,5 г лиофилизированного порошка UGT-A последовательно добавляли в реакционную смесь, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин с проведением реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%:80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb D составлял более 40% получали 0,054 г Reb M с чистотой более 95% после очистки последующими обработками, такими как разделение силикагелевой смолой, кристаллизация и т.д.
Пример 6: синтез Reb M ферментативным способом с Reb A в качестве субстрата (способ 2)
В этом примере в каталитическом синтезе Reb M использовали лиофилизированный порошок UGT-A, получаемый способом в примере 2, и лиофилизированный порошок UGT-B, получаемый способом в примере 4.
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,51 г UDP-глюкозы, 0,145 г Reb A и 1,5 г каждого из лиофилизированных порошков UGT-A и UGT-B последовательно добавляли в реакционную смесь, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин для проведения реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%:80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb A составлял более 40%. 0,05 г Reb M с чистотой более 95% получали после очистки последующими обработками, такими как разделение силикагелевой смолой, кристаллизация и т.д.
Пример 7: синтез Reb M ферментативным способом с Reb D в качестве субстрата (способ 3)
В этом примере в качестве донора глюкозила использовали систему регенерации UDP-глюкозы, состоящую из сахарозы, сахарозосинтетазы (AtSUS1 для краткого обозначения в дальнейшем) из Arabidopsis thaliana и UDP.
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,182 г UDP, 51,3 г сахарозы, 0,17 г Reb D, 1,5 г лиофилизированного порошка UGT-A и 0,5 г лиофилизированного порошка AtSUS1 последовательно добавляли в реакционную смесь, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин для проведения реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола, и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%:80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb D составлял более 80%. Получали 0,11 г Reb M с чистотой более 95% после очистки последующими обработками, такими как разделение силикагелевой смолой, кристаллизация и т.д.
Пример 8: синтез Reb M ферментативным способом с Reb A в качестве субстрата (способ 4)
В этом примере в качестве донора глюкозила использовали систему регенерации UDP-глюкозы, состоящую из сахарозы, сахарозосинтетазы (в дальнейшем обозначаемую как AtSUS1) из Arabidopsis thaliana и UDP.
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,364 г UDP, 51,3 г сахарозы, 0,145 г Reb A, 1,5 г каждого из UGT-A и UGT-B и 0,5 г лиофилизированного порошка AtSUS1 последовательно добавляли в реакционную смесь, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин для проведения реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%: 80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb A составлял более 80%. Получали 0,108 г Reb M с чистотой более 95% после очистки последующими обработками, такими как разделение силикагелевой смолой, кристаллизация и т.д.
Пример 9: синтез Reb M цельноклеточным каталитическим синтезом с Reb D в качестве субстрата
В этом примере в каталитическом синтезе использовали Reb M рекомбинантные клетки, содержащие UGT-A, получаемые способом в примере 1.
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,255 г UDP-глюкозы, 3 мл толуола, 0,17 г Reb D и 10 г рекомбинантных клеток, содержащих UGT-A, последовательно добавляли в реакционную смесь, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин для проведения реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола, и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%:80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb D составлял более 40%. Получали 0,052 г Reb M с чистотой более 95% после очистки последующими обработками, такими как, центрифугирование, разделение путем пропускания супернатанта через силикагелевую смолу, кристаллизация и т.д.
Пример 10: синтез Reb M цельноклеточным каталитическим синтезом с Reb A в качестве субстрата
150 мл 0,05 моль/л фосфатного буфера (pH 7,0), 0,51 г UDP-глюкозы, 3 мл толуола, 0,145 г Reb A и 10 г целых клеток, содержащих UGT-A и UGT-B, одновременно последовательно добавляли в реакционный раствор, перемешивали до однородного состояния, затем помещали на водяную баню при 30°C и перемешивали при 160 об/мин для проведения реакции в течение 2 часов. После завершения реакции отбирали 500 мкл реакционного раствора и добавляли в равный объем безводного метанола и перемешивали до однородного состояния. Смесь центрифугировали в течение 10 мин при 8000 об/мин. Супернатант отбирали и пропускали через мембрану фильтра с последующей детекцией с использованием высокоэффективной жидкостной хроматографии (хроматографические условия: хроматографическая колонка: Agilent eclipse sb-C18 4,6×250 мм; длина волны детекции: 210 нм; подвижная фаза: 1% водный раствор муравьиной кислоты:метанол=20%:80%; скорость потока: 1,0 мл/мин; температура колонки: 25°C). Показатель преобразования Reb A составлял более 40%. Получали 0,05 г Reb M с чистотой более 95% после очистки последующими обработками, такими как центрифугирование, разделение путем пропускания супернатанта через силикагелевую смолу, кристаллизация и т.д.
Указанные выше примеры используют только для описания технической концепции и признака настоящего изобретения, для обеспечения возможности понимания специалистом в данной области и таким образом осуществления содержания настоящего изобретения, а не ограничения объема патентной защиты настоящего изобретения. Любые эквивалентные изменения или модификации, проводимые в рамках объема и сущности настоящего изобретения, должны быть включены в объем патентной защиты настоящего изобретения.








