Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ МИКРО-МЕЗОПОРИСТОГО ЦЕОЛИТА Y И ЦЕОЛИТ, ПОЛУЧЕННЫЙ ЭТИМ СПОСОБОМ
Вид РИД
Изобретение
Изобретение относится к неорганической химии, в частности к способам получения кристаллических цеолитных материалов, обладающих микро-мезопористой структурой и кислотными свойствами.
Цеолит Y используется в качестве компонента катализаторов процессов нефтепереработки, нефтехимии и органического синтеза. Микропористая структура цеолита Y образована системой каналов размером 0,7 нм, соединяющих полости размером 1,3 нм. Размер канала в кристаллической структуре цеолита Y накладывает ограничения на размеры молекул, способных проникнуть внутрь цеолитного кристалла. В результате стерических ограничений в процессе каталитических превращений эффективно используются лишь приповерхностные слои цеолитного кристалла. В связи с этим практическую важность имеют способы регулирования текстурных свойств цеолитов с целью эффективного использования объема кристалла цеолита и обеспечения доступности реагентов к активным центрам цеолита и отвода продуктов реакции.
Каталитическая активность цеолита Y обусловлена совокупностью его кислотных и текстурных свойств. Кислотные центры в цеолите Y связаны с атомами алюминия в кристаллическом каркасе цеолита и распределены равномерно по объему цеолитного кристалла. Каталитические свойства цеолита Y зависят как от концентрации кислотных центров, так и от их типа. Описано, что для использования цеолита Y в качестве компонента катализатора процесса каталитического крекинга ключевым моментом является наличие двух типов кислотных центров, которые дифференцируются с использованием метода термопрограммированной десорбции (ТПД) аммиака как слабые и сильные центры, как показано в [М.-Y. He. The development of catalytic cracking catalyst: acidic property related catalytic performance. - Catalysis Today. - 2002. - v. 73. - p. 49-55] или с использованием ИК-спектроскопии адсорбированной молекулы-зонда пиридина, как Льюисовские и Бренстедовские центры, как показано в [D. Chen, S. Sharma, N. Cardona-Vartinez et al. Acidity Studies of fluid cracking catalysts by microcalorimetry and infrared spectroscopy. - Journal of Catalysis. - 1992. - V. 136. - Р. 392-402].
Описаны и широко используются на практике приемы регулирования кислотных свойств цеолита Y путем частичного деалюминирования цеолитного каркаса [Дж. Рабо. Химия цеолитов и катализа на цеолитах. - В 2-х томах. – Пер. с англ. - М. - Мир. - 1980]. Экстракция алюминия из тетраэдрических позиций каркаса происходит в результате термического и химического (кислотного) воздействия на цеолитный материал. Одновременно с деалюминированием в результате частичного разрушения кристаллического каркаса формируются мезопоры, способные облегчить транспорт реагентов и продуктов реакции. Однако образующиеся мезопоры по своей конфигурации (полости и нерегулярные поры с широким распределением по размеру) и локализации (каверны на поверхности кристалла или малодоступные полости в объеме кристалла) не являются оптимальными. Кроме того, доля мезопор в объеме пор цеолита определяется глубиной деалюминирования, поэтому достижение значительных объемов мезопор в деалюминированном цеолите Y сопряжено с уменьшением концентрации алюминия в цеолите и, следовательно, с уменьшением количества кислотных центров. В результате деалюминирования цеолита Y формируется спектр кислотности цеолита, в котором значительную долю составляют сильные кислотные центры, обладающие сильными крекирующими свойствами.
Описан прием регулирования текстурных характеристик деалюминированного цеолита Y путем щелочной обработки цеолита, приводящий к десилилированию цеолитного материала [K.P. de Jong, J. Zecevic, H. Friedrich et al. Zeolite Y crystals with trimodal porosity as ideal hydrocracking catalysts. - Angew. Chem. 2010. - V. 122. - Р. 10272-10276]. В результате щелочного воздействия на деалюминированный цеолит Y формируется материал, пористая структура которого образована цеолитными микропорами, небольшими мезопорами размером 2-8 нм и крупными мезопорами размером 8-50 нм. Образование развитой пористой структуры сопровождается ростом соотношения слабых и сильных кислотных центров в пользу слабых центров. На основе носителя с измененной кислотностью и тримодальной пористостью получены высокоэффективные катализаторы гидрокрекинга: платиносодержащий катализатор гидрокрекинга гексадекана и сквалана и никель-молибденсодержащий катализатор гидрокрекинга вакуумного газойля.
Описано, что регулирование спектра кислотности цеолитного носителя в составе катализатора гидрокрекинга высокомолекулярных продуктов синтеза Фишера-Тропша позволяет направленно изменять выход продуктов гидрокрекинга [T. Hanaoka, T. Miyazawa, K. Shimura, S. Hirata. Effect of catalyst preparation on hydrocarbon product distribution in hydrocracking of Fisher-Tropsch product with low Pt-loaded Catalysts. - Catalysis. - 2015. - V. 5 - Р. 1983-2000]. Показано, что при дифференциации кислотных центров по данным ТПД аммиака на слабые центры с температурой десорбции 100-250°С, центры средней силы с температурой десорбции 250-450°С и сильные центры с температурой десорбции 450-800°С существует прямая зависимость между ростом количества центров средней силы в катализаторе и увеличением выходов групп углеводородов С1-С8 и C9-C15.
Анализ предшествующего уровня техники по типам и способам получения микро-мезопористых цеолитных материалов с регулируемой совокупностью текстурных и кислотных характеристик позволил обнаружить два существующих подхода.
Известен способ получения цеолита Y с внутрикристалличной тримодальной пористостью, образованной микропорами размером 0,7 нм и мезопорами двух типов 2-5 и 10-50 нм, предусматривающий суспендирование деалюминированного цеолита Y с отношением Si/Al=6-40 в растворе, содержащем гидроксид натрия или гидроксид калия, или карбонат натрия, или цитрат натрия с концентрацией 0,001-0,5 М, обработку цеолита в этом растворе при температуре окружающей среды с последующей фильтрацией, промывкой, сушкой, ионным обменом, промывкой, сушкой и прокаливанием (RU 2510293, 22.12.2009). В результате достигается регулирование текстурных и кислотных характеристик цеолита Y, заключающихся в увеличении объема мезопор на 0,05-0,21 мл/г и в уменьшении кислотности, измеренной методом термопрограммированной десорбции (ТПД) аммиака, на 0,05-0,10 ммоль/г.
Существенным недостатком данного способа является растворение и переход в раствор цеолитного материала с потерями цеолита 17-25% масс, что фиксируется по уменьшению объема микропор на 0,075-0,15 мл/г и уменьшению отношения Si/Al на 2-10 единиц.
Наиболее близкими по технической сущности и достигаемому результату являются способ получения цеолитного материала с микро-мезопористой структурой и кристаллической структурой исходного силиката, и цеолит, полученный этим способом, обладающий кислотными центрами с энергией активации десорбции аммиака 140-190 кДж/моль, доля которых в общем спектре кислотности составляет не менее 0,5, и развитой регулярной пористой структурой с объемом пор не менее 0,45 см3/г, в котором доля микропор составляет 0,01-0,60, а доля мезопор составляет 0,10,-0,85 (RU 2282587, 08.04.2005). Способ предусматривает суспендирование микропористого кристаллического силиката с цеолитной структурой в щелочном растворе с концентрацией гидроксид-ионов 0,2-0,3 моль/л до достижения остаточного содержания цеолитной фазы в суспензии 1-60% масс., введение в суспензию силиката катионного поверхностно-активного вещества с последующим добавлением кислоты до образования геля с pH=7,5-9,0, гидротермальную обработку геля при 100-150°С в течение 10-120 ч с последующим выделением готового продукта.
Недостатком данного способа является его многостадийность, необходимость длительной гидротермальной обработки, формирование мезопористой фазы за счет растворения исходного силиката, а также значительная доля сильных кислотных центров с энергией активации десорбции аммиака 140-190 кДж/моль.
В основу настоящего изобретения положена задача создания нового типа микро-мезопористого цеолита Y, обладающего совокупностью таких кислотных и текстурных характеристик, которые позволили бы эффективно его применять в каталитических превращениях крупных органических молекул, в том числе в процессе гидрокрекинга вакуумного газойля, состоящего из объемных молекул с числом атомов углерода до 20-25, а именно наличием кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль, доля которых в общем спектре кислотности составляет 0,5-0,6, и бимодальной пористой структурой с микропорами 0,7 нм и мезопорами 2-10 нм.
Решение поставленной задачи достигается тем, что предлагается способ получения микро-мезопористого цеолита Y, включающий суспендирование и активацию деалюминированного цеолита Y в растворе гидроксида аммония с последующим смешением суспензии с катионным поверхностно-активным веществом ПАВ-галогенидом цетилтриметиламмония, гидротермальной обработкой в его присутствии, сушкой, прокаливанием и выделением готового продукта, согласно которому концентрацию раствора гидроксида аммония и галогенида цетилтриметиламмония выбирают так, чтобы обеспечить отношение ОН/цеолит 10-25 ммоль/г, отношение ПАВ/цеолит 0,8-2,0 ммоль/г, отношение H2O/цеолит 1,8-3,6 моль/г, а гидротермальную обработку проводят при температуре 60-95°С и атмосферном давлении в течение 1-1,5 ч.
Решение поставленной задачи также достигается тем, что предлагается микро-мезопористый цеолит Y – компонент катализатора гидрокрекинга вакуумного газойля, полученный указанным способом, при этом доля мезопор в его общем объеме пор составляет 0,5-0,7, а в его спектре кислотности доля кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль составляет 0,5-0,6.
Предлагаемый способ позволяет получать микро-мезопористый цеолит Y, обладающий кислотными центрами с энергией активации десорбции аммиака 95-140 кДж/моль, концентрация которых в 1,1-1,3 раза выше, чем в исходном деалюминированном цеолите Y, и пористой структурой с долей мезопор в общем объеме пор в 1,25-1,75 раза больше, чем у него. Достижение заявляемых характеристик кислотности и текстуры происходит в результате процесса частичной рекристаллизации микропористой цеолитной структуры деалюминированного цеолита Y под совокупным воздействием гидроксида аммония и катионного ПАВ в ходе процедур активации и гидротермальной обработки.
Исходный деалюминированный цеолит Y суспендируют в растворе гидроксида аммония с концентрацией, обеспечивающей отношение ОН/цеолит 10-25 ммоль/г. В ходе активации цеолита при перемешивании суспензии при комнатной температуре в течение 20-30 мин происходит частичный разрыв связей Si-О-Si в кристалле цеолита, что в дальнейшем облегчает проникновение молекул и мицелл ПАВ в объем цеолитного кристалла. При отношении ОН/цеолит < 10 ммоль/г процесс активации цеолита замедляется, при отношении ОН/цеолит > 25 ммоль/г процесс деструкции цеолита Y интенсифицируется, в результате чего снижается объем микропор в микро-мезопористом цеолите Y.
Суспензию деалюминированного цеолита Y в растворе гидроксида аммония смешивают с раствором катионного ПАВ, обеспечивающим в получаемой смеси отношение ПАВ/цеолит 0,8-2,0 ммоль/г и отношение H2O/цеолит 1,8-3,6 моль/г. Уменьшение отношения ПАВ/цеолит до величины ниже 0,8 ммоль/г приводит к уменьшению содержания мезопор в микро-мезопористом рекристаллизованном цеолите Y. Увеличение отношения ПАВ/цеолит до величины более 2,0 ммоль/г не влияет на содержание мезопор в рекристаллизованном цеолите Y и, следовательно, технологически нецелесообразно. В качестве катионного ПАВ используют галогенид цетилтриметиламмония C16H33N(CH3)3Hal, где Hal - Br или О.
Уменьшение отношения H2O/цеолит до величины ниже 1,8 моль/г не обеспечивает протекания процесса рекристаллизации и формирования микро-мезопористого цеолита Y, обладающего заявляемыми характеристиками. Увеличение отношения H2O/цеолит до величины более 3,6 моль/г не влияет на свойства микро-мезопористого цеолита Y, но приводит к уменьшению его выхода с единицы объема реакторного сосуда, в котором проводится синтез, и поэтому технологически нецелесообразно.
Гидротермальную обработку смеси суспензии деалюминированного цеолита Y в растворе гидроксида аммония и раствора катионного ПАВ проводят при температуре 60-95°С в течение 1,0-1,5 ч. Уменьшение температуры гидротермальной обработки ниже 60°С и длительности гидротермальной обработки ниже 1 часа приводит к уменьшению объема мезопор в микро-мезопористом цеолите Y. Увеличение температуры гидротермальной обработки выше 95°С не позволяет проводить синтез при атмосферном давлении и приводит к необходимости использования автоклавного оборудования, работающего под давлением, что технологически нецелесообразно. Увеличение длительности гидротермальной обработки более 1,5 ч не влияет на характеристики кислотности и текстуры микро-мезопористого цеолита Y и, следовательно, технологически нецелесообразно.
После гидротермальной обработки цеолит сушат и прокаливают по известной технологии.
Полученный предлагаемым способом материал имеет:
- кристаллическую структуру цеолита Y;
- химический состав, оцениваемый по отношению SiO2/Al2O3, близкий к химическому составу исходного деалюминированного цеолита Y;
- микро-мезопористую структуру с долей мезопор в общем объеме пор, составляющей 0,5-0,7, что в 1,25-1,75 раза выше, чем у исходного деалюминированного цеолита Y;
- кислотность с долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль, составляющей 0,5-0,6, что в 1,1-1,3 раза выше, чем у исходного деалюминированного цеолита Y.
Полученный материал сочетает в себе преимущества, заключающиеся в совокупности развитой микро-мезопористой структуры и кислотности с долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль, составляющей 0,5-0,6.
Далее изобретение будет подробно раскрыто в описании и примерах его реализации со ссылкой на прилагаемые чертежи, на которых:
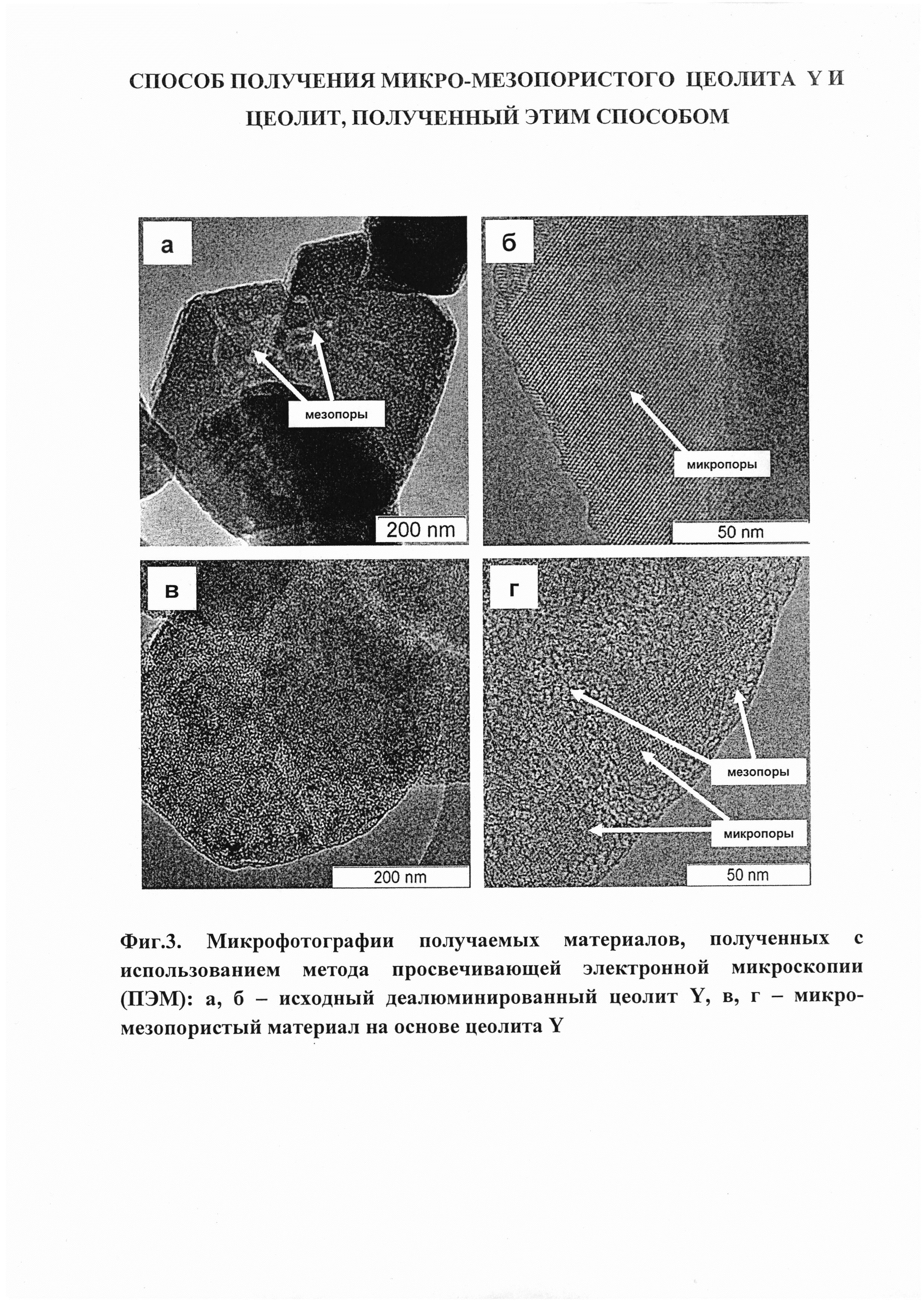
- фиг. 1 изображает порошковые дифрактограммы исходного и получаемых материалов;
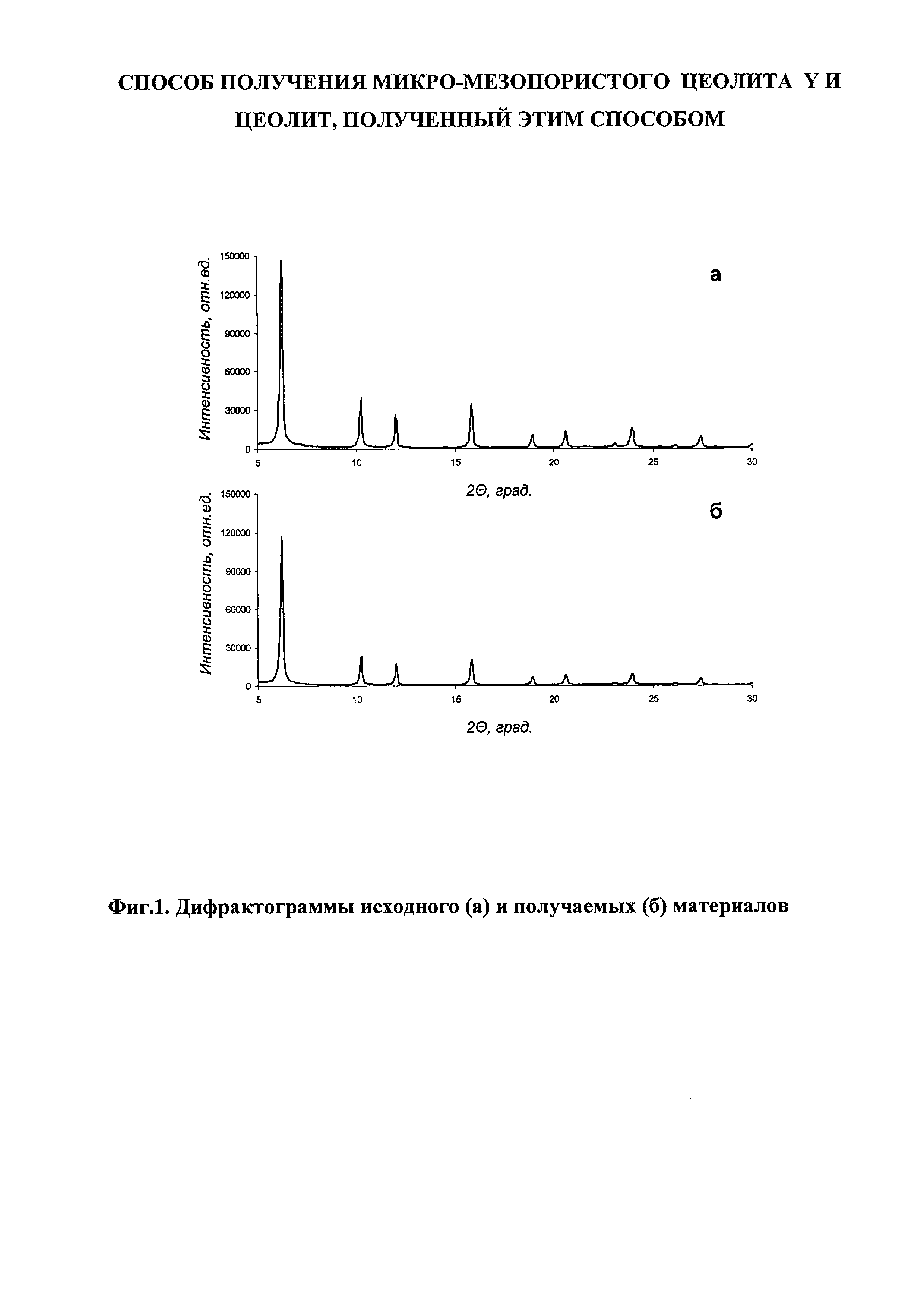
- фиг. 2 изображает изотермы низкотемпературной адсорбции - десорбции азота исходного и получаемых материалов;
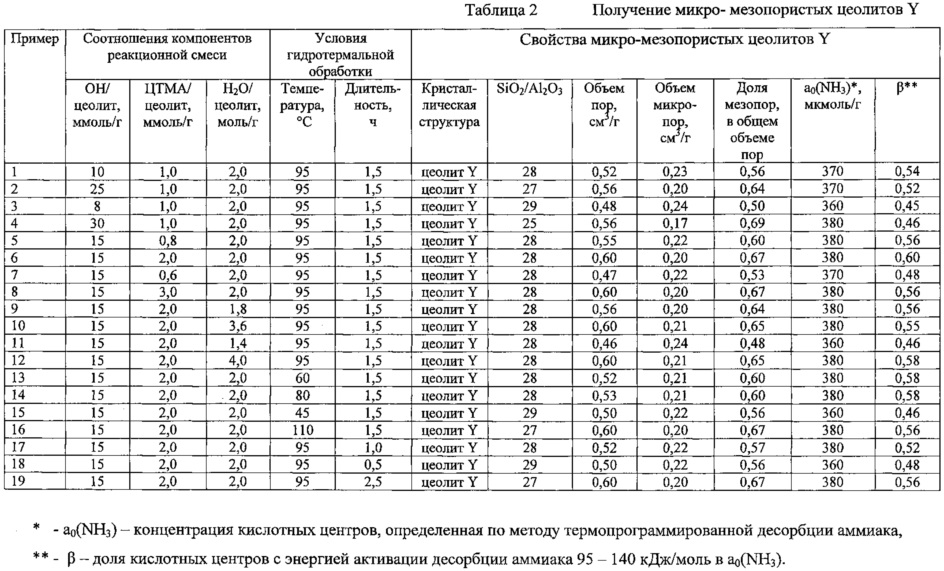
- фиг. 3 изображает микрофотографии исходного и получаемого материалов, полученных с использованием метода просвечивающей электронной микроскопии (ПЭМ).
Предлагаемый способ получения микро-мезопористого цеолита Y включает стадию активации исходного деалюминированного цеолита Y в растворе гидроксида аммония с последующим смешиванием с раствором катионного поверхностно-активного вещества (ПАВ) и стадию гидротермальной обработки смеси с выделением готового продукта.
В качестве исходного материала используют деалюминированный цеолит Y, имеющий не более 8 атомов алюминия в составе элементарной ячейки. Полученный микро-мезопористый материал сохраняет кристаллическую структуру исходного деалюминированного цеолита Y, как это видно на фиг. 1, где кривая «а» изображает дифрактограмму исходного деалюминированного цеолита Y, а кривая «б» - дифрактограмму микро-мезопористого цеолита Y.
Активацию исходного деалюминированного цеолита Y осуществляют в виде его суспензии, после того, как его суспендируют в растворе гидроксида аммония с концентрацией, обеспечивающей отношение ОН/цеолит 10-25 ммоль/г, после чего щелочную суспензию цеолита смешивают с раствором катионного ПАВ, обеспечивающим в получаемой смеси отношение ПАВ/цеолит 0,8-2,0 ммоль/г и отношение H2O/цеолит 1,8-3,6 моль/г. Гидротермальную обработку смеси суспензии деалюминированного цеолита Y в растворе гидроксида аммония и раствора катионного ПАВ проводят при температуре 60-95°С в течение 1,0-1,5 ч, после чего материал сушат и прокаливают.
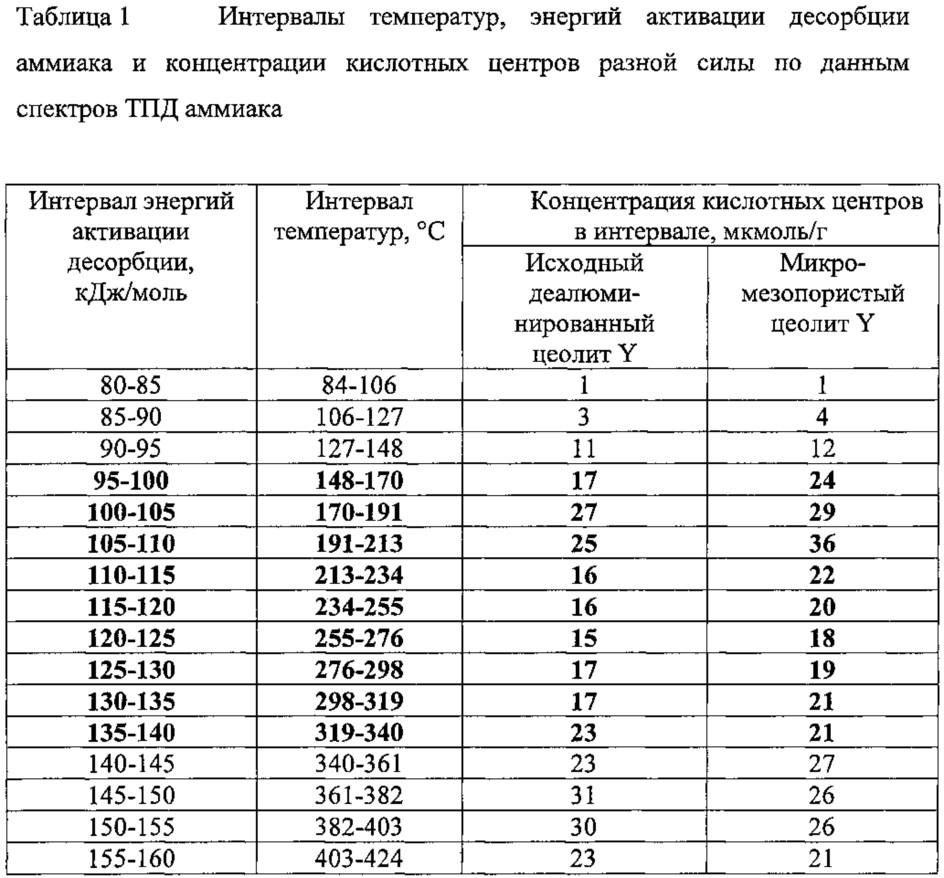
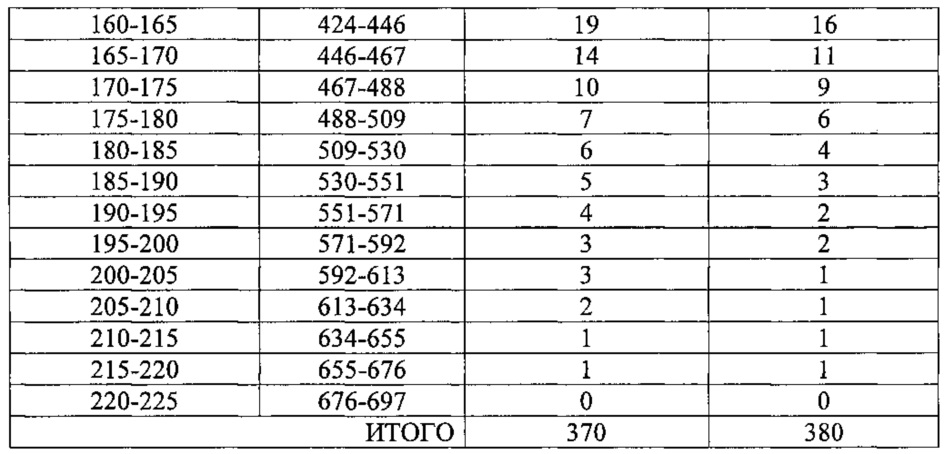
Полученный предлагаемым способом микро-мезопористый цеолит Y обладает кислотными центрами с энергией активации десорбции аммиака 95-140 кДж/моль, доля которых в общем спектре кислотности составляет 0,5-0,6, что в 1,1-1,3 раза выше, чем в исходном деалюминированном цеолите Y, и объемом пор, в 1,2-1,4 раза превышающим объем пор исходного деалюминированного цеолита Y. Концентрация кислотных центров a0(NH3) в микро-мезопористом цеолите Y и энергия активации десорбции аммиака Еакт(NH3), по которой оценивают силу кислотных центров, определяют с использованием метода термопрограммированной десорбции (ТПД) аммиака. Доли кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль определяют с использованием метода оценки неоднородности адсорбционных центров из данных о ТПД в соответствии с [В.В. Ющенко. Расчет спектров кислотности катализаторов по данным термопрограммированной десорбции аммиака, Журнал физической химии, 1997, том 71, №4, с. 628-632]. По этому методу профили ТПД разбивают на участки с одинаковым шагом температуры, как показано в табл. 1, для каждого участка вычисляют интервал изменения энергии активации десорбции и на основании этих величин определяют число центров в каждом участке.
Как следует из табл. 1, в интервале температур 148-340°С аммиак десорбируется с кислотных центров с энергией активации десорбции 95-140 кДж/моль, доля которых в исходном деалюминированном цеолите Y составляет 0,46, а в микро-мезопористом цеолите Y составляет 0,57. Таким образом, в результате реализации заявляемого способа доля кислотных центров с энергией активации десорбции 95-140 кДж/моль возрастает в 1,24 раза.
Объем пор, объем микропор, объем мезопор и диаметр мезопор рассчитывают по изотермам низкотемпературной адсорбции-десорбции азота, что показано на фиг. 2, где кривая «а» изображает изотерму низкотемпературной адсорбции-десорбции азота для исходного деалюминированного цеолита Y, а кривая «б» - для микро-мезопористого цеолита Y. Наличие подъема на кривой «б» по сравнению с кривой «а» в интервале относительных давлений p/p0 от 0,3 до 0,5 на оси абсцисс указывает на наличие мезопор в микро-мезопористом цеолите Y, в результате чего объем пор в этом материале увеличивается в 1,2-1,4 разапо сравнению с исходным деалюминированным цеолитом Y.
Для получения микро-мезопористого цеолита Y в качестве исходного был использован деалюминированный цеолит Y с следующими характеристиками:
- мольное отношение SiO2/Al2O3 = 30,
- объем пор 0,43 см3/г,
- объем микропор 0,26 см3/г,
- объем мезопор 0,17 см3/г,
- концентрация кислотных центров, a0(NH3) = 370 мкмоль/г,
- доля кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль, β=0,46.
Ниже приведены конкретные примеры, описывающие заявленный способ, а также приведены свойства полученных материалов.
Пример 1
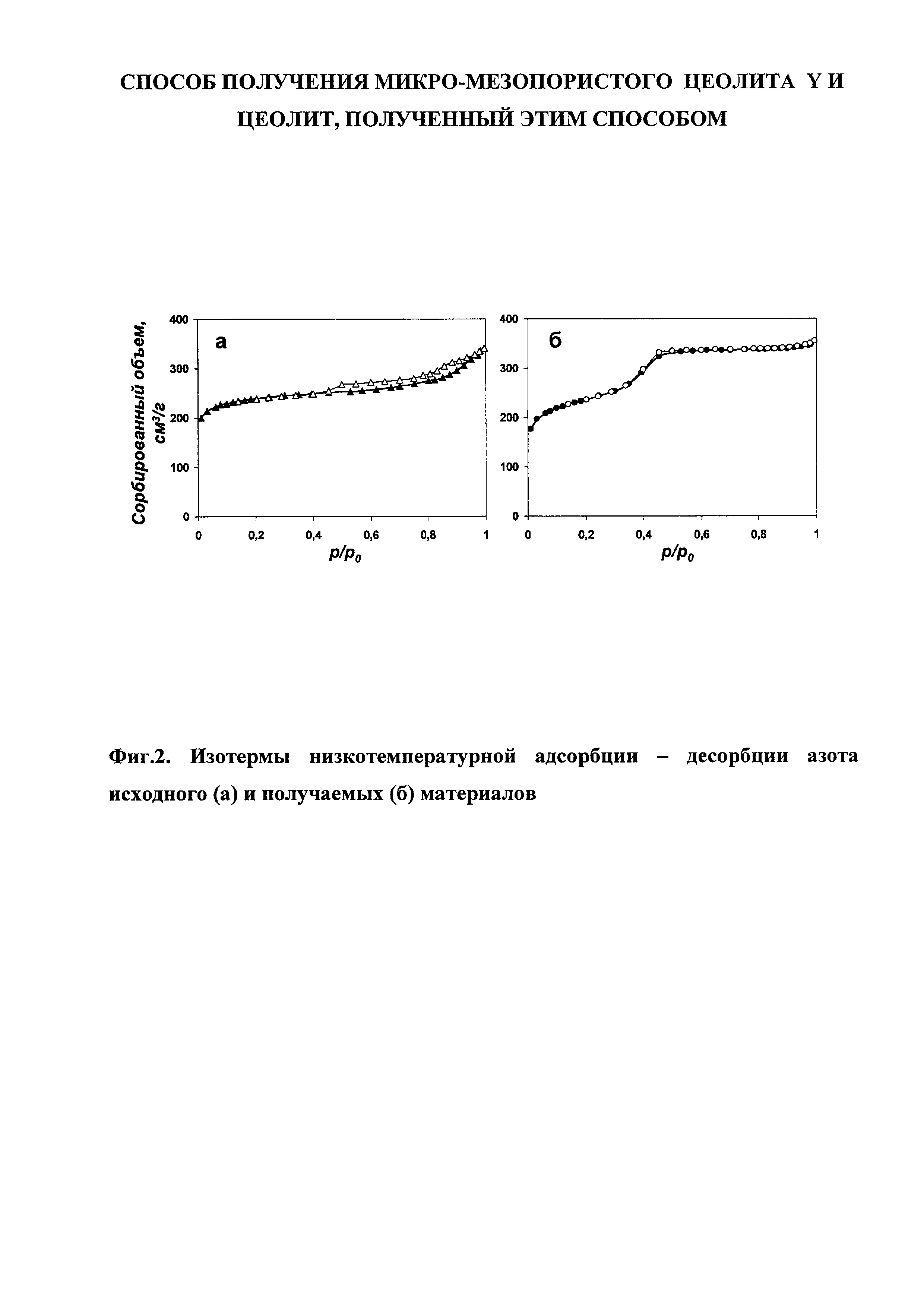
Микро-мезопористый цеолит Y приготавливают следующим образом. В 316,7 г воды растворяют 14 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором 3,64 г бромида цетилтриметиламмония (далее ЦТМАБ) в 32,8 г воды. В полученной смеси отношение ОН/цеолит составляет 10 ммоль/г, отношение ЦТМАБ/цеолит составляет 1 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Смесь суспензии цеолита в растворе NH4OH и раствора ЦТМАБ перемешивают при комнатной температуре в течение 5 мин, после чего смесь подвергают гидротермальной обработке при 95°С в течение 1,5 ч. По окончании гидротермальной обработки материал отделяют на фильтре, промывают дистиллированной водой, высушивают при 100°С в течение 12 ч и прокаливают при 550°С в течение 18 ч. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,52 см3/г с долей мезопор 0,56, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,54. Свойства полученного материала представлены в таблице 2.
Пример 2
Микро-мезопористый цеолит Y приготавливают следующим образом. В 300,9 г воды растворяют 35 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 1. В полученной смеси отношение ОН/цеолит составляет 25 ммоль/г, отношение ЦТМАБ/цеолит составляет 1 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=27, объемом пор 0,56 см3/г с долей мезопор 0,64, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,52. Свойства полученного материала представлены в таблице 2.
Пример 3
Микро-мезопористый цеолит Y приготавливают следующим образом. В 318,8 г воды растворяют 11,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 1. В полученной смеси отношение ОН/цеолит составляет 8 ммоль/г, отношение ЦТМАБ/цеолит составляет 1 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=29, объемом пор 0,48 см3/г с долей мезопор 0,50, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,45. Свойства полученного материала представлены в таблице 2.
Пример 4
Микро-мезопористый цеолит Y приготавливают следующим образом. В 295,7 г воды растворяют 42 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 1. В полученной смеси отношение ОН/цеолит составляет 30 ммоль/г, отношение ЦТМАБ/цеолит составляет 1 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=25, объемом пор 0,56 см3/г с долей мезопор 0,69, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,46. Свойства полученного материала представлены в таблице 2.
Примеры 1-4 показывают влияние отношения ОН/цеолит на свойства микро-мезопористого цеолита Y.
Пример 5
Микро-мезопористый цеолит Y приготавливают следующим образом. В 317,9 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором 2,91 г ЦТМАБ в 26,2 г воды. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 0,8 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,55 см /г с долей мезопор 0,60, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,56. Свойства полученного материала представлены в таблице 2.
Пример 6
Микро-мезопористый цеолит Y приготавливают следующим образом. В 278,6 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором 7,28 г ЦТМАБ в 65,5 г воды. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 2,0 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,60 см3/г с долей мезопор 0,67, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,60. Свойства полученного материала представлены в таблице 2.
Пример 7
Микро-мезопористый цеолит Y приготавливают следующим образом. В 324,4 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором 2,18 г ЦТМАБ в 19,7 г воды. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 0,6 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,47 см3/г с долей мезопор 0,53, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,48. Свойства полученного материала представлены в таблице 2.
Пример 8
Микро-мезопористый цеолит Y приготавливают следующим образом. В 245,8 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором 10,92 г ЦТМАБ в 98,3 г воды. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 3,0 ммоль/г, отношение H2O/цеолит составляет 2,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,60 см3/г с долей мезопор 0,67, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,56. Свойства полученного материала представлены в таблице 2.
Примеры 5-8 показывают влияние отношения ЦТМАБ/цеолит на свойства микро-мезопористого цеолита Y.
Пример 9
Микро-мезопористый цеолит Y приготавливают следующим образом. В 242,6 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 6. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 2,0 ммоль/г, отношение H2O/цеолит составляет 1,8 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,56 см3/г с долей мезопор 0,64, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,56. Свойства полученного материала представлены в таблице 2.
Пример 10
Микро-мезопористый цеолит Y приготавливают следующим образом. В 566,6 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 6. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 2,0 ммоль/г, отношение H2O/цеолит составляет 3,6 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,60 см3/г с долей мезопор 0,65, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,55. Свойства полученного материала представлены в таблице 2.
Пример 11
Микро-мезопористый цеолит Y приготавливают следующим образом. В 170,6 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 6. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 2,0 ммоль/г, отношение Н2О/цеолит составляет 1,4 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,46 см3/г с долей мезопор 0,48, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,46. Свойства полученного материала представлены в таблице 2.
Пример 12
Микро-мезопористый цеолит Y приготавливают следующим образом. В 638,6 г воды растворяют 21,2 г 25% раствора NH4OH. В полученный раствор добавляют 10 г деалюминированного цеолита Y. Полученную суспензию перемешивают при комнатной температуре в течение 20 минут, после чего смешивают с раствором ЦТМАБ, который готовят аналогично примеру 6. В полученной смеси отношение ОН/цеолит составляет 15 ммоль/г, отношение ЦТМАБ/цеолит составляет 2,0 ммоль/г, отношение Н2О/цеолит составляет 4,0 моль/г. Дальнейшие обработки проводят аналогично примеру 1. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,60 см3/г с долей мезопор 0,65, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,58. Свойства полученного материала представлены в таблице 2.
Примеры 9-12 показывают влияние отношения H2O/цеолит на свойства микро-мезопористого цеолита Y.
Пример 13
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят при 60°С. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,52 см3/г с долей мезопор 0,60, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,58. Свойства полученного материала представлены в таблице 2.
Пример 14
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят при 80°С. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,53 см3/г с долей мезопор 0,60, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,58. Свойства полученного материала представлены в таблице 2.
Пример 15
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят при 45°С. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=29, объемом пор 0,50 см3/г с долей мезопор 0,56, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,46. Свойства полученного материала представлены в таблице 2.
Пример 16
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят при 110°С в автоклаве при повышенном давлении. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=27, объемом пор 0,60 см3/г с долей мезопор 0,67, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,56. Свойства полученного материала представлены в таблице 2.
Примеры 6, 13-16 показывают влияние температуры гидротермальной обработки на свойства микро-мезопористого цеолита Y.
Пример 17
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят в течение 1 ч. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=28, объемом пор 0,52 см3/г с долей мезопор 0,57, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,52. Свойства полученного материала представлены в таблице 2.
Пример 18
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят в течение 0,5 ч. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=29, объемом пор 0,50 см3/г с долей мезопор 0,56, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,48. Свойства полученного материала представлены в таблице 2.
Пример 19
Микро-мезопористый цеолит Y получают аналогично примеру 6, но гидротермальную обработку проводят в течение 2,5 ч. В результате получают материал с кристаллической структурой цеолита Y, отношением SiO2/Al2O3=27, объемом пор 0,60 см3/г с долей мезопор 0,67, и долей кислотных центров с энергией активации десорбции аммиака 95-140 кДж/моль β=0,56. Свойства полученного материала представлены в таблице 2.
Примеры 6, 17-19 показывают влияние длительности гидротермальной обработки на свойства микро-мезопористого цеолита Y.
Вместо бромида цетилтриметиламмония может быть использован другой его галогенид, например, хлорид, что не оказывает существенного влияния на свойства цеолита.
Таким образом, как видно из приведенных выше примеров, получен новый материал микро-мезопористый цеолит Y, обладающий пористой структурой, образованной двумя типами пор - цеолитных микропор и мезопор. На фиг. 3 представлены изображения ПЭМ-изображения материалов: фиг. 3а и 3б - исходного деалюминированного цеолита Y, а фиг. 3в и 3г - микро-мезопористого цеолита Y по примеру 6. В исходном деалюминированном цеолите Y мезопоры присутствуют в виде каналов, хаотично расположенных в цеолитном кристалле, как показывает фиг. 3а. В микро-мезопористом цеолите Y мезопоры равномерно распределены по объему цеолитного кристалла, как показывает фиг. 3в. Фиг. 3г показывает, что в результате реализации заявляемого способа в цеолитном кристалле микро-мезопористого цеолита Y создается система взаимосвязанных микро- и мезопор, в результате чего для крупных органических молекул доступным становится весь объем цеолитного кристалла, тогда как в исходном деалюминированном цеолите Y доступными оказываются лишь участки в объеме цеолитного кристалла, граничащие с мезопорами.
Как следует из приведенных выше примеров, в результате реализации заявляемого способа достигается увеличение объема пор микро-мезопористых цеолитов Y в 1,2-1.4 раза по сравнению с исходным деалюминированным цеолитом Y. При этом полученные материалы сохраняют высокую кристалличность, что подтверждается рентгенофазовым анализом и высокими величинами объемов микропор 0,20-0,23 см3/г.
Как следует из приведенных выше примеров, в результате реализации заявляемого способа формируется спектр кислотности микро-мезопористых цеолитов Y с кислотными центрами с энергией активации десорбции аммиака 95-140 кДж/моль, доля которых в общем спектре кислотности составляет 0,5-0,6.
Как видно из приведенных выше примеров, достигнуто упрощение способа получения микро-мезопористых цеолитов Y, при котором процесс осуществляют в две стадии: активации цеолита при комнатной температуре и гидротермальной обработки суспензии цеолита при температуре 60-95°С в течение 1-1,5 ч.
Областью использования микро-мезопористого цеолита Y являются различные сорбционные и каталитические процессы с участием крупных органических молекул, в первую очередь процесса гидрокрекинга вакуумного газойля, состоящего из объемных молекул с числом атомов углерода до 20-25, размер которых сопоставим с размерами мезопор в микро-мезопористом цеолите Y.