Результат интеллектуальной деятельности: ВИРИОНЫ И ВИРУСОПОДОБНЫЕ ЧАСТИЦЫ ВИРУСА МОЗАИКИ АЛЬТЕРНАНТЕРЫ КАК УСИЛИТЕЛИ ИММУННОГО ОТВЕТА
Вид РИД
Изобретение
Область техники
Изобретение относится к области вирусологии и иммунологии, а именно к способу получения вирусоподобных частиц и способам усиления иммунного ответа на антигены, смешанные с вирусоподобными частицами или нативным вирусом. Изобретение может быть использовано в медицине, ветеринарии и биотехнологии для получения антител.
Уровень техники
Вакцинация является основным способом профилактики инфекционных заболеваний. Цель вакцинации - создание сильного иммунного ответа, обеспечивающего длительную защиту от инфекции.
Основные типы вакцин, лицензированных для клинического использования, - живые аттенуированные, инактивированные и субъединичные, содержащие белки возбудителей заболевания или их отдельные фрагменты - эпитопы. Основным преимуществом вакцин нового поколения (субъединичных) является их безопасность, однако такие вакцины обычно обладают низкой иммуногенностью, что приводит к необходимости многократной иммунизации и применению адъювантов.
Адъювантами называют неспецифические стимуляторы иммунного ответа или соединения, создающие депо для антигена в организме хозяина, которые объединяются с вакциной для усиления иммунного ответа. Несмотря на прогресс в понимании механизмов действия адъювантов и разработки новых препаратов, при вакцинации человека традиционно используют водно-масляные эмульсии, соединения алюминия (алюминиевые квасцы, фосфат и гидроокись алюминия) и химические полимеры. При введении подкожно или внутримышечно они могут вызывать побочные эффекты, такие как гранулемы, абсцессы и рубцы, эффективность действия некоторых из этих адъювантов зависит от состава антигена или они являются слабыми иммуностимуляторами.
Один из подходов к повышению эффективности и безопасности вакцинации является использование вирусоподобных частиц (ВПЧ). Вирусоподобные частицы формируются в результате самосборки вирусных структурных белков в отсутствие вирусного генома и по своему строению и морфологии схожи с нативными вирионами. ВПЧ могут быть использованы в качестве вакцины для гомологичного вируса, из которого получены, в качестве платформы для презентации чужеродных эпитопов при производстве вакцин и для усиления иммунного ответа. Интерес к новым ВПЧ связан с разработкой и успешным применением ВПЧ вакцин против гепатита В и вируса папилломы человека.
Использование вирусов растений и ВПЧ на основе фитовирусов для презентации чужеродных эпитопов описано в ряде работ и патентах [Canizares et al. Use of virus vectors for vaccine production in plants. Immunol. Cell. Biol. 2005, 83, 263-270; Turpen et al. Production of peptides in plants as viral coat protein fusions. US Patent 5977438. Nov. 1999; Werner et al. International Patent Application PCT/EP2006/009029 (WO/2007/031339); Werner et al. Immunoabsorbent nanoparticles based on a tobamovirus displaying protein A. Proc. Natl. Acad. Sci. USA, 2006, 103, 17678-17683; McCormick & Palmer. Genetically engineered Tobacco mosaic virus as nanoparticle vaccines. Expert Rev Vaccines. 2008, 7, 33-41; Steinmetz et al., Structure-based engineering of an icosahedral virus for nanomedicine and nanotechnology. Curr. Top. Microbiol. Immunol. 2009, 327, 23-58; Denis et al., Immunogenicity of papaya mosaic virus-like particles fused to a hepatitis С virus epitope: evidence for the critical function of multimerization. Virology 2007, 363, 59-68; Acosta-Ramirez et al., Translating innate response into long-lasting antibody response by the intrinsic antigen-adjuvant properties of papaya mosaic virus. Immunology, 2007, 124, 186-197; Lacasse et al., Novel plant virus-based vaccine induces protective cytotoxic T-lymphocyte-mediated antiviral immunity through dendritic cell maturation. J. Virology, 2008, 82, 785-794; Leclerc et al., Adjuvant viral particle. US Patent 7641896, Jan. 5 2010].
Получение новых типов вакцин на основе химерных вирусов растений и ВПЧ имеет ряд преимуществ: вирусы растений не патогенны для млекопитающих, в том числе для человека, обладают высокой иммуногенностью и способностью вызывать как гуморальный, так и клеточный иммунный ответ. В некоторых случаях такие вакцины не требуют применения адъювантов [Marusic et al. Chimeric plant virus particles as immunogenes for inducing murine and human immune response against human immunodeficiency virus type 1. J. Virology 2001, 75, 8434-8439; Saini & Vrati. A Japanese encephalitis virus peptide present on Johnson grass mosaic virus-like particles induces virus-neutralizing antibodies and protects mice against lethalchallenge. J. Virology 2003, 77, 3487-3494].
Недавние исследования демонстрируют, что вирусоподобные частицы, полученные из структурных белков вируса мозаики папайи (ВМП) и вируса мозаики мальвы, принадлежащих к роду потексвирусов, обладают сильной адъювантной активностью и могут быть использованы для усиления иммунного ответа при вакцинации. Вирусы рода Potexvirus семейства Flexivirda представляют собой нитевидные вирионы длиной 470-580 нм и шириной 13-15 нм с однонитевой позитивной геномной РНК.
Показано, что вирусоподобные частицы ВМП, полученные в результате самосборки рекомбинантного белка оболочки (БО) ВМП при экспрессии в E. coli, можно использовать в качестве адъюванта при иммунизации животных химерными ВПЧ, несущими на своей поверхности М2е эпитопы вируса гриппа. Адъювантная активность оценивается по увеличению уровня IgG к пептиду М2е более чем в 10 раз по сравнению с иммунизацией без адъюванта. Сильное повышение иммуногенности ВПЧ-М2е содержащей вакцины, приводит к 100% защите мышей от заражения летальными дозами вируса гриппа. Механизм усиления иммунного ответа не известен, однако авторы отмечают значительную разницу в длине химерных ВПЧ и ВПЧ, используемых в качестве адъюванта - средняя длина 100 и 150 нм соответственно. Похожие результаты получены при совместной иммунизации мышей и хорьков ВПЧ ВМП и коммерческой трехвалентной инактивированной вакциной против гриппа. Показано усиление гуморального ответа на НА и NP белки вируса гриппа и клеточно-опосредованного иммунного ответа на NP и M1 белки, представленные в вакцине, но не иммуногенные, а также длительная защита животных к заражению гетеросубтипическим штаммом вируса гриппа (WSN/33). На лабораторных животных продемонстрировано применение ВПЧ ВМП как иммуностимулятора для профилактики вирусных и бактериальных заболеваний, вызываемых вирусом гриппа и пневмококком. [Mathieu et al., Induction of innate immunity in lungs with virus-like nanoparticles leads to protection against influenza and Streptococcus pneumoniae challenge. Nanomedicine: Nanotechnology, Biology, and Medicine 2013, 9, 839-848; Savard. et al., Improvement of the trivalent inactivated Flu vaccine using PapMV nanoparticles. PLoS One. 2011; 6: e21522; Rioux et al., PapMV nanoparticles improve mucosal immune responses to the trivalent inactivated flu vaccine. J. Nanobiotechnology 2014, 12,19; Denis et al., Development of a universal influenza A vaccine based on the M2e peptide fused to the papaya mosaic virus (PapMV) vaccine platform. Vaccine. 2008, 26 (27-28), 3395-403; Leclerc, Malva mosaic virus and virus-like particles and uses thereof. Patent WO 2009033276 A1 2009].
В нескольких работах показано, что иммуногенность ВПЧ зависит от их структуры и длины: так называемые диски, построенные из 20 субъединиц рекомбинантного белка оболочки, слитого с целевым пептидом, не иммуногены. Содержание дисков в препаратах ВПЧ ВМП может достигать 80%, в зависимости от метода получения.
Таким образом, метод, используемый для получения и выделения ВПЧ, явно имеет решающее значение для достижения более высоких уровней иммуногенности.
Известен способ получения вирусоподобных частиц из белка оболочки ВМП in vitro при рН 4,0 и низкой ионной силе, однако, такие частицы не стабильны при 5,0 и 6,0, а также в присутствии 0.2М Na Cl. При рН 8,0 сборка БО ВМП ограничивается образованием небольших агрегатов со спиральной структурой с коэффициентами седиментации 13-33S [Erickson & Bancroft. The Assembly of Papaya Mosaic Virus Protein. Virology 1976, 72, 514-517].
Известен способ получения вирусоподобных частиц ВМП в результате самосборки рекомбинантного белка оболочки ВМП при экспрессии в E. coli., однако, такие ВПЧ содержат РНК бактериального происхождения. [Tremblay et al. Effect of mutations K97A and E128A on RNA binding and self assembly of papaya mosaic potexvirus coat protein. FEBS J. 2006, 273, 14-25].
В качестве прототипа изобретения может быть рассмотрен патент [US 20140255439: Leclerc & Savard. Virus-like particles and process for preparing same, дата публикации 11.09.2014]. Способ получения ВПЧ in vitro из рекомбинантного белка и фрагмента РНК вируса мозаики папайи включает конструирование рекомбинантной плазмиды, кодирующей белок оболочки ВМП, экспрессию полученного гена в бактериальных клетках, выделение рекомбинантного белка с помощью металл-аффинной хроматографии, конструирование плазмиды, имеющей промотор для ДНК-зависимой РНК-полимеразы и фрагмент кДНК ВМП, получение РНК методом транскрипции in vitro и, наконец, инкубацию рекомбинантного белка и РНК при нейтральных рН и температуре от 2 до 37°. Полученные ВПЧ могут быть использованы в качестве адъювантов и, когда белок оболочки слит с антигеном, в качестве вакцин. Рассмотренный способ получения ВПЧ из рекомбинантного белка и РНК вируса мозаики папайи имеет ряд слабых сторон. Во-первых, он представляет собой сложный, многоступенчатый и дорогостоящий процесс. Во-вторых, препараты рекомбинантного белка ВМП, полученные из лизата E. coli, могут содержать неидентифицированные бактериальные компоненты, присутствие которых является нежелательным из-за потенциальных рисков или побочных эффектов. Наконец, РНК, входящая в состав ВПЧ, может стимулировать Т-клеточный ответ посредством активации Толл-подобных рецепторов. Как известно, активация Т-клеточных ответов может приводить к серьезным побочным действиям. [Bachmann et al. Patent. Vlp-antigen conjugates and their uses as vaccines WO 2006037787 A2 2006]. Тем не менее, данный метод применяется, так как авторы не смогли получить ВПЧ ВМП в отсутствие РНК в физиологических условиях.
Раскрытие изобретения
Задачей изобретения является разработка простого и эффективного способа получения вирусоподобных частиц in vitro из белка оболочки вируса растения со спиральной структурой в отсутствие РНК в физиологических условиях и их использование в качестве адъюванта для усиления иммунного ответа.
Поставленная задача решается тем, что вирусоподобные частицы получают in vitro из белка оболочки вируса мозаики альтернантеры (ВМАльт) в отсутствие РНК. При этом вирусоподобные частицы получают в физиологических условиях посредством инкубирования белка оболочки ВМАльт в 0.15М NaCl при рН 7,0-7,5.
Поставленная задача решается также тем, что вирусоподобные частицы и вирионы ВМАльт используются для усиления иммунного ответа на чужеродные белки, находящиеся с ними в смеси при иммунизации. При этом иммунизация животных или человека проводится смесью антигена и адъюванта, где в качестве адъюванта используют вирусоподобные частицы ВМАльт стабильные в физиологических условиях. Возможен вариант, когда для усиления иммунного ответа на антиген при иммунизации животных или человека в качестве адъюванта используют вирионы ВМАльт.
Краткое описание рисунков
Рисунок 1 представляет внешний вид вирионов ВМАльт, выделенного из растений. Электронная микроскопия (А), атомно-силовая микроскопия (Б).
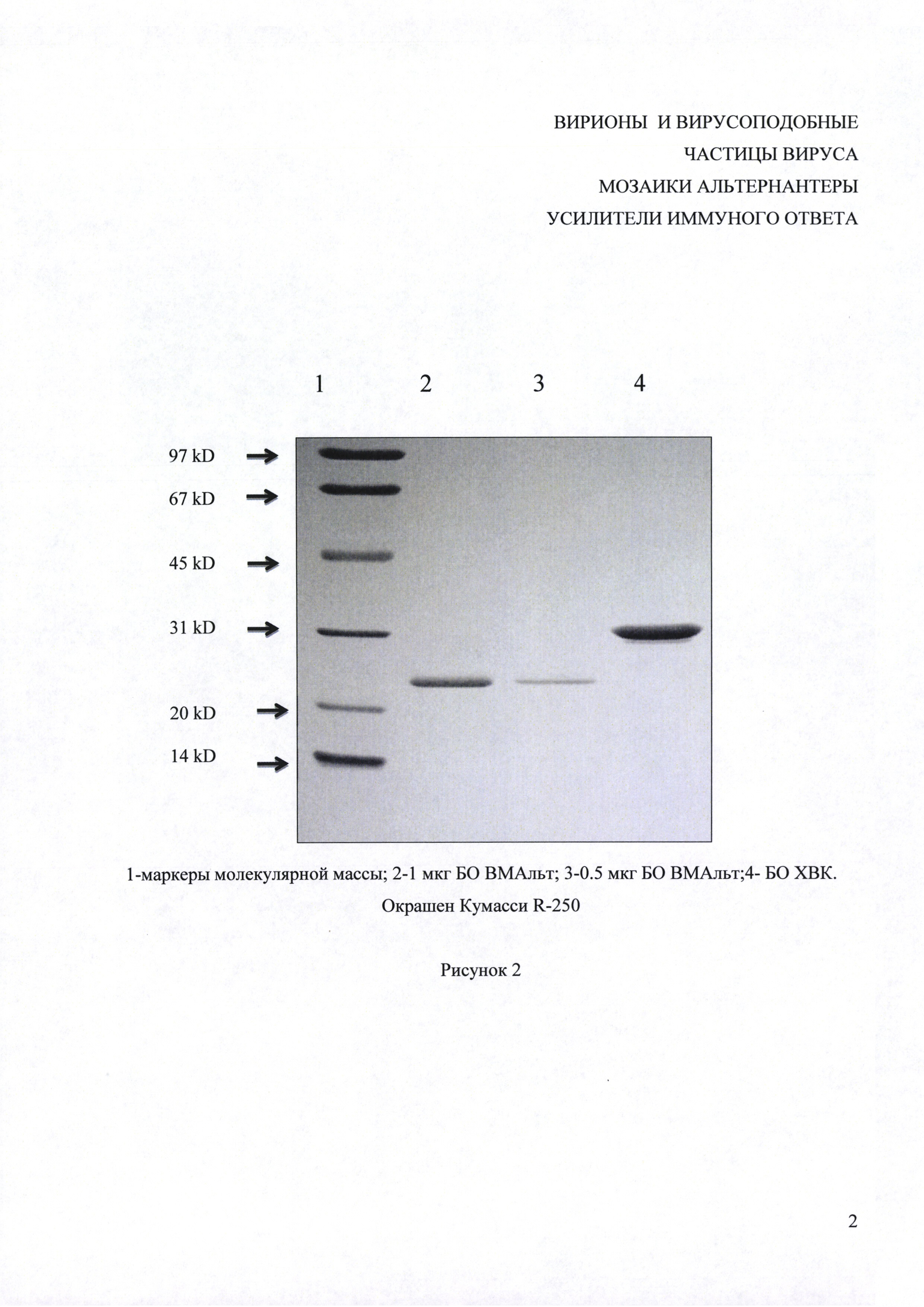
Рисунок 2 представляет электрофоретический анализ в 8-20%-ном ДСН-ПААГ препарата очищенного БО ВМАльт, показывающий белок оболочки ВМАльт с м.м. 23 кДа.
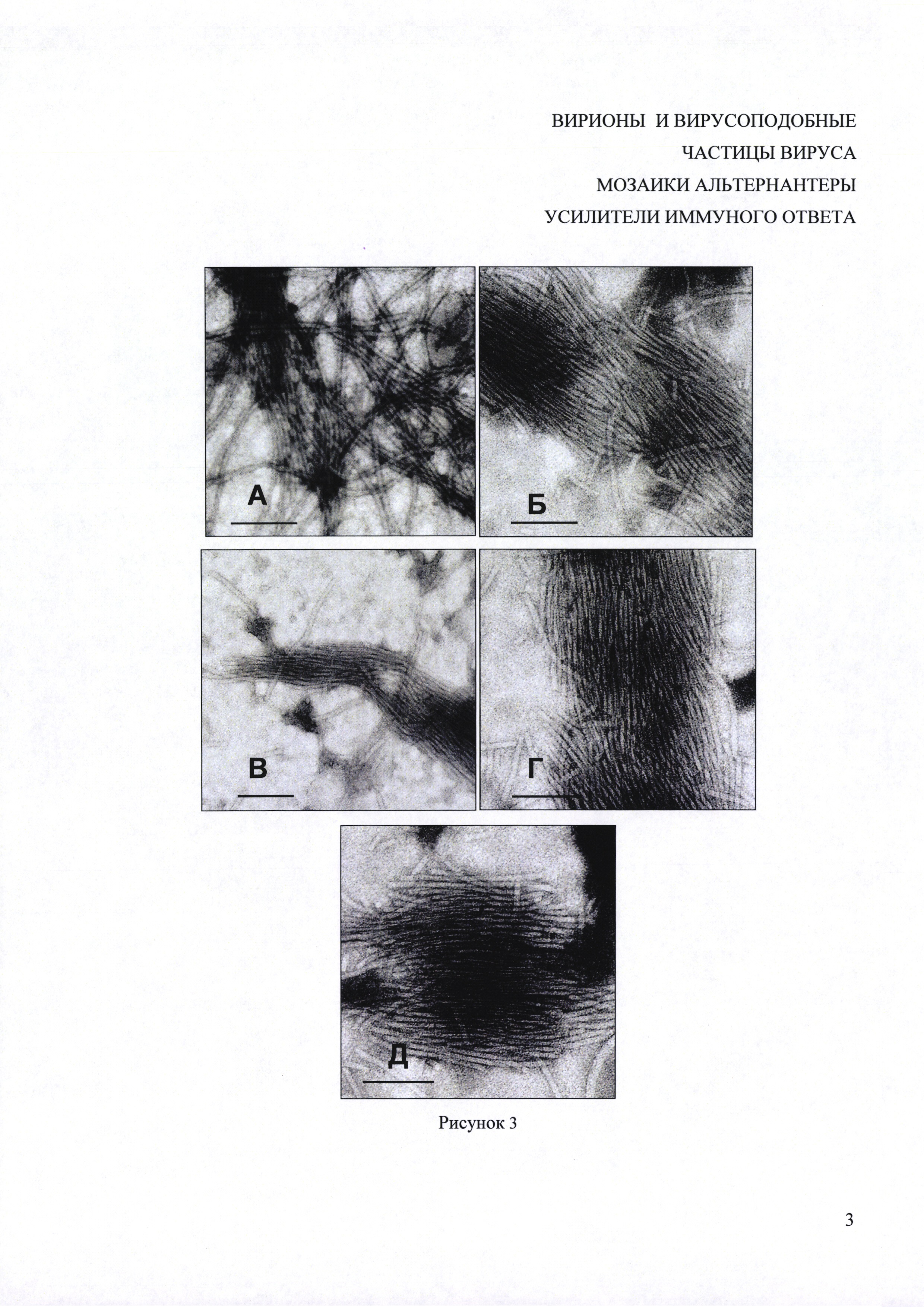
Рисунок 3 представляет внешний вид ВПЧ, полученных из белка оболочки ВМАльт в воде до (А) и после добавления 0.15М NaCl (Б); в 0.01 М Трис-HCl буфере, рН 7,4 до (В) и после добавления 0.15М NaCl (Г); в 0.15М NaCl (Д). Электронная микроскопия. Контрастирование 2% раствором уранил ацетата. Размер метки, 200 нм.
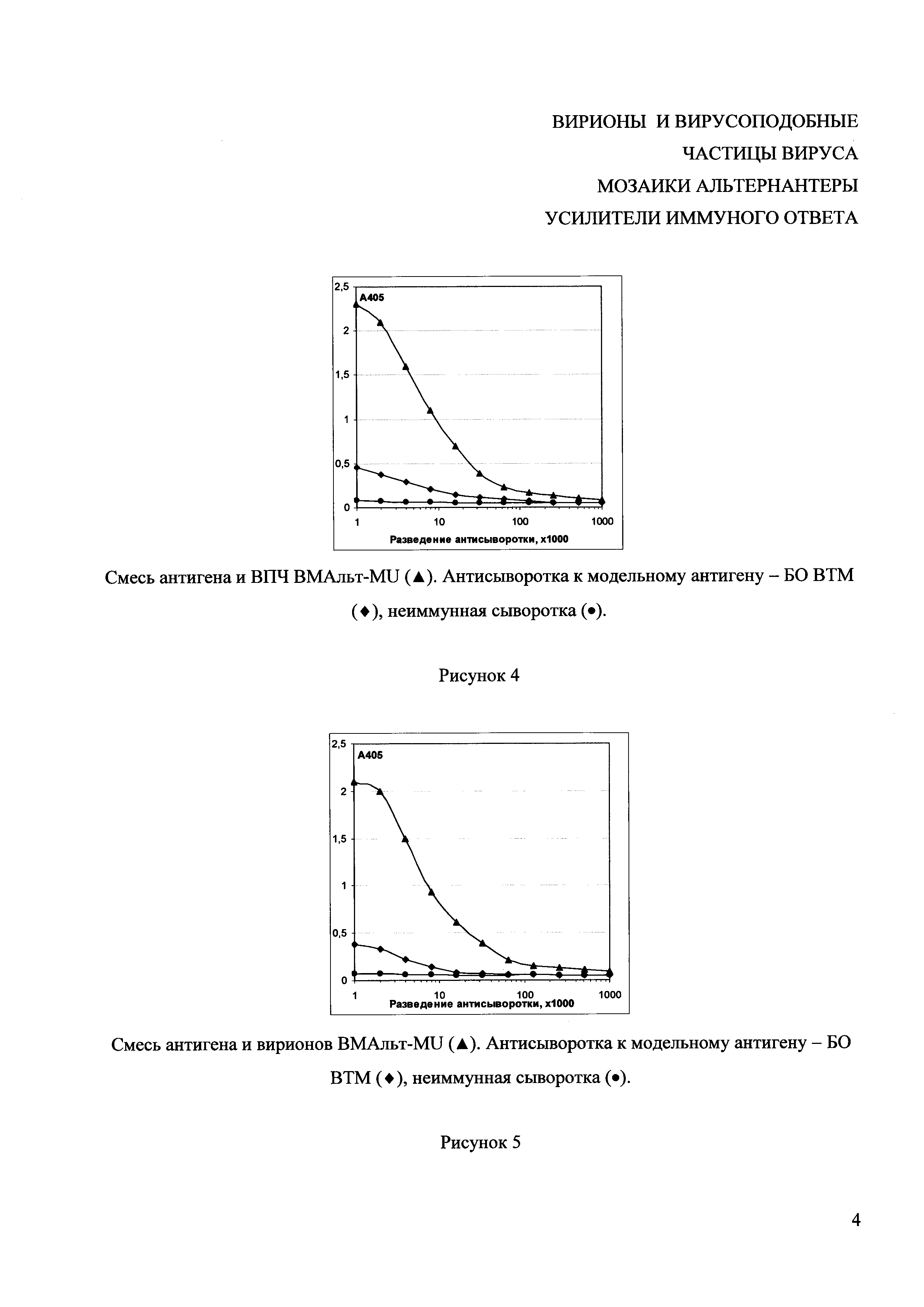
Рисунок 4 представляет собой график, иллюстрирующий результаты определения титра мышиных антисывороток к модельному антигену - БО вируса табачной мозаики (ВТМ), полученных при иммунизации животных смесью антигена и ВПЧ ВМАльт. ИФА.
Рисунок 5 представляет собой график, иллюстрирующий результаты определения титра мышиных антисывороток к модельному антигену - БО ВТМ, полученных при иммунизации животных смесью антигена и вирионов ВМАльт. ИФА
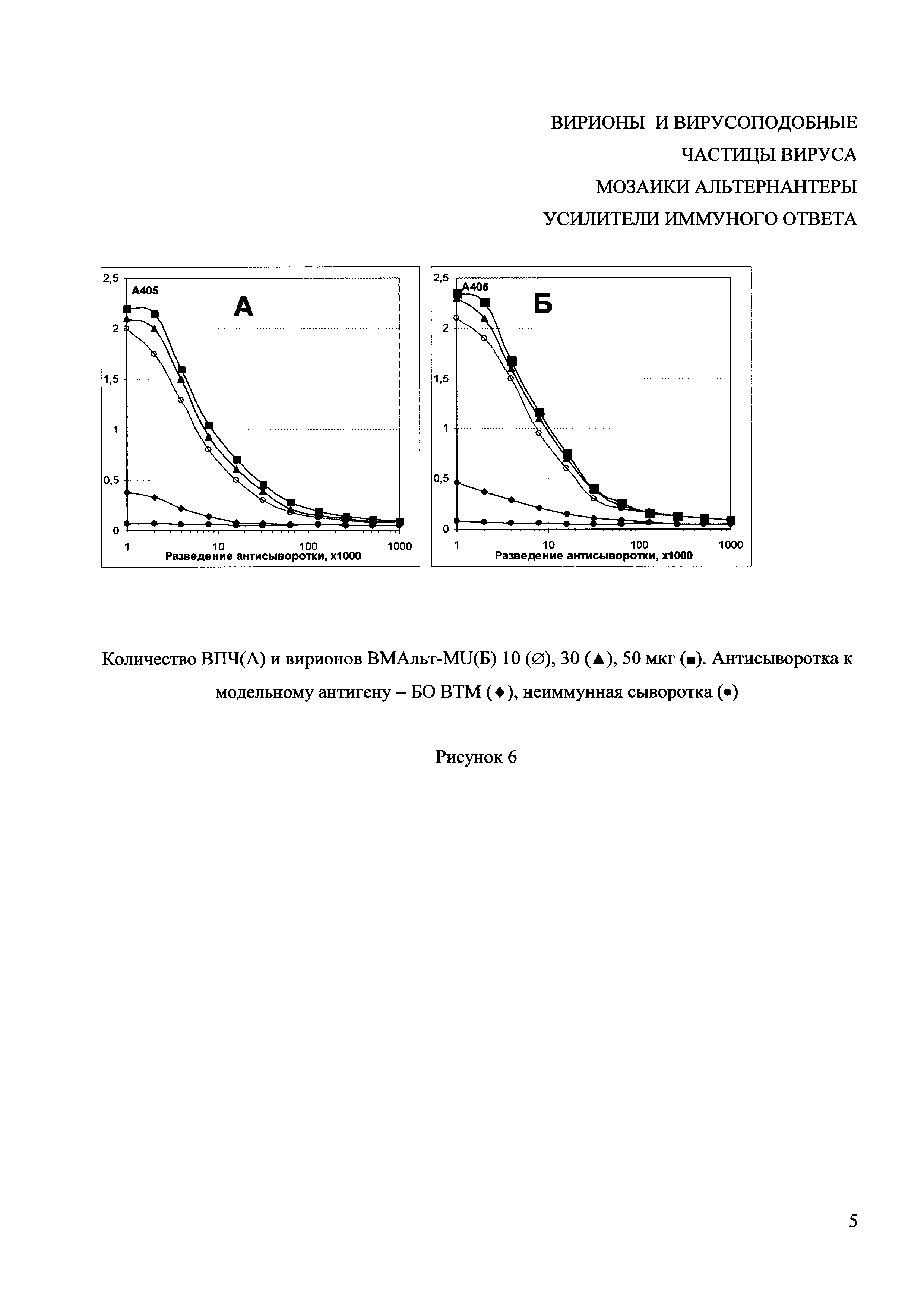
Рисунок 6 представляет собой график, иллюстрирующий влияние дозы вирионов и ВПЧ ВМАльт на интенсивность стимуляции иммунного ответа к антигену. ИФА.
Осуществление изобретения
Препаративное выделение вирионов ВМАльт осуществляют стандартным методом, разработанным для потексвирусов. БО ВМАльт, выделенный обработкой вирусной суспензии в Трис-HCl буфере, рН 7.4 нейтральным солевым раствором LiCl, с концентрацией 1-5 мг/мл инкубируют в течение 20 мин в 0.01М Трис-HCl буфере, рН 7,4 или в воде в присутствие 0.15 М NaCl или в 0.01 М Трис-HCl буфере, рН 7,4 или в воде и добавляют NaCl до конечной концентрации 0.15М. Полученные ВПЧ или вирионы ВМАльт смешивают с антигеном в массовом соотношении 3:1. Смесь готовят непосредственно перед инъекцией или за некоторое время до нее. Животному внутрибрюшинно или подкожно вводят смесь антигена и вирусных частиц. В результате введения такой смеси у животного развивается иммунный ответ на введенный антиген, выражающийся в появлении в сыворотке крови антител, специфичных к данному антигену.
Пример 1. Выделение и очистка вирионов ВМАльт.
Для препаративного выделения вирионов ВМальт листья зараженных растений портулака Portulaca grandiflora гомогенизировали с помощью ножевого гомогенизатора (число оборотов 800 об/мин) в двух объемах 0,05 М Трис-HCl буфера, рН 8,0, содержащего 10 мМ ЭДТА. После гомогенизации измельченную растительную массу, содержащую частицы ВМальт, очищали от крупных частиц (неразрушенные клетки, ядра, крупные фрагменты клеточной стенки и др.) фильтрацией под вакуумом через двойную марлевую ткань. Дальнейшая очистка гомогената листьев осуществлялась низкоскоростным центрифугированием при 10000 об/мин в течение 20 мин (ротор JA-14, «Beckman») при t+4°C. К осветленному гомогенату добавляли 1/5 часть хлороформа (по объему) и непрерывно встряхивали полученную смесь в течение 10 мин. Методом низкоскоростного центрифугирования при 10000 об/мин (15 мин, t+4°C, ротор JA-14, «Beckman») осуществляли разделение фаз в полученной эмульсии. Верхнюю водную фазу, содержащую вирусные частицы, аккуратно отбирали и добавляли полиэтиленгликоль (ПЭГ) (Мr 6000) до конечной концентрации 5% и NaCl до 2%. После полного растворения компонентов раствор выдерживали в течение 2 ч при t+4°C. Образовавшийся осадок вируса отделяли центрифугированием при 10000 об/мин и растворяли в мл 0,1 М фосфатного буфера (рН 7,5) при постоянном перемешивании при t+4C. Полученный экстракт осветляли центрифугированием при 10000 об/мин в течение 20 мин при t+4°C. Дальнейшую очистку вируса проводили с помощью двух циклов ультрацентрифугирования. При первом цикле осветленный экстракт ультрацентрифугировали с использованием 30%-ной сахарозной подушки в роторе Ti-50 при 32000 об/мин в течение 180 мин, t+4°C. Полученные осадки растворяли в 0,1 М фосфатного буфера (рН 7,5). При втором цикле раствор осветленного вируса ультрацентрифугировали без сахарозной подушки в роторе Ti-50 при 32000 об/мин в течение 120 мин, t+4°C. Вирусный осадок растворяли 0.01М Трис-HCl буфера, рН 7.5 Концентрацию вируса определяли спектрофотометрически используя коэффициент экстинкции: Е260нм0.1%=2,84. Анализ препарата ВМАльт методами просвечивающей электронной микроскопии (ПЭМ) и атомно-силовой микроскопии (АСМ) представлен на Рис. 1.
Пример 2. Выделение белка оболочки ВМАльт и получение ВПЧ в физиологических условиях.
Белок оболочки ВМАльт выделяли обработкой вирусной суспензии в Трис-HCl буфере, рН 7.5 нейтральным солевым раствором LiCl, доводя его до конечной концентрации 2 М, помещали на -20°C на ночь, после чего проводили центрифугирование при 10000 об/мин 15 мин (центрифуга «Eppendorf»). Супернатант, содержащий БО диализовали против тридистилированной воды, проводя смену воды три раза. Белок после диализа ультрацентрифугировали в роторе Ti-50 при 40000 об/мин 1 час. Концентрацию белка определяли спектрофотометрически, используя коэффициент экстинкции: E280нм0.1%=0.7. Очищенный препарат БО при электрофоретическом анализе в денатурирующем полиакриламидном геле с додецилсульфатом натрия (ПААГ-ДСН) был представлен единственным компонентом с мол. массой 23 кДа (Рис. 2, дорожки 2, 3).
ВПЧ получали двумя способами:
1. Препарат БО ВМАльт с концентрацией 1-5 мг/мл инкубировали в воде или в 0.01М Трис-HCl рН 7,4 в течение 20 мин и добавляли 5 М NaCl до конечной концентрации 0.15 М.
2. Препарат БО ВМАльт с концентрацией 1-5 мг/мл инкубировали в воде или в 0.01М Трис-HCl рН 7,4 в присутствие 0.15М NaCl в течение 20 мин.
Пример 3. Анализ препаратов ВМАльт и ВПЧ ВМАльт методами просвечивающей электронной микроскопии и атомно-силовой микроскопии.
Для приготовления образцов для просвечивающей электронной микроскопии исследуемые образцы сорбировали на медных сетках для электронной микроскопии, покрытых формваровой пленкой (при нанесении пленки использовали 0,5% раствор формвара в дихлорэтане) в течение 15-20 секунд, после чего сетки негативно контрастировали 2% раствором уранилацетата. Наблюдения проводили с помощью электронных микроскопов JEM-1011 (JEOL, Japan) с цифровой фотокамерой GATAN ES500W и LEO-912AB (LEO, Germany).
Для приготовления образцов для атомно-силовой микроскопии на свежесколотую слюду или высокоориентированный пиролитический графит на 5-10 минут наносили 5-10 мкл исследуемого препарата. Затем образец два раза промывали в капле дистиллированной водой и высушивали на воздухе. Сканирование проводили на микроскопах Nanoscope IIIa (Digital Instruments, Santa Barbara, США) и SmartSPM (Аист-НТ, Россия) в резонансном режиме на воздухе. Типичная скорость сканирования - 1 Гц. Использовали кантилеверы fpN01S с резонансной частотой 118-190 кГц, жесткостью 5,3 Н/м и гарантированным радиусом закругления иглы 10 нм (НИИФП им. Ф.В. Лукина, Россия).
Для обработки и анализа АСМ-изображений использовали программу ФемтоСкан Онлайн (Центр перспективных технологий, Россия). Среднюю высоту частиц по АСМ-изображениям определяли при помощи автоматизированной функции программы ФемтоСкан, которая основана на пороговом анализе. Пороговая плоскость вычислялась как средняя высота поверхности, определенная по максимуму на гистограмме, плюс двойное среднеквадратичное отклонение (удвоенный уровень шума). Все части изображения, находящиеся выше этого порогового уровня, считались объектами, и их высота над пороговой плоскостью вычислялась автоматически. При статистическом анализе учитывались только отдельно лежащие частицы.
Анализ препарата ВМАльт методами ПЭМ и АСМ показал, что в поле зрения можно увидеть длинные гибкие нитевидные частицы, имеющие характерный для потексвирусов вид (Рис. 1). Статистический анализ показал, что средняя длина вирионов ВМАльт составила по данным электронной микроскопии 520-570 нм и средний диаметр -11 нм. Анализ препаратов с помощью АСМ позволил измерить среднюю высоту частиц, которая составила 6-8 нм.
Анализ препарата ВПЧ методами ПЭМ и АСМ проводили для изучения структуры и свойств ВПЧ, образованных из БО ВМАльт в разных условиях: в 0.15 М NaCl, а также в воде и в 0.01 М Трис-HCl буфере, рН 7,4 до и после добавления NaCl. Во всех случаях (Рис 3 А-Д) наблюдались длинные гибкие нитевидные частицы однородные по ширине и высоте, не отличающиеся по морфологии от вирионов ВМАльт. Средняя высота ВПЧ, как и случае вирионов ВМАльт, составила 6-8 нм. Средняя длина ВПЧ составила 400 нм, дисков не наблюдали. Средняя длина ВПЧ ВМП, полученных способом, описанном в прототипе составляла 90 нм (Mathieu et al., Induction of innate immunity in lungs with viruslike nanoparticles leads to protection against influenza and Streptococcus pneumoniae challenge. Nanomedicine: Nanotechnology, Biology, and Medicine 2013, 9, 839-848). Больший размер ВПЧ, приближающийся к размерам вириона обеспечивает более эффективную стимуляцию иммунного ответа.
Ранее нами было показано (Mukhamedzhanova et al., Characterization of Alternanthera mosaic virus and its Coat ProteinOpen Virol J. 2011; 5: 136-140), что БО ВМАльт в отсутствии РНК способен полимеризоваться in vitro с образованием вирусоподобных частиц и протяженных пучков при рН 4,0 и низкой ионной силе и в отличие от БО ВМП при рН 8,0. Представленные результаты показывают, что БО ВМАльт образует нитевидные ВПЧ и при нейтральных рН: в 0,01 М Трис-HCl буфере, рН 7,4 или в воде он формирует ВПЧ, сравнимые по размерам с вирусными частицами или превосходящие их по длине. После добавления к ВПЧ 0.15 М NaCl их структура остается неизменной. Также показано, что ВПЧ могут быть получены из БО ВМАльт инкубацией в 0,01 М Трис-HCl буфере, рН 7,4 или в воде в присутствие 0.15 М NaCl. Полученные ВПЧ оставались стабильными, по крайне мере, в течение 6 месяцев при 4°C.
Таким образом, результатом изобретения является новый способ получения ВПЧ ВМАльт в физиологических условиях.
Пример 4. Выделение белка оболочки ВТМ.
В качестве модельного антигена был выбран БО ВТМ, вируса относящегося к другой таксономической группе и не родственного антигенно с БО ВМАльт. Для получения БО ВТМ сначала были выделены вирионы ВТМ. Для этого листья зараженных ВТМ растений табака гомогенизировали с помощью ножевого гомогенизатора (число оборотов 800 об/мин) в двух объемах 0,1 М фосфатного буфера (рН 7,8), содержащем 20 мМ ЭДТА и 0,1% β-меркаптоэтанол. После гомогенизации измельченную растительную массу очищали фильтрацией под вакуумом через двойную марлевую ткань. Дальнейшая очистка гомогената листьев осуществлялась низкоскоростным центрифугированием, при 10000 об/мин в течение 20 мин (ротор JA-14, «Beckan») при t+4°C. К осветленному гомогенату добавляли 1/5 часть хлороформа (по объему) и непрерывно встряхивали полученную смесь в течение 10 мин. Методом низкоскоростного центрифугирования при 10000 об/мин (15 мин, t+4°C, ротор JA-14, «Beckan») осуществляли разделение фаз в полученной эмульсии. Верхнюю водную фазу аккуратно отбирали и добавляли полиэтиленгликоль (ПЭГ) (Мr 6000) до конечной концентрации 2% и NaCl до 1%. После полного растворения компонентов раствор выдерживали в течение 2 ч при t+4°C. Образовавшийся осадок вируса отделяли центрифугированием при 10000 об/мин и растворяли в мл 0,1 М фосфатного буфера (рН 7,8) при постоянном перемешивании при t+4C. Полученный экстракт осветляли центрифугированием при 10000 об/мин в течение 20 мин при t+4°C. Окончательную очистку вируса проводили путем ультрацентрифугирования препарата с использованием 20%-ной сахарозной подушки в роторе Ti-50 при 32000 об/мин в течение 120 мин, t+4°C. Полученные осадки растворяли в 10 мМ Трис-HCl буфере (рН 7,8) или в воде.
Белок оболочки ВТМ выделяли ацетатным методом. Суспензию вируса с концентрацией 3 мг/мл помещали в ледяную баню и по каплям при перемешивании добавляли двойной объем ледяной уксусной кислоты. Смесь инкубировали до выпадения осадка РНК. Хлопьевидный осадок РНК отделяли центрифугированием (10000 об/мин, центрифуга «Eppendorf») +4°C в течение 20 мин. К супернатанту, содержащему белок, добавляли равный объем воды и диализовали в течение суток против двух-трех смен воды (по 1 л) при +4°C. При достижении рН 4.5 (что соответствует изоэлектрической точке БО ВТМ) белок выпадал в осадок, который собирали центрифугированием (10000 об/мин, центрифуга «Eppendorf») в течение 20 мин. Осадок растворяли в воде.
Пример 5. Способность ВПЧ и вирионов ВМАльт усиливать иммунный ответ при совместной иммунизации с белком оболочки ВТМ.
Беспородных белых мышей иммунизировали внутрибрюшинно смесью ВПЧ или вирионов ВМАльт и антигена - БО ВТМ, в массовом соотношении 3:1. Доза ВПЧ или вирионов ВМАльт составляла 30 мкг, а БО ВТМ - 10 мкг на 1 инъекцию. Контрольную группу мышей иммунизировали по такой же схеме одним БО. Смесь для инъекции готовили непосредственно перед иммунизацией. Объем инъецируемой смеси составлял 0,5 мл на 1 животное. Каждая группа состояла из 5 животных. Проведено 3 иммунизации с двухнедельным интервалом между ними. Кровь, индивидуально от каждой мыши, брали из хвостовой вены через неделю после последней иммунизации. Кровь выдерживали 2 ч при комнатной температуре до формирования сгустка, помещали на ночь в холодильник и на следующий день сгусток отделяли центрифугированием 10000 g 10 мин. Полученную сыворотку использовали для определения титра антител к БО ВТМ. Титр определяли в пуле, полученном путем смешивания равных объемов антисывороток от каждого животного, с помощью непрямого метода иммуноферментного анализа (ИФА). На планшетах MaxiSorp (Nunc) БО ВТМ (5 мкг/мл в в деионизованной воде) в объеме 100 мкл на лунку. Планшеты выдерживали ночь в холодильнике, промывали PBST (PBS, 0,1% Твин 20, рН 7,4) 5 раз по 200 мкл на лунку и вносили тестируемые антисыворотки в двойных серийных разведениях, приготовленных на PBST, начиная с разведения 1/1000. В качестве отрицательного контроля использовали преиммунную мышиную сыворотку.
Инкубировали 1 ч при 37°C на термостатируемом шейкере, промывали, как описано и добавляли противомышиные Ig, конъюгированные с пероксидазой хрена (Promega) в рабочем разведении 1/20000, приготовленном на PBS, содержащим 0,5% бычьего сывороточного альбумина. Инкубировали 1 ч при 37°C на шейкере, промывали, как описано и добавляли субстрат - ABTS с перекисью водорода в 0,05 М цитратно-фосфатном буфере рН 4,4. Оптическую плотность в лунках определяли на ридере Titerteck Multiscan при длине волны 405 нм через 20 мин после добавления субстрата. Титром антисыворотки считали ее последнее разведение, оптическая плотность в котором втрое превышала соответствующее значение преиммунной мышиной сыворотки.
Результаты определения титров антисывороток показывают, что иммунизация животных смесью ВПЧ или вирионов ВМАльт и БО ВТМ приводит к десятикратному увеличению концентрации антител к БО ВТМ в крови иммунизированного животного по сравнению с иммунизацией одним БО. Титр антител на 7 день после последней иммунизации смесью ВПЧ ВМАльт или вирионов ВМАльт и БО составил 1/600000 и 1/580000 соответственно (Рис. 4 и 5).
В прототипе, титр антисыворотки к модельному антигену - нуклеопротеину вируса гриппа на 21 день после инъекции составил 1/200000.
Данный пример показывает, что адъювант на основе ВПЧ или вирионов ВМАльт более эффективен при равном количестве антигена, использованного для иммунизации, чем адъювант на основе ВПЧ ВМП.
Таким образом, другим результатом изобретения является создание нового эффективного адъюванта на основе ВПЧ или вирионов ВМАльт.
Пример 6. Влияние дозы ВПЧ и вирионов ВМАльт на образование антител к БО ВТМ вирусу при совместной иммунизации с белком-антигеном.
Беспородных белых мышей иммунизировали внутрибрюшинно смесью ВПЧ или вирионов ВМАльт и БО ВТМ в массовом соотношении 5:1, 3:1 и 1:1. Доза ВПЧ или вирионов ВМАльт составляла 50 мкг, 30 мкг и 10 мкг и БО ВТМ - 10 мкг на 1 инъекцию. Для иммуноферментного определения титра антител к БО и к вирусу на планшетах MaxiSorp (Nunc) сорбировали БО ВТМ (5 мкг/мл в деионизованной воде) в объеме 100 мкл на лунку. Остальные процедуры осуществляли, как описано в Примере 5.
Результаты определения титров мышиных антисывороток, представленные на рисунке 6, показали, что при совместной иммунизации животных смесью БО и ВПЧ или вирионов ВМАльт в массовом соотношении 5:1, 3:1 и 1:1, в крови иммунизированных животных возникают антитела к БО. Титр антител на 7 день после последней иммунизации составил 1/500000-1/530000-1/590000 для ВПЧ и 1/490000-1/520000-1/570000 для вирионов ВМАльт-MU. Следовательно, в выбранном интервале концентраций доза не оказывала ощутимого влияния на эффективность стимуляции иммунного ответа.
Данный пример показывает, что ВПЧ или вирионы ВМАльт, используемые в качестве адъюванта, обладают высокой иммуногенностью в широком интервале концентраций.