Результат интеллектуальной деятельности: АНТИПРОТЕИНАЗНЫЙ ПРЕПАРАТ
Вид РИД
Изобретение
Изобретение относится к области медицины, а именно к антипротеиназному препарату, который может быть использован для коррекции состояний, связанных с повышенной протеолитической активностью в тканях, крови и других биологических жидкостях.
Многие тяжелые заболевания (панкреатит, сепсис, шоки различной этиологии и т.п.) сопровождаются активацией процессов протеолиза. Одним из наиболее эффективных путей коррекции таких патологических состояний является селективное подавление активности протеолитических ферментов, которое достигается введением ингибиторов протеолитических ферментов.
Известны препараты на основе выделяемого из поджелудочной железы крупного рогатого скота ингибитора - Трасилол, Контрикал, Гордокс [1].
Недостатком этих препаратов является то, что проявляя высокую ингибиторную активность по отношению к трипсину, данные препараты малоэффективны по отношению к наиболее агрессивным при патологии организма протеиназам - лейкоцитарной и панкреатической эластазе, катепсину G. К тому же, лечебное действие этих препаратов кратковременно вследствие их низкой молекулярной массы (порядка 6500) и быстрого выведения из организма.
Наиболее близким к заявляемому по технической сущности и достигаемому эффекту является антипротеиназный препарат на основе ингибитора протеолитических ферментов белковой природы - овомукоида из белка утиных яиц при следующем соотношении компонентов:
|
Это препарат обладает поливалентной антипротеиназной активностью по отношению к панкреатическим и лейкоцитарным протеиназам, не подавляет активность протеиназ свертывающей системы крови, а также обладает пролонгированным лечебным действием, обусловленным высокой молекулярной массой овомукоида (31000).
Недостатком этого препарата является невысокая антипротеиназная активность и невысокое лечебное действие.
Целью изобретения является повышение антипротеиназной активности препарата и повышение лечебного действия.
Поставленная цель достигается тем, что антипротеиназный препарат на основе ингибитора протеиназ белковой природы - овомукоида из белка утиных яиц, натрия хлорида и воды для инъекций дополнительно содержит маннитол при следующем соотношении компонентов:
|
Овомукоид из белка утиных яиц - гликопротеин с молекулярной массой 31000 - способен взаимодействовать с протеолитическими ферментами, ингибируя их активность. Выделение овомукоида из белка утиных яиц проводят по методике [3].
Маннитол - диуретик, который вызывает перемещение жидкости из тканей в сосудистое русло [4]. Перемещение жидкости, а следовательно, и содержащихся в ней ферментов из тканей в сосудистое русло, где и происходит взаимодействие ферментов с овомукоидом и нейтрализация протеолитической активности ферментов, и приводит к повышению эффективности лечебного действия препарата, которое проявляется в повышении времени антиферментного действия препарата.
Неожиданным эффектом является повышение антипротеиназной активности овомукоида под действием маннитола.
Препарат готовят следующим образом.
Пример 1. 10.0 г полученного в асептических условиях, очищенного ультрафильтрацией и лиофильно высушенного овомукоида из белка утиных яиц, 8.8 г хлорида натрия, 200 г маннитола растворяют в воде для инъекций и доводят объем раствора до 1 л. Раствор фильтруют через стерилизующий фильтр, и антипротеиназный препарат готов к употреблению.
Антипротеиназную активность препарата определяют по подавлению овомукоидом амидазной активности трипсина, используя в качестве субстрата n-нитроанилид-Nα-бензоил-D,L-аргинина по методике [5].
При pH крови (7.4) 2 мл препарата, содержащие 10 мг овомукоида, ингибируют активность 11.8 мг трипсина.
Пример 2. Препарат готовят по примеру 1, используя 10.0 г овомукоида из белка утиных яиц, 9.2 г хлорида натрия, 250 г маннитола и воду до 1 л.
При pH 7.4 1 мл препарата, содержащий 10 мг овомукоида, ингибирует активность 12.1 мг трипсина.
Пример 3. Препарат готовят по примеру 1, используя 8.0 г овомукоида из белка утиных яиц, 9.0 г хлорида натрия, 250 г маннитола и воду до 1 л.
При pH 7.4 1.25 мл препарата, содержащий 10 мг овомукоида, ингибирует активность 12 мг трипсина.
Пример 4. Препарат готовят по примеру 1, используя 5.0 г овомукоида из белка утиных яиц, 9.0 г хлорида натрия, 150 г маннитола и воду до 1 л.
При pH 7.4 2 мл препарата, содержащие 10 мг овомукоида, ингибируют активность 11.9 мг трипсина.
Пример 5. (контрольный, по прототипу). Препарат готовят по примеру 1 без использования маннитола.
При pH 7.4 2 мл препарата, содержащие 10 мг овомукоида, ингибируют активность 8.3 мг трипсина.
Пример 6. Лечебный эффект препарата изучают на 54 крысах линии Вистар обоего пола на фоне острого деструктивного панкреатита. Моделирование воспаления поджелудочной железы осуществляют путем введения медицинской консервированной желчи в общий билиопанкреатический проток путем канюляции его через просвет двенадцатиперстной кишки тупой иглой 0.4 мм диаметром. Объем вводимой желчи 0.1 мл на 100 г веса животного. Животных разделяют на три группы по 18 особей: контрольную и две опытные группы для изучения эффективности действия заявленного препарата и препарата сравнения. Сравниваемые препараты вводят внутривенно однократно через 2 часа после развития острого панкреатита из расчета 10 мг овомукоида на 1 кг массы тела. В контрольной группе никакого лечения не проводят.
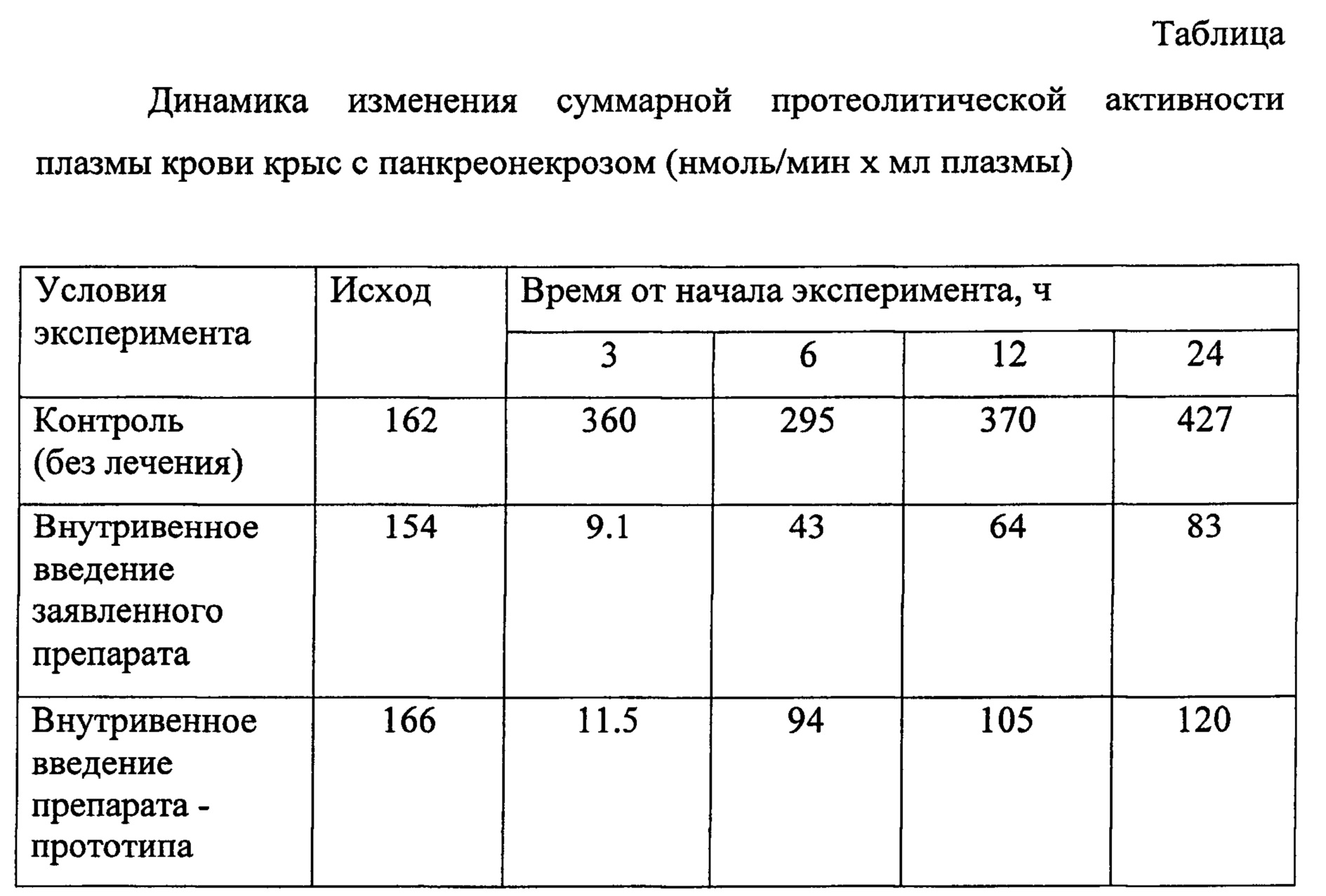
В динамике развития заболевания изучают суммарную протеолитическую активность плазмы крови (см. табл.).
При выбранной модели заболевания у крыс контрольной серии развивается картина крупноочагового прогрессирующего панкреонекроза с геморрагиями в некротизированных тканях, жировыми некрозами и нагноением. Происходит резкое увеличение протеолитической активности плазмы крови.
При внутривенном введении заявленного антипротеиназного препаратов и препарата-прототипа эти явления в значительной степени регрессируют на фоне существенного снижения суммарной протеолитической активности плазмы крови. Через три часа после введения препаратов общая протеолитическая активность плазмы крови уменьшается более, чем в 30 раз по сравнению с животными контрольной серии, достигая минимального значения.
Заявленный препарат по сравнению с препаратом-прототипом обладает повышенным лечебным действием за счет пролонгирования его действия. Так, через 24 часа после введения заявленного препарата уровень протеолитической активности плазмы составляет 54% от исходной, а для препарата-прототипа эта величина составляет 72%.
Таким образом, введение в состав антипротеиназного препарата маннитола обеспечивает повышение антипротеиназной активности препарата с 8.3 до 11.8-12.1 мг трипсина на 10 мг овомукоида и повышение лечебного действия за счет пролонгирования действия препарата.
Предельные содержания маннитола обусловлены тем, что ниже 150 г маннитола/л эффективность его действия незначительна, а выше 250 г маннитола/л эффективность его действия существенно не увеличивается.
Источники информации
[1] Машковский М.Д. Лекарственные средства, Москва, Новая волна, 2005. С. 663.
[2] Патент РФ №2053789, МПК A61K 38/55, опубл. 10.02.1996, Бюл №4, 1996.
[3] Патент РФ №2460734, МПК C07K 1/14, C07K 1/30, C07K 1/34, C07K 1/36, C07K 14/81, опубл. 10.09.2012, Бюл. №25, 2012.
[4] Машковский М.Д. Лекарственные средства, Москва, Новая волна, 2005. С. 509.
[5] Kakade M.L., Simons М., Liener Y.E. The Evaluation of Natural vs. Synthetic Substrates for Measuring the Antitryptic Activity of Soybean Samples//Cereal Chemistry. 1969. V. 46. №5. P. 518-523.

