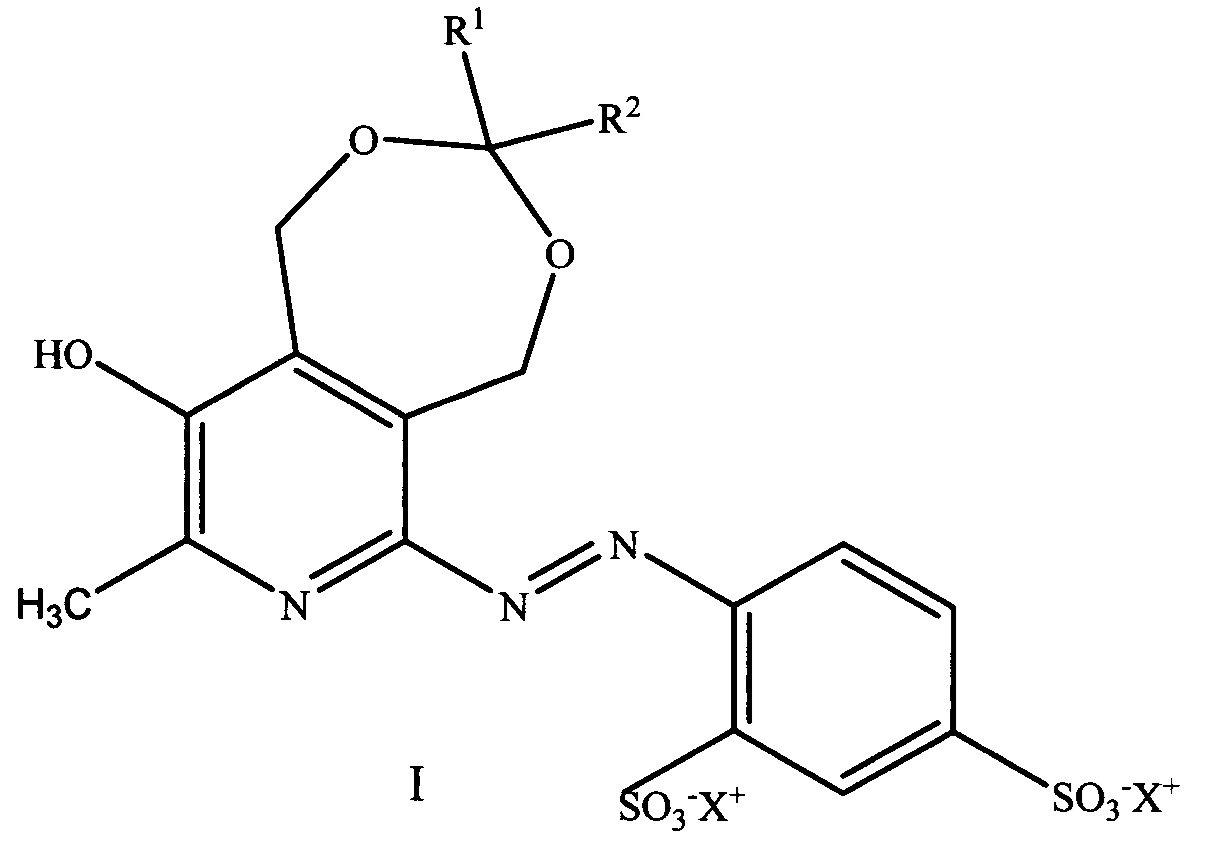
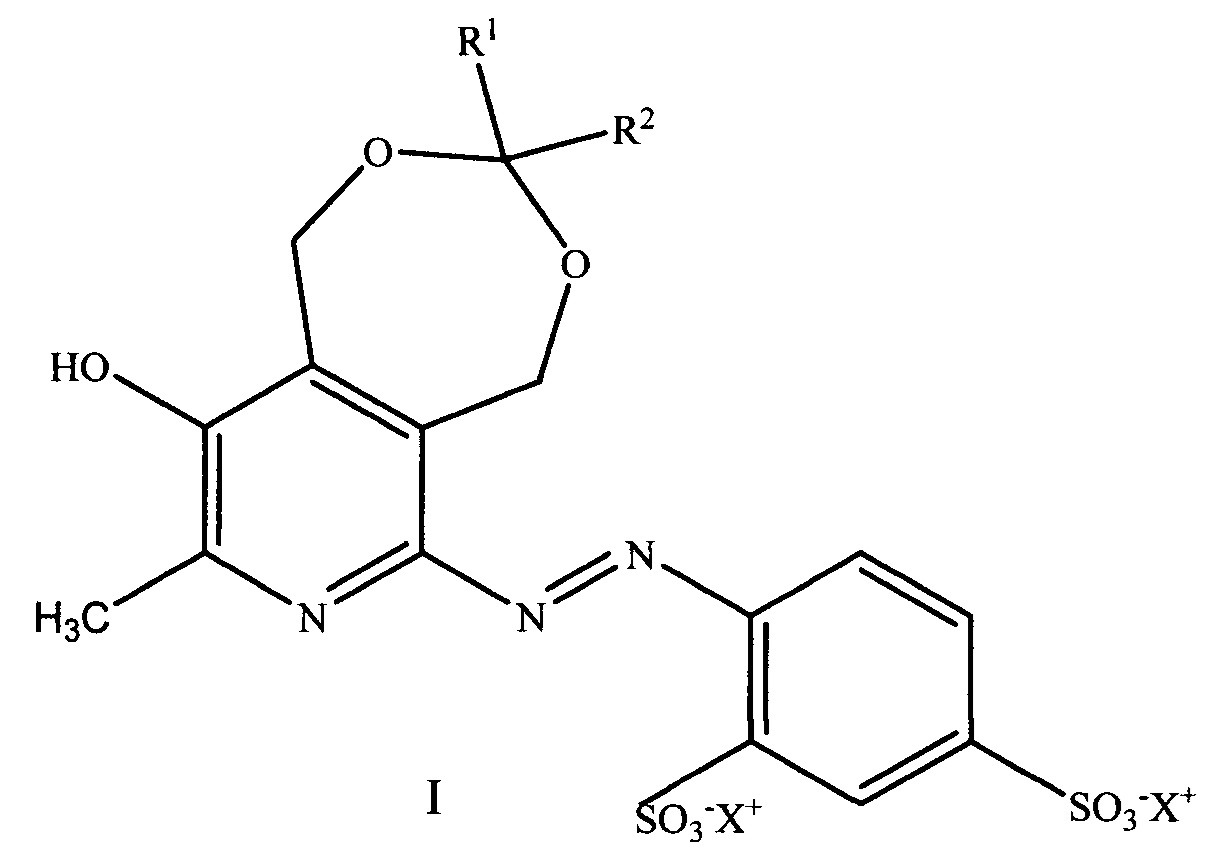
Результат интеллектуальной деятельности: Ингибиторы образования конечных продуктов гликирования на основе азопроизводных фенилсульфокислот
Вид РИД
Изобретение
Изобретение относится к физиологически активным веществам гетероциклического ряда, обладающим высокой антигликирующей активностью (блокируют неферментативное взаимодействие белков с глюкозой и образование конечных продуктов гликирования) и представляющим собой производные 4-((пиридин-2-ил)диазенил)фенилсульфокислот и их солевые и сокристальные формы общей формулы I:
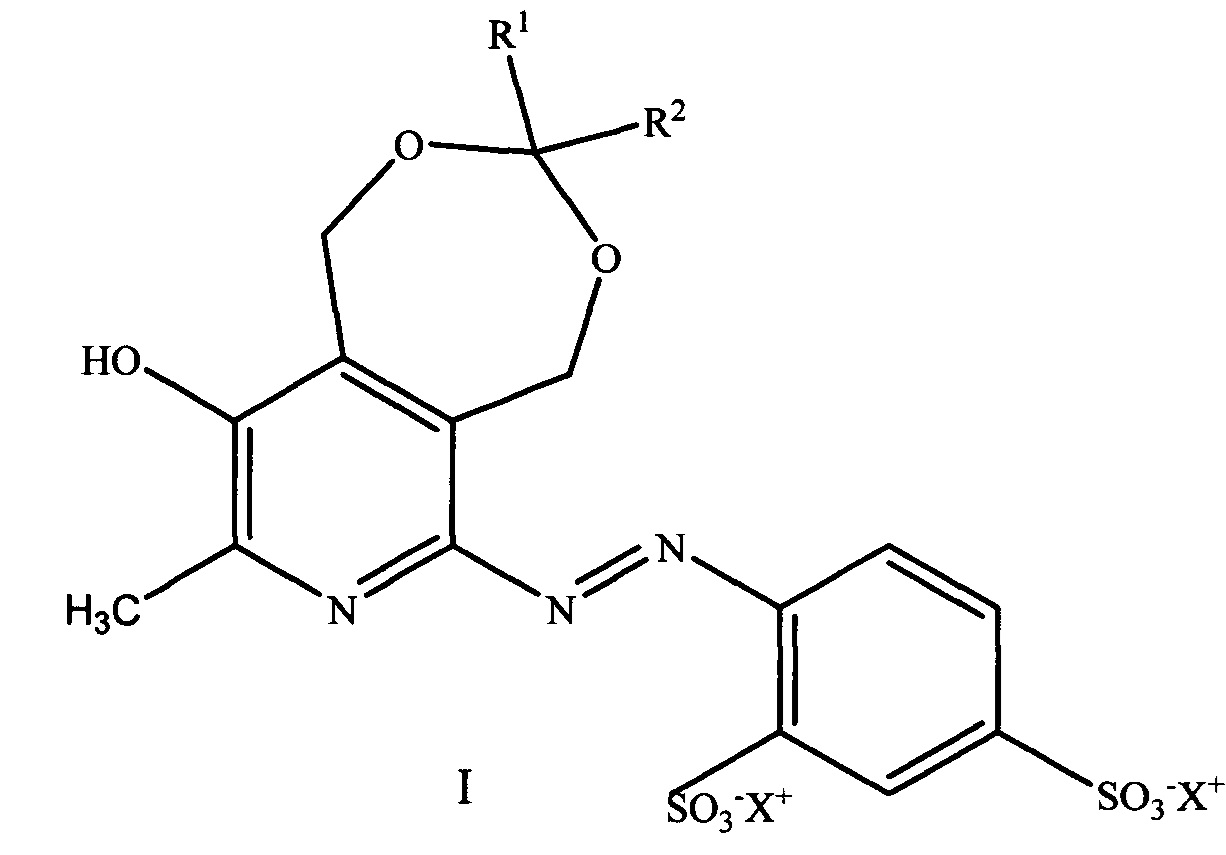 ,
,
где R1=Н, СН3; R2=Н, СН3, С3Н7, i-C3H7, C5H11, С7Н15, C8H17;
X+ = катионы щелочных металлов, такие как Na+и K+.
Соединения формулы I являются эффективными ингибиторами образования конечных продуктов гликирования (далее КПГ) и могут найти широкое применение в медицине в области лечения социально-значимых заболеваний, а именно - осложнения сахарного диабета, атеросклероз, ревматоидный артрит, остеоартрит, нейродегенеративные заболевания, включая болезни Альцгеймера и Паркинсона.
Гликирование (неферментативное гликозилирование, реакция Майяра) - химическая реакция, в которой карбонильные группы восстановленных сахаров связываются с аминогруппами долгоживущих белков, липидов или пептидов, с образованием конечных продуктов гликирования (КПГ) ([1] S. Khangholi, F.A. Abdul Majid, N.J.A. Berwary, F. Ahmad, R. Bin Abd Aziz, Planta Med., 2016; 82: 32-45; [2] V.P. Singh, A. Bali, N. Singh, A.S. Jaggi, Korean J. Physiol. Pharmacol., 2014, 18: 1-14).
Внутри- и внеклеточное накопление КПГ считают важным фактором патогенеза таких заболеваний, как атеросклероз ([3] М. Busch, S. Franke, С. Ruster, G. Wolf, European Journal of Clinical Investigation, 2010, 40 (8): 742-755), сердечная недостаточность, воспаление, ревматоидный артрит и остеоартрит, нейродегенеративные заболевания, включая болезни Альцгеймера и Паркинсона ([4] J. Li, D. Liu, L. Sun, Y. Lu, Z. Zhang, Journal of the Neurological Sciences, 2012, 317: 1-5).
Особенно интенсивно данный процесс протекает при сахарном диабете, при этом скорость образования КПГ зависит от уровня и длительности экспозиции глюкозы ([5] R. Ramasamy, S.F. Yan, A.M. Schmidt, Ann. N.Y. Acad Sci., 2011, 1243: 88-102; [6] М.И. Балаболкин. Сахарный Диабет, 2002, 4: 8-16).
Эффекты КПГ могут быть классифицированы как рецептор-независимые или -зависимые, и КПГ могут действовать внутриклеточно или циркулировать и действовать на рецепторы клеточной поверхности, такие как рецептор для КПГ (РКПГ). Поскольку гликирование происходит в течение длительного периода времени, КПГ влияют на долгоживущие белки. Например, главными мишенями для них являются структурные компоненты соединительной ткани, и в частности коллаген типа IV, а также другие долгоживущие белки, в том числе миелин, тубулин, кристаллин, активатор плазминогена 1, фибриноген, которые могут также подвергаться гликированию ([7] S.-Y. Goh, М.Е. Cooper. J Clin Endocrinol Metab, 2008, 93 (4): 1143-1152).
Связываясь с мембранными РКПГ, конечные продукты гликирования активируют некоторые внутриклеточные сигнальные пути. Например, усиливают транскрипцию ядерного фактора NF-кВ и его генов-мишеней, активируют протеинкиназу С и NADPH-оксидазу, что приводит к увеличению образования провоспалительных цитокинов, свободных радикалов, хемоаттрактантов ([1], [8] S.C. Но, P.W. Chang, Am. J. Plant. Sci., 2012, 3: 995 - 1002). Все вышеперечисленное лежит в основе патогенеза таких последствий сахарного диабета, как диабетические атеросклероз, нефро-, нейро-, ретино-, кардио-, ангиопатии, которые являются причиной высокого риска инвалидизации и смертности среди пациентов с сахарным диабетом.
Применение соединений, обладающих высокой антигликирующей активностью, позволит уменьшить образование КПГ в организме, тем самым улучшая качество жизни пациентов, снижая риск возникновения атеросклероза, ревматоидного артрита, остеоартрита, нейродегенеративных заболеваний, включая болезни Альцгеймера и Паркинсона, а также таких осложнений сахарного диабета, как диабетические атеросклероз, нефро-, нейро-, ретино-, кардио-, ангиопатии, которые являются причиной высокого риска инвалидизации и смертности среди пациентов с сахарным диабетом.
Все вышеперечисленное обусловливает повышенный интерес в мире к поиску ингибиторов образования конечных продуктов гликирования, поскольку препаратов, специфически угнетающих образование КПГ и разрешенных для клинического применения, на сегодняшний день в мире на дату представления настоящей заявки не существует.
Проведенный заявителем анализ российских и зарубежных патентных баз данных, научной литературы и Интернет-ресурсов показал, что существуют аналоги заявленного технического решения по назначению, способные ингибировать образование КПГ, которые, однако, обладают значительными недостатками, а именно недостаточно высокой эффективностью и/или существенными побочными эффектами, например высокой токсичностью и т.д.
Далее заявителем приведена информация о выявленных препаратах, вышедших на стадию клинических испытаний. Первым и наиболее изученным веществом, ингибирующим гликирование белков, является аминогуанидин (АГ) ([9] A. Cerami, Р.С. Ulrich, М. Brownlee, Pat US 4758583 A, опубл. 19.07.1988). Он предназначен для предотвращения формирования КПГ и глюкозопроизводных поперечносшитых молекул коллагена. Механизм антигликирующего действия аминогуанидина связывают с его способностью захватывать реактивные дикарбонильные интермедиаты. Однако клинические испытания данного препарата были остановлены в связи с его недостаточной эффективностью и наличием побочных эффектов.
В настоящее время проводятся клинические испытания пиридоксамина ([10] R. Khalifah, B.G. Hudson, Pat US 6716858B1, опубл. 06.04.2004), также обладающего антигликирующими свойствами, но он тоже проявляет невысокую активность, сопоставимую с аминогуанидином, снятым с клинических испытаний. Других аналогов заявленного технического решения, используемых по назначению и вошедших на стадию клинических исследований, на дату предоставления настоящей заявки заявителем не выявлено.
Таким образом, на дату представления заявочных материалов, проблема создания высокоактивных ингибиторов образования КПГ, разрешенных к клиническому применению, остается нерешенной не только в РФ, но и за рубежом.
Заявленное техническое решение иллюстрируется следующими материалами: схемой, на которой представлена схема синтеза целевых веществ, таблицами 1, 2, на которых представлены результаты определения антигликирующей активности заявленного технического решения по сравнению с прототипом (аминогуанидином).
Задачей заявленного технического решения является создание соединений, обладающих высокой антигликирующей активностью, которые обеспечивают возможность вывода на рынок новых лекарственных средств, не имеющих аналогов в мире.
Техническим результатом предлагаемого изобретения является создание соединений, обладающих значительно более высокой антигликирующей активностью по сравнению с ингибиторами образования КПГ, вышедшими на стадию клинических исследований.
Сущность предлагаемого изобретения состоит в том, что получают производные 4-(пиридин-2-илдиазенил)фенилсульфокислот общей формулы I, обладающие более высокой (до 19 раз и более) антигликирующей активностью по сравнению с прототипом (аминогуанидином).
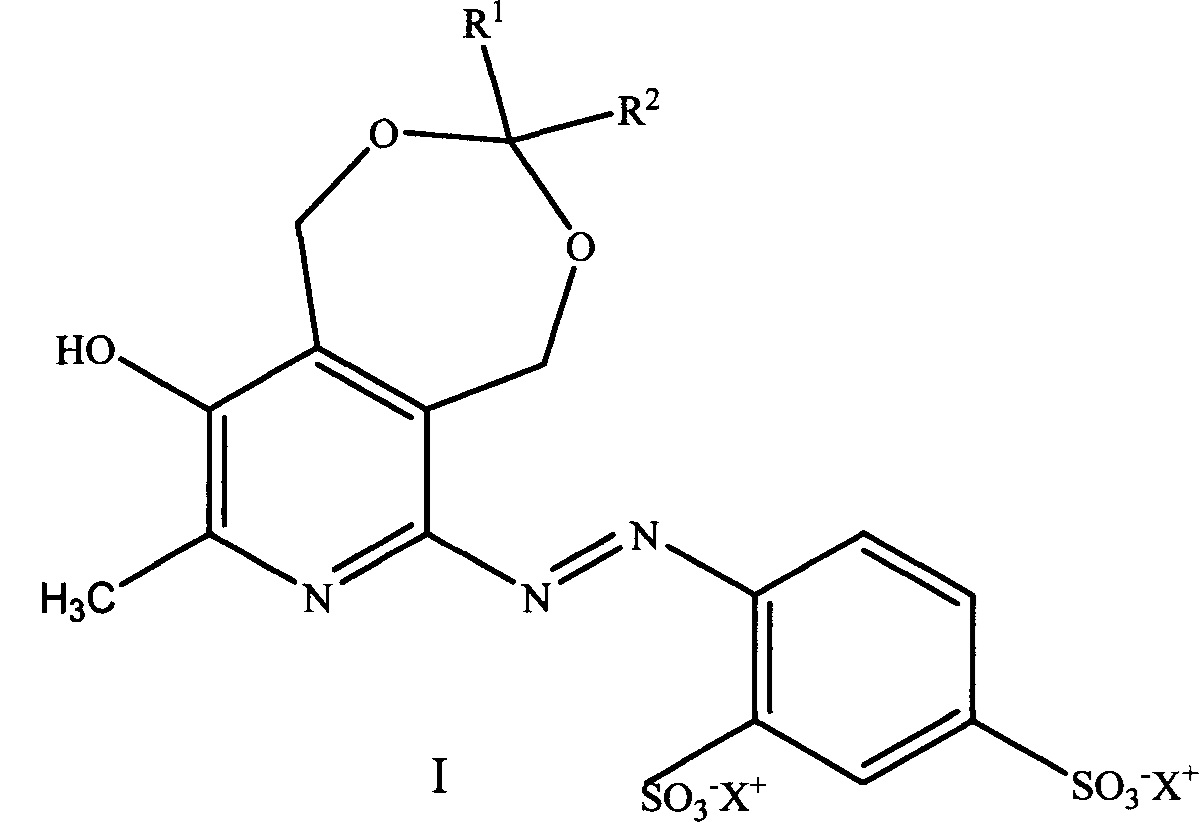 ,
,
где R1=Н, СН3; R2=Н, СН3, С3Н7, i-C3H7, С5Н11, С7Н15, С8Н17;
X+ = катионы щелочных металлов, такие как Na+и K+.
Заявленные соединения синтезируют по реакции азосочетания семичленных ацеталей пиридоксина 1(а-з) с диазониевой солью, полученной из 4-аминобензол-1,3-дисульфоксилоты при температуре 0-5°C согласно нижеприведенной схеме:
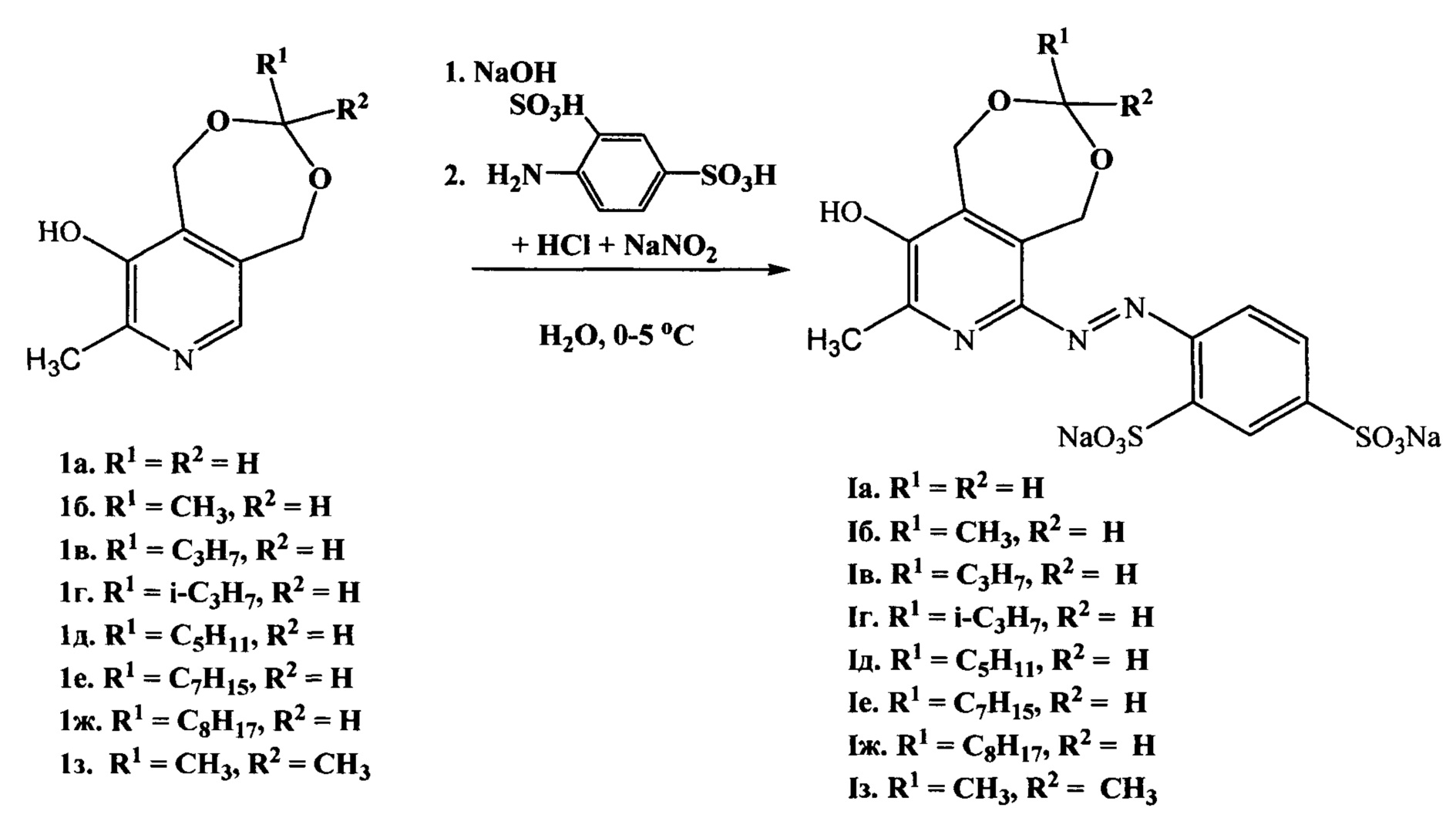
Синтез и физико-химические характеристики новых соединений I(а-з) приведены в примерах конкретного выполнения. Спектры ЯМР 1Н зарегистрированы на приборе «Bruker» AVANCE 400 (400 МГц). Химический сдвиг определяют относительно сигналов остаточных протонов дейтерированного растворителя. Эксперимент ВЭЖХ/МС сверхвысокого разрешения проведен с использованием масс-спектрометра TripleTOF 5600, АВ Sciex (Германия). Температуру плавления веществ определяют на приборе OptiMelt МРА100 (Stanford Research Systems).
Примеры конкретного выполнения заявленного технического решения
Пример 1. Синтез 4-((9-гидрокси-8-метил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Ia)
К раствору 1,27 г (5 ммоль) 4-аминофенил-1,3-дисульфокислоты в 50 мл 0.2 М соляной кислоты, предварительно охлажденному до 5°C, добавляют 0.35 г (5 ммоль) нитрита натрия в 5 мл воды. Полученную реакционную массу перемешивают 5 мин, затем переливают ее к раствору 0.90 г (5 ммоль) ацеталя 1а и 0.8 г (20 ммоль) гидроксида натрия в 50 мл воды. Реакционную массу перемешивают 1 ч при комнатной температуре, после чего нейтрализуют 1 М соляной кислотой до pH 8. Затем растворитель отгоняют в вакууме, сухой остаток последовательно промывают 50 мл ацетона, 10 мл этилового спирта и растворяют в 20 мл ДМСО. Нерастворившийся остаток отфильтровывают. К фильтрату добавляют 150 мл хлороформа, выпавший осадок отфильтровывают, промывают хлороформом и высушивают в вакууме.
Выход 28%. Т. пл 250°C (с разложением). ЯМР 1H (400 МГц, ДМСО-d6), δ, м.д.: 2.20 (с, CH3., 3Н); 4.78 (с, CH2, 2Н); 4.92 (с, CH2, 2Н); 5.30 (с, CH2, 2Н); 7.50, 7.58 (АВХ, 3JAB=8.0 Гц, 4JAX=-1.8 Гц, 2СН., 2Н); 7.65 (с, ОН, 1H); 8.13 (д. АВХ, 4JAX=-1.8 Гц, СН, 1Н). ЯМР 13С {Н} (100 МГц, D2O), δ, м.д: 18.80 (с, CH3.); 65.81 (с, CH2); 66.02 (с, CH2); 97.51 (с, С); 119.64 (с, Car.); 125.54 (с, Car.); 129.80 (с, Car.); 133.70 (с, Car.); 138.39 (с, Car.); 138.73 (с, Car.); 142.23 (с, Car.); 144.10 (с, Car.); 151.05 (с, Car..); 152.47 (с, Car.); 166.30 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 444.0177, C15H14N3O9S2, рассчитано [M-2Na+H]- 444.0177.
Пример 2. Синтез 4-((9-гидрокси-3,8-диметил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Iб)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь Iб вместо ацеталя 1а. Выход 46%. ЯМР 1H (400 МГц, ДМСО-d6), δ, м.д.: 1.30 (д, 3J=5.0 Гц., CH3., 3Н); 2.19 (с, CH3., 3Н); 4.53, 5.02 (АВ, 2Jнн=-15 Гц, CH2, 2Н); 5.03, 5.54 (АВ, 2Jнн=-14.8 Гц, CH2, 2Н); 5.10 (к, 3J=5.0 Гц., СН., 1Н); 7.50, 7.58 (АВХ, 3JAB=8.4 Гц, 4JAX=-1.7 Гц, 2СН, 2Н); 8.13 (АВХ, 4JAX=-1.7 Гц, СН., 1H). ЯМР 13С {Н} (100 МГц, D2O), δ, м.д: 19.46 (с, CH3.); 20.08 (с, CH3.); 62.74 (с, CH2); 63.05 (с, CH2); 101.92 (с, С); 116.09 (с, Car.); 125.51 (с, Car.); 127.11 (с, Car.); 129.77 (с, Car.); 139.58 (с, Car.), 139.89 (с, Car.); 140.56 (с, Car.); 145.10 (с, Car.); 150.38 (с, Car.); 151.10 (с, Car.); 170.30 (с, Car.).
Пример 3. Синтез 4-((9-гидрокси-3-пропил-8-метил-1,5-дигидро-[1,3]диоксепино[5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Iв)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь Iв вместо ацеталя 1а. Выход 24%. Т. пл. 250°C (с разложением). ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.92 (т, 3Jнн=7.1 Гц, CH3, 3Н); 1.34-1.43 (м, CH2, 2Н); 1.58-1.64 (м, CH2, 2Н); 2.20 (с, CH3, 3Н); 4.54, 5.02 (АВ, 2Jнн=-16 Гц, CH2, 2Н); 5.03, 5.55 (АВ, 2Jнн=-14 Гц, CH2, 2Н); 4.90 (т, 3Jнн=5.6 Гц, СН, 1H); 7.50, 7.56 (АВХ, 3JAB=10.0 Гц, 4JAX=-2.0 Гц, 2CHar., 2Н); 7.65 (с, OH, 1Н); 8.13 (АВХ, 4JAX=-2.0 Гц, CHar., 1Н). ЯМР 13С {Н} (100 МГц, D2O), δ, м.д.: 13.33 (с, CH3); 17.61 (с, CH2); 19.05 (с, CH3); 34.78 (с, CH2); 63.75 (с, CH2); 63.92 (с, CH2); 106.61 (с, С); 117.19 (с, Car.); 125.52 (с, Car.); 129.86 (с, Car.); 133.35 (с, Car.); 136.95 (с, Car.); 138.55 (с, Car.); 144.14 (с, Car.); 147.38 (с, Car.); 151.22 (с, Car.); 154.40 (с, Car.); 165.16 (с, Car.). HRMS-ESI: найдено [М-2Na+H]- 486.0646, C18H20N3O9S2, вычислено [M-2Na+H]- 486.0646.
Пример 4. Синтез 4-((9-гидрокси-3-изо-пропил-8-метил-1,5-дигидро-[1,3]диоксепино [5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Ir)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь 1г вместо ацеталя 1а. Выход 32%. Т.пл. 243°C (с разложением). ЯМР 1H (400 МГц, ДМСО-d6), δ, м.д.: 0.91 (д, 3Jнн=6.8 Гц, CH3, 3Н); 0.93 (д, 3Jнн=6.8 Гц, CH3, 3Н); 1.91-2.03 (м, СН, 1Н); 2.29 (с, CH3, 3Н); 4.55, 4.82 (AB, 2Jнн=-14 Гц, CH2, 2Н); 4.97, 5.29 (AB, 2Jнн=-16 Гц, CH2, 2Н); 4.52 (д, 3Jнн=6.9 Гц, СН, 2Н); 7.49, 7.57 (АВХ, 3JAB=8.0 Гц, 2CHar., 2Н); 7.98 (д. АВХ, CHar., 1Н). ЯМР 13С {Н} (100 МГц, ДМСО-d6), δ, м.д.: 18.04 (с, CH3); 19.91 (с, CH3); 30.10 (с, СН); 61.13 (с, CH2); 61.90 (с, CH2); 108.69 (с, С); 114.32 (с, Car.); 125.46 (с, Car.); 127.77 (с, Car.); 133.54 (с, Car.); 134.24 (с, Car.); 137.24 (с, Car.); 137.40 (с, Car.); 143.08 (с, Car.); 145.35 (с, Car.); 160.45 (с, Car.); 176.81 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 486.0646, C18H20N3O9S2, вычислено [M-2Na+H]- 486.0646.
Пример 5. Синтез 4-((9-гидрокси-3-пентил-8-метил-1,5-дигидро-[1,3]диоксепино [5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Iд)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь 1д вместо ацеталя 1а. Выход 21%. Т.пл. 280°C (с разложением). ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.88 (т, 3Jнн=6.7 Гц, CH3., 3Н); 1.25-1.42 (м, 3CH2, 6Н); 1.55-1.66 (м, CH2, 2Н); 2.19 (с, CH3, 3Н); 4.53, 5.01 (AB, 2Jнн=-16 Гц, CH2, 2Н); 5.01, 5.55 (AB, 2Jнн=-16 Гц, CH2, 2Н); 4.88 (т, 3Jнн=5.8 Гц, СН, 1H); 7.50, 7.58 (АВХ, 3JAB=8.0 Гц, 4JAX=-1.9 Гц, 2CHar., 2Н); 8.12 (д. АВХ, 4JAX=-1.9 Гц, CHar., 1Н). ЯМР 13С {Н} (100 МГц, D2O), δ, м.д.: 13.51 (с, CH3); 18.81 (с, CH3); 22.12 (с, CH2); 23.76 (с, CH2); 30.95 (с, CH2); 32.69 (с, CH2); 63.72 (с, CH2); 63.91 (с, CH2); 106.84 (с, С); 119.56 (с, Car.); 125.53 (с, Car.); 129.75 (с, Car.); 133.31 (с, Car.); 138.47 (с, Car.); 138.76 (с, Car.); 142.32 (с, Car.); 144.17 (с, Car.); 151.24 (с, Car.); 152.48 (с, Car.); 166.36 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 514.0959, C20H24N3O9S2, вычислено [M-2Na+H]- 514.0959.
Пример 6. Синтез 4-((9-гидрокси-3-гептил-8-метил-1,5-дигидро-[1,3]диоксепино [5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Ie)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь 1е вместо ацеталя 1а. Выход 30%. Т.пл. 290°C (с разложением). ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.87 (т, 3Jнн=6.8 Гц, CH3, 3Н); 1.22-1.42 (м, 5CH2, 10Н); 1.57-1.65 (м, CH2, 2Н); 2.19 (с, CH3, 3Н); 4.53, 5.00 (AB, 2Jнн=-16 Гц, CH2, 2Н); 5.00, 5.54 (АВ, 2Jнн=-14 Гц, CH2, 2Н); 4.88 (т, 3Jнн=6.3 Гц, СН, Н); 7.49, 7.57 (АВХ, 3JAB=8.0 Гц, 4JAX=-2.3 Гц, 2CHar., 2Н); 8.13 (д. АВХ, 4JAX=-2.3 Гц, CHar., 1H). ЯМР 13С {Н} (100 МГц, ДМСО-d6), δ, м.д.: 13.99 (с, CH3); 19.42 (с, CH3); 22.10 (с, CH2); 24.38 (с, CH2); 28.68 (с, CH2); 28.84 (с, CH2); 31.24 (с, CH2); 33.11 (с, CH2); 63.05 (с, CH2); 63.17 (с, CH2); 105.20 (с, С); 116.01 (с, Car.); 125.49 (с, Car.); 127.03 (с, Car.); 129.68 (с, Car.); 139.59 (с, Car.); 139.75 (с, Car.); 140.52 (с, Car.); 145.21 (с, Car.); 150.31 (с, Car.); 151.07 (с, Car.); 170.42 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 542.1272, C22H28N3O9S2, вычислено [M-2Na+H]- 542.1272.
Пример 7. Синтез 4-((9-гидрокси-3-октил-8-метил-1,5-дигидро-[1,3]диоксепино [5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Iж)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь 1ж вместо ацеталя 1а. Выход 29%. Т.пл. 300°C (с разложением). ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 0.86 (т, 3Jнн=7.5 Гц, CH3, 3Н); 1.24-1.40 (м, 6CH2, 12Н); 1.57-1.65 (м, CH2,2Н); 2.19 (с, CH3, 3Н); 4.53, 5.00 (AB, 2Jнн=-14 Гц, CH2, 2Н); 5.01, 5.54 (АВ, 2Jнн=-14 Гц, CH2, 2Н); 4.88 (т, 3Jнн=5.8 Гц, СН, 1H); 7.50, 7.57 (АВХ, 3JAB=8.4 Гц, 4JAX=-2.2 Гц, 2CHar., 2Н); 8.12 (д. АВХ, 4JAX=-2.2 Гц, CHar., 1H). ЯМР 13С {Н} (100 МГц, ДМСО-d6), δ, м.д.: 13.99 (с, CH3); 19.44 (с, CH3); 22.12 (с, CH2); 24.37 (с, CH2); 28.66 (с, CH2); 28.89 (с, CH2); 28.99 (с, CH2); 31.30 (с, CH2); 33.12 (с, CH2); 63.04 (с, CH2); 63.17 (с, CH2); 105.20 (с, С); 116.05 (с, Car.); 125.50 (с, Car.); 127.06 (с, Car.); 129.77 (с, Car.); 139.60 (с, Car.); 139.83 (с, Car.); 140.54 (с, Car.); 145.16 (с, Car.); 150.33 (с, Car.); 151.08 (с, Car.); 170.35 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 556.1429, C23H30N3O9S2, вычислено [M-2Na+H]- 556.1429.
Пример 8. Синтез 4-((9-гидрокси-3,3,8-триметил-1,5-дигидро-[1,3]диоксепино [5,6-с]пиридин-6-ил)диазенил)фенил-1,3-дисульфоната натрия (Iз)
Синтезируют и разрабатывают аналогично соединению Ia, используя ацеталь 1з вместо ацеталя 1а. Выход 28%. Т.пл. 264°C (с разложением). ЯМР 1Н (400 МГц, ДМСО-d6), δ, м.д.: 1.42 (с, 2CH3, 6Н); 2.18 (с, CH3, 3Н); 4.69 (с, CH2, 2Н); 5.24 (с, CH2, 2Н); 7.75, 7.82 (АВХ, 3JAB=8.0 Гц, 4JAX=-1.9 Гц, 2CHar., 2Н), 7.65 (с, OH, 1H), 8.13 (д. АВХ, 4JAX=-1.9 Гц, CHar., 1Н). ЯМР 13С {Н} (100 МГц, D2O), δ, м.д.: 18.42 (с, CH3); 23.14 (с, CH3); 59.99 (с, CH2); 60.53 (с, CH2); 103.76 (с, С); 119.60 (с, Car.); 125.53 (с, Car.); 129.80 (с, Car.); 133.12 (с, Car.); 137.39 (с, Car.); 138.41 (с, Car.); 142.29 (с, Саг.); 144.16 (с, Car.); 149.95 (с, Car.); 152.56 (с, Car.); 166.16 (с, Car.). HRMS-ESI: найдено [M-2Na+H]- 472.0490, C17H18N3O9S2, вычислено [M-2Na+H]- 472.0490.
Пример 9. Определение антигликирующей активности.
Реакцию гликирования воспроизводят по методу A. Jedsadayanmata ([11] А. Jedsadayanmata, Naresuan University Journal, 2005, 13(2): 35-41). Реакционная смесь содержит растворы бычьего сывороточного альбумина (1 мг/мл) и глюкозы (500 мМ) в фосфатном буфере (pH 7.4). Для предупреждения бактериального роста в буферный раствор вносят азид натрия в конечной концентрации 0.02%. Все вещества растворяют в диметилсульфоксиде (ДМСО). В экспериментальные образцы добавляют 30 мкл раствора изучаемых веществ в различных концентрациях, в контрольные образцы добавляют ДМСО в аналогичном объеме. Все экспериментальные образцы инкубируют в течение 24 часов при 60°C. По истечении срока инкубации проводят определение специфической флуоресценции гликированного бычьего сывороточного альбумина (БСА) на спектрофлуориметре F-7000 (Hitachi, Япония) при длине волны возбуждения 370 нм и испускания 440 нм. В качестве вещества сравнения используют известный ингибитор гликирования аминогуанидин (таблица 1) ([12] P.J. Thornalley, Archives of Biochemistry and Biophysics, 2003, 419: 31-40).
Статистическую обработку результатов проводят с использованием непараметрического критерия Манна-Уитни, табличного редактора Microsoft Excel 2007 и программы GraphPad Prism 5.0. Расчет показателя IC50 проводят методом регрессионного анализа (таблица 2).
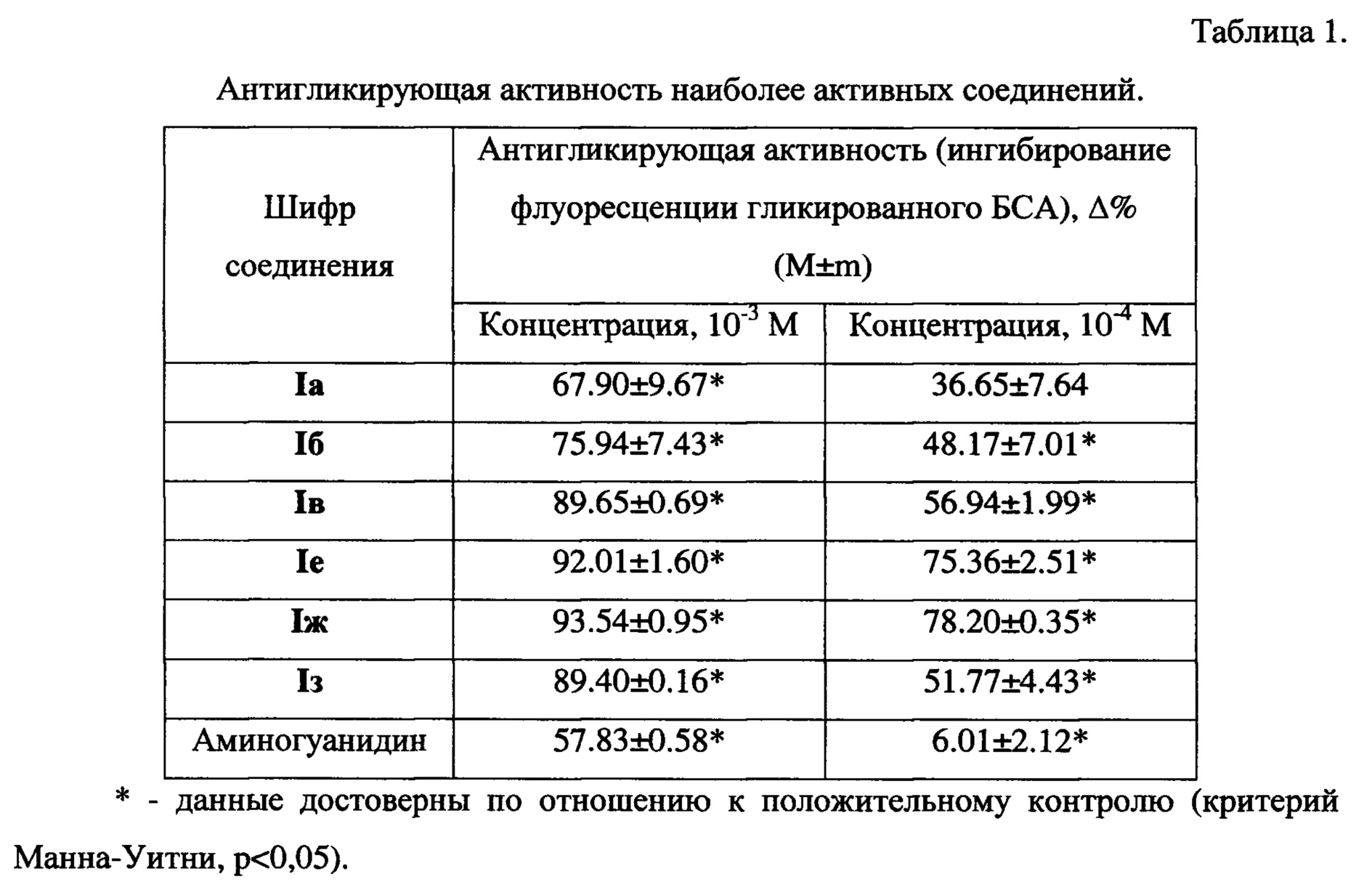
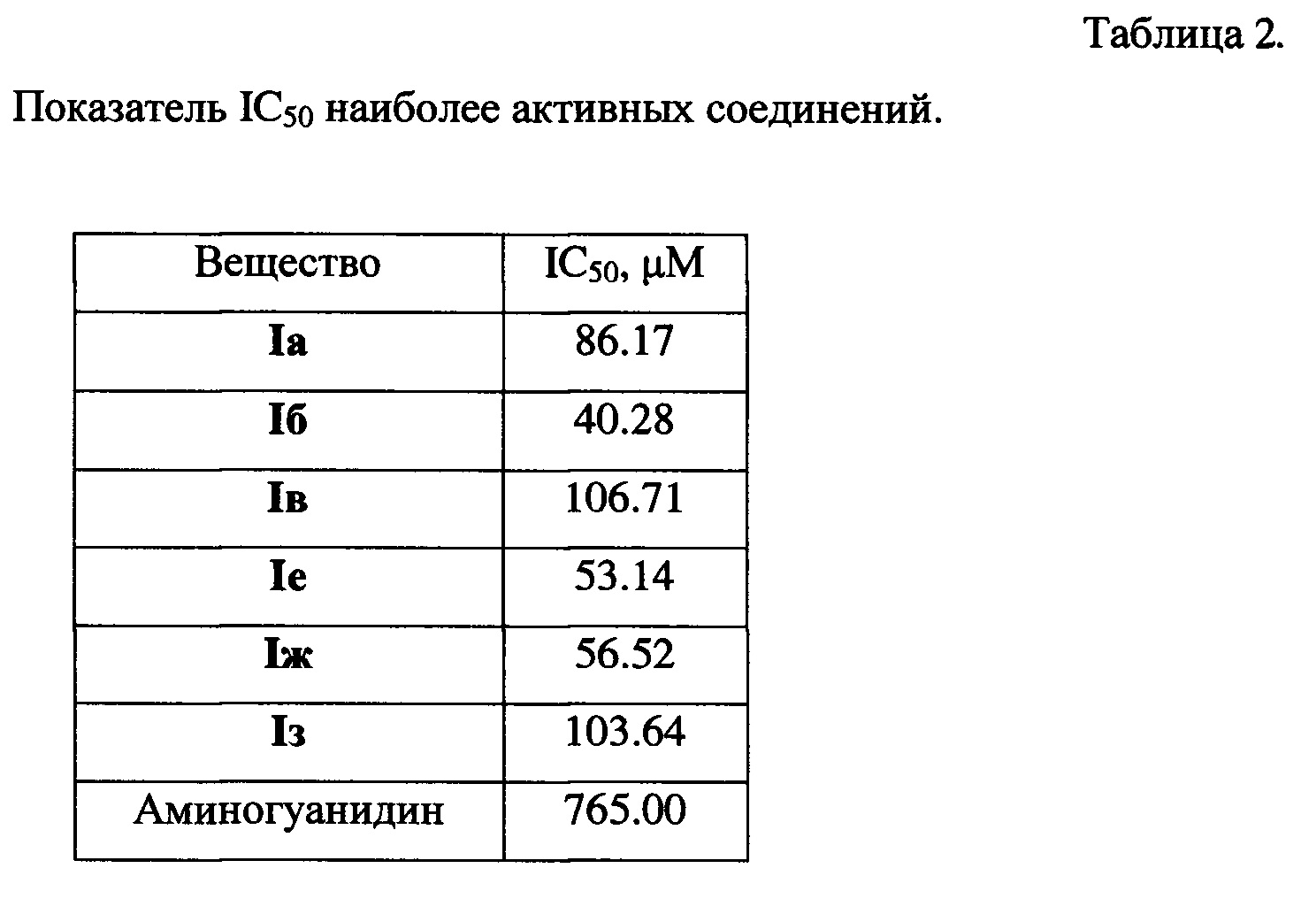
Анализ данных, приведенных в таблице 1 и таблице 2, позволяет сделать вывод, что заявленные вещества проявляют высокий уровень антигликирующей активности (таблица 1), что позволяет определить зависимость их эффекта от концентрации и рассчитать показатель IC50 (таблица 2).
Таким образом, полученные результаты свидетельствуют о том, что все заявленные вещества по активности превосходят прототип аминогуанидин в 7-19 раз.
Исходя из вышеизложенного, можно сделать вывод, что заявленное техническое решение позволяет создать новые высокоэффективные и безопасные лекарственные средства профилактики и лечения микро- и макрососудистых осложнений сахарного диабета, атеросклероза, нейродегенеративных заболеваний, тем самым улучшая качество жизни пациентов.
Заявленное техническое решение соответствует критерию «новизна», предъявляемому к изобретениям, так как из исследованного уровня техники не выявлены технические решения, обладающие заявленной совокупностью отличительных признаков, обеспечивающих достижение заявленных результатов.
Заявленное техническое решение соответствует критерию «изобретательский уровень», предъявляемому к изобретениям, так как не является очевидным для специалиста в данной области науки и техники.
Заявленное техническое решение соответствует критерию «промышленная применимость», т.к. может быть реализовано на любом специализированном предприятии с использованием стандартного оборудования, известных отечественных материалов и технологий.