Результат интеллектуальной деятельности: ТЕРАПЕВТИЧЕСКИЙ ИЛИ ПРОФИЛАКТИЧЕСКИЙ АГЕНТ ДЛЯ СИНДРОМА РАСПАДА ОПУХОЛИ
Вид РИД
Изобретение
Область техники, к которой относится изобретение
Настоящее изобретение имеет отношение к лечению и профилактике синдрома распада (лизиса) опухоли, содержащему в качестве действующего вещества 2-фенилтиазольное соединение, представленное формулой (I), или его фармацевтически приемлемую соль.
Уровень техники
Синдром распада опухоли (в дальнейшем в этом документе иногда упоминаемый как "TLS") является нарушением обмена веществ, обусловленным массивным и внезапным высвобождением клеточных компонентов в кровь при гибели опухолевых клеток путем применения химиотерапии, лучевой терапии и т.д. или когда происходит спонтанный лизис опухолей. При быстрой гибели опухолевых клеток, одновременно с их гибелью, в кровь попадают нуклеиновые кислоты, белки, калий, фосфор и т.п., что в результате вызывает гиперурикемию, гиперкалиемию, гиперфосфатемию, гипокальцемию, уремию и т.п.
Среди прочего, гиперурикемия является результатом метаболизма пуриновых оснований, включенных в нуклеиновые кислоты и т.п. в клетках, осуществляемого ксантиноксидазой с последующей выработкой мочевой кислоты посредством превращения гипоксантина и ксантина; высокие концентрации уратов, которые превышают пределы их растворимости в теле, приводят к отложению кристаллов в почках и мочевыводящих путях, что вызывает почечную дисфункцию или даже острую мочекислую нефропатию, т.е. острую почечную недостаточность, что приводит к смерти. Поскольку симптомы обычно наблюдаются от 12 до 72 часов после начала терапии, необходимо правильно оценить пациентов на степень риска, классифицировать пациентов на группы высокого риска, промежуточного риска и низкого риска и предпринять достаточные профилактические меры и тщательный контроль и, когда это происходит, необходимо произвести соответствующее лечение на ранних стадиях.
У пациентов с высокой вероятностью развития синдрома распада опухоли, увеличивают объем мочи путем предварительного приема жидкости, достаточной для предотвращения острой мочекислой нефропатии, и, поскольку кристаллы предрасположены к развитию при кислой реакции мочи, то предпринимаются попытки подщелачивания мочи. Кроме того, для снижения уровней мочевой кислоты осуществляется терапевтический способ, при котором ингибируется образование мочевой кислоты посредством аллопуринола, ингибитора ксантиноксидазы, или терапевтическим способом, при котором мочевая кислота разрушается посредством расбуриказы, фермента уратоксидазы. Следует отметить, что ингибитором ксантиноксидазы является агент, который был клинически применен в качестве терапевтического агента для подагры и гиперурикемии.
Тем не менее известно, что поскольку механизм действия ингибитора ксантиноксидазы аллопуринола осуществляется через ингибирование образования мочевой кислоты, аллопуринол не эффективен при уже высоких уровнях мочевой кислоты. В дополнение к этому, поскольку для появления эффекта снижения уровня мочевой кислоты аллопуринолом необходимо несколько дней, то начало химиотерапии для лизиса опухолей, возможно, должно быть отложено при применении агента в профилактических целях (непатентный документ 1). В дополнение к этому, ингибирование ксантиноксидазы аллопуринолом может приводить к повышенным концентрациям ксантина в моче и его отложении в мочевыводящих путях и вызывать развитие острой обструктивной уропатии (непатентный документ 1). Из-за этих ограничений для случаев при промежуточном риске синдром распада опухоли аллопуринол используется для профилактики не менее чем за 12 часов до начала химиотерапии, при увеличении объема мочи путем инфузии достаточного количества жидкости (непатентный документ 2). Что касается схемы приема (режима дозирования) подлежащего введению аллопуринола, то рекомендуется вводить (дозу) от 50 до 100 мг/м или 10 мг/кг/день, дробно, каждые 8 часов (непатентный документ 1).
С другой стороны, в лечении или предупреждении синдрома распада опухоли недавно была показана пригодность расбуриказы, которая является рекомбинантной уратоксидазой, обладающей способностью разрушать мочевую кислоту в крови, (непатентный документ 3). Тем не менее следует соблюдать осторожность, так как это может вызывать повышенную чувствительность, гемолитическую анемию и метгемоглобинемию. В дополнение к этому, из-за того, что частота приема препарата (расбуриказы) ограничена, так как в теле пациентов, которым она была введена, образуются антитела, и из-за высокой стоимости ее производства и высокой цены по сравнению с низкомолекулярными агентами, она не используется часто и рекомендуется для применения в основном у пациентов с высоким риском синдрома распада опухоли (непатентный документ 1). Для случаев с промежуточным риском, рекомендованное введение расбуриказы должно осуществляться в лечебных целях, когда гиперурикемия уже присутствует, или при повышении риска, например, когда гиперурикемия появляется во время химиотерапии (непатентный документ 2).
Как известно, 2-[3-циано-4-(2-метилпропокси)фенил]-4-метилтиазол-5-карбоновая кислота (международное непатентованное наименование: фебуксостат), которая используется в настоящем изобретении, влияет на снижение уровней мочевой кислоты путем ее ингибирующего действия на ксантиноксидазу, было исследовано соотношение между уровнем дозы и ее эффективности, и, как было обнаружено, является терапевтическим агентом для гиперурикемии и подагры (непатентные документы 4-6). Фебуксостат, как и аллопуринол, является ингибитором ксантиноксидазы.
Непатентные документы
[Непатентный документ 1] Journal of Clinical Oncology, vol.26, No. 16, 2008, 2767-2778.
[Непатентный документ 2] Clinical Practice Guidelines for Pediatric Leukemia/Lymphoma 2011 [Shoni Hakketsubyo Rinpashu no Shinryo Gaidorain 2011-nenban].
[Непатентный документ 3] Journal of Clinical Oncology, vol.19, No.3, 2001, 697-704.
Непатентный документ 4] Journal of Clinical Rheumatology, vol.17, No.4, 2011, S35-S43.
[Непатентный документ 5] Journal of Clinical Rheumatology, vol.17, No.4, 2011, S44-S49.
[Непатентный документ 6] Journal of Clinical Rheumatology, vol.17, No.4, 2011, S50-S56.
Раскрытие изобретения
Проблемы, решаемые с помощью изобретения
Целью настоящего изобретения является обеспечение нового терапевтического или профилактического агента для синдрома распада опухоли.
Средства решения задач
При введении соединения по настоящему изобретению пациенту с высоким риском, у которого уже выявлена гиперурикемия из-за распада опухоли, авторы настоящего изобретения обнаружили, что уровни мочевой кислоты в крови значительно снижались, и в то же самое время также значительно улучшалась функция почек.
В дополнение к этому, при профилактическом введении низкой дозы соединения по настоящему изобретению пациентам с гематопоэтическими опухолями с низким или промежуточным риском синдрома распада опухоли, и впоследствии с выполнением химиотерапии на опухолевых клетках, авторы настоящего изобретения обнаружили, что во всех случаях соединение поддерживало уровни мочевой кислоты в крови в пределах нормы, или уровни снижались до уровней нормального диапазона (7,5 мг/дл или менее) и также улучшилась функция почек. Кроме того, у тяжелобольного пациента с особенно повышенным уровнем лейкоцитов в крови (WBC) среди этих пациентов, был обнаружен эффект значительного снижения уровней мочевой кислоты в моче. Таким образом, настоящее изобретение состоит из
Терапевтического или профилактического агента для синдрома распада опухоли, содержащего в качестве действующего вещества 2-фенилтиазольное соединение, представленное следующей формулой (I):
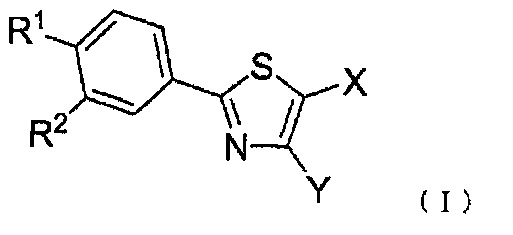
где:
R1 представляет C1-C8 алкоксигруппу, морфолиновую группу, 4-метил-пиперазин-1-ильную группу или пиперидиновую группу;
R2 представляет нитрогруппу или цианогруппу;
X представляет карбоксильную группу или С2-С7 алкоксикарбонильную группу; и
Y представляет атом водорода или C1-С6 алкильную группу;
или его фармацевтически приемлемую соль.
Синдром распада опухоли является синдромом распада опухоли у пациента с высоким риском, или
с промежуточным риском, или
у пациента с низким риском.
Синдром распада опухоли включает гиперурикемию, обусловленную химиотерапией или лучевой терапией для злокачественной опухоли.
Синдром распада опухоли наблюдается, не будучи обусловленным противоопухолевой терапией, и при нем происходят гиперурикемия и пониженная функция почек.
Терапевтический или профилактический агент по любому из пп. (1) - (6), где синдром распада опухоли наблюдается, когда гиперурикемия присутствует до проведения противоопухолевой терапии.
Синдром распада опухоли наблюдается, когда функция почек снижается до проведения противоопухолевой терапии.
Терапевтический или профилактический агент по изобретению, или его фармацевтически приемлемую соль вводят из расчета от 0,5 до 1000 мг/день, от 1 до 7 дней/неделю.
Терапевтический или профилактический агент по изобретению может понизить уровни мочевой кислоты в крови после проведения противоопухолевой терапии до нормальных уровней, или поддерживать их в пределах нормальных уровней.
Терапевтический или профилактический агент по изобретению может улучшить функцию почек после проведения противоопухолевой терапии по сравнению с функцией почек до начала противоопухолевой терапии, или поддерживать функцию почек в норме.
Терапевтический или профилактический агент по изобретению может понизить уровни экскреции (выведения) мочевой кислоты с мочой после проведения противоопухолевой терапии до нормальных уровней, или поддерживать их в пределах нормальных уровней.
Терапевтический или профилактический агент по изобретению, в котором 2-фенилтиазольное соединение, представленное формулой (I), является 2-[3-циано-4-(2-метилпропокси)фенил]-4-метилтиазол-5-карбоновой кислотой или ее фармацевтически приемлемой солью.
Эффекты изобретения
Согласно изобретению возможно лечение или предотвращение синдрома распада опухоли путем введения 2-фенилтиазольного соединения, представленного формулой (I), или его фармацевтически приемлемой соли.
В дополнение к этому, соединения по настоящему изобретению могут в достаточной степени понижать уровни мочевой кислоты в крови и, таким образом, могут вводиться пациентам с промежуточным риском и пациентам с высоким риском не только в качестве терапевтических агентов, но также в качестве профилактических агентов при синдроме распада опухоли.
Кроме того, настоящее изобретение предоставляет возможность не только в достаточной степени снижать уровни мочевой кислоты в крови и поддерживать их в пределах нормы, но также снижать уровни мочевой кислоты при выведении с мочой и поддерживать их в пределах нормы, и может улучшать функцию почек или предотвращать их ухудшение.
Краткое описание чертежей
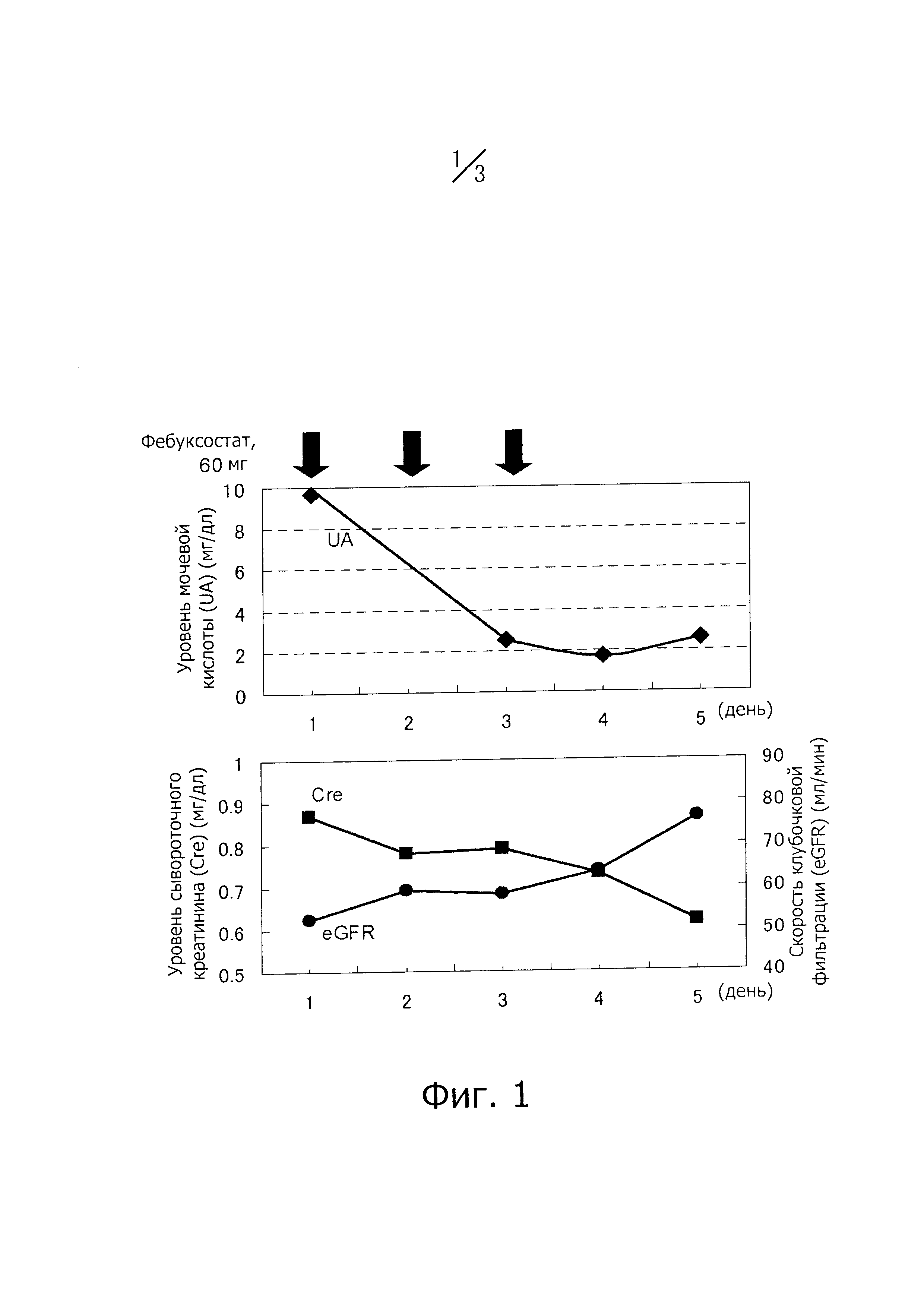
На фиг. 1 представлена динамика уровня мочевой кислоты (UA) в крови, уровня сывороточного креатинина (Cre) и рассчитанную скорость клубочковой фильтрации (eGFR) у пациента с высоким риском синдрома распада опухоли после введения фебуксостата пациенту в примере 1.
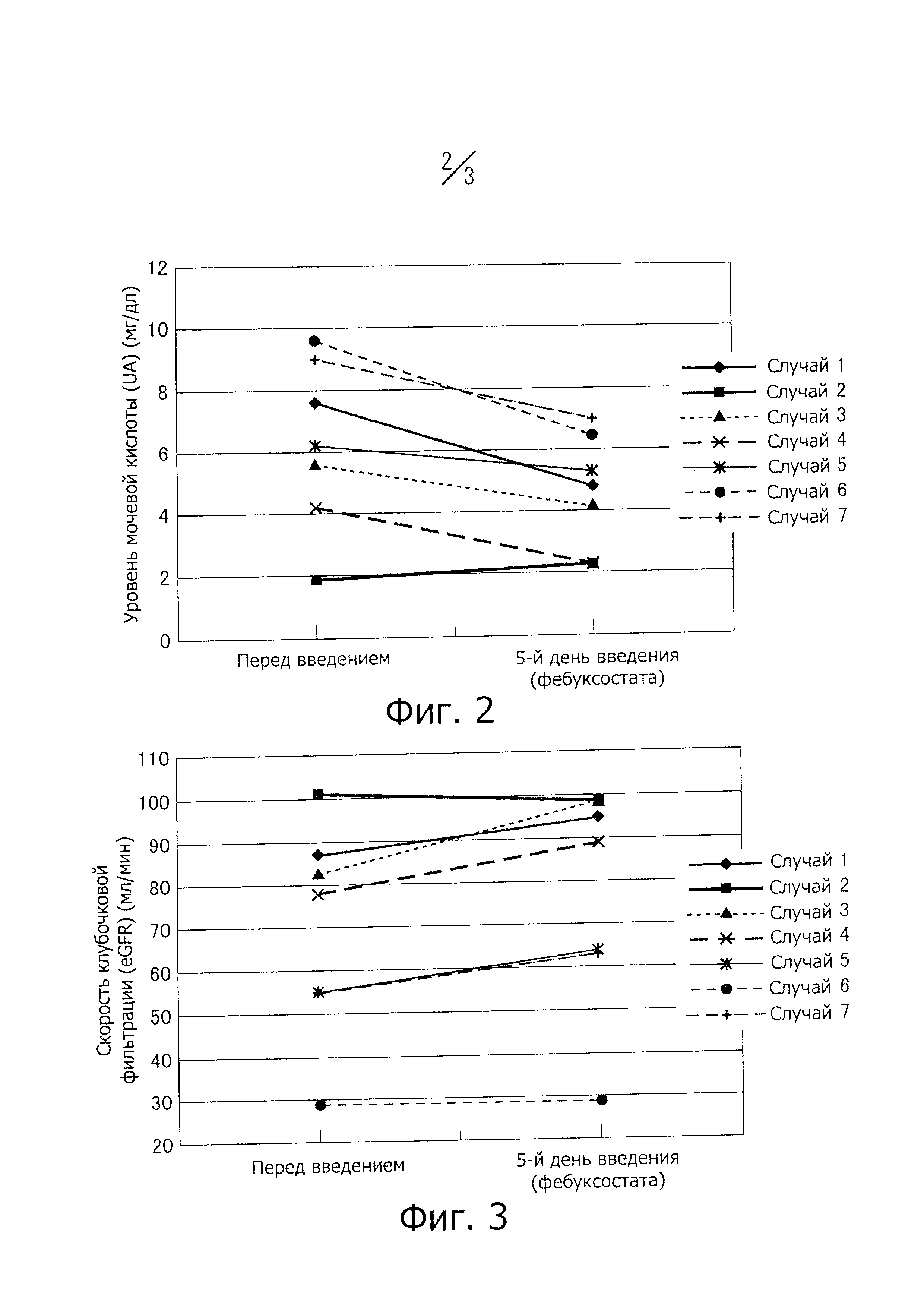
На фиг. 2 представлены изменения уровня мочевой кислоты (UA) в сыворотке до и после введения фебуксостата, которое проводили непосредственно перед химиотерапией, или за день до химиотерапии у пациентов с гематологическими злокачественными опухолями с низким или промежуточным риском синдрома распада опухоли в примере 2.
На фиг. 3 представлены изменения рассчитанной скорости клубочковой фильтрации (eGFR) до и после введения фебуксостата, которое проводили непосредственно перед химиотерапией, или за день до химиотерапии у пациентов с гематологическими злокачественными опухолями с низким или промежуточным риском синдрома распада опухоли в примере 2.
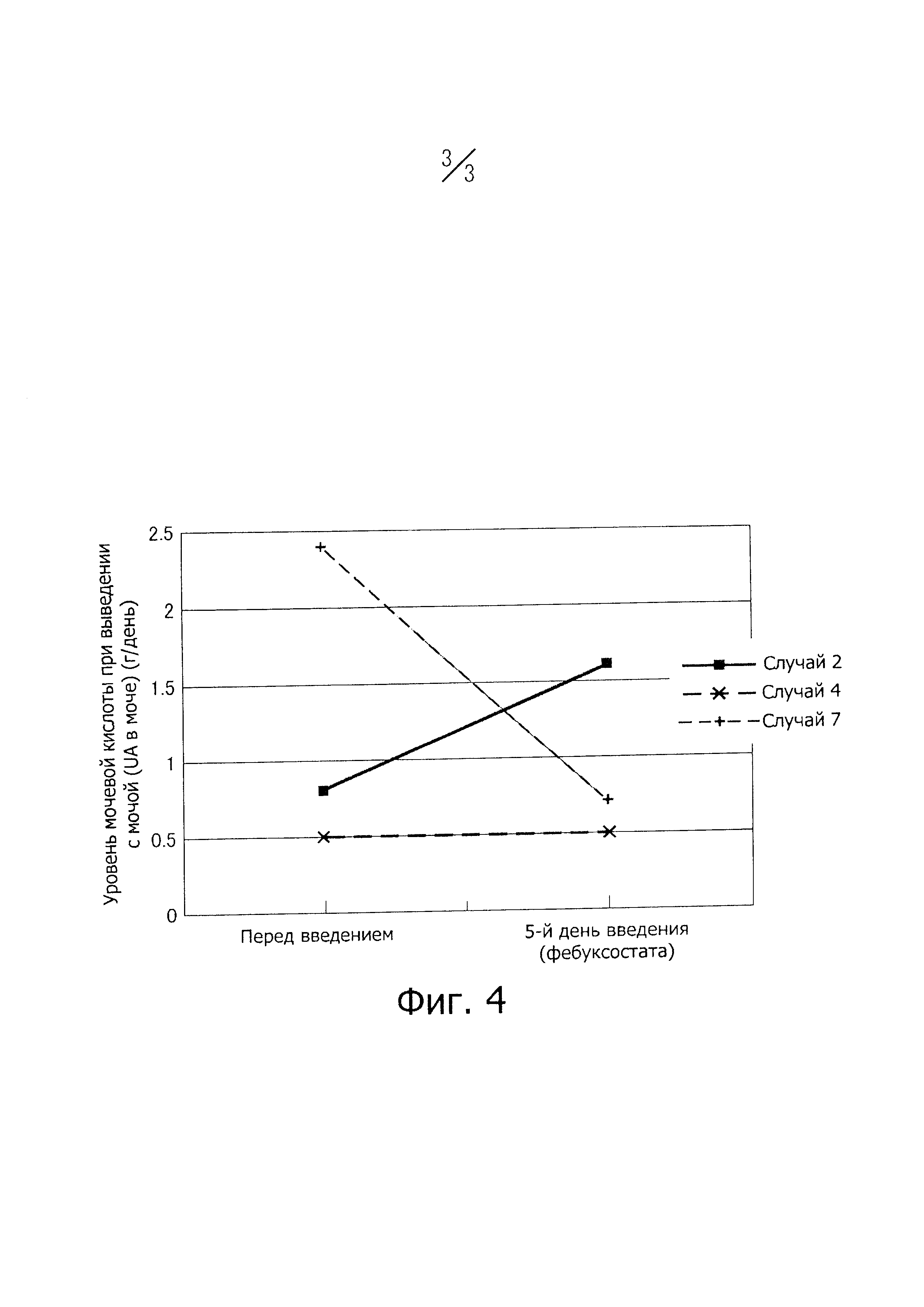
На фиг. 4 представлены изменения уровня экскреции мочевой кислоты (UA) в моче до и после введения фебуксостата, которое проводили непосредственно перед химиотерапевтическим агентом, или за день до химиотерапевтического агента у пациентов с гематологическими злокачественными опухолями с низким или промежуточным риском синдрома распада опухоли в примере 2.
Осуществление изобретения
2-фенилтиазольные соединения по настоящему изобретению представлены следующей формулой (I):
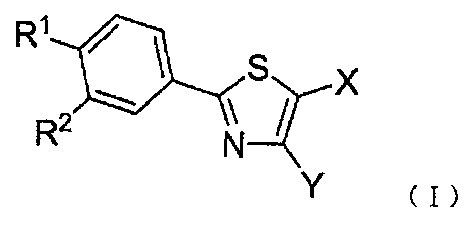
где:
R1 представляет C1-C8 алкоксигруппу, морфолиновую группу, 4-метил-пиперазин-1-ильную группу или пиперидиновую группу;
R2 представляет нитрогруппу или цианогруппу;
X представляет карбоксильную группу или С2-С7 алкоксикарбонильную группу; и
Y представляет атом водорода или C1-С6 алкильную группу;
или его фармацевтически приемлемые соли, включают, например, 2-[3-циано-4-(2-метилпропокси)фенил]-4-метилтиазол-5-карбоновую кислоту. Дополнительно, соединения, представленные формулой (I), могут быть получены известными способами, например, способом, описанным в международной публикации WO 92/09279.
"C1-C8-алкоксигруппа" в R1 указанной выше формулы (I) означает группу, состоящую из линейной или разветвленной С1-С8-алкильной группы, такой как, например, метальная, этильная, н-пропильная, н-бутильная, н-пентильная, н-гексильная, н-гептильная, н-октильная, изопропильная, изобутильная, втор-бутильная, трет-бутильная, изопентильная, неопентильная, трет-пентильная, изогексильная, 2-метилпентильная и 1-этилбутильная группы, и из оксигруппы, подходящие конкретные примеры которой включают метокси, этокси, н-пропилокси, н-бутилокси, изопропилокси, изобутилокси, втор-бутилокси, трет-бутилокси, изопентилокси, неопентилокси группы и т.п.. Более предпочтительные примеры включают изобутилоксигруппу. Предпочтительными группами для R1 являются C1-C8-алкоксигруппы и более предпочтительной группой является изобутилоксигруппа.
Предпочтительной группой для R2 является цианогруппа.
"С2-С7-алкоксикарбонильная группа" в X указанной выше формулы (I) означает группу, состоящую из С1-С6-алкоксигруппы, среди указанных выше C1-C8-алкоксигрупп в R1, и состоящую из карбонильной группы, подходящие конкретные примеры которой включают метоксикарбонильную группу, этоксикарбонильную группу и т.п.. Предпочтительной группой для X является карбоксильная группа.
"С1-С6-алкильная группа" в Y указанной выше формулы (I) означает линейную или разветвленную C1-С6-алкильную группу, такую как, например, метальная, этильная, н-пропильная, н-бутильная, н-пентильная, н-гексильная, изопропильная, изобутильная, втор-бутильная, трет-бутильная, изопентильная, неопентильная, трет-пентильная, изогексильная, 2-метилпентильная и 1-этилбутильная группы, подходящие конкретные примеры которой включают метальные, этильные, пропильные, изопропильные группы и т.п.. Более предпочтительные примеры включают метальную группу. Предпочтительными группами для Y являются C1-С6-алкильные группы и более предпочтительной группой является метильная группа.
Среди соединений, представленных формулой (I), предпочтительной является 2-[3-циано-4-(2-метилпропокси)фенил]-4-метилтиазол-5-карбоновая кислота.
Кроме того, возможно, что топироксостат (topiroxostat) (4-[5-(пиридин-4-ил)-1Н-1,2,4-триазол-3-ил]пиридин-2-карбонитрил) и ингибиторы ксантиноксидазы, описанные в международной публикации WO 2005/121153, международной публикации WO 2010/113942 или международной публикации WO 2007/043457, также могут применяться в качестве соединений в настоящем изобретении.
Синдром распада опухоли в настоящем изобретении является метаболическим нарушением, обусловленным массивным и внезапным высвобождением клеточных компонентов в циркулирующую кровь при гибели опухолевых клеток при терапии, такой как химиотерапия или лучевая терапия, или когда происходит спонтанный лизис опухолей с высоким пролиферативным потенциалом, и определяется как смертельная болезнь, что приводит к гиперурикемии, гиперкалиемии, гиперфосфатемии, гипокальциемии и даже острой почечной недостаточности и аритмии. В соответствии с руководящими принципами Американского общества клинической онкологии (ASCO) от 2008 года, синдром распада опухоли определяется в соответствии с диагнозом и степенью тяжести путем деления его на лабораторный TLS и клинический TLS. Первый определяется в случае, когда существуют 25% или более отклонений относительно исходного уровня в любых двух или нескольких уровнях фосфорной кислоты, кальция, калия и мочевой кислоты в сыворотке (таблица 1), и второй (клинический TLS) определяется путем деления его на степени от 0 до 5 на основании уровней сывороточного креатинина, степени тяжести аритмии и пароксизма (таблица 2).


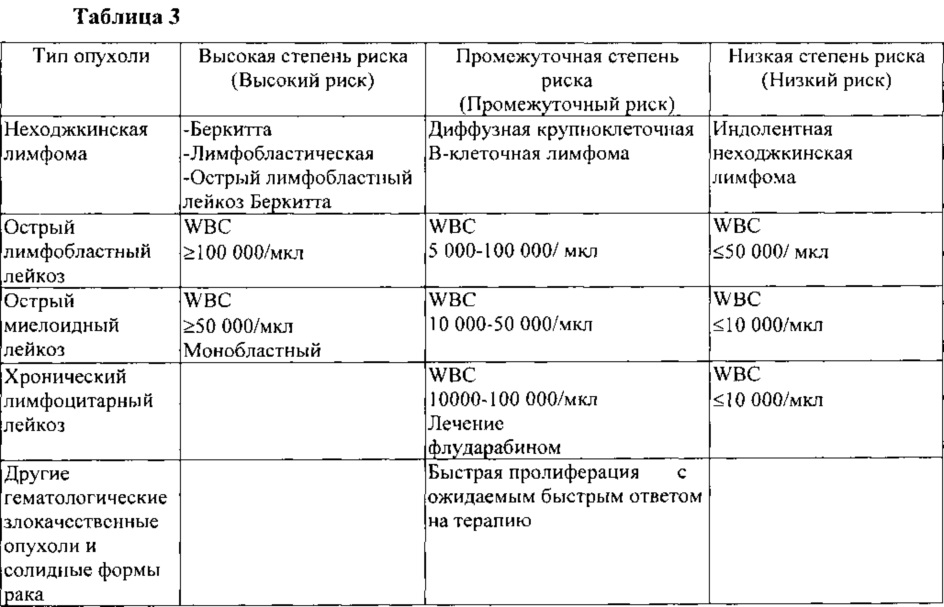
Профилактика синдрома распада опухоли считается важной, поскольку после того как он развился, его трудно лечить, так как симптомы прогрессируют быстро. По этой причине определяются пациенты с риском развития синдрома распада опухоли, и до начала противоопухолевого лечения проводится профилактика. Такие пациенты с риском развития синдрома распада опухоли определены как пациенты с высоким риском, промежуточным риском или низким риском, в зависимости от типа опухоли (таблица 3). В дополнение к этому, в случае, когда синдром распада опухоли уже развился до противоопухолевой терапии, например, когда проводится химиотерапия и присутствует гиперурикемия и снижается функция почек, считается, что пациент имеет риск, соответствующий риску пациента с высоким риском синдрома распада опухоли, поскольку это приведет в дальнейшем к риску развития острой почечной недостаточности из-за терапии, такой как химиотерапия.
В руководящих принципах Американского общества клинической онкологии (ASCO) от 2008 года и т.п., управление гидратацией плюс расбуриказа рекомендуется для пациентов с высоким риском, управление гидратацией плюс аллопуринол рекомендуется для пациентов с промежуточным риском, или лечение расбуриказой рекомендуется для педиатрических пациентов. В дополнение к этому, даже у пациентов с промежуточным риском, лечение расбуриказой рекомендуется, когда гиперурикемия уже развилась.
Эффективное управление синдромом распада опухоли обычно определяется как исходное введение агента, понижающего уровень мочевой кислоты перед терапией, такой как химиотерапия или лучевая терапия, и продолжение введения уже после лечения опухоли химиотерапией, лучевой терапией и т.д., в результате чего через 48 часов после начала введения агента, понижающего уровень мочевой кислоты, уровни мочевой кислоты в крови достигают 7,5 мг/дл или менее, если пациент 13-летнего возраста или старше, или 6,5 мг/дл или менее, если пациент моложе 13-летнего возраста, который сохраняется до 24 часов после окончания введения агента, понижающего уровень мочевой кислоты. Дополнительно, клиническая значимость управления синдромом распада опухоли определяется как ингибирование развития синдрома распада опухоли, а также ингибирование развития почечной дисфункции, такой как острая почечная недостаточность, связанная с синдромом распада опухоли, или уклонением от диализа.
То есть в настоящем изобретении "нормальным уровнем" является целевой уровень для эффективного управления синдромом распада опухоли и означает состояние, при котором уровни мочевой кислоты в сыворотке составляют 7,5 мг/дл или менее, и в отношении функции почек, рассчитанные скорости клубочковой фильтрации составляют около 60 мл/мин или более, или уровни креатинина сыворотки крови составляют около 1,1 мг/дл или менее.
Соединения по настоящему изобретению являются ингибиторами ксантиноксидазы, но в то же время являются эффективными не только у пациентов с промежуточным риском, но также у пациентов с высоким риском, поскольку их эффекты снижения уровней мочевой кислоты в крови дают более сильные восстановления, чем таковые от ингибиторов ксантиноксидазы, применяемых при традиционных лечениях синдрома распада опухоли. Дополнительно, они (соединения по настоящему изобретению) являются эффективными не только у пациентов, у которых еще не развился синдром распада опухоли, но также у пациентов, у которых развился синдром распада опухоли. Опухоли в синдроме распада опухоли по настоящему изобретению включают гематопоэтические опухоли, солидные опухоли и т.п.
Дополнительно, профилактические или терапевтические агенты настоящего изобретения, даже при низкой дозе, поддерживают уровни мочевой кислоты в пределах нормы или снижают их до нормальных уровней, предотвращают функцию почек от ухудшения, или улучшают функцию почек и оказывают влияние на предупреждение или лечение синдрома распада опухоли. Профилактические или терапевтические агенты настоящего изобретения также могут поддерживать уровни мочевой кислоты при выведении с мочой в пределах нормы или снижать их до пределов нормального диапазона.
При необходимости, соединения, представленные приведенной выше формулой (I), могут быть превращены в их фармацевтически приемлемые соли. Такие соли включают, например, соли с неорганическими кислотами, такими как соляная кислота, бромистоводородная кислота, йодистоводородная кислота, серная кислота, азотная кислота, фосфорная кислота и угольная кислота; соли с органическими кислотами, такими как муравьиная кислота, уксусная кислота, пропионовая кислота, трифторуксусная кислота, фталевая кислота, щавелевая кислота, малоновая кислота, янтарная кислота, фумаровая кислота, малеиновая кислота, молочная кислота, яблочная кислота, винная кислота, лимонная кислота, бензойная кислота, метансульфоновая кислота, этансульфоновая кислота, бензолсульфоновая кислота и п-толуолсульфоновая кислота, соли с аминокислотами, такими как лизин, аргинин, орнитин, глутаминовая кислота и аспарагиновая кислота; соли со щелочными металлами, таким как натрий, калий и литий; соли со щелочноземельными металлами, такими как кальций и магний; соли с металлами, такими как алюминий, цинк и железо; соли с органическими основаниями, такими как метиламин, этиламин, t-октиламин, диэтиламин, триметиламин, триэтиламин, этилендиамин, пиперидин, пиперазин, пиридин, пиколин, этаноламин, диэтаноламин, триэтаноламин, циклогексиламин, дициклогексиламин, N-метилглюкамин, трис(гидроксиметил)аминометан и Ν,Ν'-дибензилэтилендиамин; соли аммония и т.п.
Активный ингредиент настоящего изобретения может использоваться в любой лекарственной форме твердого препарата, полутвердого препарата, жидкого препарата и т.д., и в любом препарате композиций для перорального и парентерального применений (инъекциях, трансдермальных композициях, глазных каплях, суппозиториях, интраназальных композициях, средствах для ингаляции и т.п.).
Терапевтический или профилактический агент для синдрома распада опухоли настоящего изобретения, содержащий в качестве активного ингредиента 2-фенилтиазольное соединение или его фармацевтически приемлемую соль получают вместе с носителями, вспомогательными веществами и другими добавками, обычно используемыми для приготовления фармацевтических препаратов. Носители и вспомогательные вещества для приготовления фармацевтических препаратов могут быть как в твердой, так и в жидкой форме и включают, например, лактозу, стеарат магния, крахмал, тальк, желатин, агар, пектин, смолу акации, оливковое масло, кунжутное масло, масло какао, этиленгликоль и т.д. и другие, которые обычно используются. Введение может быть в любой форме для перорального введения, такого как посредством таблеток, пилюль, капсул, гранул, порошков или жидких препаратов, или для парентерального введения, такого как посредством инъекций, таких как внутривенные инъекции и внутримышечные инъекции, суппозиториев или посредством трансдермального введения.
Дозировкой активного ингредиента настоящего изобретения является количество, которое является эффективным для лечения или предупреждения синдрома распада опухоли и может быть определена в зависимости от симптома, возраста, веса пациента, типа одновременного лечения, частоты лечения, природы желаемого эффекта, способа введения или т.п.. Обычно, дозировка составляет от около 0,5 до 1000 мг в день, предпочтительно от 10 до 120 мг для взрослых и от 3 до 120 мг для детей; например, вводится 3, 5, 10, 20, 30, 40, 50, 60, 80 или 120 мг в день. Доза для введения составляет от около 0,1 до 1000 мг, предпочтительно от 1 до 120 мг. Для детей вводится количество, которое является соответствующим образом уменьшенным по сравнению с количеством для взрослых. Введение начинается до развития заболевания или после развития заболевания и может выполняться ежедневно или периодически, обычно от 1 до 3 раз/день, от 1 до 7 дней/неделю. Предпочтительно, чтобы терапевтический или профилактический агент по настоящему изобретению был получен в составе композиций, так чтобы эти условия могли быть выполнены.
Примеры
Пример 1. Исследование эффектов на уровни мочевой кислоты в сыворотке и функции почек у пациента с синдромом распада опухоли (фиг. 1)
Для исследования терапевтических эффектов фебуксостата у пациента с высоким риском синдрома распада, пациенту с высоким риском синдрома распада, у которого не происходила противоопухолевая терапия и с уже проявляющейся гиперурикемией, были произведены переливания свежей замороженной плазмы и эритроцитарной массы, и затем, в дополнение к увеличению объема мочи путем подачи жидкости и для подщелачивания мочи, перорально вводили фебуксостат (60 мг) в течение 3 дней, и уровни мочевой кислоты в сыворотке и функции почек сравнивали с уровнями мочевой кислоты в сыворотке и функциями почек до введения фебуксостата.
Пациент, участник исследования
53-летняя женщина, миелодиспластический синдром (MDS), уровень лейкоцитов в крови (WBC) 15400/мкл
Результаты
Уровень мочевой кислоты в сыворотке (UA): UA составлял 9,7 мг/дл за день до дня от начала введения фебуксостата, тогда как на 4-й день, через 3 дня введения фебуксостата (60 мг/день), уровень мочевой кислоты в сыворотке снижался до 1,7 мг/дл, свидетельствуя о снижении вплоть до 82,4%.
Сывороточный креатинин (Cre) и рассчитанная скорость клубочковой фильтрации (eGFR): Сывороточный Cre составлял 0,87 мг/дл (рассчитанная скорость клубочковой фильтрации: eGFR 53 мл/мин) до введения фебуксостата, тогда как на 4-й день, через 3 дня введения фебуксостата (60 мг/день), уровень креатинана снижался до 0,73 мг/дл и eGFR повышался до 64 мл/мин.
Как показано в этих результатах, путем введения фебуксостата уровень мочевой кислоты в сыворотке быстро снижался и в то же самое время функция почек также была улучшена, что доказывало эффективность этого лекарственного средства для лечения синдрома распада опухоли.
Пример 2. Исследование профилактических эффектов на уровни мочевой кислоты в сыворотке, функцию почек и уровни мочевой кислоты при выведении с мочой у пациентов с гематологическими злокачественными опухолями при проведении химиотерапии (таблица 4, фиг. 2-4)
Для исследования профилактических эффектов фебуксостата на синдром распада опухоли, 10 мг фебуксостата (начальная доза при подагре и гиперурикемии) вводили перорально один раз в день, ежедневно, непосредственно перед химиотерапией или за день до химиотерапии, проводили на пациентах с гематологическими злокачественными опухолями при низком или промежуточном риске синдрома распада опухоли, и уровень мочевой кислоты в сыворотке и функцию почек на пятый день введения сравнивали с уровнем мочевой кислоты в сыворотке и функцией почек до начала введения фебуксостата. Для случаев, в которых был возможен сбор мочи, уровень экскреции мочевой кислоты на пятый день введения сравнивали с уровнем экскреции мочевой кислоты до начала введения фебуксостата.
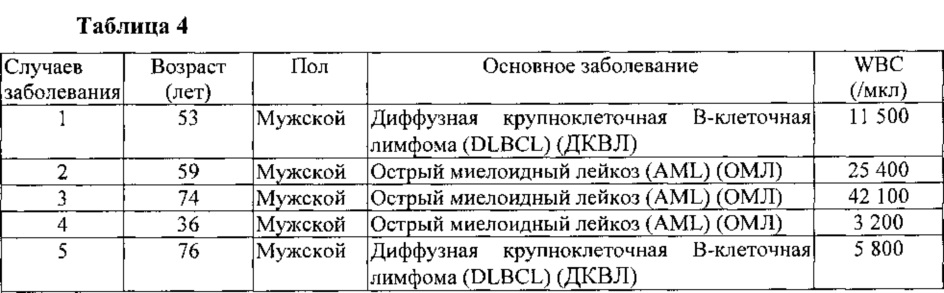
Пациент, участник исследования (таблица 4)
Таблица 4 демонстрирует возраст, пол, основное заболевание и уровень лейкоцитов в крови пациентов с гематологическими злокачественными опухолями.
Семь случаев мужчин и женщин (6 мужчин и 1 женщина), возраст от 36 до 79 лет (средний возраст 70 лет), острый миелоидный лейкоз (AML, 3 случая), диффузная крупноклеточная В-клеточная лимфома (DLBCL, 2 случая), хронический миеломоноцитарный лейкоз (CMML, 1 случай), хронический миелоидный лейкоз (CML, 1 случай), уровень лейкоцитов в крови (WBC) от 3 200 до 347 000/мкл

Результаты
Уровень мочевой кислоты в сыворотке (UA) (фиг. 2): UA составлял в среднем 6,3 мг/дл до начала введения, тогда как было показано, что уровень мочевой кислоты в сыворотке снижается в среднем до 4,6 мг/дл на пятый день введения фебуксостата. Следует отметить, что хотя в двух случаях наблюдали повышение UA, это было повышение от 1,9 мг/дл до 2,3 мг/дл; уровень UA до ведения было трудно понизить, так как он был низким, но UA поддерживали в пределах нормальных уровней.
Рассчитанная скорость клубочковой фильтрации (eGFR) (фиг. 3): eGFR составляла в среднем 69,7 мл/мин до начала введения, тогда как она повышалась в среднем до 76,9 мл/мин на пятый день введения фебуксостата. Следует отметить, что хотя в случае 2 наблюдали снижение eGFR, это было снижение от 101 мл/мин до 99 мл/мин, и eGFR поддерживали в пределах нормальных уровней. В других случаях eGFR могла быть поддержана или улучшена, и во всех случаях была предупреждена острая почечная недостаточность.
Уровень мочевой кислоты при выведении с мочой (UA в моче) (фиг. 4): Для случаев, когда сбор мочи был возможен, UA в моче составляла в среднем 1,2 г/день перед началом введения, тогда как уровень UA в моче снижался в среднем до 0,9 г/день на пятый день введения фебуксостата. В одном случае UA в моче могла быть поддержана в пределах нормальных уровней, и в тяжелом случае, при котором WBC был высоким, UA в моче была резко снижена от 2,4 до 0,7 г/день, несмотря на то что была выполнена химиотерапия. Следует отметить, что хотя в случае 2 наблюдали повышение UA, это было только небольшое повышение, от 0,8 г/день до 1,6 г/день.
Как показано в этих результатах, профилактическое введение низкой дозы 10 мг фебуксостата было, во всех случаях, способно поддерживать уровни мочевой кислоты в сыворотке в пределах нормальных уровней или снижать их до нормальных уровней, несмотря на то что была выполнена химиотерапия, и в то же время также улучшать функцию почек. Кроме того, в конкретно тяжелом случае, возможно было значительно снизить уровень мочевой кислоты при выведении с мочой. Таким образом, это лекарственное средство оказалось эффективным для профилактики синдрома распада опухоли.
Пример 3. Исследование профилактических эффектов на уровни мочевой кислоты в сыворотке при проведении химиотерапии у пациентов со злокачественной опухолью с синдромом распада опухоли
Для исследования профилактических эффектов фебуксостата на синдром распада опухоли фебуксостат вводят перорально один раз в день, ежедневно, непосредственно перед химиотерапией проводили на взрослых пациентах со злокачественной опухолью с синдромом распада опухоли и оценку проводят с использованием уровней мочевой кислоты в сыворотке в качестве показателей. В дополнение к этому, близкое исследование с фебуксостатом также проводили у педиатрических пациентов со злокачественной опухолью с синдромом распада опухоли.
Результаты этих экспериментов доказывают, что фебуксостат является эффективным для предупреждения синдрома распада опухоли.
Промышленная применимость
Настоящее изобретение может применяться для лечения или предупреждения синдрома распада опухоли.