Результат интеллектуальной деятельности: Применение rac-N-{ 4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил} -N-метил-имидазолинийиодида в качестве мультикиназного ингибитора
Вид РИД
Изобретение
Область техники, к которой относится изобретение
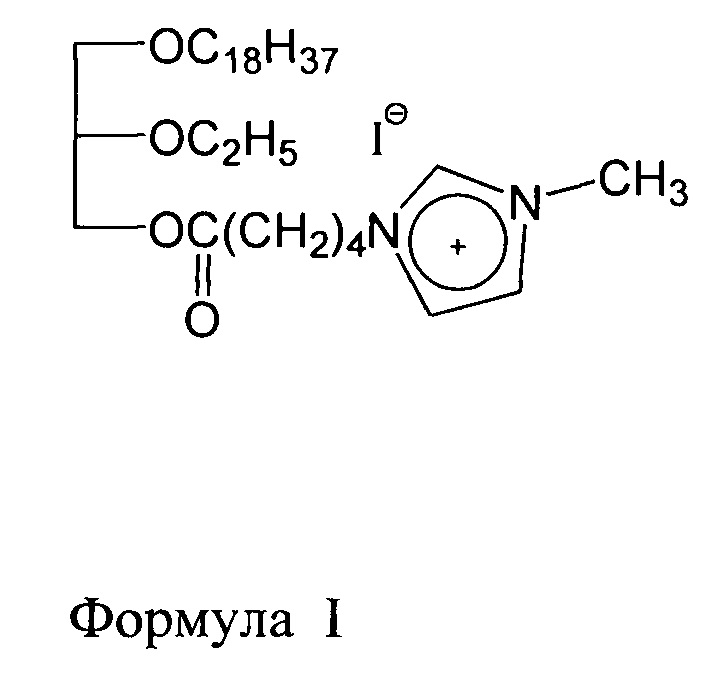
Изобретение относится к применению биологически активного вещества rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодида формулы I - соединения класса алкильных катионных глицеролипидов с гетероциклическим полярным доменом в качестве мультикиназного ингибитора на основе выявленной активности - ингибирования протеинкиназ Ins-R, Src, Met и Pim-1. Соединение применимо для ингибирования названных протеинкиназ в неопластических клетках, в механизме возникновения которых они участвуют.
Уровень техники
Поскольку протеинкиназы участвуют в целом ряде различных процессов, происходящих в клетке, они играют важную роль и в развитии патологических состояний, опосредованных наличием неопластических клеток, что делает их потенциальными мишенями лекарственных препаратов. Ингибирование протеинкиназ-мишеней - одна из задач при создании таргетных препаратов. Представляют интерес ингибиторы протеинкиназ, имеющие сразу несколько мишеней, и преимуществом таких ингибиторов является то, что эффект их действия может быть кумулятивен.
Одной из протеинкиназ-мишеней лекарственных препаратов является Src. Эти белки играют важную роль в клеточной адгезии, инвазии, пролиферации и выживании клеток. Снижение активности Src позволяет снизить активность макрофагов, что приводит к противовоспалительному действию ингибиторов этой протеинкиназы [Se Eun Byeon, Young-Su Yi, Jueun Oh, 1 Byong Chul Yoo, Sungyoul Hong, Jae Youl Cho. The Role of Src Kinase in Macrophage-Mediated Inflammatory Responses. Hindawi Publishing Corporation Mediators of Inflammation. Vol 2012. Article ID 512926]. Избыточная активация протеинкиназы Src часто встречается в опухолевых тканях, и Src является центральным посредником нескольких сигнальных путей канцерогенеза, а следовательно, и одной из мишеней противоопухолевых препаратов [Kim L.C., Song L., Haura E.B. Src kinases as therapeutic targets for cancer. Nature Reviews Clinical Oncology. 2009. 6(10). 587-595]. Протеинкиназа Src также может быть мишенью при нарушениях миелоидной пролиферации [ Korade-Mirnics, Seth J. Corey. Src kinase-mediated signaling in leukocytes. Journal of Leukocyte Biology. 2000. Vol. 68 no. 5. 603-613; Robinson L.J., Xue J., Corey S.J. Src family tyrosine kinases are activated by Flt3 and are involved in the proliferative effects of leukemia-associated Flt3 mutations. Exp Hematol. 2005. 33(4). 469-479; Chaturvedi P., Reddy M.V., Reddy E.P. Src kinases and not JAKs activate STATs during IL-3 induced myeloid cell proliferation. Oncogene. 1998. 16(13). 1749-1758]. Протеинкиназа Src опосредует развитие кожных заболеваний как опухолевых, так и предопухолевых [Choi C.W., Kim Y.H., Sohn J.H., Lee H., Kim W.S. Focal adhesion kinase and Src expression in premalignant and malignant skin lesions. Exp Dermatol. 2015. 24(5). 361-634].
Korade-Mirnics, Seth J. Corey. Src kinase-mediated signaling in leukocytes. Journal of Leukocyte Biology. 2000. Vol. 68 no. 5. 603-613; Robinson L.J., Xue J., Corey S.J. Src family tyrosine kinases are activated by Flt3 and are involved in the proliferative effects of leukemia-associated Flt3 mutations. Exp Hematol. 2005. 33(4). 469-479; Chaturvedi P., Reddy M.V., Reddy E.P. Src kinases and not JAKs activate STATs during IL-3 induced myeloid cell proliferation. Oncogene. 1998. 16(13). 1749-1758]. Протеинкиназа Src опосредует развитие кожных заболеваний как опухолевых, так и предопухолевых [Choi C.W., Kim Y.H., Sohn J.H., Lee H., Kim W.S. Focal adhesion kinase and Src expression in premalignant and malignant skin lesions. Exp Dermatol. 2015. 24(5). 361-634].
Инсулиновый рецептор (Ins-R), принадлежащий к классу тирозинкиназ, играет ключевую роль в регуляции метаболизма глюкозы. Снижение активности инсулиновых рецепторов приводит к затруднению клеточного деления и облегчает инициацию клеточной гибели при действии антинеопластических агентов [Malaguarnera R., Sacco A., Voci C, Pandini G, Vigneri R, Belifore A. Proinsulin Binds with High Affinity the Insulin Receptor Isoform A and Predominantly Activates the Mitogenic Pathway. Endocrinology. 2012. 153. 2152-2163]. Ингибирование инсулинового рецептора способствует гибели клеток как в случаях солидных опухолей, так и при нарушениях миелоидной пролиферации [Belfiore A., Malaguarnera R. Insulin receptor and cancer. Endocr Relat Cancer. 2011 18(4). 125-147; Wahner Hendrickson A.E., Haluska P., Schneider P.A., Loegering D.A., Peterson K.L., Attar R., Smith B.D., Erlichman C., Gottardis M., Karp J.E., Carboni J.M., Kaufmann S.H. Expression of insulin receptor isoform A and insulin-like growth factor-1 receptor in human acute myelogenous leukemia: effect of the dual-receptor inhibitor BMS-536924 in vitro. Cancer Res. 2009. 69(19). 7635-7643]. Помимо онкологических заболеваний, инсулиновый рецептор важен при развитии ряда кожных заболеваний, поскольку он играет тормозящую роль в регуляции развития и дифференцировки клеток кожи [Sadagurski М., Yakar S., Weingarten G., Holzenberger M., Rhodes C.J., Breitkreutz D., Leroith D., Wertheimer E. Insulin-like growth factor 1 receptor signaling regulates skin development and inhibits skin keratinocyte differentiation. Mol Cell Biol. 2006. 26(7). 2675-2687]. Также избыточная активация инсулинового рецептора является признаком аутоиммунных заболеваний [Terry J. Smith. Insulin-Like Growth Factor-I Regulation of Immune Function: A Potential Therapeutic Target in Autoimmune Diseases? Pharmacol Rev. 2010. 62(2). 199-236].
Протеинкиназа Met играет важную роль в инвазии, ангиогенезе и метастазировании опухоли, поэтому ее ингибирование является актуальной задачей при терапии опухолей различного тканевого происхождения [Takeuchi S, Wang W, Li Q, Yamada T, Kita K, Donev IS, Nakamura T, Matsumoto K, Shimizu E, Nishioka Y, Sone S, Nakagawa T, Uenaka T, Yano S. Dual Inhibition of Met Kinase and Angiogenesis to Overcome HGF-Induced EGFR-TKI Resistance in EGFR Mutant Lung Cancer. The American Journal of Pathology. 2012. 181(3). 1034-1043; Cao H.H., Cheng С.Y., Su Т., Fu X. Q., Guo H., Li Т., Tse A.K., Kwan H.Y., Yu H., Yu Z.L. Quercetin inhibits HGF/c-Met signaling and HGF-stimulated melanoma cell migration and invasion. Mol Cancer. 2015. 14. 103]. Протеинкиназа Met опосредует как развитие солидных опухолей, так и играет роль при остром миелоидном лейкозе [Kentsis A., Reed C., Rice K.L., Sanda Т., Rodig S.J., Tholouli Е., Christie A., Valk P.J., Delwel R., Ngo V., Kutok J.L., Dahlberg S.E., Moreau L.A., Byers R.J., Christensen J.G., Vande Woude G., Licht J.D., Kung A.L., Staudt L.M., Look A.T. Autocrine activation of the MET receptor tyrosine kinase in acute myeloid leukemia. Nat Med. 2012. 18(7). 1118-1122]. Помимо того, что протеинкиназа Met известна как мишень противоопухолевой терапии, она регулирует развитие неопухолевых эритроидных, миелоидных, лимфоидных клеток и тромбоцитов [Ilangumaran S., Villalobos-Hernandez A., Bobbala D., Ramanathan S. The hepatocyte growth factor (HGF)-MET receptor tyrosine kinase signaling pathway: Diverse roles in modulating immune cell functions. Cytokine. 2016. S1043-4666(15)30126-5]. Ингибирование Met - потенциальная задача восстановления иммунного гомеостаза, терапии аутоиммунных заболеваний и, в частности, кожных заболеваний [Baek J.H., Birchmeier C., Zenke M., Hieronymus T. The HGF receptor/Met tyrosine kinase is a key regulator of dendritic cell migration in skin immunity. J Immunol. 2012. 189(4). 1699-1707].
Протеинкиназа Pim-1 (от proviral integration Moloney virus) защищает клетки от апоптоза и способствует злокачественной трансформации клеток [Moroy T., Grzeschiczek A., Petzold S., Hartmann K.U. Expression of Pim-1 transgene accelerates limphoproliferation and inhibits apoptosis in lpr/lpr mice. Proc. Nat. cad. Sci. 1993. 90(22). 10734-10738]. Гиперэкспрессия гена или повышенная активность белка Pim-1 наблюдается как при онкологических заболеваниях системы крови, так и в солидных опухолях, например при раке простаты [Sivertsen E.A., Galtrland Е., Mu D., et al. 2006. Gain of chromosome 6p is an infrequent cause of increased PIM1 expression in B-cell non-Hodgkin's lymphomas. Leukemia. 20. 539-542.; Deutsch A., Aigelrransreiter A., Behan-Schmid C., Beham A., Linkesch W., Neumeister P. 2005. Aberrant somatic hypermutaion in extranodal marginal zone B-cell lymphoma of MALT type. Blood. 106. 125a-126a. Abstr 417; Roh M., Franco O.E., Hayward S.W., van der Meer R., Abdulkadir S.A. A role for polyploidy in the tumorigenicity of Pim-1-expressing human prostate and mammary epithelial cells. PLoS One. 2008. 3. Е2572]. Ингибирование активности протеинкиназы Pim-1 является важным компонентом лекарственной терапии солидных опухолей и гемобластозов. Помимо этого, протеинкиназа Pim-1 является потенциальной мишенью при терапии аутоиммунных заболеваний, таких как аллергические, и ее ингибирование ослабляет гиперчувствительность дыхательных путей к аллергенам и уменьшает астму [Yoo Seob Shin, Katsuyuki Takeda, Yoshiki Shiraishi, Yi Jia, Meiqin Wang, Leila Jackson, A. Dale Wright, Laura Carter, John Robinson, Erik Hicken, Erwin W. Gelfand Inhibition of Pim1 Kinase Activation Attenuates Allergen-Induced Airway Hyperresponsiveness and Inflammation. Am J Respir Cell Mol Biol. 2012. 46(4). 488-497]. Помимо этого, гиперэкспрессия Pim-1 характерна для псориаза, и эта протеинкиназа рассматривается как мишень для терапии кожных заболеваний [Mark R. Walter. Elucidating new drug targets in psoriasis by gene profiling: an opportunity to be seized. Ann Transl Med. 2015. 3(6). 78].
Раскрытие изобретения
Настоящее изобретение представляет собой применение rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодида в качестве ингибитора протеинкиназ Ins-R, Met, Src и Pim-1.
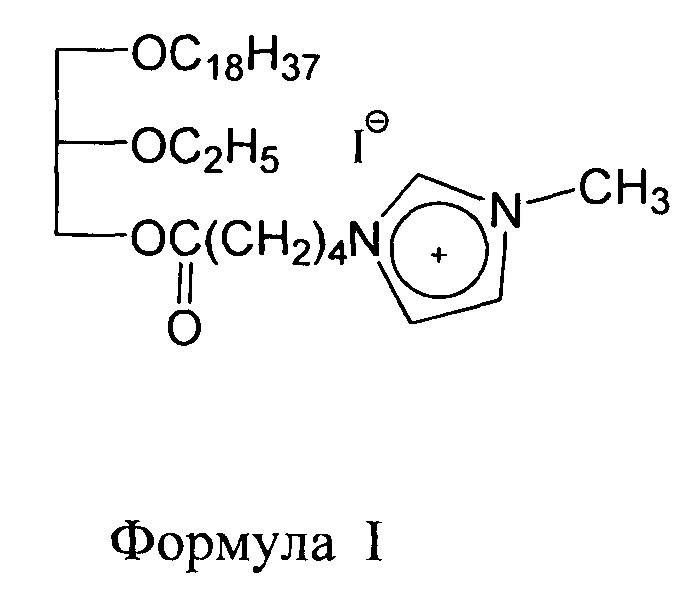
По сравнению со своим фосфатсодержащим функциональным аналогом - известным противоопухолевым липидом эдельфозином (1-октадецил-2-метил-sn-глицеро-3-фосфохолин), бесфосфорный катионный глицеролипид rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодид индуцирует апоптоз неопластических клеток за счет ингибирования протеинкиназ Ins-R, Met, Src, Pim-1, участвующих в канцерогенезе, что представляет преимущество этого соединения по отношению к эдельфозину. Ингибируемые rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодидом все эти протеинкиназы являются важными биомишенями не только в онкологии, но и как показано в уровне техники, при иммунных заболеваниях, заболеваниях кожи и нарушениях миелоидной пролиферации. На этом основана возможность применения данного соединения, так называемого «мультикиназного» ингибитора, то есть соединения, способного ингибировать все эти протеинкиназы, в разработке препарата на его основе или в комбинации с другими активными компонентами, известными на момент раскрытия изобретения; которые могут вводиться одним из известных на настоящий момент способов (например, перорально, внутривенно, внутримышечно и т.д.) в соответствующей лекарственной форме.
Применение настоящего ингибитора - бесфосфорного катионного глицеролипида - отличается от указанного в US 20090326031 А1, 31.12.2009 тем, что относится к ингибированию конкретных протеинкиназ Ins-R, Met, Src, Pim-1, которые не указаны в US 20090326031 А1, 31.12.2009. Как показано в уровне техники, данные протеинкиназы являются важными мишенями терапии, направленной на борьбу с избыточной клеточной пролиферацией, а также на патологии, опосредованные их повышенной активностью. В настоящем изобретении, в отличие от WO 2014071378 А1, 08.05.2014, бесфосфорный катионный глицеролипид ингибирует несколько протеинкиназ-мишеней, одной из которых является Ins-R, ее роль при различных патологиях описана в уровне техники.
Новизна
Применение rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодида в качестве мультикиназного ингибитора протеинкиназ Ins-R, Met, Src и Pim-1, раскрываемое в настоящем изобретении, ранее не описано в литературе.
Общие препаративные методы
Вещество, биологические свойства которого представлены в настоящем изобретении, может быть синтезировано с использованием известных химических превращений. Для синтеза описываемого соединения, активность которого представлена в изобретении, пригодны общие методы, описанные ниже.
Методы синтеза и характеристики полученных соединений
rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодид был получен, как было описано ранее [Н.В. Плявник, Т.В. Крамарева, Г.А. Серебренникова. Синтез катионных алкильных глицеролипидов с гетероциклическими азотистыми основаниями в качестве полярного домена. Биоорганическая химия. 2011. 37(4). 1-7].
Биологические характеристики rac-N-{4-[(2-этокси-3-октадецилокси)пропил]окси-карбонилбутил}N-метил-имидазолинийиодида
Пример 1
Внесли в чистые лунки 96-луночного планшета 15 мкл протеинкиназ Ins-R, Met, Src, Pim-1 и в контрольные лунки 15 мкл реакционного буфера Kinase-Glo® Plus Buffer (KB). Перенесли в каждую лунку, кроме контрольных, по 15 мкл раствора исследуемого соединения (rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодид или эдельфозин) до конечных концентраций 10 мкМ. Количество повторов - 8. Стряхнули капли со стенок лунок, ресуспендировали. Инкубировали смесь при комнатной температуре в течение 30 мин, прикрыв крышкой, после чего в каждую лунку добавили 15 мкл субстрат-АТР смеси, перемешали. Инкубировали киназную реакцию при 37°C в течение 30-120 мин, закрыв планшеты крышками от испарения.
Приготовили реагент: растворили Kinase-Glo® Plus Substrate в 10 мл буфера Kinase-Glo® Plus Buffer, разлили полученный раствор по 1 мл в эппендорфы. По окончании киназной реакции добавили в каждую лунку по 30 мкл реагента, инкубировали планшет 10 мин при комнатной температуре, закрыв крышкой, и измерили люминесценцию на Beckman Coulter© DTX 880 Multimode Detector. Параметры измерения: время измерения - 100, 400, 1000 мс, чувствительность измерения - expected high activity.
Конечные концентрации веществ в киназной реакции
Протеинкиназа 50 нг на лунку;
субстрат поли(Glu, Tyr 4:1) 5 мкг на лунку = 0,25 мкг/мкл;
исследуемые соединения rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодид 1 мкМ, эдельфозин 1-10 мкМ.
АТР 5 мкМ.
ДМСО 1,25%.
Объем реакционной смеси 45 мкл.
КВ вместо протеинкиназы - 100% АТР = 100% ингибирование = 0% активности протеинкиназы.
КВ + 5% ДМСО вместо ингибитора - 100% активность протеинкиназы = 0% ингибирования.


Пример 2
Для экспериментов использована линия неопластических клеток А549 (аденокарцинома легкого человека), с выраженной экспрессией протеинкиназ Ins-R, Met, Src и Pim-1. Клетки культивировали в среде DMEM (Панэко, Россия). В культуральную среду добавляли следующие компоненты до конечных концентраций: 10% эмбриональной телячьей сыворотки, 2 mM L-глутамина, 100 ЕД/мл пенициллина и 100 мкг/мл стрептомицина (среды и добавки производства ПанЭко, Россия), инкубация проводилась при 37°С, 5% CO2, в увлажненной атмосфере. В экспериментах использована культура в логарифмической фазе роста. Клетки рассевали в лунки 96-луночного планшета (NUNC, США) (5000 клеток в 190 мкл культуральной среды), инкубировали 24 часа при 37°С, 5% СО2, в увлажненной атмосфере. Вносили по 10 мкл раствора rac-N-{4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил}-N-метил-имидазолинийиодида в культуральной среде, приготовленных серийными разведениями из исходного раствора 10 мМ в ДМСО, до 10 конечных концентраций 0.1-50 мкмоль/л. Контролем служили клетки без препарата (интактный контроль). В эксперименте клетки инкубировали 72 часа при 37°С, 5% СО2, в увлажненной атмосфере и за 1 час до окончания инкубации в лунки вносили по 20 мкл водного раствора МТТ (5 мг/мл, ПанЭко, Россия). После окончания инкубации клеток с МТТ-реагентом культуральную среду отбирали, клетки ресуспендировали в 100 мкл ДМСО и измеряли оптическую плотность раствора на планшетном спектрофотометре Multiscan FC (Thermo Scientific, США) при длине волны 571 нм. Процент клеток, выживших при действии каждой концентрации исследуемого вещества, подсчитывали как частное от деления средней оптической плотности в лунках после инкубации с данной дозой к средней оптической плотности контрольных лунок (значения последних приняты за 100%). Каждую концентрацию изучали с 3-кратной статистикой, приводили усредненные данные по результатам трех независимых экспериментов (см. рис. 1).
Биологические свойства химического соединения согласно изобретению могут успешно применяться в создании терапевтических, в частности, противоопухолевых средств, ингибирующих киназы.
![Применение rac-N-{ 4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил} -N-метил-имидазолинийиодида в качестве мультикиназного ингибитора](https://fips.edrid.ru/images/rid/01/ca/b4/8f50adab9f55cfd15fdb25c6c2318e1c.jpg)
![Применение rac-N-{ 4-[(2-этокси-3-октадецилокси)пропил]оксикарбонилбутил} -N-метил-имидазолинийиодида в качестве мультикиназного ингибитора](https://fips.edrid.ru/images/rid/01/ca/b4/3b3e31a3df07e3290515624fe4209894.jpg)

