Результат интеллектуальной деятельности: СПОСОБ АКТИВАЦИИ ЦИТОТОКСИЧЕСКИХ ЛИМФОЦИТОВ ЧЕЛОВЕКА
Вид РИД
Изобретение
Изобретение относится к области медицины, в частности к способам получения активированных лимфоцитов, и может быть использовано для адоптивной иммунотерапии онкологических больных.
Последнее время все большее значение в терапии различных онкологических заболеваний приобретают комплексные подходы с использованием методов адоптивной иммунотерапии на основе культивируемых in vitro лимфоцитов. На сегодняшний день нет общепринятого метода получения активированных лимфоцитов in vitro [Курилин В.В. и соавт. Медицинская иммунология. 2013. Т. 3, №15. С. 235-246; Титов К.С. и соавт. Российский биотерапевтический журнал. 2011. Т. 2, №10. С. 51-54].
Известен «Способ получения активированных лейкоцитов для адъювантной адоптивной иммунотерапии злокачественных новообразований» по патенту RU 2414915. В нем лейкоциты выделяют из периферической крови, культивируют в среде RPMI или DMEM с 2-10% сыворотки пациента (или АВ сыворотки донора), затем к среде добавляют Г-КСФ в концентрации 500-5000 МЕ/мл. Культивирование проводят в течение 48-72 ч в условиях СО2-инкубатора. При этом лейкоциты выделяют из стабилизированной гепарином периферической крови посредством смешивания с полиглюкином в течение 30 мин.
Основным недостатком способа является добавление гранулоцитарного колониестимулирующего фактора (Г-КСФ), который регулирует пролиферацию, дифференцировку и продолжительность жизни клеток гранулоцитарного ряда, а не лимфоцитов и короткие сроки культивирования клеток, не позволяющие проводить адоптивную иммунотерапию в течение длительного периода времени без дополнительного забора крови.
Известны три идентичных способа генерации антиген-специфических цитотоксических клеток с противоопухолевой активностью: по патенту RU 2458985 «Способ генерации антиген-специфических цитотоксических клеток с противоопухолевой активностью»; «Способ генерации антиген-специфических цитотоксических клеток с противоопухолевой активностью против клеток рака яичников» по патенту RU 2508298 и «Способ генерации антиген-специфических цитотоксических клеток с противоопухолевой активностью при раке молочной железы» по патенту RU 2521506. В основе способов лежит совместное культивирование неприлипающей фракции мононуклеарных клеток (МНК), выделенных из периферической крови больных с дендритными клетками (ДК), активированными опухолевым антигеном, полученными из моноцитов прилипающей фракции МНК, отличающийся тем, что для совместного культивирования берут зрелые ДК, полученные добавлением к антиген-активированным с помощью аутологичных опухолевых клеток незрелым ДК провоспалительного цитокина ФНО-α (фактор некроза опухоли), а совместное культивирование неприлипающей фракции МНК и зрелых антиген-активированных ДК проводят в присутствии рекомбинантного человеческого интерлейкина-12 и рекомбинантного человеческого интерлейкина-18.
Недостатки способа заключаются в существенном усложнении культивирования клеток: изначальным разделением на фракции и использованием опухолевых антигенов для активирования дендритных клеток.
Известен «Способ лечения больных раком легкого» по патенту RU 2500435. В нем предложено до проведения лечебной процедуры из крови больного произвести забор лимфоцитов методом лимфоцитафереза и приготовить лейкоцитарную массу. Затем произвести активацию ронколейкином 20 мл лейкоцитарной массы из расчета соответственно 1000 Ед на 1 мл путем инкубации в термостате с последующим двукратным центрифугированием.
Главные недостатки способа заключаются в использовании высоких концентраций интерлейкина-2 (IL-2) в среде для культивирования клеток и сроках культивирования клеток, не позволяющих проводить адоптивную иммунотерапию в течение длительного периода времени без дополнительного забора крови.
Известен «Способ получения активированных мононуклеарных лейкоцитов» по патенту RU 2402338. Он описывает способ культивирования клеток в питательной среде RPMI-1640, с добавлением 10% фетальной бычьей сыворотки, IL-2 и циклодекстрина. Активацию in vitro концентрата лимфоцитов и макрофагов, выделенного из крови донора или пациента, осуществляют комплексом, включающим фармакопейный препарат рекомбинантного IL-2 в диапазоне субоптимальных доз 50-100 ME в 1 мл среды культивирования и β-циклодекстрин в концентрации 1×10-5-1×10-3 М в среде культивирования при молярном соотношении компонентов 1:1, или 1:3, или 1:10. Клетки инкубировали в СО2-инкубаторе в течение 18-48 ч.
Недостатки способа заключаются в том, что используют продукты животного происхождения, а именно среду с добавлением 10% фетальной бычьей сыворотки для выращивания лимфоцитов человека, культивируют две фракции: лимфоцитов и макрофагов. Проводят краткосрочное культивирование периферических мононуклеаров 18-48 часов, не позволяющее проводить адоптивную иммунотерапию в течение длительного периода времени без дополнительного забора крови.
Известен «Способ получения питательной среды «Лимфокар» для культивирования лимфоцитов периферической крови человека и животных» по патенту RU 2236457. Он состоит в использовании, для культивирования лимфоцитов периферической крови человека и животных, среды RPMI-1640, содержащей фитогемагглютинин-П и эмбриональную телячью сыворотку.
Недостатки способа заключаются в том, что среди компонентов среды для выращивания лимфоцитов человека используются продукты животного происхождения, а именно сыворотка эмбрионов телят, и не используют цитокины для активации лимфоцитов.
Известен «Способ получения депонированных лимфокин-активированных киллеров» по патенту RU 2400238. В способе выделяют мононуклеарные лимфоциты из периферической крови или злокачественного выпота и инкубируют в среде RPMI-1640 или DMEM с добавлением 2-10% АВ сыворотки человека, интерлейкина-2 в концентрации 0,5-1,0 млн МЕ/мл в CO2-инкубаторе в течение 48-72 ч. Затем взвесь полученных ЛАК-клеток депонируют в культуральной среде на стерилизованные пористые титановые носители.
Главные недостатки способа заключаются в использовании высоких концентраций IL-2 в среде для культивирования клеток, использование дополнительных пористых носителей и сроках культивирования клеток, не позволяющих проводить адоптивную иммунотерапию в течение длительного периода времени без дополнительного забора крови.
Наиболее близким к предлагаемому техническому решению является способ активации цитотоксических лимфоцитов [Абакушина Е.В. и соавт. Медицинская иммунология. 2014. Т. 16, №5. С. 449-456 и Абакушина Е.В. и соавт. Медицинская иммунология. 2014, Т. 16, №6, С.. 567-476]. В нем культивирование МНК в концентрации 1-2×106 кл/мл проводят на протяжении 7-9 дней в питательной среде X-vivo 20 (Lonza, США) с добавлением 5-10% эмбриональной телячьей сыворотки или аутологичной сыворотки, с 250 МЕ/мл TJL-2 (ронколейкин) и 50 нг/мл IL-15 в СО2-инкубаторе при 37°C.
Недостатками данного способа являются: использование продуктов животного происхождения фетальной телячьей сыворотки в среде для культивирования лимфоцитов человека, сложность получения аутологичной сыворотки больного, которая требует постоянного дополнительного забора крови, а также использование высоких концентраций IL-15.
Задачей изобретения является устранение указанных недостатков.
Технический результат.
Предлагаемое изобретение позволяет получить большое количество активированных лимфоцитов с высокой жизнеспособностью, цитотоксической и функциональной активностью.
Сущность изобретения включает забор венозной крови у онкологического больного или донора, выделение из нее МНК и их культивирование в CO2-инкубаторе при 37°C. Активацию и культивирование МНК проводят в полной питательной среде, содержащей рекомбинантный человеческий альбумин, пируват натрия, гентамицин, L-глутамин, с добавлением от 125 до 500 нг/мл рекомбинантного человеческого интерлейкина-2 (IL-2) от 2,5 до 5 нг/мл рекомбинантного человеческого интерлейкина-15 (IL-15) на протяжении 10-14 дней. В результате данной процедуры получают активированные цитотоксические лимфоциты. При этом через каждые 48-72 часа обновляют половину объема питательной среды, определяют в ней концентрацию цитокинов, оценивают фенотип и маркеры активации МНК, оценивают их жизнеспособность, а также пролиферативную и цитотоксическую активность. Активированные цитотоксические лимфоциты, полученные предложенным способом, используют для фундаментальных исследований по выявлению новых закономерностей и морфо-функциональных особенностей активированных лимфоцитов человека и для проведения адоптивной иммунотерапии больным.
Перечень чертежей
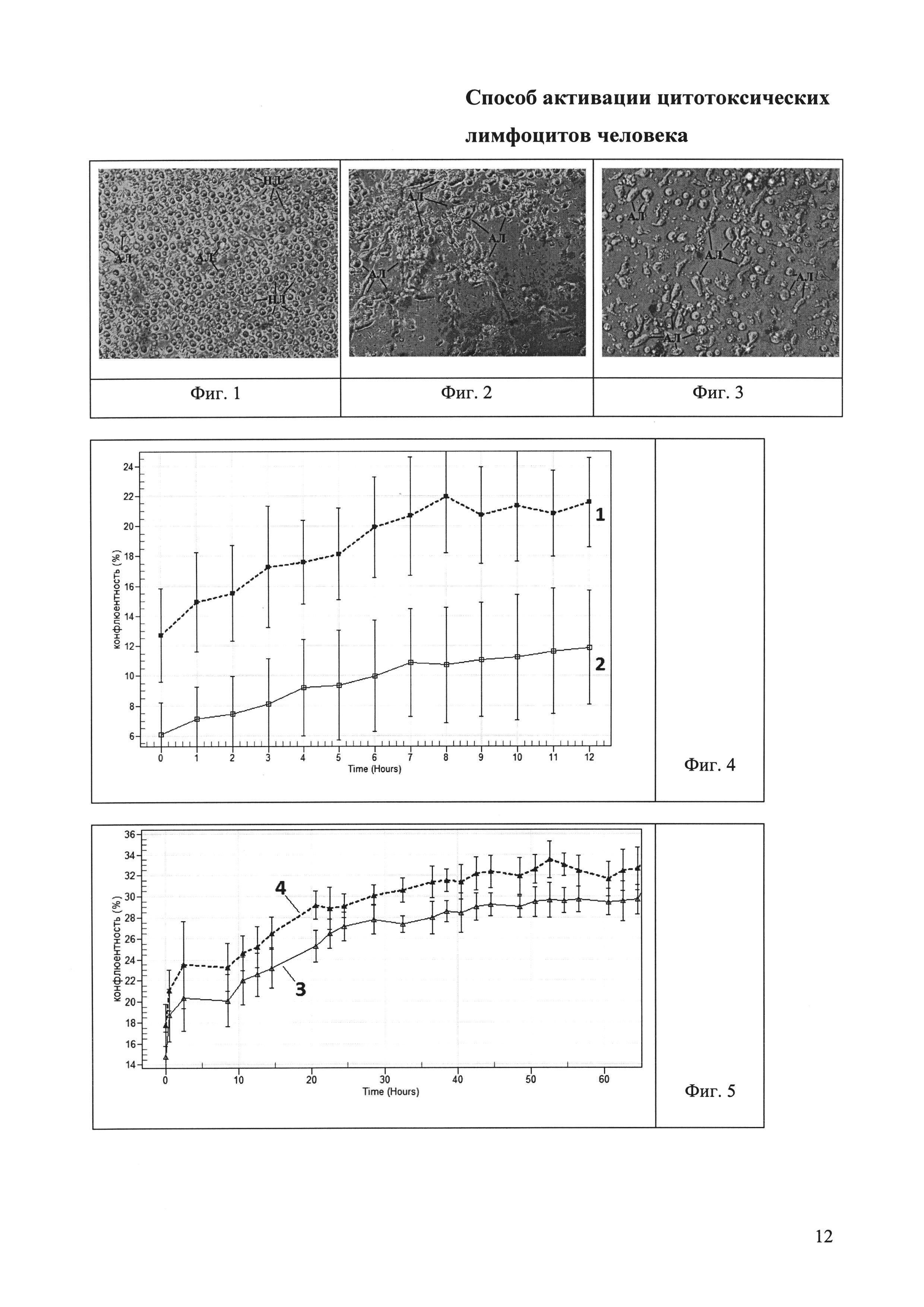
Фиг. 1 - морфология лимфоцитов на 3 день культивирования. Без окраски. Увеличение: ×400. НЛ - не активированный лимфоцит. АЛ - активированный лимфоцит.
Фиг. 2 - морфология лимфоцитов на 5 день культивирования. Без окраски. Увеличение: ×400. АЛ - активированный лимфоцит.
Фиг. 3 - морфология лимфоцитов на 10 день культивирования. Без окраски. Увеличение: ×400. АЛ - активированный лимфоцит.
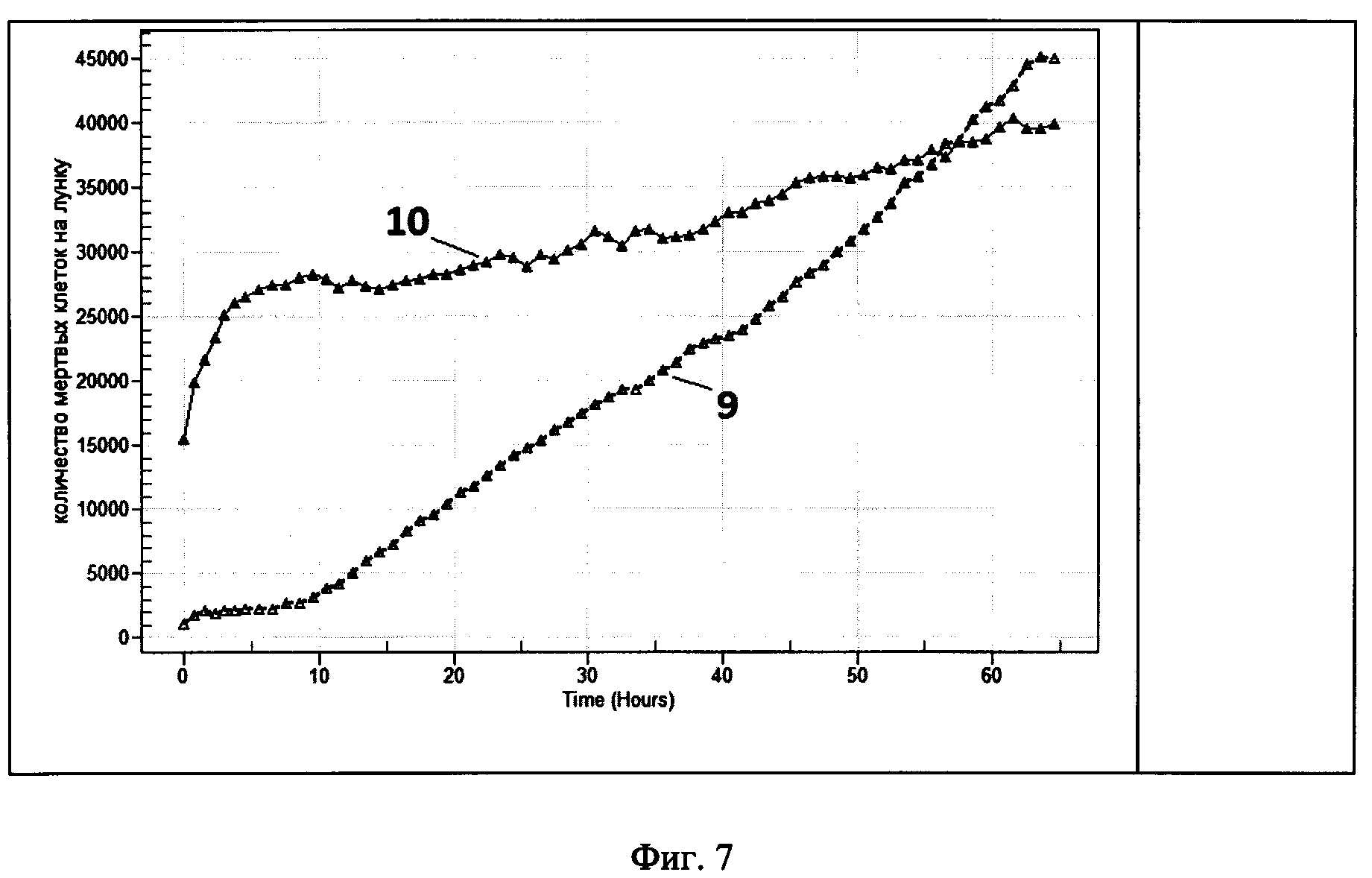
Фиг. 4 - Влияние IL-2 на пролиферативную активность лимфоцитов донора: 1 - с добавлением IL-2 (250 МЕ/мл); 2 - без добавления IL-2.
Фиг.5 - Влияние IL-2 и IL-15 на пролиферативную активность лимфоцитов больного: 3-IL-2 (в концентрации 250 МЕ/мл) без IL-15; 4 - IL-2 (в концентрации 250 МЕ/мл) и IL-15 (2,5 нг/мл).
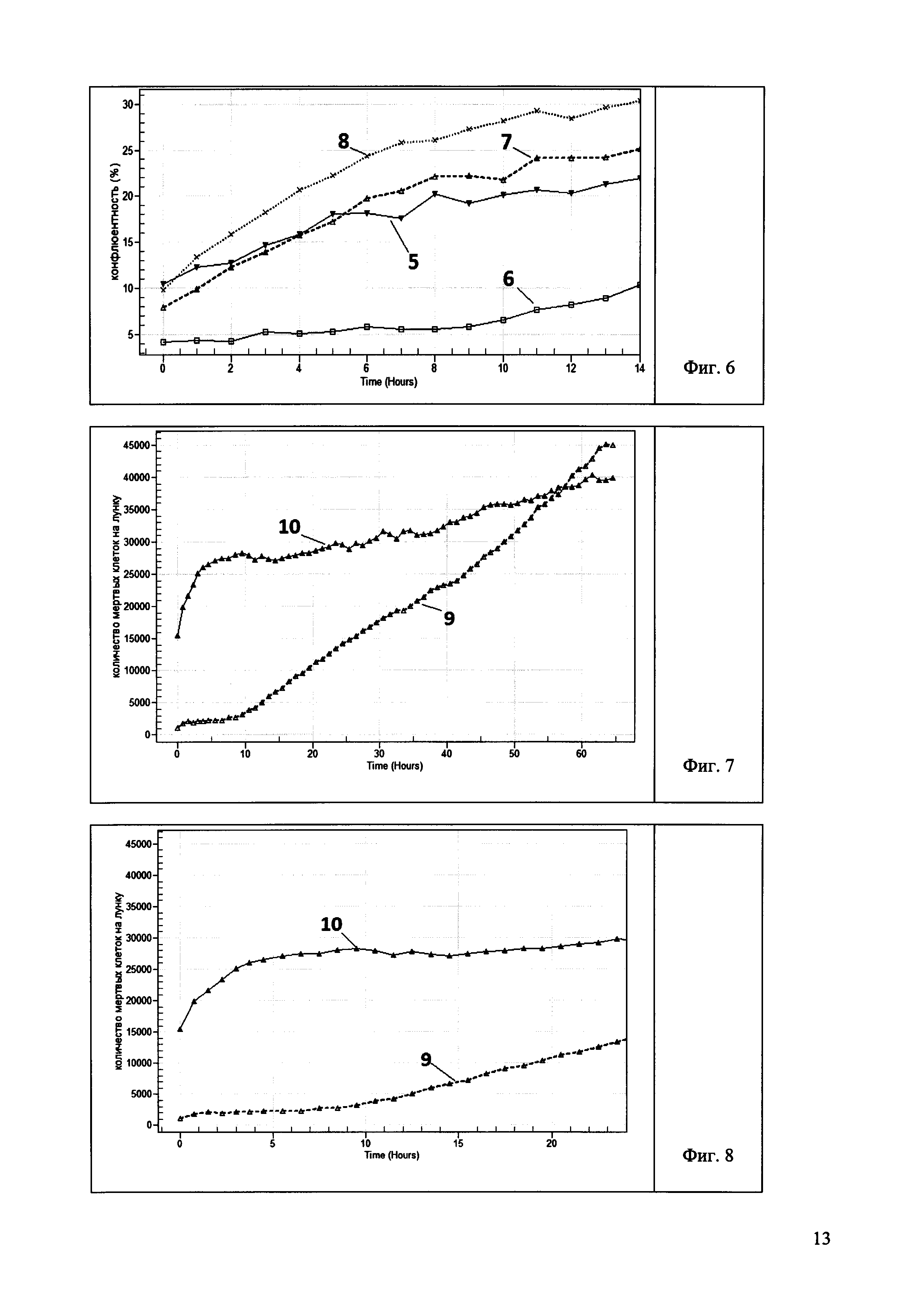
Фиг. 6 - Пролиферативная активность лимфоцитов в различные сроки после активации: 5 - цитотоксические лимфоциты донора на 5 день; 6 - цитотоксические лимфоциты донора на 7 день; 7 - цитотоксические лимфоциты больного на 1 день; 8 - МНК донора на 0 день.
Фиг. 7 - Цитотоксическая активность активированных лимфоцитов (3 день) и нативных лимфоцитов: 9 - нативные МНК в среде с IL-2; 10 - активированные лимфоциты 3 день в среде с IL-2.
Фиг. 8 - Цитотоксическая активность активированных лимфоцитов (3 день) и нативных лимфоцитов: 9 - нативные МНК в среде с IL-2; 10 - активированные лимфоциты 3 день в среде с IL-2.
Порядок реализации способа
1. Для выделения МНК, гепаринизированную венозную кровь разбавляют в 2 раза фосфатно-солевым буфером (ФСБ) (Gibco by life technologies, Великобритания), наслаивают ее на градиент Hystopague-1077 (Sigma, Великобритания) плотностью 1,077 г/см3 и центрифугируют при 2000 об/мин в течение 20 мин, что приводит к оседанию эритроцитов и гранулоцитов на дно пробирки. В результате центрифугирования МНК образуют интерфазное кольцо, которое собирают пипеткой и двукратно отмывают центрифугированием в 10-кратном объеме ФСБ при 1500 об/мин.
2. Выделенные МНК подсчитывают, ресуспендируют в концентрации 1-2×106 кл/мл в приготовленной питательной среде, содержащей рекомбинантный человеческий альбумин, пируват натрия, гентамицин, L-глутамин с добавлением от 125 до 500 МЕ/мл (нг/мл) человеческого рекомбинантного IL-2 (ронколейкин, Биотех, Россия) и от 2,5 до 5 нг/мл человеческого рекомбинантного IL-15 (ImmunoTools, Германия) и помещают в пластиковые флаконы с вентилируемой крышкой (Corning-Costar, США) в СО2-инкубатор при 37°C. На 3 день культивирования получают активированные цитотоксические лимфоциты. В качестве питательной среды могут быть использованы X-vivo 20 (Lonza, США), RPMI-1640 или DMEM.
3. Ежедневно проводят морфологическую оценку культуры лимфоцитов и визуальную оценку питательной среды на присутствие патогенной микрофлоры. Для поддержания жизнеспособности активированных цитотоксических лимфоцитов на протяжении 10-14 дней через каждые 48-72 часа обновляют половину объема среды. На 3, 6, 10 и 14 день культивирования определяют концентрацию цитокинов в питательной среде, фенотип и маркеры активации цитотоксических лимфоцитов, оценивают их жизнеспособность, а также пролиферативную и цитотоксическую активность.
Примеры реализации способа
Пример 1. Оценка морфологии клеток в культуре
Морфологию клеток в культуре оценивают ежедневно при помощи инвертированного микроскопа Eclipse TS100 (Nikon, Япония) или его аналога (Фиг. 1). С 3-го дня культивирования некоторые лимфоциты адгезируют к пластику флакона, увеличиваются в размерах, изменяют форму и начинают делиться, что приводит к формированию групп (Фиг. 2). При последующем длительном культивировании на протяжении 10-14 дней большинство МНК сохраняют морфологию больших гранулярных лимфоцитов. У некоторых пациентов лимфоциты самопроизвольно отлипают от пластика флакона после 10 дня культивирования, что свидетельствует о завершении процесса активации (Фиг. 3).
Пример 2. Оценка жизнеспособности и пролиферативной активности МНК
Подсчет МНК производят на автоматическом анализаторе жизнеспособности клеток ТС 10 (BioRad, США) или с помощью камеры Горяева при каждом пересаживании. Для определения жизнеспособности культивируемых клеток используют 0,1% краситель трипановый синий (Bio-Rad, Великобритания). Жизнеспособность культивируемых клеток до 10 дня культивирования составляет более 95-97%.
Пролиферативную активность лимфоцитов оценивают во время культивирования МНК без добавления цитокинов, а также в присутствии 125-500 нг/мл IL-2 и 2,5-5 нг/мл IL-15 в течение 72 ч в полной питательной среде в СО2-инкубаторе при помощи автоматического анализатора IncuCyte zoom (Essen Bioscience, США). Каждый час автоматически получают изображение заданных областей наблюдения. Полученные данные обрабатывают с помощью программы IncuCyte Software и строят графики изменения конфлюентности в зависимости от времени наблюдения, т.е. пролиферативной активности лимфоцитов, которые находятся на поверхности пластикового флакона и попадают в зону анализа прибора (Фиг. 4, 5, 6). Увеличение пролиферативной активности к 6-7 дню составляет 20-40%, а к 14 дню количество клеток увеличивается примерно в два раза. Из графиков следует, что добавление 250 нг/мл IL-2 и 2,5 нг/мл IL-15 в полную питательную среду увеличивает конфлюентность лимфоцитов на протяжении 5 дней культивирования и практически не изменяется с 7 дня культивирования. Добавление IL-2 в концентрации 125 нг/мл уменьшает пролиферативную активность, а в концентрации 500 нг/мл несколько увеличивает скорость пролиферации, но негативно сказывается на жизнеспособности лимфоцитов (>93%).
Пример 3. Определение цитотоксической активности лимфоцитов in vitro по отношению к опухолевой клеточной линии К562 колориметрическим методом
Для оценки цитотоксической активности активированных лимфоцитов используют нерадиоактивный колориметрический ферментативный анализ по выходу лактатдегидрогеназы (ЛДГ) из мертвых клеток (CytoTox96, Promega, США). Для этого клетки-мишени линии К562 и клетки-эффекторы нативные и активированные МНК смешивают в различных соотношениях эффектор/мишень: 25:1, 12,5:1 и 6:1 и инкубировали 3 часа в СО2-инкубаторе. Выход ЛДГ из перфорированных клеток в среду культивирования измеряют в 30-минутном ферментативном тесте. Оценку оптической плотности образцов оценивают при длине волны 490 нм на фотометре ChroMate 4300 (Awareness Technology, США), процент специфического лизиса клеток-мишеней определяют по формуле, приведенной в инструкции к набору реагентов: СЛ=100×[(ЭМ-С)-(М-С)-(Э-С)]/[Ммакс.-М], где СЛ - процент специфического лизиса клеток-мишеней; ЭМ - значение выхода лактатдегидрогеназы (ЛДГ) из клеток-мишеней и клеток эффекторов в экспериментальных точках; М - фоновое значение клеток-мишеней; Э - фоновое значение клеток эффекторов; С - фоновое значение культуральной среды; Ммакс - максимальное значение выхода ЛДГ из клеток мишеней. Специфический лизис клеток-мишеней К562 активированными лимфоцитами на 3 день культивирования увеличивается более чем на 20% по сравнению с неактивированными лимфоцитами, что означает повышение цитотоксической активности культивированных МНК.
Пример 4. Автоматическое определение цитотоксической активности лимфоцитов in vitro по отношению к опухолевой клеточной линии К562 с использованием флуоресцентных красителей
Предложенный способ оценки цитотоксической активности активированных лимфоцитов на 0 и 3 день культивирования осуществляют на приборе IncuCyte zoom (Essen BioScience, США) с помощью флюоресцентного окрашивания этидием гомодимером (EtHd-1) (в концентрации 2 мкМ/мл) мертвых клеток в красный цвет. Для осуществления данного способа используют различные соотношения клеток мишеней линии К562 и эффекторов 1:10, 1:20 и 1:40. Клеточную смесь выращивают в полной питательной среде с IL-2 и IL-15, с добавлением EtHd-1 в концентрации 2 мкМ/мл на протяжении 65 ч в СО2-инкубаторе. Каждые 1,5 часа производят автоматическое измерение уровня флуоресценции EtHd-1 при длине волны 528/617 нм в опытных лунках. Полученные данные обрабатывают с помощью программы IncuCyte Software и строят графики зависимости количества мертвых клеток от времени для оценки цитотоксической активности лимфоцитов больных (Фиг. 7). Показано, что цитотоксическая активность лимфоцитов постепенно увеличивается, достигая максимума через 2-3 дня культивирования, что подтверждается увеличением поверхностной экспрессии маркеров активации лимфоцитов в эти же сроки. Сравнивая цитотоксическую активность лимфоцитов на 0 и 3 день, видно, что у активированных лимфоцитов на третий день она выше в несколько раз (Фиг. 8).
Пример 5. Определение фенотипа и маркеров активации цитотоксических лимфоцитов методом проточной цитометрии
Субпопуляционный состав суспензионных лимфоцитов и экспрессию маркеров активации определяют на 0, 3, 6, 10 и 14 день культивирования лимфоцитов. Оценивают фенотип В-, Т-, NKT-, NK- клеток и маркеры активации (HLA-DR, CD38, CD69, CD314, CD25) лимфоцитов больных или доноров. Для фенотипирования лимфоциты отмывают ФСБ центрифугированием и окрашивают конъюгированными с РЕ или FITC антителами к CD3, CD4, CD8, CD16, CD20, CD25, HLA-DR, CD38, CD56, CD69 (Beckman Coulter, Франция) и CD314 (eBioScience, США). Фенотипирование флуоресцентно меченых лимфоцитов проводят на проточном цитофлуориметре FACScan (Becton Dickinson, США), анализируют не менее 5000 событий в секторе живых клеток-мишеней. В процессе активации происходит незначительное перераспределение долей клеточных субпопуляций среди МНК. Так процент В-лимфоцитов незначительно уменьшается к 14 дню культивирования. Доля Т- и NKT-клеток начинает увеличиваться с 6 дня. Количество NK-клеток к 10 дню возрастает в 1,4 раза. Лимфоциты активируются in vitro начиная с 3-го дня, а в большей степени после 5 дня культивирования. Тенденция к увеличению экспрессии поздних активационных маркеров сохраняется до 14 дня культивирования. Содержание маркера ранней активации CD69 начинает в несколько раз увеличиваться на всех лимфоцитах и на NK-клетках со 2-го дня культивирования. Экспрессия раннего маркера активации CD38 после 5-го дня культивирования на всех лимфоцитах возрастает в 2 раза, а на Т-клетках в 3,5 раз. Количество всех активированных HLA-DR+ клеток к 6 дню увеличивалось в 2 раза.
Процент активированных CD25+ клеток максимально возрастал в 1,7 раз только к 14 дню культивирования. Таким образом, прослеживается волнообразное нарастание экспрессии активационных рецепторов, начиная от ранних маркеров и заканчивая более поздними. В культуре лимфоцитов больший прирост и активация наблюдаются у цитотоксических лимфоцитов, которые и будут использоваться для адоптивной иммунотерапии. На протяжении всего времени наблюдения лимфоциты хорошо активируются и пролиферируют in vitro с сохранением высокой жизнеспособности.
Пример 6. Определение концентраций цитокинов в культуральной среде
Для оценки уровня цитокинов в среде культивирования МНК на 0, 3 и 10 день был проведен иммуноферментный анализ (ИФА) с помощью набора реагентов (Вектор Бест, Россия) для определения концентрации IL-2, IL-4, IL-6, IL-10, IFN-α, IFN-γ и FNO-α. На 3 день культивирования лимфоцитов в полной питательной среде в разной степени увеличивается содержание всех исследуемых цитокинов, что свидетельствует об увеличении функциональной активности МНК. Многократно увеличивается концентрация IFN-γ, IL-4, IL-6, FNO-α и уменьшается концентрация IL-10. Содержание цитокина IFN-α в среде культивирования на 10 день увеличивается незначительно по сравнению с 3 днем. Концентрация IL-2 превышает максимальное значение (1000 пг/мл) у всех исследуемых образцов как на 3 день, так и на 10 день культивирования.
Подтверждение достижения технического результата
Предложенный способ активации цитотоксических лимфоцитов является эффективным и безопасным. Способ отличается упрощенным методом активации цитотоксических лимфоцитов in vitro, без разделения МНК на фракции и использования антигенов опухолевых клеток. Благодаря уменьшению концентраций цитокинов (IL-2 и IL-15) и их совместному добавлению к полной питательной среде, не содержащей белков животного происхождения, предлагаемый способ может снизить выраженность побочных эффектов иммунотерапии. Цитотоксические лимфоциты, полученные предложенным способом, используют для проведения фундаментальных исследований по изучению морфофункциональных особенностей активированных лимфоцитов человека и проведения адоптивной иммунотерапии онкологическим больным, в том числе для пациентов с сильно выраженным негативным ответом на введение IL-2. Добавление комбинации IL-2 и IL-15 в полную питательную среду способствует повышению жизнеспособности, пролиферативной активности и функциональной противоопухолевой активности культивируемых лимфоцитов. Также цитокины положительно влияют на поверхностную экспрессию маркеров активации лимфоцитов.
Предлагаемое изобретение позволяет увеличить количество и функциональную активность цитотоксических лимфоцитов за счет долгосрочного культивирования лимфоцитов в течение 10-14 дней, что дает возможность проводить адоптивную иммунотерапию в течение длительного периода времени без дополнительного забора крови.
Более того, проведенные нами исследования свидетельствуют о том, что при активации цитотоксических лимфоцитов в бессывороточной среде можно использовать более низкие концентрации IL-15 в комбинации с IL-2 для увеличения жизнеспособности клеток и сохранения их функциональной активности.