Результат интеллектуальной деятельности: СЫРЬЕВОЙ КОНЦЕНТРАТ И ШИХТА ДЛЯ ПРОИЗВОДСТВА СИЛИКАТНОГО СТЕКЛА
Вид РИД
Изобретение
Получение стекла представляет собой сложный физико-химический процесс, основными стадиями которого являются силикатообразование, стеклообразование, осветление, гомогенизация и охлаждение стекломассы.
Если процессы силикато- и стеклообразования для натрий-кальций-силикатных стекол могут заканчиваться при 1150-1250°С, то для освобождения стекломассы от газовых включений (осветления) необходима температура 1450-1550°С [1].
Протекающие процессы осветления и гомогенизации занимают при указанной температуре длительное время, поэтому для ускорения процесса осветления необходимо использовать различные «грязные» с точки зрения экологии осветляющие добавки, например сульфат. Выбросы выделяющегося SO3, например в Европе, ограничены согласно директиве ЕС № 2008/50/EC от 21 мая 2008 года, превышение которых ведет к остановке деятельности предприятия.
Качество подготовки традиционных сырьевых материалов и стекольной шихты напрямую влияет на процессы осветления и гомогенизации. Например, сегрегация компонентов стекольной шихты отрицательно сказывается на протекании всех стадий получения стекла.
Традиционные сырьевые материалы, такие как карбонаты щелочных и щелочноземельных металлов, при нагревании выделяют большое количество углекислого газа, который, с одной стороны, положительно влияет на процессы осветления и гомогенизации, с другой стороны, уносит пылевидные составляющие шихты, служит источником загрязнения окружающей среды.
На процессы осветления и гомогенизации отрицательно влияет декрепитация карбонатов щелочноземельных металлов при нагревании. Процесс термического разложения известняка, магнезита, доломита, содержащие карбонаты Mg и Ca, сопровождается растрескиванием, пылением, образованием пылевидных частиц, часть которых уносится печными газами и откладывается на огнеупорах и в регенеративной системе стекольной печи, а другая часть, оставшаяся в расплаве, является источником “мошки” в стекломассе.
Целью изобретения является получение сырьевого концентрата для производства силикатного стекла на основе предварительной обработки традиционных компонентов стекольной шихты и составление шихты на его основе, позволяющих снизить температуру и/или сократить время варки силикатного стекла без использования или с уменьшенным количеством осветляющих добавок по сравнению с традиционным способом получения силикатного стекла.
В патенте RU2152363 [2] описан способ получения щелочного концентрата для замены кальцинированной соды и поташа при варке стекла. Сырьевой концентрат содержит гранулы, включающие частицы кремнезема, покрытые силикатами натрия и калия. Плотность концентрата - 0,8-0,95 г/см, размер гранул - до 0,2 мм. Концентрат получают смешиванием кремнезема с гидроксидами калия и натрия при соотношении их (3-4):1, упариванием смеси при температуре 100-200°С с выдержкой 1-1,5 ч. Затем осуществляют термообработку при 350 - 550°С.
Представленный способ получения и применения ЩК имеет ряд недостатков:
- ввиду летучести NaOH расчетное (теоретическое) значение Na2O и K2О в получаемом ЩК не соответствует практическому, определяемому, например, методом пламенной фотометрии [3];
- ЩК, полученный по описанному способу, содержит остаточный NaOH более 5 % и обнаруживается методом РФА. На практике это означает, что при выполнении любых технологических операций с ЩК необходимо использовать средства защиты органов дыхания [4];
- использование ЩК, полученного по вышеописанному способу, приводит к появлению обильной «мошки» в стекле, вызванной отсутствием в шихте кальцинированной соды, положительно влияющей на осветление, при одновременном присутствии сырьевых источников, содержащих карбонаты щелочноземельных металлов, «пылящих» при нагревании [3].
В заявке RU2007131721 [5],признанной патентоспособной, предлагается способ получения ЩК на основе смеси кварцевого песка и гидроксида натрия, термообработанной при температуре 600°С с целью использования β → α перехода из низкотемпературной полиморфной модификации кристаллического кремнезема в высокотемпературную. Полиморфное превращение кварцевого зерна сопровождается увеличением объема и растрескиванием, что по мнению авторов должно способствовать более полному взаимодействию кварца и каустика.
Но ввиду короткого временного интервала (3-10 мин для термообработки смеси по указанному способу) взаимодействия каустика и кварца, появление α - высокотемпературной модификации носит следовый характер, что подтверждается полученными данными рентгенофазового анализа (РФА) [3].
Кроме того, рассматриваемому способу получения и применения ЩК присущи все недостатки, отмеченные при рассмотрении RU2152363.
В патенте RU 2107666 [6] предлагается способ подготовки шихты для производства стекла, включающий обработку кварцевого песка водным раствором гидроксида натрия при температуре 170-200°С, смешивание компонентов шихты, отличающийся тем, что предварительно смешивают компоненты шихты, а после обработки водным раствором гидроксида натрия осуществляют дополнительную термообработку при 400 - 700°С.
Однако ввиду более длительной термообработки смеси, включающей «кипячение» всех сырьевых компонентов шихты в водном растворе каустика с последующей прокалкой смеси, проблема конечного содержания Na2O в получаемом промежуточном продукте и в стекле стоит еще более остро, чем в рассматриваемых выше способах. Несмотря на то что авторы указывают на отсутствие мошки в стекле, сваренном по предлагаемому способу, предпосылки для ее возникновения есть, а именно: отсутствие в шихте карбоната натрия с одновременным присутствием остаточных карбонатов магния и кальция, т.к. ни полное их разложение, ни завершение реакций силикатообразования при указанных условиях протекать не может.
В патенте WO2010031834 [7] предлагается уменьшить декрепитацию сырьевых материалов, содержащих карбонаты щелочноземельных металлов (мел, известняк, доломит) путем обработки указанных материалов раствором в т.ч. каустика слабой концентрации (0,05-5%) от веса обрабатываемого сырьевого материала. Указанная процедура позволяет снизить декрепитационные свойства сырьевых материалов в несколько раз, но не интенсифицирует процессы силикатообразования и не способна привести к снижению температуры варки силикатного стекла.
Наиболее близким к предлагаемому способу получения шихты для силикатного стекла является патент US2013281281 [8], в котором карбонаты щелочных и щелочноземельных металлов, а также алюминийсодержащее сырье частично или полностью, в различных сочетаниях, замещаются на соответствующие гидроксиды с целью введения в расплав паров воды, образующихся при их разложении и способствующих осветлению стекломассы. Указанный способ позволяет получить стекло с улучшенным осветлением по сравнению со стеклом на обычных сырьевых материалах, однако процессы силикатообразования по указанному способу интенсифицированы незначительно. Кварцевой песок, сырьевые компоненты, содержащие карбонаты кальция и магния не подвергаются предварительной обработке, что говорит об отсутствии предварительных процессов силикатообразования и интенсивного физико-химического взаимодействия компонентов шихты до загрузки в печь, каустик вводится непосредственно в стекольную шихту, что возможно лишь частично в связи с его агрессивностью по отношению к огнеупорам и «закипанию» стекломассы при полной замене кальцинированной соды на каустик.
Прототипы сырьевых концентратов, рассмотренных выше, содержат остаточный NaOH более 5%, уменьшенное значение Na2O и наиболее существенный недостаток - обильная мошка в стекле на основе шихт с их использованием.
Указанные выше способы не решают поставленной цели изобретения - получить силикатное стекло с меньшими временными и энергозатратами без использования или уменьшенным значением осветляющих добавок по сравнению со стеклом на традиционных компонентах.
Поставленная цель достигается путем получения новых видов сырьевых концентратов для производства силикатного стекла на основе предварительной термообработки смеси традиционного кремнесодержащего материала и гидроксида шелочного металла, или смеси традиционного кремнесодержащего сырьевого материала, сырьевого материала, содержащего карбонат магния и гидроксида шелочного металла.
Использование шихты для производства силикатного стекла, по первому варианту, на основе сырьевых концентратов вышеописанного состава, с добавлением оставшихся традиционных сырьевых компонентов согласно выбранному рецепту для традиционной шихты силикатного стекла, с обязательным использованием осветляющих добавок (например, сульфата) позволяет снизить температуру варки стекла и уменьшить время гомогенизации, осветления стекломассы или уменьшить количество осветляющей добавки с равным временем гомогенизации и осветления для шихты на традиционной основе.
Использование шихты для производства силикатного стекла, по второму варианту, на основе сырьевых концентратов выше описанного состава, с заменой оставшихся традиционных сырьевых компонентов, не вошедших в состав используемого сырьевого концентрата, на соответствующие гидроксиды щелочноземельных металлов и алюминия, позволяет снизить температуру варки стекла и сократить время осветления и гомогенизации стекломассы без использования осветляющих добавок.
Под традиционными осветлителями понимаются: селитра, оксиды мышьяка (III) и сурьмы (III), диоксид церия, сульфат натрия, азотнокислый аммоний NH4NO3, сернокислый аммоний (NH4)2SO4, хлористый аммоний NH4Cl,фторид кальция CaF2, фтористые и аммонийные соли, хлористый натрий.
Под гидроксидами щелочных металлов общей формулой MOH понимаются гидроксиды: LiOH, NaOH, KOH, RbOH, CsOH, а также техногенные отходы, содержащие MOH.
Под гидроксидами щелочноземельных металлов общей формулой Me(OH)2 понимаются гидроксиды: Mg(OH)2,Ca(OH)2, а также техногенные отходы, содержащие Me(OH)2.
Под традиционными сырьевыми источниками, содержащими карбонаты щелочных металлов понимаются: природная и искусственная сода, природный и искусственный сульфат натрия, поташ, содовопоташная смесь и селитра, искусственный углекислый литий Li2CO3.
Под традиционными сырьевыми источниками, содержащими карбонаты щелочноземельных металлов понимаются: известняк, мрамор, доломит, магнезит, доломитизированный известняк, технические CaCO3 и MgCO3 , а также их пылевидные отходы.
Под сырьевыми источниками, содержащими SiO2 понимаются природные источники кристаллического кварца - кварцевые пески, горный хрусталь, горный кварц; скрытокристаллические - халцедон, агат, кремень, а также пылевидные отходы кристаллического кварца размером менее 0,1 мм.
Под алюминийсодержащими сырьевыми компонентами понимаются: технический ок-сид алюминия, полевые шпаты, пегматиты, каолины, а также отходы горнообогатительных фабрик - полевошпатовый и нефелиновый концентраты, горные породы: граниты, трахиты, вулканический пепел и др.
Проведенные исследования оптимизации технологических параметров получения сырьевого концентрата на основе кремнесодержащего сырья и гидроксида щелочного металла показали, что температура синтеза сырьевого концентрата может быть снижена по сравнению с прототипами, описанными выше, до 325°С с выдержкой при указанной температуре от 1 до 10 минут.
Продукт реакции в хорошо классифицируемом порошкообразном виде имеет объемную массу 1,22 т/м3 и выражен основными кристаллическими фазами в виде β-кварца и метасиликата натрия со следами дисиликата, каустика и Na2CO3 как продукта взаимодействия каустика и атмосферных паров воды (рис.1). Увлажнение смеси каустика и кварцесодержащего материала не требуется.
С целью поддержания заданного значения Na2O в составе ЩК опытным путем был определен поправочный коэффициент на улетучивание Na2O из смеси каустика и кварцевого песка - Кул = 1,05 для каустика в твердом виде по аналогии с расчетом рецепта шихты, например, на кальцинированной соде, равном 1,032.
Для уменьшения остаточного NaOH в состав сырьевого концентрата вводили сырьевые источники, содержащие карбонат магния. MgCO3 имеет меньшее значение температуры диссоциации по сравнению с карбонатом кальция. Разложение MgCO3 на оксид и углекислый газ начинается от 450°С, при 550°С давление насыщенных паров СО2 составляет 747 мм рт.ст. [9].
Выделяющийся в процессе разложения карбоната магния СО2 мог бы связать одну часть остаточного NaOH в ЩК до Na2CO3, другая часть NaOH вступила бы в реакцию с MgCO3 с образованием гидроксида Mg и водяных паров, дополнительно интенсифицирующих процессы силикатообразования.
Исходя из температуры разложения MgCO3, при котором давление парциальных паров углекислого газа имеет максимальное значение, термообработку смеси кварцесодержащего сырья, каустика в твердом виде и сырьевого источника содержащего MgCO3 проводили при 560 °С в течение 10 мин. Проведенные исследования показали, что при использовании в составе сырьевого концентрата традиционных сырьевых материалов, содержащего карбонат(ы) Mg или Mg и Ca, содержание остаточного NaOH в сырьевом концентрате не фиксируется методом РФА.
Фазовый состав сырьевого концентрата, имеющего объемную массу 1,33 т/м3 в составе с техническим MgCO3 и сырьевого концентрата, имеющего объемную массу 1,36 т/м3 в составе с доломитом, выражен β-кварцем, метасиликатом натрия со следами дисиликата и силикатом(ми) щелочноземельных металлов (рис.1). Сырьевой концентрат с уменьшенным значением NaOH получился в виде рассыпающегося спека, легко отделяемого от стенок тигля, в порошкообразном виде.
Интенсивное силикатообразование в виде ди- и метасиликата натрия, силикатов магния, кальция и двойных силикатов магния и кальция создает предпосылки для образования эвтектик и раннего появления жидкой фазы в шихте на основе вышерассмотренных сырьевых концентратов.
Сравнительные варки стекол на шихтах с использованием прототипа сырьевого концентрата - щелочного концентрата состава (Na2O, SiO2) и шихтах с использованием сырьевых концентратов составов (Na2O, SiO2, MgO) и (Na2O, SiO2, MgO, CaO) показали, что температура варки на прототипе сырьевого концентрата снижается до 60°С, тогда как на сырьевом концентрате, имеющем в своем составе дополнительно оксиды магния и кальция температура может быть снижена от 70 до 100°С в зависимости от состава стекла и вида сырьевого концентрата.
Использование пылевидного кварцевого сырья и отходов доломита с размерами частиц менее 0,1 мм для получения сырьевого концентрата положительно влияет на уменьшение содержание остаточного NaOH в синтезируемом продукте вследствие увеличения площади контакта реагирующих веществ, находящихся в твердой фазе и способствует более полному протеканию реакций силикатообразования.
Использование кварцевого сырья с размерами частиц менее 0,1 мм возможно по всем вариантам получения силикатного стекла с улучшенным осветлением.
Все вышеописанные виды сырьевого концентрата способны к длительному хранению (рис.2).
Пример осуществления изобретения:
Для проведения экспериментальных варок стекол на основе шихт с использованием описанных в настоящем изобретении видов сырьевых концентратов был выбран следующий состав силикатного стекла: SiO2 - 71,86; Na2O - 13,82; Al2O3 - 2,12; CaO - 10,1; MgO - 2,1.
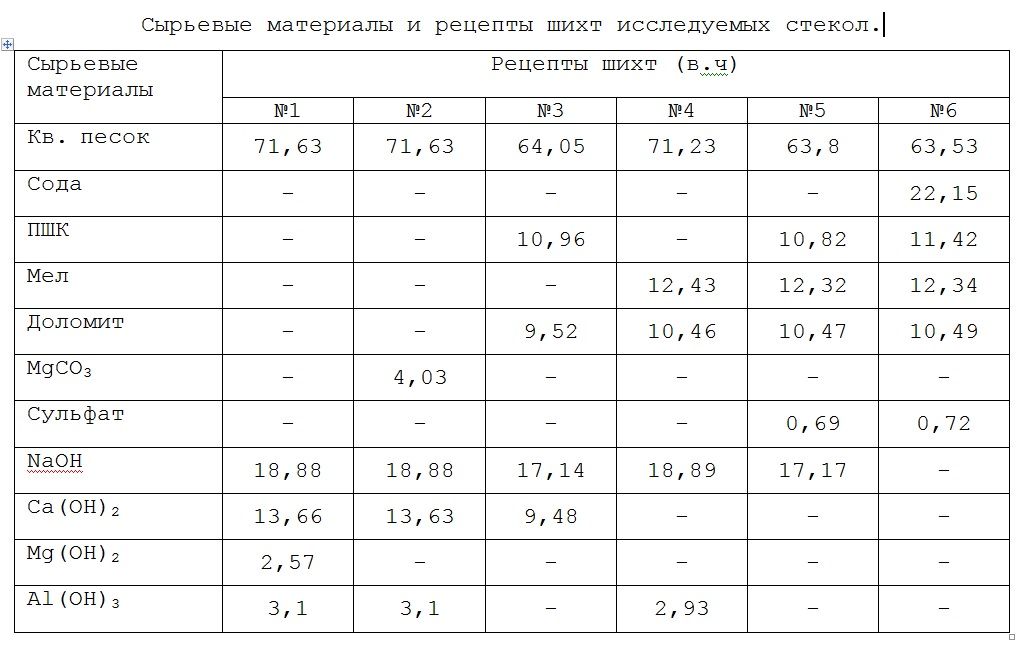
Сырьевые материалы и рецепты шихт по выбранному составу приведены в таблице.
В шихты №5, №6 в качестве осветляющей добавки вводился сульфат натрия в количестве 0,6% от веса шихты.
Сырьевые концентраты, используемые в составах №1-№5, готовились отдельно с последующим смешиванием с остальными компонентами стекольных шихт в соответствии с рецептами в таблице.
Все шихты увлажнялись 3,5% воды.
Варка проводилась в корундовых тиглях объемом 100 мл без досыпки шихты в лабораторной печи с силлитовыми нагревателями, время подъема температуры от 1300°С до максимальной температуры варки 1480°С составило 1 час, после чего печь была выключена. Для снятия термических напряжений в стекломассе температура в печи была снижена до 800°С с последующей герметизацией загрузочного отверстия.
Таблица
Охлажденные тигли разрезались на алмазном круге с последующей шлифовкой и полировкой среза. Образцы исследовались на наличие непровара, крупных и мелких пузырей, мошки (рис.3). Визуальный анализ образцов стекол показал отсутствие непровара.
Наибольшее количество пузырей как крупного, так и мелкого размера содержал образец №6 на основе традиционных материалов с добавлением сульфата в качестве осветлителя.
Наименьшее количество пузырей как крупного, так и мелкого размера содержал образец №2 на основе сырьевого концентрата, приготовленного из термообработанной смеси технического MgCO3, кварцевого песка и чешуированного каустика при 560°С с последующей выдержкой 10 мин. при достижении заданной температуры. В данной шихте оставшиеся сырьевые компоненты, не вошедшие в состав ЩК, содержащие CaO и Al2O3, заменили на Ca(OH)2 и Al(OH)3.
Минимальное содержание газовой фазы в стекле образца №2 по сравнению с остальными образцами можно объяснить оптимальным количеством выделяющихся водяных паров в расплав стекла при разложении гидроксидов и «работой» в согласованной паре. Гидроксид алюминия разлагается при температуре от 180°С, тогда как гидроксид кальция «отдает» воду от 580°С [10], что обуславливает равномерное, растянутое в процессе варки осветление.
Образец №5 сварен на основе сырьевого концентрата, полученного при термообработке смеси кварцесодержащего материала и каустика при 325 °С в течение 3 минут, с добавлением в шихту сульфата с целью осветления стекломассы и содержал меньшее количество пузырей крупного и мелкого размера по сравнению с образцом №6, сваренном на традиционных материалах, что свидетельствует о возможности уменьшения количества осветляющей добавки.
Источники информации
1. Гулоян Ю.А . Физико-химические основы технологии стекла. - Владимир : «Транзит-Икс». - 2008.- С.398-399.
2. Пат. RU2152363 России, МПК C03B1/00, C03C1/02. Сырьевой концентрат для производства стекла и керамики и способ его получения /Молчанов В.Н., Поляков В.Н., Демидов И.А. и др./ - опубл. 10.07.2000; http://www1.fips.ru/.
3. Минько Н.И., Лавров Р.В. Бессодовая технология силикатных стекол. //УДК 666.1. Сборник докладов 7-й международной конференции «Стеклопрогресс XXI». - Саратов: ООО «Буква». - 2014. - С.31-37.
4. Захаров И.С., Голубев М.Н., Шевченко О.У. Изготовление стеклянных изделий с применением заменителя соды - щелочного концентрата // Сборник научных статей Курского ГТУ. - Курск.- 2000 г. - С.55-57.
5. Заявка RU2007131721 России, МПК C03C 1/00. Щелочной концентрат для получения стекла и способ его применения с целью снижения атмосферных выбросов углекислоты и твердых составляющих шихты /Молчанов В.Н., Лавров Р.В./ - опубл. 27.02.2009; http://www1.fips.ru/.
6. Пат. RU 2107666, 27.03.1998. Голубев М.Н., Захаров И.С. Способ подготовки шихты для производства стекла//http://www1.fips.ru.
7. Пат. WO2010031834,26.10.2007. Pickbrenner Arnd. Manufacture of material on the basis of calcium-and/or magnesium carbonate having a redused decrepitation tendency // http://worldwide.espacenet.com.
8. Пат. US2013281281,24.10.2013. Dejneka Matthew. Silicate glasses having low seed concentration // http://worldwide.espacenet.com.
9. В.А Киреев. Краткий курс физической химии. Из-во химической литературы,М.-1963.- С.255.
10. Справочник химика. Основные свойства неорганических соединений / под редакцией Б.П Никольского // Издательство Л., Ленинградское отделение Издательства «Химия»,1964. - Т.2. - 1168 с.

