Результат интеллектуальной деятельности: СПОСОБ ОЧИСТКИ СТОЧНОЙ ЖИДКОСТИ ОТ ФОСФАТОВ И СУЛЬФАТОВ
Вид РИД
Изобретение
Изобретение относится к области очистки высококонцентрированных фосфор- и сульфатсодержащих сточных вод и может быть использовано для очистки городских сточных вод, а также для очистки стоков предприятий пищевой и целлюлозно-бумажной промышленности при их сбросе в водоем.
Известен способ очистки сточных вод от фосфатов (Справочник проектировщика. Канализация населенных мест и промышленных предприятий. М.: Стройиздат, 1981, с. 297-299), заключающийся в известковании сточной жидкости с повышением pH до 10,5-11, при котором возможно снижение фосфатов до ПДК (0,6 мг/л по PO4 3-).
Недостатком этого способа является низкий эффект удаления сульфатов (10-20%) и образование большого количества химического осадка, подлежащего вывозу с площадки очистных сооружений канализации (ОСК) и его размещению на полигоне твердых бытовых отходов (ТБО).
Известен также способ очистки кислых сточных вод от фосфатов и сульфатов (патент РФ №2071451, 1992 г., C02F 1/58) путем их обработки высокоактивным оксихлоридом алюминия (ОХА), активизированного фосфорной кислотой H3PO4, с последующим доведением pH до 11,5-12,5 известью. Суть активизирования ОХА фосфорной кислотой заключается в снижении pH ОХА фосфорной кислотой с 2,2-2,35 до 1,5-1,8.
Недостатком этого способа является увеличение эксплуатационных затрат на приобретение дорогостоящей фосфорной кислоты, необходимой для проведения активизирования ОХА.
Наиболее близкими по технической сущности и заявляемому способу являются способы раздельного осаждения сульфатов и фосфатов: сульфаты осаждают хлоридом бария BaCl2·2H2O (Методика технологического контроля работы очистных сооружений городской канализации. М.: Стройиздат, 1977, с. 83), а фосфаты - путем ввода в сточную жидкость одного из возможных реагентов [сернокислого железа Fe2(SO4)3, сернокислого закисного железа FeSO4, сернокислого алюминия Al2(SO4)3·18H2O или хлорного железа FeCl3·6H2O] (Справочник проектировщика. Канализация населенных мест и промышленных предприятий. М.: Стройиздат, 1981, с. 297-299).
Недостатком этого способа являются крайне медленное осаждение кристаллов BaSO4, которые по размерам близки к коллоидным частицам. Минимальная продолжительность их осаждения составляет шесть и более часов. При такой продолжительности требуется увеличение капитальных затрат на строительство дополнительного количества отстойников физико-химической очистки. Однако даже при этом нельзя гарантировать получение стабильных значений по сульфатам и фосфатам, что связано с неравномерным поступлением стоков на ОСК.
Задачами заявляемого изобретения являются:
- повысить процент удаления сульфатов и фосфатов из сточной жидкости;
- снизить количество образующегося химического осадка;
- снизить материальные затраты на реагенты за счет отказа от применения дорогостоящей фосфорной кислоты;
- ускорить процессы осаждения кристаллов BaSO4;
- сократить продолжительность отстаивания, уменьшить требуемое количество отстойников физико-химической очистки, а значит, и снизить капитальные затраты;
- создать условия для получения стабильных значений концентраций по сульфатам и фосфатам.
Поставленная задача решается тем, что в заявляемом способе очистки сточной жидкости от сульфатов и фосфатов стоки после полной биологической очистки поступают на I ступень физико-химической очистки, где в результате введения хлорного железа (FeCl3·6H2O) происходит осаждение фосфатов в виде труднорастворимой соли фосфата железа (FePO4). Для осаждения фосфатов хлорное железо вводится в камеру реакции с небольшим избытком при интенсивном перемешивании воздухом. Избыток необходим для образования крупных, хорошо оседающих кристаллов FePO4. Не связанное с фосфатами железо образует хлопья гидроксида железа Fe(OH)3, осаждающиеся и удаляемые вместе с кристаллами фосфата железа. На II ступени после предварительного подкисления сточной жидкости соляной кислотой и снижения рН с 7,2-7,6 до 4 и ввода хлорида бария (BaCl2·2H2O) в количестве 130-640 мг/л при исходной концентрации ион-сульфатов (SO4 2-), равной 150-350 мг/л, происходит осаждение сульфатов в виде труднорастворимой соли сульфата бария (BaSO4). Процесс осаждения кристаллов сульфата бария в отстойниках II ступени ускоряется за счет ввода избыточного активного ила в количестве 100-300 мг/л, который является зашламителем. Избыточный активный ил подается из сооружений биологической очистки. Химический осадок из отстойников I и II ступеней направляется на фильтр-прессы, обезвоженный химический осадок вывозится на полигон ТБО, а фильтрат с мельчайшими кристалликами BaSO4, получаемый при обезвоживании осадка, возвращается в камеру реакции II ступени. Кристаллики (зародыши и дозародыши) оказываются в фильтрате в результате их продавливания через ячейки фильтровальной ткани фильтр-пресса при обезвоживании химического осадка. Ускорение процесса осаждения сульфата бария происходит благодаря кристалликам, являющимся центрами кристаллизации.
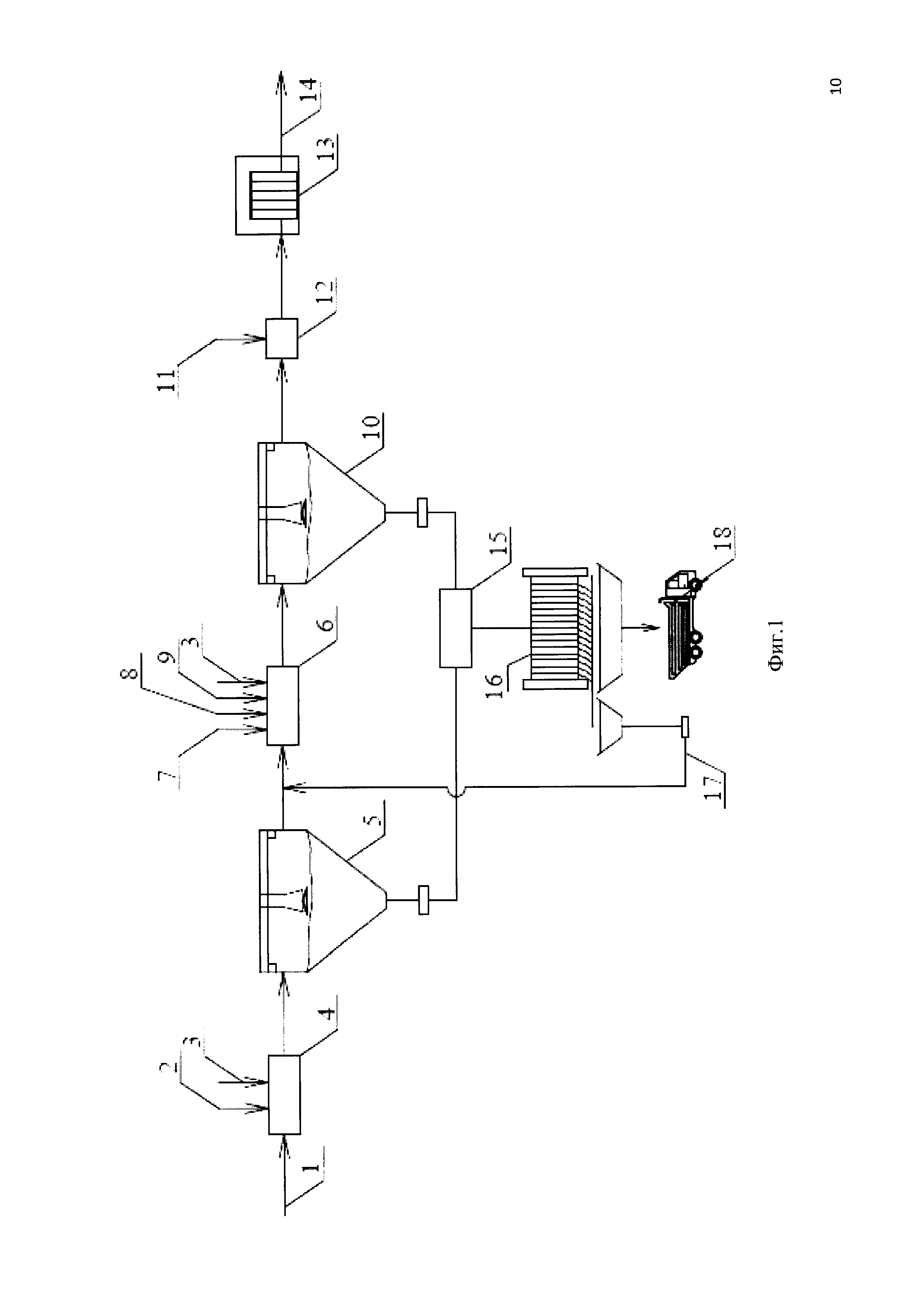
На чертеже представлена общая схема узла физико-химической очистки стоков, предназначенная для снижения сульфатов (SO4 2-) со 150-350 мг/л до 100 мг/л и фосфатов (PO4 3-) с 20-30 мг/л до 0,6 мг/л при их сбросе в водоем.
Схема узла физико-химической очистки стоков включает: подачу сточной жидкости (1) из биореактора с последующим вводом хлорида железа (2) и подачей воздуха (3) в камеру реакции I ступени (4); отстойник физико-химической очистки I ступени (5); камеру реакции II ступени (6) с вводом соляной кислоты (7), хлорида бария (8), избыточного активного ила (9); отстойник физико-химической очистки II ступени (10); ввод щелочи (11) в смеситель (12) с последующей доочисткой стоков в мембранных модулях (13) и выпуском очищенной сточной воды (14) в водоем; сборник химического осадка (15) обеих ступеней; камерный фильтр-пресс (16); возврат фильтрата (17); вывоз обезвоженного осадка (18).
Способ осуществляется следующим образом: предварительно очищенные на стадии биологической очистки стоки (1) из биореактора с содержанием сульфатов 150-350 мг/л и фосфатов 20-30 мг/л поступают в камеру реакции I ступени (4), в которую подается хлорное железо (2) FeCl3·6H2O с небольшим избытком для удаления фосфатов. Избыток реагента необходим для образования крупных, хорошо оседающих кристаллов. Применение этого реагента обосновано тем, что он позволяет сократить расход соляной кислоты на II ступени физико-химической очистки. Для перемешивания сточной жидкости с реагентом, зарождения и роста кристаллов FePO4 в камеру реакции I ступени (4) нагнетается воздух (3). Не связанное с фосфатами железо образует гидроксид железа Fe(OH)3. Из камеры реакции стоки поступают в отстойники физико-химической очистки I ступени (5), где происходит осаждение кристаллов ортофосфорной кислоты FePO4 и гидроксидов железа Fe(OH)3. Осевшие кристаллы FePO4 и гидроксида железа Fe(OH)3 удаляются из отстойников I ступени (5) в сборник химического осадка (15) и далее откачиваются в камерные фильтр-прессы (16) для обезвоживания до влажности 75%. Показатели параметров для I ступени представлены в таблице 1.
Очищенная от фосфатов сточная жидкость из отстойников I ступени (4) направляется в камеру реакции II ступени (6), куда вводится соляная кислота HCl (7) в количестве, обеспечивающем снижение pH с 7,2-7,6 до 4. Ввод соляной кислоты необходим не только для полноты химической реакции, но и получения более крупных кристаллов BaSO4. Расход соляной кислоты HCl, а следовательно, и затраты на ее приобретение в заявляемом способе сокращаются благодаря использованию хлорида железа FeCl3·6H2O на I ступени.
После подкисления сточной жидкости соляной кислотой вводится хлорид бария BaCl2·2H2O (8) в количестве 130-640 мг/л, необходимом для связывания всего введенного бария с сульфатами. Для перемешивания сточной жидкости и реагентов в камеру реакции II ступени (6) вводится воздух (3). При этом в очищенной сточной жидкости остаточные концентрации бария не будут превышать 0,74 мг/л, сульфатов 100 мг/л, хлоридов 300 мг/л.
В заявляемом способе с целью ускорения процесса осаждения кристаллов BaSO4, сокращения продолжительности отстаивания, снижения капитальных затрат и достижения стабильных результатов по сульфатам и фосфатам в камеру реакции II ступени (6) вводится избыточный активный ил (9), образующийся на стадии биологической очистки стоков. Избыточный активный ил представляет собой частицы органического происхождения, заселенные бактериями, простейшими и микроскопическими животными. Активный ил в данном случае выполняет функцию зашламителя. При этом используется его высокая способность к укрупнению мельчайших (коллоидных) частиц (в предлагаемом способе к ним относятся кристаллы BaSO4). В условиях низких значений pH=4 ил с течением времени подвергается частичной денатурации, т.е. уменьшению размеров частиц за счет увеличения их плотности. Благодаря этому такие частицы имеют еще большую скорость осаждения. Доза вводимого ила 100-300 мг/л. При введении ила в количестве менее 100 мг/л нельзя достичь требуемого эффекта осаждения кристаллов BaSO4. При введении ила более 300 мг/л будет наблюдаться повышенный вынос частиц ила с очищенной сточной жидкостью. Эти частицы, попадая в сооружения доочистки (14), приведут к быстрому засорению мембранных модулей и увеличению числа промывок, что связано с увеличением эксплуатационных затрат. При введении избыточного активного ила (9) продолжительность отстаивания сокращается с 6 часов до 1,5-2 часов.
Из камеры реакции II ступени (6) смесь сточной жидкости, реагентов и ила направляется в отстойники физико-химической очистки II ступени (10), где происходит осаждение кристаллов BaSO4 и частиц ила. Химический осадок из отстойников II ступени (10) откачивается в сборник химического осадка (15), откуда он направляется в камерные фильтр-прессы (16) на обезвоживание. Фильтрат (17) с мельчайшими кристалликами BaSO4, прошедшими при обезвоживании осадка, образующегося на II ступени очистки, возвращается в камеру реакции II ступени (6) для их использования в качестве центров кристаллизации. Обезвоженный химический осадок (18) вывозится с площадки ОСК и размещается на полигоне ТБО. Показатели параметров для II ступени представлены в таблице 2.

Примечание. 1. При сбросе сточной жидкости в рыбохозяйственный водоем первой категории предельно допустимая концентрация фосфатов не должна превышать 0,6 мг/л.
2. При сбросе очищенных стоков в городской коллектор остаточная концентрация фосфатов не должна превышать 4,2 мг/л.