СПОСОБ ПОЛУЧЕНИЯ 10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ
Вид РИД
Изобретение
Предлагаемое изобретение относится к области органической химии, конкретно, к способу получения 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов (1):
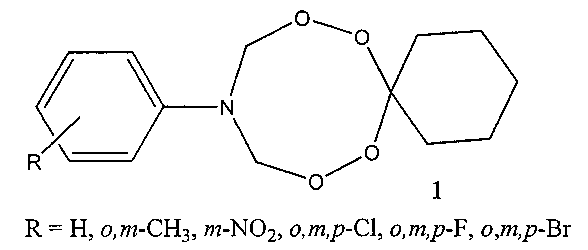
N-Содержащие тетраоксаны применяются в медицине в качестве препаратов, обладающих противомалярийной (Opsenica I., Opsenica D., Lanteri C.A., Anova L., Milhous W.K., Smith K.S., Solaja B.A. // J. Med. Chem. - 2008. - Vol. 51. - p. 2261-2266), противоопухолевой и антигельминтной активностью (Vennerstrom J.L., Arbe-Barnes S., Bran R., Chavman S.A., Chiv F.C.K. // Nature. - 2004. - Vol. 430. - p. 900-904).
Известен способ (Amewu R., Stachulski A.V., Ward S.A., Berry N.G., Bray P.G., Davies J., Labat G., Vivas L., O′Neill P.M. // Org. Biomol. Chem. - 2006 - Vol. 4 - p. 4431-4436) получения N-содержащих 7,8,15,16-тетраоксадиспирогексадеканаминов формулы (2) взаимодействием тетраоксансодержащего кетона со вторичными аминами по схеме:
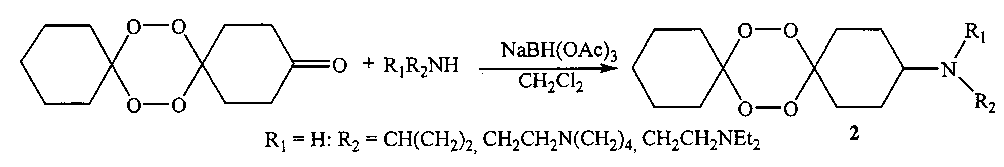
Известный способ не позволяет получать 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Известен двухстадийный метод синтеза азотсодержащего 1,2,4,5-тетраоксана (Ellis G.L., Amewu R., Sabbani S., Stocks P.A., Shone A., Stanford D., Gibbons P., Davies J., Vivas L., Charnand S., Bongard E., Hall C, Rimmer K., Lozanom S., Jesus M., Gargallo D., Ward S.A., O′Neill P.M. // J. Med. Chem. - 2008 - Vol. 51. - p. 2170-2177) формулы (3) с выходом 56% взаимодействием на первой стадии циклического азотсодержащего кетона с Н2О2 с последующей циклизацией образующегося бис-гидроксипероксида с циклоундеканоном по схеме:
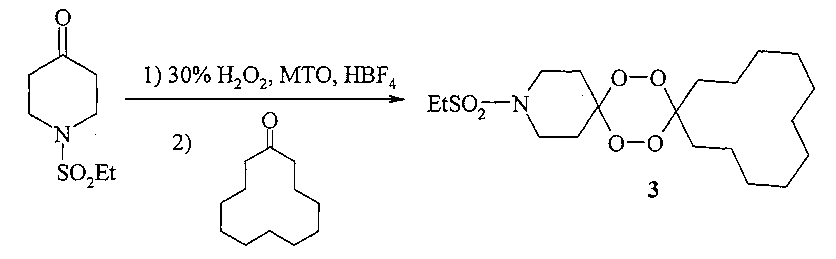
Известным способом не могут быть получены 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы общей формулы (1).
Таким образом, в литературе отсутствуют сведения о селективном получении 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов формулы (1).
Предлагается новый способ селективного получения 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов общей формулы (1).
Сущность способа заключается во взаимодействии анилинов (анилин, о,м-метиланилин, м-нитроанилин, о,-м,-n-хлоранилин, о,-м,-n-фторанилин, о-,м-,n-броманилин) с 7,8,10,12,13-пентаоксаспиро[5.7]тридеканом в присутствии катализатора Sm(NO3)3·6H2O, взятыми в мольном соотношении анилин: 7,8,10,12,13-пентаоксаспиро[5.7]тридекан: Sm(NO3)3·6H2O=10:(10-12):(0.5-0.7), предпочтительно 10:11:0.5, при комнатной температуре (20°C) и атмосферном давлении в хлористом метилене в качестве растворителя в течение 20-40 мин. Выход 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканов (1) составляет 64-98%. Реакция протекает по схеме:
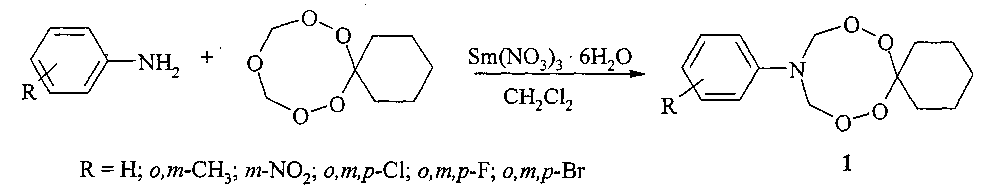
10-Арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы (1) образуются только лишь с участием анилинов (анилин, о,м-метиланилин, м-нитроанилин, о-,м-,n-хлоранилин, о,-м,-n-фторанилин, о,м-,n-броманилин) и 7,8,10,12,13-пентаоксаспиро[5.7]тридекана. В присутствии других соединений первичных аминов (например, алкиламины, гетариламины) целевые продукты (1) не образуются. Без катализатора реакция не идет.
Проведение указанной реакции в присутствии катализатора Sm(NO3)3·6H2O больше 7 мол. % не приводит к существенному увеличению выхода целевого продукта (1). Использование катализатора Sm(NO3)3·6H2O менее 3 мол. % снижает выход (1), что связано, возможно, со снижением каталитически активных центров в реакционной массе. Реакции проводили при температуре 20°C. При температуре выше 20°C (например, 60°C) снижается селективность реакции и увеличиваются энергозатраты, а при температуре ниже 20°C (например, -10°C) снижается скорость реакции. Опыты проводили в хлористом метилене, т.к. в нем хорошо растворяются исходные реагенты.
Существенные отличия предлагаемого способа:
В известном способе реакция идет с участием в качестве исходных соединений 1-(этилсульфонил)пиперидин-4-она, перекиси водорода и циклоундеканона. Способ не позволяет получать 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы (1).
В предлагаемом способе в качестве исходных реагентов применяются анилины и 7,8,10,12,13-пентаоксаспиро[5.7]тридекан, a Sm(NO3)3·6H2O применяется в каталитических количествах. В отличие от известных способов, предлагаемый способ позволяет синтезировать индивидуальные 10-арил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридеканы (1).
Способ поясняется следующими примерами:
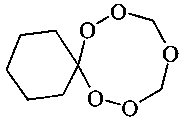
ПРИМЕР 1. Способ получения 7,8,10,12,13-пентаоксаспиро[5.7]тридекана. В сосуд Шленка, установленный на магнитной мешалке, при температуре ~20°С помещают 5 мл тетрагидрофурана, 1.46 мл (20 ммоль) водного раствора (37%) формальдегида и 1.48 г (10 ммоль) 1,1-бис(гидроперокси)циклогексана, затем добавляют 0.062 г (0.5 ммоль) Sm(NO3)2*6H2O. Реакционную смесь перемешивают при температуре ~20°С в течение 5 ч, выделяют 7,8,10,12,13-пентаоксаспиро[5.7]тридекан с выходом 95%.
ПРИМЕР 2. В сосуд Шленка, установленный на магнитной мешалке, в атмосфере аргона помещают 5 мл хлористого метилена, 0.06 г (0.5 ммоль) Sm(NO3)3·6H2O, 1.27 г (10 ммоль) о-хлоранилина, 2.09 г (11 ммоль) 7,8,10,12,13-пентаоксаспиро[5.7]тридекана. Реакционную смесь перемешивают при комнатной температуре (~20°С) в течение 30 мин. Из реакционной массы выделяют 10-(о-хлорфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекан с выходом 69%.
Другие примеры, подтверждающие способ, приведены в табл. 1.
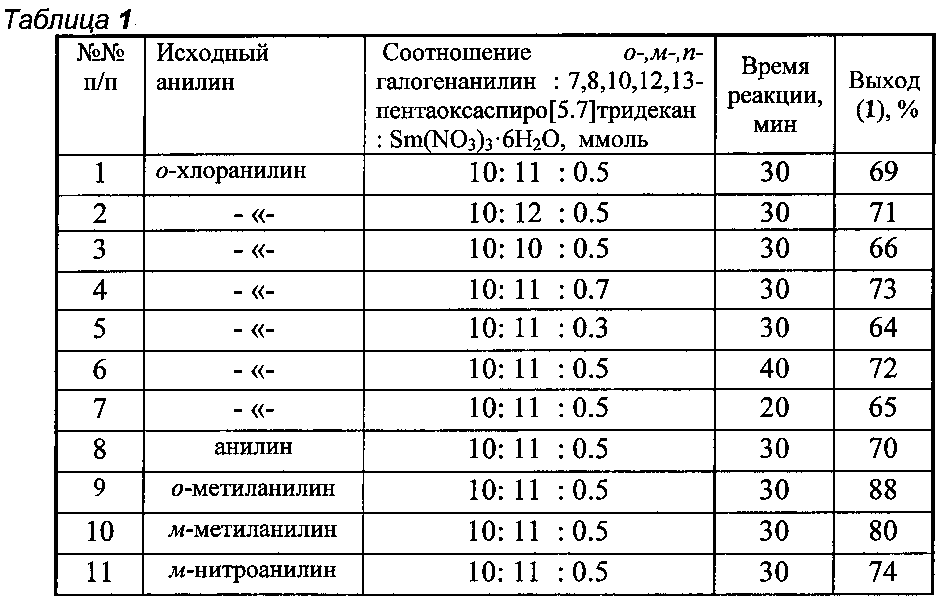
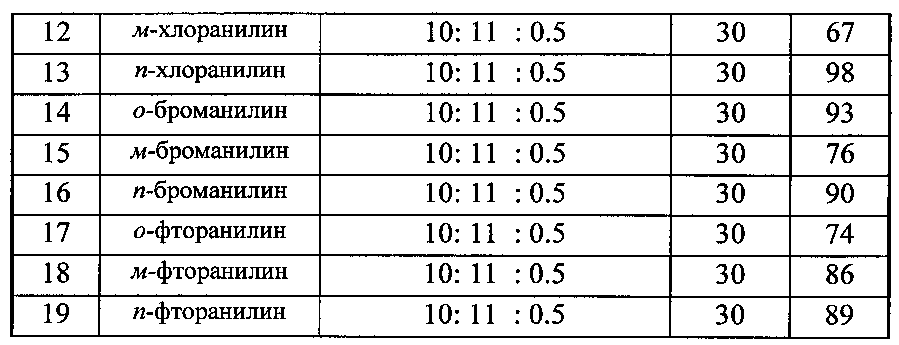
Все опыты проводили в хлористом метилене при комнатной температуре (~20°С).
Спектральные характеристики 7,8,10,12,13-пентаоксаспиро[5.7]тридекана: δН (400 MHz, CDCl3, 25°С) 1.43-1.44 (m, 4Н, Н2С), 1.54-1.55 (m, 2Н, Н2С), 1.76-1.83 (m, 4Н, Н2С), 5.17 (d, 4Н, J 12 Hz, ОН2СО); δC (100 MHz, CDCl3, 25°С) 22.35 (CH2CH2), 25.18 (СН2), 29.98 (CH2CH2), 92.30 (OCH2O), 109.98 (С). MALDI TOF, m/z: 212.387 [M+Na-H]+ (55%), m/z: 250.318 [M+Na+K-2H]+ (19%).
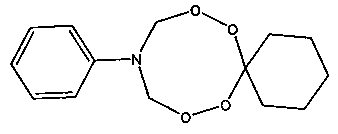
Спектральные характеристики 10-фенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.41-1.44 (м, 3Н, H2C); 1.54-1.69 (м, 2Н, H2C); 5.20 (д, 4Н, J=10 Гц, H2C); 6.99-7.33 (м, 4Н, НС). Спектр ЯМР 13C (δ, м.д., J/Гц): 22.98, 25.70, 30.62, 87.99, 109.00, 113.56, 117.15, 120.40, 129.32, 141.25.
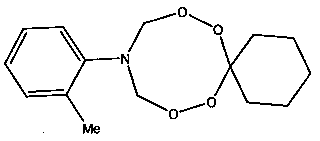
Спектральные характеристики 10-о-метилфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1H (δ, м.д., DMSO-d6, J/Гц): 1.30-1.38
(м, 3Н, Н2С); 1.64-1.65 (м, 2Н, Н2С); 5.15 (д, 4Н, J=10 Гц, Н2С); 6.64-6.86 (м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.44, 25.32, 30.54, 55.86, 78.66, 110.85, 111.42, 118.10, 121.31, 135.84, 146.91.
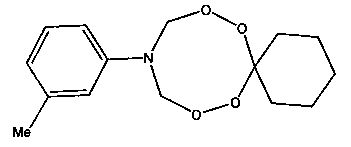
Спектральные характеристики 10-м-метилфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.34-1.42 (м, 3Н, Н2С); 1.68-1.69 (м, 2Н, Н2С); 5.10 (д, 4Н, J=10 Гц, Н2С); 6.62-7.10 (м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.51, 25.34, 30.62, 56.17, 78.92, 110.77, 114.07, 118.91, 129.16, 138.32, 146.78.
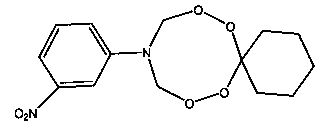
Спектральные характеристики 10-м-нитрофенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.34-1.42 (м, 3Н, Н2С); 1.68-1.69 (м, 2Н, Н2С); 5.13 (д, 4Н, J=10 Гц, H2C); 7.71-7.49 (м, 4Н, НС). Спектр ЯМР 13C (δ, м.д., J/Гц): 22.62, 24.92, 29.49, 78.55, 106.47, 111.11, 114.07, 119.34, 130.45, 138.32, 148.94.
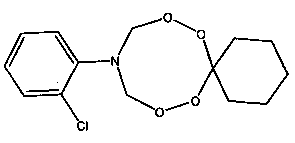
Спектральные характеристики 10-(о-хлорфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.32-1.40 (м, 3Н, Н2С); 1.68-1.76 (м, 2Н, Н2С); 5.25 (д, 4Н, J=10 Гц, Н2С); 6.60 (т, 1H, J=10 Гц НС); 6.69 (т, 1Н, J=10 Гц НС); 7.13 (т, 1Н, J=10 Гц НС); 7.27 (д, 1Н, J=10 Гц НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.46, 25.33, 30.54, 78.38, 109.35, 113.44, 119.02, 128.18, 129.42, 142.64.
Спектральные характеристики 10-м-хлорфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.32-1.40 (м, 3Н, Н2С); 1.67-1.69 (м, 2Н, Н2С); 5.12 (д, 4Н, J=10 Гц, Н2С); 6.56-70.22 (м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.44, 25.30, 30.57, 78.44, 112.27, 112.94, 116.92, 130.81, 134.03, 148.54.
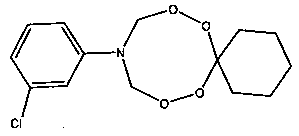
Спектральные характеристики 10-(n-хлорфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1H (δ, м.д., CDCl3, J/Гц): 1.43-1.53 (м, 3H, Н2С); 1.69-1.76 (м, 2Н, Н2С); 5.29 (с, 4Н, Н2С); 6.95-7.42 (м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.46, 25.29, 30.57, 78.68, 109.21, 115.64, 128.95, 145.85.
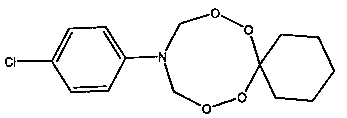
Спектральные характеристики 10-о-бромфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.30-1.39 (м, 3Н, Н2С); 1.66-1.73 (м, 2Н, Н2С); 5.23 (д, 4Н, J=10 Гц, Н2С); 6.41 (т, 1Н, J=10 Гц НС); 6.63 (т, 1Н, J=10 Гц НС); 7.03 (д, 1H, J=10 Гц НС); 7.17 (т, 1Н, J=10 Гц НС). Спектр ЯМР 13C (δ, м.д., J/Гц): 22.45, 25.31, 30.51, 78.48, 109.17, 113.62, 119.67, 128.84, 132.74, 143.60.
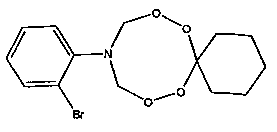
Спектральные характеристики 10-(м-бромфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.33-1.40 (м, 3Н, Н2С); 1.63-1.67 (м, 2Н, Н2С); 5.11 (д, 4Н, J=10 Гц, Н2С); 6.65-7.20
(м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.44, 25.28, 30.55, 78.41, 112.07, 114.85, 120.45, 122.82, 131.09, 149.64.
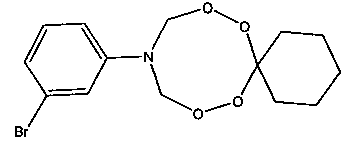
Спектральные характеристики 10-n-бромфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.33-1.40 (м, 3Н, Н2С); 1.65-1.73 (м, 2Н, Н2С); 5.09 (д, 4Н, J=10 Гц, Н2С); 6.74 (д, 2Н, J=10 Гц, НС); 7.23 (д, 2Н, J=10 Гц, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.47, 25.30, 30.57, 78.60, 107.29, 115.50, 131.86, 146.24.
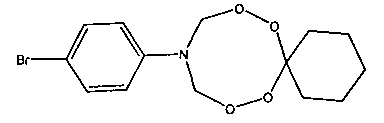
Спектральные характеристики 10-(о-фторфенил)-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.33-1.40 (м, 3Н, Н2С); 1.67-1.68 (м, 2Н, Н2С); 5.12 (д, 4Н, J=10 Гц, Н2С); 6.40-6.49 (м, 2Н, НС); 7.06-7.23 (м, 2Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.43; 25.29; 30.57; 78.52; 99.90, 100.10 (J=25 Гц); 104.09, 104.26 (J=21 Гц); 109.25, 109.75 (J=62 Гц); 130.69; 149.13; 162.76, 164.66 (J=237 Гц).
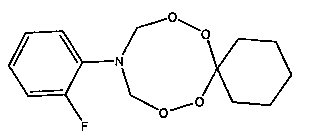
Спектральные характеристики 10-м-фторфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.33-1.40 (м, 3Н, Н2С); 1.66-1.67 (м, 2Н, Н2С); 5.11 (д, 4Н, J=10 Гц, Н2С); 6.40-6.59 (м, 2Н, НС); 7.07-7.21 (м, 2Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.43; 25.28; 30.56; 78.52; 99.88, 100.13 (J=25 Гц); 104.08, 104.29 (J=21 Гц); 109.27, 109.75 (J=48 Гц); 130.69; 149.12; 162.51, 164.90 (J=239 Гц).
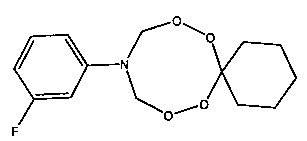
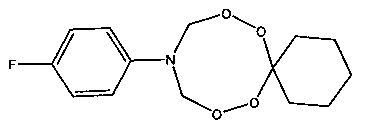
Спектральные характеристики 10-n-фторфенил-7,8,12,13-тетраокса-10-азаспиро[5.7]тридекана: Спектр ЯМР 1Н (δ, м.д., DMSO-d6, J/Гц): 1.33-1.40 (м, 3Н, Н2С); 1.66-1.67 (м, 2Н, Н2С); 5.09 (д, 4Н, J=10 Гц, Н2С); 6.73-7.07 (м, 4Н, НС). Спектр ЯМР 13С (δ, м.д., J/Гц): 22.48; 25.31; 30.60; 79.23; 99.88, 100.13 (J=25 Гц); 115.58, 115.76 (J=22 Гц); 145.51; 154.75, 156.60 (J=231 Гц).
![СПОСОБ ПОЛУЧЕНИЯ 10-АРИЛ-7,8,12,13-ТЕТРАОКСА-10-АЗАСПИРО[5.7]ТРИДЕКАНОВ](https://fips.edrid.ru/images/rid/f5/c8/55/95181c6a2adec6dc2c7a2a6e05dd511a.png)

