Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ КОМПОЗИЦИИ НА ОСНОВЕ МОДИФИЦИРОВАННОГО ГИАЛУРОНАТА НАТРИЯ, КОМПОЗИЦИЯ НА ОСНОВЕ МОДИФИЦИРОВАННОГО ГИАЛУРОНАТА НАТРИЯ И ЕЕ ПРИМЕНЕНИЕ
Вид РИД
Изобретение
Настоящее изобретение относится к области химико-фармацевтической промышленности, биотехнологии и медицины, а именно к способу получения композиции на основе модифицированного гиалуроната натрия и ее применению в различных областях медицины, ветеринарии и косметологии.
Сущность изобретения состоит в способе получения композиции на основе модифицированного сополимера гиалуроната натрия и гепарина, заключающемся в создании поперечных ковалентных связей между гидроксильными группами остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамина, входящих в состав гиалуроната натрия, и остатков α-D-глюкозамина и уроновой кислоты, относящихся к гепарину, посредством введения активного сшивающего бифункционального агента -(полиэтиленгликоль)диглицидилового эфира (ПЭГДЭ) в щелочной среде. После процесса химической сополимеризации реакцию со сшивающим агентом останавливают. Полученную реакционную смесь нейтрализуют до рН 7,0, затем подвергают тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм, концентрируют и перемешивают до полной гомогенизации.
В качестве исходного сырья используют гиалуронат натрия неживотного происхождения фармакопейной чистоты, подвергнутый тангенциальной фильтрации для избавления от низкомолекулярных фрагментов, способных инициировать воспалительный ответ.
Биосовместимость, биодеградируемость и неиммуногенность композиции на основе модифицированного гиалуроната натрия позволяют применять ее в разных областях медицины и ветеринарии, в т.ч. хирургии и эндопротезировании, ортопедии, травматологии, офтальмологии, дерматологии, эстетической медицине и косметологии.
Описание изобретения
Область техники, к которой относится изобретение
Изобретение относится к области химико-фармацевтической промышленности, биотехнологии и медицины, а именно, к способу получения композиции на основе модифицированного гиалуроната натрия и ее применению в различных областях медицины, ветеринарии и косметологии.
Уровень техники
В настоящее время полисахариды широко используются в разных областях медицины, ветеринарии и косметологии, поскольку обладают такими важными характеристиками, как биосовместимость, неиммуногенность и биодеградируемость.
Основным компонентом предлагаемой композиции является полисахарид гиалуронан, относящийся к группе несульфатированных гликозаминогликанов. Он является одним из основных компонентов внеклеточного матрикса, входит в состав соединительной, эпителиальной и нервной тканей, содержится во многих биологических жидкостях (синовиальной жидкости, слюне и др.), продуцируется некоторыми бактериями в составе внешней полисахаридной капсулы (например, Streptococcus, Pasteurella). С эволюционной точки зрения гиалуронан является консервативной молекулой и обнаруживается у всех позвоночных.
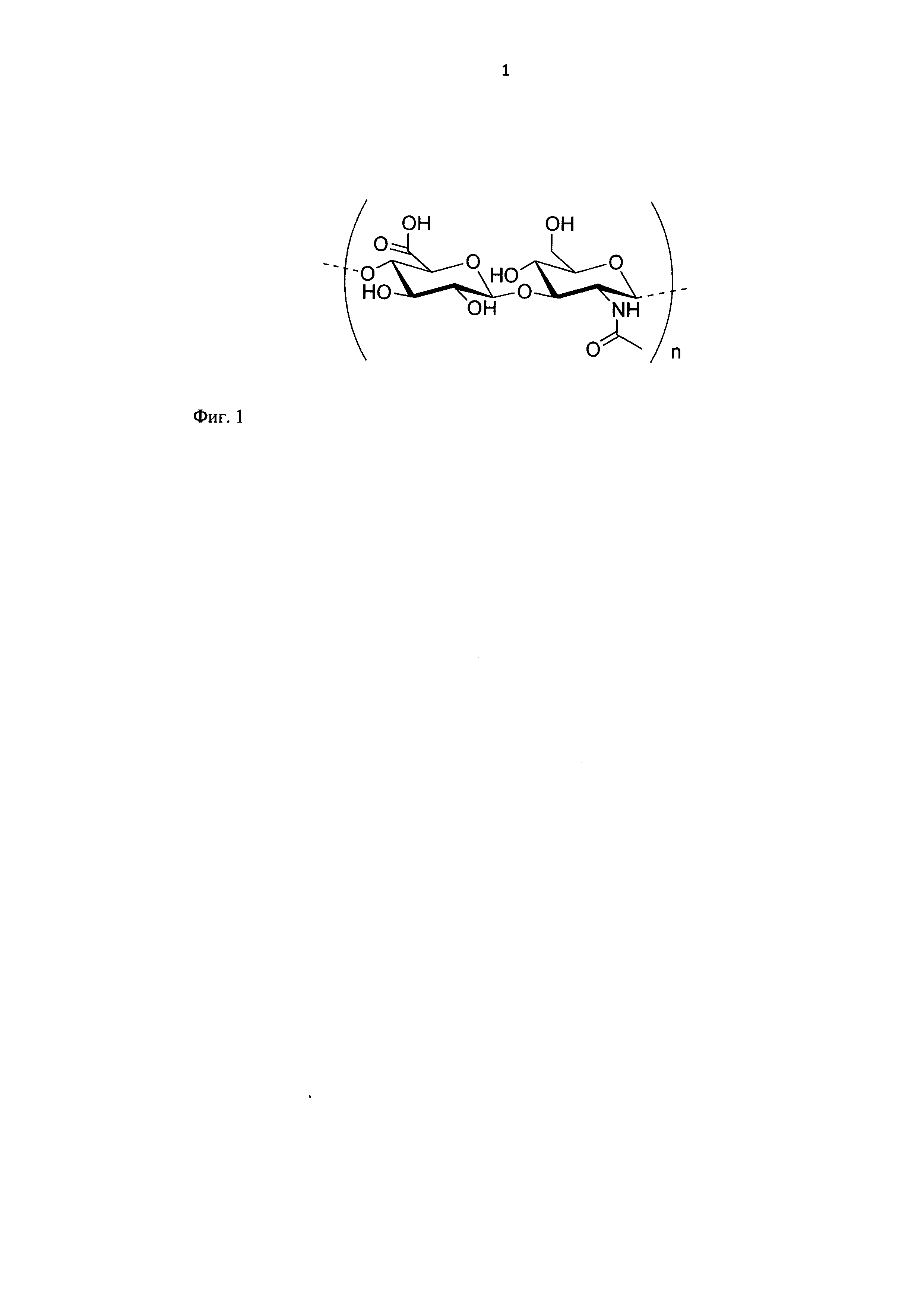
По химическому строению выделенный из различных источников гиалуронан идентичен - это полианионный, линейный гетерополисахарид, построенный из регулярно чередующихся остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамина, соединенных β-1,3- и β-1,4-гликозидными связями (Фиг. 1). Число дисахаридных повторов, образующих одну молекулу гиалуронана, варьирует в зависимости от источника, процедуры выделения и метода определения. Природный гиалуронан имеет молекулярную массу от нескольких сотен дальтон до десяти млн дальтон (в среднем - 1-2 млн Да).
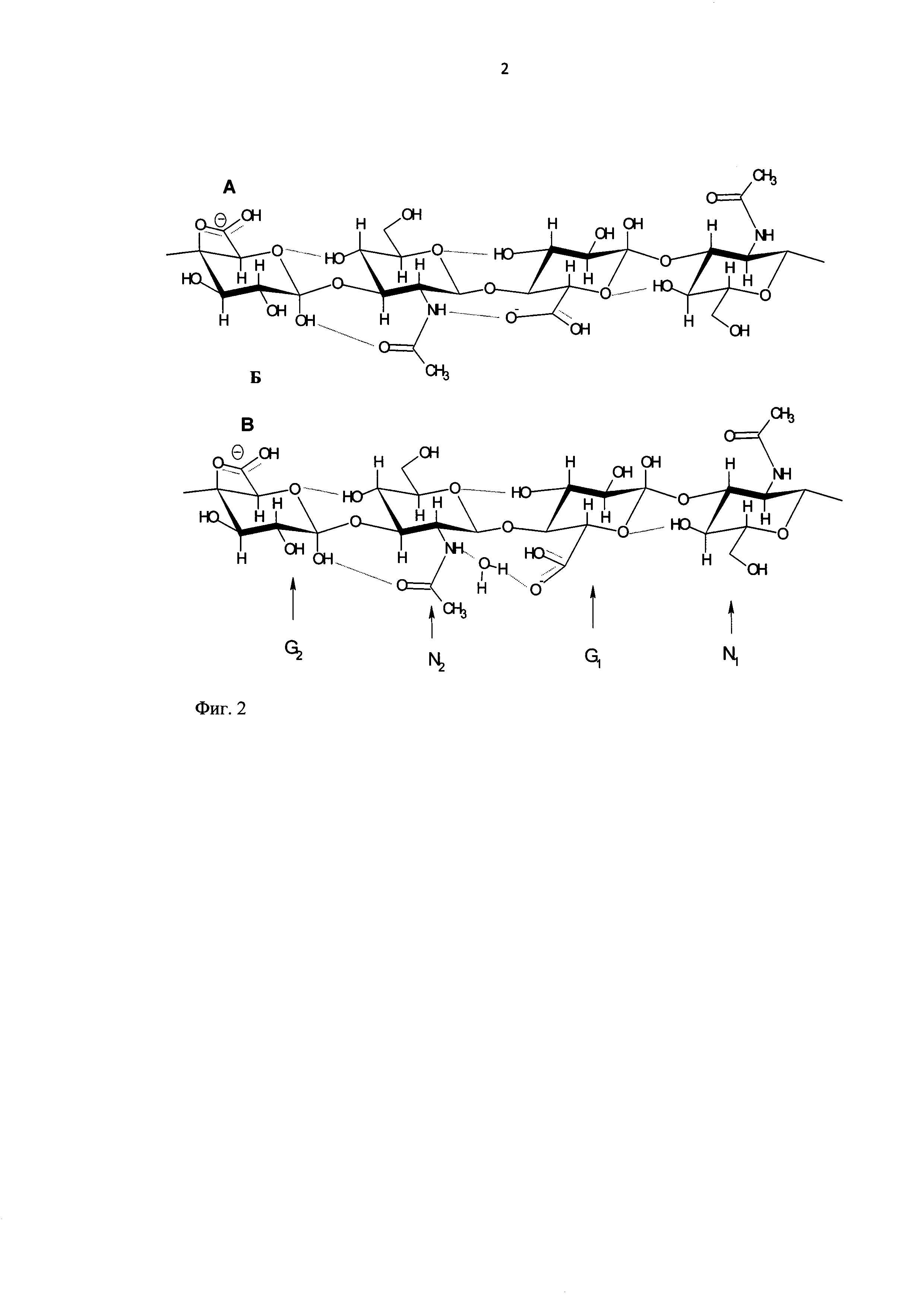
Молекула гиалуронана обладает большим количеством водородных связей, формирующихся как внутри макромолекулы между соседними углеводными остатками, так и между соседними молекулами, а в водном растворе еще и с молекулами воды (Фиг. 2). Образующаяся структура энергетически стабильна [1] и может существовать в разнообразных конформационных состояниях (вытянутые цепи, расслабленные спирали, стержневидные структуры и др.). Цепи гиалуронана, взаимодействуя друг с другом, формируют фибриллы, сети, стопки [2].
В физиологических условиях (рН ≈ 7) карбоксильные группы гиалуронана диссоциированы, и молекула полимера обладает отрицательным зарядом высокой плотности, притягивающим массу осмотически активных катионов щелочных металлов, магния, кальция и др., благодаря чему одна молекула гиалуронана может связывать огромное количество воды (до 1000 раз больше собственного веса). Принимая расширенные конформации, занимающие большой объем относительно своей массы, гиалуронан даже при очень низких концентрациях образует высоковязкие водные растворы, а при относительно высоких концентрациях (1-4 мас.%) - псевдогели, растворы колоссальной вязкости. Уже при небольших концентрациях гиалуронана происходит межмолекулярное взаимодействие и структурирование - формируется межмолекулярная трехмерная ячеистая сетчатая структура, которая и обусловливает уникальные свойства гиалуронана [3].
Образуемые в биополимерах поперечные сшивки разделяют на физические (образованные в результате электростатического взаимодействия или водородных связей) и химические (ковалентные связи). Плотность поперечных сшивок напрямую влияет на фундаментальные свойства гидрогелей, такие как степень набухания, механическая прочность и эластичность, проницаемость, диффузионные характеристики [4].
Большим недостатком применения нативного гиалуронана является нестабильность препаратов in vivo по причине быстрой деградации гиалуронидазами и свободными радикалами, в результате которой уменьшается молекулярная масса гиалуронана и изменяются его вязко-эластичные свойства и физические характеристики. Поэтому крайне актуальной задачей является создание более стабильных форм гиалуронана. Одним из подходов к этой проблеме является ковалентное перекрестное сшивание гиалуронана, осуществляемое с помощью различных реагентов, например, карбодиимидов (US 7879818, US 20070224277), дивинилсульфона (US 4582865, US 4605601, US 4636524, ЕР 0939086), полифункциональных эпоксидов (US 4716224, US 4772419, US 4716154), в т.ч. 1,4-бутандиолдиглицидилового эфира (WO 2013021249, US 4716224), полиспиртов (US 4957744), альдегидов (US 4713448, US 5128326, US 4582865), бискарбодиимидов (US 5356883), поликарбоновых кислот (ЕР 0718312), комплекса О-ацил-О′-алкил карбонат-замещенного пиридина (ЕР 2408823), олиго- или полипептида (ЕР 2094736), полифункционального азиридина (US 20050222081).
Преимуществами перекрестно-сшитых форм гиалуроната натрия являются большая стабильность по сравнению с неперешитым гиалуронаном вследствие меньшей площади поверхности, доступной для энзиматической деградации, и, следовательно, пролонгированное пребывание в месте введения in vivo (до нескольких месяцев или даже лет), улучшенные вязко-эластичные свойства.
Кроме того, для многих сшивающих агентов необходимо использование в избыточных количествах, что затрудняет прогнозирование степени сшивания гиалуроната натрия и его последующей очистки. Некоторые сшивающие агенты, например, карбодиимиды и альдегиды, являются токсичными, и присутствие даже следовых количеств сшивающих агентов в композициях для медицинского применения недопустимо.
На основании анализа литературных данных и экспериментов по определению токсического действия на животных моделях в качестве бифункционального сшивающего агента для модификации гиалуроната натрия был выбран (полиэтиленгликоль)диглицидиловый эфир (ПЭГДЭ) - широко используемый в фармакологии, недорогой, простой в использовании, высокоэффективный и безопасный реагент, в малых количествах не оказывающий токсического действия на организм человека и животных. Запатентованных аналогов методики не обнаружено.
Дополнительным аспектом применения изобретения является возможность использования перекрестно-сшитого гиалуроната натрия в качестве средства доставки и депо для дополнительных лекарственных компонентов, например, факторов роста. Гиалуронан может удерживать белковые факторы исключительно за счет слабых неспецифических электростатических взаимодействий. Добиться линейной кинетики высвобождения фактора роста представляется маловозможным. Поэтому в качестве дополнительного компонента в состав предлагаемой композиции включен гепарин, поскольку он способен удерживать белковые факторы за счет прочных аффинных взаимодействий, что повышает их стабильность in vivo и позволяет добиться линейной кинетики высвобождения ростовых факторов.
Гепарин - сульфатированный внутриклеточный гликозаминогликан, молекула которого представлена несколькими полисахаридными цепями, связанными с общим белковым ядром. Полисахаридные цепи гепарина состоят из соединенных 1,4-гликозидными связями повторяющихся дисахаридов - α-D-глюкозамина и уроновой кислоты. Белковое ядро состоит в основном из остатков серина и глицина; приблизительно две трети сериновых остатков связано с полисахаридными цепями. Благодаря наличию значительного количества отрицательно заряженных сульфатных и карбоксильных групп молекула гепарина представляет собой сильный природный полианион, способный к образованию комплексов со многими белковыми и синтетическими соединениями поликатионной природы, несущими суммарный положительный заряд.
Таким образом, сополимеризация гиалуроната натрия с гепарином дает возможность использования заявленной композиции не только в качестве терапевтического агента, но и в качестве биополимерного носителя для направленной доставки (к конкретному пораженному органу/ткани) и контролируемого пролонгированного высвобождения дополнительных биологически активных и лекарственных компонентов, в т.ч. белковой природы.
Раскрытие изобретения
Описывается способ получения модифицированного сополимера гиалуроната и гепарина, заключающийся в создании поперечных ковалентных связей между гидроксильными группами остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамина, входящих в состав гиалуроната натрия, и остатков α-D-глюкозамина и уроновой кислоты, относящихся к гепарину, посредством введения активного сшивающего бифункционального агента - (полиэтиленгликоль)диглицидилового эфира (ПЭГДЭ) в щелочной среде (Фиг. 3). После процесса химической сополимеризации реакцию со сшивающим агентом останавливают. Полученную реакционную смесь нейтрализуют до показателя рН 7, затем подвергают тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм.
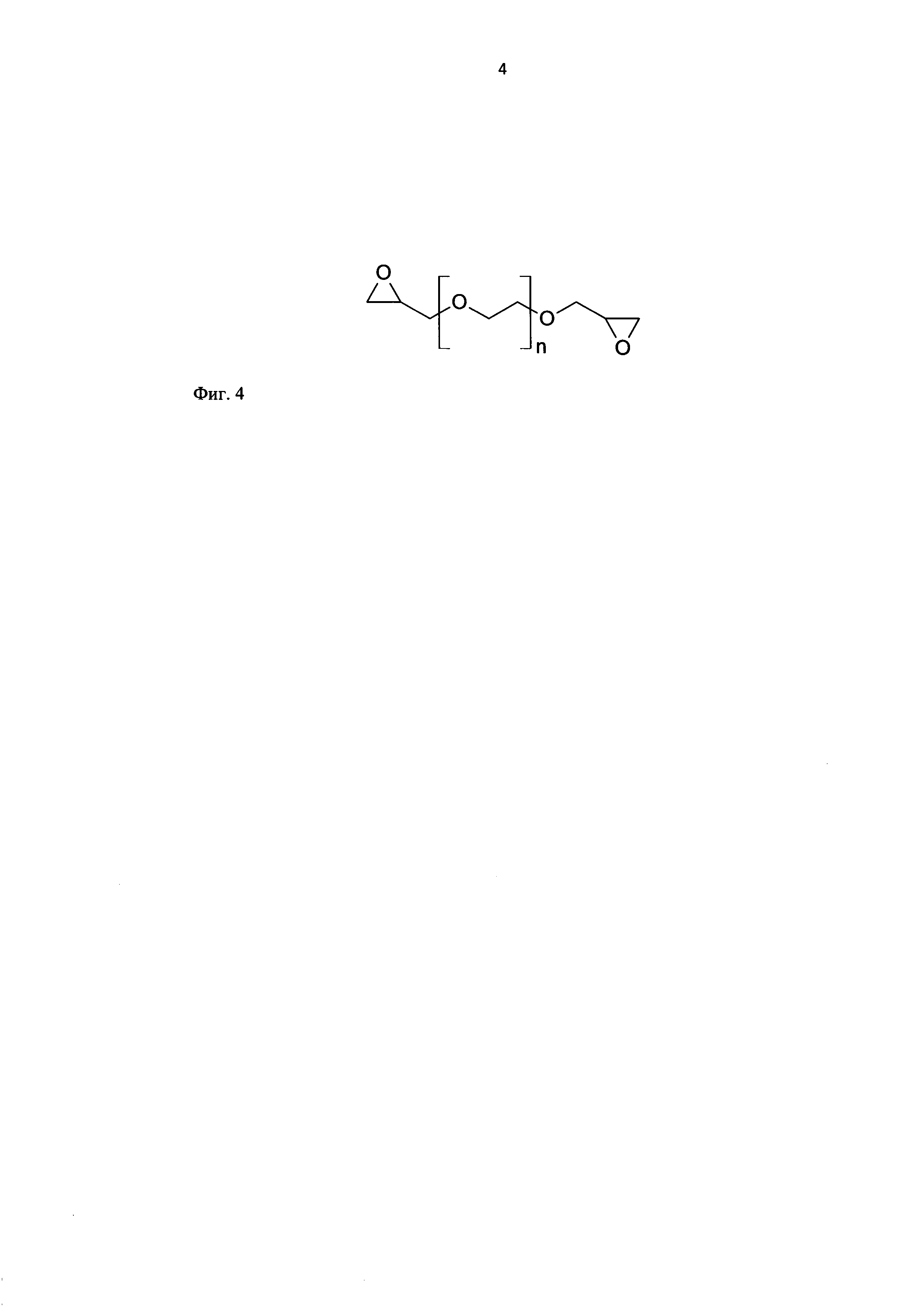
(Полиэтиленгликоль)диглицидиловый эфир - недорогой, простой в использовании, безопасный сшивающий агент, активно применяющийся в фармацевтике ввиду отсутствия токсического воздействия на организм; формула - С3Н5О2-(C2H4O)n-С3Н5О (Фиг. 4), где мономером является молекула этиленгликоля, средняя молярная масса - 526 г/моль.
Исходным сырьем может быть гиалуронат натрия с любой молекулярной массой (предпочтительно - 10-200 кДа), подвергнутый процедуре тангенциальной фильтрации для дополнительной очистки и избавления от низкомолекулярных фрагментов, способных инициировать воспалительный ответ. Далее гиалуронат натрия растворяют в растворе гидроксида натрия - это необходимо для реакции с ПЭГДЭ и уменьшения вязкости раствора, что облегчает механическое перемешивание и гомогенизацию реакционного раствора.
Сшивающий бифункциональный агент ПЭГДЭ добавляют к раствору гиалуроната натрия и гепарина, поддерживая температуру от 0 до 30°С. Время реакции находится в пределах 18-24 ч на каждой стадии. ПЭГДЭ взаимодействует с гидроксильными группами гиалуроната натрия и гепарина преимущественно в 6-м положении гликозидного остова при щелочном рН. Полученный сополимер характеризуется наличием сульфатированных групп и прогнозируемыми характеристиками.
Важным преимуществом изобретения является возможность регулирования как степени сополимеризации гиалуроната натрия с гепарином, так и степени поперечного сшивания гиалуроната натрия путем изменения количества сшивающего агента, добавляемого в реакционную смесь, что позволяет получать широкий ряд производных гиалуронана, отличающихся своими характеристиками, такими как вязкоупругие свойства, механическая прочность и проч., под конкретные медицинские, ветеринарные и косметологические задачи.
Желаемая степень поперечного ковалентного сшивания (процент гидроксильных групп, участвующих в поперечном сшивании) является полностью воспроизводимой, что подтверждается данными ЯМР. Следовательно, композиции на основе модифицированного гиалуроната натрия, полученные по одним и тем же протоколам, обладают постоянными физико-химическими характеристиками.
Еще одним преимуществом, обеспечиваемым настоящим изобретением, является возможность включения в состав композиции на основе гиалуроната натрия дополнительных компонентов, в т.ч. белковой природы, для адресной доставки к поврежденному органу/ткани и контролируемого пролонгированного высвобождения. Например, такими дополнительными компонентами могут являться костные морфогенетические белки (bone morphogenetic proteins, BMP), используемые для направленной регенерации костной и хрящевой тканей в ортопедии и травматологии [5]. В составе композиции сополимера гиалуроната натрия и гепарина BMP могут быть доставлены непосредственно в пораженный остеоартрозом сустав и, высвобождаясь в течение длительного времени, способствовать направленной регенерации гиалинового хряща и костной ткани, подверженных деструктивным изменениям. Возможность использования гидрогеля гиалуроновой кислоты с гепарином для контролируемой доставки костного морфогенетического белка ВМР-2 показана в работах Хи с соавт.[6] и Bhakta с соавт. [7].
Дополнительным преимуществом, обеспечиваемым настоящим изобретением, является возможность стерилизации композиций на основе производных поперечно сшитого гиалуроната натрия (например, термическая стерилизация до 120°С или газовая стерилизация окисью этилена) без изменения технологических свойств.
Композиция на основе модифицированного гиалуроната натрия по изобретению является биосовместимой, неиммуногенной, устойчивой к деградации ферментами, что позволяет использовать ее в различных областях медицины, ветеринарии и косметологии:
1) в ревматологии, ортопедии и травматологии в качестве средства для внутрисуставного введения пролонгированного действия при терапии остеоартрозов дегенеративно-дистрофического и травматического генеза различной локализации (главным образом, крупных синовиальных суставов - коленного и тазобедренного), а также в военной и ортопедической хирургии и спортивной медицине в качестве средства для восстановления работоспособности суставов, в частности после травм различного генеза и при повышенных нагрузках;
2) в офтальмологии в составе глазных капель для терапии синдрома «сухого глаза», при хирургическом лечении офтальмологических заболеваний, травм глаза, повреждений роговицы в качестве вископротектора, протектора клеток эндотелия при операциях;
3) в ветеринарии в качестве средства для лечения неинфекционных артритов синовиальных суставов, а также для восстановления работоспособности суставов после травм и при повышенных нагрузках, например, у скаковых лошадей;
4) в качестве биополимерного носителя для направленной доставки (к конкретному пораженному органу/ткани) и контролируемого пролонгированного высвобождения дополнительных биологически активных и лекарственных компонентов, в т.ч. белковой природы;
5) в эстетической медицине в качестве внутридермальных микроимплантатов, инъекционных препаратов, заполняющего материала в пластической хирургии и инструментальной косметологии для эстетической коррекции и эндопротезирования проблемных зон;
6) в косметологии в качестве увлажняющих агентов, основ для различных косметологических композиций по уходу за кожей: кремов, гелей, губной помады, лосьонов и прочих средств.
Краткое описание графических изображений:
Фиг. 1. Структурная формула дисахаридного звена молекулы гиалуронана.
Фиг. 2. Структурная формула тетрасахаридного участка молекулы гиалуроновой кислоты, состоящего из двух повторяющихся дисахаридных единиц: А - в отсутствие водного окружения, Б - в наиболее энергетически выгодной конформации (в водном окружении) (по Scott J.E. [2] с изменениями).
Фиг. 3. Химическая схема модификации гиалуроната натрия с помощью ПЭГДЭ.
Фиг. 4. Структурная формула сшивающего агента ПЭГДЭ.
Осуществление изобретения
Задачей настоящего изобретения является получение композиции на основе модифицированного сополимера гиалуроната натрия и гепарина посредством введения активного сшивающего бифункционального агента - (полиэтиленгликоль) диглицидилового эфира (ПЭГДЭ) в щелочной среде.
Реализацию изобретения рассмотрим на характерных примерах.
Пример 1.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 30 мг гиалуроната натрия, затем добавляли 200 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 750 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 24 ч при перемешивании (160 об/мин, +5°С).
Реакцию останавливали добавлением 3 мл метанола и оставляли перемешиваться в течение 10 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 500 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл.
Концентрацию гиалуроната натрия определяли по следующей методике. Взвешивали последовательно пять полипропиленовых пробирок объемом 1,5 мл на аналитических весах, записывали их вес. В каждую пробирку помещали по 50 мкл геля, центрифугировали пробирки на центрифугевортексе в течение 20 с при 2800 об/мин. Пробирки помещали в термостат и выдерживали их при 90°С в течение 20 мин с открытыми крышками. Каждую пробирку с высушенными образцами взвешивали на аналитических весах, вычитали из полученного значения вес соответствующей пустой пробирки, определяли среднее арифметическое значение массы сухого остатка по пяти образцам. Масса сухого остатка в образце должна составлять (1,4±0,2) мг, что соответствует концентрации гиалуроната натрия 20 мг/мл.
Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 2.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 25 мг гиалуроната натрия, затем добавляли 250 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +20°С (200 об/мин). Затем к реакционной смеси добавляли 400 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 18 ч при перемешивании (160 об/мин). Затем к смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего добавляли еще 400 мкл ПЭГДЭ. Реакционную смесь оставляли перемешиваться в течение 24 ч при +20°С (160 об/мин).
Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще 10 ч при +10°С (30 об./мин). Полученный гель переносили в колбу на 500 мл, добавляли 425 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 продолжали концентрирование геля до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 3.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 25 мг гиалуроната натрия, затем добавляли 250 мкл 10%-ного гепарина. Смесь оставили перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 756 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 24 ч при перемешивании (160 об/мин).
Реакцию останавливали добавлением 3 мл метанола и оставляли перемешиваться еще в течение 10 ч при +10°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 500 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 4.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 25 мг гиалуроната натрия, затем добавляли 250 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 577 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 18 ч при перемешивании (160 об/мин). Затем к смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего вносили еще 577 мкл ПЭГДЭ. Реакционную смесь оставляли перемешиваться в течение 24 ч при +15°С (160 об/мин).
Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще в течение 10 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 425 мл ddH2O и нейтрализовывали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 5.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 50 мг гиалуроната натрия, затем добавляли 100 мкл 10%-ного гепарина. Смесь оставили перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 855 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 18 ч при перемешивании (160 об/мин). Затем к смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего добавляли еще 425 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакционную смесь оставляли перемешиваться в течение 36 ч при +10°С (160 об/мин).
Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще в течение 10 ч при +5° (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 425 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 6.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 10 мг гиалуроната натрия, затем добавляли 100 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 395 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 10 ч при перемешивании (160 об/мин). Затем к смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего вносили еще 282 мкл ПЭГДЭ (ρ=1,14 г/см). Реакционную смесь оставляли перемешиваться в течение 18 ч при +15°С (160 об/мин).
Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще в течение 10 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 425 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 7.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 10 мг гиалуроната натрия, затем добавляли 100 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об./мин). Затем к реакционной смеси добавляли 635 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 24 ч при перемешивании (160 об/мин). Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще в течение 12 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 300 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 8.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 1%-ного раствора гидроксида натрия и 40 мг гиалуроната натрия, затем добавляли 50 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 587 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 24 ч при перемешивании (160 об/мин).
Реакцию останавливали добавлением 4 мл этанола (96%) и оставляли перемешиваться еще в течение 12 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 300 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 9.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 2%-ного раствора гидроксида натрия и 30 мг гиалуроната натрия, затем добавляли 300 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 3 ч при +15°С (200 об/мин). Затем к реакционной смеси добавляли 400 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 18 ч при перемешивании (160 об/мин). Затем к смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего вносили еще 400 мкл ПЭГДЭ. Реакционную смесь оставляли перемешиваться в течение 24 ч при +15°С (160 об/мин).
Реакцию останавливали добавлением 5 мл метанола и оставляли перемешиваться еще в течение 10 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 1000 мл, добавляли 600 мл ddH2O и нейтрализовывали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Пример 10.
В колбу, снабженную верхнеприводной мешалкой, объемом 250 мл помещали 25 мл 0,5%-ного раствора гидроксида натрия и 25 мг гиалуроната натрия, затем добавляли 250 мкл 10%-ного гепарина. Смесь оставляли перемешиваться в течение 12 ч при +8°С (200 об/мин). Затем к реакционной смеси добавляли 625 мкл ПЭГДЭ (ρ=1,14 г/см3). Реакцию проводили еще в течение 24 ч при перемешивании (160 об/мин). К смеси добавляли 50 мл раствора, содержавшего 0,5% раствора гиалуроната натрия, 0,005% гепарина и 0,05% гидроксида натрия, после чего вносили еще 625 мкл ПЭГДЭ. Реакционную смесь оставляли перемешиваться в течение 24 ч при +15°С (160 об/мин).
Реакцию останавливали добавлением 4 мл метанола и оставляли перемешиваться еще в течение 12 ч при +5°С (30 об/мин). Полученный гель переносили в колбу на 500 мл, добавляли 400 мл ddH2O и нейтрализовали раствором 1 М соляной кислоты до рН 7,0. Затем к гелю добавляли 50 мл физиологического фосфатного буфера (2 мМ Na2HPO4/NaH2PO4, 145,5 мМ NaCl, рН 7,0). Полученный продукт подвергали тангенциальной фильтрации, используя мембрану с порогом отсечения 0,22 мкм. По достижении коэффициента преломления n20=1,3355 концентрирование геля продолжали до концентрации 20 мг/мл (методику определения концентрации гиалуроната натрия см. в примере 1). Полученный сконцентрированный продукт перемешивали посредством верхнеприводной мешалки еще в течение 2 ч при 30 об/мин для его полной гомогенизации.
Список использованных источников
1. Scott J.E. Secondary structures in hyaluronan solutions: chemical and biological implications. The biology of hyaluronan // Ciba Found. Symp - 1989 - Vol. 143 - P. 6-15.
2. Хабаров В.Н., Бойков П.Я., Селянин М.А. Гиалуроновая кислота: получение, свойства, применение в биологии и медицине - М.: Практическая медицина, 2012 - 224 с.
3. Белодед А.В. Микробиологический синтез и деградация гиалуроновой кислоты бактериями p.Streptococcus: дис. канд. биол. наук - М., 2008. - С. 174.
4. Lolvmcin A.M., Peppcis N.A. Molecular analysis of interpolymer complexation in graft copolymer networks // Polymer. - 2000 - Vol. 41. - No. 1. - P. 73-80.
5. Sykaras N., Lynne A. Opperman bone morphogenetic proteins (BMPs): how do they function and what can they offer the clinician // J. Oral Sci. - 2003. - Vol. 45. - P. 57-73.
6. Xu X., Jha A.K, Duncan R.L., Jia X.Q. Heparin-decorated, hyaluronic acid-based hydrogel particles for the controlled release of bone morphogenetic protein 2 // Acta Biomater - 2011 - Vol. 7. - P. 3050-3059.
7. Bhakta G., Rai В., Lim Z.X. et al. Hyaluronic acid-based hydrogels functionalized with heparin that support controlled release of bioactive BMP-2 // Biomaterials - 2012. - Vol. 33 - P. 6113-6122.
Способ получения композиции на основе модифицированного гиалуроната натрия и гепарина, заключающийся в создании поперечных ковалентных связей между гидроксильными группами остатков D-глюкуроновой кислоты и D-N-ацетилглюкозамина, входящих в состав гиалуроната натрия, и остатков α-D-глюкозамина и уроновой кислоты, относящихся к гепарину, посредством введения активного сшивающего бифункционального агента - (полиэтиленгликоль)диглицидилового эфира (ПЭГДЭ) в щелочной среде.