Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ПРОИЗВОДНЫХ ПРОПИОНОВОЙ КИСЛОТЫ
Вид РИД
Изобретение
Настоящее изобретение относится к новому способу получения (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоты или ее соли.
В частности, объектом настоящего изобретения является способ получения соединения формулы (I),
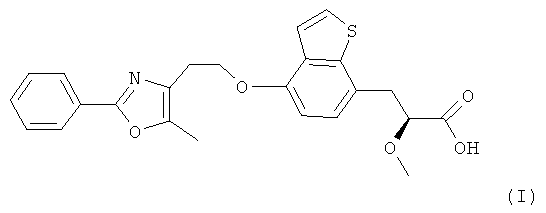 ,
,
или его соли, в котором соединение формулы (II),
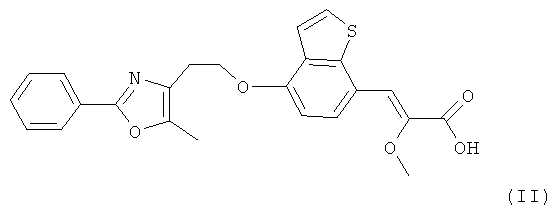
или его соль гидрируют
а) в присутствии катализатора, содержащего иридий, или
б) в присутствии катализатора, содержащего рутений и соединение формулы (IV), (V), (VI) или (VII),
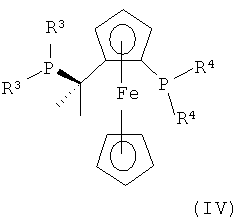 ,
, 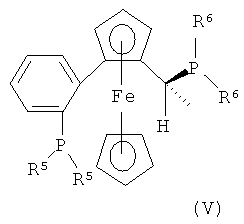 ,
,
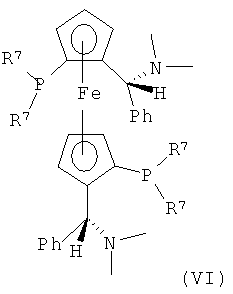 или,
или, 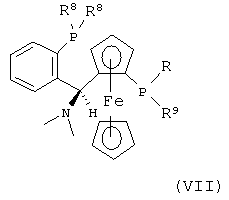
в котором
R3 представляет собой алкил, циклоалкил или арил,
R4 представляет собой циклоалкил, алкил или гетероарил,
R5 представляет собой циклоалкил или арил,
R6 представляет собой циклоалкил или арил,
R7 представляет собой циклоалкил или арил,
R8 представляет собой циклоалкил или арил,
R9 представляет собой циклоалкил или арил.
Соединение формулы (I) известно в соответствующей области и описано, например, в международной заявке на изобретение WO 02/092084. Оно особенно полезно в профилактике и/или лечении сахарного диабета типа I и II.
Способ согласно настоящему изобретению позволяет осуществить синтез соединения формулы (I) с высоким энантиомерным избытком. Он может быть осуществлен в дихлорметане, что позволяет избежать использования сложных смесей растворителей. Способ с использованием катализатора, содержащего иридий, обеспечивает особенно высокий выход и высокий энантиомерный избыток соединения формулы (I). Помимо этого оптически чистое соединение формулы (I) получают без применения многократной кристаллизации диастереомерных солей.
Термин «катализатор» относится к комплексу рутения или иридия, соответственно, с хиральным лигандом. В подобных комплексах рутения рутений предпочтительно характеризуется степенью окисления II. В подобных комплексах иридия иридий предпочтительно характеризуется степенью окисления I.
Термин «алкил» относится к разветвленному или неразветвленному одновалентному алкильному радикалу, содержащему от одного до восьми атомов углерода, предпочтительно, от одного до четырех атомов углерода. Данный термин дополнительно иллюстрируют такие радикалы, как метил, этил, н-пропил, изопропил, изобутил, н-бутил, трет-бутил и им подобные, причем метил, трет-бутил и изопропил являются предпочтительными.
Термин «алкоксигруппа» относится к группе алкил-О-. Предпочтительной алкоксигруппой является метоксигруппа.
Термин «циклоалкил» относится к одновалентному карбоциклическому радикалу, содержащему от 3 до 10 атомов углерода, предпочтительно, от 3 до 6 атомов углерода, такому как циклопропил, циклобутил, циклопентил или циклогексил. Циклогексил является предпочтительным циклоалкилом.
Термин «арил» относится к фенильной или нафтильной группе, предпочтительно, к фенильной группе, которая может необязательно быть моно- или полизамещенной, в частности, моно-, ди- или тризамещенной, галоидом, гидроксигруппой, CN, CF3, NO2, NH2, N(H, алкил), N(алкил)2, карбоксигруппой, аминокарбонилом, алкилом, алкоксигруппой, фенилом и/или фенилоксигруппой. Предпочтительными заместителями являются галоид, алкил, CF3 и алкоксигруппа, в особенности, алкил, CF3 и алкоксигруппа.
Термин «гетероарил» относится к ароматическому 5- или 6-членному циклу, который может включать 1, 2 или 3 атома, выбранных из азота, кислорода и/или серы, такому как фурил, пиридил, 1,2-, 1,3- и 1,4-диазинил, тиенил, изоксазолил, оксазолил, имидазолил или пирролил. Термин «гетероарил» также относится к бициклическим ароматическим группам, включающим два 5- или 6-членных цикла, в которых один или оба цикла могут включать 1, 2 или 3 атома, выбранных из азота, кислорода или серы, таким как, например, индол или хинолин, или к частично гидрированным бициклическим ароматическим группам, таким как, например, индолинил. Гетероарильная группа может характеризоваться мотивом замещения, подобным описанному выше в связи с термином «арил». Предпочтительными гетероарильными группами являются 2-тиенил и 2-фурил. Особенно предпочтительным является 2-фурил.
Термин «галогенид» относится к атому галогена, несущему отрицательный заряд, такому как фторид, хлорид, бромид и иодид.
Термин «фармацевтически приемлемые соли» включает в свой объем соли соединения формулы (I) с фармацевтически приемлемыми основаниями, такими как соли щелочных металлов, например соли натрия и калия, соли щелочноземельных металлов, например, соли кальция и магния, а также соли аммония или алкилзамещенного аммония, такие как, например, соли триметиламония. Предпочтительной фармацевтически приемлемой солью соединения формулы (I) является натриевая соль.
Термин «η5» означает η5 - координацию в стандартном для координационной химии понимании. Он указывает на число электронов, общих для металлического ядра и лиганда в координационном соединении или комплексе.
Предпочтительный способ представляет собой способ согласно настоящему изобретению, в котором катализатор содержит иридий и соединение формулы (III), (VIII) или (IX),
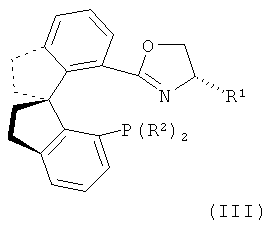 ,
, 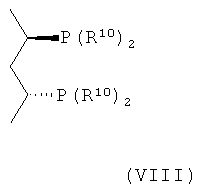 ,
,
или 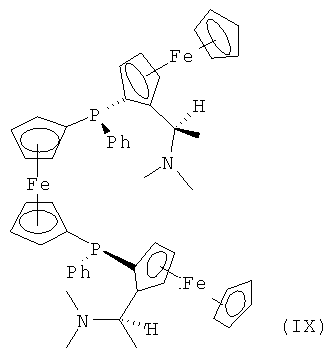 ,
,
в котором
R1 представляет собой водород, алкил, арил или арилалкил,
R2 представляет собой арил,
R10 представляет собой арил.
Еще более предпочтительным является способ согласно вышеприведенному определению, в котором катализатор содержит иридий и соединение формулы (III),
 ,
,
в котором R1 и R2 отвечают вышеприведенному определению.
Также особенно предпочтительным является способ, как он определен выше, в котором катализатор содержит иридий и соединение формулы (X),
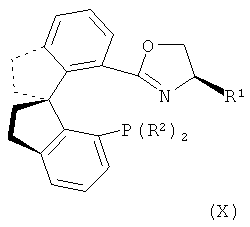
в котором R1 и R2 отвечают вышеприведенному определению.
R1 предпочтительно представляет собой водород, алкил, фенил или бензил, более предпочтительно, водород, алкил или бензил.
В частности, предпочтительным является способ, как он определен выше, в котором R1 представляет собой водород, изопропил, фенил или бензил. Более предпочтительно, R1 представляет собой водород, изопропил или бензил.
Также предпочтительным является способ, как он определен выше, в котором R2 представляет собой фенил или фенил, замещенный одним или двумя алкилами.
Кроме того, предпочтительным является способ согласно настоящему изобретению, в котором R2 представляет собой фенил, 3,5-диметилфенил или 3,5-ди-трет-бутилфенил.
Также является предпочтительным способ согласно настоящему изобретению, в котором R10 представляет собой 3,5-диметилфенил.
Соединение формулы (IX) представляет собой (S,R,R)-1,1'-бис[((1-N,N-диметиламино) этилферроценил)(фенилфосфино)]ферроцен.
Предпочтительное соединение формулы (VIII) представляет собой (S,S)-[1,3-диметил-1,3-пропандиил] бис[ди(3,5-диметилфенил)фосфин].
Особенно предпочтительным является способ согласно настоящему изобретению, в котором соединение формулы (III) представляет собой (Sa,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-дифенилфосфино-1,1'-спиробииндан,
(Sa,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-диметилфенил)фосфино-1,1'-спиробииндан,
(Sa,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан,
(Sa,S)-7-[4,5-дигидро-4-фенилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан,
(Sa,S)-7-[4,5-дигидро-4-изопропилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан или
(Sa)-7-[4,5-дигидрооксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан.
Также является предпочтительным способ согласно настоящему изобретению, в котором соединение формулы (III) представляет собой
(Sa,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан,
(Sa,S)-7-[4,5-дигидро-4-изопропилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан или
(Sa)-7-[4,5-дигидрооксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан.
Кроме того, является предпочтительным способ согласно настоящему изобретению, в котором соединение формулы (X) представляет собой
(Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-дифенилфосфино-1,1'-спиробииндан,
(Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-диметилфенил)фосфино-1,1'-спиробииндан,
(Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан,
(Sa,R)-7-[4,5-дигидро-4-фенилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан или
(Sa,R)-7-[4,5-дигидро-4-изопропилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил) фосфино-1,1'-спиробииндан.
Помимо этого, предпочтительным является способ, как он определен выше, в котором катализатор представляет собой Ir(L1)(L2)nY,
в котором
L1 представляет собой соединение формулы (III), (VIII) или (IX), как оно определено выше,
L2 представляет собой циклооктен, 1,5-циклооктадиен, этилен, 1,5-гексадиен или норборнадиен,
Y представляет собой хлорид, иодид, бромид, фторид, трифторацетат, тетрафторборат, тетракис [3,5-бис(трифторметил)фенил]борат, тетрафенилборат, гексафторантимонат, гексафторфосфат, трифлат, мезилат, перхлорат, пербромат, периодат, нитрат, гидросульфат или ацетилацетонат, и
n принимает значения 1 или 2.
Также является предпочтительным способ, как он определен выше, в котором катализатор представляет собой Ir(L1)(L2)nY, в котором L1 представляет собой соединение формулы (X) и в котором L2, Y и n отвечают вышеприведенным определениям.
Особенно предпочтительным является способ, в котором L1 представляет собой соединение формулы (III).
Y предпочтительно представляет собой хлорид, тетрафторборат, гексафторфосфат или тетракис [3,5-бис(трифторметил)фенил]борат, более предпочтительно, тетрафторборат или тетракис[3,5-бис(трифторметил)фенил]борат.
Предпочтительно, n принимает значение 1.
В частности, предпочтительным является способ по настоящему изобретению, в котором катализатор представляет собой
[Ir(S,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетракис[3,5-бис(трифторметил)фенил]борат,
[Ir(S,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетрафторборат,
[Ir(S,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]трифторметансульфонат,
[Ir(S,S)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]хлорид,
[Ir(S,S)-7-[4,5-дигидро-4-изопропилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетракис[3,5-бис(трифторметил)фенил]борат или [Ir(S,S)-7-[4,5-дигидрооксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетракис[3,5-бис(трифторметил)фенил]борат.
Также особенно предпочтительным является способ согласно настоящему изобретению, в котором катализатор представляет собой
[Ir((Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетракис[3,5-бис(трифторметил)фенил]борат,
[Ir((Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]тетрафторборат,
[Ir((Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]трифторметансульфонат или
[Ir((Sa,R)-7-[4,5-дигидро-4-бензилоксазол-2-ил]-7'-ди(3,5-ди-трет-бутилфенил)фосфино-1,1'-спиробииндан)(1,5-циклооктадиен)]хлорид.
Также предпочтительным является способ, как он определен выше, в котором катализатор содержит рутений и соединение формулы (IV), (V), (VI) или (VII),
 ,
,  ,
,
 или
или 
в котором радикалы R3-R9 отвечают вышеприведенным определениям.
R3 предпочтительно представляет собой алкил, циклогексил, фенил, алкилфенил или диалкилфенил.
В частности, предпочтительным является способ, в котором R3 представляет собой трет-бутил, циклогексил, фенил, 2-метилфенил или 3,5-диметилфенил.
Также R4 предпочтительно представляет собой алкил, циклогексил, фенил, нафтил, фурил, или же фенил, замещенный одним-тремя заместителями, независимо друг от друга выбранными из трифторметила, алкила и алкоксигруппы.
Способ согласно настоящему изобретению, в котором R4 представляет собой трет-бутил, циклогексил, фенил, 3,5-ди-трифторметилфенил, 4-трифторметилфенил, 3,5-диметил-4-метоксифенил, 1-нафтил или 2-фурил также является предпочтительным.
R5 предпочтительно представляет собой циклогексил, фенил, или же фенил, замещенный одним-тремя заместителями, независимо друг от друга выбранными из алкила и алкоксигруппы.
Кроме того, способ согласно настоящему изобретению, в котором R5 представляет собой фенил, циклогексил, 3,5-диметил-4-метоксифенил или 3,5-диметилфенил, также является предпочтительным.
R6 предпочтительно представляет собой циклогексил, норборнил, фенил, или же фенил, замещенный одним-тремя заместителями, независимо друг от друга выбранными из алкила и трифторметила.
Кроме того, предпочтительным является способ, как он определен выше, в котором R6 представляет собой фенил, циклогексил, 3,5-диметилфенил, 3,5-ди-трифторметилфенил или норборнил.
R7 предпочтительно представляет собой циклогексил, фенил, или же фенил, замещенный одним-тремя заместителями, независимо друг от друга выбранными из алкила, трифторметила и алкоксигруппы.
Также является предпочтительным способ согласно настоящему изобретению, в котором R7 представляет собой циклогексил, фенил, 3,5-диметилфенил, 3,5-ди-трифторметилфенил, 3,5-диметил-4-метоксифенил или 2-метилфенил.
Особенно предпочтительным является способ согласно настоящему изобретению, в котором R8 представляет собой циклогексил или фенил.
Способ согласно настоящему изобретению, в котором R9 представляет собой циклогексил или фенил также является предпочтительным.
Помимо этого, особенно предпочтительным является способ согласно настоящему изобретению, в котором соединение формулы (IV), (V), (VI), (VII) или (VIII) представляет собой
(S)-1-[(R)-2-(дифенилфосфино)ферроценил]этилди-трет-бутилфосфин,
(S)-1-[(R)-2-(дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфин,
(S)-1-[(R)-2-(ди(4-тpифтopмeтилфeнил)фocфинo)фeppoцeнил]этилди-трет-бyтилфосфин,
(S)-1-[(R)-2-(ди(3,5-диметил-4-метоксифенил)фосфино)ферроценил]этилди-трет-бутилфосфин,
(S)-1-[(R)-2-(ди-2-фурилфосфино)ферроценил]этилди-трет-бутилфосфин,
(αR,αR)-2,2'-биc(α-N,N-димeтилaминoфeнилмeтил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен,
(αR,αR)-2,2'-биc(α-N,N-димeтилaминoфeнилмeтил)-(S,S)-1,1'-биc[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен,
(R)-1-дифенилфосфино-2-[(S)-α-(N,N-диметиламино)-о-дифенилфосфинофенил)метил]ферроцен,
(S)-1-[(8)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин,
(R)-1-[(R)-2-(2'-дициклогексилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин или
(R)-1-[(R)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(2-норборнил)фосфин.
Кроме того, также является предпочтительным способ согласно настоящему изобретению, в котором соединение формулы (IV), (V), (VI) или (VII) представляет собой
(S)-1-[(R)-2-(дифенилфосфино)ферроценил]этилди-трет-бутилфосфин или
(S)-1-[(R)-2-(ди(3,5-диметил-4-метоксифенил)фосфино)ферроценил]этилди-трет-бутилфосфин.
В частности, предпочтительным является способ, как он определен выше, в котором катализатор представляет собой Ru(L3)(L4)(L5)mYp, в котором
L3 представляет собой соединение формулы (IV), (V), (VI) или (VII), как оно определено выше,
L4 представляет собой η5-2,4-диметилпентадиенил, циклопентадиенил или η5-2,3,4-триметилпентадиенил,
L5 представляет собой галогенид, ацетонитрил, диэтиловый эфир, воду, ацетон, тетрагидрофуран, диоксан, пиридин, имидазол или тиофен,
Y представляет собой тетракис[3,5-бис(трифторметил)фенил]борат,
тетрафторборат, тетрафенилборат, гексафторантимонат, гексафторфосфат, трифлат, мезилат, гидросульфат или перхлорат,
m принимает значения 0 или 1, и
p принимает значения 0 или 1.
L5 предпочтительно представляет собой иод.
m предпочтительно равно 1, p предпочтительно равно 1.
Особенно предпочтительным является способ, как он определен выше, в котором катализатор представляет собой
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(дифенилфосфино)ферроценил] этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(дициклогексилфосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(ди(4-трифторметилфенил)фосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(ди(3,5-диметил-4-метоксифенил)фосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(ди-2-фурилфосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиентил)((αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис(дифенилфосфино)ферроцен)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-диметилпентадиенил)((αR,αR)-2,2'-бис(α-N,N-диметиламинофенилметил)-(S,S)-1,1'-бис[ди(3,5-диметил-4-метоксифенил)фосфино]ферроцен)(ацетонитрил)]-тетрафторборат,
[RuI(η5-2,4-димeтилпeнтадиeнил)((R)-1-дифeнилфocфинo-2-[(S)-α-(N,N-диметиламино)-о-дифенилфосфинофенил)метил]ферроцен)],
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(S)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин)(ацетонитрил)]тетрафторборат,
[Ru(η5-2,4-димeтилпeнтaдиeнил)((R)-1-[(R)-2-(2'-дициклoгeкcилфocфинoфeнил)ферроценил]этилди(бис-3,5-трифторметилфенил)фосфин)(ацетонитрил)] тетрафторборат или
[Ru(η5-2,4-диметилпентадиенил)((R)-1-[(R)-2-(2'-дифенилфосфинофенил)ферроценил]этилди(2-норборнил)фосфин)(ацетонитрил)]тетрафторборат.
Также особенно предпочтительным является способ согласно настоящему изобретению, в котором катализатор представляет собой
[Ru(η5-2,4-диметилпентадиенил)((S)-1-[(R)-2-(дифенилфосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)]тетрафторборат или
[Ru(η5-2,4-димeтилпeнтaдиeнил)((S)-1-[(R)-2-(ди(3,5-димeтил-4-мeтoкcифeнил)фосфино)ферроценил]этилди-трет-бутилфосфин)(ацетонитрил)] тетрафторборат.
Согласно настоящему изобретению, соединение формулы (II) может быть прогидрировано в атмосфере водорода.
В том случае, если используют катализатор, содержащий иридий, способ предпочтительно осуществляют при температуре от 10 до 120°C, более предпочтительно, от 40 до 100°C, особенно предпочтительно, от 60 до 80°C.
В том случае, если используют катализатор, содержащий иридий, способ предпочтительно осуществляют в растворителе, выбранном из спиртов, фторированных спиртов, тетрагидрофурана, метилтетрагидрофурана, дихлорметана, диалкиловых простых эфиров, ароматических растворителей, таких как бензол, толуол, CF3-C6H5, моно- и полифторированных ароматических растворителей, а также их смесей, более предпочтительно, в метаноле, тетрагидрофуране, дихлорметане и их смесях, наиболее предпочтительно, в смеси метанол/терагидрофуран 3:2.
В том случае, если используют катализатор, содержащий иридий, способ предпочтительно осуществляют при давлении водорода в диапазоне от 1 до 200 бар, более предпочтительно, от 10 до 100 бар, особенно предпочтительно, от 40 до 60 бар. В том случае, если используют лиганд формулы (III) с конфигурацией (S,S), предпочтительным является давление 10 бар. В том случае, если используют лиганд формулы (III) с конфигурацией (Sa,R), предпочтительным является давление 30 бар.
В том случае, если используют катализатор, содержащий иридий, соотношение между субстратом и катализатором (моль/моль) предпочтительно составляет от 10 до 50000, более предпочтительно, между 100 и 10000, особенно предпочтительно, между 1000 и 5000.
В том случае, если используют катализатор, содержащий рутений, способ предпочтительно осуществляют при температуре от 10 до 120°C, более предпочтительно, от 20 до 80°C, особенно предпочтительно, от 30 до 50°C.
В том случае, если используют катализатор, содержащий рутений, способ предпочтительно осуществляют в растворителе, выбранном из спиртов, тетрагидрофурана, дихлорметана, фторированных спиртов, метилтетрагидрофурана, простых эфиров и их смесей, предпочтительно, в метаноле, тетрагидрофуране, дихлорметане и их смесях, наиболее предпочтительно, в смеси дихлорметан/тетрагидрофуран 1:1 или в дихлорметане, особенно предпочтительно, в дихлорметане.
В том случае, если используют катализатор, содержащий рутений, способ предпочтительно осуществляют при давлении водорода от 1 до 200 бар, более предпочтительно, от 10 до 100 бар, особенно предпочтительно, от 40 до 60 бар.
В том случае, если используют катализатор, содержащий рутений, соотношение между субстратом и катализатором (моль/моль) предпочтительно составляет от 10 до 50000, более предпочтительно, между 100 и 10000, особенно предпочтительно, между 1000 и 5000.
Предпочтительную (S)-конфигурацию соединения формулы (I) получают с лигандами, описываемыми в таблицах в экспериментальной части. В том случае, если хиральный лиганд или катализатор приводит к преимущественному получению соединения формулы (I) с (R)-конфигурацией, очевидно, что для получения соединения формулы (I) с (S)-конфигурацией должны быть задействованы лиганд или катализатор с противоположной конфигурацией. Оба энантиомера хиральных лигандов в равной степени легкодоступны.
Объектом настоящего изобретения также является соединение формулы (I), как оно определено выше, или его соль, полученные с помощью способа согласно настоящему изобретению.
Кроме того, объектом настоящего изобретения также является применение катализатора, как он определен выше, для получения соединения формулы (I), как оно определено выше.
Катализаторы для применения в способе согласно настоящему изобретению могут быть получены посредством взаимодействия соединения формулы [Ir(L)Cl]2, [Ir(L)2] BARF (тетракис[3,5-бис(трифторметил)фенил]борат) или [Ir(L)2]BF4, где L обозначает нейтральный лиганд, например, COD (ЦОД, 1,5-циклооктадиен), с требуемым лигандом формулы (III), (VIII), (IX) или (X), например, (S,S)-3,5-Xyl-Skewphos (1,3-диметил-1,3-пропандиил]бис[ди(3,5-диметилфенил)фосфин) или (S,R,R)-TRIFER (1,1'-бис[((1-N,N-диметиламино)этилферроценил)(фенилфосфино)]ферроцен), в подходящем растворителе, таком как, например, дихлорметан или метанол. Катализатор может быть использован в выделенном виде или полученным in situ. Соединения [Ir(COD)Cl]2 и [Ir+(COD)2]BF4 или являются коммерчески доступными, например, от компании Strem Chemicals Inc., Ньюбургпорт, Массачуссетс, США или могут быть получены с помощью способов, которые известны сами по себе, например, описанных в J. Herde и др., Inorg. Syn. 1974, 18-20 или М.Green и др., J. Chem. Soc. 1971, 2334-2337.
Термин «нейтральный лиганд», как он употребляется в контексте, обозначает способный к легкому обмену лиганд, такой как олефин, например, этилен, пропилен, циклооктен, 1,5-гексадиен, норборнадиен, 1,5-циклооктадиен, нитрил, такой как ацетонитрил или бензонитрил, или же также и растворитель, такой как, например, тетрагидрофуран, толуол и т.п. В том случае, когда наличествует более чем один подобный лиганд, они также могут быть отличны друг от друга. Предпочтительным нейтральным лигандом является циклооктадиен.
Примеры
Сокращения
η5-2,4-ДМП=η5-2,4-диметилпентадиенил,
ТГФ=тетрагидрофуран,
NCMe=ацетонитрил,
ТФУК=трифторуксусная кислота,
COD=ЦОД=1,5-циклооктадиен,
BARF=тетракис[3,5-бис(трифторметил)фенил]борат,
КТ=комнатная температура,
S/C=соотношение субстрат-катализатор (моль/моль),
ВЭЖХ=высокоэффективная жидкостная хроматография,
ЭИ=энантиомерный избыток=[(S)-(R)]/[(S)+(R)].
DBT=DTB=ДТБ=3,5-ди-трет-бутилфенил
трифлат=трифторметансульфонат.
Все ферроценилдифосфиновые лиганды коммерчески доступны от компании Solvias AG, СН-4002, Базель. Рутениевые комплексы коммерчески доступны от компании Umicore AG, D-63457, Ханау-Вольфганг или могут быть получены согласно статье О.Briel и др. в сборнике "Catalysis of Organic Reactions" (Катализ органических реакций), 2009, 203, CRC Press, Бока Ратон. Оксазолинмонофосфиновые лиганды (лиганды SIPHOX (спиро-фосфин-оксазолиновые)) и их соответствующие иридиевые комплексы коммерчески доступны от университета Нанкай, Тянцзин, 300071, Китай, или могут быть получены согласно статье Q.L.Zhou и др. J. Am. Chem. Soc. 2008, 130, 8584. Xyl-Skewphos и 3,5-tBu-MeOBIPHEP ((6,6'-диметоксибифенил-2,2'-диил)бис[бис(3,5-ди-трет-бутилфенил)фосфин]) коммерчески доступны от компании Solvias AG, СН-4002, Базель. TRIFER коммерчески доступен от компании Phoenix Chemicals, 34 Тэрсби Роад, Бромборроу, Уиррал СН62, 3PW, Великобритания (UK) или могут быть получены согласно статье P.McCormack и др. Angew. Chem. Int. Ed. 2007, 46, 4141-44.
Ниже представлена нумерация атомов в лигандах SIPHOX:
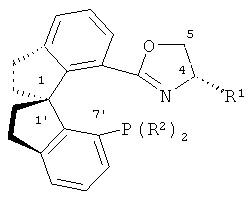
Ниже представлена асимметрическая конфигурация лиганда (Sa,R) SIPHOX:
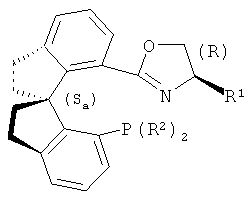
Конфигурации SIPHOX (Sa,S) или (Sa,R) могут также обозначаться (S,S) или (S,R), соответственно.
|
|
Синтез иридиевых металлокомплексов: примеры 1а-1з
Пример 1а: Получение [Ir(S,S)-Xyl-Skewphos (COD)]BF4
В 25-мл пробирку Шленка загружают 100 мг (S,S)-Xyl-Skewphos (0,18 ммоля), 60 мг [Ir(COD)Cl]2 (0,09 ммоля) и 5 мл дихлорметана. К образующемуся раствору темно-красного цвета добавляют двумя порциями 35 мг тетрафторбората серебра (0,18 ммоля) и перемешивают получаемую таким образом суспензию в течение 2 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 6 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 8 мл гексана и сушат под высоким вакуумом, что приводит к 563 мг (85%) [Ir((S,S)-Xyl-Skewphos)(COD)]BF4 в виде твердого вещества красного цвета. Масс-спектрометрия с фурье-преобразованием (МСФП): 853,4 m/z [Ir((S,S)-Xyl-Skewphos)(COD)]+, 31ЯМР (спектроскопия ядерного магнитного резонанса) (CDCl3): 14,6 м.д. (s).
Пример 1б: получение [Ir((S,R,R)-Trifer)(COD)BARF
В 100-мл пробирку Шленка загружают 400 мг (S,R,R)-TRIFER (0,44 ммоля), 584 мг Ir(COD)2]BARF (0,46 ммоля) и 40 мл метанола. Образующийся раствор оранжевого цвета перемешивают в течение 5 часов при КТ. После этого добавляют 12 мл воды и отфильтровывают образующиеся кристаллы. Промывают осадок на фильтре 32 мл смеси метанола и воды (4:1) и сушат под высоким вакуумом, что приводит к 804 мг (88%) [Ir((S,R,R)-TRIFER)(COD)]BARF в виде кристаллов оранжевого цвета. МСФП: 1213,2 m/z [Ir((S,R,R)-TRIFER)(COD)]+. 31Р-ЯМР (CDCl3): 6,2 м.д. (s).
Пример 1в: Получение [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BARF
В 25-мл пробирку Шленка загружают 100 мг (Sa,R)-DBT-Bn-SIPHOX (0,127 ммоля), 168 мг [Ir(COD)2]BARF (0,132 ммоля) и 10 мл метанола. Образующийся раствор желтого цвета перемешивают в течение 2 часов при КТ, затем реакционную смесь досуха выпаривают на роторном испарителе (50°C/5 мбар). Остаток растворяют в 5 мл метанола. Добавляют 0,5 мл воды и перемешивают образующуюся суспензию желтого цвета в течение 30 минут при КТ. Кристаллы отфильтровывают, промывают 3,5 мл смеси МеОН и воды (6:1) и сушат под высоким вакуумом, что приводит к 189 мг (76%) [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BARF в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]+, 31Р-ЯМР (CDCl3): 16,5 м.д. (s).
Пример 1г: Получение [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)BF4
В 25-мл пробирку Шленка загружают 56 мг (Sa,R)-DBT-Bn-SIPHOX (0,070 ммоля), 24 мг [Ir(COD)Cl]2 (0,035 ммоля) и 5 мл дихлорметана. К образующемуся раствору оранжевого цвета добавляют 14 мг тетрафторбората серебра (0,071 ммоля) и перемешивают образующуюся суспензию оранжевого цвета в течение 2 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 9 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 11 мл гексана и сушат под высоким вакуумом, что приводит к 69 мг (83%) [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BF4 в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]+, 31P-ЯМР (CDC13): 16,6 м.д. (s).
Пример 1д: Получение [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)OTf
В 25-мл пробирку Шленка загружают 100 мг (Ra,S)-DBT-Bn-SIPHOX (0,127 ммоля), 44 мг [Ir(COD)Cl]2 (0,505 ммоля) и 4 мл дихлорметана. К образующемуся раствору оранжевого цвета добавляют 34 мг трифторметансульфоната серебра (0,130 ммоля) и перемешивают получаемую таким образом суспензию оранжевого цвета в течение 2 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 6 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 11 мл гексана и сушат под высоким вакуумом, что приводит к 134 мг (85%) [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]OTf в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]+, 31Р-ЯМР (CDCl3): 16,6 м.д. (s).
Пример 1е: Получение [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BF4
В 25-мл пробирку Шленка загружают 100 мг (S,S)-DBT-Bn-SIPHOX (0,127 ммоля), 43 мг [Ir(COD)Cl]2 (0,063 ммоля) и 5 мл дихлорметана. К образующемуся раствору оранжевого цвета добавляют 26 мг тетрафторбората серебра (0,131 ммоля) и перемешивают получаемую таким образом суспензию оранжевого цвета в течение 2 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 6 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 8 мл гексана и сушат под высоким вакуумом, что приводит к 148 мг (99%) [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BF4 в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]+, 31Р-ЯМР (CDCl3): 16,0 м.д. (s).
Пример 1ж: Получение [Ir((S,S)-DBT-Bn-SIPHOX)(COD)BF4
В 25-мл пробирку Шленка загружают 200 мг (S,S)-DBT-Bn-SIPHOX (0,254 ммоля), 87 мг [Ir(COD)Cl]2 (0,128 ммоля) и 5 мл дихлорметана. К образующемуся раствору оранжевого цвета добавляют 43 мг тетрафторбората натрия (0,384 ммоля) и перемешивают получаемую таким образом суспензию оранжевого цвета в течение 5 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 8 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 11 мл гексана и сушат под высоким вакуумом, что приводит к 259 мг (87%) [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BF4 в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]+, 31P-ЯМР (CDCl3): 16,0 м.д. (s).
Пример 1з: Получение [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]BF4
В 25-мл пробирку Шленка загружают 40 мг (Ra,S)-DBT-Bn-SIPHOX (0,058 ммоля), 18 мг [Ir(COD)Cl]2 (0,026 ммоля) и 4 мл дихлорметана. К образующемуся раствору оранжевого цвета добавляют 9 мг тетрафторбората натрия (0,076 ммоля) и перемешивают получаемую таким образом суспензию оранжевого цвета в течение 3 часов при КТ. Реакционную смесь фильтруют через дикалит спидекс и промывают осадок на фильтре 6 мл дихлорметана. Объединенные фильтраты упаривают на роторном испарителе досуха (50°C/5 мбар). Образующийся неочищенный продукт промывают 11 мл гексана и сушат под высоким вакуумом, что приводит к 51 мг (86%) [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]BF4 в виде твердого вещества оранжевого цвета. МСФП: 1088,5 m/z [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]+, 31Р-ЯМР (CDCl3): 16,6 м.д. (s).
Синтез 2-Метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоты посредством асимметричного гидрирования (Z)-2-метокси-3-(4-[2-(5-метил-2-фенилоксазол-4-ил)этокси)бензо[b]тиофен-7-ил)акриловой кислоты: примеры 2-19 и сравнительный пример А
Пример 2.1
В герметизированном боксе с перчатками (содержание кислорода: ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 35,9 мг [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BARF (0,018 ммоля, S/C 250), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,93 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,6% (степень превращения >99,9%) и энантиомерной чистотой 99,5%.
Методика ВЭЖХ для химической очистки (% по площади, (S)-фенилэтиламин не учитывается): колонка YMC-Pack Pro С18, 150×4,6 мм, подвижная фаза: подвижная фаза А: вода с 0,1% ТФУК, Б: NCMe с 0,1% ТФУК, температура 22°C, объемная скорость 2 мл/мин, изократическое элюирование А/Б 51/49% в течение 10 минут, градиент от 51/49% к 5/95% в течение 10 минут и 5 минут при 5/95%, детектирование при длине волны 285 нм. Времена удерживания: 11,2 минуты: (S)- и (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота, 12,4 минуты: (Е)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловая кислота, 14,0 минуты: (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловая кислота.
Методика ВЭЖХ для определения энантиомерного избытка (% по площади): колонка Chiralpak-ADH, 25 см×4,6 мм, элюирование смесью 85% гептана и 10% этанола с 0,4% трифторуксусной кислоты, объемная скорость 0,7 мл/мин, температура 30°C, детектирование при длине волны 270 нм. Времена удерживания: 22,4 минуты: (11)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота, 26,3 минуты: (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота.
Пример 2.2
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 2,70 мг [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BF4 (0,0023 ммоля, S/C=2000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при давлении водорода 30 бар и температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 89,9% (степень превращения >99,9%) и энантиомерной чистотой 99,8%. Неочищенный продукт растворяют в 50 мл этилацетата. Добавляют 10 мл воды и 3 мл 2М водного раствора HCl и перемешивают двухфазную смесь при температуре 55°C в течение 15 минут. Органический слой отделяют, экстрагируют водный слой 20 мл этилацетата и перемешивают объединенные органические фракции над 0,5 г активированного угля (Darko KB) при КТ в течение 2 часов. После фильтрования через целит бесцветный раствор сушат над 3 г сульфата натрия и досуха выпаривают (40°C/10 мбар). Неочищенный продукт растворяют в 50 мл изопропилацетата при кипячении с обратным холодильником (температура масляной бани 100°C) и оставляют охлаждаться до комнатной температуры, в результате чего начинается самопроизвольная кристаллизация. Отфильтровывают образующиеся кристаллы, промывают 10 мл изопропилацетата и сушат при температуре 75°C и давлении 500 мбар в течение 4 часов, что приводит к 1,60 г (79%) чистой (S)-2-метокси-3- {4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоты (кислота I) в виде кристаллов белого цвета с химической чистотой 99,6% и энантиомерной чистотой ЭИ=99,8%.
Примеры 3.1-3.4
Сходным образом с описанным в примере 2 осуществляют нижеуказанные синтезы с гидрированием при температуре 60°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием иридиевых комплексов общей формулы [Ir(фосфорсодержащий лиганд)(COD)]BARF в качестве катализатора, что приводит к неочищенной 2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I), как это перечислено в таблице 1.
|
Пример 4
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 8,96 мг [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BARF (0,0046 ммоля, S/C=1000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (8)-1-фенилэтиламина (0,93 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,2% (степень превращения 99,8%) и энантиомерной чистотой 99,3%.
Примеры 5.1-5.2
Сходным образом с описанным в примере 4 осуществляют нижеуказанные синтезы с гидрированием при температуре 60°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием иридиевых комплексов общей формулы [Ir(фосфорсодержащий лиганд)(COD)]BARF в качестве катализатора, что приводит к неочищенной 2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I), как это перечислено в таблице 2.
|
Пример 6.1
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 4,48 мг [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BARF (0,0023 ммоля, S/C=2000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,93 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,2% (степень превращения >99,9%) и энантиомерной чистотой 99,4%.
Пример 6.2
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7- ил}акриловой кислоты (4,59 ммоля), 4,48 мг [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BARF (0,0023 ммоля, S/C=2000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при давлении водорода 30 бар и температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,0% (степень превращения >99,9%) и энантиомерной чистотой 99,8%.
Пример 7
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 8,96 мг [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BARF (0,0046 ммоля, S/C=1000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,93 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 8 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к 2,24 г неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоты (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,2% (степень превращения >99,9%) и энантиомерной чистотой 99,2%. Неочищенный продукт растворяют в 50 мл этилацетата. Добавляют 10 мл воды и 3 мл 2М водного раствора HCl и перемешивают двухфазную смесь при температуре 55°C в течение 15 минут. Органический слой отделяют, экстрагируют водный слой 20 мл этилацетата и перемешивают объединенные органические фракции над 0,5 г активированного угля (Darko KB) при КТ в течение 30 минут. После фильтрования через целит бесцветный раствор сушат над 3 г сульфата натрия и досуха выпаривают (40°C/10 мбар). Неочищенный продукт растворяют в 50 мл изопропилацетата при кипячении с обратным холодильником (температура масляной бани 100°C) и оставляют охлаждаться до комнатной температуры, в результате чего начинается самопроизвольная кристаллизация. Отфильтровывают образующиеся кристаллы, промывают 10 мл изопропилацетата и сушат при температуре 60°C/10 мбар в течение 2 часов, что приводит к 1,40 г (70%) чистой (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде кристаллов белого цвета с химической чистотой 99,8% и энантиомерной чистотой ЭИ>99,9%.
Пример 8.1
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 4,48 мг [Ir((S,S)-DBT-Bn-SIPHOX)(COD)]BARF (0,0023 ммоля, S/C=2000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,93 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 10 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,9% (степень превращения >99,9%) и энантиомерной чистотой 99,6%.
Пример 8.2
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 5,40 мг [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BF4 (0,0046 ммоля, S/C=1000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 10 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 89,7% (степень превращения 91,1%) и энантиомерной чистотой 99,8%.
Пример 8.3
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 2,84 мг [Ir((Ra,S)-DBT-Bn-SIPHOX)(COD)]OTf (0,0023 ммоля, S/C=2000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 8°C в течение 2 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,7% (степень превращения 99,7%) и энантиомерной чистотой 99,8%.
Пример 8.4
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 1,80 мг [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)]BF4 (0,0015 ммоля, S/C 3'000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 60 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,3% (степень превращения 99,4%) и энантиомерной чистотой 99,7%.
Пример 8.5
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 0,77 мг [Ir(COD)Cl]2 (0,0012 ммоля, S/C=2000), 1,81 мг (Ra,S)-DBT-Bn-SIPHOX (0,0023 ммоля) и 10 мл тетрагидрофурана. Образующийся раствор желтого цвета перемешивают в течение 30 минут при температуре внешней среды. После этого добавляют 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 24 мл метанола, 6 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,5%) (степень превращения >99,9%) и энантиомерной чистотой 99,5%.
Пример 8.6
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 1,14 мг [Ir(COD)2]BF4 (0,0023 ммоля, S/C=2000), 1,99 мг (Ra,S)-DBT-Bn-SIPHOX (0,0025 ммоля) и 10 мл тетрагидрофурана. Образующийся раствор желтого цвета перемешивают в течение 30 минут при температуре внешней среды. После этого добавляют 2,00 г (г)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 24 мл метанола, 6 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 60°C в течение 20 часов, а затем при температуре 80°C в течение 2 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4- ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,7% (степень превращения >99,9%) и энантиомерной чистотой 99,6%.
Пример 8.7
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 185 мл 2,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (4,59 ммоля), 1,80 мг [Ir((Sa,R)-DBT-Bn-SIPHOX)(COD)BF4 (0,0015 ммоля, S/C 3'000), 24 мл метанола, 16 мл тетрагидрофурана и 0,12 мл (S)-1-фенилэтиламина (0,92 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 80°C в течение 22 часов при давлении водорода 30 бар. После этого открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 96,7% (степень превращения 99,9%) и энантиомерной чистотой 99,5%.
Пример 9
Сходным образом с описанным в примере 4 осуществляют нижеуказанный синтез с гидрированием при температуре 40°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием [Ir((S,S)-Xyl-Skewphos)(COD)]BF4 (S/C=1000) в качестве катализатора, что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,8% (степень превращения 99,4%) и энантиомерной чистотой 85%.
Пример 10
Сходным образом с описанным в примере 2 осуществляют нижеуказанный синтез с гидрированием при температуре 60°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием [Ir((S,R,R)-Trifer)(COD)]BARF (S/C 250) в качестве катализатора, что приводит к неочищенной (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,0% (степень превращения >99,9%) и энантиомерной чистотой 86%.
Пример 11
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 1,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (2,30 ммоля),1,99 мг [Ru(η5-2,4-DMP)((R)-(S)-PPF-PtBu2)(NCMe)]BF4 (0,0023 ммоля, S/C=1000), 12 мл метанола, 8 мл дихлорметана и 0,06 мл (8)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,6% (степень превращения >99,9%) и энантиомерной чистотой 89%.
Методика ВЭЖХ для химической очистки (% по площади, (S)-фенилэтиламин не учитывается): колонка YMC-Pack Pro C18, 150×4,6 мм, подвижная фаза: подвижная фаза А: вода с 0,1% ТФУК, Б: NCMe с 0,1% ТФУК, температура 22°C, объемная скорость 2 мл/мин, изократическое элюирование А/Б 51/49% в течение 10 минут, градиент от 51/49% к 5/95% в течение 10 минут и 5 минут при 5/95%, детектирование при длине волны 285 нм. Времена удерживания: 11,2 минуты: (S)- и (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота, 12,4 минуты: (Е)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловая кислота, 14,0 минуты: (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловая кислота.
Методика ВЭЖХ для определения энантиомерного избытка (% по площади): колонка Chiralpak-ADH, 25 см×4,6 мм, элюирование смесью 90% гептана и 10% этанола с 0,5% трифторуксусной кислоты, объемная скорость 0,7 мл/мин, температура 30°C, детектирование при длине волны 270 нм. Времена удерживания: 22,1 минуты: (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4- ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота, 26,0 минуты: (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовая кислота.
Примеры 12.1-12.5
Сходным образом с описанным в примере 11 осуществляют нижеуказанные синтезы с гидрированием при температуре 40°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием рутениевых комплексов общей формулы [Ru(η5-2,4-ВМР)(фосфорсодержащий лиганд)(МСМе)]BF4 в качестве катализатора, что приводит к неочищенной 2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I), как это перечислено в таблице 3.
|
Пример 13
Сходным образом с описанным в примере 11 осуществляют нижеуказанные синтезы с гидрированием при температуре 40°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием рутениевого комплекса [RuI(η5-2,4-DMP)((S)-(R)-PPPhCHNMe2F-PP)] в качестве катализатора, что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 98,7% (степень превращения 99,2%) и энантиомерной чистотой 46%.
Пример 14
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 2,26 мг [Ru(η5-2,4-DMP)((S)-(R)-(3,5-Me2-4-MeOPh)2PF-PtBu2)(NCMe)]BF4 (0,0023 ммоля, S/C=1000) и 6 мл дихлорметана. Получаемый таким образом раствор фиолетового цвета перемешивают в течение 2 часов при КТ. После этого добавляют 1,00 г (2)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (2,30 ммоля), 4 мл дихлорметана, 10 мл ТГФ и 0,06 мл (8)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при перемешивании при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,5% (степень превращения >99,9%) и энантиомерной чистотой 87%).
Пример 15
Сходным образом с описанным в примере 14 осуществляют нижеуказанные синтезы с гидрированием при температуре 40°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием рутениевого комплекса [Ru(η5-2,4-DMP)((S)-(R)-2-Fur2PF-PtBu2)(NCMe)]BF4 в качестве катализатора, что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,3% (степень превращения >99,9%) и энантиомерной чистотой 73%.
Пример 16
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 1,99 мг [Ru(η5-2,4-DMP)((R)-(S)-PPF-PtBu2)(NCMe)]BF4 (0,0023 ммоля, S/C=1000) и 5 мл дихлорметана. Получаемый таким образом раствор фиолетового цвета перемешивают в течение 2 часов при КТ. После этого добавляют 1,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (2,30 ммоля), 2,5 мл дихлорметана, 7,5 мл ТГФ и 0,06 мл (8)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при перемешивании при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,2% (степень превращения >99,9%) и энантиомерной чистотой 90%.
Примеры 17.1-17.2
Сходным образом с описанным в примере 16 осуществляют нижеуказанные синтезы с гидрированием при температуре 40°C и давлении водорода 30 бар (время взаимодействия: 16 часов) с использованием рутениевых комплексов общей формулы [Ru(η5-2,4-DMP)(фосфорсодержащий лиганд)(NCMe)]BF4 в качестве катализатора, что приводит к неочищенной 2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I), как это перечислено в таблице 4.
|
Пример 18
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 0,66 мг [Ru(η5-2,4-DMP)((R)-(S)-PPF-PtBu2)(NCMe)]BF4 (0,0008 ммоля, S/C 3'000) и 5 мл дихлорметана. Получаемый таким образом раствор фиолетового цвета перемешивают в течение 2 часов при КТ. После этого добавляют 1,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7- ил}акриловой кислоты (2,30 ммоля), 2,5 мл дихлорметана, 7,5 мл ТГФ и 0,06 мл (S)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при перемешивании при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,5% (степень превращения 99,9%) и энантиомерной чистотой 89%.
Пример 19
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 0,66 мг [Ru(η5-2,4-DMP)((R)-(S)-PPF-PtBu2)(NCMe)]BF4 (0,0008 ммоля, S/C=3000) и 5 мл дихлорметана. Получаемый таким образом раствор фиолетового цвета перемешивают в течение 2 часов при КТ. После этого добавляют 1,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (2,30 ммоля), 10 мл дихлорметана и 0,06 мл (S)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при перемешивании при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к (R)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,5% (степень превращения 99,9%) и энантиомерной чистотой 90%.
Сравнительный пример А
В герметизированном боксе с перчатками (содержание кислорода ≤2 м.д.) загружают в автоклав из нержавеющей стали объемом 50 мл 0,62 мг [Ru(OAc)2((5)-TMBTP)] (0,0008 ммоля, S/C=3000) (получаемый согласно европейскому патенту EP 1670792 B1; ТМВТР=2,2',5,5'-тетраметил-4,4'-бис(дифенилфосфино)-3,3'-битиофен) и 5 мл метанола. Получаемый таким образом раствор оранжевого цвета перемешивают в течение 2 часов при КТ. После этого добавляют 1,00 г (Z)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4 ил)этокси]бензо[b]тиофен-7-ил}акриловой кислоты (2,30 ммоля), 4 мл метанола, 6 мл ТГФ и 0,06 мл (S)-1-фенилэтиламина (0,47 ммоля). Закупоривают автоклав и осуществляют гидрирование при перемешивании при температуре 40°C и давлении водорода 30 бар. По прошествии 16 часов открывают автоклав и досуха выпаривают желтоватый раствор на роторном испарителе (50°C/5 мбар), что приводит к неочищенной (S)-2-метокси-3-{4-[2-(5-метил-2-фенилоксазол-4-ил)этокси]бензо[b]тиофен-7-ил}пропионовой кислоте (кислота I) в виде твердого вещества белого цвета с химической чистотой 99,7% (степень превращения 99,9%) и энантиомерной чистотой 89%.

