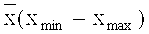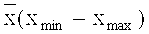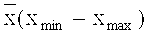Результат интеллектуальной деятельности: АНТИБАКТЕРИАЛЬНОЕ СРЕДСТВО И СПОСОБ ЛЕЧЕНИЯ КИШЕЧНОГО ИЕРСИНИОЗА ИЛИ ПСЕВДОТУБЕРКУЛЕЗА ИЛИ ЭШЕРИХИОЗА
Вид РИД
Изобретение
Изобретение относится к области экспериментальной медицины, инфектологии и микробиологии и может быть использовано для повышения колонизационной резистентности слизистой оболочки кишечника чувствительного организма к патогенным бактериям и предотвращения развития кишечной инфекции.
В ходе длительной коэволюции человеческого организма и микроорганизмов сформировался единый микробно-тканевой комплекс, объединяющий микроорганизмы и стенку кишечника человека. Функционирование этого комплекса связано с работой самого кишечника, находящегося под постоянным нейро-гуморальным контролем, и с жизнедеятельностью многих видов микроорганизмов, между которыми установились весьма определенные иерархические взаимоотношения [Олескин А.В. Надорганизменный уровень взаимодействия в микробных популяциях // Миробиология. - 1993. - Т. 62, вып. 3. - С. 389-405].
Многочисленные функции микробно-тканевого комплекса, связанные с трофическим и энергетическим обеспечением организма, регулированием дифференцировки и регенерации тканей, детоксикацией и выведением токсических веществ, стимуляцией иммунной системы и выработкой иммуноглобулинов и т.д., во многом определяют состояние здоровья или болезни [Минушкин О.Н., Ардатская М.Д., Дубинин А.В. Дисбактериоз кишечника // Рос. мед. журнал. - 1999. - №3. - С. 40-45]. При рассогласовании взаимоприемлемых отношений между микрофлорой и слизистой оболочкой кишечника и возникновении микроэкологических нарушений в нем с неизбежностью наступает расстройство пищеварения, нарушение детоксикации и выделения токсических веществ, нарушение регуляции гомеостаза, кроветворения, иммунной защиты [Kelly D., Conway S., Aminov R. Commensal gut bacteria: mechanism of immune modulation // Trends Immunol. - 2005. - Vol.26. - P. 326-333].
На протяжении многих лет с целью восстановления нормальной кишечной микрофлоры при дисбиотических состояниях применяли пробиотикотерапию. Сами по себе пробиотики - это безвредные (непатогенные) микроорганизмы, которые при введении в организм в определенных дозах могут оказывать на него положительное влияние [Sanders М.Е., Gibson G., Gill H.C. et al. Probiotics: their potential to impact human health. Council for Agricultural Science and Technology (CAST). Issue Paper, CAST, Ames, 2007. 20 р.]. Но даже при длительном применении пробиотиков, как об этом свидетельствует опыт клиницистов, их положительный эффект носит временный характер или полностью отсутствует [Токарева Н. Коррекция и профилактика дисбактериоза // Эффективная фармакотерапия. - 2011. - №3. - С.77-84]. Сочетанное применение при дисбактериозе пробиотикотерапии и антибиотикотерапии существенным образом ситуацию не изменило [Шевелева М.А., Раменская Т.В. Современные представления о применении различных групп пробиотических средств при антибиотикотерапии // Антибиотики и химиотерапия. - 2009. - Т.54, №3-4. - С.61-68; Андреева И.В. Когда следует назначать пробиотики? // Клин, микробиол. антимикроб, химиотер. - 2011. - Т.13, №3. - С.279-282]. И это вполне объяснимо. Ряд пробиотических микроорганизмов, входящих в состав коммерческих препаратов, чувствительны ко многим антибактериальным препаратам. С другой стороны, антибактериальным препаратам присущи побочные эффекты, такие как аллергические проявления, токсические воздействия на живой организм, а также явления, связанные с химиотерапевтическим эффектом самих антибактериальных препаратов, что, в свою очередь, не содействует улучшению состояния больного и выздоровлению. Указанные обстоятельства привели к пересмотру концепции пробиотикотерапии [Чичерин И.Ю., Погорельский И.П., Дармов И.В., Лундовских И.А., Гаврилов К.Е. Пробиотики: вектор развития // Практическая медицина. - 2012. - №3 (58). - С.180-188]. Коммерческие пробиотические препараты, поступающие в аптечную сеть, стали рассматриваться в качестве первого поколения препаратов для коррекции микроэкологических нарушений в кишечнике, а сами пробиотические микроорганизмы - стартовыми штаммами, продуцирующими метаболиты и/или сигнальные молекулы с определенной структурой, на основе которых планируется создание метабиотиков для предотвращения и лечения заболеваний кишечника, сопровождающихся нарушением качественного и количественного состава кишечной микрофлоры [Shenderov В.А. Metabiotics: novel idea or natural development of probiotic conception // Microbial Ecology in Health and Disease. - 2013. - Vol.24: 20399 - http://dx.doi.org/10.3402/mehd.v24i0.20399].
В практическом плане, с точки зрения реализации идеи использования микробных метаболитов для восстановления кишечной микрофлоры, важное значение имеют экспериментальные данные, в ходе которых был изучен состав надосадочной жидкости нативной культуры Lactobacillus plantarum 8Р-А3, определена ее антибактериальная активность в опытах in vitro и установлена протективная эффективность при заражении конвенциональных белых мышей бактериями псевдотуберкулеза и кишечного иерсиниоза [Чичерин И.Ю., Погорельский И.П., Лундовских И.А., Дармов И.В., Маракулин И.В. Оценка возможности профилактики, лечения и коррекции дисбиотических нарушений кишечной микрофлоры при экспериментальном псевдотуберкулезе // Журн. инфектологии. - 2012. - Т.4, №4. - С.71-79]. Полученные результаты дают основание полагать, что микробные метаболиты можно использовать для повышения колонизационной резистентности слизистой оболочки кишечника, нормализации дисбиотических изменений кишечной микрофлоры и, в конечном счете, предотвратить адгезию, колонизацию и диссеминацию патогенных кишечных бактерий и развитие инфекционного процесса, для лечения болезней кишечника, вызванных патогенными бактериями. Так, известен способ получения иммуноглобулинового препарата для профилактики и терапии бактериальных и вирусных инфекций, а также иммуноглобулиновый препарат для профилактики указанных инфекций и суппозитории на основе иммуноглобулинового препарата [патент RU 2255766]. Область применения этого препарата достаточно ограничена, а для его получения требуется специальное оборудование и доноры (животные или люди) для выделения из их крови иммуноглобулинов. К недостаткам этого изобретения следует отнести необходимость осуществления стерилизации иммуноглобулинового препарата, содержащего иммуноглобулины IgG, IgA и IgM, с использованием γ-облучения с мощностью поглощенной дозы 3-6 кГр·ч-1, суммарной дозой 12-30 кГр.
Наиболее близким к предлагаемому по совокупности существенных признаков является изобретение [заявка на изобретение 2010133050/15 от 06.08.2010], в котором описано комплексное лекарственное средство для лечения бактериальных инфекций и способ лечения бактериальных инфекций. Само комплексное лекарственное средство содержит активированную потенцированную форму антител к гамма-интерферону человека, активированную потенцированную форму антител к CD4 рецептору и активированную потенцированную форму антител к гистамину. Комплексное лекарственное средство и способ лечения предлагаются для применения при таких бактериальных инфекциях, как псевдотуберкулез, коклюш, иерсиниоз, а также пневмония различной этиологии, включая атипичных возбудителей. Способ получения комплексного лекарственного средства предусматривает получение активированных потенцированных водных или водно-спиртовых растворов антител к гамма-интерферону человека, антител к CD4 рецептору и антител к гистамину, активность которых обусловлена процессом последовательного многократного разведения матрично-исходных растворов антител в водном или водно-спиртовом растворителе в сочетании с внешним механическим воздействием - вертикальным встряхиванием каждого разведения. Как свидетельствует многолетняя инфектологическая практика, рабочие активированные потенцированные растворы, приготовленные, по существу, по гомеопатической технологии, не будут эффективны при таких разных инфекционных заболеваниях. Действительно, псевдотуберкулез, кишечный иерсиниоз, коклюш, атипичные пневмонии отличаются по этиологическому агенту, т.е. возбудителю, вызывающему конкретное инфекционное заболевание. Биологические свойства возбудителей, относящихся к разным видам, как и патогенность, сильно отличаются; возбудители проникают в чувствительный организм разными путями; патогенез вызываемых заболеваний совершенно различный, требующий совершенно разного как этиотропного, так и симптоматического лечения.
Кроме того, технология получения рабочих активированных потенцированных растворов антител отличается многократностью разведения при встряхивании, согласно гомеопатической технологии, что может привести к повторению их контаминирования различными микроорганизмами, в том числе условно-патогенными. Данное обстоятельство предполагает проведение контроля обсемененности препаратов посторонними микроорганизмами (или установления предельно допустимой их концентрации).
Задачей изобретения является создание антибактериального средства и разработка способа его применения с целью профилактики и лечения кишечных инфекций бактериальной природы.
Технический результат, который может быть достигнут при использовании предлагаемого антибактериального средства и способа его применения, заключается в обеспечении высокого уровня колонизационной резистентности слизистой оболочки кишечника вследствие сохранения и поддержания локальной иммунной толерантности, предотвращающей адгезию, инвазию и транслокацию возбудителей кишечных инфекций через кишечную стенку в капилляры кровеносной системы, по которым они разносятся по всему организму. Вследствие высокой колонизационной резистентности слизистой оболочки кишечника, достигаемой с помощью предлагаемого антибактериального средства, возбудители кишечных инфекций не прикрепляются к эпителиоцитам слизистой оболочки, не размножаются и не колонизируют ее, а в процессе перистальтических сокращений кишечника вместе с кишечным содержимым удаляются из организма.
Поставленная задача решается предлагаемым антибактериальным средством, включающим молочную кислоту, калий фосфорнокислый одно-замещенный, аминокислоты (валин, треонин, аспарагиновая кислота), жирные кислоты (масляная, пропионовая, бутандиоловая), сорбит, галактозу, витамины B1, В5 при следующем соотношении компонентов (масс.%):
|
аминокислоты
|
жирные кислоты
|
Стерилизацию раствора проводят с помощью фильтрования через фильтр («Владисарт», Россия) с диаметром пор 0,22 мкм.
Существенным отличием предлагаемого антибактериального средства является наличие в его составе молочной кислоты, калия фосфорнокислого однозамещенного, аминокислот, жирных кислот, многоатомного спирта, углевода и витаминов В1 и В5.
Как отмечается в работе [Глушанова Н.А. Биологические свойства лактобацилл // Бюл. сибирской медицины. - 2003. - №4. - С.50-58], молочная кислота, продуцируемая лактобациллами, является наиболее важным антибактериальным фактором, который, наряду с другими продуктами метаболизма, высоко активен в отношении патогенных и условно-патогенных микроорганизмов (сальмонелл, эшерихий, псевдомонад, стафилококков и др.). Именно молочная кислота является основным компонентом (70-80%) из всех компонентов нативной культуры лактобацилл, определяемых хроматографически, которые в совокупности обладают выраженным антибактериальным действием в отношении патогенных бактерий псевдотуберкулеза и кишечного иерсиниоза как в опытах in vitro, так и в опытах in vivo [Чичерин И.Ю., Погорельский И.П., Лундовских И.А., Дармов И.В., Малов А.А. Антибактериальная активность и состав надосадочной жидкости нативной культуры Lactobacillus plantarum 8Р-А3 // Журн. Междунар. Медицины. - 2013. - №1 (2). - С.131-139].
Описание способа
Конвенциональным белым мышам вводят через рот (per os) суспензию бактерий, вызывающих кишечное заболевание. Вводимая доза бактерий составляет 10 среднесмертельных доз (10LD50), гарантирующая развитие у животных манифестной формы кишечного заболевания. Предлагаемое антибактериальное средство вводят per os инфицированным животным через 2 часа после инфицирования при профилактическом курсе или через 24 часа при лечебном курсе терапии бактериальной инфекции. Контрольным группам животных предлагаемое антибактериальное средство не вводят. Диагностируют заболевание животных с использованием бактериологического метода и путем выявления значимых симптомов болезни. Вынесение суждения об эффективности перорального введения предлагаемого антибактериального средства инфицированным животным производят на основании улучшения их самочувствия и выздоровления, а также выделения из внутренних органов погибших в опытах животных чистой культуры бактерий, которыми были заражены подопытные животные. Выделение из внутренних органов бактерий, вызвавших заболевание животных и их гибель, свидетельствует о генерализации инфекции.
Предлагаемое антибактериальное средство, имитирующее метаболиты лактобактерий, образующиеся при их выращивании в жидкой питательной среде в микроаэрофильных условиях, оказывает ингибирующее влияние на патогенные бактерии в кишечнике при одновременном стимулирующем влиянии на собственную кишечную микрофлору и локальную иммунную систему с выработкой секреторных иммуноглобулинов, тем самым повышая барьерную функцию слизистой оболочки кишечника и предотвращая развитие кишечной инфекции.
Возможность осуществления заявляемого изобретения показана на следующих примерах.
Пример 1.
Готовят антибактериальное средство при следующем количественном соотношении компонентов (масс.%):
|
аминокислоты
|
жирные кислоты
|
Выбирают штамм возбудителя псевдотуберкулеза - острой зоонозной бактериальной инфекции, при септической форме которой летальность достигает 70% и больше. Выращивают культуру выбранного штамма псевдотуберкулезного микроба при температуре (5±3)°C в течение 4 суток, после чего готовят бактериальную суспензию на изотоническом растворе хлорида натрия, исходя из расчета концентрации бактерий 10LD50 в водимом объеме суспензии для перорального заражения животных. Указанная концентрация бактерий, равная 10 среднелетальным дозам псевдотуберкулезного микроба, обеспечивает гарантированное развитие инфекционного процесса при пероральном введении бактериальной суспензии.
Берут 3 группы конвенциональных белых мышей массой 18-20 г, рассаживают по 10 животных в 3 кювета с крышками. Животным трех групп (двух опытных и одной контрольной) вводят перорально суспензию бактерий псевдотуберкулезного микроба в объеме 0,2 мл, содержащем 10LD50 бактерий возбудителя. Животным первой опытной группы через 2 часа после инфицирования перорально вводят антибактериальное средство в объеме 0,2 мл; в последующем антибактериальное средство в том же объеме вводят на протяжении 7 дней.
Животным второй опытной группы пероральное введение антибактериального средства в объеме 0,2 мл начинают через 24 часа после инфицирования бактериями псевдотуберкулезного микроба и продолжают в течение 7 дней.
Животные третьей группы являются контрольными: им не проводят ни профилактический, ни лечебный курс антибактериальным средством.
Наблюдение за всеми животными проводят в течение 21 дня, отмечая исход инфицирования. В случае гибели инфицированных животных проводят паталогоанатомическое исследование и выделение из внутренних органов культуры псевдотуберкулезного микроба. В таблице 1 приведены результаты инфицирования конвенциональных белых мышей.
Представленные в таблице 1 данные свидетельствуют о том, что в результате инфицирования возбудителем псевдотуберкулеза все подопытные животные контрольной группы погибли в срок от 5 до 15 суток от начала введения per os суспензии бактерий псевдотуберкулеза. При этом от всех погибших животных из внутренних органов выделена чистая культура псевдотуберкулезного микроба, а также из фекалий животных в количестве 2,6·107-6,6·107 КОЕ·г-1. Животные обеих опытных групп, которым перорально вводили антибактериальное средство в режиме профилактического и лечебного курсов, оказались защищенными от патогенных иерсиний и не погибли.
Пример 2.
Готовят антибактериальное средство при следующем количественном соотношении компонентов (масс.%):
|
аминокислоты
|
жирные кислоты
|
Выбирают штамм возбудителя кишечного иерсиниоза - зоонозной бактериальной инфекции с выраженным полиморфизмом клинических проявлений и поражением желудочно-кишечного тракта. Выращивают культуру выбранного штамма бактерий кишечного иерсиниоза при температуре 28°C в течение 2 суток, после чего готовят бактериальную суспензию на изотоническом растворе хлорида натрия, исходя из расчета концентрации бактерий 10LD50 в водимом объеме суспензии для перорального заражения животных. Указанная концентрация бактерий, равная 10 среднелетальным дозам бактерий кишечного иерсиниоза, обеспечивает гарантированное развитие инфекционного процесса при пероральном введении бактериальной суспензии.
Берут 3 группы конвенциональных белых мышей массой 18-20 г, рассаживают по 10 животных в 3 кювета с крышками. Животным трех групп (двух опытных и одной контрольной) вводят перорально суспензию бактерий кишечного иерсиниоза в объеме 0,2 мл, содержащем 10LD50 бактерий возбудителя. Животным первой опытной группы через 2 часа после инфицирования перорально вводят антибактериальное средство в объеме 0,2 мл; в последующем антибактериальное средство в том же объеме вводят на протяжении 7 дней.
Животным второй опытной группы пероральное введение антибактериального средства в объеме 0,2 мл начинают через 24 часа после инфицирования бактериями кишечного иерсиниоза и продолжают в течение 7 дней.
Животные третьей группы являются контрольными: им не проводят ни профилактический, ни лечебный курс антибактериальным средством.
Наблюдение за всеми животными проводят в течение 21 дня, отмечая исход инфицирования. В случае гибели инфицированных животных проводят паталогоанатомическое исследование и выделение из внутренних органов культуры бактерий кишечного иерсиниоза. В таблице 2 приведены результаты инфицирования конвенциональных белых мышей.
Представленные в таблице 2 данные свидетельствуют о том, что в результате инфицирования возбудителем кишечного иерсиниоза 9 из 10 подопытных животных контрольной группы погибли в срок от 8 до 17 суток от начала введения per os суспензии бактерий кишечного иерсиниоза. При этом от всех погибших животных из внутренних органов выделена чистая культура бактерий кишечного иерсиниоза, а также из фекалий животных в количестве 6,8·105-7,1·105 КОЕ·г-1. Животные обеих опытных групп, которым перорально вводили антибактериальное средство в режиме профилактического и лечебного курсов, оказались защищенными от патогенных иерсиний и не погибли.
Следует отметить, что из 10 инфицированных животных контрольной группы одно животное не погибло, что, очевидно, связано с биологическими особенностями бактерий кишечного иерсиниоза, в частности, с меньшей патогенностью в сравнении с бактериями псевдотуберкулеза.
Пример 3.
Готовят антибактериальное средство при следующем количественном соотношении компонентов (масс.%):
|
аминокислоты
|
жирные кислоты
|
Выбирают штамм диареегенного энтероинвазивного возбудителя эшерихиоза - острой инфекционной болезни, протекающей с клинической картиной острого гастроэнтерита или энтероколита. Выращивают культуру выбранного штамма эшерихий при температуре 37°C в течение 2 суток, после чего готовят бактериальную суспензию на изотоническом растворе хлорида натрия, исходя из расчета концентрации бактерий 10LD50 в водимом объеме суспензии для перорального заражения животных. Указанная концентрация бактерий, равная 10 среднелетальным дозам бактерий возбудителя эшерихиоза, обеспечивает гарантированное развитие инфекционного процесса при пероральном введении бактериальной суспензии.
Берут 3 группы конвенциональных белых мышей массой 18-20 г, рассаживают по 10 животных в 3 кювета с крышками. Животным трех групп (двух опытных и одной контрольной) вводят перорально суспензию эшерихий в объеме 0,2 мл, содержащем 10LD50 бактерий возбудителя. Животным первой опытной группы через 2 часа после инфицирования перорально вводят антибактериальное средство в объеме 0,2 мл; в последующем антибактериальное средство в том же объеме вводят на протяжении 7 дней.
Животным второй опытной группы пероральное введение антибактериального средства в объеме 0,2 мл начинают через 24 часа после инфицирования суспензией эшерихий и продолжают в течение 7 дней.
Животные третьей группы являются контрольными: им не проводят ни профилактический, ни лечебный курс антибактериальным средством.
Наблюдение за всеми животными проводят в течение 21 дня, отмечая исход инфицирования. В случае гибели инфицированных животных проводят паталогоанатомическое исследование и выделение из внутренних органов культуры бактерий кишечного иерсиниоза. В таблице 3 приведены результаты инфицирования конвенциональных белых мышей.
Представленные в таблице 3 данные свидетельствуют о том, что в результате инфицирования возбудителем эшерихиоза 8 из 10 подопытных животных контрольной группы погибли в срок от 8 до 17 суток от начала введения per os суспензии энтероинвазивных эшерихий. При этом от всех погибших животных из внутренних органов выделена чистая культура эшерихий, а также из фекалий животных в количестве 3,7·105-4,1·105 КОЕ·г-1. Животные обеих опытных групп, которым перорально вводили антибактериальное средство в режиме профилактического и лечебного курсов, оказались защищенными от патогенных иерсиний и не погибли.
Из 10 инфицированных энтероинвазивными эшерихиями животных контрольной группы двое не погибли, что следует связать с биологическими особенностями эшерихий: лишь энтерогеморрагические штаммы могут вызвать в 3-5% случаев летальный исход.
Заявленное антибактериальное средство и способ его применения для лечения кишечных инфекций бактериальной природы позволяют сохранить экологическое преимущество микроорганизмам собственной кишечной микрофлоры и, тем самым, повысить колонизационную резистентность слизистой оболочки кишечника. Сохранение количественного и качественного состава кишечной микрофлоры в сочетании с локальной выработкой иммуноглобулинов в ответ на стимуляцию иммунной системы обеспечивают состояние невосприимчивости к патогенным бактериям, попадающим в желудочно-кишечный тракт и вызывающим инфекционный процесс.
|
|
|