Результат интеллектуальной деятельности: ВЕЩЕСТВО, СТИМУЛИРУЮЩЕЕ ЭКСПРЕССИЮ ГЕНА КОАКТИВАТОРА PGC-1α
Вид РИД
Изобретение
Изобретение относится к биологии и медицине, а именно к биохимии и фармакологии, и может быть использовано для повышения работоспособности поперечно-полосатой мускулатуры, например при утомлении либо при атрофиях.
Мышечная и нервная ткани играют центральные роли в реализации физической активности и контроле пределов переносимости нагрузок. Одним из базовых процессов при этом является рост числа и общей метаболической активности митохондрий, например миоцитов. Среди известных факторов стимуляции функций митохондрий, кроме упражнений и применения ограничений калорийности пищи, можно указать на ряд препаратов природного происхождения - природные флавоноиды, ресвератрол и др. (Rahman S. and Hanna M.G. Diagnosis and therapy in neuromuscular disorders: diagnosis and new treatments in mitochondrial diseases // J Neurol Neurosurg Psychiatry, 2009, 80: 943-953; Lira V.A., Benton C.R., Yan Z, Bonen A. PGC-1 alpha regulation by exercise training and its influences on muscle function and insulin sensitivity //. Am J Physiol Endocrinol Metab. 2010, 299(2): E145-161; Wallace D.C. A mitochondrial paradigm of metabolic and degenerative diseases, aging, and cancer: a dawn for evolutionary medicine //. Ann Rev Genetics 2005, 39: 359-407; Saft C., Andrich J., Wieczorek S., Arning L., Taherzadeh-Fard E. PGC-1 alpha as modifier of onset age in Huntington disease // Molecular Neurodegeneration 2009, 4: 1750-1756; Lagouge M, Argmann C, Gerhart-Hines Z, Meziane H, Lerin C, Daussin F, et al. Resveratrol improves mitochondrial function and protects against metabolic disease by activating SIRT1 and PGC-1 alpha. // Cell 2006; 127: 1109-1122).
Из научной литературы известно о методах исследования регуляции гена, определяющего биогенез митохондрий, пути катаболизма углеводов и жиров в клетке (гомеостаз холестерина и степень ожирения организма) в ответ на внешние стимулы (Little J.P., Safdar A., Cermak N., Tarnopolsky M.A., Gibala M.J. Acute endurance exercise increases the nuclear abundance of PGC-1 alpha in trained human skeletal muscle // Am J Physiol Regul Integr Comp Physiol, 2010; 298(4): R912-917; Consitt L.A., Bell J.A., Koves T.R., Muoio D.M., Hulver M.W., Haynie K.R., Dohm G.L., Houmard J.A. Peroxisome proliferator-activated receptor-gamma coactivator-1 alpha overexpression increases lipid oxidation in myocytes from extremely obese individuals // Diabetes, 2010; 59(6):1407-1415; Holloway G.P., Bonen A., Spriet L.L. Regulation of skeletal muscle mitochondrial fatty acid metabolism in lean and obese individuals // Am J Clin Nutr. 2009, 89(1): 455S-462S).
В настоящее время обнаружены специфические факторы, играющие роль активаторов и коактиваторов ключевых комплексов генов, запускающих каскад процессов биогенеза митохондрий, включения или/и выключения метаболических путей распада или ресинтеза жиров и углеводов, разработаны и испытываются препараты, в сотни раз усиливающие эффект природных стимуляторов. При этом известно, что активация продукта гена коактиватора путем специфической модификации включает адаптивные системы организма, препятствующие развитию сердечно-сосудистых заболеваний, диабета, миопатий (Finck B.N., Kelly D.P. Peroxisome proliferator-activated receptor gamma coactivator-1 (PGC-1) regulatory cascade in cardiac physiology and disease. Circulation // 2007, 115(19): 2540-2548). Эти патологии, в свою очередь, тесно связаны с биогенезом митохондрий, а также регуляцией путей распада и синтеза глюкозы и липидов. Важная роль в этих процессах принадлежит ядерным рецепторам пролифератору пероксисом (PPARγ), которые являются переносчиками регуляторных сигналов на комплекс транскрипционных факторов. Ключевая роль в запуске процессов принадлежит коактиватору 1 альфа этих рецепторов, причем стимуляция экспрессии гена коактиватора-1-альфа резко ускоряет процессы биогенеза митохондрий (Langenickel I., Bao J., Joseph J.J., Schwartz D.R., Mantell B.S., Xu X., Raghavachari N., Sack M.N. PGC-1 alpha integrates insulin signaling, mitochondrial regulation, and bioenergetic function in skeletal muscle // J. Biol. Chem. 2008, 283 (33): 22464-22472; Sugden M.C., Caton P.W., Holness M.J. PPAR control: it′s SIRTainly as easy as PGC // J. Endocrinol., 2010, 204(2): 93-104).
Наиболее близким по своей сущности и достигаемому эффекту к предлагаемому веществу, которое стимулирует экспрессию гена коактиватора PGC-1α, является трекрезан (пат. РФ №2460524, МПК A61K 31/205, A61P 21/00, 2012 г.), принимаемый здесь в качестве прототипа.
Трекрезан - родоначальник нового класса адаптогенов и иммуномодуляторов, который относится к триэтаноламмониевым солям ароксиуксусных кислот, имеющим протатрановую структуру, уменьшающим пораженность эластических волокон и стабилизирующим клеточные мембраны (Воронков М.Г., Расулов М.М. // Хим.-фарм. Ж., 2007, №1, с. 3-9; Воронков М.Г., Мирскова А.Н., Расулов М.М. Иммуномодуляторная эффективность трекрезана // Химико-фармацевтический ж., 2007, №5, с. 7-11).
Задачей настоящего изобретения является использование известного биологически активного соединения в качестве вещества, повышающего стимулирующие и регуляторные функции ключевых генов и их продуктов, лежащих в основе запуска регуляторных процессов биогенеза митохондрий.
Поставленная задача достигается тем, что в качестве активатора биогенеза митохондрий применяют биологически активное соединение - комплекс трис-(2-гидроксиэтил)амина с бис-(2-метилфеноксиацетатом) цинка (цинкотран) формулы: (HOCH2CH2)3N·Zn(OOCCH2OC6H4-CH3-2)2
Впервые показано, что введение цинкатрана стимулирует экспрессию гена коактиватора PGC-1α. Новая физиологическая активность цинкатрана - стимулировать экспрессию гена коактиватора PGC-1α - не была известна ранее и в литературе не описана.
Трикрезан и цинкатран относятся к одной группе протатранов, чем объясняется схожесть биологического воздействия, однако наличие цинка в молекуле цинкотрана усиливает это воздействие.
Возможность осуществления изобретения может быть проиллюстрирована следующими представленными ниже примерами.
Пример 1.
Эксперименты проводят на крысах (n=45) линии Вистар массой 180-200 г. Животные делят на 3 группы: первая получает раствор цинкатрана из расчета 5 мг/кг массы внутрибрюшинно, в течение 7 дней, вторая получает трекрезан (препарат сравнения) из расчета 10 мг/кг массы внутрибрюшинно в течение 7 дней. Крысы третьей группы контрольные и получают эквиобъемную инъекцию физиологического раствора в те же часы, когда производится инъекция испытуемого препарата (плацебо), также в течение 7 дней.
Крысы содержатся в стандартных условиях. Работа выполняется с соблюдением принципов Хельсинкской декларации о гуманном отношении к животным. Наблюдения проводят в дневное время (с 11 до 15 ч).
Статическую работоспособность оценивают при подвешивании крыс на горизонтальный экран-сетку. Крыс помещают на горизонтальную сетку, плавно отпускают, экран переворачивают, при этом животное пытается удержаться, противодействуя силе тяжести. Животное остается висеть, зацепившись за сетку лапами. Регистрируют длительность удержания животного на сетке. Если в течение трех минут крыса падает вниз, ее снова сажают на сетку, в общей сложности до трех раз. Подсчитывают суммарное время удержания по всем трем повторам вместе и латентность первого падения.
Динамическую работоспособность животных определяют в тесте принудительного плавания. Учитывают продолжительность плавания крыс с грузом (8% от массы тела) до появления первых признаков утомления (5, 16 = Бобков Ю.Г., Виноградов В.М., Катков В.Ф. и др. Фармакологическая коррекция утомления. - М.: Медицина, 1984. - 208 с.).
После курса воздействия цинкатрана и плацебо животных декапитируют для взятия образцов тканей. Быстро извлекают 100-200 мг мышечной ткани, выделяют препарат суммарной мРНК и рассматривают экспрессию ключевого гена (в частности - PCG-1α) биогенеза митохондрий, методом ПЦР в реальном времени (РТ-ПЦР).
Статистическую обработку данных проводят с использованием общепринятых методов (Зайцев Г.Н. Математический анализ биологических данных. - М.: Наука, 1991. - 184 с.).
Для выделения препарата суммарной мРНК используют гуанидинизотиоцианатный метод. Поперечно-полосатые мышцы (100 мг мышц бедра) гомогенизируют растиранием после быстрого замораживания в жидком азоте в присутствии 1 мл препарата Trizol®Reagent (фирма Invitrogen, USA) в соответствии с протоколом производителя. Гомогенат инкубируют при 15-30°C в течение 5 мин для полной диссоциации белково-нуклеиновых комплексов. Добавляют 0,2 мл хлороформа на 1 мл препарата TRIzol, встряхивают 15 с и инкубируют 2 мин при 15-30°C. Затем гомогенат центрифугируют 15 мин при 12000 g при 2-8°C. Супернатант переносят в стерильную пробирку и осаждают РНК, добавляя равный объем изопропанола, инкубируют при 15-30°C в течение 10 мин и центрифугируют 10 мин при 12000 g при 2-8°C. Осадок РНК промывают 75% спиртом, высушивают на воздухе и растворяют в бидистиллированной воде, содержащей 0,5% SDS, затем инкубируют при 55°C в течение 10 мин и замораживают при -70°C. Аликвоту в 2,5 мкл препарата выделенной мРНК растворяют в бидистиллированной воде, обработанной диэтилпирокарбонатом и спектрофотометрически при 260 нм оценивают количество. Качество препаратов мРНК оценивают по соотношению 260:280 - препараты с соотношением больше 1,6 берут для дальнейшего анализа. Суммарный препарат мРНК подвергают процедуре обратной транскрипции. Для получения кДНК в реакционную смесь в объеме 50 мкл добавляют 1,5-2,0 мкг мРНК; 5 мкл модифицированного десятикратного РТ буфера «Сибэнзим», обеспечивающего конечные концентрации MgCl2 - 25 мМ; 10 мкл смеси dNTP до конечной концентрации - 1,5 мМ; 2,5 мкл смеси гексапраймеров фирмы Силекс М (для «рэндом» обратной транскрипции мРНК); 1 мкл ингибиторов РНКаз и добавляют 0,5 мкл препарата обратной транскриптазы фирмы «Сибэнзим» (200 ед.акт. в 1 мкл). Реакцию проводят при 25°C в течение 10 мин, затем 60 мин при 37°C и 5 мин при 95°C. Затем препарат быстро охлаждают в ледяной бане и хранят при -20°C не более 2-3 суток.
Анализ экспрессии генов участвующих в реакциях биогенеза митохондрий. Специфическую экспрессию гена PGC-1α исследуют методом РТ-ПЦР (ПЦР в реальном времени) на приборе ДНК-технологии ДТ-322.
1. Синтез на матрице РНК кДНК. Для синтеза кДНК с использованием препаратов суммарной РНК применяют реактивы фирмы Силекс М и прилагающиеся протоколы. Для синтеза кДНК в пробирке, помещенной в лед, смешивают следующие компоненты:
- РНК матрица - 2 мкл (тотальная РНК 0.1-5 мкг) (поли(А)+РНК 10-0,5 нг или специфическая РНК - 0.01 пг и менее)
- праймер - 1 мкл (специфический 15-20 пмолей, случайный гексапраймер 0,5 нг),
- вода, свободная от РНКаз, - до 18 мкл.
Перемешивают центрифугированием 30 с при 10000 g. Смесь инкубировали 5 мин при 70°C, переносят пробирку в лед, затем центрифугируют 30 с при 10000 g.
Помещают пробирку в лед и добавляют:
- ×10-кратный ОТ буфер (фирма «Силекс-М» - 2,5 мкл;
- 1,5 мМ смесь дезоксинуклеотидтрифосфатов (dNTP) - 4 мкл;
- обратная транскриптаза вируса лейкемии мышей Молони - M-MLV (Moloney Murine Leukemia Virus) - 0,5 мкл (100 ед. акт., «Сибэнзим»).
Смесь инкубируют в течение 60 мин при 37°C (при использовании случайных гексапраймеров перед инкубацией при 37°C смесь инкубируют в течение 10 мин при 25°C). Реакцию останавливают прогреванием смеси в течение 10 мин при 70°C. Смесь переносят в лед. Полученную кДНК используют либо сразу же для проведения РТ ПЦР, либо для синтеза второй цепи и последующего клонирования. Хранят полученную кДНК при -20°C либо при -70°C.
2. Количественный анализ специфической мРНК коактиватора-1-альфа гамма-рецептора (PGC-1α). Количественный анализ экспрессии гена PGC-1α проводят через оценку уровня специфической мРНК. Критерием уровня мРНК служат количественный анализ суммарной кДНК, проводимый методом РТ-ПЦР. Реакцию РТ ПЦР проводят с использованием наборов реактивов фирмы «Синтол» (Комплект реагентов для проведения ПЦР-РВ в присутствии SYBR Green I Кат. № R-402). Количественное определение специфических кДНК для PGC-1 проводят на РТ-ПЦР приборе. Условия амплификации: смесь инкубируют 2 мин при 50°C, затем 10 мин при 95°C. После этого проводят амплификацию в следующем режиме - денатурация при 95°C в течение 15 с, отжиг и элонгация при 60°C - 60 с (сбор данных осуществляют на стадии полимеризации). Затравки конструируют по программе «Праймер Экспресс Версия 3.0»:
для β-актина:
- прямая = 5′-CTGGAACGGTGAAGGTGACA-3′
- обратная = 5′-CGGCCACATTGTGAACTTTG-3′;
для кДНК копии мРНК PGC-1α:
- прямая = 5′-GTGCAGCCAAGACTCTGTATGG-3′
- обратная = 5′-GTCCAGGTCATTCACATCAAGTTC-3′
Стандарты получают путем амплификации контрольных образцов в ПЦР реакции в условиях, оптимизированных для РТ-ПЦР. Измерения осуществляют относительно стандартных значений, проводя 4-кратные последовательные разбавления для получения стандартной кривой из 8 точек.
Экспоненциальная стадия PCR описывается уравнением:
 ,
,
где Pn - количество молекул продукта (величины репортерной флуоресценции) образовавшихся к циклу n, P0 - исходное количество молекул, содержащих амплифицируемый фрагмент, Е - эффективность амплификации. В идеальных условиях E=2, т.е. на каждом цикле цепной реакции происходит удвоение количества продукта. После логарифмирования обеих частей уравнения 1 можно преобразовать его к виду:

Пороговым циклом (threshold cycle, С(T)) называют такой цикл n, на котором достигается некий заданный уровень репортерной флуоресценции - пороговая флуоресценция PC(T)=const. Для n=С(T) уравнение 2 принимает вид:

Значение С(T) прямо пропорционально логарифму количества субстрата.
Таким образом, ПЦР-РВ позволяет сравнивать количества субстрата при условии, что эффективность реакции и заданный уровень пороговой флуоресценции одинаковы для каждой из сравниваемых реакций.
3. Определение содержания митохондрий в клетках мышц по содержанию митохондриальной ДНК (мтДНК).
Препарат мтДНК выделяют из мышц. Для этого 0,1 г мышц (преимущественно 4-главые мышцы бедра) измельчают из замороженного в жидком азоте состояния. Замороженный порошок ткани переносят в пробирку типа Эппендорф объемом 2 мл и добавляя 800 мкл буфер состава - 50 мМ Трис-HCl, pH 8,0, 25 мМ ЭДТА и 400 мМ NaCl, 100 мкл 10% SDS, и 20 мкл раствора протеиназы K (10 мг/мл). Смесь перемешивают и инкубируют при 65°C в течение 3 ч. После инкубации белки и клеточный дебрис осаждают добавлением 300 мкл 6 М NaCl, инкубируют при +4°C в течение 15 мин. Центрифугируют смесь при 16000 g в течение 10 мин. 500 мл надосадочной жидкости переносят в новый Эппендорф, содержащий 500 мкл раствора 8 М гуанидина гидрохлорида (pH 8,0) и 0,49 М ацетата аммония, и медленно перемешивают при комнатной температуре в течение 90 мин. Нуклеиновые кислоты осаждают добавлением 800 мкл холодного 100% изопропилового спирта с последующим центрифугированием при 10000 g в течение 5 мин. Осадок промывают 400 мкл 70% изопропилового спирта. После просушивания осадка его ресуспендируют в 150 мл ТЕ-буфера (10 мМ Трис-HCl, pH 8,0, 1 мМ ЭДТА и 50 мг/мл РНКазы («Сибэнзим»). Образцы ДНК хранят при t -20°C. Качество и концентрацию ДНК оценивают спектрофотометрически при 260 нм и электрофоретически.
Количественная оценка содержания мтДНК в мышечной ткани.
Количественный анализ мтДНК проводят методом количественной РТ ПЦР. Для этого используют препараты ДНК, выделенные из образцов ткани методом, изложенным в разделе 2.
Для проведения ПЦР в реальном времени используют реактивы фирмы «Синтол». Для анализа берут 10 нг образца ДНК на реакцию. Относительные количества ядерной и мтДНК определяют путем сравнения кинетики размножения выбранного фрагмента гена β-актина, локализованного в ядерном геноме, и митохондриального гена цитохрома b. Условия реакции: реакционная смесь в объеме 25 мкл содержит те же компоненты, что и при анализе специфической экспрессии PGC-1. ДНК добавляют в количестве 10 нг и затравки в количестве 50 нмоль. Условия реакции: смесь инкубируют 2 мин при 50°C, затем 10 мин при 95°C. Амплификация включает 40 циклов в режиме - денатурация при 95°C в течение 15 с, отжиг при 60°C в течение 20 с и элонгация при 72°C - 15 с (данные регистрируют на стадии полимеризации). Затравки конструируют с использованием программы «Праймер Экспресс Версия 3.0»
для β-актина:
- прямая = 5′-TCACCCACACTGTGCCCATCTACGA-3′
- обратная = 5′-ACCCACACTGTGCCCATCTAC-3′;
для цитохрома b:
- прямая = 5′-TATTCCTTCATGTCGGACGA-3′
- обратная = 5′-AAATGCTGTGGCTATGACTG-3′
Все реакции проводят в сериях по 3 раза. Анализ полученных данных проводят с использованием пакета программ SPSS 13.0 (SPSS Inc., США), позволяющего рассчитывать средние значения изменения уровней мРНК генов и стандартные ошибки. Данные считают достоверными при p<0,05.
Для количественного анализа содержания митохондрий в тканях мышц по митохондриальной ДНК значения CT (цикла пересечения с пороговой линией) для ядерного гена β-актина и митохондриального гена цитохрома b определяют в одном и том же амплификационном эксперименте.
В опытах наблюдают хорошую воспроизводимость в пределах одного и между разными повторными опытами. Значения CT используют как меру количества копий анализируемой последовательности ДНК в начале амплификации, а различия в значениях CT используют для количественной оценки числа копий мтДНК по отношению к копийности гена β-актина в соответствии с следующей формулой: Относительное количество копий (Rc)=2ΔCТ, где ΔCT - разница CT D-актина и CT цитохрома b.
Результаты. Установлено, что при введении цинкатрана в дозе уже 5 мг/кг работоспособность животных увеличивается (табл. 1). Применение цинкатрана в дозе 10 мг/кг усиливает этот эффект (табл. 1).
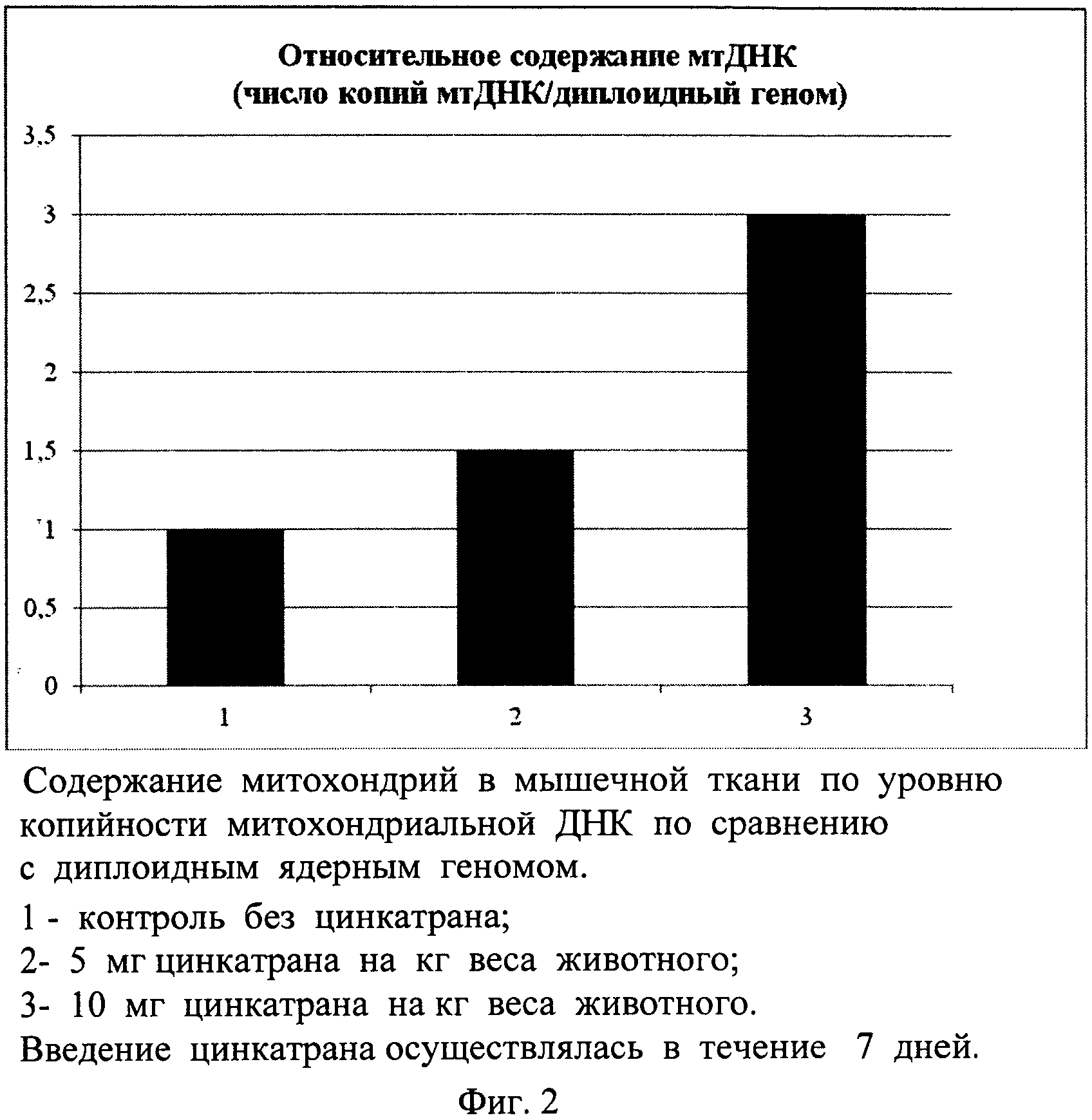
Соотношения между изучаемым геном - мишенью PGC-1α и мРНК β-актина - представлены на фиг. 1 и 2.
Из рисунков видно двукратное и более увеличение экспрессии гена PGC-1α в мышечных волокнах как при введении цинкатрана в дозе в 5 мг/кг массы, так и при введении препарата в дозе 10 мг/кг.
Таким образом, при введении раствора цинкатрана в дозе 10 мг/кг внутрибрюшинно в течение 7 дней достигается максимальная активация экспрессии гена PGC-1α в мышечных волокнах. Это значит, что применение цинкатрана стимулирует каскад реакций биогенеза митохондрий и увеличение их числа, и, соответственно, биоэнергетики миоцитов. Проведенные исследования доказывают возможность контроля числа митохондрий в миоцитах при помощи анализа количества митохондриальной ДНК, что имеет диагностическое значение.