Результат интеллектуальной деятельности: НОВЫЕ ПИПЕРАЗИНЫ В КАЧЕСТВЕ ПРОТИВОМАЛЯРИЙНЫХ СРЕДСТВ
Вид РИД
Изобретение
Настоящее изобретение относится к новым соединениям формулы I. Настоящее изобретение также относится к родственным вопросам, включая способы получения соединений, фармацевтические композиции, содержащие одно или большее количество соединений формулы I, и, в особенности, их применение в качестве лекарственных средств, предназначенных для лечения или предупреждения малярийных инфекций или для лечения или предупреждения других протозойных заболеваний, таких как сонная болезнь, болезнь Чагаса, амебиаз, лямблиоз, трихомониаз, токсоплазмоз и лейшманиоз.
Уровень техники
Многочисленные тяжелые заболевания, поражающие людей, а также домашних животных и домашний скот, вызваны протозойными микроорганизмами такими как, например, Kinetoplastida, Apicomplexa, Anaerobic Protozoa, Microsporidia и Plasmodium. Из этих заболеваний наиболее клинически значимым является малярия.
Малярия является одним из самых тяжелых и сложных заболеваний, поражающих человечество в 21 веке. Это заболевание поражает примерно 300 миллионов человек во всем мире и от него гибнут от 1 до 1,5 миллионов человек в год. Малярия является инфекционным заболеванием, вызываемым четырьмя видами протозойных паразитов Plasmodium, из этих четырех Р.falciparum является наиболее опасным. Все попытки разработать вакцины против Р.falciparum оказались неудачными. Поэтому терапевтическими и профилактическими средства борьбы с малярией ограничиваются лекарственными препаратами. Существуют несколько классов противомалярийных лекарственных средств. Наиболее широко использующимися являются хинолиновые противомалярийные средства, например, хлорхин, который является особенно эффективным лекарственным средством, применяющимся как для профилактики, так и для лечения. Однако резистентность по отношению ко многим имеющимся в настоящее время противомалярийным лекарственным средствам быстро развивается, что угрожает людям в зонах эпидемии малярии. Сообщения о штаммах малярийных паразитов, резистентных ко многим лекарственным средствам, делают поиски новых противомалярийных средств особенно необходимыми.
Р.falciparum попадает в организм человека с помощью укусов самки комара Anopheles (он также может передаваться при переливании крови от бессимптомных доноров; почти все инфицированные компоненты крови, включая эритроциты, тромбоцитарную массу, лейкоциты, криопреципитаты и свежую плазму, могут передавать малярию). Паразит Plasmodium первоначально размножается в печени и на последующих стадиях инфекционного цикла размножается в эритроцитах. На этой стадии паразит разрушает гемоглобин и использует продукты разрушения в качестве питательных веществ для роста.
Ограничения существующего арсенала противопротозойных химиотерапевтических средств подчеркивают необходимость новых лекарственных средств в этой области терапии. Настоящее изобретение относится к разработке новых обладающих низкой молекулярной массой, непептидных, нехинолиновых соединений формулы I, которые применимы для лечения и/или предупреждения протозойных инфекций, предпочтительно для лечения и/или предупреждения малярии, в частности, малярии, вызванной Plasmodium falciparum.
В WO 2007/046075 также раскрыты производные пиперазина в качестве противомалярийных средств. Соединением, предлагаемым в WO 2007/046075, которое является наиболее сходным с некоторыми соединениями, заявленными в настоящем изобретении, является соединение примера 54, которое в настоящем изобретении соответствует сравнительному соединению примера 1. Однако соединения, заявленные в настоящем изобретении, которые являются наиболее сходными по структуре с соединением примера 54, предлагаемым в WO 2007/046075, обладают активностью in vitro по отношению к штамму Р.falciparum NF54, находящемуся на эритроцитарных стадиях, в присутствии 50% сыворотки, значительно более высокой по сравнению с активностью соединения примера 54, предлагаемого в WO 2007/046075 (см. приведенную ниже таблицу 1).
Подробное описание изобретения:
i) Настоящее изобретение относится к новым соединениям формулы I:
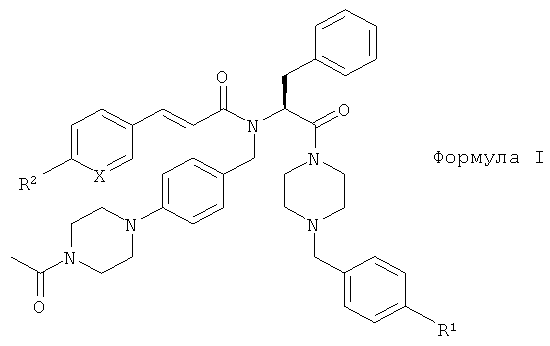
в которой
- Х обозначает СН или N;
R1 обозначает -NO2, -N(CH3)2 или -NCH3(CH2CH2OH); и
R2 обозначает водород, метил, этил, н-пропил, изопропил, трет-бутил, цианогруппу, галоген, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, метилсульфонил, ацетил или ацетиламиногруппу; или
- Х обозначает CH, R1 обозначает водород и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, метилсульфонил, ацетиламиногруппу или метоксикарбонил; или
- X обозначает CH, R1 обозначает цианогруппу и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, трифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает хлор и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает метоксигруппу или изопропоксигруппу и R2 обозначает трифторметил; или
- X обозначает CH, R1 обозначает метилсульфонил или этилсульфонил и R2 обозначает трифторметил, этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу или дифторметоксигруппу, предпочтительно трифторметил, трет-бутил, н-пропоксигруппу или изопропоксигруппу.
ii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления i), в которых
- X обозначает CH или N;
R1 обозначает -NO2, -N(CH3)2 или -NCH3(CH2CH2OH); и
R2 обозначает водород, метил, этил, н-пропил, изопропил, трет-бутил, цианогруппу, галоген, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, метилсульфонил, ацетил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает водород и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, метилсульфонил, ацетиламиногруппу или метоксикарбонил; или
- X обозначает CH, R1 обозначает цианогруппу и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, трифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает хлор и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает метоксигруппу или изопропоксигруппу и R2 обозначает трифторметил.
iii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления i), в которых
X обозначает CH или N;
R1 обозначает -NO2, -N(CH3)2 или -NCH3(CH2CH2OH); и
R2 обозначает этил, изопропил, трет-бутил, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает водород и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, метилсульфонил, ацетиламиногруппу или метоксикарбонил; или
- X обозначает CH, R1 обозначает цианогруппу и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, трифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает хлор и R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу; или
- X обозначает CH, R1 обозначает метоксигруппу или изопропоксигруппу и R2 обозначает трифторметил.
iv) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления i), в которых
R1 обозначает -NO2, -N(CH3)2 или -NCH3(CH2CH2OH); и
R2 обозначает водород, метил, этил, н-пропил, изопропил, трет-бутил, цианогруппу, галоген, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, метилсульфонил, ацетил или ацетиламиногруппу.
v) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления i), в которых
R1 обозначает -NO2, -N(CH3)2 или -NCH3(CH2CH2OH); и
R2 обозначает этил, изопропил, трет-бутил, метоксигруппу, этоксигруппу, н-пропоксигруппу, изопропоксигруппу, трифторметил, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу.
vi) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления iv) или v), в которых Х обозначает СН.
vii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления iv) или v), в которых Х обозначает N.
viii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-vii), в которых R1 обозначает -NO2.
ix) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-vii), в которых R1 обозначает -N(CH3)2.
x) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-vii), в которых R1 обозначает -NCH3(CH2CH2OH).
xi) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-x), в которых R2 обозначает этил, изопропил, трет-бутил, этоксигруппу, н-пропоксигруппу или изопропоксигруппу.
xii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим варианту осуществления xi), в которых R2 обозначает изопропоксигруппу.
xiii) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-x), в которых R2 обозначает трифторметил, дифторметоксигруппу, метилсульфонил или ацетиламиногруппу.
xiv) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-x), в которых R2 обозначает метоксигруппу.
xv) В другом варианте осуществления настоящее изобретение относится к соединениям формулы I, соответствующим любому из вариантов осуществления iv)-x), в которых R2 обозначает водород, метил, н-пропил, цианогруппу, галоген или ацетил.
Термин "галоген" при использовании в настоящем изобретении означает фтор, хлор, бром или йод, предпочтительно фтор или хлор.
Если соединения, соли, фармацевтические композиции, заболевания и т.п.указаны во множественном числе, это также означает одно соединение, соль и т.п.
Любое указание на соединение формулы I выше и ниже в настоящем изобретении следует понимать, как указание и на соли, предпочтительно фармацевтически приемлемые соли соединения формулы I, если это является подходящим или целесообразным.
Термин "фармацевтически приемлемые соли" означает нетоксичные соли присоединения с неорганической или органической кислотой и/или основанием. См. публикацию "Salt selection for basic drugs". Int. J. Pharm. 1986, 33, 201-17.
Настоящее изобретение также включает изотопно-меченые, предпочтительно меченые с помощью 2H (дейтерий) соединения формулы I, эти соединения идентичны соединениями формулы I с тем отличием, что один или большее количество заменены атомами, обладающими таким же атомным номером, но атомной массой или массовым числом, отличающимся от атомной массы или массового числа, обычно встречающихся в природе. Изотопномеченые, предпочтительно меченые с помощью 2H (дейтерий) соединения формулы I и их соли входят в объем настоящего изобретения. Замещение водорода более тяжелым изотопом 2H (дейтерий) может привести к большей метаболической стабильности, приводящей, например, к увеличенному периоду полувыведения in vivo или возможности использования меньших доз, или может привести к уменьшению ингибирования ферментов цитохромов Р450, что приводит, например, к улучшенному профилю безопасности. В одном варианте осуществления настоящего изобретения соединения формулы I не являются изотопно-мечеными или они мечены только одним или большим количеством атомов дейтерия. В одном подварианте осуществления соединения формулы I совсем не являются изотопно-мечеными. Изотопно-меченые соединения формулы I можно получить по методикам, аналогичным описанным ниже в настоящем изобретении, но с использованием соответствующих изотопозамещенных вариантов подходящих реагентов или исходных веществ.
Примеры предпочтительных соединений формулы I выбраны из группы, включающей:
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(6-трифторметилпиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(6-метоксипиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(6-этоксипиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-метансульфонилфенил)-акриламид,
(S)-3-(4-Ацетиламинофенил)-N-[4-(4-ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-пропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-дифторметоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трет-бутилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-диметиламинобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-трифторметилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(6-трифторметилпиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(6-метоксипиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперизин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(6-этоксипиридин-3-ил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-этоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-метансульфонилфенил)-акриламид,
(S)-3-(4-Ацетиламинофенил)-N-[4-(4-ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-пропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-этилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-дифторметоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-изопропилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-3-(4-трет-бутилфенил)-акриламид, и
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-нитробензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметилфенил)-акриламид.
Дополнительные примеры предпочтительных соединений формулы I выбраны из группы, включающей:
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил}циннамамид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-N-{1-[4-(4-(диметиламино)бензил)пиперазин-1-ил]-1-оксо-3-фенилпропан-2-ил}-3-(п-толил)акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил}-3-(4-пропилфенил)акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил}-3-(4-метоксифенил)акриламид,
(S)-3-(4-Ацетилфенил)-N-[4-(4-ацетилпиперазин-1-ил)бензил]-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил}акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-3-(4-цианофенил)-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил} акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил}-3-(4-фторфенил)акриламид, и
(S)-N-[4-(4-Ацетилпиперазин-1-ил)бензил]-3-(4-хлорфенил)-N-{1-(4-(4-(диметиламино)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил} акриламид.
Дополнительные примеры предпочтительных соединений формулы I выбраны из группы, включающей:
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-этилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-трет-бутилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-этоксифенил)-акриламид,
Метиловый эфир (S)-4-(2-{[4-(4-ацетилпиперазин-1-ил)-бензил]-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-карбамоил}-винил)-бензойной кислоты,
(S)-N-[4-(4-Ацетилпиперизин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперидин-1-ил)-2-оксоэтил]-3-(4-метансульфонилфенил)-акриламид,
(S)-3-(4-Ацетиламинофенил)-N-[4-(4-ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-пропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-[1-бензил-2-(4-бензилпиперазин-1-ил)-2-оксоэтил]-3-(4-изопропилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-метансульфонилфенил)-акриламид,
(S)-3-(4-Ацетиламинофенил)-N-[4-(4-ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-пропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилииперазин-1-ил)-бензил]-N-{1-6ензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-дифторметоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-цианобензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трет-бутилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-метансульфонилфенил)-акриламид,
(S)-3-(4-Ацетиламинофенил)-N-[4-(4-ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-пропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-этилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-дифторметоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-хлорбензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трет-бутилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-метоксибензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметилфенил)-акриламид, и
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-изопропоксибензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трифторметилфенил)-акриламид.
Дополнительные примеры предпочтительных соединений формулы I выбраны из группы, включающей:
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-(метилсульфонил)-бензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-изопропоксифенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-(метилсульфонил)-бензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-трет-бутилфенил)-акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-(метилсульфонил)-бензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-пропоксифенил)-акриламид,
(S)-N-(4-(4-Ацетилпиперазин-1-ил)бензил)-N-(1-(4-(4-(метилсульфонил)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил)-3-(4-(трифторметил)фенил)акриламид,
(S)-N-[4-(4-Ацетилпиперазин-1-ил)-бензил]-N-{1-бензил-2-[4-(4-(этилсульфонил)-бензил)-пиперазин-1-ил]-2-оксоэтил}-3-(4-пропоксифенил)-акриламид, и
(S)-N-(4-(4-Ацетилпиперазин-1-ил)бензил)-N-(1-(4-(4-(этилсульфонил)бензил)пиперазин-1-ил)-1-оксо-3-фенилпропан-2-ил)-3-(4-(трифторметил)фенил)акриламид.
Соединения формулы I и их фармацевтически приемлемые соли можно использовать в качестве лекарственных средств, например, в форме фармацевтических композиций, предназначенных для энтерального или парентерального введения, и они являются подходящими для лечения и/или предупреждения заболеваний, указанных в настоящем изобретении, предпочтительно таких, как малярия.
Приготовление фармацевтических композиций можно провести по методикам, которые должны быть известны любому специалисту в данной области техники (см., например, Remington, The Science and Practice of Pharmacy, 21 st Edition (2005), Part 5, "Pharmaceutical Manufacturing" [published by Lippincott Williams & Wilkins]), путем внесения описанных соединений формулы I или их фармацевтически приемлемых солей, необязательно в комбинации с другим терапевтически полезными веществами в галенову вводимую форму вместе с подходящими нетоксичными инертными фармацевтически приемлемыми твердыми или жидкими носителями и при необходимости с обычными фармацевтическими вспомогательными веществами.
В одном варианте осуществления настоящее изобретение относится к способу лечения или предупреждения заболеваний, указанных в настоящем изобретении, предпочтительно таких, как малярия, указанный способ включает введение субъекту соединения формулы I в фармацевтически активном количестве.
Соединения формулы I или указанные выше фармацевтические композиции также можно применять в комбинации с одним или большим количеством других терапевтически полезных веществ, например, с другими противомалярийными средствами, такими как хинолины (например, хинин, хлорхин, амодиахин, мефлохин, примахин и тафенохин), пероксидные противомалярийные средства (например, артемизинин, артеметер и артезунат), пириметаминсульфадоксиновые противомалярийные средства (например, фансидар®), гидроксинафтохиноны (например, атоваквон), противомалярийные средства акридинового типа (например, пиронаридин), и другими противопротозойными средствами, такими как этилстибамин, гидроксистилбамидин, пентамидин, стилбамидин, хинапирамин, пуромицин, пропамидин, нифуртимокс, меларсопрол, ниморазол, нифуроксим, аминитрозол и т.п.
Настоящее изобретение также относится к применению соединения формулы I для приготовления фармацевтической композиции, необязательно предназначенной для применения в комбинации с одним или большим количеством других терапевтически полезных веществ, таких как указанные в предыдущем абзаце, предназначенной для предупреждения и/или лечения заболеваний, указанных в настоящем изобретении, предпочтительно таких, как малярия.
Соединения формулы I, предлагаемые в настоящем изобретении, можно получить по методикам, описанным в настоящем изобретении, предпочтительно так, как это описано в экспериментальном разделе.
Обычно все химические превращения можно осуществить в соответствии с хорошо известными стандартными методологиями или так, как это описано в приведенных ниже методиках.
Получение соединений формулы I, за исключением соединений, в которых R1 обозначает -NCH3(CH2CH2OH):
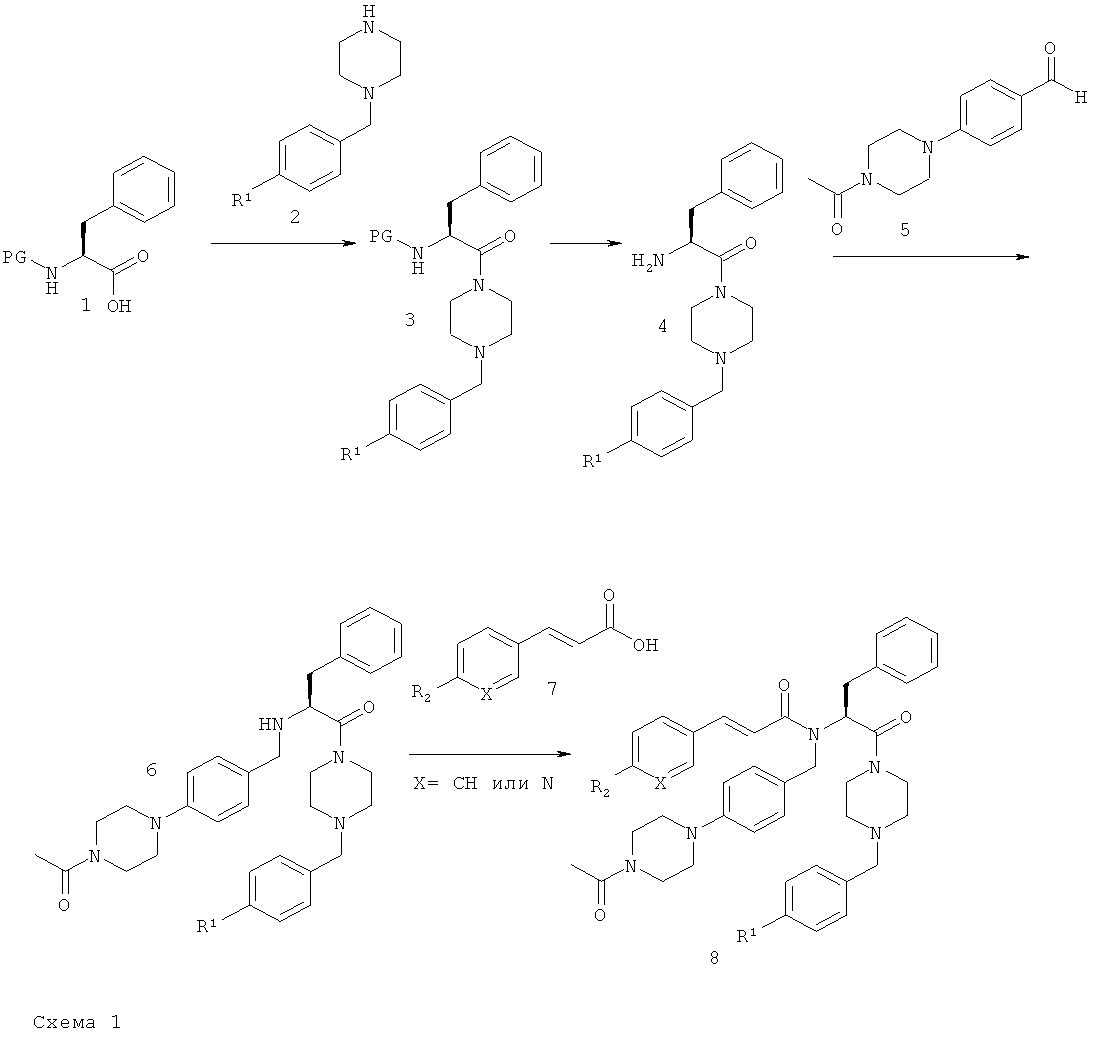
Boc-Phe-OH 1 можно ввести в реакцию сочетания с производным бензилпиперазина 2 посредством реакции сочетания с образованием пептида с использованием активирующих реагентов, таких как TBTU (или PyBOP/HOBt), в присутствии основания, такого как ДИПЭА (или NEM), в ДХМ (или ДМФ) при КТ и получить промежуточный продукт 3. Альтернативно, на начальной стадии реакции сочетания с образованием пептида также можно использовать Cbz-Phe-ОН и получить соединение 3. Удаление защитной группы Boc обычно проводят по реакции соединения 3 с 4 н. раствором HCl в диоксане с использованием в качестве растворителя ДХМ, тогда как удаление защитной группы Cbz проводят путем гидрирования с помощью катализатора Pd/C в MeOH, и получают промежуточный амин 4. Реакция восстановительного аминирования свободного амина 4 и альдегида 5 в MeOH, проводимая при кипячении с обратным холодильником, дает нестабильный имин (не представлен на схеме), который затем восстанавливают с помощью NaBH4 при КТ и получают промежуточный вторичный амин 6. Альтернативно, восстановительное аминирование можно провести в растворителе, таком как CH3CN, в присутствии восстановительного реагента, такого как NaBH(OAc)3, и получить искомый промежуточный вторичный амин 6. Затем соединение 6 можно ввести в реакцию сочетания с карбоновой кислотой 7 с использованием реагента реакции сочетания с образованием пептида, такого как TBTU, PyBOP/HOBt или реагент Госеза, в растворителе, таком как ДХМ (или ДМФ), при КТ в присутствии основания, такого как ДИПЭА (или NEM). Альтернативно, карбоновую кислоту 7 можно превратить в соответствующий хлорангидрид кислоты (не представлен на схеме) с помощью оксалилхлорида в ДХМ и получить конечные соединения 8 формулы I.
В случае, когда R1=-NCH3(CH2CH2OH), соединения формулы I получают в соответствии со схемой 2.
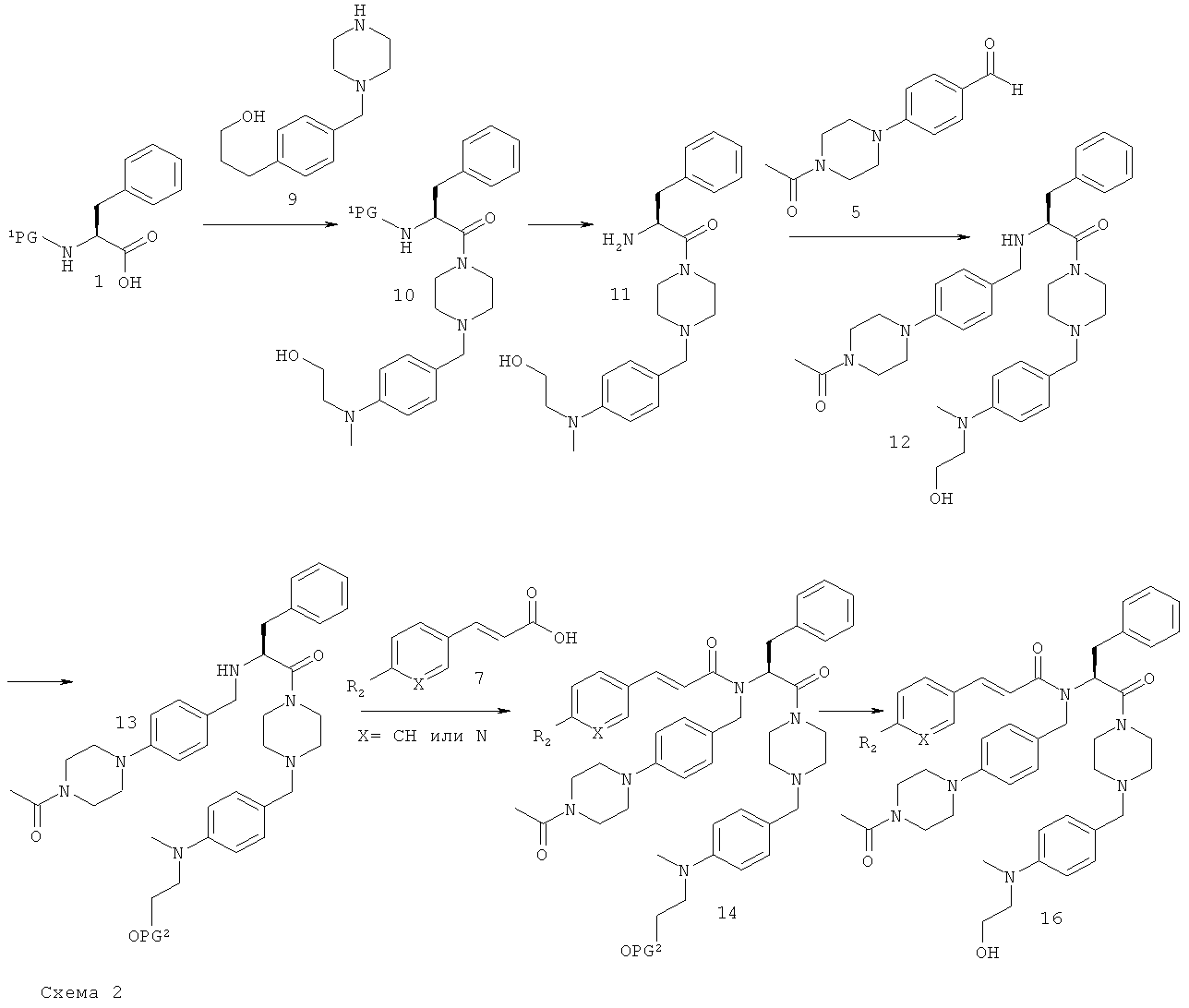
Boc-Phe-OH 1 вводят в реакцию сочетания с производным бензилпиперазина 9 посредством реакции сочетания с образованием пептида с использованием активирующих реагентов, таких как TBTU (или PyBOP/HOBt), в присутствии основания, такого как ДИПЭА (или NEM), в ДХМ (или ДМФ) при КТ и получают промежуточный продукт 10. Альтернативно, на начальной стадии реакции сочетания с образованием пептида также можно использовать Cbz-Phe-OH и получить соединение 10. Удаление защитной группы Boc обычно проводят по реакции соединения 10 с 4 н. раствором HCl в диоксане с использованием в качестве растворителя ДХМ, тогда как удаление защитной группы Cbz проводят путем гидрирования с помощью катализатора Pd/C в MeOH, и получают промежуточный амин 11. Реакция восстановительного аминирования свободного амина 11 и альдегида 5 в CH3CN, проводимая при КТ в присутствии восстановительного реагента, такого как NaBH(OAc)3, дает промежуточный вторичный амин 12. Свободную гидроксигруппу соединения 12 защищают с использованием в качестве силилирующего реагента, например, TBDMSC1, и получают соединение 13, которое затем вводят в реакцию сочетания с карбоновой кислотой 7 с использованием реагента реакции сочетания с образованием пептида, такого как TBTU (или PyBOP/HOBt), в растворителе, таком как ДХМ (или ДМФ), при КТ в присутствии основания, такого как ДИПЭА. Альтернативно, карбоновую кислоту 7 можно активировать путем превращения в соответствующий хлорангидрид кислоты (не представлен на схеме) с помощью оксалилхлорида в ДХМ и затем получить соединение 14. Последующее удаление защитной группы в слабокислой среде, такой 1 М водный раствор НС1 в МеОН, или с использованием фторсодержащих реагентов, таких как ТБАФ, дает конечные соединения 16 формулы I.
Соединения формулы I также можно получить в соответствии с путем синтеза, представленным на схеме 3.
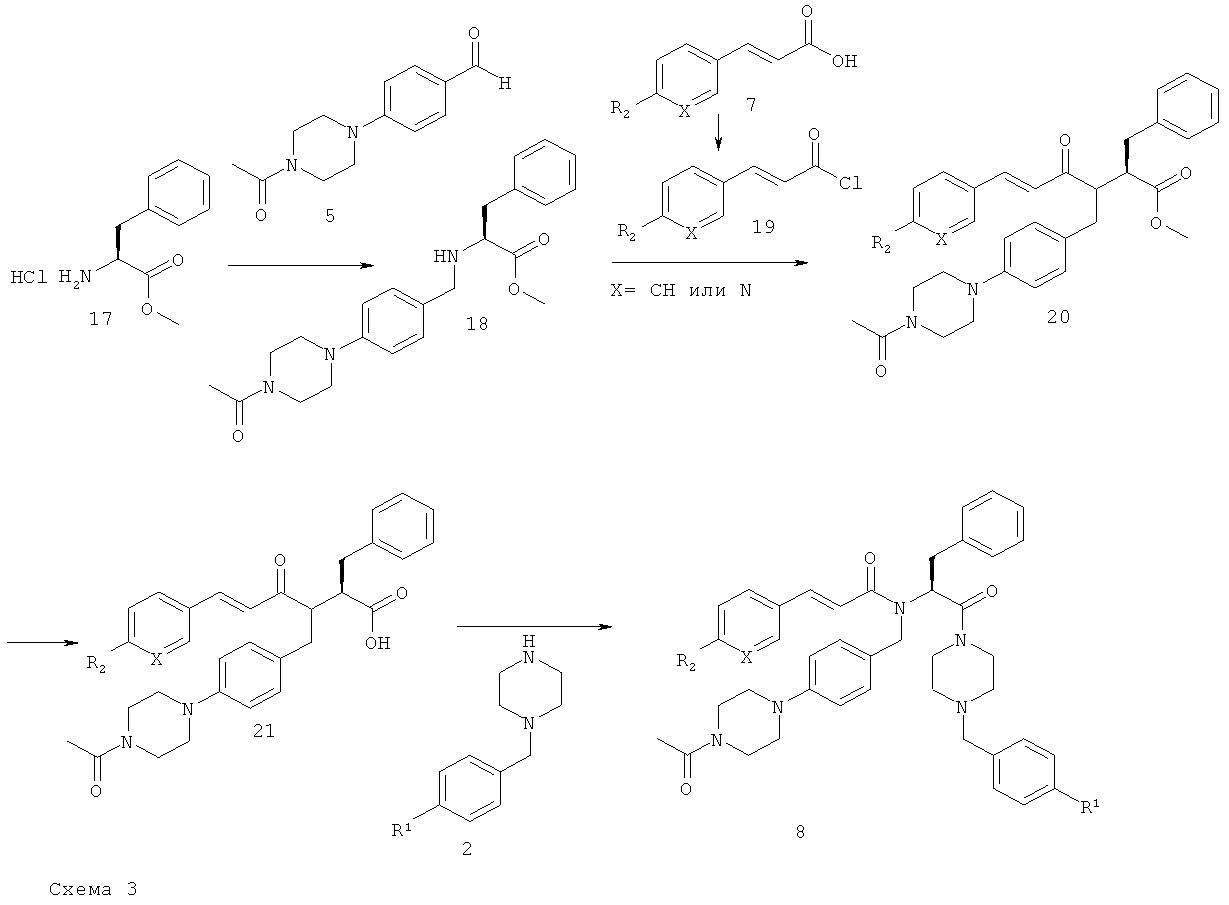
Реакция восстановительного аминирования аминокислоты H-Phe-OMe.HCl 17 и альдегида 5 в MeOH, проводимая при кипячении с обратным холодильником, дает соответствующий имин, который затем восстанавливают в присутствии восстановительного реагента, такого как NaBH4, при КТ и получают вторичный амин 18. Соединение 18 также можно получить с использованием условий, описанных выше для получения соединений 6 и 12. Затем сложный эфир 18 вводят в реакцию сочетания с хлорангидридом кислоты 19, полученным из карбоновой кислоты 7 с помощью оксалилхлорида в ДХМ или реагента Госеза. Альтернативно, соединение 18 можно непосредственно ввести в реакцию сочетания с карбоновой кислотой 7 посредством реакции сочетания с образованием пептида с использованием в качестве реагентов сочетания TBTU (или PyBOP/HOBt) в растворителе, таком как ДХМ (или ДМФ), при КТ в присутствии основания, такого как ДИПЭА (или NEM). Осторожно проводимая реакция омыления сложного эфира 20 с помощью 0,5 н. водного раствора LiOH в ТГФ, проводимая при 0°С, дает кислоту 21. Конечная реакция сочетания с образованием пептида с бензилпиперазином 2 дает конечные соединения 8 формулы I.
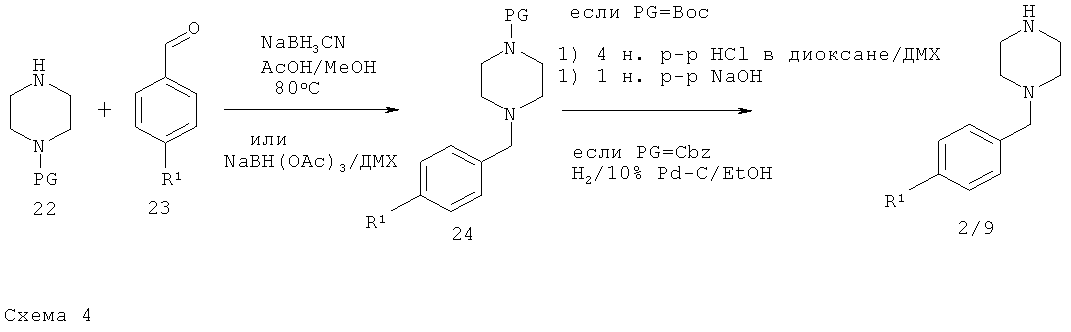
Бензилпиперазины 2 и 9 имеются в продаже и/или их можно синтезировать в соответствии с представленной ниже схемой синтеза 4:
Коричные кислоты 7 имеются в продаже или/и их можно синтезировать в соответствии с представленном ниже путем синтеза:
Путь А: Реакция Кневенагеля
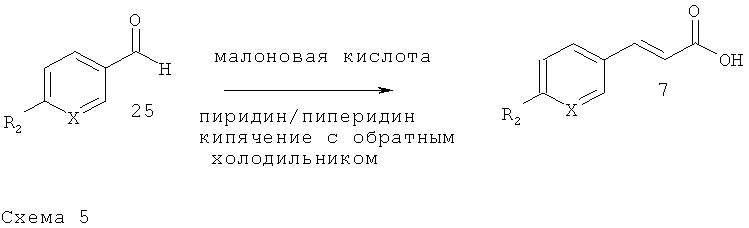
Коричные кислоты 7 получают путем кипячения с обратным холодильником альдегида 25 с малоновой кислотой в смеси пиперидин/пиридин (WO 00/66566).
Путь В: Реакция Хорнера-Эммонса
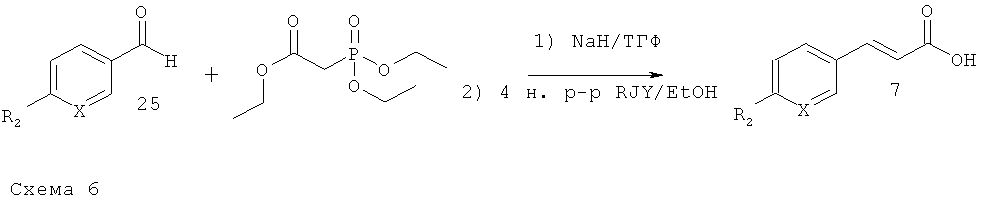
Коричные кислоты 7 получают за две стадии по реакции альдегидов 25 с триэтилфосфоноацетатом 26 в присутствии основания, такого как NaH, в апротонном растворителе, таком как ТГФ, с последующим омылением полученного сложного этилового эфира с помощью 4 н. раствора KOH в EtOH.
Приведенные ниже примеры иллюстрируют настоящее изобретение. Все температуры приведены в градусах Цельсия и давления приведены в мбар. Если не указано иное, реакции протекают при КТ. Отношения количеств растворителей друг к другу всегда указаны в виде отношений объемов. Химические названия конечных продуктов и промежуточных продуктов образованы на основании химических структурных формул с помощью программы ChemDrawPro Automatic Nomenclature.
Условия проведения аналитической ВЭЖХ:
(I) Agilent 1100 series, детектирование: УФ/вид, и МС (МС: Thermo Finnigan с одной квадрупольной линзой). Колонки (4,6×50 мм, 5 мкм): Waters X-Bridge С 18 или Waters Atlantis Т3.
Проведение в щелочной среде: Элюенты: A: MeCN, В: концентрированный NH3 в воде (1,0 мл/л). Градиентный режим: от 5 до 95% за 1,5 мин. Скорость потока: 4,5 мл/мин.
Проведение в кислой среде: Элюенты: А: вода+0,04% ТФК, В: MeCN. Градиентный режим: от 5 до 95% за 1,5 мин. Скорость потока: 4,5 мл/мин.
Условия проведения препаративной ВЭЖХ:
Gilson, детектирование: УФ/вид. + МС или УФ/вид. + ИДРС.
Проведение в щелочной среде: Элюенты: А: MeCN, В: H2O+0,5% NH3 (25% водный раствор).
(II) колонка Waters X-Bridge, 19×50 мм, 5 мкм. Градиентный режим: от 20 до 90% А за 5 мин. Скорость потока: 40 мл/мин.
(III) колонка Waters X-Bridge, 30×75 мм, 10 мкм. Градиентный режим: от 20 до 90% А за 6 мин. Скорость потока: 75 мл/мин.
В настоящем изобретении используются следующие аббревиатуры:
|
|
Получение соединений формулы I по пути синтеза, представленному на схеме 1 - общие методики и примеры:
Общая методика А - стадия 1
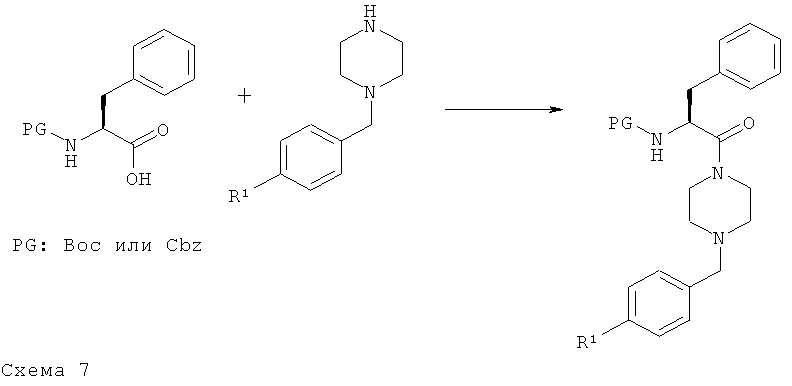
При перемешивании к суспензии 1 ммоля Boc-Phe-OH или Cbz-Phe-OH в 0,6 мл сухого ДХМ (или ДМФ) в атмосфере азота последовательно добавляют 1 ммоль TBTU и 2 ммоля NEM. Полученную светло-желтую суспензию перемешивают при КТ в течение 1 ч, затем раствор добавляют 1 ммоль бензилпиперазина в 0,25 мл сухого ДХМ (или ДМФ). Полученную реакционную смесь дополнительно перемешивают при КТ в течение ночи. После завершения перемешивания реакционную смесь разбавляют с помощью ДХМ и реакцию останавливают насыщенным раствором NaHCO3. Водную фазу экстрагируют с помощью ДХМ (х3), объединенные органические фазы последовательно промывают с помощью H2O и рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) и получают искомое соединение. Промежуточные продукты 1
|
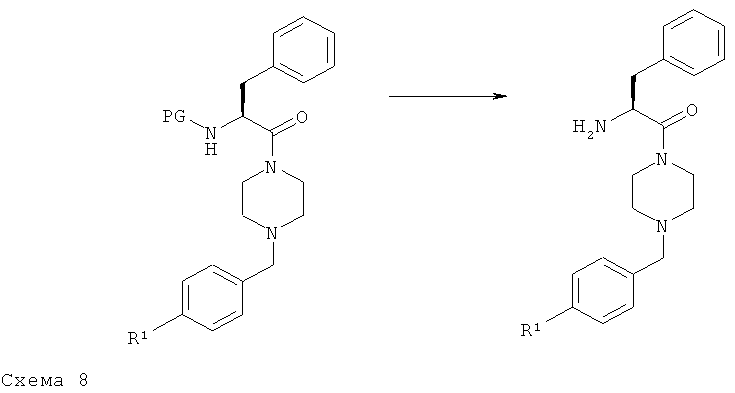
Схема 8
Если PG=Boc:
К раствору 1 ммоля содержащего защитную группу Вое амина в 9 мл сухого ДХМ при 0°С по каплям добавляют 4,5 мл 4 н. раствора HCl в диоксане. Полученную реакционную смесь перемешивают в атмосфере азота при КТ в течение 4 ч, охлаждают до 0°С и осторожно нейтрализуют 1 н.водным раствором NaOH до pH=7. Затем водную фазу экстрагируют с помощью ДХМ (х3). Объединенные органические фазы последовательно промывают с помощью H2O и рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении и получают свободный первичный амин, который используют на следующей стадии без дополнительной очистки.
Если PG=Cbz:
Смесь 2 ммолей содержащего защитную группу Cbz амина, 10% Pd-C (100 мг) в сухом EtOH (25 мл) перемешивают в атмосфере водорода при КТ в течение 3 ч. Реакционную смесь фильтруют через целит и концентрируют при пониженном давлении и получают свободный первичный амин, который используют на следующей стадии без дополнительной очистки.
Промежуточные продукты 2
|
Общие методики С1 и С2 - стадия 3
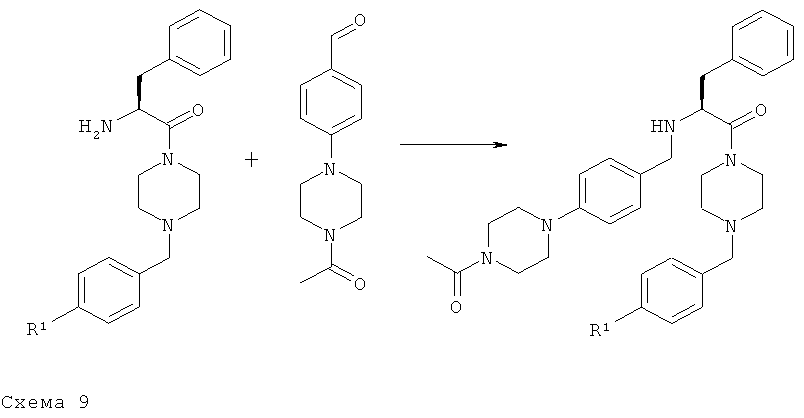
Общая методика С1:
Раствор 1 ммоля амина и 1 ммоля альдегида в 5 мл сухого МеОН в атмосфере азота кипятят с обратным холодильником в течение 24 ч. Затем полученную смесь охлаждают до КТ, затем порциями добавляют 1,5 ммоля NaBH4. Полученную гетерогенную смесь дополнительно перемешивают при КТ в течение 2 ч, реакцию останавливают насыщенным водным раствором NaHCO3 и смесь экстрагируют с помощью EtOAc (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) и получают искомое соединение.
Общая методика С2:
К раствору 1 ммоля амина и 1 ммоля альдегида в 5 мл сухого CH3CN порциями добавляют 1,5 ммоля NaBH(OAc)3. Полученную гетерогенную смесь дополнительно перемешивают при КТ в течение 4 ч, реакцию останавливают насыщенным водным раствором NaHCO3 и смесь экстрагируют с помощью EtOAc (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) и получают искомое соединение.
Промежуточные продукты 3
|
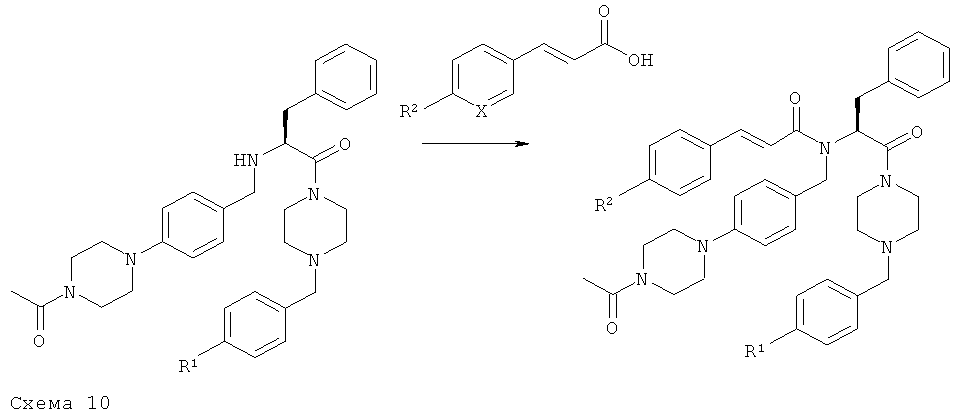
Общая методика D1:
К раствору 1 ммоля коричной кислоты в 5 мл сухого ДХМ в атмосфере азота добавляют 1,4 ммоля 1-хлор-N,N-2-триметилпропениламина (реагент Госеза). Полученную смесь перемешивают при КТ в течение 1 ч, затем добавляют раствор 1 ммоля амина и 3 ммолей ДИПЭА в 4 мл сухого ДХМ. Реакционную смесь дополнительно перемешивают при КТ в течение ночи. После завершения перемешивания добавляют насыщенный водный раствор МаНСОз и смесь экстрагируют с помощью ДХМ (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) или с помощью препаративной ВЭЖХ и получают конечное соединение.
Общая методика D2:
К раствору (или суспензии) 1,05 ммоля коричной кислоты в 3,5 мл сухого ДХМ в атмосфере азота при 0°С добавляют 1,1 ммоля оксалилхлорида и 3 капли ДМФ. Полученную смесь перемешивают при КТ в течение 1 ч, охлаждают до 0°С, затем добавляют раствор 1 ммоля амина и 2 ммолей ДИПЭА в 3 мл сухого ДХМ. Реакционную смесь дополнительно перемешивают при КТ в течение ночи. После завершения перемешивания добавляют насыщенный водный раствор NaHCO3 и смесь экстрагируют с помощью ДХМ (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) или с помощью препаративной ВЭЖХ и получают конечное соединение.
|
|
|
|
|
|
Получение соединений формулы I по пути синтеза, представленному на схеме 2 - общие методики и примеры:
Стадия 1: трет-Бутиловый эфир (S)-[1-бензил-2-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-2-оксоэтил]-карбаминовой кислоты.
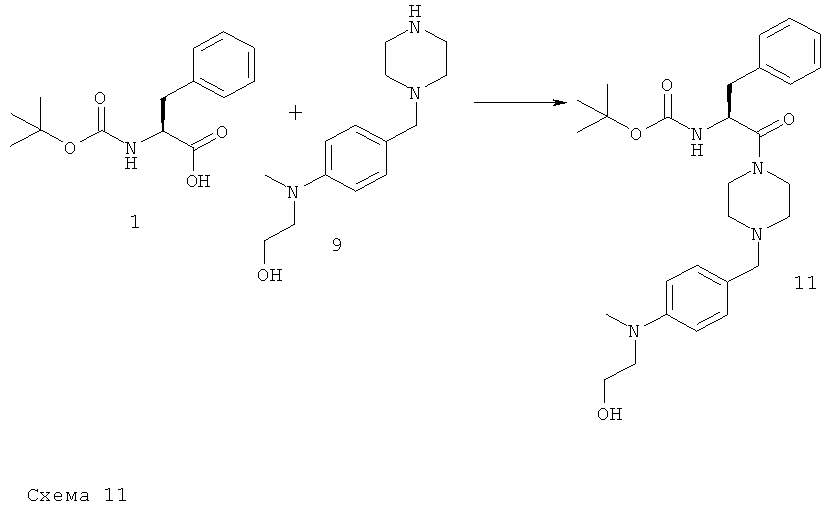
В соответствии с общей методикой А используют 60 ммолей Boc-Phe-OH для получения искомого соединения с выходом 50%. Rt=0,87; [М+Н]+=497,42 (аналитическая ВЭЖХ I, колонка X-Bridge, щелочная среда).
Стадия 2: (S)-2-Амино-1-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-3-фенилпропан-1-он.
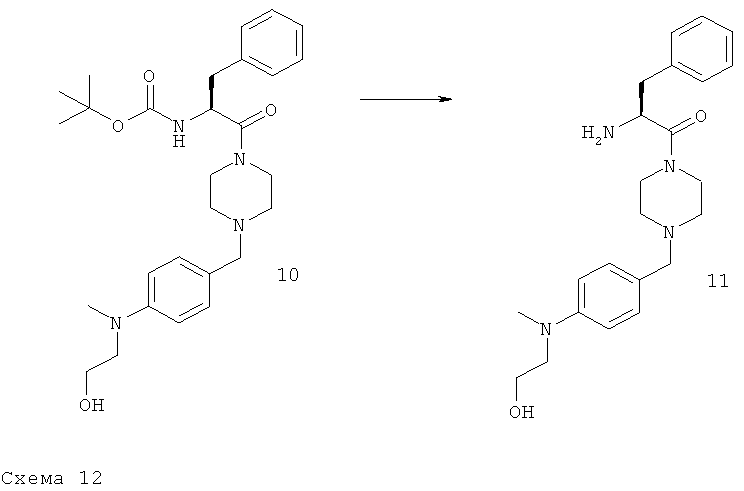
В соответствии с общей методикой В используют 12 ммолей содержащего защитную группу Вое амина 10 для получения искомого соединения с количественным выходом. Rt=0,69; [М+Н]+=397,18 (аналитическая ВЭЖХ I, колонка X-Bridge, щелочная среда).
Стадия 3: (S)-2-[4-(4-Ацетилпиперазин-1-ил)-бензиламино]-1-(4-{4-[(2-гидроксиэтил)-метиламино]-бензил}-пиперазин-1-ил)-3-фенилпропан-1-он.
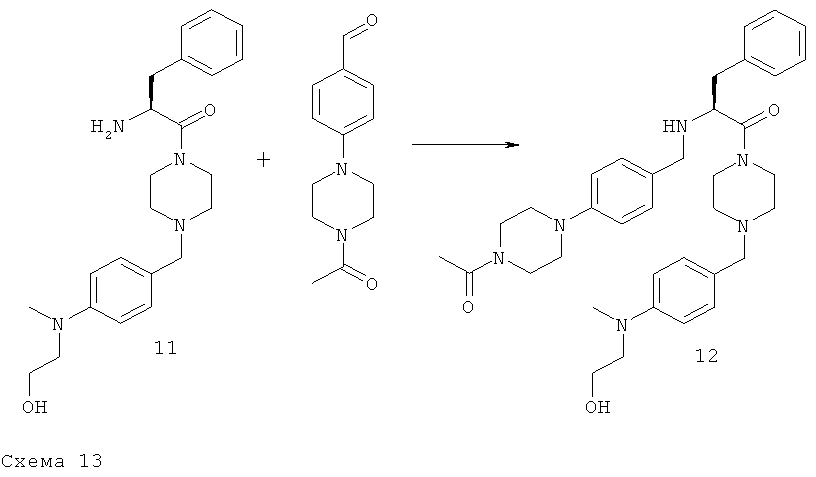
В соответствии с общей методикой С2 используют 11,4 ммоля свободного амина 11 для получения искомого соединения с количественным выходом. Rt=0,74; [М+Н]+=613,24 (аналитическая ВЭЖХ I, колонка X-Bridge, щелочная среда).
Общая методика Е - стадия 4: (S)-2-[4-(4-Ацетилпиперазин-1-ил)-бензиламино]-1-[4-(4-{[2-(трет-бутилдиметилсиланилокси)-этил]-метиламино}-бензил)-пиперазин-1-ил]-3-фенилпропан-1-он.
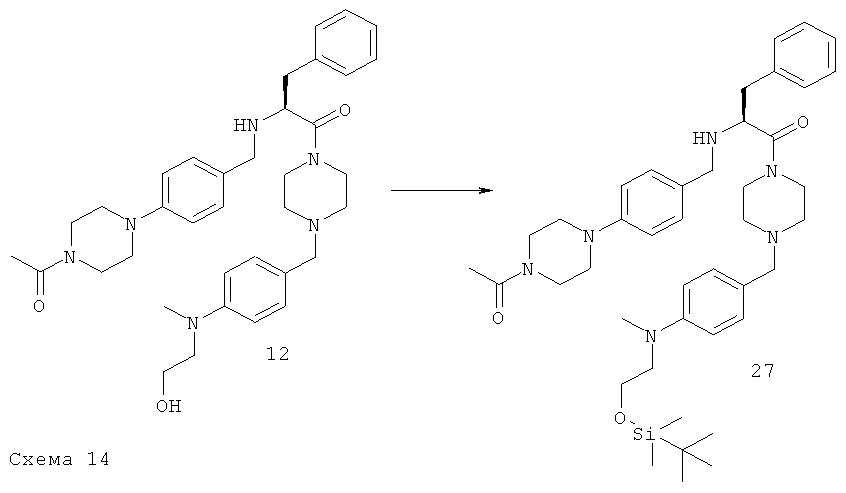
Схема 14
3 ммоля TBDMSC1 при КТ порциями добавляют к раствору 1 ммоля содержащего гидроксигруппу соединения 12 и 3 ммолей имидазола в 5 мл сухого ДМФ. Желтый раствор перемешивают при КТ в течение 16 ч, реакцию останавливают с помощью H2O и смесь экстрагируют с помощью EtOAc (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F; ДХМ/МеОН, от 92:8 до 95:5) и получают искомое соединение в виде желтого вспененного вещества с выходом 81%. Rt=1,12 мин; [М+Н]+=727,31. (аналитическая ВЭЖХ I, колонка X-Bridge, щелочная среда).
Стадия 5
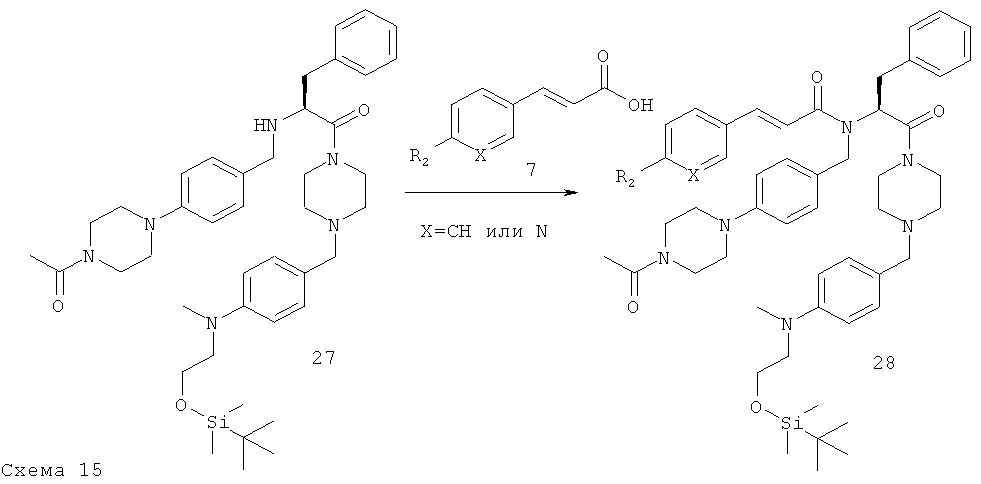
Соединения формулы 28 получают в соответствии с общими методиками D1 или D2.
|
|
Общая методика F - стадия 6
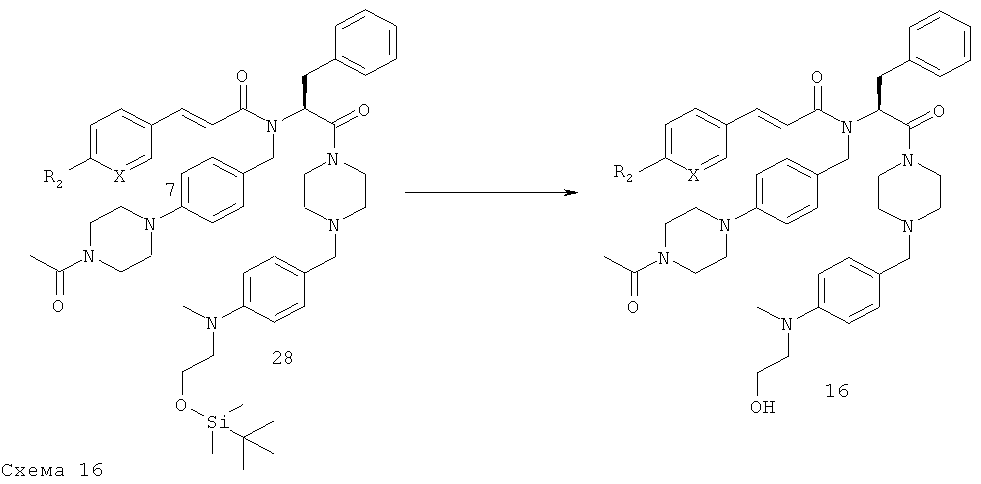
К раствору 1 ммоля содержащего защитную группу спирта 28 в 3,5 мл сухого ТГФ в атмосфере азота при 0°С добавляют 3,5 ммоля ТБАФ (1 М раствор в ТГФ). Полученную смесь перемешивают при КТ в течение 4 ч и охлаждают до 0°С. После завершения добавляют H2O и смесь экстрагируют с помощью ДХМ (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) или с помощью препаративной ВЭЖХ и получают конечное соединение.
|
|
Получение соединений формулы I по пути синтеза, представленному на схеме 3 - общие методики и примеры:
Стадия 1: Метиловый эфир (S)-2-[4-(4-ацетилпиперазин-1-ил)-бензиламино]-3-фенилпропионовой кислоты.
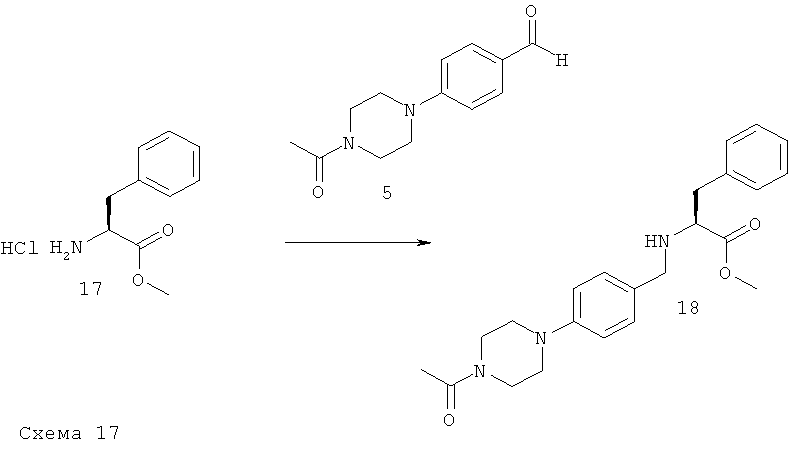
Вторичный амин 18 получают в соответствии с общими методиками С1 или С2 и используют на следующей стадии без дополнительной очистки. Rt=0,82; [М+Н]+=396,20 (аналитическая ВЭЖХ I, колонка X-Bridge, щелочная среда).
Стадия 2
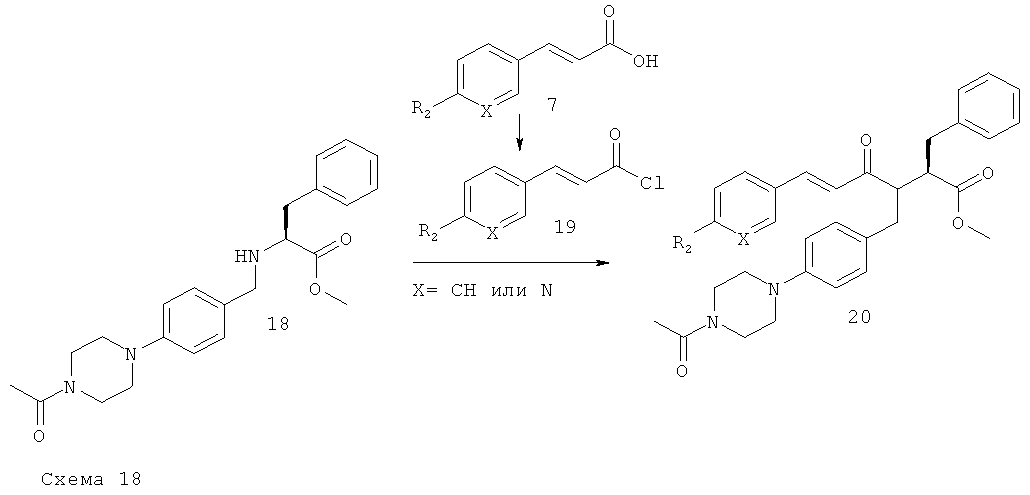
Соединения формулы 20 получают в соответствии с общими методиками D1 или D2.
|
Общая методика G - стадия 3
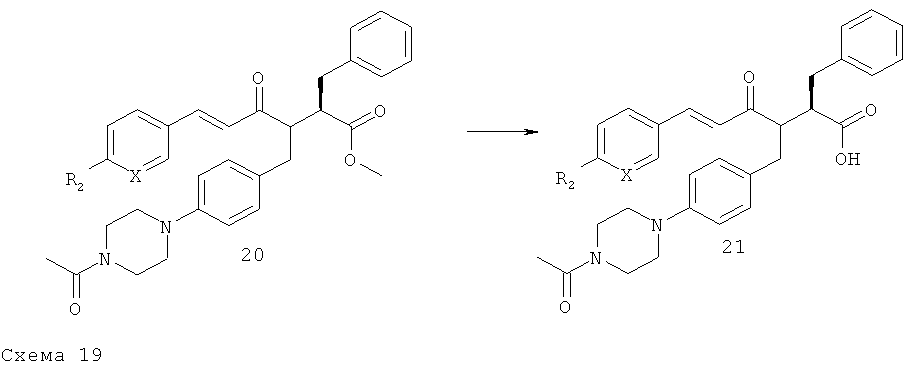
К раствору 1 ммоля сложного метилового эфира 20 в 8 мл Et2O и 2 мл H2O при 0°С по каплям добавляют 10 ммолей 2М водного раствора NaOH. Реакционную смесь дополнительно перемешивают при КТ в течение 2-3 ч. После завершения перемешивания водную фазу подкисляют 1 н. раствором НС1 до рН=2-3 и затем экстрагируют с помощью EtOAc (x3). Объединенные органические фазы промывают рассолом, сушат над Na2SO4, фильтруют и концентрируют при пониженном давлении. Остаток используют на следующей стадии без дополнительной очистки.
|
Стадия 4
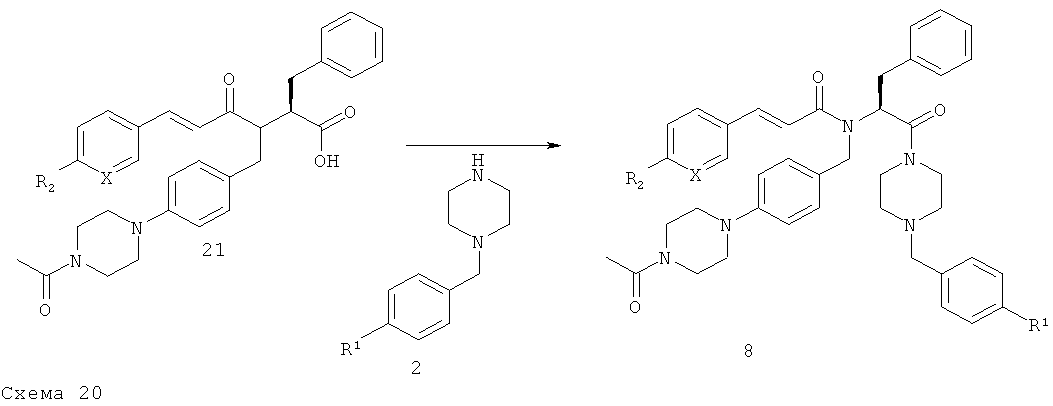
Соединения формулы 8 получают в соответствии с общей методикой А. Остаток очищают с помощью флэш-хроматографии (SiO2 60F) или с помощью препаративной ВЭЖХ и получают конечное соединения.
|
|
Соединения примеров 66-73 получают в соответствии с общей методикой D2.
|
|
Противомалярийная активность in vitro: Исследование Plasmodium falciparum m vitro
Активность т vitro по отношению к Р. falciparum, находящемуся на эритроцитарных стадиях, в эритроцитах человека определяют с помощью исследования включения [3H]-гипоксантина. В этом исследовании используют один штамм, чувствительный ко всем известным лекарственным средствам (Р.falciparum NF54), и активность всех исследуемых соединений сравнивают с активностью стандартных лекарственных средств, хлорхина (Sigma C6628) и артезуната (Sigma 36, 159-3). В 96-луночных микропланшетах для титрования соединения, исследуемые дважды, серийно разводят в среде для скрининга [среда RPMI 1640 с добавлением HEPES (N-2-гидроксиэтилпиперазин-N-2-этансульфоновая кислота) (5,94 г/л), NaHCO3 (2,1 г/л), неомицин (100 Ед./мл) и Albumax (5 г/л) или сыворотки человека (конечная концентрация 50%)] в соответствующем диапазоне концентраций. Затем культуры паразитов инкубируют в среде для скрининга, содержащей промытые эритроциты человека, характеризующиеся гематокритом, равном 2,5% (паразитемия 0,3%), и добавляют к серийно разведенным соединениям и инкубируют в увлажненной атмосфере при 37°С, 4% CO2, 3% 02 и 93% N2. Через 48 ч в каждую лунку планшета добавляют [3H-гипоксантин (0,5 мкКи). Планшеты инкубируют в таких же условиях в течение еще 24 ч, затем проводят сбор клеток с помощью устройства для сбора клеток Betaplate (Wallac) и промывают дистиллированной водой. Высушенные фильтры вставляют в пластмассовую фольгу, содержащую 10 мл сцинтилляционной жидкости, и с помощью жидкостного сцинтилляционного счетчика Betaplate проводят подсчет. Значения IC50 рассчитывают по сигмоидальным зависимостям ингибирования с использованием программы Microsoft Excel.
|
Исследования противомалярийной эффективности in vivo Противомалярийную активность in vivo определяют для групп, состоящих из 3 самок мышей NMRI (20-22 г), которых в день 0 путем внутривенного введения инфицируют штаммом Р. berghei GFP-ANKA (0,2 мл гепаринизированной суспензии физиологического раствора, содержащей 2×107 зараженных паразитами эритроцитов). У контрольных мышей в день 3 после инфицирования паразитемия обычно достигает примерно 40%. Соединения готовят в смеси Tween 80/этанол (7%/3%) обычно при концентрациях, составляющих 10 мг/мл. Соединения вводят при объеме, равном 10 мл/кг, перорально в виде разовых доз (1×100 мг/кг, через 24 ч после инфицирования). Через 48 ч после введения лекарственного средства (в день 3 после инфицирования) из хвоста отбирают 1 мкл крови, повторно суспендируют в 1 мл ЗФФ и паразитемию определяют с помощью аппарата FACScan (Becton Dickinson) путем подсчета 100000 эритроцитов. Активность рассчитывают, как разность средних значений для контрольной группы и для экспериментальных групп и ее выражают в процентах от значения для контрольной группы.
|