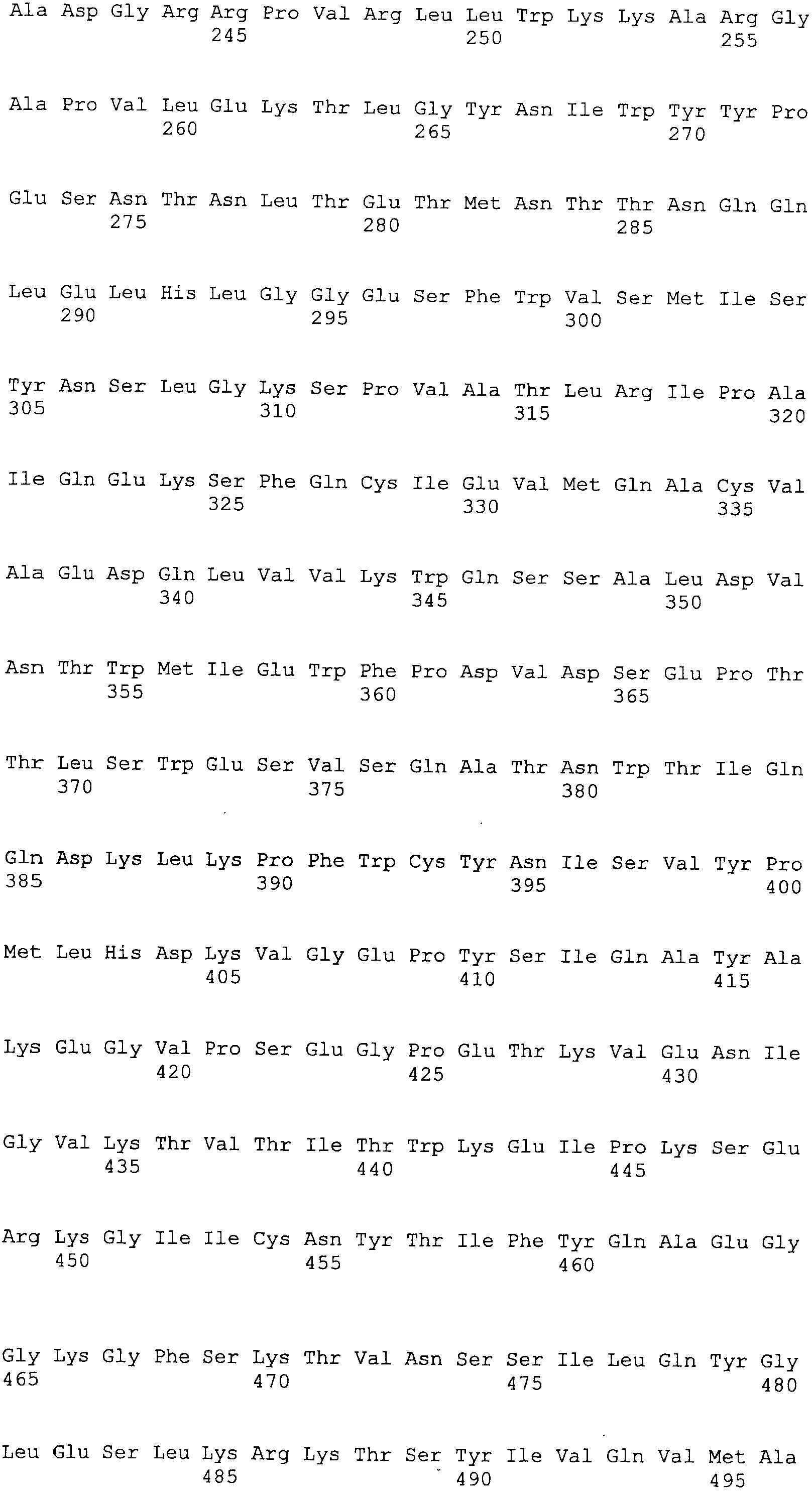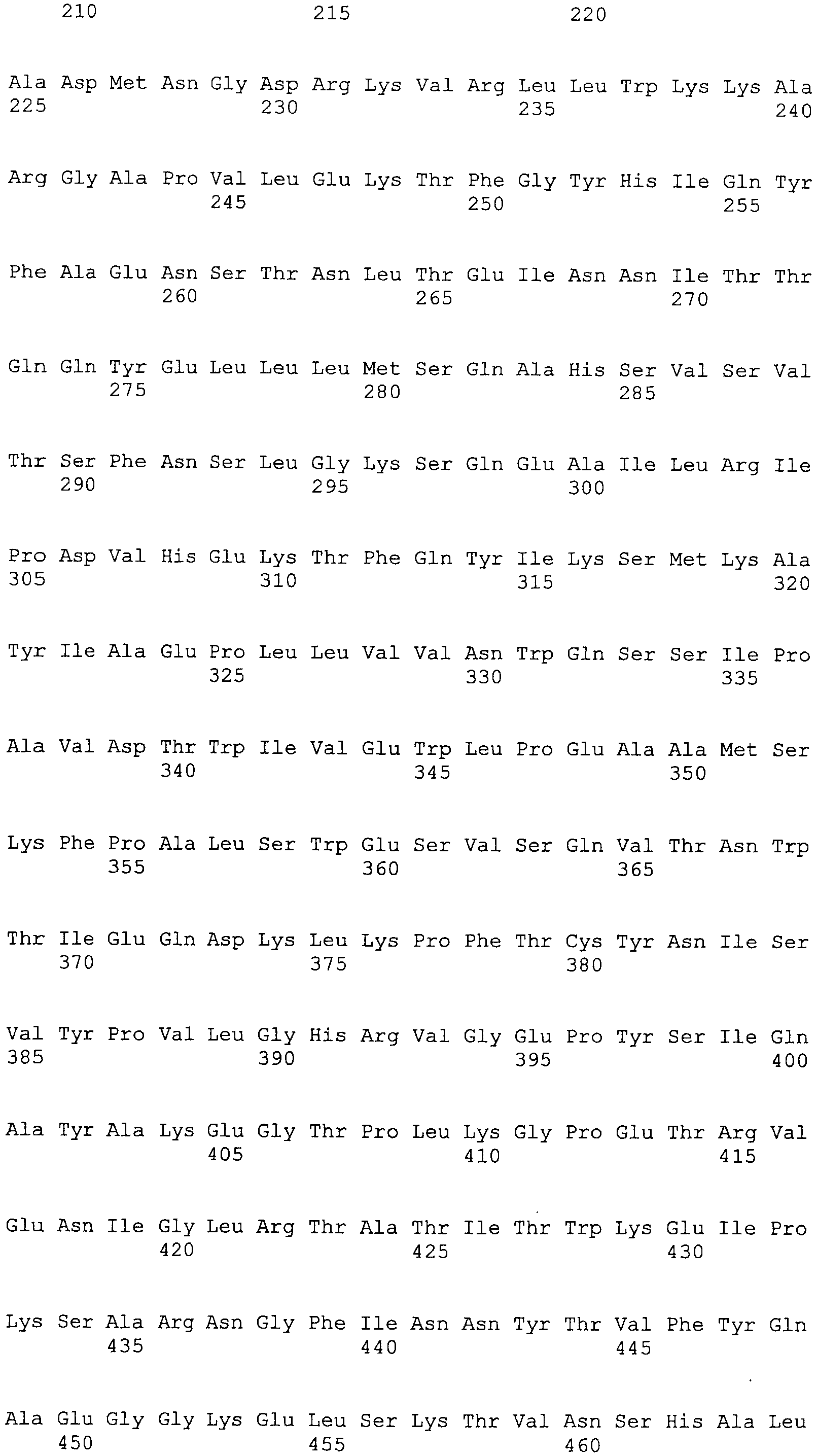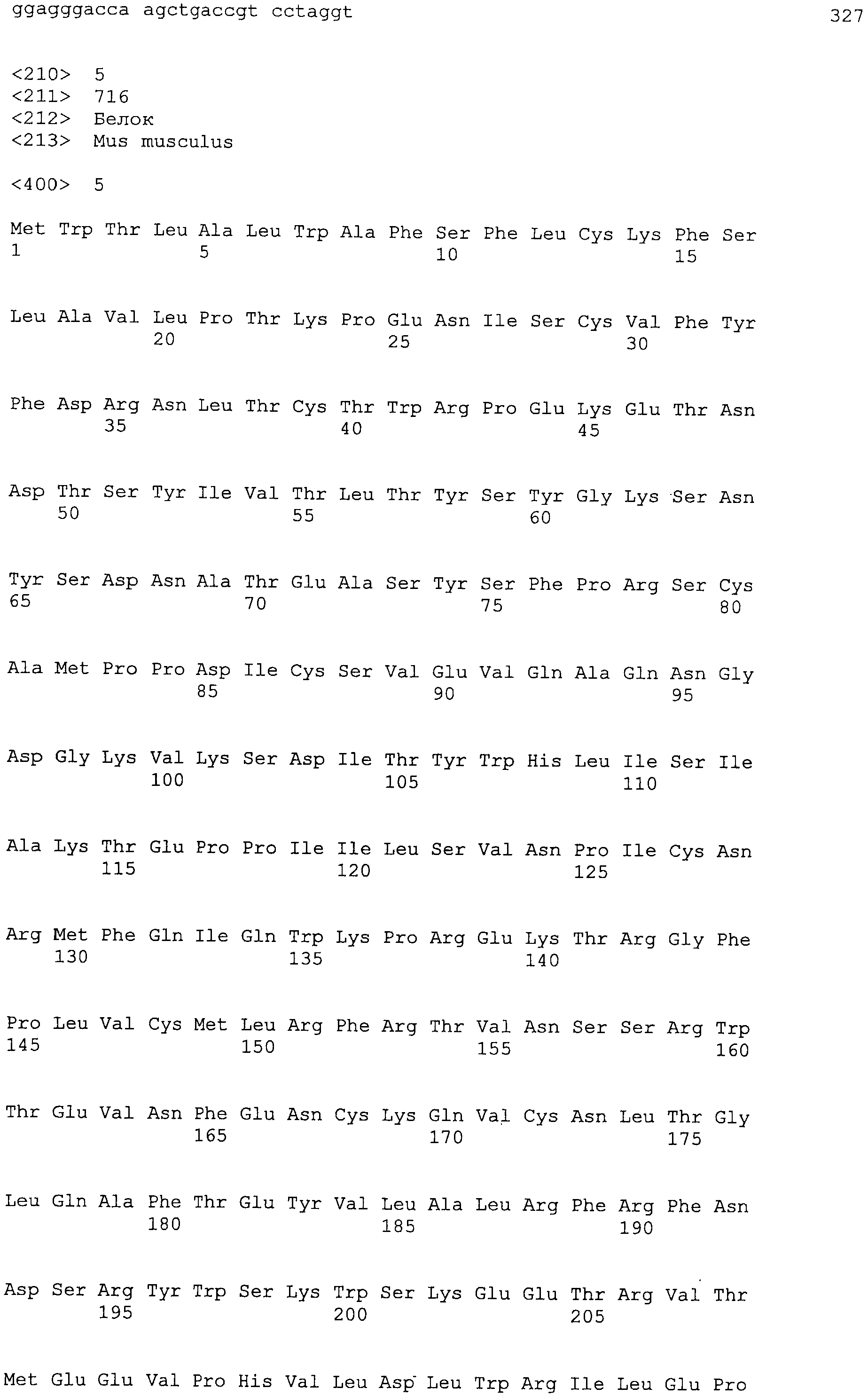Результат интеллектуальной деятельности: ТЕРАПЕВТИЧЕСКОЕ СРЕДСТВО ОТ ЗУДА
Вид РИД
Изобретение
Техническая область
Настоящее изобретение относится средствам для лечения или профилактики зуда.
Уровень техники
Многие цитокины известны в качестве гуморальных факторов, вовлеченных в рост и дифференцировку различных типов клеток, или в активацию функций дифференцированных зрелых клеток. Стимулированные цитокинами клетки продуцируют различные типы цитокинов, тем самым образуя в организме сети из множества цитокинов. Биологический гомеостаз поддерживается посредством тонкого равновесия взаимной регуляции цитокинов в этих сетях. Полагают, что многие воспалительные заболевания являются следствием нарушений в таких цитокиновых сетях. Таким образом, значительное внимание привлекает терапия на основе моноклональных антител. Например, было показано, что антитела против TNF и антитела против рецептора для IL-6 являются клинически высоко эффективными. С другой стороны, существует множество примеров неудач, когда отсутствуют терапевтические эффекты, если блокируют только один цитокин, такой как IL-4, вследствие активации компенсаторных каскадов при конкретных патологических состояниях.
Авторы настоящего изобретения добились успеха в выделении нового рецептора цитокинов NR10, который является высокогомологичным gp130, рецептору для передачи сигнала IL-6 (патентный документ 1). NR10 образует гетеродимер с рецептором онкостатина M (OSMR) и функционирует в качестве рецептора IL-31 (непатентный документ 1). NR-10 также известен как glm-r (непатентный документ 2), GPL (непатентный документ 3), IL-31RA (непатентный документ 4), и т.д. Также было описано, что у трансгенных мышей, сверхэкспрессирующих IL-31, самопроизвольно развивается зудящий дерматит (непатентный документ 4).
Однако нельзя утверждать, что инициированная экспрессия цитокинов у мышей или высокая концентрация цитокинов в крови у мышей с патологией являются истинными причинами заболевания. Совершенно неясно, вызывает ли блокада антителом передачи сигнала терапевтический эффект. Например, у трансгенных мышей, у которых сверхэспрессирован IL-18 в кератиноцитах, развивается зудящий дерматит. В модели самопроизвольного атопического дерматита у мышей NC/Nga концентрация IL-18 в крови возрастает при прогрессировании патологического состояния. Из этих данных было предположено, что причиной заболевания является сверхэкспрессия IL-18. Однако в действительности введение нейтрализующего антитела не оказывало терапевтического действия (непатентный документ 5).
Таким образом, ингибирование функции цитокинов не обязательно вызывает терапевтический эффект при заболеваниях с повышенной экспрессией цитокинов. Таким образом, из уровня экспрессии цитокина трудно предсказать, на какое заболевание ингибирование цитокинов оказывает терапевтический эффект. Таким образом, важно идентифицировать заболевания, при которых ингибирование передачи сигнала цитокина-мишени в действительности оказывает терапевтическое действие.
Документы уровня техники для настоящего изобретения представлены ниже.
Патентный документ 1: WO00/75314.
Непатентный документ 1: IL-31 is associated with cutaneous lymphocyte antigen-positive skin homing T cells in patients with atopic dermatitis., J Allergy Clin Immunol. 2006 Feb;117(2):418-25.
Непатентный документ 2: A novel type I cytokine receptor is expressed on monocytes, signals proliferation, and activates STAT-3 and STAT-5.J Biol Chem 277, 16831-6, 2002.
Непатентный документ 3: GPL, a novel cytokine receptor related to GP130 and leukemia inhibitory factor receptor. J Biol Chem 278, 49850-9, 2003.
Непатентный документ 4: Interleukin 31, a cytokine produced by activated T cells, induces dermatitis in mice. Nat Immunol 5, 752-60, 2004.
Непатентный документ 5: Administration of anti-interleukin 18 antibody fails to inhibit development of dermatitis in atopic dermatitis-model mice NC/Nga., British Journal of Dermatology 149: 39-45, 2003.
ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Проблемы, решаемые изобретением
Ввиду обстоятельств, описанных выше, было выполнено настоящее изобретение. Задачей настоящего изобретения является предоставление средств для лечения или профилактики зуда.
Средства для решения проблем
Авторы настоящего изобретения провели специализированные исследования для выполнения задачи, описанной выше. Авторы настоящего изобретения открыли, что антагонисты NR10, такие как нейтрализующие антитела против NR10, пригодны в качестве терапевтических или профилактических средств от зуда, тем самым, выполнив настоящее изобретение.
Настоящее изобретение относится к средствам для лечения или профилактики зуда. Более конкретно, настоящее изобретение относится к:
[1] профилактическому или терапевтическому средству от зуда, которое содержит в качестве активного ингредиента антагонист NR10;
[2] профилактическому или терапевтическому средству согласно [1], где антагонист NR10 представляет собой антитело, обладающее нейтрализующей активностью против NR10;
[3] профилактическому или терапевтическому средству согласно [2], где антитело представляет собой моноклональное антитело;
[4] профилактическому или терапевтическому средству согласно [3], где антитело представляет собой моноклональное антитело, обладающее нейтрализующей активностью против NR10 человека;
[5] профилактическому или терапевтическому средству согласно любому из [2]-[4], где антитело представляет собой рекомбинантное антитело; и
[6] профилактическому или терапевтическому средству согласно любому из [2]-[5], где антитело представляет собой химерное антитело, гуманизированное антитело или антитело человека.
Краткое описание фигур
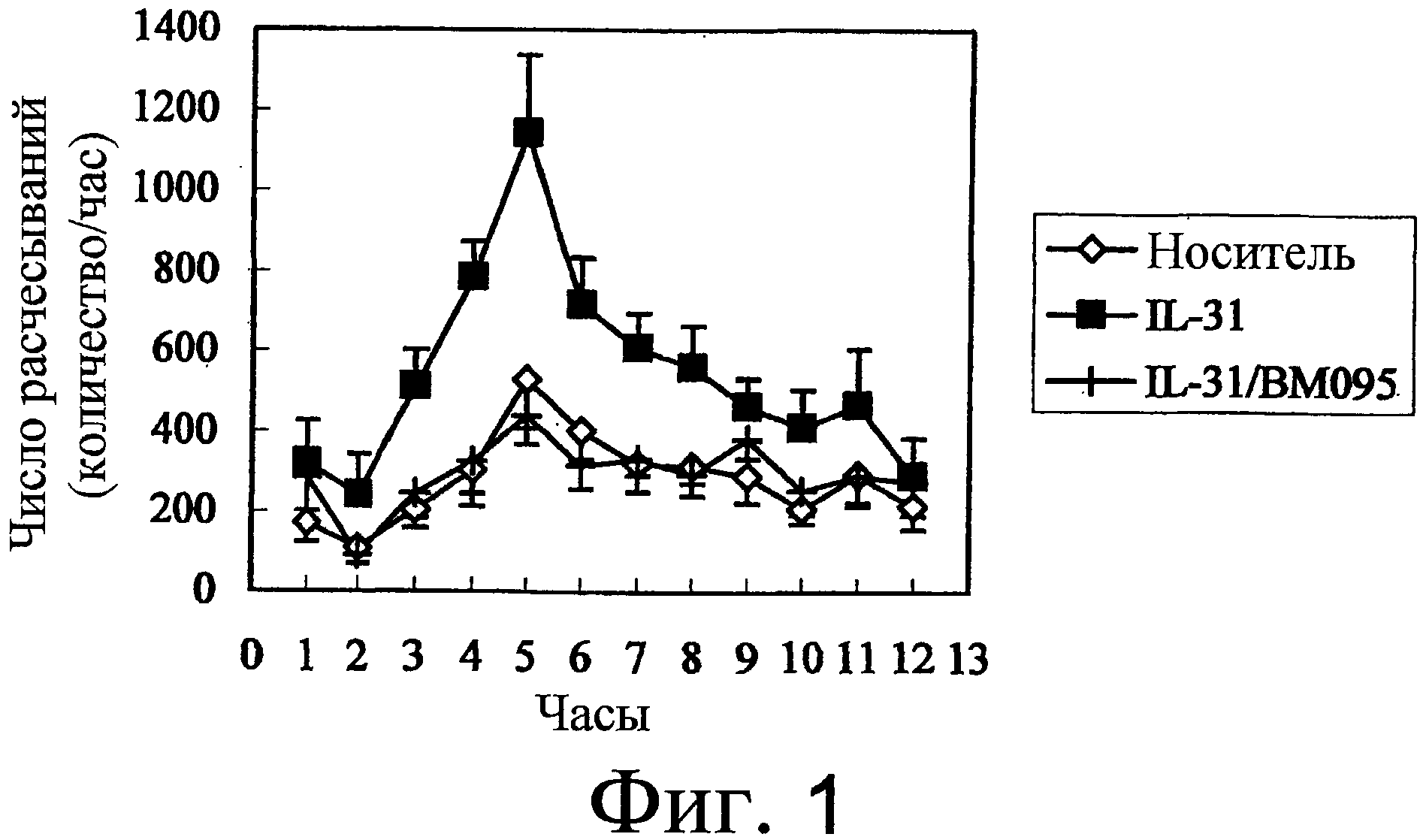
На фиг. 1 представлен график, на котором показана оценка индуцируемого IL-31 поведения расчесывания. Среднее значение ± стандартная ошибка.
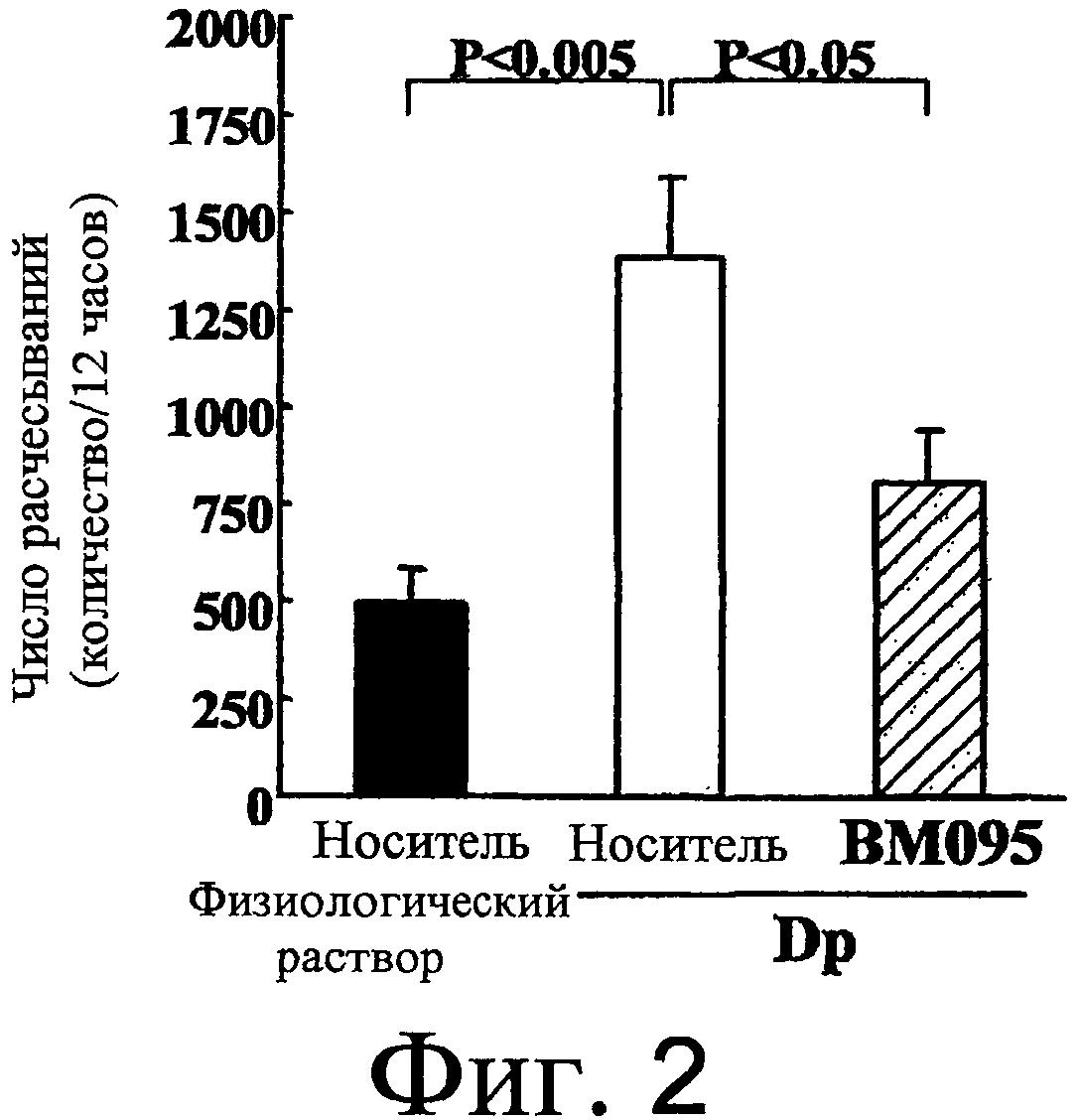
На фиг. 2 представлен график, на котором показана оценка индуцированного антигеном клещей поведения расчесывания. Среднее значение ± стандартная ошибка.
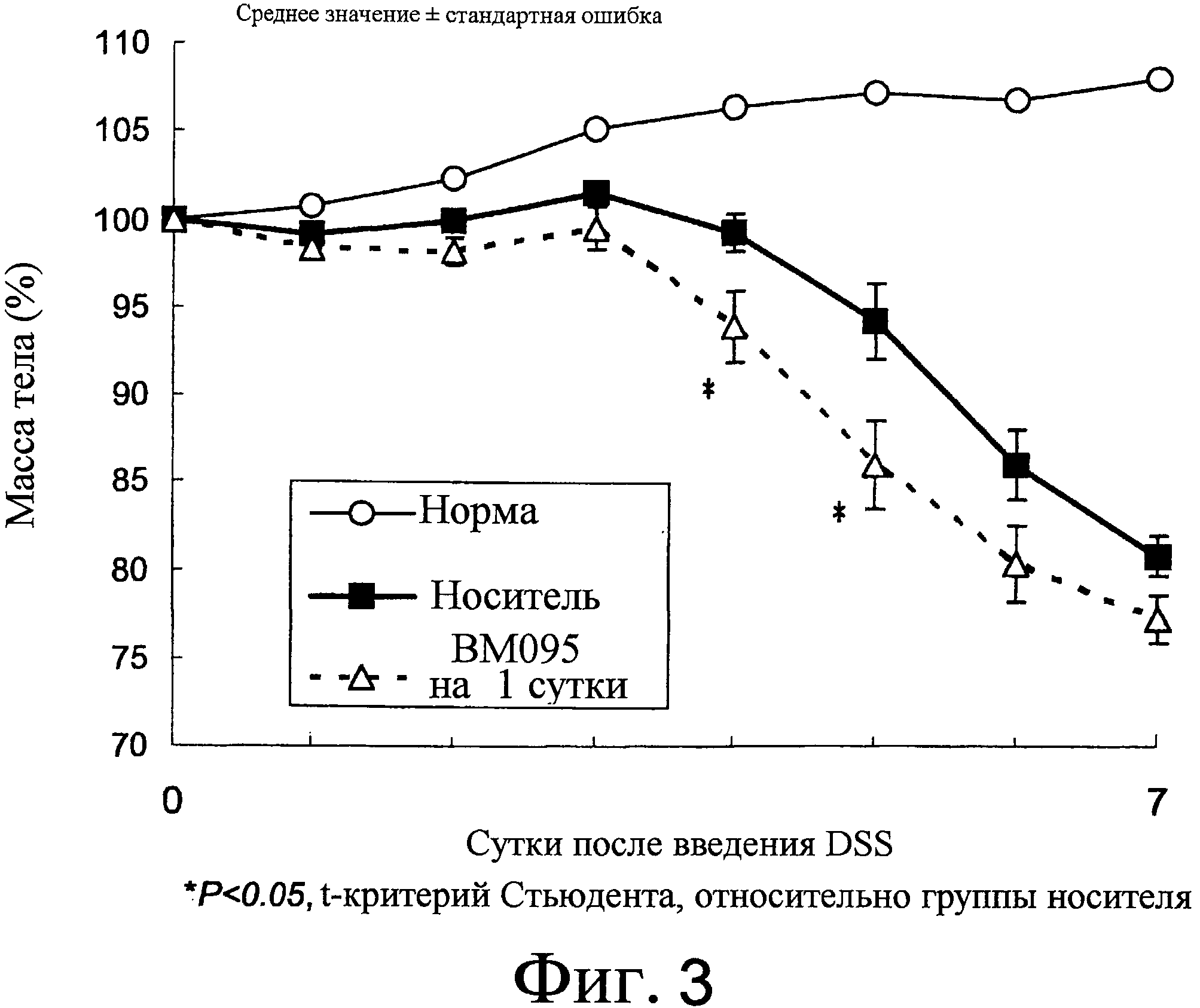
На фиг. 3 представлен график, на котором показаны процентные изменения массы тела с течением времени в модели колита DSS на мышах.
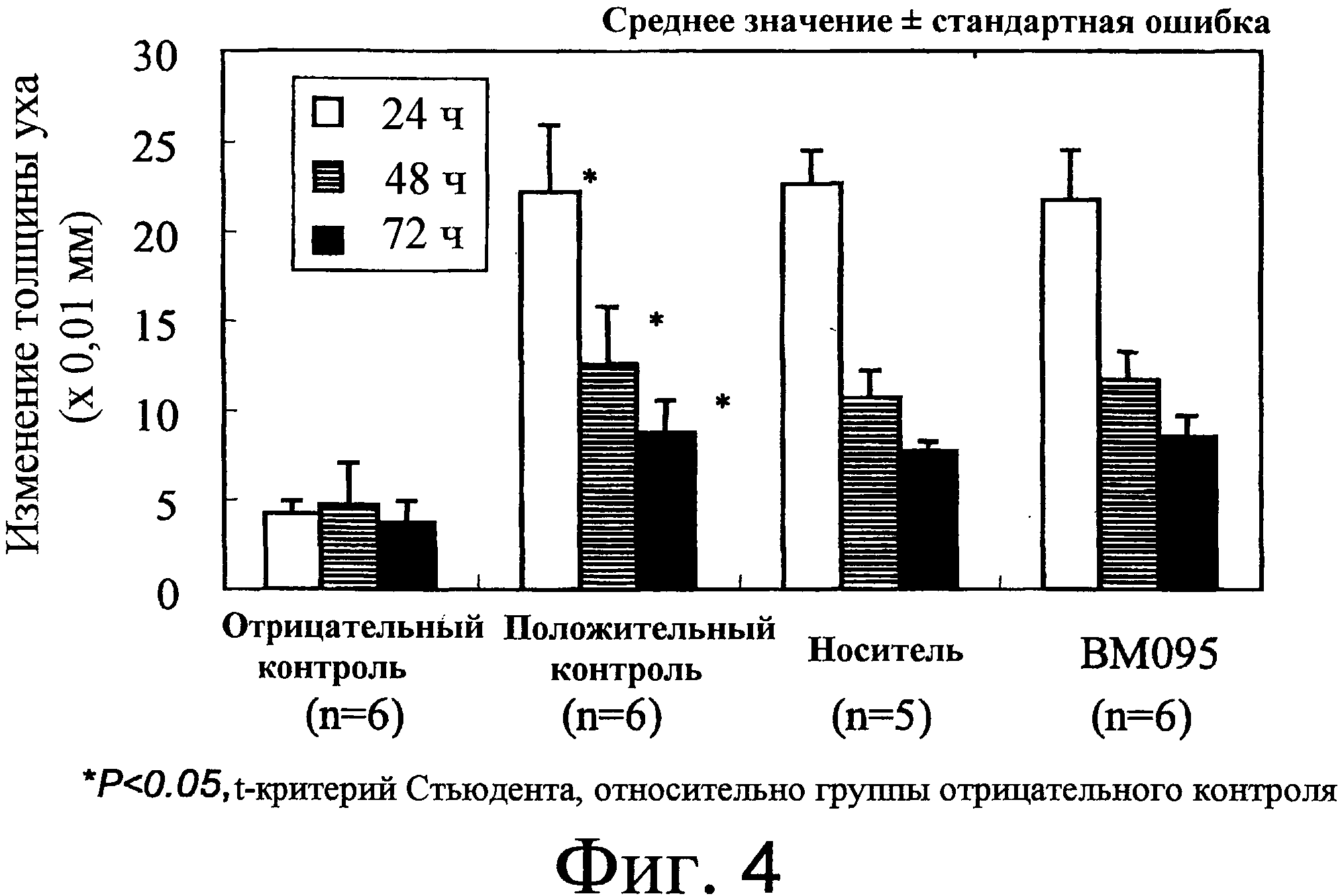
На фиг. 4 представлен график, на котором показаны изменения толщины уха с течением времени в модели индуцированного пикрилхлоридом контактного дерматита.
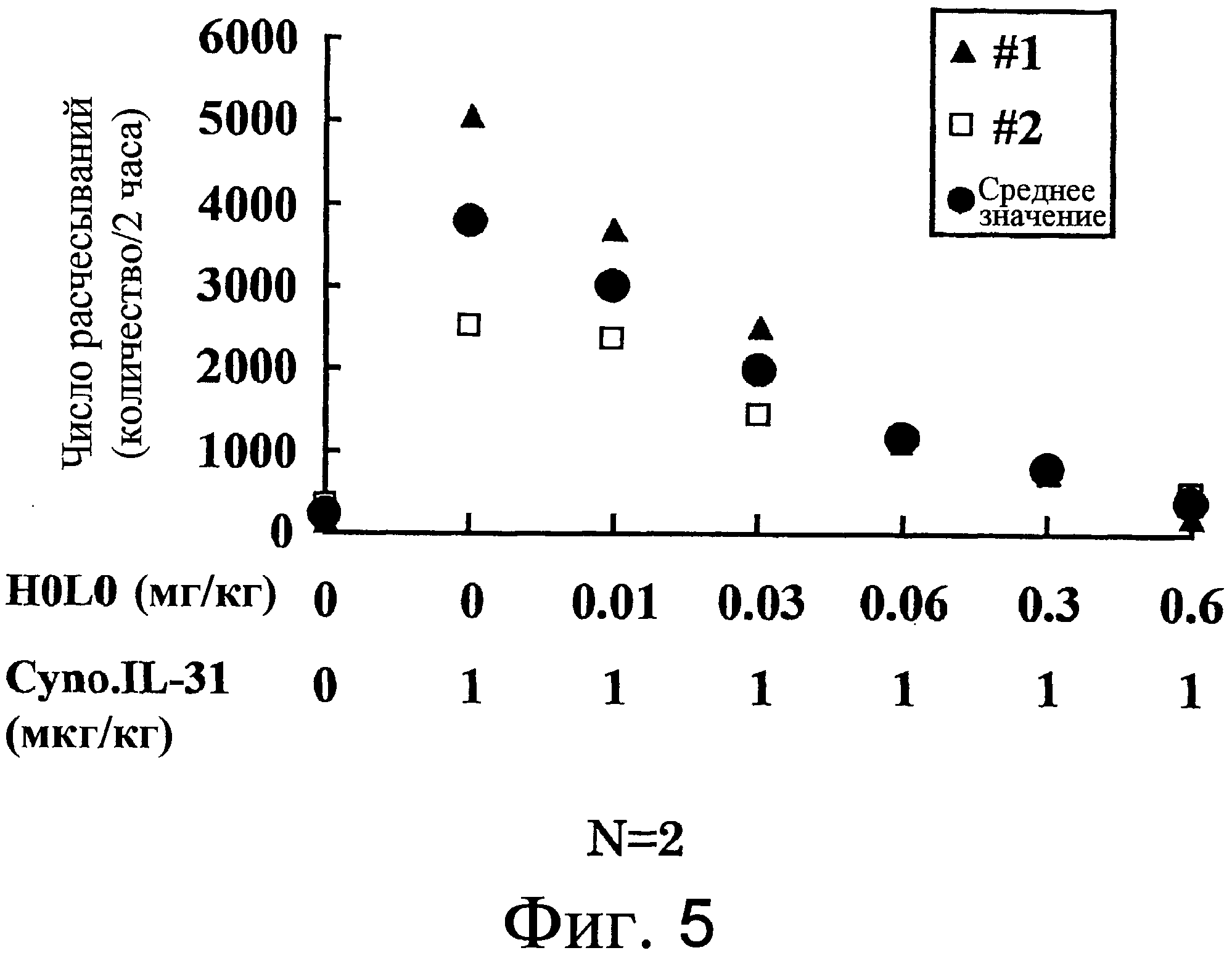
На фиг. 5 представлен график, на котором показан эффект антитела против NR10 H0L0 в отношении супрессии зуда с использованием в качестве индикатора количества расчесываний.
Способ осуществления изобретения
NR10 представляет собой белок, который образует гетеродимер с рецептором онкостатина M (OSMR) и функционирует в качестве рецептора IL-31. NR10 также известен как glm-r (J Biol Chem 277 16831-6, 2002), GPL (J Biol Chem 278, 49850-9, 2003), IL31RA (Nat Immunol 5, 752-60, 2004), и т.п. Таким образом, NR10 в настоящем изобретении также включает белки, имеющие эти названия.
NR10 в настоящем изобретении включает NR10, происходящий из человека, мышей и других млекопитающих. Предпочтительный NR10 включает, но не ограничивается конкретно ими, NR10, происходящий из человека и мышей. Существует множество известных вариантов по сплайсингу происходящего из человека NR10 (WO 00/075314). Среди указанных выше вариантов по сплайсингу, NR10.1 состоит из 662 аминокислот и содержит трансмембранный домен. NR10.2 представляет собой растворимый подобный рецептору белок, состоящий из 252 аминокислот, без трансмембранного домена. При этом известные варианты по сплайсингу NR10, которые функционируют в качестве трансмембранных рецепторных белков, включают NR10.3 и IL-31RAv3. NR10 человека по настоящему изобретению конкретно не ограничен, при условии, что он образует гетеродимер с рецептором онкостатина M (OSMR) и функционирует в качестве рецептора IL-31. Предпочтительный NR10 включает NR10.3 (также называемый ILRAv4 (Nat Immunol 5, 752-60, 2004)) и IL-31RAv3. NR 10.3 (IL31RAv4) состоит из 662 аминокислот (WO 00/075314; Nat Immunol 5, 752-60, 2004) и IL31RAv3 состоит из 732 аминокислот (регистрационный номер GenBank No: NM_139017). Аминокислотная последовательность IL31RAv4 представлена в SEQ ID NO: 6, и аминокислотная последовательность IL31RAv3 представлена в SEQ ID NO: 7. При этом происходящий из мыши NR10 включает белки, содержащие аминокислотную последовательность SEQ ID NO: 5.
В настоящем изобретении термин антагонист NR10 относится к веществу, которое блокирует внутриклеточную передачу сигнала, опосредуемую активацией NR10, через связывание с NR10 и, таким образом, приводит к утрате или подавлению биологической активности клеток. Биологическая активность включает, но не ограничивается ими, например, активность индукции или подавления продукции биологически активного вещества (например, хемокинов, воспалительных цитокинов и т.д.), активность стимуляции или подавления секреции биологически активного вещества, активность роста, активность индукции роста, активность выживания, активность дифференцировки, активность индукции дифференцировки, транскрипционную активность, активность мембранного транспорта, активность связывания, протеолитическую активность, активность фосфорилирования/дефосфорилирования, активность окисления-восстановления, активность переноса, нуклеолитическую активность, активность дегидратации, активность индукции клеточной гибели и активность индукции апоптоза.
Наличие антагонистической активности можно определять способами, известными специалистам в данной области. Например, тестируемое соединение может контактировать с NR10, экспрессированным на клеточной поверхности, в присутствии лиганда для определения того, произойдет ли внутриклеточная передача сигнала, которая служит признаком активации NR10. Это определение можно проводить, например, способом, описанным в ссылке "Dillon SR, et al., Interleukin 31, a cytokine produced by activated T cells, induces dermatitis in mice. Nat Immunol. 2004 Jul; 5(7):752-60". Соединения, которые ингибируют внутриклеточную передачу сигнала, отвечающую на стимуляцию лигандом, считают антагонистами NR10.
Антагонисты по настоящему изобретению могут представлять собой встречающиеся в природе или искусственные соединения. В настоящем изобретении можно использовать известные антагонисты. Можно использовать новые соединения, которые, как определено способами, описанными выше, обладают антагонистической активностью.
Один из вариантов осуществления антагониста NR10 по настоящему изобретению включает антитела, которые связываются с NR10. Такие антитела, которые связываются с NR10, конкретно не ограничены; однако предпочтительными являются антитела, которые специфично связываются с NR10. Предпочтительный вариант осуществления антител, которые связываются с NR10, включает антитела, обладающие нейтрализующей активностью против NR10. В настоящем изобретении "антитело, обладающее нейтрализующей активностью против NR10," относится к антителу, обладающему активностью подавления биологической активности, основанной на NR10. В настоящем изобретении "антитела, обладающие нейтрализующей активностью против NR10," могут представлять собой поликлональные или моноклональные антитела; однако в предпочтительном варианте осуществления антитела представляют собой моноклональные антитела.
Антитела по настоящему изобретению конкретно не ограничены, при условии, что они связываются с NR10, и они включают рекомбинантные антитела, такие как химерные антитела, гуманизированные антитела и антитела человека. Химерные антитела содержат, например, константные области тяжелой и легкой цепи антитела человека и вариабельные области тяжелой и легкой цепи антитела не являющегося человеком млекопитающего, такого как мышь. Химерные антитела можно получать известными способами. Например, антитела можно получать клонированием гена антитела из гибридомы, встраиванием его в соответствующий вектор и введением этой конструкции в хозяев (см., например, Carl, A. K. Borrebaeck, James, W. Larrick, THERAPEUTIC MONOCLONAL ANTIBODIES, Published in the United Kingdom by MACMILLAN PUBLISHERS LTD, 1990). Конкретно, синтезируют кДНК вариабельных областей (V-областей) антитела из мРНК гибридом с использованием обратной транскриптазы. После получения ДНК, кодирующих V-области представляющего интерес антитела, их связывают с ДНК, кодирующими константные области (C-области) требуемого антитела человека. Полученные конструкции встраивают в экспрессирующие векторы. Альтернативно ДНК, кодирующие V-области антитела, можно встраивать в экспрессирующие векторы, содержащие ДНК, кодирующие C-области антитела человека. ДНК встраивают в экспрессирующие векторы, так чтобы они экспрессировались под регуляцией участков регуляции экспрессии, например, энхансеров и промоторов. На следующей стадии клетки-хозяева можно трансформировать экспрессирующими векторами для обеспечения экспрессии химерного антитела.
Гуманизированные антитела также называют переформированными антителами человека, и их получают переносом определяющих комплементарность областей (CDR) антитела, происходящего из не являющегося человеком млекопитающего, такого как мышь, в CDR антитела человека. Также для их получения известны общие способы генетической рекомбинации. Конкретно, синтезируют последовательность ДНК, сконструированную так, чтобы CDR антитела мыши были связаны с каркасными областями (FR) антитела человека, с помощью ПЦР с использованием в качестве праймеров нескольких олигонуклеотидов, которые имеют участки, охватывающие концы как CDR, так и FR. Затем полученную ДНК лигируют с ДНК, кодирующей константную область антитела человека, встраивают в экспрессирующий вектор и вводят хозяину для продукции антитела (см. публикацию патентной заявки Европы № EP 239400 и публикацию международной патентной заявки № WO 96/02576). FR, подлежащие связыванию с CDR, выбирают таким образом, чтобы CDR образовывали подходящий антигенсвязывающий участок. Если необходимо, в каркасные области вариабельной области антитела можно вносить аминокислотную замену, делецию, добавление и/или вставку, так чтобы CDR переформированного антитела человека образовывали надлежащий антигенсвязывающий участок (Sato, K. et al., Cancer Res. (1993) 53, 851-856).
Способы получения антител человека также известны. Например, желаемые антитела человека с антигенсвязывающей активностью можно получать путем (1) сенсибилизации лимфоцитов человека представляющими интерес антигенами или клетками, экспрессирующими представляющие интерес антигены in vitro; и (2) слияния сенсибилизированных лимфоцитов с клетками миеломы человека, такими как U266 (см. публикацию японской патентной заявки Kokoku No. (JP-B) H01-59878 (рассмотренная, принятая японская патентная заявка, опубликованная для опротестования)). Альтернативно, желаемое антитело человека также можно получать иммунизацией трансгенного животного, имеющего полный набор генов антител человека, требуемым антигеном (см. публикации международных патентных заявок №№ WO 93/12227, WO 92/03918, WO 94/02602, WO 94/25585, WO 96/34096 и WO 96/33735).
Более того, известны способы получения антител человека сортировкой фаговых библиотек антител человека. Например, с использованием способа фагового дисплея вариабельную область антитела человека экспрессируют в качестве одноцепочечного антитела (scFv) на поверхности фага, и можно отбирать фаги, которые связываются с антигеном. Посредством анализа генов выбранных фагов можно определять последовательности ДНК, кодирующие вариабельные области антител человека, которые связываются с антигеном. Если идентифицируют последовательности ДНК scFv, которые связываются с антигеном, можно конструировать соответствующие экспрессирующие векторы, содержащие эти последовательности, с получением антител человека. Такие способы хорошо известны. В качестве ссылки могут быть приведены WO 92/01047, WO 92/20791, WO 93/06213, WO 93/11236, WO 93/19172, WO 95/01438, WO 95/15388 и т.п.
Аминокислотная последовательность вариабельной области тяжелой или легкой цепи может иметь замену, делецию, добавление и/или вставку одной или нескольких аминокислот в аминокислотной последовательности вариабельной области тяжелой или легкой цепи антитела, у которого была подтверждена нейтрализующая активность против NR10. Хорошо известные специалистам в данной области способы получения аминокислотной последовательности вариабельной области тяжелой или легкой цепи антитела, обладающего активностью нейтрализации NR10, в которой одна или несколько аминокислот заменены, удалены, добавлены и/или вставлены в аминокислотной последовательности вариабельной области тяжелой или легкой цепи, включают способы внесения мутаций в белки. Например, специалисты в данной области могут получить мутанты, функционально эквивалентные вариабельной области тяжелой или легкой цепи антитела, обладающего активностью нейтрализации NR10, путем внесения соответствующих мутаций в аминокислотную последовательность вариабельной области тяжелой или легкой цепи антитела, обладающего активностью нейтрализации NR10, с использованием сайт-направленного мутагенеза (Hashimoto-Gotoh, T, Mizuno, T, Ogasahara, Y, и Nakagawa, M. (1995) An oligodeoxyribonucleotide-directed dual amber method for site-directed mutagenesis. Gene 152, 271-275, Zoller, MJ, and Smith, M.(1983) Oligonucleotide-directed mutagenesis of DNA fragments cloned into M13 vectors. Methods Enzymol. 100, 468-500, Kramer, W, Drutsa, V, Jansen, HW, Kramer, B, Pflugfelder, M, и Fritz, HJ (1984) The gapped duplex DNA approach to oligonucleotide-directed mutation construction. Nucleic Acids Res. 12, 9441-9456, Kramer W, and Fritz HJ (1987) Oligonucleotide-directed construction of mutations via gapped duplex DNA Methods. Enzymol. 154, 350-367, Kunkel, TA (1985) Rapid and efficient site-specific mutagenesis without phenotypic selection. Proc Natl Acad Sci USA. 82, 488-492) или сходные с ними. Таким образом, также к вариабельным областям тяжелых или легких цепей антитела по настоящему изобретению относятся вариабельные области тяжелых или легких цепей антитела, которые содержат одну или несколько аминокислотных мутаций в вариабельных областях тяжелых или легких цепей и обладают активностью нейтрализации NR10.
Когда заменяют аминокислотный остаток, предпочтительно проводят мутацию аминокислоты в отличающуюся аминокислоту(ы), которая сохраняет свойства боковой цепи аминокислоты. Примерами свойств боковой цепи аминокислот являются: гидрофобные аминокислоты (A, I, L, M, F, P, W, Y и V), гидрофильные аминокислоты (R, D, N, C, E, Q, G, H, K, S и T), аминокислоты, содержащие алифатические боковые цепи (G, A, V, L, I и P), аминокислоты, имеющие содержащие гидроксильную группу боковые цепи (S, T и Y), аминокислоты, имеющие содержащие серу боковые цепи (C и M), аминокислоты, имеющие содержащие карбоновую кислоту и амид боковые цепи (D, N, E и Q), аминокислоты, содержащие основные боковые цепи (R, K и H), и аминокислоты, содержащие ароматические боковые цепи (H, F, Y и W) (аминокислоты представлены в скобках с помощью однобуквенного кода). Аминокислотные замены в пределах каждой группы называют консервативными заменами. Хорошо известно, что полипептид, содержащий модифицированную аминокислотную последовательность, в которой один или несколько аминокислотных остатков данной аминокислотной последовательности удалены, добавлены и/или заменены другими аминокислотами, может сохранять исходную биологическую активность (Mark, D. F. et al., Proc. Natl. Acad. Sci. USA; (1984) 81:5662-6; Zoller, M. J. and Smith, M., Nucleic Acids Res. (1982) 10:6487-500; Wang, A. et al., Science (1984) 224:1431-3; Dalbadie-McFarland, G. et al., Proc. Natl. Acad. Sci. USA (1982) 79:6409-13). Такие мутанты обладают идентичностью аминокислот по меньшей мере 70%, более предпочтительно по меньшей мере 75%, более предпочтительно по меньшей мере 80%, еще более предпочтительно по меньшей мере 85%, еще более предпочтительно по меньшей мере 90%, и наиболее предпочтительно по меньшей мере 95%, с вариабельными областями тяжелых и легких цепей до мутаций аминокислот. В настоящем документе идентичность последовательности определяют как процент остатков, идентичных остаткам в исходной аминокислотной последовательности вариабельной области тяжелой цепи или вариабельной области легкой цепи, определенный после выравнивания последовательностей и внесения соответствующим образом пропусков для максимального увеличения идентичности последовательности, при необходимости. Идентичность аминокислотных последовательностей можно определять способом, описанным выше.
Альтернативно аминокислотные последовательности вариабельных областей тяжелой или легкой цепи, которые имеют замену, делецию, добавление и/или вставку одной или нескольких аминокислот в аминокислотной последовательности вариабельных областей тяжелой или легкой цепи и сохраняют нейтрализующую активность против NR10, можно получать из нуклеиновых кислот, которые гибридизуются в строгих условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, кодирующей аминокислотную последовательность вариабельных областей тяжелой или легкой цепи. Строгие условия гибридизации для выделения нуклеиновой кислоты, гибридизующейся в строгих условиях с нуклеиновой кислотой, включающей нуклеотидную последовательность, кодирующую аминокислотную последовательность вариабельных областей тяжелой или легкой цепи, включают, например, условия 6M мочевины, 0,4% SDS, 0,5x SSC, и 37°C, или условия гибридизации со строгостью, эквивалентной этой. При более строгих условиях, например, условиях 6M мочевины, 0,4% SDS, 0,1x SSC и 42°C, можно ожидать выделения нуклеиновых кислот со значительно более высокой гомологией. Последовательности выделенных нуклеиновых кислот можно определять известными способами, описанными ниже. Общая гомология нуклеотидной последовательности выделенной нуклеиновой кислоты представляет собой по меньшей мере 50% идентичность последовательности или более, предпочтительно 70% или более, более предпочтительно 90% или более (например, 95%, 96%, 97%, 98%, 99% или более).
Нуклеиновые кислоты, которые гибридизуются в строгих условиях с нуклеиновой кислотой, состоящей из нуклеотидной последовательности, кодирующей аминокислотную последовательность вариабельных областей тяжелой или легкой цепи, также можно выделять с использованием, вместо описанных выше способов с использованием технологий гибридизации, способов амплификации генов, таких как полимеразная цепная реакция (ПЦР) с использованием праймеров, синтезированных на основе информации нуклеотидной последовательности, кодирующей аминокислотную последовательность вариабельных областей тяжелой или легкой цепи.
Конкретно, идентичность одной нуклеотидной последовательности или аминокислотной последовательности с другой последовательностью можно определять с использованием алгоритма BLAST, Karlin and Altschul (Proc. Natl. Acad. Sci. USA (1993) 90, 5873-7). На основе этого алгоритма были разработаны программы, такие как BLASTN и BLASTX (Altschul et al., J. Mol. Biol. (1990) 215, 403-10). Для анализа нуклеотидных последовательностей согласно BLASTN на основе BLAST, параметры устанавливают, например, как score = 100 и wordlength = 12. С другой стороны, параметры, используемые для анализа аминокислотных последовательностей с помощью BLASTX на основе BLAST, включают, например, score= 50 и wordlength= 3. При использовании программ BLAST и Gapped BLAST используют параметры по умолчанию для каждой программы. Конкретные способы для таких анализов известны в данной области (см. web-сайт National Center for Biotechnology Information (NCBI), Basic Local Alignment Search Tool (BLAST); http://www.ncbi.nlm.nih.gov).
Альтернативно антитела по настоящему изобретению могут представлять собой низкомолекулярные антитела. Низкомолекулярные антитела по настоящему изобретению включают фрагменты антител, лишенные некоторых частей целого антитела (например, целого IgG), и они конкретно не ограничены, при условии, что они сохраняют активность нейтрализации NR10. Низкомолекулярные антитела по настоящему изобретению конкретно не ограничены, при условии, что они содержат часть целых антител. Низкомолекулярные антитела предпочтительно содержат вариабельную область тяжелой цепи (VH) или вариабельную область легкой цепи (VL). Особенно предпочтительные низкомолекулярные антитела содержат как VH, так и VL. Кроме того, предпочтительные примеры низкомолекулярных антител по настоящему изобретению включают низкомолекулярные антитела, содержащие CDR антитела. CDR, содержащиеся в низкомолекулярных антителах, могут включать некоторые или все из шести CDR антитела.
Низкомолекулярные антитела по настоящему изобретению предпочтительно имеют меньшую молекулярную массу, чем целые антитела. Однако низкомолекулярные антитела могут образовывать мультимеры, например димеры, тримеры или тетрамеры, и, таким образом, их молекулярная масса может превышать молекулярную массу целых антител.
Пример низкомолекулярных антител по настоящему изобретению включает антитела ScFv. Антитела ScFv представляют собой одноцепочечные полипептиды, полученные связыванием вариабельной области тяжелой цепи ([VH]) и вариабельной области легкой цепи ([VL]) через линкер, или сходные с ним (Huston, J. S. et al., Proc. Natl. Acad. Sci. U.S.A. (1988) 85, 5879-5883; Pluckthun "The Pharmacology of Monoclonal Antibodies" Vol. 113, eds., Resenburg and Moore, Springer Verlag, New York, pp. 269-315, (1994)). Порядок связывания вариабельных областей тяжелой цепи и легкой цепи, подлежащих связыванию, конкретно не ограничен, и они могут быть расположены в любом порядке. Примеры расположения приведены ниже.
[VH] линкер [VL]
[VL] линкер [VH]
Аминокислотная последовательность вариабельной области тяжелой цепи или вариабельной области легкой цепи может содержать замену, делецию, добавление и/или вставку. Более того, вариабельная область тяжелой цепи и вариабельная область легкой цепи также могут быть лишены некоторых частей или в них могут быть добавлены другие полипептиды, при условии, что они обладают активностью связывать антиген при связывании вместе. Альтернативно вариабельные области могут быть химеризованными или гуманизированными.
В настоящем изобретении линкеры, которые связывают вариабельные области антитела, включают произвольные пептидные линкеры, которые можно встраивать с использованием способов генетической инженерии, или синтетические линкеры, такие как линкеры, описанные в Protein Engineering, 9(3), 299-305, 1996.
Предпочтительными линкерами в настоящем изобретении являются пептидные линкеры. Длина пептидных линкеров конкретно не ограничена, и специалисты в данной области могут соответствующим образом выбрать длину, в зависимости от цели. Типичная длина составляет от одной до 100 аминокислот, предпочтительно от 3 до 50 аминокислот, более предпочтительно от 5 до 30 аминокислот, и особенно предпочтительно от 12 до 18 аминокислот (например, 15 аминокислот).
Аминокислотные последовательности таких пептидных линкеров включают, например:
Ser;
Gly-Ser;
Gly-Gly-Ser;
Ser-Gly-Gly;
Gly-Gly-Gly-Ser (SEQ ID NO: 8);
Ser-Gly-Gly-Gly (SEQ ID NO: 9);
Gly-Gly-Gly-Gly-Ser (SEQ ID NO: 10);
Ser-Gly-Gly-Gly-Gly (SEQ ID NO: 11);
Gly-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: 12);
Ser-Gly-Gly-Gly-Gly-Gly (SEQ ID NO: 13;
Gly-Gly-Gly-Gly-Gly-Gly-Ser (SEQ ID NO: 14);
Ser-Gly-Gly-Gly-Gly-Gly-Gly (SEQ ID NO: 15);
(Gly-Gly-Gly-Gly-Ser (SEQ ID NO: 10))n; и
(Ser-Gly-Gly-Gly-Gly (SEQ ID NO: 11))n,
Синтетические химические линкеры (химические поперечно-сшивающие агенты) включают поперечно-сшивающие агенты, которые обычно используют для поперечного сшивания пептидов, например, N-гидроксисукцинимид (NHS), дисукцинимидилсуберат (DSS), бис(сульфосукцинимидил)суберат (BS3), дитиобис(сукцинимидилпропионат) (DSP), дитиобис(сульфосукцинимидилпропионат) (DTSSP), этиленгликоль-бис (сукцинимидилсукцинат) (EGS), этиленгликоль-бис(сульфосукцинимидилсукцинат) (сульфо-EGS), дисукцинимидилтартрат (DST), дисульфосукцинимидилтартрат (сульфо-DST), бис[2-(сукцинимидоксикарбонилокси)этил]сульфон (BSOCOES) и бис[2-(сульфосукцинимидоксикарбонилокси)этил]сульфон (сульфо-BSOCOES). Эти поперечно-сшивающие агенты являются коммерчески доступными.
Антитела по настоящему изобретению включают антитела, в которых к аминокислотной последовательности антитела по настоящему изобретению добавлены два или более аминокислотных остатков. Кроме того, к настоящему изобретению относятся слитые белки, которые получены слиянием одного из описанных выше антител и второго пептида или белка. Эти слитые белки можно получать лигированием полинуклеотида, кодирующего антитело по настоящему изобретению, и полинуклеотида, кодирующего второй пептид или полипептид, в рамке считывания, встраиванием его в экспрессирующий вектор, и экспрессией слитой конструкции в хозяине. Для этой цели доступны некоторые способы, известные специалистам в данной области. Пептид- или полипептид-партнер, слитый с антителом по настоящему изобретению, может представлять собой известный пептид, например, FLAG (Hopp, T. P. et al., BioTechnology 6, 1204-1210 (1988)), 6x His, состоящий из шести остатков His (гистидина), 10x His, гемагглютинин вируса гриппа (HA), фрагмент c-myc человека, фрагмент VSV-GP, фрагмент p18HIV, T7-метку, HSV-метку, E-метку, фрагмент T-антигена SV40, lck-метку, фрагмент α-тубулина, B-метку и фрагмент белка C. Другие полипептиды-партнеры, подлежащие слиянию с антителами по настоящему изобретению, включают, например, GST (глутатион-S-трансферазу), HA (гемагглютинин вируса гриппа), константную область иммуноглобулина, β-галактозидазу и MBP (связывающий мальтозу белок). Полинуклеотид, кодирующий один из этих коммерчески доступных пептидов или полипептидов, можно подвергать слиянию с полинуклеотидом, кодирующим антитело по настоящему изобретению. Слитный полипептид можно получать путем экспрессии слитой конструкции.
Более того, антитела по настоящему изобретению могут представлять собой конъюгированные антитела, которые связаны с любыми из различных молекул, включающих полиэтиленгликоль (PEG), гиалуроновую кислоту, радиоактивные вещества, флуоресцентные вещества, люминесцентные вещества, ферменты и токсины. Такие конъюгированные антитела можно получать путем химической модификации полученных антител. Способы модификации антител являются общепризнанными в данной области (например, US 5057313 и US 5156840). "Антитела" по настоящему изобретению также включают такие конъюгированные антитела.
Кроме того, предпочтительный вариант осуществления антител против NR10 в настоящем изобретении включает, но не ограничивается конкретно ими, антитела, которые распознают домен 1. В настоящем изобретении домен 1 относится к участку из аминокислот в положениях от 21 до 120 (от LPAKP до LENIA) в аминокислотной последовательности NR10 человека SEQ ID NO: 7, где нумерация аминокислот основана на последовательности, включающей сигнальный пептид.
Антитела по настоящему изобретению могут отличаться по аминокислотной последовательности, молекулярной массе, изоэлектрической точке, наличию/отсутствию цепей сахаров и конформации, в зависимости от клетки или хозяина, продуцирующих антитело, или способа очистки, как описано ниже. Однако полученное антитело относится к настоящему изобретению, при условии, что оно обладает функцией антагониста NR10. Например, когда антитело по настоящему изобретению экспрессируется в прокариотических клетках, например E. coli, на N-конец исходной аминокислотной последовательность антитела добавляют остаток метионина. Такие антитела относятся к настоящему изобретению.
Моноклональные антитела, обладающие нейтрализующей активностью против NR10, можно получать, например, следующим способом: моноклональные антитела против NR10 получают с использованием в качестве антигена NR10 или его фрагмента, происходящих из млекопитающего, такого как человек или мышь, известными способами, а затем из полученных таким образом моноклональных антител против NR10 отбирают антитела, обладающие нейтрализующей активностью против NR10. В частности, для иммунизации в соответствии с общепринятыми способами иммунизации в качестве сенсибилизирующего антигена используют желаемый антиген или клетки, экспрессирующие желаемый антиген. Моноклональные антитела против NR10 можно получать путем слияния полученных иммунных клеток с известными исходными клетками с использованием общепринятых способов слияния клеток, и скрининга их в отношении продуцирующих моноклональное антитело клеток (гибридом) общепринятыми способами скрининга. Животные, подлежащие иммунизации, включают, например, млекопитающих, таких как мыши, крысы, кролики, овцы, обезьяны, козы, ослы, коровы, лошади и свиньи. Антиген можно получать с использованием известной последовательности гена NR10 в соответствии с известными способами, например, способами с использованием бакуловируса (например, WO 98/46777).
Гибридомы можно получать, например, в соответствии со способом Milstein et al. (Kohler, G. and Milstein, C., Methods Enzymol. (1981) 73: 3-46) или сходными с ним. Когда иммуногенность антигена является низкой, иммунизацию можно проводить после связывания антигена с макромолекулой, обладающей иммуногенностью, такой как альбумин.
Варианты антител по настоящему изобретению, которые обладают активностью нейтрализации NR10, включают моноклональные антитела, которые обладают активностью нейтрализации NR10 человека. Антигены, используемые для получения моноклональных антител, которые обладают активностью нейтрализации NR10 человека, конкретно не ограничены, при условии, что они обеспечивают получение антител, которые обладают активностью нейтрализации NR10 человека. Например, известно, что существует ряд вариантов NR10 человека, и в качестве иммуногена можно использовать любой вариант, при условии, что он обеспечивает получение антител, которые обладают активностью нейтрализации NR10 человека. Альтернативно, в тех же условиях, в качестве иммуногена можно использовать пептидный фрагмент NR10 или белок, в котором в природную последовательность NR10 внесены искусственные мутации. NR10.3 человека является одним из предпочтительных иммуногенов для получения антител, которые обладают активностью связывания и/или нейтрализации NR10, по настоящему изобретению.
Более того, активность нейтрализации антитела против NR10 можно измерять, например, путем выявления эффекта подавления роста IL-31-зависимой клеточной линии, как описано в справочных примерах.
При этом моноклональные антитела также можно получать путем иммунизации посредством ДНК. Иммунизация посредством ДНК представляет собой способ, в котором векторную ДНК, сконструированную так, чтобы ген, кодирующий антигенный белок, мог экспрессироваться у животного, подлежащего иммунизации, вводят животному, и в организме животного экспрессируется иммуноген, обеспечивая стимуляцию иммунной системы. По сравнению с общепринятыми способами иммунизации на основе введения белковых антигенов, ожидается, что иммунизация посредством ДНК является преимущественной в том, что:
- она обеспечивает стимуляцию иммунной системы при сохранении структуры мембранного белка; и
- не требуется очистка иммуногена.
С другой стороны, трудно комбинировать иммунизацию посредством ДНК со средством для стимуляции иммунной системы, таким как адъювант.
Для получения моноклонального антитела посредством иммунизации ДНК, животному, подлежащему иммунизации, сначала вводят ДНК, кодирующую NR10. ДНК, кодирующую NR10, можно синтезировать известными способами, такими как ПЦР. Полученную ДНК встраивают в соответствующий экспрессирующий вектор и вводят животному, подлежащему иммунизации. Экспрессирующие векторы, которые можно использовать, включают коммерчески доступные экспрессирующие векторы, такие как pcDNA3.1. Вектор можно вводить в живой организм общепринятыми способами. Например, иммунизацию ДНК можно проводить путем введения золотых частиц, покрытых экспрессирующим вектором, в клетки с помощью генной пушки. Вспомогательное введение с использованием экспрессирующих NR10 клеток после иммунизации ДНК представляет собой предпочтительный способ получения моноклонального антитела.
После иммунизации млекопитающего, как описано выше, и подтверждения повышения уровня желаемого антитела в сыворотке, собирают иммунные клетки млекопитающего и подвергают их слиянию. Предпочтительными иммунными клетками, в частности, являются клетки селезенки.
Для слияния с указанными выше клетками иммунной системы используют миеломные клетки млекопитающих. Предпочтительно, чтобы миеломные клетки имели соответствующие селективные маркеры для скрининга. Селективный маркер относится к фенотипу, который позволяет (или не позволяет) выживание в конкретных условиях культивирования. Известные селективные маркеры включают дефицит гипоксантингуанинфосфорибозилтрансферазы (в дальнейшем в настоящем документе сокращаемый как "дефицит HGPRT") и дефицит тимидинкиназы (в дальнейшем в настоящем документе сокращаемый как "дефицит TK"). Дефицитные по HGPRT или TK клетки проявляют чувствительность к гипоксантин-аминоптерин-тимидину (в дальнейшем в настоящем документе обозначаемую как "чувствительность к HAT"). В селективной среде HAT, чувствительные к HAT клетки не могут синтезировать ДНК и, таким образом, погибают. Однако при слиянии с нормальными клетками они могут продолжать синтезировать ДНК через каскад спасения нормальных клеток и, таким образом, могут расти даже в селективной среде HAT.
Дефицитные по HGPRT или TK клетки можно отбирать с использованием среды, содержащей 6-тиогуанин, 8-азагуанин (в дальнейшем в настоящем документе сокращаемый как "8AG") или 5'-бромдезоксиуридин. В то время как нормальные клетки погибают вследствие включения этих аналогов пиримидинов в ДНК, клетки, лишенные этих ферментов, могут выживать в селективной среде, поскольку они не могут встраивать эти аналоги пиримидинов. Другой селективный маркер, называемый маркером устойчивости к G418, придает устойчивость к 2-дезоксистрептаминовым антибиотикам (аналогам гентамицина) благодаря гену устойчивости к неомицину. Различные миеломные клетки, пригодные для слияния клеток, известны.
Слияние иммунных клеток и миеломных клеток можно по существу проводить в соответствии с известными способами, например, способом Kohler и Milstein (Kohler. G. and Milstein, C., Methods Enzymol. (1981) 73, 3-46).
Более конкретно, слияние клеток можно проводить, например, в обычной культуральной среде в присутствии средства, обеспечивающего слияние клеток. Средство, обеспечивающее слияние клеток, включает, например, полиэтиленгликоль (PEG) и вирус Сендай (HVJ). При необходимости, также можно добавлять вспомогательное средство, такое как диметилсульфоксид, для повышения эффективности слияния.
Иммунные клетки и миеломные клетки можно использовать в произвольно определенном соотношении. Например, соотношение иммунных клеток и миеломных клеток предпочтительно составляет от 1 до 10. Культуральные среды, используемые для слияния клеток, включают, например, среды, которые пригодны для роста клеток миеломной клеточной линии, такие как RPMI 1640 и MEM, и другие общепринятые культуральные среды, используемые для этого типа клеточной культуры. Кроме того, культуральные среды также можно дополнять сывороткой, такой как эмбриональная телячья сыворотка (FCS).
Заданные количества иммунных клеток и миеломных клеток хорошо перемешивают в культуральной среде, а затем смешивают с раствором PEG, предварительно нагретым до 37°C, с получением слитых клеток (гибридом). В способе слияния клеток, например, PEG со средней молекулярной массой приблизительно 1000-6000 можно добавлять к клеткам, как правило, в концентрации от 30% до 60% (масс./об.). Затем, несколько раз проводят последовательное добавление соответствующей культуральной среды, приведенной выше, и удаление супернатанта центрифугированием для устранения средства для слияния клеток и прочих, которые являются неблагоприятными для роста гибридом.
Полученные гибридомы можно подвергать скринингу с использованием селективной среды в соответствии с селективным маркером, которым обладают миеломные клетки, используемые для слияния клеток. Например, дефицитные по HGPRT или TK клетки можно подвергать скринингу путем культивирования их в среде HAT (среде, содержащей гипоксантин, аминоптерин и тимидин). Конкретно, если для слияния клеток используют чувствительные к HAT миеломные клетки, то клетки, успешно слитые с нормальными клетками, можно селективно выращивать в среде HAT. Культивирование клеток с использованием указанной выше среды HAT продолжают в течение периода времени, достаточного для гибели всех клеток (неслитых клеток), за исключением требуемых гибридом. Конкретно, как правило, требуемые гибридомы можно отбирать культивированием клеток в течение от нескольких суток до нескольких недель. Затем можно проводить скрининг и клонирование по отдельности гибридом, которые продуцируют представляющее интерес антитело, проведением обычных способов лимитирующих разведений. Альтернативно антитела, которые распознают NR10, можно получать способом, описанным в WO 03/104453.
Скрининг и отдельное клонирование представляющего интерес антитела можно пригодным образом проводить с помощью известных способов скрининга на основе реакции антиген-антитело. Например, антиген связывают с носителем, таким как гранулы, изготовленные из полистирола или сходных с ним, и коммерчески доступные 96-луночные микропланшеты для титрования, а затем подвергают реакции с культуральным супернатантом гибридомы. Далее, носитель промывают, а затем подвергают реакции со вторичным антителом, меченным ферментом, или сходными с ним. Когда культуральный супернатант содержит представляющее интерес антитело, реактивное к сенсибилизирующему антигену, вторичное антитело связывается с носителем через это антитело. В конце, проводят детекцию вторичного антитела, связанного с носителем, для определения того, содержит ли культуральный супернатант представляющее интерес антитело. Гибридомы, продуцирующие желаемое антитело, способное связываться с антигеном, можно клонировать способом лимитирующих разведений или сходными с ним. Для этой цели в качестве антигена можно использовать не только антиген, используемый для иммунизации, но также белок NR10, по существу эквивалентный ему. Например, в качестве антигена можно использовать клеточную линию, экспрессирующую NR10, внеклеточный домен NR10 или олигопептид, состоящий из неполной аминокислотной последовательности, составляющей домен.
В дополнение к описанному выше способу получения гибридомы с помощью иммунизации не являющегося человеком животного антигеном, представляющие интерес антитела также можно получать сенсибилизацией лимфоцитов человека антигеном. Конкретно, сначала лимфоциты человека сенсибилизируют белком NR10 in vitro. Затем сенсибилизированные лимфоциты подвергают слиянию с соответствующим партнером по слиянию. Например, в качестве партнера по слиянию можно использовать происходящие из человека миеломные клетки со способностью к непрерывному делению (см. публикацию японской патентной заявки Kokoku No. (JP-B) H1-59878 (рассмотренную, принятую японскую патентную заявку, опубликованную для опротестования)). Антитела, полученные этим способом, представляют собой антитела человека, обладающие активностью связывания белка NR10.
Антитела, полученные описанным выше способом, можно получать способами, известными специалистам в данной области. Например, на основе последовательности распознающего NR10 антитела, антитело можно получать способами генетической рекомбинации, известными специалистам в данной области. Конкретно, на основе последовательности распознающего NR10 антитела можно конструировать полинуклеотид, кодирующий антитело, встраивать его в экспрессирующий вектор, а затем экспрессировать в соответствующих клетках-хозяевах (см. например, Co, M. S. et al., J. Immunol. (1994) 152, 2968-2976; Better, M. and Horwitz, A. H., Methods Enzymol. (1989) 178, 476-496; Pluckthun, A. and Skerra, A., Methods Enzymol. (1989) 178, 497-515; Lamoyi, E., Methods Enzymol. (1986) 121, 652-663; Rousseaux, J. et al., Methods Enzymol. (1986) 121, 663-669; Bird, R. E. and Walker, B. W., Trends Biotechnol. (1991) 9, 132-137).
Векторы включают векторы M13, векторы pUC, pBR322, pBluescript и PCR-Script. Альтернативно, когда целью является субклон и вырезанная кДНК, векторы включают, например, pGEM-T, pDIRECT и pT7, в дополнение к векторам, описанным выше. Экспрессирующие векторы особенно пригодны при использовании векторов для продукции антител по настоящему изобретению. Например, когда целью является экспрессия в E. coli, таких как JM109, DH5α, HB101 и XL1-Blue, экспрессирующие векторы не только обладают описанными выше характеристиками, которые позволяют амплификацию вектора в Е. coli, но большинство из них также обладают промотором, который позволяет эффективную экспрессию в E. coli, например, промотором lacZ (Ward et al., Nature (1989) 341, 544-546; FASEB J. (1992) 6, 2422-2427), промотором araB (Better et al., Science (1988) 240, 1041-1043), промотором T7 или сходными с ним. Такие векторы включают pGEX-5X-1 (Pharmacia), "систему QIAexpress" (Qiagen), pEGFP или pET (в этом случае, хозяином предпочтительно являются BL21, которые экспрессируют РНК-полимеразу T7), в дополнение к векторам, описанным выше.
Векторы могут содержать сигнальные последовательности для секреции антитела. В качестве сигнальной последовательности для секреции антитела можно использовать сигнальную последовательность pelB (Lei, S. P. et al J. Bacteriol. (1987) 169, 4379), когда белок секретируется в периплазму E. coli. Вектор можно вводить в клетки-хозяева, например, способами с хлоридом кальция или электропорации.
В дополнение к векторам для E. coli, векторы для продукции антител по настоящему изобретению включают, например, экспрессирующие векторы млекопитающих (например, pcDNA3 (Invitrogen), pEF-BOS (Nucleic Acids Res. 1990, 18(17), p5322), pEF и pCDM8), экспрессирующие векторы из насекомых (например, "бакуловирусную систему Bac-to-BAC" (Gibco-BRL) и pBacPAK8), экспрессирующие векторы из растений (например, pMH1 и pMH2), экспрессирующие векторы из животных (например, pHSV, pMV и pAdexLcw), ретровирусные экспрессирующие векторы (например, pZIPneo), экспрессирующие векторы дрожжей (например, "Pichia Expression Kit" (Invitrogen), pNV11 и SP-Q01) и экспрессирующие векторы Bacillus subtilis (например, pPL608 и pKTH50).
Когда целью является экспрессия в клетках животных, таких как клетки CHO, COS и NIH3T3, векторы должны иметь промотор, необходимый для экспрессии в клетках, например, промотор SV40 (Mulligan et al., Nature (1979) 277, 108), промотор MMLV-LTR, промотор EF1α (Mizushima et al., Nucleic Acids Res. (1990) 18, 5322) и промотор CMV, и более предпочтительно они имеют ген для селекции трансформированных клеток (например, ген устойчивости к лекарственному средству, который позволяет оценку с использованием средства (неомицина, G418 или сходных с ними). Векторы с такими характеристиками включают, например, pMAM, pDR2, pBK-RSV, pBK-CMV, pOPRSV и pOP13.
Кроме того, для стабильной экспрессии генов и амплификации генов в клетках можно использовать следующий способ: в клетки CHO, дефицитные по каскаду синтеза нуклеиновых кислот, вводят вектор (например, pSV2-dhfr (Molecular Cloning 2nd edition, Cold Spring Harbor Laboratory Press, 1989)), который обладает геном DHFR, который компенсирует дефицит, и вектор амплифицируют с использованием метотрексата (MTX). Альтернативно, для временной экспрессии гена используют следующий способ: клетки COS с геном, экспрессирующим T-антиген SV40, на их хромосоме, трансформируют вектором (pcD и т.п.) с ориджином репликации SV40. Также можно использовать ориджины реплекации, происходящие из вируса полиомы, аденовируса, вируса папилломы крупного рогатого скота (BPV) и т.п. Для амплификации числа копий гена в клетках-хозяевах, экспрессирующие векторы могут дополнительно иметь селективные маркеры, такие как ген аминогликозидтрансферазы (APH), ген тимидинкиназы (TK), ген ксантин-гуанин-фосфорибозилтрансферазы E. coli (Ecogpt) и ген дигидрофолатредуктазы (dhfr).
Антитела по настоящему изобретению, полученные способами, описанными выше, можно выделять из клеток-хозяев или из окружения клеток (из среды или сходных с ней) и очищать до гомогенного состояния. Антитела можно выделять и очищать способами, обычно используемыми для выделения и очистки антител, и тип этого способа не ограничен. Например, антитела можно выделять и очищать путем надлежащего выбора и комбинирования колоночной хроматографии, фильтрации, ультрафильтрации, высаливания, осаждения растворителем, экстракции растворителем, дистилляции, иммунопреципитации, SDS-полиакриламидного гель-электрофореза, изоэлектрофокусирования, диализа, перекристаллизации и т.п.
Способы хроматографии включают, например, аффинную хроматографию, ионообменную хроматографию, гидрофобную хроматографию, гель-фильтрацию, обращенно-фазовую хроматографию и адсорбционную хроматографию (Strategies for Protein Purification and Characterization: A Laboratory Course Manual. Ed Daniel R. Marshak et al., Cold Spring Harbor Laboratory Press, 1996). Способы хроматографии, описанные выше, можно проводить с использованием жидкостной хроматографии, например, ВЭЖХ и FPLC. Колонки, которые можно использовать для аффинной хроматографии, включают колонки с белком A и колонки с белком G. Колонки с использованием белка A включают, например, Hyper D, POROS и Sepharose FF (GE Amersham Biosciences). Настоящее изобретение включает антитела, которые являются в высокой степени очищенными с использованием этих способов очистки.
Активность связывания NR10 полученных антител можно определять способами, известными специалистам в данной области. Способы определения антигенсвязывающей активности антитела включают, например, ELISA (твердофазный иммуноферментный анализ), EIA (иммуноферментный анализ), RIA (радиоиммунный анализ) и способ флуоресцентных антител. Например, при использовании иммуноферментного анализа, содержащие антитело образцы, такие как очищенные антитела и культуральные супернатанты антителопродуцирующих клеток, добавляют в покрытые антигеном планшеты. Добавляют вторичное антитело, меченное ферментом, таким как щелочная фосфатаза, и планшеты инкубируют. После промывания добавляют субстрат фермента, такой как п-нитрофенилфосфат, и измеряют поглощение для оценки антигенсвязывающей активности.
Более того, нейтрализующую активность антитела против NR10 можно определять, например, способом, описанным в справочных примерах, в которых наблюдается эффект ингибирования роста IL-31-зависимой клеточной линии.
Антагонисты NR10 или антитела, обладающие нейтрализующей активностью против NR10 в настоящем изобретении, можно использовать в качестве профилактических или терапевтических средств от зуда. Авторы настоящего изобретения вводили антитела, обладающие нейтрализующей активностью против NR10 мыши, модельным животным с зудом, и показали, что антитела обладают выраженным терапевтическим эффектом. Более того, ожидается, что антагонисты NR10, не являющиеся антителами, также обладают терапевтическим эффектом против зуда, как показано в примерах.
Авторы настоящего изобретения открыли, что антагонистические антитела против NR10 обладают терапевтическим эффектом против зуда. С другой стороны, было выявлено, что в модели острого контактного дерматита и в модели острого колита DSS, антагонистические антитела против NR10 сами по себе не обладают эффектом против этих заболеваний.
В настоящем изобретении лечение зуда отличается от лечения заболеваний и симптомов, которые вызывают зуд (например, заболеваний, описанных ниже, таких как атопический дерматит и гепатит типа C). Таким образом, терапевтические или профилактические средства по настоящему изобретению от зуда нацелены на сам зуд, и они не предназначены для лечения или профилактики заболеваний и симптомов, которые вызывают зуд. Терапевтические или профилактические средства по настоящему изобретению вводят пациентам, нуждающимся в лечении или профилактике зуда, для лечения или профилактики зуда, но не для лечения или профилактики заболеваний и симптомов, которые вызывают зуд.
Зуд, подлежащий лечению с помощью настоящего изобретения, конкретно не ограничен, и он может представлять собой зуд любого типа. Конкретные примеры зуда, подлежащего лечению с помощью настоящего изобретения, включают, например, зуд при чесотке, педикулезе, укусах и ужалениях насекомыми, крапивнице, атопическом дерматите, контактном дерматите, красном плоском лишае, потнице, герпетиформном дерматите, ксеродерме, обструкции желчных путей, первичном билиарном циррозе (PBC), инфекционном гепатите, таком как гепатит C, уремии, хронической почечной недостаточности, диализе почек, лимфоме, лейкозе, стойкой красной полицитемии, беременности, употреблении лекарственных средств (барбитуратах, салицилатов и т.д.), гипертиреоидизме, сахарном диабете и злокачественных опухолях органов.
Профилактические или терапевтические средства по настоящему изобретению от зуда содержат в качестве активного ингредиента описанный выше антагонист NR10 или антитело, обладающее нейтрализующей активностью против NR10. Выражение "содержит в качестве активного ингредиента антагонист NR10" означает включение антагониста NR10 в качестве по меньшей мере одного активного ингредиента, и оно не ограничивает состав антагониста NR10. Терапевтические или профилактические средства по настоящему изобретению от зуда могут содержать другие ингредиенты, которые обеспечивают профилактику или лечение зуда, в сочетании с антагонистом NR10.
Зуд, от которого используют терапевтические или профилактические средства по настоящему изобретению, конкретно не ограничен, и он может развиваться по любой причине; однако предпочтительно зуд представляет собой зуд, вовлекающий IL-31. Такой зуд, вовлекающий IL-31, включает зуд, вызываемый IL-31, и зуд с высокой экспрессией IL-31.
Антагонисты NR10 по настоящему изобретению можно изготавливать в качестве составов в соответствии со стандартными способами (см., например, Remington's Pharmaceutical Science, latest edition, Mark Publishing Company, Easton, USA). Кроме того, они могут содержать фармацевтически приемлемые носители и/или добавки, если необходимо. Например, они могут содержать поверхностно-активные вещества (например, PEG и Tween), эксципиенты, антиоксиданты (например, аскорбиновую кислоту), красители, вкусовые добавки, консерванты, стабилизаторы, буферные средства (например, фосфорную кислоту, лимонную кислоту и другие органические кислоты), хелатирующие агенты (например, ЭДТА), суспендирующие вещества, обеспечивающие изотоничность вещества, связующие вещества, дезинтегрирующие вещества, смазывающие вещества, промоторы текучести и модифицирующие вещества. Однако, не ограничиваясь ими, средства для профилактики или лечения воспалительных заболеваний по настоящему изобретению могут содержат другие широко используемые носители. Такие носители конкретно включают легкую безводную кремниевую кислоту, лактозу, кристаллическую целлюлозу, маннит, крахмал, кармелозу кальция, кармелозу натрия, гидроксипропилцеллюлозу, гидроксипропилметилцеллюлозу, поливинилацетальдиэтиламиноацетат, поливинилпирролидон, желатин, триглицерид жирной кислоты средней длины цепи, полиоксиэтилен-гидрогенизированное касторовое масло 60, сахарозу, карбоксиметилцеллюлозу, кукурузный крахмал и неорганическую соль. Также средства могут содержать другие низкомолекулярные полипептиды, белки, такие как сывороточный альбумин, желатин и иммуноглобулин, и аминокислоты, такие как глицин, глутамин, аспарагин, аргинин и лизин. Когда антагонист NR10 изготавливают в качестве водного раствора для инъекции, антагонист NR10 можно растворять в изотоническом растворе, содержащем, например, физиологический раствор, декстрозу или другие адъюванты. Адъюванты могут включать, например, D-сорбит, D-маннозу, D-маннит и хлорид натрия. Кроме того, вместе с ними можно использовать соответствующие солюбилизирующие вещества, например, спирты (например, этанол), полиспирты (например, пропиленгликоли и PEG) и неионные детергенты (полисорбат 80 и HCO-50).
Если необходимо, антагонисты NR10 можно инкапсулировать в микрокапсулы (микрокапсулы, изготовленные из гидроксиметилцеллюлозы, желатина, полиметилметакрилата и т.п.) и преобразовывать в компоненты коллоидных систем для доставки лекарственных средств (липосомы, микросферы с альбумином, микроэмульсии, наночастицы и нанокапсулы) (например, см. "Remington's Pharmaceutical Science 16th edition" &, Oslo Ed. (1980)). Более того, известны способы получения лекарственных средств с замедленным высвобождением, и их можно использовать для антагонистов NR10 (Langer et al., J. Biomed. Mater. Res. (1981) 15, 167-277; Langer, Chem. Tech. (1982) 12, 98-105; патент США № 3773919; европейская патентная заявка (EP) № 58481; Sidman et al., Biopolymers (1983) 22, 547-56; EP 133988).
Средства для профилактики или лечения зуда по настоящему изобретению можно вводить либо перорально, либо парентерально, но предпочтительно их вводят парентерально. Конкретно, эти средства вводят пациентам путем инъекции или подкожного введения. Инъекции включают, например, внутривенные инъекции, внутримышечные инъекции и подкожные инъекции, для системного или местного введения. Средства можно вводить в области предполагаемого подавления воспаления или в окружающие их области путем местной инфузии, в частности, внутримышечной инъекции. Способы введения можно надлежащим образом выбирать в соответствии с возрастом и состоянием пациента. Дозу для однократного введения можно выбирать, например, из диапазона от 0,0001 до 100 мг активного ингредиента на кг массы тела. Альтернативно, например, когда средства вводят пациентам-людям, дозу активного ингредиента можно выбирать из диапазона от 0,001 до 1,000 мг/кг массы тела. Доза для однократного введения предпочтительно содержит, например, приблизительно от 0,01 до 50 мг/кг массы тела антагониста NR10. Однако доза средства для профилактики или лечения зуда по настоящему изобретению не ограничивается этими примерами.
Настоящее изобретение также относится к лекарственным средствам от зуда, которые содержат антагонист IL-31 в качестве активного ингредиента. Такие антагонисты IL-31 конкретно не ограничены, при условии, что они представляют собой вещества, которые ингибируют биологическую активность IL-31 путем связывания с IL-31. Предпочтительные антагонисты IL-31 включают, например, антитела против IL-31 (например, WO 2006/088955, WO 2006/88956 и WO 2006/122079). Получение, изменение, модификацию, продукцию, очистку, введение, включение в состав, и т.п. антител против IL-31 можно проводить в соответствии с представленным выше описанием, касающимся антител против NR10.
Все документы уровня техники, цитированные в настоящем описании, включены в настоящий документ в качестве ссылок.
ПРИМЕРЫ
Ниже настоящее изобретение описано конкретно с использованием примеров, однако его не следует истолковывать, как ограниченное ими.
Пример 1
Оценка индуцируемого IL-31 поведения расчесывания
Десять мкг IL-31 мыши (собственно полученного) внутривенно вводили нормальной самке мышей BALB/с в возрасте 9 недель (Charles River Laboratories Japan). Проводили мониторинг и анализ поведения расчесывания в течение 12 часов сразу после введения с использованием системы для подсчета расчесываний (MicroAct; NeuroScience Inc.). В результате группа, в которой вводили IL-31 (n=8), продемонстрировала значимое повышение количества расчесываний с пиком приблизительно через пять часов после введения, по сравнению с группой, в которой вводили носитель (PBS, содержащей 0,5% сыворотку мыши BALB/c) (n=8). Это индуцированное IL-31 поведение расчесывания полностью подавлялось при внутривенном введении 350 мг/кг BM095, нейтрализующего антитела против NR10 мыши, перед введением IL-31 (n=8) (фиг. 1). Этот результат демонстрирует, что нейтрализующее антитело против NR10 обладает эффектом подавления индуцируемого IL-31 зуда.
Эффект нейтрализующего антитела против NR10 в модели индуцированного антигеном клещей дерматита
Пять мкг неочищенного экстракта Dermatophagoides pteronyssinus (Dp) (Cosmo Bio LSL) вводили в качестве антигена клещей внутрикожно самкам мышей NC/Nga Tnd Crlj SPF в возрасте 9 недель (Charles River Laboratories Japan) на вентральной стороне их ушей три раза в неделю в течение трех недель для индукции дерматита (Int Arch Allergy Immunol 2004;133:55-63). В контрольной группе растворителя для Dp вводили 5 мкл нормального солевого раствора (Otsuka Pharmaceutical Co.) по той же схеме (n=7). В этой модели патологии нейтрализующее антитело против NR10 мыши BM-095 внутривенно вводили в дозе 20 мг/кг на 0, 3, 7, 10, 14, 17 и 21 сутки (n=8). Для контрольной группы носителя внутривенно вводили 200 ммоль/л NaCl/20 ммоль/л натрий-ацетатного буфера (pH 5,5) по той же схеме (n=8).
Зуд оценивали путем подсчета количества расчесываний во время измерения, составляющего 12 часов, на 21 сутки с использованием системы подсчета расчесываний (MicroAct; NeuroScience Inc.). Результат показал, что число расчесываний было значимо повышено в контрольной группе носителя по сравнению с контрольной группой растворителя для Dp (p<0,005). В группе введения BM095 число расчесываний было значимо снижено по сравнению с контрольной группой носителя (p<0,05) (фиг. 2).
Этот результат демонстрирует, что нейтрализующее антитело против NR10 обладает эффектом супрессии зуда.
Пример 2
Эффект H0L0 в отношении подавления индуцируемого IL-31 зуда у яванских макаков
Исследовали эффект антитела против NR10 человека H0L0 (аминокислотная последовательность тяжелой цепи/SEQ ID NO: 17; аминокислотная последовательность легкой цепи/SEQ ID NO: 18) на зуд, индуцированный внутривенным введением IL-31 яванского макака яванскому макаку в возрасте от 4 до 5 лет. PBS (носитель) или H0L0 внутривенно вводили в дозе 0,01, 0,03, 0,06, 0,3 и 0,6 мг/кг. Через двадцать четыре часа после внутривенного введения внутривенно вводили 1 г/кг IL-31 яванского макака, а затем его поведение записывали с помощью видеокамеры в течение двух часов. Подсчитывали число расчесываний, при воспроизведении записанного видео, принимая три или более последовательных расчесывающих действий как расчесывание. Результат показал, что H0L0 снижало число индуцируемых IL-31 яванского макака расчесываний зависимым от дозы образом (фиг. 5). Этот результат демонстрирует, что антитело против NR10 H0L0 обладает эффектом супрессии зуда.
Справочный пример 1
Получение клеточных линий Ba/F3, экспрессирующих NR10 и OSMR
кДНК NR10 человека (См. WO 00/75314 SEQ ID NO: 1/SEQ ID NO: 16) встраивали в экспрессирующий вектор pCOS1 (Biochem. Biophys. Res. Commun. 228, p838-45, 1996) и полученный вектор назвали pCosNR10.3. кДНК рецептора онкостатина M (OSMR, регистрационный номер GenBank № NM003999) выделяли посредством ПЦР из библиотеки плацент человека и аналогичным образом конструировали экспрессирующий вектор pCos1-hOSMR. 10 мкг каждого из векторов одновременно вводили в IL-3-зависимую происходящую из про-B-клеток клеточную линию мыши Ba/F3 посредством электропорации (BioRad Gene Pulser, 960 мкФ, 0,33 кВ). После введения добавляли IL-31 человека и клетки культивировали с получением клеточной линии, которая пролиферирует IL-31-зависимым образом. Аналогично, также получали зависимую от IL-31 мыши клеточную линию, образованную из клеток Ba/F3, экспрессирующих гены NR10 мыши и OSMR мыши.
Обе клеточные линии проявляли ED50, составляющую несколько нг/мл, и хорошо пролиферировали. Зависимая от IL-31 человека клеточная линиям не отвечала на IL-31 мыши, и при добавлении белка NR10 человека (внеклеточный домен) происходило ее подавление. При этом зависимая от IL-31 мыши клеточная линия не отвечала на IL-31 человека, и при добавлении белка NR10 мыши (внеклеточный домен) не происходило ее подавления.
Справочный пример 2
Получение белка NR10 (внеклеточный домен)
кДНК NR10 человека использовали в качестве матрицы для амплификации посредством ПЦР только внеклеточного домена. Затем к амплифицированной области присоединяли последовательность FLAG-метки на C-конце и встраивали в экспрессирующий вектор pCXND3 (WO2005/005636) (pCXND3-NR10-flag). Десять мкг линеаризованного вектора вводили в клеточную линию клеток яичника китайского хомяка DG44 посредством электропорации (BioRad Gene PulserII, 25 мкФ, 1,5 кВ). Получили клеточную линию, обладающую высоким уровнем экспрессии. Супернатант клеточной линии, культивированной в большом масштабе, очищали с использованием колонки с антителом против FLAG (Sigma) и гель-фильтрации с получением очищенного образца, который подвергали экспериментам, описанным ниже. Также аналогичным образом получали NR10 мыши (внеклеточный домен), на C-конец которого добавлена последовательность FLAG-метки.
Справочный пример 3
Выделение scFv, имеющего нейтрализующую активность против NR10 мыши, и получение химерного IgG BM095
Клоны-кандидаты подвергали скринингу из фаговой библиотеки антител человека способом сортировки с использованием биотинилированного белка NR10 мыши (внеклеточный домен). Из этих клонов очищали секреторные scFv и добавляли их в систему для анализа роста зависимых от IL-31 клеток Ba/F3, описанную в справочном примере 1. В результате успешно получили клон, обладающий выраженной активностью подавления роста, BM095.
Для конструирования экспрессирующего вектора последовательности вариабельной области тяжелой цепи (VH) и вариабельной области легкой цепи (VL) человека в BM095 связывали с константной областью IgG2a (после CH1) и константной областью λ-цепи, соответственно, с помощью ПЦР. Эта аминокислотная последовательность VH представлена в SEQ ID NO: 1, а нуклеотидная последовательность, кодирующая эту аминокислотную последовательность, представлена в SEQ ID NO: 2. Аминокислотная последовательность VL представлена в SEQ ID NO: 3, а нуклеотидная последовательность, кодирующая эту аминокислотную последовательность, представлена в SEQ ID NO: 4. Соответствующие линеаризованные экспрессирующие векторы одновременно вводили в клетки DG44 и отбирали клеточную линию, экспрессирующую химерный IgG на высоком уровне. Из супернатанта крупномасштабной культуры этой клеточной линии получали очищенный образец с помощью колоночной хроматографии с белком A (rProtein A Sepharose Fast Flow, GE Amersham Biosciences) и катионообменной (SP-TOYOPEARL 650M, TOSOH) колоночной хроматографии. Затем использовали смолу ActiClean Etox (Sterogen) для снижения уровня пирогенов ниже предела детекции.
Справочный пример 4
Эффективность BM095 при индуцированном декстрана сульфатом натрия (DSS) колите
Создавали модель индуцированного DSS колита (J Immunol 2003; 171:5507-5513), которая описана в качестве патологической модели воспалительного заболевания кишечника (IBD), для исследования эффекта BM-095, нейтрализующего антитела против NR10 мыши. Водный раствор 5% (масс./об.) соли декстрана сульфата натрия (Wako Pure Chemical Industries) приготавливали с использованием дистиллированной воды, стерилизованной фильтрацией через 0,22-мкм фильтр (Millipore). Самцам мышей Balb/cAnN Crj в возрасте шести недель (Charles River Laboratories Japan) позволяли свободно употреблять раствор из бутылок с водой в течение семи суток. Измеряли массу тела и процентное изменение массы тела относительно массы тела на первые сутки введения DSS использовали для оценки эффективности лекарственного средства.
Для тестирования улучшения патологического состояния в этой модели при нейтрализации передачи сигнала IL-31 нейтрализующее антитело против NR10 мыши BM095 вводили внутривенно в дозе 10 мг/кг за сутки до введения DSS, и оценивали снижение массы тела (n=10). В контрольной группе носителя внутривенно вводили носитель (смесь ацетатного буфера (20 ммоль/л ацетата натрия, 20 ммоль/л хлорида натрия) и фосфатно-солевого буфера (PBS; GIBCO) в объемном отношении 1:5) за сутки до введения DSS (группа носителя; n=10). Более того, также проводили мониторинг процентных изменений массы тела у мыши Balb/cAnN Crj того же возраста и пола, что и мыши в группе введения DSS (n=1) для оценки процентных изменений массы тела у нормальной мыши.
Изменения массы тела с течением времени представлены на фиг. 3. Введение DSS приводило к снижению процентной массы тела в группе носителя. С другой стороны, группа введения BM095 показала сходные с группой носителя изменения массы тела; однако после четырех и пяти суток введения DSS наблюдали значимое снижение процентной массы тела в группе BM095 по сравнению с группой носителя. Из этих результатов введение BM095 не имело терапевтического эффекта на колит в этой модели.
Хотя было описано, что экспрессия IL-31RA повышена в этой модели (WO 2004/003140), описанные выше экспериментальные результаты показали, что нейтрализующие антитела против этой молекулы не имеют терапевтического эффекта на колит в этой модели.
Справочный пример 5
Эффективность BM095 в модели индуцированного пикрилхлоридом контактного дерматита
Дерматит вследствие реакции гиперчувствительности замедленного типа, сенсибилизированной/индуцированной нанесением пикрилхлорида, которое описано в качестве модели острого контактного дерматита (Clin Immunol 2003; 108: 257-262), вызывали для оценки эффекта BM-095, нейтрализующего антитела против NR10 мыши. Самок мышей Balb/cAnN Crj в возрасте восьми недель (Charles River Laboratories Japan) сенсибилизировали нанесением 50 мкл 7% раствора (этанол:ацетон = 3:1, об./об.) пикрилхлорида (nacalai tesque, Inc.) на кожу живота. Через пять суток вызывали контактный дерматит нанесением 20 мкл 1% раствора (ацетон: оливковое масло = 1:4, об./об.) пикрилхлорида на кожу правого уха (индукция). Для контроля в целях оценки влияния растворителя на толщину уха, на кожу левого уха той же мыши наносили 20 мкл растворителя (ацетон:оливковое масло = 1:4, об./об.) (положительный контроль; n=6). Толщину правого и левого ушей измеряли с помощью толщиномера с циферблатным индикатором (OZAKI MFG. CO., LTD.) непосредственно перед индукцией и через 24, 48 и 72 часов после индукции. Изменение толщины уха относительно толщины непосредственно перед индукцией использовали для оценки эффективности лекарственного средства.
Для оценки установления патологического состояния группу, в которой смешанный раствор этанола-ацетона (3:1, об./об.) без пикрилхлорида наносили на кожу живота во время сенсибилизации, и через пять суток наносили 20 мкл 1% раствора пикрилхлорида на кожу правого уха и 20 мкл растворителя (ацетон:оливковое масло = 1:4, об./об.) на кожу левого уха, исследовали в качестве контрольной группы (группа отрицательного контроля; n=6).
Для оценки эффекта введения антитела против NR10 на патологическое состояние в этой модели исследовали группу, в которой острый контактный дерматит вызывали способом, использованным ранее для группы положительного контроля, и внутривенно вводили 10 мг/кг BM095 за сутки до сенсибилизации и за сутки до индукции (группа BM095, n=6), и группу, в которой вводили носитель (смесь ацетатного буфера (20 ммоль/л ацетата натрия, 20 ммоль/л хлорида натрия) и фосфатно-солевого буфера (PBS; GIBCO) в объемном отношении 1:5) по той же схеме (группа носителя, n=5).
Изменения толщины уха с течением времени вплоть до 72 часов после индукции представлены на фиг. 4. Уши были значительно утолщенными в группе положительного контроля во все моменты времени, составляющие 24, 48 и 72 часов после индукции, по сравнению с группой отрицательного контроля, что показывает на установление патологического состояния. В то же время группа BM-095 показала изменения толщины уха с течением времени, сходные с группой носителя, и, таким образом, не наблюдали значительной супрессии.
Эти результаты показали, что введение BM095 не оказывает терапевтического эффекта против острого контактного дерматита, наблюдаемого в этой модели.
Промышленная применимость
Антагонисты NR10, такие как нейтрализующие антитела против NR10 по настоящему изобретению, пригодны в качестве терапевтических или профилактических средств против зуда.