Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ ТОНКОСЛОЙНЫХ ХИРАЛЬНЫХ ПЛАСТИН ДЛЯ ПЛАНАРНОЙ ХРОМАТОГРАФИИ СТЕРЕОИЗОМЕРОВ И ИХ РАЦЕМИЧЕСКИХ СМЕСЕЙ
Вид РИД
Изобретение
Предложение относится к области аналитической химии, а именно к способу получения тонкослойных пластинок для планарной хроматографии (ТСХ, ПТСХ), и может быть использовано для хирального распознавания стереоизомеров и рацемических смесей природных и синтетических органических соединений в аналитической химии, фармацевтике, медицине, экологии, биохимии и других областях.
Важнейшей характеристикой хиральных сорбентов является хиральный селектор, закрепленный на поверхности сорбента. Известны способы прививки селектора методами иммобилизации (химического - ковалентного связывания) [J. Chromatogr. А. 2002. V. 897. Р. 113-129] или импрегнации (физического - нековалентного связывания) [J. Planar Chromatogr. 2004. V. 17. P. 173-176]. Энантиоселективность хирального селектора заключается в его способности образовывать комплексы с рацематом двух диастереомерных пар, отличающихся друг от друга термодинамической стабильностью [J.Chromatogr., А., 2001, V. 906. рр.3-33].
Известно, что не существует универсальных хиральных фаз для анализа и разделения всего многообразия оптических мономеров [J.Org.Chem., 1981, V. 46, №16, pp.125-134].
В настоящее время известны способы получения хроматографических хиральных фаз (сорбентов) для высокоэффективной жидкостной хроматографии (ВЭЖХ) [SU 1429016, 1998; US 4919803, 1990; US 5439979, 1995; US 62656115, 2001], капиллярного электрофореза [RU 2348455, 2006], тонкослойной хроматографии [US 54399792, 1995].
Известны способы импрегнирования планарных слоев с использованием в качестве хиральных селекторов (+)-винной и (+)-аскорбиновой кислот [J. Pharm. Biomed. Anal., 2000. V. 21, P. 1143-1147]; L-лизина, L-аргинина, эритромицина [Biomed. Chromatogr. 2001. 15, P. 155-165].
Известны промышленно выпускаемые хиральные тонкослойные пластинки Machery-Nagel (Durёn, Germany), состоящие из гидрофобного силикагеля (RP -18), с поливиниловым спиртом в качестве связующего, импрегнированного (2S, 4R, 2'К.8)-N-(2эгидрокси-додецил)-4-гидроксипролином и ионами двухвалентной меди - пластинки Chiraplate [J. Chrom., 1988, V.448, pp.11-30].
Известны способы получения хиральных ТСХ-пластин (Merck, Германия), импрегнированных L-серином [J. Pharm. Biomed. Anal. 2000. V. 21, P. 1143-1147]; L-аргинином (Sigma, США) [J. Chromatorg. A. 1996. V. 721. P. 369-372].
В настоящее время известен новый класс энантиоселективных селекторов - макроциклических гликопептидных антибиотиков (тиострептон, рифамицин Б, ванкомицин) [Anal.Chem, 1994, V.66, pp.1473-1484].
Известны способы получения хроматографических фаз с хиральными агентами нового типа с импрегнированным макроциклическим антибиотиком эритромицином для разделения энантиомеров аминокислот, ванкомицина и верапамила [J. Chromatography А. 1996. V. 736. Р. 235-238]. Описан способ получения сорбента для разделения оптических изомеров методом ВЭЖХ с иммобилизированным гликопептидным антибиотиком эремомицином [RU 2255802, 2005].
Недостатком указанных аналогов является то обстоятельство, что известные хроматографические фазы для колоночной ВЭЖХ, капиллярного электрофореза и планарной хроматографии, полученные разными способами химической (иммобилизация) и физической (импрегнирование) модификации поверхности кремнеземных матриц известными хиральными агентами, обладают избирательной энантиоселективностью, кроме того, процесс их получения многостадиен и сложен. Существенный недостаток указанных аналогов проявляется и при попытке использования их в качестве адсорбентов для ТСХ-пластин в планарной хроматографии и связан он с тем, что не учитывается влияние полимерного или неорганического связующего в кремнеземной матрице на качество хиральных ТСХ-пластин.
Наиболее близким по технической сущности и достигаемому результату является способ получения [RU 2012143015, 2012] хиральных планарных пластинок для тонкослойной хроматографии оптических изомеров с химически привитым (иммобилизированным) гликопептидным антибиотиком эремомицином, произведенным по известному протоколу [RU 2255802, 2005]. Способ получения известной силикагелевой хиральной фазы для ТСХ заключается в ковалентном связывании (иммобилизации) эремомицина на поверхности кремнеземной матрицы с силиказолевым связующим. Способ иммобилизации заключается в том, что вначале кремнезем с неорганическим связующим в водном буферном растворе обрабатывают γ-глицидоксипропилтриметоксисиланом, а затем в щелочном растворе к кремнезему и неорганическому связующему (золь кремниевой кислоты), модифицированным эпоксигруппами на первой стадии процесса, прививается гликопептидный антибиотик эремомицин.
Существенным недостатком известного способа-прототипа является сложный многостадийный процесс химического (ковалентного) связывания хирального селектора методом поверхностной сборки, занимающий значительное (до 14 дней) время до получения конечного продукта и заключающийся в обработке кремнеземной матрицы кислотой для гидроксилирования ее поверхности с последующей промывкой последовательно водой и спиртом; обработке органосиланами (γ-глицидоксипропилтриалкоксисиланом) в течение 7 суток с образованием спейсера, содержащего глицидоксипропильную группу на поверхности силикагеля; ковалентной (способом иммобилизации) прививкой гликопептидного антибиотика эремомицина в щелочном водном (рН 8-11) растворе в течение 7 суток.
Технической задачей заявляемого решения является разработка низкотемпературного закрепления хирального агента - гликопептидного антибиотика эремомицина нековалентным связыванием молекул с поверхностью кремнеземного сорбента методом импрегнирования с получением тонкослойных пластинок с силиказолевым связующим для планарной хроматографии стереоизомеров и их рацематов.
Положительным результатом является простая технология нековалентного (физического) связывания хирального селектора эремомицина за счет π-π-взаимодействий и водородных связей с поверхностью кремнеземной матрицы и кремнеземного связующего планарного слоя ТСХ-пластин с получением универсального хирального слоя для разделения стереоизомеров разных классов органических соединений и их рацемических смесей методом высокоэффективной планарной хроматографии.
Технологический результат достигается в разрабатываемом способе за счет того, что такая фаза характеризуется стабильностью в водно-органических растворах и, благодаря наличию большого числа ассиметричных центров и функциональных групп, демонстрирует высокую энантиоселективность по отношению к различным классам хиральных соединений.
Указанная задача и технический результат достигаются за счет того, что способ получения тонкослойных хиральных пластин для планарной хроматографии стереоизомеров и их рацемических смесей методом импрегнирования характеризуется тем, что производят нековалентное связывание с поверхностью адсорбента, закрепленного на ТСХ-пластине связующим, гликопептидного антибиотика эремомицина со следующей структурной формулой
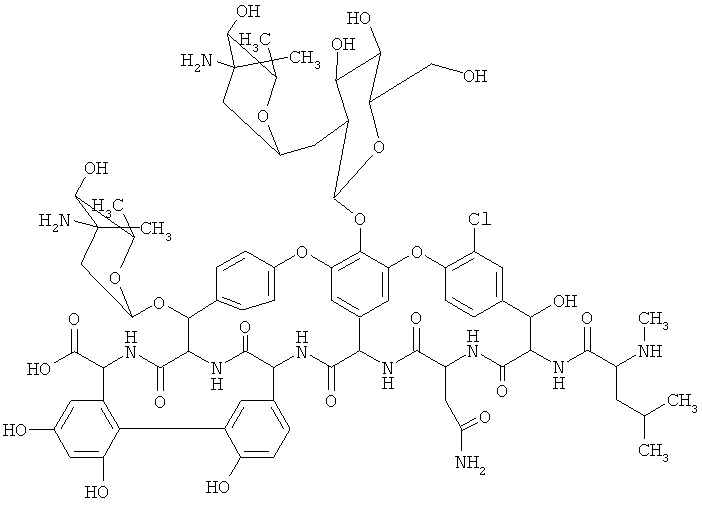 ,
,
при этом в качестве адсорбента используют силикагель с силиказолем, активированный 0,2М Н2SO4 при температуре 25°С в течение 20-60 мин и промытый деминерализованной водой до рН 5-7, а нековалентное связывание гликопептидного антибиотика эремомицина с поверхностью адсорбента производят методом импрегнирования в щелочном водном растворе при рН 8,0-12,0.
Способ характеризуется также тем, что процесс проводят при температуре не выше 25°С в одну стадию в течение 10 мин - 1 суток.
Сущность данного способа получения хиральных планарных пластин заключается в том, что закрепление хирального агента гликопептидного антибиотика эремомицина на поверхности кремнезема осуществляется методом импрегнирования (физического закрепления) в водных щелочных растворах (с рН 8-10) при комнатной температуре (20-25°С) с перемешиванием (60-120 об/мин) раствора в течение 1-24 часов.
Излагаемая сущность данного способа раскрывается далее на примерах его экспериментального осуществления.
Пример 1. Силикагелевые планарные пластинки с силиказолевым связующим активировали 0,2М серной кислотой при 25°С в течение 40 мин для достижения максимальной степени гидроксилирования поверхности (αон=4,6÷4,9 ОН - групп/нм2) и промывали деминерализованной водой до рН=5÷7.
Эремомицин с концентрацией 1 мг/мл растворяли в деминерализованной воде при температуре 25°С доводили до рН 8,56 1М раствором гидроксида натрия. В полученный раствор при перемешивании (60 об/мин) погружали ТСХ-пластинки на 10 мин при температуре 25°С. Затем ТСХ-пластины высушивали на воздухе при температуре 20-25°С в течение 24 часов.
Данные по элементному анализу кремнеземного слоя с хиральным селектором приведены в табл.1. Данные хроматографического разделения рацемических смесей стандартных L- и D-аминокислот приведены в табл.2.
Пример 2. Способ по примеру 1, время импрегнирования 30 мин. Данные по элементному анализу кремнеземного слоя ТСХ-пластин приведены в табл.1. Результаты разделения рацемической смеси аминокислот показаны в табл.2.
Пример 3. Способ по примеру 1, время импрегнирования 60 мин. Данные по элементному анализу кремнеземного слоя ТСХ-пластин приведены в табл.1. Результаты разделения рацемической смеси аминокислот показаны в табл.2.
Пример 4. Способ по примеру 1, время импрегнирования 1 сутки. Данные по элементному анализу кремнеземного слоя ТСХ-пластин приведены в табл.1. Результаты разделения рацемической смеси аминокислот показаны в табл.2.
Пример 5. Способ по примеру 1, время импрегнирования 2 суток. Данные по элементному анализу кремнеземного слоя ТСХ-пластин приведены в табл.1. Результаты разделения рацемической смеси аминокислот показаны в табл.2.
Получившиеся данные для пластин, импрегнированных в течение суток (пример 4), практически не отличаются от данных по прививке селектора в течение 2 суток (пример 5) и сопоставимы с результатами, полученными при иммобилизации пластин в течение 14 дней, что подтверждается высокой энантиоселективностью эремомицина по отношению к реперным стереоизомерам аминокислот в обоих случаях. Сравнительные характеристики разделения энантиомеров аминокислот на иммобилизованных и импрегнированных эремомицином пластинах приведены в табл.3.
Лучшие результаты по разделению рацемических смесей аминокислот достигнуты для пластин с временем импрегнирования 1 сутки (Rs 5,48 для фенилаланина и 6,03 для триптофана); энантиомеры аминокислот на пластинах, импрегнированных эремомицином в течение 10 и 30 мин, практически не разделяются (табл.2).
|
|
|
Приведенные данные свидетельствуют о соответствии предлагаемого технического решения всем требуемым критериям, защищаемым патентом.
Таким образом, регистрируемый способ позволяет существенно упростить процедуру введения гликопептидного антибиотика эремомицина в качестве хирального агента в кремнеземный слой тонкослойных пластин за счет использования метода низкотемпературного импрегнирования - физического, нековалентного связывания хирального селектора с сорбентом.
Совокупность существенных признаков данного способа показывает оригинальность, новизну, применимость тонкослойных хиральных пластин для планарной хроматографии стереоизомеров и их рацемических смесей.