Результат интеллектуальной деятельности: ВАКЦИНА ДЛЯ ПРОФИЛАКТИКИ И ЛЕЧЕНИЯ РОТАВИРУСНОЙ ИНФЕКЦИИ, СОДЕРЖАЩАЯ ГИБРИДНЫЙ БЕЛОК В КАЧЕСТВЕ АКТИВНОГО АГЕНТА (ВАРИАНТЫ)
Вид РИД
Изобретение
Группа изобретений относится к молекулярной биологии, биотехнологии, медицине и может быть использована в качестве средств для профилактики и лечения ротавирусной инфекции, вызываемой различными штаммами ротавирусов.
Термин "гибридный (химерный) белок" в данном тексте обозначает белок, полученный в результате экспрессии рекомбинантной молекулы ДНК, в которой соединены друг с другом в одной рамке считывания кодирующие участки нескольких разных генов.
По данным Всемирной организации здравоохранения, ротавирус (род Rotavirus, семейство Rotaviridiae) является одной из ведущих причин возникновения тяжелой диареи, приводящей к дегидратации организма у детей младшего возраста. Большинство детей инфицируется до достижения 5-летнего возраста. Большинство случаев острых ротавирусных гастроэнтеритов наблюдается в странах с низкими доходами населения, при этом поражаются дети в возрасте до 1 года. В большинстве стран с низкими доходами населения в Азии и Африке эпидемиология ротавирусной инфекции характеризуется эпизодами относительно интенсивной циркуляции вируса по сравнению с фоновой передачей на протяжении года. Однако в странах умеренного климата с высокими доходами типичной является четкая зимняя сезонность [1].
Ротавирус повреждает энтероциты, расположенные на микроворсинках тонкого кишечника, что приводит к снижению абсорбции и диарее. Широкий спектр клинических проявлений колеблется от преходящей легкой диареи до тяжелой диареи и рвоты, вызывающих дегидратацию, нарушение электролитного баланса, шок и при отсутствии лечения смерть.
Иммунитет к ротавирусной инфекции в большинстве случаев возникает в раннем детстве после перенесенного заболевания. Иммунитет нестойкий, поэтому у взрослых с низким уровнем антител заболевание может повториться. Невосприимчивость у переболевших обусловлена не только гуморальными, но и секреторными антителами.
Зарегистрированные вакцины для профилактики ротавирусной инфекции содержат живые аттенуированные штаммы ротавируса человека и/или животного, которые размножаются в кишечнике человека. На международном рынке имеются две ротавирусные вакцины: моновалентная (RV1) и пентовалентная (RV5). Вакцина RV1 получена на основе человеческого штамма, тогда как вакцина RV5 содержит 5 рекомбинантных вирусов, полученных на основе человеческого и бычьего штаммов ротавируса.
Использование вакцин на основе рекомбинантных белков позволяет избежать рисков, связанных с введением вируса в организм, пусть и аттенуированного. Так, выбранные участки белков не несут функций природных белков ротавирусов (например, гемагглютинирующая активность) и, соответственно, не вызывают побочных эффектов, характерных для вакцин, полученных с использованием ротавирусов. Вакцинные препараты, получаемые с помощью технологии рекомбинантной ДНК, обладают большей фармацевтической чистотой (не содержат аллергенов в виде яичных белков), чем вирионы, выращенные в куриных эмбрионах, и не содержат консервантов (формальдегид, мертиолят). Технология получения рекомбинантных белков с использованием клеток бактерий позволяет получить в течение 2-3 дней в ферментерах небольшого объема, занимающих меньшую площадь и требующих меньших технических ресурсов по сравнению с культивированием живого вируса, аналогичное или большее количество вакцинных доз (10-литровый ферментер обеспечивает в среднем 1000000 доз).
Белок наружного капсида VP4 ответственен за адаптацию ротавирусов к росту in vitro, контролирует их вирулентность на уровне организма, является вирусным гемагглютинином и, по-видимому, обеспечивает проникновение вируса в клетку. В экспериментах с нейтрализующими моноклональными антителами к VP4 показано, что они сообщают организму протективный иммунитет против гомологичного и некоторых гетерологичных серотипов ротавируса.
Белок VP8 является N-концевым триптическим фрагментом белка VP4. Данный белок (VP8) является высокоиммуногенным полипептидом и индуцирует эффективную гомотипическую защиту против заболевания, причем эффект наблюдали у детенышей, привитых данным полипептидом самок. Белок VP8 содержит пять нейтрализующих эпитопов.
Использование эпитопов белка VP8 для создания вакцины от ротавирусной инфекции позволит обеспечить протективный иммунитет против гомологичного и некоторых гетерологичных серотипов ротавируса.
Полипептид внутреннего капсида VP6 (42 кД) является мажорным белком вириона. Введение данного белка индуцирует выработку нейтрализирующих секреторных антител (IgA). Такие антитела содержатся в большом количестве в молоке кормящей самки, что обеспечивает защиту новорожденных животных [2].
Таким образом, защиту ребенка от заболевания ротавирусной инфекцией возможно обеспечить вакцинацией матери белками VP6, VP8. Антитела IgA секретируются также на эпителиях, что обеспечивает защиту взрослого от инфекции. Удобнее вакцинировать единой конструкцией, содержащей последовательности VP6, VP8. Продукция химерного белка, содержащего не полноразмерные белки, а их иммуногенные эпитопы, более выгодна.
Известен химерный белок, содержащий субъединичный белок ротавируса или его иммуногенную часть, а также другой белок, адъювант используется в совокупности с химерным белком [3]. Другой белок не влияет на экспрессию и иммуногенность белка ротавируса, предотвращает формирование комплексов ротавирусным субъединичным белком и обеспечивает его очистку. Ротавирусный субъединичный белок выбирают из VP1, VP2, VP3, VP4, VP6, VP7, NSP1, NSP2, NSP3, NSP4 или NSP5.
Известно изобретение, по которому в трансформанте экспрессируется эпитоп белка вируса, вызывающего эпизоотическую диарею свиней (PEDV), и белок ротавируса (VP8 или BVP5) [4]. Данные полипептиды функционально связаны в единой векторной конструкции. Заявлена также вакцинная композиция, которая может содержать получаемый в трансформанте рекомбинантный белок. Назначение вакцины - индуцировать формирование нейтрализующих указанные вирусы антител и уменьшать степень заражения ими животных. Создается рекомбинантный вектор, вектор вводят в Agrobacterium с последующей трансформацией клеток растений данными бактериями.
Известна векторная конструкция для экспрессии целевого гена в растениях, целевым геном заявлен ген из группы GFP, ротавирусных белков VP6, VP2, VP4 и VP7 [5]. Предусмотрена трансформация клеток растений бактериями, содержащими описанную векторную конструкцию.
Перспективнее использовать несколько генов, кодирующих иммуногенные эпитопы белков ротавируса в одной конструкции и, соответственно, один гибридный белок, обеспечивающий более широкий спектр активностей, соответственно, обеспечивающий большую степень защиты от патогена.
Известен рекомбинантный белок-носитель (VP6), в последовательность которого введены эпитопы других белков других вирусов с сохранением эпитопов VP6 на поверхности белка [6].
К недостаткам аналогов можно отнести ограниченность их действия за счет использования в качестве компонента гибридного белка только одного белка ротавируса. Также недостатком аналогов является сложность получения активного белка ввиду сложности его правильной пространственной укладки из-за использования полноразмерного белка ротавируса в качестве компонента гибридного белка.
Прототипом изобретения (гибридный белок SEQ ID NO:1, SEQ ID NO:2) является рекомбинантный химерный белок, несущий эпитопы белков VP4 ротавирусов Р[4]223, Р[4]56 и VP7 ротавируса G1[142], G4[208], P[8]296 и G2[87] [7].
К недостаткам прототипа можно отнести ограниченность иммунного ответа на ротавирусную инфекцию: лишь по одному механизму - синтез нейтрализующих антител, предотвращающих попадание вируса в энтероцит. Такой механизм обеспечивает только профилактический эффект вакцины.
Известен рекомбинантный ген, содержащий нукледотидную последовательность, кодирующую первый эпитопН1-d структурного гена флагеллина Salmonella и хотя бы один эпитоп гетерологичного организма, включенного в последовательность флагеллина таким образом, что флагеллин способен связываться с антителом к флагеллину, причем хотя бы один эпитоп гетерологичного организма помещен вместо ДНК, находящейся между естественными EcoRV сайтами гена H1-d Salmonella [8]. В данном изобретении в составе химерного белка заявлен лишь первый эпитоп гена H1(FliC1) Salmonella, а также в примерах указан белок VP7 в качестве второго возможного элемента конструкции. Использование обоих эпитопов - FliC1, FliC2 - в единой конструкции позволит получить более сильный иммунный ответ на вводимый иммуноген, использование исключительно эпитопов гена H1, связанных гибкими мостиками, а также использование нескольких иммуногенных эпитопов белков, индуцирующих формирование иммунного ответа по разным механизмам, VP6 и VP8, позволит обеспечить комплексную защиту от вируса.
Известны рекомбинантные химерные белки, среди которых заявлены белки, включающие фрагменты VP4, VP7, FIjb: VP4 l-336::VP7::FIjb [9]. Данное изобретение является наиболее близким к предлагаемому (SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6) - прототипом. К недостаткам данной конструкции можно отнести сложность получения активного, растворимого белка за счет возникновения сложностей, связанных с приобретением неправильной третичной структуры гибридным белком значительного размера.
Заявленная группа изобретений относится к объектам одного вида одинакового назначения, обеспечивающим получение одного и того же технического результата (варианты).
Технический результат от использования группы изобретений состоит в упрощении получения активного растворимого гибридного белка за счет уменьшения размера белка благодаря использованию лишь фрагментов белков - иммуногенных эпитопов, связанных гибкими мостиками.
Технический результат от использования группы изобретений также состоит в расширении спектра активностей гибридного белка на основе белков ротавируса - в обеспечении наряду с профилактическим терапевтического действия. Нейтрализующие IgA антитела, связываясь с белком клеточной оболочки вируса (VP8), останавливают проникновение вируса в энтероциты и индуцируют его выведение из клеток, а при связывании белка внутреннего капсида VP6 IgA-антителами непосредственно в энтероците останавливается внутриклеточное размножение вируса. Ввиду этого целесообразно использовать в качестве иммуногена, помимо фрагмента белка VP4, также белок именно внутреннего капсида (VP6), поскольку именно он остается на поверхности вирусной частицы после попадания в энтероцит.
Введение в конструкцию гибридного белка эпитопов белка VP6 ротавируса позволит остановить репликацию вируса внутри энтероцитов за счет выработки антител к данному белку, что окажет терапевтический эффект.
Технический результат от использования группы изобретений главным образом состоит увеличении валентности вакцины против ротавируса: после прививания вакцинами, заявленными в изобретении, у человека вырабатывается иммунитет к ротавирусам групп A-С. После вакцинации в организме вырабатываются антитела на эпитопы белков VP6, VP8 разных ротавирусов. Формируется способность вырабатывать антитела в ответ на попадание в организм ротавируса. В дальнейшем при попадании в организм ротавируса A, В или С иммунный ответ будет быстро вырабатываться, что выразится в том, что удастся избежать заражения либо заболевание пройдет в легкой форме. Такой подход к вакцинации позволит элиминировать данное заболевание.
Технический результат от использования вакцины, содержащей гибридный белок, в состав которого дополнительно введены фрагменты флагеллина (SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6), заключается в увеличении ее иммуногенности и более быстром ответе на терапию и вакцинацию гибридным белком.
Технический результат от использования в качестве адъюванта эпитопов FliC1, FliC2 флагеллина, нетоксичного агента, в приведенной конструкции белка состоит в усилении иммунного ответа и более быстром ответе на терапию и вакцинацию гибридным белком. На данный момент флагеллин является одним из наиболее перспективных и хорошо изученных адъювантов нового поколения. Результаты исследований показывают, что рекомбинантные белки, вводимые с флагеллином, имеют повышенные иммуногенные и антигенные характеристики. Ответы на них регистрируются в более короткие сроки и вызывают более сильный клеточный и гуморальный иммунный ответ [10].
Технический результат от производства лишь одного компонента - гибридного белка - взамен производства множества отдельных компонентов вакцинной смеси (аналоги) выражается в удешевлении и сокращении сроков производства вакцины.
Сущность изобретения
Предложена группа изобретений, представляющая собой вакцины на основе высокоочищенных гибридных белков (SEQ ID NO:1, SEQ ID NO:2), включающих иммуногенные эпитопы белка VP6, иммуногенный эпитоп белка VP8 ротавируса А, фрагмент белка VP6 имеет общие и гомологичные участки с фрагментом белка VP6 ротавируса С, а также гомологичные участки с фрагментом белка VP6 ротавируса В, компоненты соединены гибкими мостиками. К группе изобретений также относятся вакцины, активный компонент которых (описанные гибридные белки) дополнительно содержит компоненты флагеллина FliC1 и FliC2 в качестве адъюванта (SEQ ID NO:3, SEQ ID NO:4, SEQ ID NO:5, SEQ ID NO:6), компоненты соединены гибкими мостиками. Представленный фрагмент белка VP6 является консенсусной последовательностью, к которой в процессе естественной инфекции образуются специфические антитела, перекрестно реагирующие с гомологичными эпитопами среди различных штаммов ротавируса групп А, В и С. Данный фрагмент содержит два иммуногенных эпитопа. Использование эпитопов нескольких белков позволяет увеличить эффективность вакцины. Используемый фрагмент белка VP8 содержит один высокоиммуногенный эпитоп. Использование гибких мостиков между эпитопами позволяет сохранить правильную пространственную укладку белка и, соответственно, обеспечивает полноценное функционирование каждого эпитопа.
Вакцины получены способом, включающим создание оптимизированной по кодонному составу для экспрессии в прокариотических либо эукариотических клетках рекомбинантной ДНК, кодирующей гибридный белок (SEQ ID NO.:1, SEQ ID NO.:2, SEQ ID NO.:3, SEQ ID NO.:4, SEQ ID NO.:5, SEQ ID NO.:6), введение такой ДНК в векторную конструкцию, обеспечивающую высокий уровень ее экспрессии в клетках прокариот либо эукариот, введение данной векторной конструкции в клетки прокариот либо эукариот, продукцию гибридного белка в указанном организме, его выделение, очистку и смешивание с физиологически приемлемым носителем.
На основании выбранных аминокислотных последовательностей были рассчитаны нуклеотидные последовательности соответствующих генов с учетом частоты встречаемости кодонов в белоккодирующих генах используемых прокариот либо эукариот, при этом кодоны выбирались с учетом уменьшения dG соответствующих мРНК.
Для получения в соответствии с настоящей группой изобретений гибридных белков могут быть использованы стандартные методы молекулярной биологии и микробиологии, известные специалистам в данной области техники. Такие методы полно представлены в научной литературе.
Краткое описание чертежей
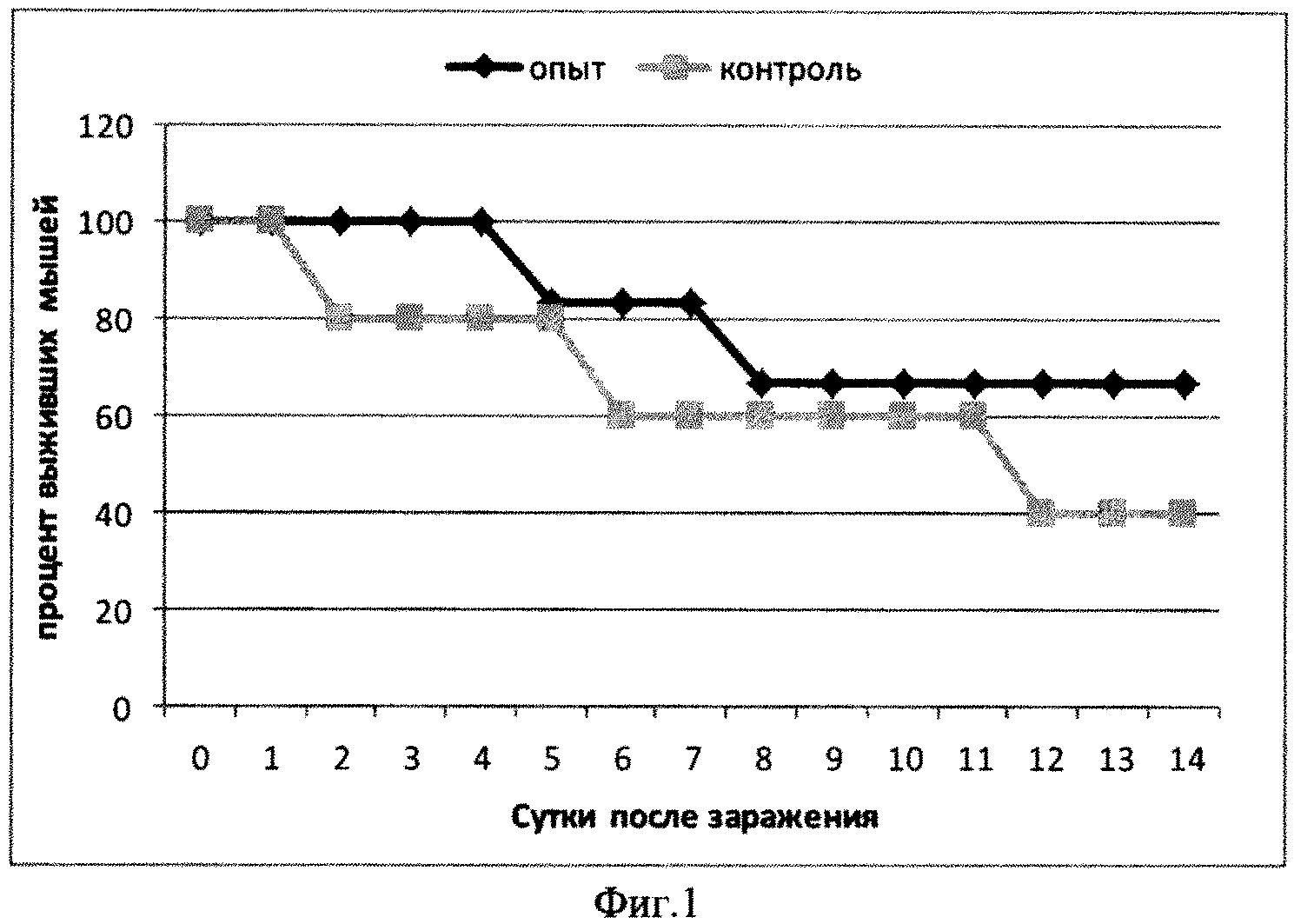
Фиг.1. Динамика гибели мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:6), интраназальное введение, после заражения 10LD/50 ротавируса антигенной группы А.
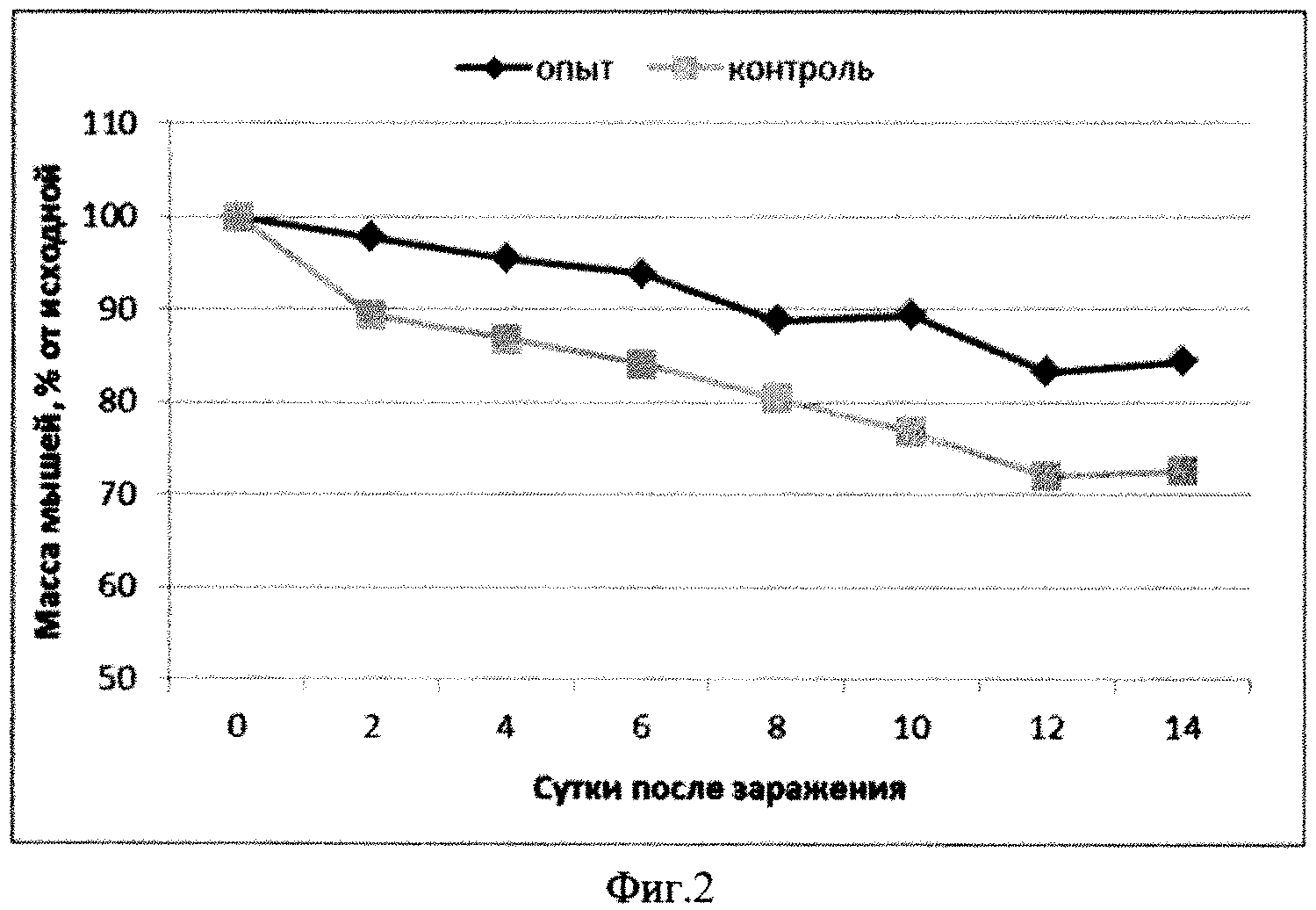
Фиг.2. Динамика массы тела выживших мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:6), интраназальное введение, после заражения 10LD/50 ротавируса антигенной группы А.
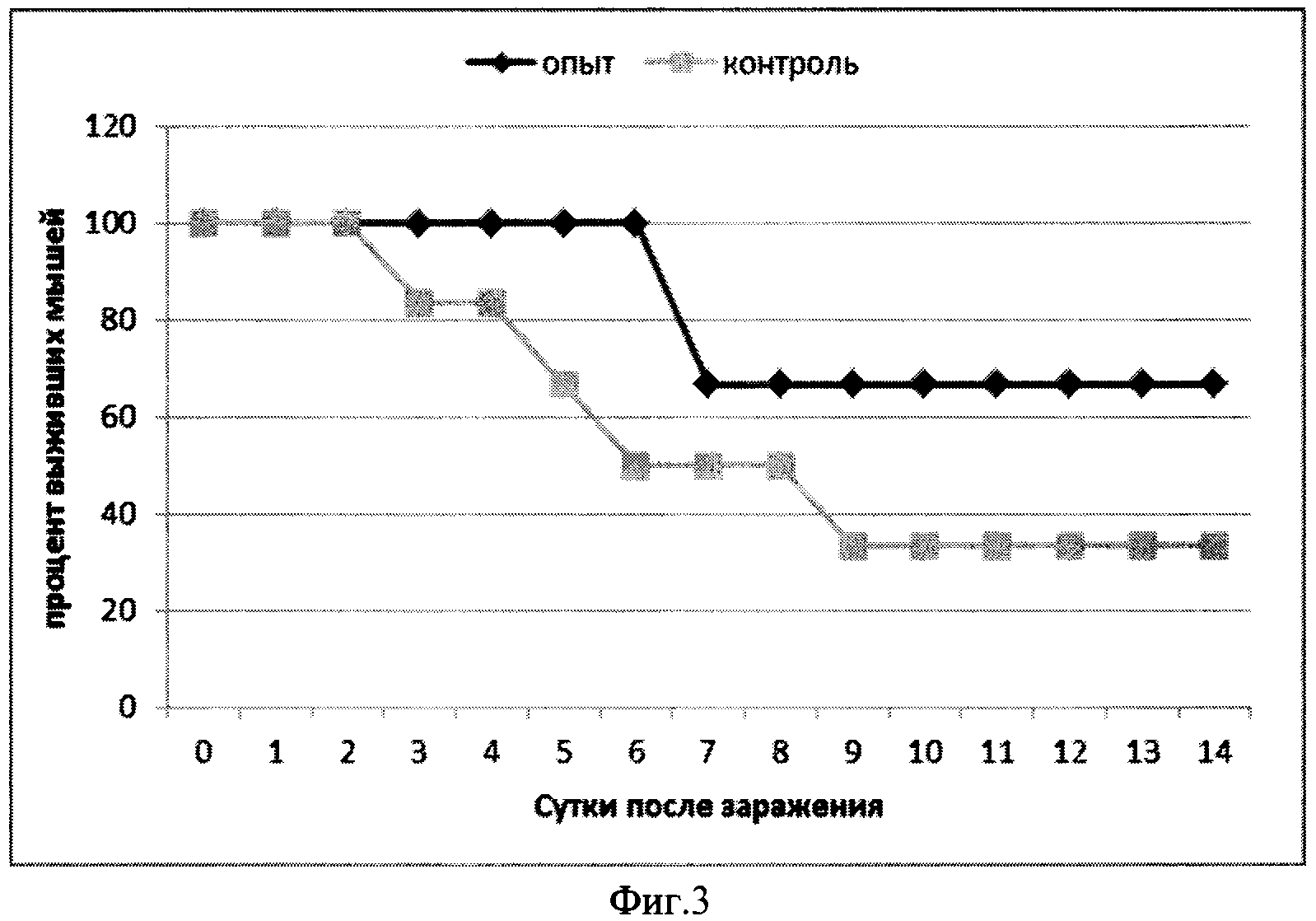
Фиг.3. Динамика гибели мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:5), внутримышечное введение, после заражения 10LD/50 ротавируса антигенной группы В.
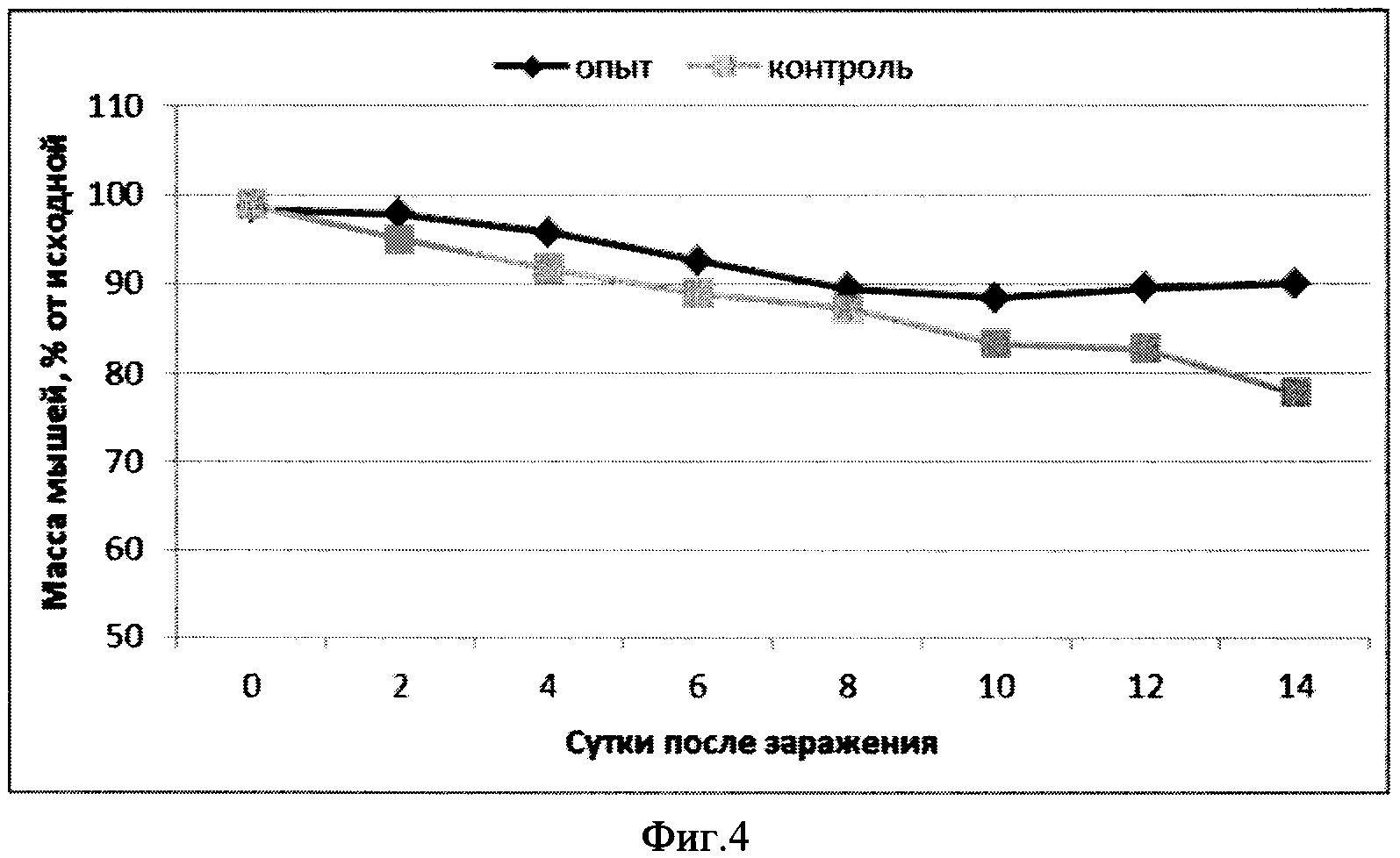
Фиг.4. Динамика массы тела выживших мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:5), внутримышечное введение, после заражения 10LD/50 ротавируса антигенной группы В.
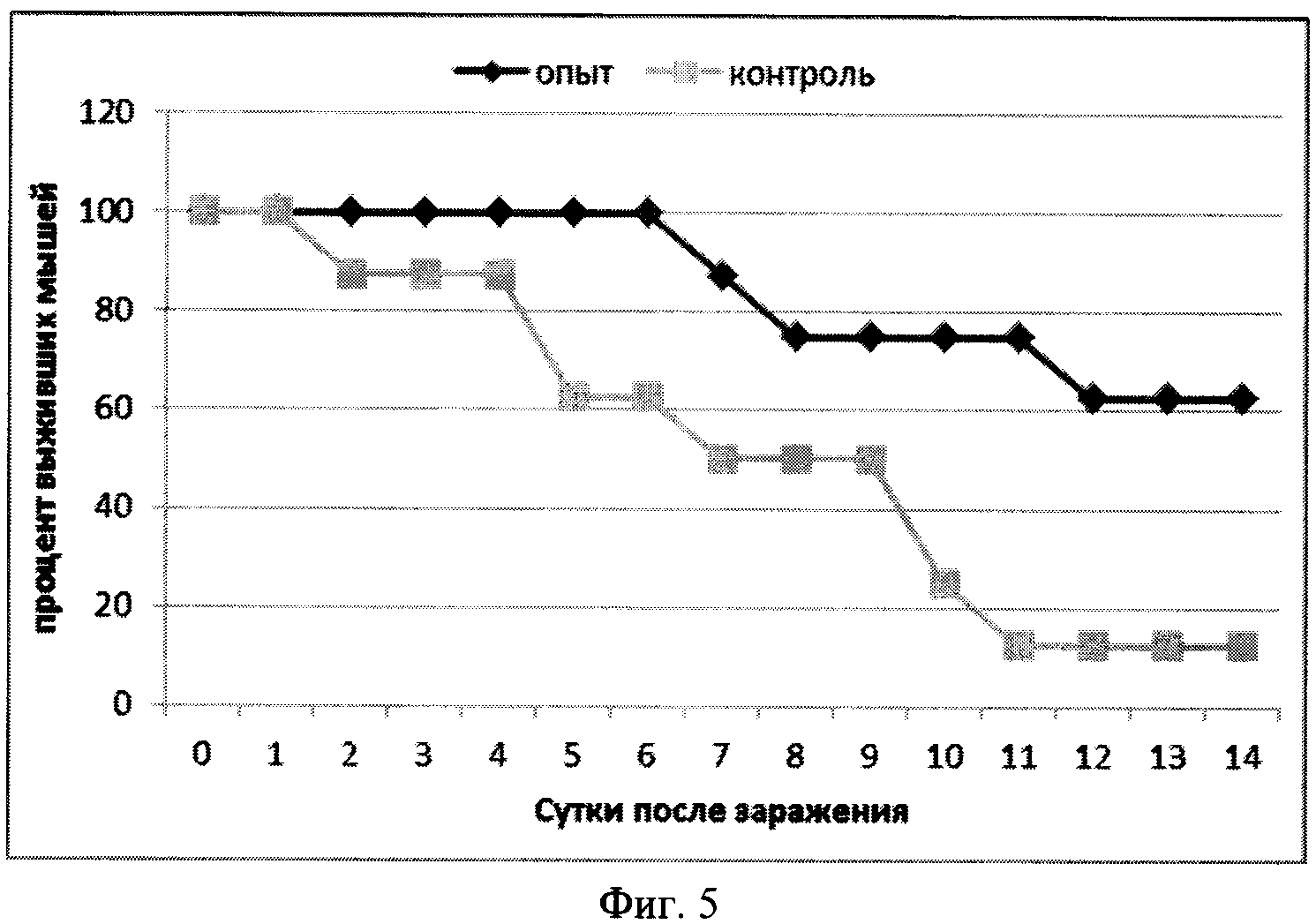
Фиг. 5. Динамика гибели мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:2), внутримышечное введение, после заражения 10LD/50 ротавируса антигенной группы С.
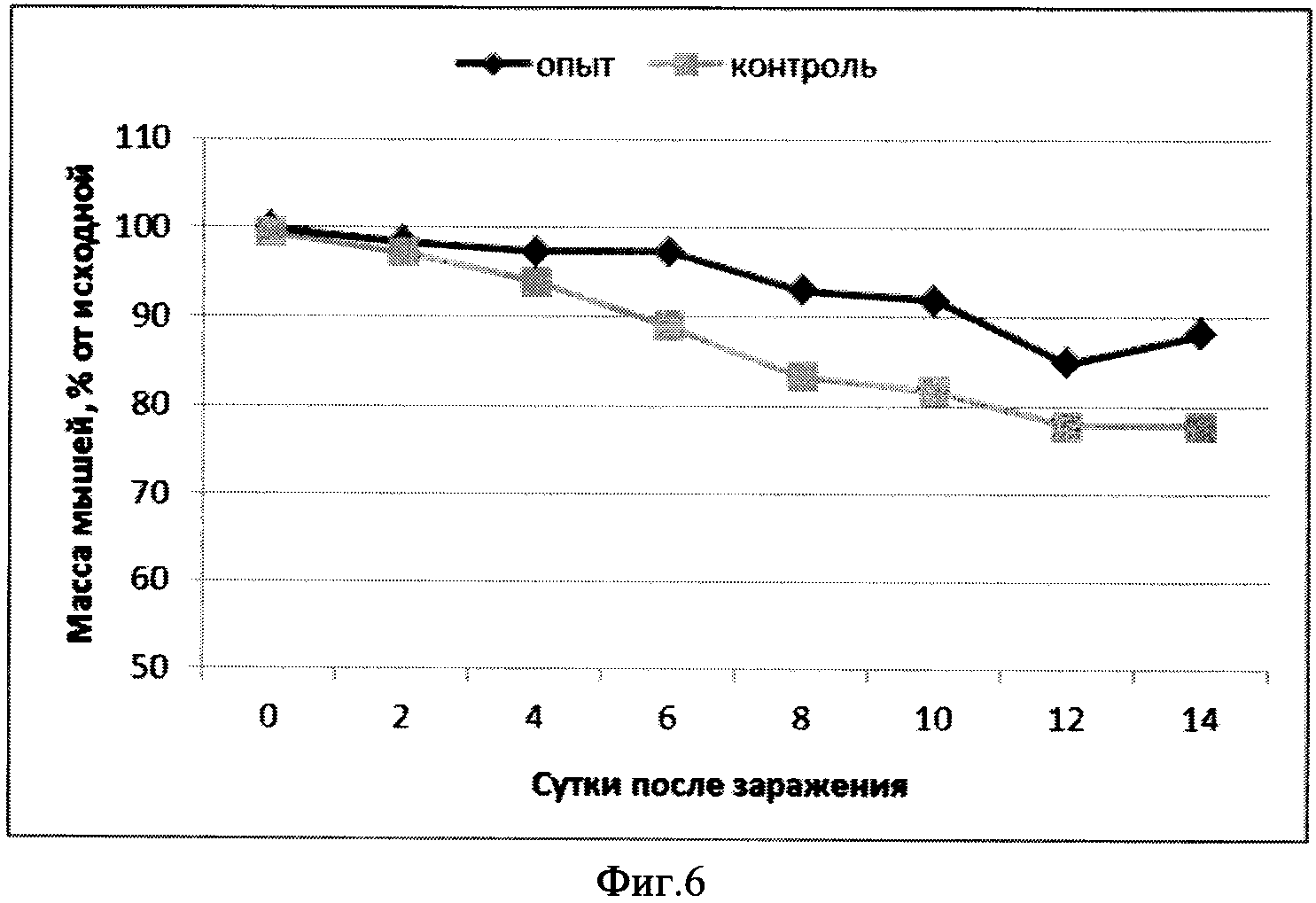
Фиг. 6. Динамика массы тела выживших мышей, иммунизированных кандидатной вакциной (SEQ ID NO.:2), внутримышечное введение, после заражения 10LD/50 ротавируса антигенной группы С.
Табл. 1. Титры сывороточных антител (IgA) после двукратной иммунизации мышей гибридным белком (SEQ ID NO.:1, SEQ ID NO.:3).
Список литературы
1. http://www.who.int/immunization/documents/WHO_PP_Rotavirus_2013_summary_R U.pdf-оттиск 10.03.2013.
2. Gil MT, de Souza CO, Asensi M, Buesa J., Homotypic protection against rotavirus-induced diarrhea in infant mice breast-fed by dams immunized with the recombinant VP8* subunit of the VP4 capsid protein. Viral Immunol. 2000; 13(2): 187-200.
3. US 19980106347 P 19981030.
4. KR 20120066559 (A), 20101214.
5. KR 20060013000, 20040805.
6. CN 102643335 (A), 20120417.
7. CN 102643348 (A), 20120417.
8. US 19920837668 19920214-expired.
9. СА 20102698413 20100406.
10. Balaram P, Kien PK, Ismail A. Toll-like receptors and cytokines in immune responses to persistent mycobacterial and Salmonella infections. Int J Med Microbiol. 2009 Mar; 299(3): 177-85. doi: 10.1016 / j.ijmm. 2008.08.004. Epub 2008 Oct 8. Review.
11. Yamada К., Wang J.C., Osawa H. et al. Efficient large-scale transformation of yeast // Biotechniques .- 1998. - V.24. - P.596-598.
12. Bogush V.G. et al., 2009, J. Neuroimmune Pharmacol., v.4, 17-27.
13. Комарова Т.В., Скулачев М.В., Зверева A.C., Шварц A.M., Дорохов Ю.Л., Атабеков И.Г. (2006). Биохимия, 71, 1043-1049.
Осуществление настоящего изобретения
Пример 1. Получение высокоочищенного гибридного белка (SEQ ID NO.:1) для вакцины против ротавирусной инфекции с использованием клеток бактерий E.coli.
1.1. Моделирование гибридного белка.
Спланированный гибридный полипептид имеет 2 домена: VP6, VP8. Для моделирования белка были произведены следующие действия.
1. Поиск иммуногенных эпитопов белков VP6, VP8 с помощью программы CPREDS (http://ailab.cs.iastate.edu/bcpreds/predict.html).
2. Построение модели целого белка для определения ориентации доменов.
3. Построение моделей для каждого домена (с использованием образцов 3D структур и ab initio).
4. Докинг моделей с использованием модели целого белка.
Для получения наиболее реалистичных результатов в автоматическом режиме использовали алгоритм I-Tasser для моделирования белков.
Смоделированный гибридный белок состоит из 175 а.о., представлена его аминокислотная последовательность - SEQ ID NO:1. Анализ аминокислотной последовательности данного белка с помощью программы ProtParam (http://au.expasy.org/tools/protparam.html) показал, что гибридный белок стабилен и имеет молекулярную массу 19,4 кДа, pI 4,41.
1.2. Создание нуклеотидной последовательности, кодирующей гибридный белок.
Перевели аминокислотную последовательность гибридного белка, включающего домены VP6, VP8, в нуклеотидную (525 п.н.), оптимизировав последнюю для экспрессии в клетках E.coli.
Синтез данной нуклеотидной последовательности осуществляли путем удлинения взаимоперекрывающихся олигонуклеотидов согласно описанным методам (Majumder, 1992). Олигонуклеотиды представляли собой фрагменты гибридного гена длиной около 70 нуклеотидов со взаимоперекрывающимися участками длиной около 20 нуклеотидов. Основные требования к праймерам заключались в том, что их длина не должна была превышать 60 нуклеотидов, а участки гибридизации должны были быть не меньше 20 нуклеотидов. Кроме того, на концах олигонуклеотидов не должно было быть длинных участков с повторяющимися G или С. В ряде случаев подбор оптимальных праймеров осуществляли эмпирически путем сдвига праймера по отношению к матрице или изменения длины праймера на 3-6 нуклеотидов. В общей сложности для синтеза гибридного гена длиной 525 п.н. было использовано 20 праймеров. Синтезированные фрагменты по 300 п.н. выделяли с помощью гель-электрофореза и клонировали в плазмидном векторе pGEM-T Easy. Клонирование осуществляли с использованием рестрикционных сайтов Kpnl, SacII, EcoRV, BamHI или посредством "тупых" концов. После секвенирования фрагменты амплифицировали, после чего соединяли в нуклеотидную последовательность гибридного белка путем их сплавления методом полимеразной цепной реакции (ПЦР). После заключительного этапа синтеза гибридного гена путем лигирования фрагментов искусственный ген клонировали в вектор pGEM-T по рестрикционным сайтам KpnI и SacI. Полученный ген был фланкирован дополнительными рестрикционными сайтами EcoRI на 5'-конце и XhoI на 3'-конце. Далее искусственный ген переклонировали в экспрессионный вектор рЕТ24а по рестрикционным сайтам EcoRI и XhoI.
1.3. Создание плазмидной ДНК, кодирующей гибридный белок. Полученный ген клонировали в плазмиде рЕТ24а для последующей экспрессии.
Для этого проводили реакцию лигирования гена и вектора рЕТ24а с использованием соответствующего буфера и лигазы при +20°С в течение 2 часов.
Смесь прогревали при +95°С в течение 10 мин и очищали от солей диализом на нитроцеллюлозных фильтрах с диаметром пор 0,025 мкм (Millipore, США). Диализ проводили против раствора, содержащего 0,5 мМ ЭДТА в 10% глицерине, в течение 10 мин.
1.4. Создание штамма E.coli для амплификации плазмидной ДНК, содержащей гибридный ген.
Полученной плазмидой трансформировали клетки Е. coli штамма DH10B/R (Gibko BRL, США) с генотипом F-mcrA Δ(mrr-hsdRMS-mcrBC) φ80dlacZΔM 15 ΔlасХ74 deoR recA1 endA1 araD139 Δ(ara, leu)769 galU galKλ,- rpsL nupG методом электропорации.
После трансформации клетки инкубировали в SOC-среде (2% бакто-триптон, 0.5% дрожжевой экстракт, 10 мМ NaCl, 2.5 мМ КСl, 10 мМ MgCl2, 10 мМ MgSO4, 20 мМ глюкоза) в течение 40 мин при +37°С.
С помощью скрининга клеток E.coli на наличие плазмид на селективной среде, содержащей LB-arap, 100 мкг/мл ампициллина, отбирали колонии клеток E.coli - штамм E.coli для амплификации плазмидной ДНК, содержащей гибридный ген.
Из выросших клонов выделяли плазмидную ДНК с использованием набора Wizard Minipreps DNA Purification System (Promega, США).
Очищенную плазмидную ДНК проверяли с помощью рестрикционного анализа и секвенирования. В ходе работы были отобраны клоны, содержащие фрагменты ДНК требуемого размера в составе плазмиды, из которых такие плазмиды были выделены для дальнейшей индукции экспрессии гена.
1.5. Создание штамма Е. coli - продуцента гибридного белка.
Для экспрессии гена, кодирующего гибридный белок, использовали клетки E.coli штамма BL21 Star (DE3) (Invitrogen, USA), с генотипом F- ompT hsdSB (rB-mB-) gal dcm rne131 (DE3), содержащие в геноме λDe3 лизоген и мутацию rne131. Мутированный ген rne (rne 131) кодирует усеченную форму РНКазы Е, что уменьшает внутриклеточное разрушение мРНК, приводя к увеличению ее ферментативной стабильности. lon- и ompT-мутации по генам протеаз позволяют получать непротеолизированные рекомбинантные белки в больших количествах.
Подготавливали клетки Е. coli штамма BL 21с генотипом F- ompT hsdSB (rB-mB-) gal dcm rne131 (DE3) следующим образом. Инкубировали клетки при +37°С в течение ночи в 5 мл L-бульона, содержащего 1% триптон, 1% дрожжевой экстракт и 1% натрий хлористый. Разводили культуру свежим L-бульоном в 50-100 раз и выращивали на качалке при +37°С до оптической плотности 0,2-0,3 при длине волны 590 нм. При достижении оптической плотности более 0,3 культуру разводили свежим L-бульоном до оптической плотности 0,1 и растили 30 мин. Переносили 100 мл культуры в стерильную центрифужную пробирку и осаждали клетки при +4°С на 5000g в течение 10 мин. Супернатант сливали, клетки ресуспендировали в деионизованной воде в исходном объеме с последующим центрифугированием. Процедуру отмывки повторяли трижды. После отмывки осадок клеток ресуспендировали в малом объеме деионизованной воды и центрифугировали 30 сек при 5000 об/мин, на микроцентрифуге.
Трансформацию компетентных клеток осуществляли методом электропорации. Для этого 1 мкл плазмидной ДНК добавляли к 12 мкл компетентных клеток, перемешивали и проводили электропорацию на генераторе высоковольтных импульсов ГВИ-1 (СПбГТУ, Санкт-Петербург) в стерильных ячейках при электрическом импульсе напряженностью 10 кВ/см длительностью 4 мсек.
После трансформации клетки инкубировали в SOC-среде (2% бакто-триптон, 0,5% дрожжевой экстракт, 10 мМ NaCl, 2,5 мМ КСl, 10 мМ MgCl2, 10 мМ MgSO4, 20 мМ глюкоза) в течение 40 мин при +37°С. 10-100 мкл клеточной суспензии высеивали на селективную LB-среду (Gibko BRL, США), содержащую ампициллин (100 мкг/мл), для отбора клонов, содержащих плазмиды (штаммов-продуцентов).
Полученная после трансформации компетентных клеток штаммов Е. coli плазмида обеспечивала высокий уровень биосинтеза рекомбинантного белка, закодированного в ней.
1.6. Получение гибридного белка в клетках E.coli индукцией синтеза белка 0.2% лактозой по методу Штудиера.
Для культивирования полученных штаммов-продуцентов использовали стандартную агаризованную LB-среду, содержащую ампициллин в концентрации 100 мкг/мл и глюкозу в концентрации 1% для блокирования неспецифической экспрессии.
Индукцию экспрессии проводили при достижении культурой клеток оптической плотности 0.6-0.8 оптических единиц при длине волны 600 нм.
В качестве индуктора использовали 0.2% лактозу (Studier, 2005).
Для автоиндукции экспрессии по методу Штудиера (Studier, 2005) использовали среду PYP-5052, состоящую из 1% пептона (Gibco, США), 0.5% дрожжевого экстракта (Gibco, США), 50 мМ Na2HPO4, 50 мМ К2НРО4, 25 мМ (NH4)2SO4, 2 мМ MgSO4, 0.5% глицерола, 0.05% глюкозы и 0.2% лактозы.
В среду PYP-5052, содержащую ампициллин в концентрации 100 мкг/мл, инокулировали единичную колония штамма-продуцента. Ферментацию проводили при +37°С в термостатированном шейкере роторного типа при 250 об/мин в течение 20 часов до отсутствия существенного изменения ОП600 за 1 час. Отбирали аликвоту клеток на анализ экспрессии гена, кодирующего вакцинный белок, методом электрофореза в ПААГ, а оставшуюся биомассу осаждали центрифугированием при 9000 g.
Белок выделяли из клеток E.coli посредством лизиса клеток. Клетки ресуспендировали в лизирующем буфере, содержащем 20 мМ трис-HCl рН 7,5, 5 мМ ЭДТА и 1 мМ феноксиметилсульфонилфторид, из расчета на 1 г клеток 5-7 мл буфера. Суспензию клеток обрабатывали ультразвуком 7 раз по 30 сек с интервалом в 30 сек (частота ультразвука составляет 22 кГц). Лизат центрифугировали 10 мин при +4°С, 5000 g. Надосадочную жидкость сливали, к осадку добавляли раствор 1 М мочевины из расчета 10 мл на 1 г клеток, интенсивно перемешивали. Повторяли центрифугирование. Супернатант сливали, осадок ресуспендировали в растворе 2 М мочевины того же объема. Повторяли центрифугирование. Супернатант сливали.
Полученный препарат содержал по данным SDS-PAGE (PolyAcrylamide Gel Electrophoresis with Sodium dodecyl sulfate) около 98% гибридного белка в концентрации 1 мг/мл.
Условия выделения и очистки подбирались экспериментальным путем и могут варьировать в известных среднему специалисту в этой области значениях.
1.7. Получение очищенного препарата гибридного белка.
К раствору гибридного белка добавляли MgCl2 до концентрации 6 мМ и проводили очистку гибридного белка с использованием метода иммобилизованной металлоаффинной хроматографии (ИМАХ) с использованием сорбента Ni-НТУ сефарозы. Связывание с данным сорбентом происходит за счет 6 остатков гистидина, имеющихся на N-конце полученного рекомбинантного белка. Белковый раствор фильтровали через ПВДФ фильтр с диаметром пор 0,22 мкн, к полученному фильтрату добавляли сорбент Ni-НТУ сефарозу, уравновешенную буфером для рефолдинга, из расчета, что 1 мл сорбента связывает не более 40 мг белка, и проводили связывание при постоянном перемешивании в течение 2 часов. Сорбент осаждали центрифугированием и в минимальном объеме наносили на гравитационную хроматографическую колонку, содержащую 2 мл сорбента.
Элюцию проводили ступенчатым градиентом имидазола от 20 до 300 с шагом в 50% от предыдущего, при этом на каждую ступеньку приходился объем элюирующего раствора, равный 5-20 объемам колонки. Выход и чистоту белка контролировали методом диск-электрофореза и измерением концентрации белка по методу Бредфорд.
Для определения содержания эндотоксинов приготавливали стандартный стоковый раствор эндотоксина с концентрацией 4000 EU на мл, полученный раствор был стабилен при хранении при +4°С в течение, по крайней мере, 2-х недель. Серию разведений стокового раствора эндотоксина с шагом в 2 раза приготавливали с использованием свободной от эндотоксинов воды в стерильных полистиреновых пробирках, заклеивающихся свободным от эндотоксина парафильмом. Готовили серию разведений образца субстанции с шагом концентрации 5, а после предварительного определения содержания эндотоксина - с шагом концентрации 2.
На дно каждого эппендорфа добавляли образец, воду или эндотоксин в 100 мкл, после чего добавляли 100 мкл лизата ЛАЛ-реактива и инкубировали в течение 1 часа при 37°С на водяной бане. Результаты оценивали по наличию или отсутствию плотного тромба на дне пробирки путем переворачивания пробирки.
Было показано, что в исследуемом образце отсутствуют факторы, ингибирующие образование тромба. Гель-тромб образовался при 1/8 разведении образца, т.е. при чувствительности метода 0,03 EU/мл, в образце с концентрацией 50 мкг/мл содержится менее 100 EU.
Конформацию рекомбинантного гибридного белка при его синтезе в клетках E.coli определяли методом диск-электрофореза в ПААГ клеток E.coli, разрушенных с использованием ультразвука после проведения индукции экспрессии, при этом анализировали осадок и супернатант, образовавшиеся после осаждения клеточных обломков. В результате денситометрического анализа было показано, что рекомбинантный белок, синтезированный в клетках E.coli штаммов-продуцентов при индукции экспрессии 0.2% лактозой, на 100% находится в супернатанте, т.е. растворимой фракции.
Культивирование бактерий при различных температурах: 20°С, 30°С и 37°С не вызывало изменения растворимости белка.
После проведения диск-электрофореза в ПААГ лизатов клеток E.coli после автоиндукции экспрессии 0.2% лактозой осуществляли анализ уровня экспрессии целевого белка в клетках E.coli методом денситометрирования. В результате денситометрического анализа было показано, что в клетках E.coli гибридный белок накапливается в количестве 45% от общего клеточного белка.
Полученный уровень экспрессии не изменялся в штамме-продуценте в течение 6 пассажей, что свидетельствует о стабильном характере экспрессии анализируемого гена.
1.8. Получение рекомбинантного гибридного белка с использованием культивирования клеток E.coli с непрерывным добавлением питательных субстратов, предпочтительно глюкозы и дрожжевого экстракта.
При культивировании штамма Escherichia coli для получения гибридного белка использовали метод периодических культур с подпиткой. Данный метод применяется для предотвращения негативных последствий лимита субстрата, при этом субстрат или другие необходимые компоненты добавляются либо непрерывно, либо по сигналу от какого-либо датчика. Для оптимизации выхода продуктов, выделяемых в среду, важно усилить биосинтетическую способность клеток бактерий, а метод культивирования с подпиткой позволяет продлить вторую фазу роста и повысить выход внеклеточных метаболитов. Данный метод можно использовать в случае потенциально токсичного субстрата (рекомбинантные белки токсичны для клеток E.coli), так как при этом его концентрация в среде будет поддерживаться на низком уровне.
Ограничение скорости поглощения субстрата скоростью его доставки оказывается способом преодоления "катаболитной репрессии" образования продукта.
Культура с подпиткой оказалась наиболее эффективным путём для достижения высокой плотности клеток и высокой продуктивности.
Штамм E.coli стерильно пересевали на скошенные косяки ЭДТА-содержащего агара и выдерживали в термостате 5 суток. Для получения инокулята осуществляли смыв культуры с косяков, засевали в жидкую среду с ЭДТА и культивировали 3-4 суток. После инокулят в количестве 10 мл переносили в стерильные 750-мл колбы с 200 мл стерильной жидкой среды и культивировали в течение 10 суток на качалке при 150-200 об/мин при температуре 28-30°С.
Твердая питательная среда использовалась для получения свежей культуры штамма.
Жидкую питательную среду применяли для получения посевного материала и для периодического культивирования. Приготовление жидкой питательной среды
1) MgSO4*7Н2O 10 мл/л
2) СаСl2*2 Н2O 20 мл/л
3) КН2РО4 + NaH2PO4*12 H2O 10 мл/л
4) EDTA 10 мл/л
5) Микроэлементы 1 мл/л
(доводили до рН 4,2) + 5,6 г/л ЭДТА:
FeCl2*4H2O 1,5 г/л
Н3ВО3 0,06 г/л
MnСl2*6Н2О 0,1 г/л
СаСl2*6 Н2O 0,12 г/л
ZnCl2 0,07 г/л
NiCl2*6 H2O 0,025 г/л
CuCl2*2Н2О 0,015г/л
Na2MoCl4 0,025 г/л
6) Витамины
Пиридоксин 20 мг
Тиамин 10 мг
Рибофлавин 10 мг
Никотиновая кислота 10 мг
Р - аминобензойная кислота 10 мг
Липоевая кислота 10 мг
Никотинамид 10 мг
Витамин В12 10 мг
Биотин 4 мг
Фолиевая кислота 4 мг
Все компоненты растворяли в 200 мл воды, стерилизовали при 0,5 атм 30 минут и добавляли в жидкую питательную среду в количестве 1 мл/л.
Компоненты питательных сред взвешивали на технических и аналитических электронных весах и растворяли в дистиллированной воде. Опыт по приготовлению питательных сред показал, что ее удобно готовить из заранее стерилизованных концентрированных растворов.
Твердую питательную среду готовили как жидкую, с добавлением 3% агара.
Оптическая плотность (ОП600) культур клеток E.coli составила 9 О.Е. Клетки осаждали центрифугированием при 13000 g в течение 6 мин при температуре 10°С. Осадок клеток взвешивали, он составил 1,9 г.
Клетки ресуспендировали в 30 мл буфера (50 мМ ТрисНСl, рН, 50 мМ ЭДТА, 20 мМ L-цистеин, рН 8.6) и разрушали с использованием ультразвука (время озвучивания - 10 мин, время импульса - 30 сек, время паузы между импульсами - 30 сек, амплитуда - 70%). После разрушения клеток тельца включения осаждали с использованием центрифугирования при 30000 g в течение 20 мин при температуре 10°С, вес сырого остатка телец включения из клеток составил 1.5 г. Осажденные тельца включения отмывали с использованием последовательной смены нескольких буферов по следующей схеме.
1. Осадок телец включения ресуспендировали в 10 мл (последняя отмывка 15 мл) буфера для отмывки.
2. Ресуспендированные тельца включения перемешивали на горизонтальном шейкере в течение 1 часа при комнатной температуре.
3. Тельца включения осаждали центрифугированием при 30000 g в течение 20 мин при температуре 10°С.
После пяти отмывок сырой вес телец включения составил 0.9 г.
Для солюбилизации белка из отмытых телец включения использовали 18 мл раствора (9 М мочевина, 2 мМ ЭДТА, 50 мМ ТрисНСl, рН 8.6). Солюбилизированные тельца включения центрифугировали при 30000 g в течение 20 мин при температуре 10°С. Образовавшийся супернатант переносили в новые фальконы и использовали для рефолдинга.
Рефолдинг проводили методом 10-кратного разведения солюбилизированных телец включения в буфере для рефолдинга при температуре +4°С по каплям. К раствору рефолдированного белка добавляли MgCl2 до 6 мМ и использовали для очистки белка метод иммобилизованной металлоаффинной хроматографии (ИМАХ) с использованием сорбента Ni-НТУ сефарозы. Белковый раствор фильтровали через ПВДФ фильтр с диаметром пор 0,22 микрона и к полученному фильтрату добавляли сорбент Ni-НТУ сефарозу, уравновешенный буфером для рефолдинга, из расчета, что 1 мл сорбента связывает не более 40 мг белка, после чего проводили связывание при постоянном перемешивании в течение 2 часов. Сорбент осаждали центрифугированием и в минимальном объеме наносили на гравитационную хроматографическую колонку, содержащую 2 мл сорбента. Элюцию проводили ступенчатым градиентом имидазола (20, 40, 100, 150, 200 и 300 мМ), при этом на каждую ступеньку приходился объем элюирующего раствора, равный 10 объемам колонки.
С использованием данного метода очистки было получено 43 мг гибридного белка с чистотой 98%.
1.9. Получение гибридного белка, очищенного перед растворением удалением растворимых клеточных компонентов, включающих ДНК, РНК, белки, липополисахариды посредством промывания буферным раствором, содержащим детергент гуанидингидрохлорид.
После проведения ферментации и разрушения клеток E.coli, отмывки телец включения (п. 1.8.) проводили солюбилизацию белка 18 мл раствора (8 М GuHCl, 2 мМ ЭДТА, 50 мМ ТрисНСl, рН 8.6), содержащего гуанидингидрохлорид. Солюбилизированные тельца включения центрифугировали при 30000 g в течение 20 мин при температуре 10°С. Образовавшийся супернатант переносили в новые фальконы и использовали для рефолдинга.
Далее проводили рефолдинг рекомбинантного белка и их очистку (см. Пример 8). В результате очистки был получен 41 мг гибридного белка с чистотой 98%.
Пример 2. Получение высокоочищенного гибридного белка (SEQ ID NO.:3) для вакцины против ротавирусной инфекции с использованием клеток E.coli.
2.1. Моделирование гибридного белка.
Спланированный гибридный полипептид является сложным мультидоменным белком (4 домена: FliC1, FliC2, VP6, VP8). Для моделирования мультидоменных белков были произведены следующие действия.
1. Определение границ доменов.
2. Построение модели целого белка для определения ориентации доменов.
3. Построение моделей для каждого домена (с использованием образцов 3D структур и ab initio).
4. Докинг моделей с использованием модели целого белка.
В спланированном гибридном полипептиде два домена имели образцы, а два нуждались в ab initio моделировании, кроме этого в ab initio моделировании требовалось сформировать гибкие мостики между доменами.
Для получения наиболее приближенных к реальности результатов в автоматическом режиме использовали алгоритм I-Tasser, признанный лучшим на последних трех CASP (Critical Assessment of protein Structure Prediction) - соревнованиях по моделированию белков. Данный анализ проводился в течение четырех дней. Однако даже с использованием данного мощного алгоритма получение адекватных данных для мультидоменного белка с необходимостью ab initio моделирования доменов и их границ не полностью достоверно (75%).
Для получения более точных данных разбили белок на используемые домены, провели их моделирование с использованием I-Tasser и далее провели их докинг.
Смоделированный гибридный белок состоит из 458 а.о., представлена его аминокислотная последовательность - SEQ ID NO:3. Анализ аминокислотной последовательности данного белка с помощью программы ProtParam (http://au.expasy.org/tools/protparam.html) показал, что гибридный белок стабилен и имеет молекулярную массу 48,6 кДа, pI 4,6.
2.2. Создана нуклеотидная последовательность, кодирующая гибридный белок, согласно п. 1.2. примера 1, создана плазмидная ДНК, кодирующая гибридный белок, согласно п. 1.3. примера 1, создан штамм E.coli для амплификации плазмидной ДНК, содержащей гибридный ген, согласно п. 1.4. примера 1, создан штамм E.coli - продуцент гибридного белка, согласно п. 1.5. примера 1, получен гибридный белок в клетках E.coli индукцией синтеза белка 0.2% лактозой по методу Штудиера, согласно п. 1.6. примера 1, получен очищенный препарат гибридного белка, согласно п. 1.7. примера 1.
Выход белка составил 1 г с 1 л среды.
Пример 3. Получение высокоочищенного гибридного белка (SEQ ID NO.:2) для вакцины против ротавирусной инфекции с использованием клеток дрожжей S.cerevisiae.
Проведено моделирование гибридного белка согласно п. 1.1. примера 1, создана нуклеотидная последовательность, кодирующая гибридный белок, согласно п. 1.2. примера 1 (нуклеотидная последовательность оптимизирована для экспрессии гена в дрожжах), создана плазмидная ДНК, кодирующая гибридный белок, согласно п. 1.3. примера 1 (использован вектор pYES2/NT, Invitrogen, USA).
3.1. Создание штамма Saccharomyces cerevisiae - продуцента гибридного белка.
Дрожжи культивировали в среде YPD до достижения середины логарифмической фазы роста, промывали 10 мМ буфером ТЕ. Клетки, содержащиеся в 100 мл среды, ресуспендировали в 5 мл 10 мМ Трис НСl буфера (рН 7,5), содержащего 40,5% ПЭГ-4000, 0,1 М ацетата лития. К 0,5 мл суспензии клеток добавляли 1 мкг плазмидной ДНК, перемешивали и инкубировали в течение ночи при комнатной температуре. Далее 50 мкл суспензии клеток высевали на селективную среду для отбора трансформантов [11].
3.2. Продукция гибридного белка в полученном штамме Saccharomyces cerevisiae
Полученный штамм-продуцент выращивали в среде YPD на ротационной качалке со скоростью 250 об/мин при температуре 28°С в течение 20-24 часов. В 5-литровый ферментер Biostat, содержащий 2 000 мл среды YPD, вводили 80 мл посевного материала. Ферментацию проводили при температуре 28°С, аэрации 1 л/мин и скорости перемешивания 1000 об/мин. Через 24 часа после засева ферментера подпитывали среду культивирования 50%-ным раствором глюкозы со скоростью 2 мл/ч и устанавливали рН-статирование культуры на уровне рН 6.8±0.1, используя для регулировки растворы 10% серной кислоты и 10% NaOH. Среднее общее время ферментирования составляет 72 часа. По данным электрофоретического анализа продукция гибридного белка в этих условиях составила не менее 300 мг/л культуральной жидкости.
3.3. Выделение и очистка рекомбинантного гибридного белка из водонерастворимой фракции клеток Saccharomyces cerevisiae.
Проводили выделение и очистку белка из водонерастворимой фракции клеток штамма-продуцента [12]. При наращивании биомассы дрожжей S.cerevisiae в 5-литровом ферментере на среде YPD без подпитки в присутствии 2% глюкозы в стартовой среде с одной ферментации получали в среднем 700-900 г влажной клеточной биомассы. 1,5 кг промытой влажной биомассы ресуспендировали в "буфере для разрушения", клетки разрушали с помощью стеклянных шариков в проточной мельнице в течение 1,5 часов, центрифугировали полученную суспензию и собирали осадок. Экстракцию целевого белка из осадка осуществляли с помощью раствора 10% лития хлористого в 90%-ной муравьиной кислоте в течение 16-18 часов с последующим центрифугированием. Осадок отбрасывали, а супернатант подвергали ультрафильтрации с последующей диафильтрацией через мембрану M15 для перевода в 10 мМ ацетат натрия, рН 4,0 и удаления белков клетки-хозяина с молекулярной массой ниже 15 кДа.
Проводили дегликозилирование белка с помощью эндо-β-N-ацетилглюкозаминидазы Н в 50 мМ натрий-цитратном буфере (рН 5,5), при 37° в течение 18 часов в присутствии 0,01% ДСН.
Окончательную очистку проводили с помощью ионнообменной хроматографии на катионообменной колонке HiPrep 16/10 SP FF (GE Healthcare) в системе ФПЛС. После прохождения фильтрата через колонку и последующей промывки колонки 10 мМ Na-фосфатным буфером, рН 7,0 и затем 10 мМ натрий-ацетатным буфером, рН 4,0, белок элюировали с колонки 10%-ным раствором NaCl в том же буфере и идентифицировали электрофоретически в 10% ПААГ-ДДс-Na, фракции с целевым белком объединяли, диализовали против деионизованной воды, замораживали при -70°С и лиофильно высушивали. Лиофилизованный препарат представляет собой субстанцию белого цвета, похожую на вату.
Выход белка составил 10 г с 1 л питательной среды.
Пример 4. Получение высокоочищенного гибридного белка (SEQ ID NO.:4) для вакцины против ротавирусной инфекции с использованием клеток дрожжей Pichia pastoris.
Проводили моделирование гибридного белка согласно п. 1.1. примера 3, создали нуклеотидную последовательность, кодирующую гибридный белок, согласно п. 1.2. примера 1 (нуклеотидная последовательность оптимизирована для экспрессии гена в дрожжах), создана плазмидная ДНК, кодирующая гибридный белок, согласно п. 1.3. примера 1 (использован вектор pHIL-Sl для получения секретируемого белка).
4.1. Подготовка клеток к трансформации.
Провели культивирование и заморозку штамма клеток Pichia pastoris SMD1163, дефектного по нескольким протеазам дрожжей, что обеспечивает стабильность секретируемого белка. Клетки высевали в стерильных условиях на агар в среде YPD (1% - дрожжевой экстракт, 2% - пептон, 2% - глюкоза, 1 мМ дитиотрейтол), культивировали при 30°С, затем пересевали в суспензию и культивировали в течение ночи. Время удвоения клеток в среде YPD всех клонов составляло 2 часа. Часть клеток ресуспендировали в YPD среде с добавлением 15% глицерина и замораживали при -86°С. Для получения компетентных клеток предварительно выращивали колонии клеток в чашке с агаром в YPD среде при 30°С в течение 2 дней. Затем содержимое одной колонии выращивали в 10 мл YPD среды при 30°С в течение ночи. Разбавляли суспензию в YPD до плотности ОД600 0.2 и конечного объема 10 мл и выращивали культуру до ОД600 0-8 в течение 4 часов. Суспензию клеток центрифугировали 5 мин при 500 g, выливали супернатант, ресуспендировали в 10 мл раствора I из указанного ниже набора для трансформации, вновь центрифугировали и ресуспендировали осадок в растворе I, после чего клетки были компетентны к трансформации. Аликвоты компетентных клеток по 50-200 мкл разливали в стерильные пробирки объемом 1.5 мл, которые хранили при температуре -90°С до использования.
4.2. Трансформация компетентных клеток.
Для трансформации использовали EasyComp Transformation Kit, входящий в состав Pichia Easy Select Kit (Invitrogen).
К 50 мкл компетентных клеток добавляли 3 мкг ДНК-конструкции, 1 мл раствора II из набора, перемешивали встряхиванием, инкубировали в течение 1 часа при 30°С, перемешивая раствор каждые 15 мин. Затем раствор инкубировали 10 мин при 42°С, разделяли на 2 микропробирки по 525 мкл, добавляли в каждую по 1 мл среды YPD и инкубировали 60 мин при 30°С для приобретения клетками резистентности к зеоцину. После этого клетки центрифугировали 5 мин при 3000 g, ресуспендировали в растворе III, добавляя его в каждую пробирку по 500 мкл, сливали суспензию из 2 пробирок в одну, вновь центрифугировали и ресуспендировали осадок в 150 мл раствора III. Полученную суспензию клеток рассевали в стерильную чашку (80 мм) на агаровый гель, приготовленный на среде YPD с добавлением 1 М сорбитола и антибиотика зеоцина в конечной концентрации 100 мкг/мл. Через 3 суток получали несколько десятков колоний на чашку. Клетки из колоний переносили на чашку с MMD (minimal medium dextrose)-arapoм и культивировали чашку 2 дня при 30°С. После этого чашку с культурами использовали для выращивания клеток в суспензии и их последующего тестирования.
4.3. Контроль экспрессии рекомбинантного белка в полученных штаммах. Контроль экспрессии целевого гена осуществляли путем электрофоретического разделения белков в полиакриламидном геле (SDS-PAGE). Для этого клетки из выросших на селективной среде колоний переносили в колбы и культивировали в 5 мл среды MGY на качалке (250 rpm) в течение 1 суток до OD600 5. После этого клетки осаждали центрифугированием при 3000 g 10 мин. Для электрофореза использовали оборудование фирмы Bio-Rad и реактивы ICN. Супернатант и внутриклеточные белки (лизат клеток) смешивали с буфером для нанесения и вносили по 10 мкл в лунки концентрирующего геля. Разделение осуществлялось при напряжении 150 В в течение часа. Затем гель окрашивали с помощью реагента "PAGE blue 83", BDH. Были отобраны штаммы, для которых выявлено наличие на электрофореграммах полос, соответствующих по молекулярной массе целевому белку. Уровень синтеза белка определяли, сравнивая интенсивность окрашивания полосы рекомбинантного белка с полосой соответствующего белка - стандарта молекулярной массы. В результате из 6 штаммов-продуцентов, согласно полученным данным, был отобран штамм Pichia pastoris 3, клетки которого синтезируют 400 мг белка на литр культуры дрожжей.
4.4. Очистка химерного белка.
После осаждения клеток питательную среду фильтровали (диаметр пор 45 мкм), затем добавляли Трис-HCl рН 6.0 до конечной концентрации 20 мМ. Среду культивирования, содержащую гибридный белок, концентрировали в 5-10 раз, используя концентраторы для белков с молекулярной массой более 10 кДа фирмы "Millipore".
После концентрирования препарат химерного белка нагревали на водяной бане до кипения (t=100°C) и кипятили 2 минуты, после чего центрифугировали при 4°С, 15000×g 15 минут.
Проводили ионообменную хроматографию на КМ-сефарозе. Колонку с КМ-сефарозой уравновешивали буфером, содержащим 20 мМ Трис-HCl рН 6.0. Препарат химерного белка наносили со скоростью 60 мл/час. Колонку промывали 20 мМ Трис-HCl рН 6.0; 20 мМ Трис-HCl рН 6.0, 200 мМ NaCl. Элюцию проводили 20 мМ Трис-HCl рН 6.0, 1 М NaCl и собирали фракции по 1 мл.
Проводили аффинную хроматографию на колонке со смолой His-bindR. Колонку с носителем промывали буфером, содержащим 50 мМ фосфат рН 8.0, 500 mM NaCl. Препарат химерного белка, полученный после концентрирования или ионообменной хроматографии, разбавляли в 2 раза, добавляли фосфат рН 8.0 до концентрации 50 мМ и наносили на колонку. После промывки колонки буфером нанесения балластные белки удаляли промывкой раствором 20 мМ имидазола в том же буфере. Белок элюировали раствором, содержащим 200 мМ имидазола.
В результате был получен препарат гибридного белка с чистотой свыше 95%.
Одним из преимуществ предлагаемого способа получения рекомбинантного белка является высокая технологичность процесса очистки белка, обусловленная простыми процедурами выделения, относительно невысокой стоимостью используемых смол и высоким выходом активного белка в результате очистки.
Суммируя вышесказанное, можно заключить, что полученный штамм дрожжей Pichia pastoris 3 синтезирует химерный белок в количестве, достаточном для его выделения в промышленном масштабе. В результате полученный высокоочищенный химерный белок может быть использован в качестве активного компонента вакцины против ротавирусной инфекции.
Выход белка составил 24 г с 1 л среды.
Пример 5. Получение высокоочищенного гибридного белка (SEQ ID NO.:5) для вакцины против ротавирусной инфекции с использованием клеток млекопитающих - СНО.
Произвели моделирование гибридного белка согласно п. 1.1. примера 3, создали нуклеотидную последовательность, кодирующую гибридный белок, согласно п. 1.2. примера 1 (нуклеотидная последовательность оптимизирована для экспрессии гена в клетках млекопитающих), создана плазмидная ДНК, кодирующая гибридный белок, согласно п. 1.3. примера 1 (использован вектор pSELECT-CGFP-zeo, InvivoGen, USA).
Анализ экспрессии целевого гена проводили на культуре клеток яичников китайского хомячка (СНО-К1, АТСС CCL 61) как наиболее широко применяемой в биотехнологической практике для наработки целевых белков.
5.1. Культивирование линии клеток СНО-К1.
Линию клеток СНО-К1 культивировали на среде DMEM, содержащей 10% инактивированной эмбриональной телячьей сыворотки, 2 мМ L-глутамина, 35 мг/л L-пролина, а также коммерческий антибиотик Mycokill-AB (PAA Laboratories) в рабочей концентрации. Пересев клеток производили 1 раз в 5 дней при концентрации клеток 105 клеток на 1 см2 с разведением 1:20. Клетки культивировали при температуре 37°С, в атмосфере 5%-ного СО2 и высокой влажности.
5.2. Трансфекция клеток.
Данную культуру клеток трансфецировали полученной плазмидой, кодирующей гибридный белок.
Клетки в количестве 70-80% от монослоя (8*104 клеток на 1 см2) промывали культуральной средой, не содержащей сыворотки. Подготавливали трансфекционную смесь: 3-4 мкг линеаризованной плазмидной ДНК смешивали с 375 мкл культуральной среды, не содержащей сыворотки. В отдельной пробирке с таким же количеством аналогичной среды смешивали коммерческий трансфецирующий реагент Lipofectamine 2000, количество которого определяли соотношением 3 мкл реактива на 1 мкг плазмидной ДНК. После этого полученные растворы объединяли и инкубировали при комнатной температуре в течение 30-40 минут.
Полученную трансфекционную смесь наслаивали на промытые клетки. По прошествии 4-6 часов после начала трансфекции трансфекционную смесь заменяли на культуральную среду DMEM с сывороткой.
Уровень экспрессии целевого гена оценивали по интенсивности флуоресценции на вторые сутки после трансфекции (36-48 часов) при помощи проточной цитофлуориметрии. В качестве отрицательного контроля использовали нетрансфецированные клетки линии СНО-К1.
5.3. Цитофлуориметрический анализ.
Для проведения цитофлуориметрического анализа клетки промывали фосфатно-солевым буфером, трипсинизировали и снимали с чашек Петри. Затем дважды отмывали от трипсина и тщательно ресуспендировали в фосфатно-солевом буфере. Полученную суспензию (106 клеток в 1 мл буфера) переносили в 5 мл круглодонные пробирки.
Напряжение каналов проточного цитофлуориметра подбиралось таким образом, чтобы аутофлуоресценция нетрансфицированных клеток не учитывалась при проведении измерений. Для этого напряжение в каналах FL1 (в котором и детектируется флуоресценция eGFP) и FL2 (который использовали в качестве контрольного пустого канала) изменяли так, чтобы в процессе измерений подавляющее большинство клеток, не содержащих ген eGFP, оказалось в области, не превышающей значение "10" на логарифмической шкале, отложенной для каналов FL1 и FL2.
После проведения калибровки все образцы измерялись при постоянных значениях напряжений по каналам FL1 и FL2. Так, если в клетках детектировали флуоресценцию eGFP, на логарифмической шкале по каналу FL1 фиксировалось появление клеток в области, превышающей значение "10", и все количественные значения уровня экспрессии гена измерялись именно в этой области.
5.4. Поддержание пулов трансфецированных клеток.
После проведения трансфекции полученные пулы культивировали согласно описанному выше протоколу (5.1.).
Для того чтобы избавиться от клеток, не содержащих трансген, производилась селекция полученных пулов трансфецированных клеток при помощи коммерческого антибиотика Zeocin (InvivoGen), вводимого в концентрации 800 мкг/мл. Так как в результате подавления транскрипционной активности трансгена наработка продукта гена устойчивости к антибиотику с течением времени снижается, после 75 суток культивирования концентрация антибиотика была постепенно снижена до 200 мкг/мл.
5.5. Получение и анализ стабильных клеточных линий.
Анализ разнородных клеточных пулов может приводить к отклонениям, связанным с тем, что трансген при липофекции многокопийно встраивается в разные участки генома, в результате чего клетки могут обладать разной жизнеспособностью, скоростью деления, устойчивостью к антибиотику и другими характеристиками, важными для эффективной экспрессии трансгена.
Поэтому на практике наработка рекомбинантных белков осуществляется путем отбора стабильных клеточных линий, полученных из одной трансфецированной клетки и, таким образом, характеризующихся однородным генотипом, что позволяет исключить влияние вышеописанных факторов и отобрать наиболее эффективный клон.
Индивидуальные клеточные клоны были получены из тотальных клеточных популяций методом лимитирующих разведений после 50 и 75 суток культивирования.
5.6. Получение индивидуальных клонов.
Культивируемые пулы снимали с планшетов и разводили в 10 мл культуральной среды. После этого концентрация клеток подсчитывалась при помощи камеры Гаряева, и производили дополнительные разведения таким образом, чтобы концентрация клеток составляла 2-3 клетки на миллилитр среды. Полученную суспензию переносили в 24-луночные планшеты по 1 мл на лунку.
После 2 недель культивирования на среде DMEM, содержащей антибиотик Zeocin в концентрации 800 мкг/мкл, производился цитофлуорометрический анализ выживших клонов. Дальнейшее поддержание полученных линий и анализ уровня экспрессии EGFP производили согласно методике, описанной для пулов трансфецированных клеток.
5.7. Результаты анализа временного профиля экспрессии гена EGFP в индивидуальных клеточных клонах.
Основным количественным показателем экспрессионной активности химерного гена в данном случае служила медиана распределения клеток по интенсивностям флуоресценции.
Достаточно высокий уровень экспрессии EGFP наблюдали у 2 клонов с введенной конструкцией.
После двух с половиной месяцев культивирования экспрессионная активность клонов, содержащих конструкцию с геном интереса, составила в среднем около 70% от исходной.
Для получения высокоочищенного химерного белка клетки СНО трансформировали иной плазмидой, обеспечивающей синтез целевого белка; продуцируемый белок очищали с помощью анионообменной хроматографии на Q-сефарозе при рН 7,0. Выход целевого белка составил 10 мг/л.
Применение способа получения гибридного белка в клетках млекопитающих возможно с использованием также других клеток млекопитающих, например НЕK293-EBNA1.
Пример 6. Получение высокоочищенного гибридного белка (SEQ ID NO.:6) для вакцины против ротавирусной инфекции с использованием растений.
Произвели моделирование гибридного белка согласно п. 1.1. примера 3, создали нуклеотидную последовательность, кодирующую гибридный белок, согласно п. 1.2. примера 1 (нуклеотидная последовательность оптимизирована для экспрессии гена в клетках растений), создана плазмидная ДНК, кодирующая гибридный белок, согласно п. 1.3. примера 1.
Для оценки экспрессии гибридного белка в растениях Nicotiana benthamiana вектор вводили в штамм Agrobaterium tumefaciens GV3101, рекомбинантные агробактерии были использованы для инфильтрации листьев N. benthamiana. Агробактерии, содержащие рекомбинантные бинарные векторы, выращивали в течение 12 ч на шейкере при 30°С. Клетки (1,5 мл) осаждали центрифугированием (4000g, 5 мин), осадок ресуспендировали в 1,5 мл буфера, содержащего 10 мМ MES (рН 5.5) и 10 мМ MgCl2, оптическую плотность доводили до OD600=0,2. Листья растений N. benthamiana инъецировали суспензией агробактерии при помощи шприца без иглы. Инфильтрированные листья оставляли на растущих растениях.
После инфильтрации листьев N. benthamiana агробактериями с вирусом-вектором происходит заражение большей части клеток листа в инфицированной области, перенос ДНК в ядро, транскрипция копии вирусной РНК. На последующей стадии происходит репликация вирусного вектора и синтез продукта на высоком уровне [13]. Максимальный синтез продукта достигается на 6-10 сутки после инфильтрации.
Наличие целевого белка в листьях растений-продуцентов регистрировали с помощью электрофореза в ПААГ. На 6-10 день после заражения фрагмент листа растирали в буфере 0.4 М сахароза, 50 мМ Трис рН 8.0, 10 мМ КСl, 5 мМ MgCl2, 10% глицерин, 10 мМ β-меркаптотанол. Полученный экстракт центрифугировали 10 минут при 14000g, супернатант ("растворимая фракция") и растворенный осадок ("мембранная фракция") анализировали с использованием электрофореза в полиакриламидном (ПААГ) градиентном (8-20%) геле по Лэммли и окрашивания Кумасси R-250.
Исходя из полученных результатов, в растениях, инфильтрированных вирусом-вектором в мембранной фракции клеток, обнаружен продукт, соответствующий по молекулярной массе 48,6 кДа. В контрольном неинфильтрированном растении этот белок отсутствовал. Выход продукта составлял около 6% фракции нерастворимых белков.
Исходя из полученных результатов, заявляемые гибридные белки возможно получить с использованием и прокариотических, и эукариотических клеточных систем, высокоочищенныи препарат белка можно получить с использованием различных типов очистки белка.
Пример 7. Определение иммуногенности препарата гибридного белка (SEQ ID NO.: 1, SEQ ID NO.: 2, SEQ ID NO.: 3, SEQ ID NO.: 4).
Проводили оценку иммуногенности препаратов полученных белков. Иммуногенность - это способность антигена инициировать иммунную систему к формированию эффекторов, нейтрализующих антигенную чужеродность.
Иммунизацию мышей линии Balb/c (самки) проводили внутрибрюшинно, вводили 20 мкг гибридного белка. Иммунизацию проводили двукратно с интервалом в 2 недели. Животные были разделены на опытные и контрольные группы по 7-8 мышей в каждой.
Образцы крови получали от 7-8 мышей каждой группы через 2 недели после второй иммунизации из хвостовой вены. Для получения сыворотки кровь инкубировали в течение 30 минут при температуре 37°С. После образования сгустков крови образцы помещали на поверхность льда и охлаждали в течение 1-го часа с последующим центрифугированием в течение 15 минут при 400 g. Сыворотку крови от мышей каждой группы пулировали и замораживали при температуре минус 20°С.
Титры антител в сыворотках иммунизированных мышей определяли с помощью иммуноферментного анализа (ИФА). ИФА проводили общепринятым методом. Использовали 96-луночные планшеты (Greiner, Германия).
Гибридный белок денатурировали следующим образом. К образцу белка добавляли детергент Tween-20 до конечной концентрации 1% (w/v), инкубировали на водяной бане в течение 1 часа при 37°С. Далее образец центрифугировали 1 час при 200°С и 2000 g, отбирали супернатант, содержащий гибридный белок. От детергента избавлялись при помощи Detergent-OUTtmMicro Kit (Millipore), свободный от детергента образец концентрировали на установке SpeedVac до первоначального объема. Дополнительную обработку конечного препарата проводили 8 М мочевиной в присутствии дитиотриэтанола (0,02 М) с последующим диализом в течение ночи против карбонатного буфера (рН 8,5).
Сорбировали гибридный белок (в карбонатном буфере, рН 9,5-9,6) на 96-луночном планшете, выдерживали ночь при 4°С. Планшет обрабатывали блокирующим буфером (0,01 М ФСБ, рН 7,2-7,4 с 5% ЭТС) в течение 1 часа при комнатной температуре, отмывали 3 раза ФБР с Tween-20. В лунки планшета добавляли 100 мкл 2-кратных разведений сыворотки (начиная с 1:200) в блокирующем буфере, инкубировали 1 час при комнатной температуре. Сыворотку исследовали в дубликате. В качестве конъюгата использовали поликлональные кроличьи антитела к Иммуноглобулину A (NeoMarkers Inc., USA) в разведении 1:7000, меченные пероксидазой хрена. В качестве субстрата использовали ТМБ. Учет реакции проводили при длине волны 450 нм. За титр принимали наибольшее разведение сыворотки, которое дает оптическую плотность, по крайней мере, в 2 раза больше, чем сыворотка неиммунизированных мышей в том же разведении.
Полученные результаты свидетельствуют о высокой иммуногенности полученных белков. При иммунизации гибридными белками в крови мышей выявлялись антитела ко всем исследованным типам ротавирусов в диапазоне от 1:5200 в случае ротавируса В, SEQ ID NO.:3, до 1:70 000 в случае ротавируса A, SEQ ID NO.:3 (Табл. 1). Разница в титрах антител, индуцируемых белками группы SEQ ID NO.:1, SEQ ID NO.:2, а также группы SEQ ID NO.:3- SEQ ID NO.:6, оказалась несущественной.
Таким образом, было показано формирование у мышей, иммунизированных вариантами гибридного белка, поливалентного иммунного ответа к ротавирусам групп А, В и С.
Пример 8. Протективность иммунного ответа, вызываемого гибридными белками (SEQ ID NO.:6, SEQ ID NO.:5, SEQ ID NO.:2), против ротавирусов групп А, В и С.
В настоящем исследовании были использованы мыши линии Balb/c (самки), 7-8 недель (массой 17-19 г), полученные из Учреждения Российской академии наук Института биоорганической химии им. академиков М.М.Шемякина и Ю.А.Овчинникова РАН (Филиал) Питомник лабораторных животных "Пущино". Лабораторные животные были клинически здоровы и свободны от гельминтов (ветеринарное свидетельство 302 № 0207364 от 11 января 2013 г.). Животных содержали в виварии ФГУ "НИИ детских инфекций" ФМБА России в соответствии с действующими санитарными правилами.
Иммунизацию мышей проводили внутримышечно и назально: внутримышечно вводили гибридный белок в составе адъюванта Фрейнда (20 мкг гибридного белка), назально вводили водный раствор гибридного белка. Иммунизацию проводили двукратно с интервалом в 2 недели.
Для изучения протективности гибридного белка на модели летальной ротавирусной инфекции использовали образцы ротавирусов А, В и С, предоставленные ФГУ "НИИ детских инфекций" ФМБА России, адаптированные к мышам. Титрование вирусов для определения одной дозы, вызывающей 50% гибели животных, проводили на мышах линии Balb/c (самки, возраст 7-8 недель). Замороженный вирус оттаивали, определяли мышиную летальную дозу (вызывающую 50% гибель) путем заражения мышей десятикратными разведениями вируса (по 3 мыши на разведение). Наблюдение за гибелью мышей вели в течение 14 суток после заражения. Титр вируса определяли по методу Рида и Менча. Для заражения мышей вирус вводили перорально в дозе 1 LD/50 (доза, вызывающая гибель 50% мышей) по 50 мкл/мышь. После заражения проводили ежедневное наблюдение за животными в течение 14 дней.
Заражали мышей образцом ротавируса А в количестве 1,5*108 бляшкообразующих единиц (БОЕ). Гибель зараженных мышей в контрольной группе начиналась на 2 день, выживаемость мышей составила 40%. В опытной группе (SEQ ID NO.:6) наблюдалась 64% выживаемость мышей (Фиг.1). Изучение динамики массы тела мышей позволило установить, что в опытной группе снижение массы тела происходило более медленно и не превысило 16%. В контрольной группе масса тела мышей уменьшилась на 28% (Фиг.2).
Заражали мышей образцом ротавируса В в количестве 1,1 *107 бляшкообразующих единиц (БОЕ). Гибель зараженных мышей в контрольной группе начиналась на 3 день, выживаемость мышей составила 35%. В опытной группе (SEQ ID NO.:5) наблюдалась 45% выживаемость мышей (Фиг.3). Изучение динамики массы тела мышей позволило установить, что в опытной группе снижение массы тела происходило более медленно и не превысило 11%, с 10 дня масса тела увеличивалась. В контрольной группе масса тела мышей уменьшилась на 22%, увеличение массы тела в изученный промежуток времени не наблюдали (Фиг.4).
Заражали мышей образцом ротавируса С в количестве 1,2*108 бляшкообразующих единиц (БОЕ). Гибель зараженных мышей в контрольной группе также начиналась на 2 день, выживаемость мышей составила 32%. В опытной группе (SEQ ID NO.:2) наблюдалась 68% выживаемость мышей (Фиг.5). Изучение динамики массы тела мышей позволило установить, что в опытной группе снижение массы тела происходило более медленно и не превысило 15%, с 12 дня наблюдали набор веса. В контрольной группе масса тела мышей уменьшилась на 22% (Фиг.6).
Пример 9. Протективное действие вакцины на основе химерного белка (SEQ ID NO.:4) на терапевтической модели летальной инфекции ротавирусом групп А, В и С.
В настоящем исследовании были использованы мыши линии Balb/c (беременные самки), 7-8 недель (массой 18-21 г), полученные из Учреждения Российской академии наук Института биоорганической химии им. академиков М.М.Шемякина и Ю.А.Овчинникова РАН (Филиал) Питомник лабораторных животных "Пущино". Лабораторные животные были клинически здоровы и свободны от гельминтов (ветеринарное свидетельство 302 № 0207364 от 11 января 2013 г.). Животных содержали в виварии ФГУ "НИИ детских инфекций" ФМБА России в соответствии с действующими санитарными правилами.
Заражали новорожденных мышей (10-дневных) образцом ротавируса А в количестве 0,5*104 бляшкообразующих единиц (БОЕ). В этот же день мышам вводили химерный белок в количестве 5 мкг на мышь с физиологически приемлемым носителем. Наблюдали выживаемость таких мышей в течение 14 дней после введения летальной дозы ротавируса А.
При совместном введении ротавируса А и вакцины на основе химерного белка мыши показали выживаемость 80% через неделю после заражения и 72% на 14 день наблюдений. В контрольной группе выживаемость составила 0% уже на 5 день эксперимента.
Заражали мышей образцом ротавируса В в количестве 1,1*105 бляшкообразующих единиц (БОЕ). В этот же день мышам вводили химерный белок в количестве 5 мкг на мышь. Наблюдали выживаемость таких мышей в течение 14 дней после введения летальной дозы ротавируса В.
При совместном введении ротавируса В и вакцины на основе химерного белка мыши показали выживаемость 76% через неделю после заражения и 66% на 14 день наблюдений. В контрольной группе выживаемость составила 0% на 8 день эксперимента.
Заражали мышей образцом ротавируса С в количестве 1,2*105 бляшкообразующих единиц (БОЕ). В этот же день мышам вводили химерный белок в количестве 5 мкг на мышь. Наблюдали выживаемость таких мышей в течение 14 дней после введения летальной дозы ротавируса С.
При совместном введении ротавируса С и вакцины на основе химерного белка мыши показали выживаемость 77% через неделю после заражения и 62% на 14 день наблюдений. В контрольной группе выживаемость составила 0% на 10 день эксперимента.
Полученные результаты подтверждают высокую иммуногенность двух вакцин, предлагаемых в данном изобретении, на основе белков SEQ ID NO.:1- SEQ ID NO.:6 и возможность их использования для терапии ротавирусной инфекции.

ПЕРЕЧЕНЬ ПОСЛЕДОВАТЕЛЬНОСТЕЙ
SEQ ID NO.:1 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков VP6 и VP8 (175 а.о., 19,4 кДа, pI 4,41).
10 20 30 40 50 60
MDVLFSLSKT LKDARDKIVE GTLYSNVSDL IQQFNQMIIT MNGNDFQTGG IGNLPIRNWN
70 80 90 100 110 120
FDFGLLGTTL LNLDANYVET ARTTIDYFID FVDNVCMDEM ARESQRNGIA GGGSGGGSTI
130 140 150 160 170
NNDNSNVSSD AEFYLIPQSQ TAMCTQYINN GLPPIQNTRN IVPVNITSRQ IKDIR
SEQ ID NO.:2 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков VP8 и VP6 (175 а.о., 19,4 кДа, pI 4,41).
10 20 30 40 50 60
MTINNDNSNV SSDAEFYLIP QSQTAMCTQY INNGLPPIQN TRNIVPVNIT SRQIKDIRGG
70 80 90 100 110 120
GSGGGSDVLF SLSKTLKDAR DKIVEGTLYS NVSDLIQQFN QMIITMNGND FQTGGIGNLP
130 140 150 160 170
IRNWNFDFGL LGTTLLNLDA NYVETARTTI DYFIDFVDNV CMDEMARESQ RNGIA
SEQ ID NO.:3 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков флагеллина: FliC1 (1-169 а.о.), FliC2 (182-276 а.о.), фрагмента белка VP6 (286-397 а.о.), фрагмента белка VP8 (402-458 а.о.), соединенных гибкими мостиками (459 а.о., 48,8 кДа, pI 4,63).
10 20 30 40 50 60
MAQVINTNSL SLLTQNNLNK SQSALGTAIE RLSSGLRINS AKDDAAGQAI ANRFTANIKG
70 80 90 100 110 120
LTQASRNAND GISIAQTTEG ALNEINNNLQ RVRELAVQSA NSTNSQSDLD SIQAEITQRL
130 140 150 160 170 180
NEIDRVSGQT QFNGVKVLAQ DNTLTIQVGA NDGETIDIDL KQINSQTLGL GGGSGGGSGG
190 200 210 220 230 240
GSAATTTENP LQKIDAALAQ VDTLRSDLGA VQNRFNSAIT NLGNTVNNLT SARSRIEDSD
250 260 270 280 290 300
YATEVSNMSR AQILQQAGTS VLAQANQVPQ NVLSLLRGGG SGGGSDVLFS LSKTLKDARD
310 320 330 340 350 360
KIVEGTLYSN VSDLIQQFNQ MIITMNGNDF QTGGIGNLPI RNWNFDFGLL GTTLLNLDAN
370 380 390 400 410 420
YVETARTTID YFIDFVDNVC MDEMARESQR NGIAGGGSGG GSTINNDNSN VSSDAEFYLI
430 440 450
PQSQTAMCTQ YINNGLPPIQ NTRNIVPVNI TSRQIKDIR
SEQ ID NO.:4 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков VP6, VP8, FliC1, FliC2, соединенных гибкими мостиками (459 а.о., 48,8 кДа, pI 4,63).
10 20 30 40 50 60
MDVLFSLSKT LKDARDKIVE GTLYSNVSDL IQQFNQMIIT MNGNDFQTGG IGNLPIRNWN
70 80 90 100 110 120
FDFGLLGTTL LNLDANYVET ARTTIDYFID FVDNVCMDEM ARESQRNGIA GGGSGGGSTI
130 140 150 160 170 180
NNDNSNVSSD AEFYLIPQSQ TAMCTQYINN GLPPIQNTRN IVPVNITSRQ IKDIRGGGSG
190 200 210 220 230 240
GGSAQVINTN SLSLLTQNNL NKSQSALGTA IERLSSGLRI NSAKDDAAGQ AIANRFTANI
250 260 270 280 290 300
KGLTQASRNA NDGISIAQTT EGALNEINNN LQRVRELAVQ SANSTNSQSD LDSIQAEITQ
310 320 330 340 350 360
RLNEIDRVSG QTQFNGVKVL AQDNTLTIQV GANDGETIDI DLKQINSQTL GLGGGSGGGS
370 380 390 400 410 420
GGGSAATTTE NPLQKIDAAL AQVDTLRSDL GAVQNRFNSA ITNLGNTVNN LTSARSRIED
430 440 450
SDYATEVSNM SRAQILQQAG TSVLAQANQV PQNVLSLLR
SEQ ID NO.:5 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков VP8, VP6, FliC1, FliC2, соединенных гибкими мостиками (459 а.о., 48,8 кДа, pI 4,63).
10 20 30 40 50 60
MTINNDNSNV SSDAEFYLIP QSQTAMCTQY INNGLPPIQN TRNIVPVNIT SRQIKDIRGG
70 80 90 100 110 120
GSGGGSDVLF SLSKTLKDAR DKIVEGTLYS NVSDLIQQFN QMIITMNGND FQTGGIGNLP
130 140 150 160 170 180
IRNWNFDFGL LGTTLLNLDA NYVETARTTI DYFIDFVDNV CMDEMARESQ RNGIAGGGSG
190 200 210 220 230 240
GGSAQVINTN SLSLLTQNNL NKSQSALGTA IERLSSGLRI NSAKDDAAGQ AIANRFTANI
250 260 270 280 290 300
KGLTQASRNA NDGISIAQTT EGALNEINNN LQRVRELAVQ SANSTNSQSD LDSIQAEITQ
310 320 330 340 350 360
RLNEIDRVSG QTQFNGVKVL AQDNTLTIQV GANDGETIDI DLKQINSQTL GLGGGSGGGS
370 380 390 400 410 420
GGGSAATTTE NPLQKIDAAL AQVDTLRSDL GAVQNRFNSA ITNLGNTVNN LTSARSRIED
430 440 450
SDYATEVSNM SRAQILQQAG TSVLAQANQV PQNVLSLLR
SEQ ID NO.:6 Аминокислотная последовательность химерного белка, который состоит из фрагментов белков FliC1, FliC2, VP8, VP6, соединенных гибкими мостиками (459 а.о., 48,8 кДа, pI 4,63).
10 20 30 40 50 60
MAQVINTNSL SLLTQNNLNK SQSALGTAIE RLSSGLRINS AKDDAAGQAI ANRFTANIKG
70 80 90 100 110 120
LTQASRNAND GISIAQTTEG ALNEINNNLQ RVRELAVQSA NSTNSQSDLD SIQAEITQRL
130 140 150 160 170 180
NEIDRVSGQT QFNGVKVLAQ DNTLTIQVGA NDGETIDIDL KQINSQTLGL GGGSGGGSGG
190 200 210 220 230 240
GSAATTTENP LQKIDAALAQ VDTLRSDLGA VQNRFNSAIT NLGNTVNNLT SARSRIEDSD
250 260 270 280 290 300
YATEVSNMSR AQILQQAGTS VLAQANQVPQ NVLSLLRGGG SGGGSTINND NSNVSSDAEF
310 320 330 340 350 360
YLIPQSQTAM CTQYINNGLP PIQNTRNIVP VNITSRQIKD IRGGGSGGGS DVLFSLSKTL
370 380 390 400 410 420
KDARDKIVEG TLYSNVSDLI QQFNQMIITM NGNDFQTGGI GNLPIRNWNF DFGLLGTTLL
430 440 450
NLDANYVETA RTTIDYFIDF VDNVCMDEMA RESQRNGIA