Результат интеллектуальной деятельности: СПОСОБ ДИАГНОСТИКИ МУЛЬТИФОРМНОЙ ГЛИОБЛАСТОМЫ С ПОМОЩЬЮ МРТ
Вид РИД
Изобретение
ОБЛАСТЬ ТЕХНИКИ
Изобретение относится к медицине, в частности к способу диагностики мультиформной глиобластомы, а именно способу диагностики мультиформной глиобластомы с помощью метода магнитно-резонансной томографии.
УРОВЕНЬ ТЕХНИКИ
Магнитно-резонансная томография (МРТ) - неинвазивный метод исследования организма человека, основанный на эффекте расщепления ядерных энергетических уровней в атомах с нечетным ядерным спином (1Н, 13С, 19F, 31Р) в постоянном магнитном поле. В отличие от компьютерной томографии, где построение изображения основано на поглощении тканями организма рентгеновского излучения, в МРТ используется электромагнитное излучение радиодиапазона, которое является безвредным [Lauterbur Р.С, NMR zeugmatographic imaging in medicine, J Med Syst.,1982, Vol.6, P.591-597]. Кроме того, MPT, основанная на магнитном резонансе ядер 1Н, более чувствительна к изменениям в мягких тканям, в которых больше протонов, тогда как КТ более применима при диагностике травм и нарушений в функционировании костной ткани.
На сегодняшний день известно несколько типов контрастных агентов, которые могут быть использованы в качестве контрастного агента для визуализации глиомы головного мозга с помощью МРТ.
Известны препараты Магневист, Гадовист и Омнискан, которые используются для диагностики глиом головного мозга. Эти препараты представляют собой хелатные комплексы ионов Gd3+ и являются позитивными Т1-контрастными агентами для МРТ. Также в литературе опубликованы данные об использовании Т2-контрастных агентов на основе магнитных наночастиц оксида железа для визуализации глиом. На сегодняшний день не все известные патологии могут быть легко обнаружены с помощью простого МРТ-исследования, поэтому для более точной диагностики различных отклонений от нормы с помощью МРТ широко применяются различные контрастные агенты, которые можно разделить на два основных класса. Первый класс включает Т1-контрастные агенты, представленные парамагнитными ионами металлов, содержащими большое количество неспаренных электронов (Gd3+, Eu3+, Cr3+, Mn2+, Fe3+) [Runge V.М., Clanton J.A., Lukehart С.М, С. Leon Partain, A. Everette James Jr., Paramagnetic agents for contrast-enhanced NMR imaging: a review. Am. J. Roentgenol., 1983, Vol.141, №6, P.1209-1215]. На рынке этот сегмент заполнен препаратами на основе хелатных комплексов ионов Gd3+ с различными лигандами (Гадовист, Магневист, Омнискан и т.д.). Т1 контрастные агенты являются позитивными контрастами - их накопление повышает интенсивность сигнала на Т1 взвешенных изображениях при МРТ-исследовании.
Ко второму классу относятся Т2-контрастные агенты, представленные магнитными наночастицами оксида железа [Josephson L., Bigler J., White D., Magn Reson Med., The magnetic properties of some materials affecting MR images. 1991, Vol.22, №2, P.204-208], стабилизированными различными биосовместимыми покрытиями. В частности, препараты Feridex и Resovist, являющиеся водной суспензией магнитных наночастиц оксида железа, с диаметром 150-200 нм стабилизированных декстраном, а также препарат Clariscan, представляющий собой также наночастицы оксида железа, но стабилизированные карбоксидекстраном, при этом диаметр частиц составляет 10-15 нм. Т2-контрастные агенты являются негативными контрастами - их накопление понижает интенсивность сигнала на режимах взвешенных по однородности магнитного поля при МРТ исследовании. Существенным является тот факт, что Т2-контрастные агенты, обладая на порядки более высоким значением магнитной восприимчивости за счет входящих в их состав нанокристаллов оксида железа, имеют Т2-релаксивность в 50-100 раз более высокую, чем Т1-контрастные агенты, что снижает необходимую дозу для эффективного контрастирования.
Благодаря низкому молекулярному весу Т1-контрастные агенты быстро выводятся из организма, а также легко преодолевают частично нарушенный ГЭБ, что позволяет использовать их для диагностики опухолей головного мозга, а также в качестве контрастных агентов для МР-ангиографии.
К сожалению, современные препараты не могут дать объективной информации о структуре опухоли и активности ангиогенеза в растущей опухолевой ткани (плотности сосудов), хотя этот фактор является важным медицинским критерием, необходимым для постановки диагноза и стадии развития заболевания.
В статье (Hilda Т.R. Wiogo, May Lim, Volga Bulmus, Jimmy Yun, and Rose Amal Stabilization of Magnetic Iron Oxide Nanoparticles in Biological Media by Fetal Bovine Serum (FBS) // Langmuir 2011, Vol.27, №2, P.843-850.) описан способ стабилизации магнитных наночастиц, имеющих карбоксильные группы на поверхности с помощью смешения с фетальной сывороткой теленка. Указано, что подобные частицы имеют средний гидродинамический диаметр 180 нм и сохраняют егов течение 16ч инкубации в питательной среде RPMI. Также показано, что иммобилизиция белков происходит нековалентно. Однако большой диаметр наночастиц (180 нм) может затруднить их диффузию по кровеносным сосудам к опухоли и тем самым понизить их эффективность в качестве контрастного агента. Нековалентная модификация поверхности может приводить к десорбции покрытия при введении в кровоток и соответственно к потере всех составляющих, закрепленных на покрытии. Кроме того, в данной статье отсутствуют данные о значении Т2-релаксивности, необходимом для оценки эффективности полученного контрастного агента для МРТ-диагностики.
Ранее также был опубликован способ визуализации глиом методом МРТ после внутривенного введения магнитных наночастиц, но конъюгированных с лактоферрином [Hui Xie, Yanhong Zhu, Weili Jiang, Qing Zhou, Hai Yang, Ning Gu, Yu Zhang, Huibi Xu, Haibo Xu, Xiangliang Yang a Lactoferrin-conjugated superparamagnetic iron oxide nanoparticles as a specific MRI contrast agent for detection of brain glioma in vivo, Biomaterials, 2011, Vol.32, P.495-502}. В данной работе была показана визуализация глиомы через 24 и 48 ч с помощью МРТ в режиме турбо-спин-эхо. Однако описанный способ обладает рядом недостатков. Используемые наночастицы оксида железа характеризовались низкой Т2-релаксивностью по сравнению с используемым в практике аналогом, препаратом Feridex. Визуализация опухоли с помощью магнитных наночастиц, оипсанных в данной работе, становится возможна только через 24 или 48 ч, что увеличивает время проведения визуализации для подтверждения анализа. Продемонстрированный характер накопления свидетельствует о накоплении наночастиц преимущественно внутри опухоли, тогда как области активной инвазии практически не контрастируются и соответственно не могут быть выявлены этим способом. Кроме того, визуализация невозможна без конъюгации магнитных наночастиц с векторной компонентой (лактоферритином).
Необходимо отметить, что чрезвычайно важным для МРТ-исследования является выбор режима с помощью которого получается изображение, а точнее взвешенности получаемого изображения. Для Т2-контрастных агентов наиболее предпочтительным являются режимы, имеющие Т2-взвешенность, однако существует режим SWI (Susceptibility Wieghted Imaging), который превосходит их по чувствительности и обладает взвешенностью по восприимчивости магнитного поля. В настоящее время в литературе отсутствуют данные об использовании режима SWI для визуализации накопления наночастиц оксида железа в глиоме.
РАСКРЫТИЕ ИЗОБРЕТЕНИЯ
Задачей, решаемой авторами настоящего изобретения, является разработка способа диагностики мультиформной глиобластомы с помощью метода МРТ, а также разработка контрастного вещества для проведения МРТ-исследования. Технический результат заключается в повышении достоверности и информативности диагностики за счет повышения контрастности областей, соответствующих тканям мультиформной глиобластомы, ее сосудов и очагов неоангиогенеза на МР-снимках.
Поставленная задача решается тем, что при введении магнитных наночастиц оксида железа с гидродинамическим диаметром менее 150 нм, их диаметр позволяет им проникать сквозь патологический ГЭБ вокруг опухоли и проникать в сосуды, питающие ее, а за счет конъюгации с антителами к фактору росту эндотелия сосудов, повышается их тропность к клеткам, экспрессирующим VEGF, и происходит их накопление в областях, соответствующих сосудам и очагам неоангиогенеза. В свою очередь, локальное изменение магнитного поля, создаваемое ими в области их накопления, за счет положительной магнитной восприимчивости может быть выявлено с помощью MP-томографии в режиме, обеспечивающем получение взвешенного по магнитной восприимчивости изображения исследуемого участка.
Поставленная задача решается также тем, что для диагностики мультиформной глиобластомы проводят МРТ-исследование до и после внутривенного введения контрастного вещества, в качестве которого используют магнитные наночастицы оксида железа, стабилизированные биосовместимым полимером и конъюгированные с моноклональными антителами к фактору роста эндотелия сосудов, имеющие гидродинамический диаметр менее 150 нм, при этом МРТ-исследование проводят в режиме, обеспечивающем получение взвешенного по магнитной восприимчивости изображения исследуемого участка, а вывод о наличии мультиформной глиобластомы делают по результатам сравнения MP-снимков до и после введения контрастного вещества согласно областям уменьшения яркости изображения на МР-снимках.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому после введения контрастного вещества МРТ-исследование проводят в течение времени циркуляции контрастного вещества в крови.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому после введения контрастного вещества МРТ-исследование проводят в течение времени, достаточного для накопления контрастного вещества в ткани мультиформной глиобластомы.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому после введения контрастного вещества МРТ-исследование проводят в течение времени циркуляции контрастного вещества в крови и в течение времени, достаточного для накопления контрастного вещества в ткани мультиформной глиобластомы.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому МРТ-исследование проводят в течение 15 мин- 4 ч.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому МРТ-исследование проводят в течение 6-72 ч.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому контрастное вещество вводят в количестве, эквивалентном дозе ионов железа, равной 6-14 мг/кг веса пациента.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому в процессе исследования осуществляют визуализацию сосудов глиобластомы, а вывод о наличии мультиформной глиобластомы делают по выявлению областей с повышенной плотностью сосудов.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому в процессе исследования осуществляют визуализацию очагов неоангиогенеза глиобластомы.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому в качестве биосовместимого полимера используют полимер, выбранный из группы, включающей бычий сывороточный альбумин, человеческий сывороточный альбумин и сополимер полиэтиленгликоля с декстраном.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому в качестве моноклональных антител используют препарат Bevacizumab.
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому в качестве режима, обеспечивающего получение взвешенного по магнитной восприимчивости изображения, используют режим Sucseptibility Wieghted Imaging (SWI).
Частным вариантом настоящего изобретения является упомянутый выше способ, согласно которому МРТ-исследование проводят при следующих параметрах: время повтора импульса 33 мс, время эхо 19 мс, кол-во повторов 1, Тип 3D, толщина среза 0,5 мм, параметры матрицы 320×320 пикселей, параметры поля снимка 45×32 мм, суммарное время исследования 2 мин 58 с.
Согласно настоящему изобретению МРТ-исследование проводят в режиме, обеспечивающем получение взвешенного по магнитной восприимчивости изображения исследуемого участка. Частным примером такого режима является режим SWI-Susceptibility weighted imaging (Haacke, E., et al., Susceptibility weighted imaging (SWI). Magnetic Resonance in Medicine, 2004: p.612-618). Сущность режима заключается в получении двух снимков, один из которых взвешен по амплитуде сигнала, а второй является фазовым изображением и показывает, насколько сильно изменяется фаза электромагнитной волны принимаемого сигнала. Далее происходит наложение второго изображения на первое таким образом, что областям с фазой, отличающейся в меньшую сторону, соответствует область уменьшения яркости (негативная фазовая маска), а областям с фазой, отличающейся в большую сторону, соответствует область увеличения яркости. Этот режим входит в пакет режимов, поставляемых с томографами фирмы Siemens, с напряженностью магнитного поля более 1 Тл, в частности приборы MAGNETOM Spectra, MAGNETOM Spyra. Режим SWI является наиболее чувствительным к локальному изменению магнитной восприимчивости магнитного поля.
Согласно настоящему изобретению для проведения МРТ-исследования могут также быть использованы аналогичные режимы, обеспечивающие получение взвешенного по магнитной восприимчивости изображения. В качестве «моноклональных антител к фактору роста эндотелия сосудов» могут быть использованы любые антитела, обладающие способностью связываться с фактором роста эндотелия сосудов. Перечень таких антител и способы их получения хорошо известны специалисту в данной области техники и не ограничиваются приведенными ниже примерами.
Например, в качестве таких антител может быть использован препарат Bevacizumab (Avastin), выпускаемый фирмой Roche, который представляет собой гуманизированное моноклональное антитело к фактору роста эндотелия сосудов. Также подобные антитела могут быть приобретены у ряда фирм, в частности Abcam (http://www.abcam.com/VEGF-antibodv-11B5-ab38909.html) или Abnova (http://www.abnova.com/products/products_detail.asp?Catalog_id=H00007422-M05).
Перечень биосовместимых полимеров, которыми могут быть стабилизированы магнитные наночастицы оксида железа, не ограничен каким-либо специальным образом. Для проведения МРТ-исследования могут быть использованы наночастицы, покрытые биосовместимым полимером. Например, известен препарат Clariscan (Amrsham Health), представляющий собой магнитные наночастицы, покрытые полиэтиленгликолем.
Известно также использование хитозана для стабилизации магнитных наночастиц (Alejandro Lopez-Cruz, Carola Barrera, Victoria L. Calero-DdelCand Carlos Rinaldi Water dispersible iron oxide nanoparticles coated with covalently linked chitosan, J. Mater. Chem., 2009, Vol.19, P.6870-6876).
При этом использование белков, а в частности альбумина, для стабилизации магнитных наночастиц более предпочтительно, так как альбумины - это консервативные белки, имеющие высокую степень гомологии между видами, тем самым снижается возможность аллергической реакции при внутривенном введении. Кроме того, в молекулах белка присутствует большое число разнообразных функциональных групп, что значительно упрощает проведение любых дальнейших модификаций полученной системы.
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
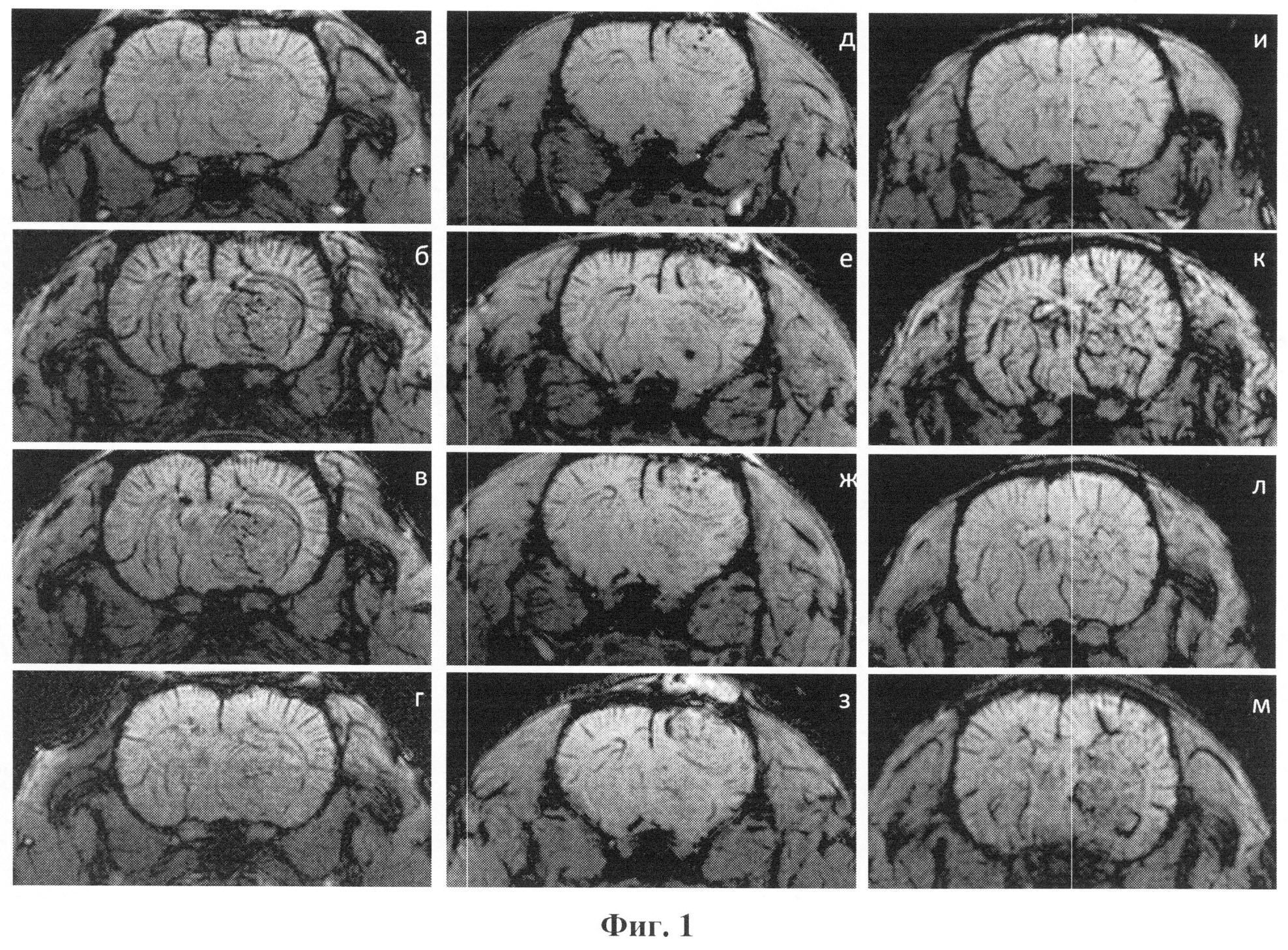
Изобретение поясняется Фигурой 1, на которой показаны МР-снимки в режиме SWI головного мозга крыс с экспериментальной глиомой С6 до (а, д, и) внутривенного введения МНЧ-БСА-IgG (левый ряд), препарата Feridex (средний ряд), МНЧ-БСА-МАб-VEGF (правый ряд), через 5 мин (б, е, к), 2 ч (в, ж, л), 24 ч (г, з, м).
ОСУЩЕСТВЛЕНИЕ ИЗОБРЕТЕНИЯ
Пример 1. Синтез магнитных наночастиц.
Для получения магнитных наночастиц использовано термическое разложение ацетилацетоната железа (III) в бензиловом спирте. Синтез НЧ проводили в трехгорлой заполненной азотом колбе с обратным водяным холодильником, термометром и газовым инжектором. В колбу помещали 45 мл бензилового спирта и 2,18 г ацетилацетоната железа (III). Затем при постоянном перемешивании реакционную смесь продували азотом и медленно нагревали до температуры 383 К, после чего выдерживали 1 ч при данной температуре для выпаривания воды из раствора. Затем температуру реакционной смеси со скоростью 25 град/ч поднимали до 473 К и выдерживали при данной температуре 40 ч. Через 40 ч реакционную смесь медленно охлаждали до комнатной температуры, добавляли 90 мл безводного ацетона и отделяли НЧ центрифугированием при 2000 g в течении 10 мин Полученный осадок дважды промывали избытком ацетона после чего высушивали на роторном испарителе до полного удаления ацетона. Диаметр полученных наночастиц составил, согласно данным просвечивающей электронной микроскопии, (14±4) нм.
Пример 2.Стабилизация магнитных наночастиц.
Для стабилизации водных коллоидных растворов наночастиц оксида железа использовали бычий сывороточный альбумин. Для этого к 10 мг частиц добавляли 5 мл дистиллированной воды и доводили pH до 11 1М раствором NaOH. Затем полученную дисперсию обрабатывали ультразвуком в течение 10 мин и добавляли к ней 40 мг полимера, растворенного в 5 мл воды. Полученную смесь инкубировали 4 ч при комнатной температуре и постоянном перемешивании, затем диализовали против дистиллированной воды и добавляли 500 мкл 1М NaOH, а затем по каплям при перемешивании 2,3 мл 25%-ного водного раствора глутарового альдегида. Полученную смесь инкубировали при перемешивании 15 мин, а затем добавляли 500 мкл 3 M глицина с pH 9,2 для связывания непрореагировавших альдегидных групп. К полученному раствору добавляли 1 мл раствора боргидрида натрия в PBS концентрацией 2 мг/мл. Затем инкубировали 60 мин. Для отделения НЧ, покрытых БСА (МНЧ-БСА) от избытка белка, раствор НЧ пропускали через целлюлозные центрифужные фильтры с диаметром пор 100 кДа. Затем полученные осадок ресуспендировали в воде и опять подвергали фильтрации. Процедуру повторяли до полного исчезновения белка в промывочной жидкости. Очистку белка от продуктов молекулярной сшивки проводили с помощью гель-фильтрации на носителе Sepharose CL-6B (высота и диаметр колонки 50 и 2,5 см соответственно, скорость потока 0,7 мл/мин).
Пример 3. Получение конъюгатов магнитных наночастиц с моноклональными антителами к фактору роста эндотелия сосудов.
К 0,5 мл раствора антител к фактору роста эндотелия сосудов, полученных в отделе фундаментальной и прикладной нейробиологии ФГБУ ГНЦССП им. В.П. Сербского, в 0,1 М карбонатном буфере pH 8,6 (50 мкг/мл) добавляли 2 мкл 14 мМ раствора реагента Траута и инкубировали 1 ч при комнатной температуре. От избытка реагента антитела отделяли с помощью гель-проникающей хроматографии на Сефадексе G-25. Затем к полученному раствору добавляли 25 мкл раствора аминополиэтиленгликоль-7500-малеимида (NH2-ПЭГ-MAL) в ДМСО с концентрацией 4 мг/мл и инкубировали 4 ч при +4°C. Для активации карбоксильных групп к 10 мл раствора НЧ, покрытых БСА в фосфатно-солевом буфере (0,45 мг/мл), добавляли 12 мкл водорастворимого карбодиимида (N-(3-диметиламинопропил)-N'-этилкарболиимидгидрохлорид) (2 мг/мл) и 20 мкл водного раствора N-гидроксисукцинимида (1,5 мг/мл). Далее добавляли полученный раствор модифицированных антител к НЧ и инкубировали 12 ч при температуре +4°C. Разделение векторных НЧ и несвязавшихся антител проводили методом гель-хроматографии на колонке с Сефарозой CL-4В. Длина колонки 40 см, диаметр 2,5 см, скорость потока 0,5 мл/мин.
Пример 4. Визуализация экспериментальной глиомы С6 с помощью МРТ в режиме SWI после внутривенного введения магнитных наночастиц, покрытых БСА и коньюгированных с моноклональными антителами к фактору роста эндотелия сосудов.
Эксперименты проводили на животных с экспериментальной моделью глиомы C6. Для визуализации глиомы животным вводили внутривенно раствор НЧ, конъюгированных с антителами к VEGF (МНЧ-БСА-MAb-anti-VEGF), а также с антителами к Сх43 (MH4-BCA-MAb-anti-Cx43). В качестве контроля использовали МНЧ-БСА, конъюгированные с неспецифическими иммуноглобулинами мыши IgG (МНЧ-БСА-IgG), а также коммерческий препарат Feridex (Guerbet, Advanced Magnetics). Введенная доза МНЧ в пересчете на концентрацию железа составляла 10 мг/кг. МРТ-сканирование проводили на томографе Clinscan 7T фирмы Bruker в режиме SWI с параметрами, перечисленными вТаблице 1.
|
Авторами настоящего изобретения было показано, что после введения полученных магнитных наночастиц становится возможным визуализировать границы и сосуды опухоли с помощью МРТ-исследования в режиме SWI через 5 мин после введения. Как видно из Фиг.1, до введения препарата магнитных наночастиц МРТ в режиме SWI не позволяет визуализировать все сосуды опухоли, тогда как через 5 мин после внутривенного введения магнитных наночастиц визуализируются области уменьшения яркости изображения, соответствующие сосудам, в которых повышена концентрация магнитных наночастиц. Подобный эффект достигает максимума непосредственно после введения магнитных наночастиц, затем происходит постепенное возвращение интенсивности к норме, что связано с постепенным понижением концентрации магнитных наночастиц за счет их выведения их кровотока. Тем не менее, визуализация сосудов остается возможной спустя 2 ч после введения магнитных наночастиц. Через 24 ч становится возможным визуализация тех тканей, где наблюдается повышенное содержание фактора роста эндотелия сосудов, который является проангиогенным фактором и способствует росту опухоли в наибольшей степени. Таким образом, с помощью предложенного способа диагностики удается не только визуализировать опухоль, но и определить ее наиболее активно развивающуюся часть.