Результат интеллектуальной деятельности: ПРОИЗВОДНЫЕ 1, 2-ДИГИДРОЦИКЛОБУТЕНДИОНА В КАЧЕСТВЕ ИНГИБИТОРОВ ФОСФОРИБОЗИЛТРАНСФЕРАЗЫ НИКОТИНАМИДА
Вид РИД
Изобретение
Область техники
Данное изобретение относится к производным 1,2-дигидроциклобутендиона и, в частности, производным 3,4-диаминоциклобут-3-ен-1,2-диона, которые применяют для ингибирования фермента фосфорибозилтрансферазы никотинамида (ФРТНАМ), и к медицинскому применению таких производных 1,2-дигидроциклобутендиона.
Уровень техники
Ингибирование фермента фосфорибозилтрансферазы никотинамида (ФРТНАМ) дает ингибирование NF-kB, ингибирование NF-kB является результатом снижения клеточных концентраций никотинамид-аденин-динуклеотида (НАД) (Beauparlant et al (2007) AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics, 2007 Oct 22-26 Abstract nr A82; и Roulson et al (2007) AACR-NCI-EORTC International Conference on Molecular Targets and Cancer Therapeutics, 2007 Oct 22-26 Abstract nr A81). Опухолевые клетки характеризуются повышенной экспрессией ФРТНАМ и высокой скоростью обновления НАД из-за высокой активности АДФ-рибозилирования, требуемого для восстановления ДНК, стабильности генома и поддержания теломера, что делает их более чувствительными к ингибированию ФРТНАМ, чем обычные клетки. Это также является разумным объяснением для применения соединений в соответствии с данным изобретением в сочетании с агентами, повреждающими ДНК, для последующих клинических испытаний.
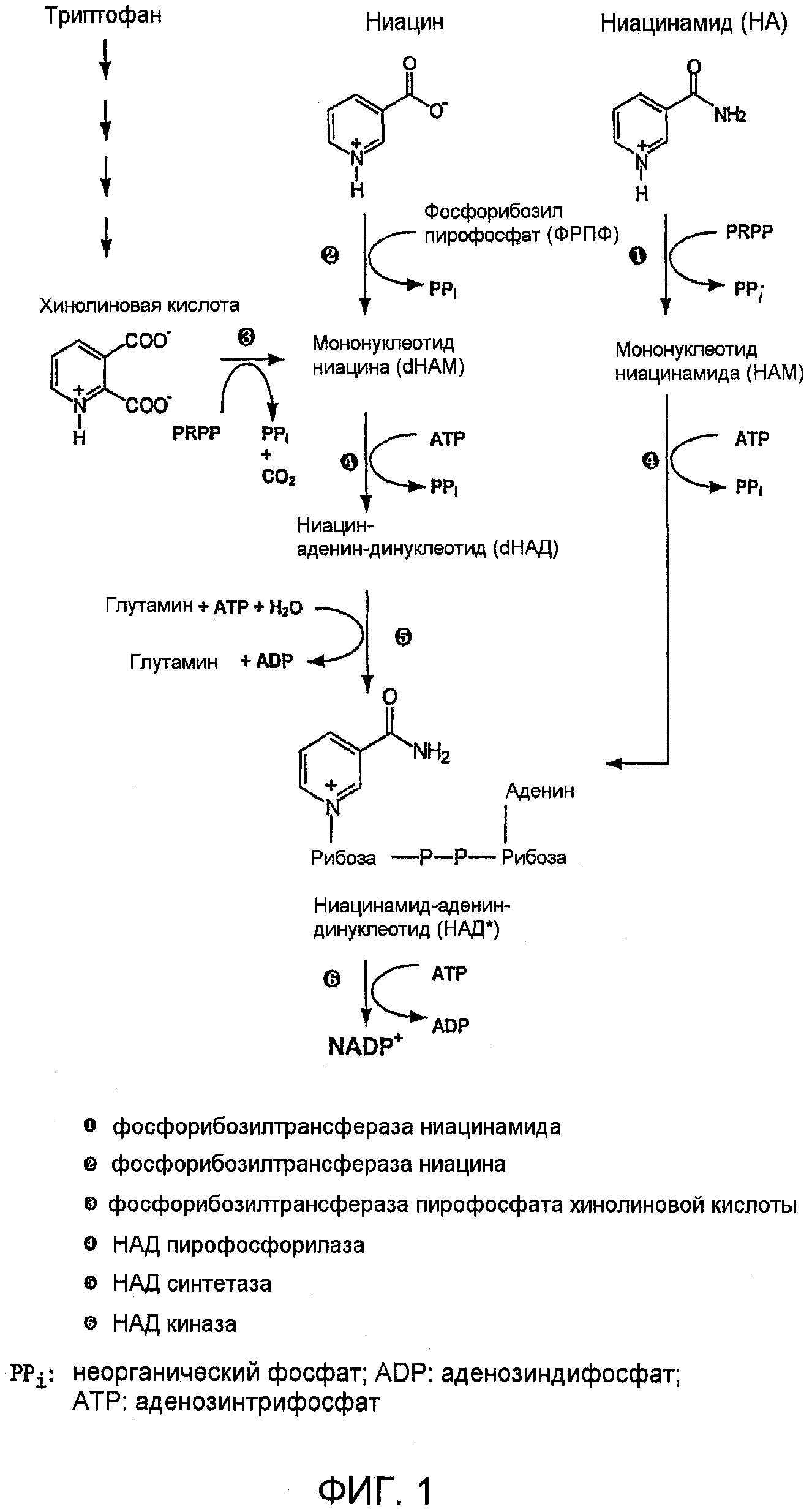
Пути биосинтеза НАД показаны на фиг. 1.
ФРТНАМ вовлечена в биосинтез никотинамид-аденин-динуклеотида (НАД) и НАД(Ф). НАД может быть синтезирован у млекопитающих тремя различными путями, начиная либо с триптофана через хинолиновую кислоту, с никотиновой кислоты (ниацина) или с никотинамида (ниацинамида).
Хинолиновая кислота взаимодействует с фосфорибозилпирофосфатом с получением мононуклеотида ниацина (dНАМ) с применением фермента фосфорибозилтрансферазы хинолиновой кислоты ❸, который найден в печени, почках и мозге.
Никотиновая кислота (ниацин) взаимодействует с ФРФФ с получением мононуклеотида ниацина (dНАМ), с применением фермента фосфорибозилтрансферазы ниацина ❷, который широко распространен в различных тканях.
Никотинамид (ниацинамид) взаимодействует с ФРФФ с получением мононуклеотида ниацинамида (НАМ) с применением фермента фосфорибозилтрансферазы никотинамида (ФРТНАМ) ❶, который также широко распространен в тканях.
Последующее добавление аденозинмонофосфата к мононуклеотидам дает образование соответствующих динуклеотидов; мононуклеотид ниацина и мононуклеотид ниацинамида взаимодействуют с АТФ с получением ниацин-аденин-динуклеотида (dНАД) и ниацинамид-аденин-динуклеотида (НАД), соответственно. Обе реакции, хотя они проходят различными путями, катализированы одним и тем же ферментом, НАД пирофосфорилазой ❹.
Следующая стадия амидирования требуется для превращения ниацин-аденин-динуклеотида (dНАД) в ниацинамид-аденин-динуклеотид (НАД). Ферментом, который катализирует эту реакцию, является синтетаза НАД ❺. НАД является непосредственным предшественником фосфата ниацинамид-аденин-динуклеотида (НАД(Ф)). Реакцию катализируют НАД киназой. Подробное описание см., например, в Cory J. G. Purine and pyrimidine nucleotide metabolism In: Textbook of Biochemistry and Clinical Correlations 3rd edition ed. Devlin, T, Wiley, Brisbane 1992, p. 529-574.
Нормальные клетки обычно используют оба предшественника, ниацин и ниацинамид, для синтеза НАД(Ф) и во многих случаях дополнительно триптофан или его метаболиты. Следовательно, мышиные глиозные клетки используют ниацин, ниацинамид и хинолиновую кислоту (Grant et al. (1998) J. Neurochem. 70: 1759- 1763). Человеческие лимфоциты используют ниацин и ниацинамид (Carson et al. (1987) J. Immunol. 138: 1904-1907; Berger et al (1982) Exp. Cell Res. 137; 79-88). Клетки печени крысы используют ниацин, ниацинамид и триптофан (Yamada et al. (1983) Int. J. Vit. Nutr. Res. 53: 184-1291; Shin et al (1995) Int. J. Vit. Nutr. Res. 65: 143-146; Dietrich (1971) Methods Enzymol. 18B; 144-149). Человеческие эритроциты используют ниацин и ниацинамид (Rocchigiani et al. (1991) Purine and pyrimidine metabolism in man VII Part B ed. Harkness et al. Plenum Press New York, p.337-3490). Лейкоциты морских свинок используют ниацин (Flechner et al. (1970), Life Science 9: 153-162).
НАД(Ф) вовлечен во множество биохимических реакций, которые жизненно важны для клеток и поэтому тщательно исследуются. Роль НАД(Ф) в развитии и росте опухолей также изучается. Было обнаружено, что многие опухолевые клетки используют ниацинамид для клеточного синтеза НАД(Ф). Ниацин и триптофан, которые являются альтернативными предшественниками во многих нормальных типах клеток, не могут использоваться опухолевыми клетками или, по крайней мере, не до такой степени, которая достаточна для выживания клетки. Селективное ингибирование фермента, который находится только на пути ниацинамида (такого как ФРТНАМ), может составлять основу выбора лекарственных средств, специфичных к опухоли. Это подтверждается ингибитором ФРТНАМ APO866 (см. Hasmann and Schemainda, Cancer Res 63(21): 7463-7442).
Известно, что различные производные 3,4-диаминоциклобут-3-ен-1,2-диона, замещенные определенным образом, имеют фармакологически полезные свойства. В частности известно, что определенные производные обладают антипролиферативным действием. Все такие соединения, однако, структурно не похожи на соединения в соответствии с данным изобретением.
Соединения, содержащие 3,4-диаминоциклобут-3-ен-1,2-дионовые группы, описаны в следующих публикациях:
Применение в качестве открывателей калиевых каналов: J. Med. Chem. (2000) 43: 1187, J. Med. Chem (2000) 43: 1203, WO 02/062761.
Применение в качестве релаксантов гладких мышц: WO 96/15103, WO 96/14300, WO 95/14005, US 5532245.
Применение в качестве связующих агентов с рецепторов хемокина: WO 02/083624.
Применение в качестве связующих агентов с рецептором интегрина: WO 00/035864, US 6420396, WO 01/47867, WO 02/04426, WO 02/10136, WO 02/42264, US 6677360.
Применение в качестве противораковых агентов: WO 02/083624, EP 1674457 Al.
СУЩНОСТЬ ИЗОБРЕТЕНИЯ
Полагают, что новые соединения в соответствии с данным изобретением действуют на фермент фосфорибозилтрансфераза никотинамида (ФРТНАМ) и что нисходящее ингибирование NF-kB является результатом снижения концентраций в клетках никотинамид-аденин-динуклеотида (НАД).
Следовательно, в данном изобретении представлены соединения общей формулы (I) по пункту 1 и применение этих соединений в медицине, см. пункты 19, 20, 22 и 23.
Ингибиторы фермента ФРТНАМ могут применяться в лечении рака (WO 97/48696), для подавления иммунитета (WO 97/48397), для лечения заболеваний, в которые вовлечен ангиогенез (WO 03/80054), для лечения ревматоидного артрита или септического шока (WO 08/025857), для профилактики и лечения ишемии (PCT/EP2009/052572) или для профилактики и лечения диабетической нефропатии (Song et al. [2008] AJP - Renal Physiology 295 F1485-F1494).
КРАТКОЕ ОПИСАНИЕ ЧЕРТЕЖЕЙ
На фиг. 1 показан путь биосинтеза НАД (из Biedermann E. et al, WO 00/50399).
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Соединения в соответствии с данным изобретением
Данное изобретение относится к определенным производным 1,2-дигидроциклобутендиона, которые применяются для ингибирования фермента фосфорибозилтрансферазы никотинамида (ФРТНАМ).
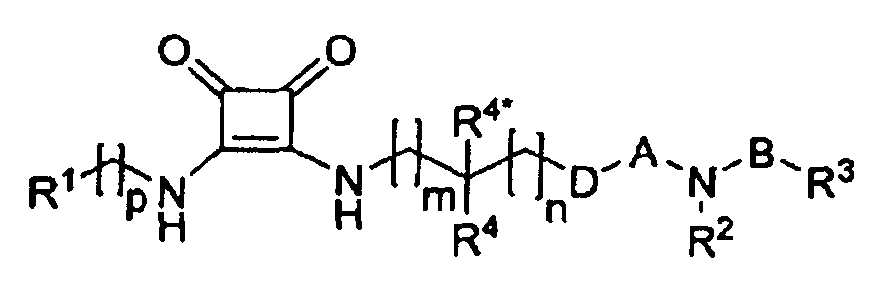
Данное изобретение относится к соединениям формулы (I)
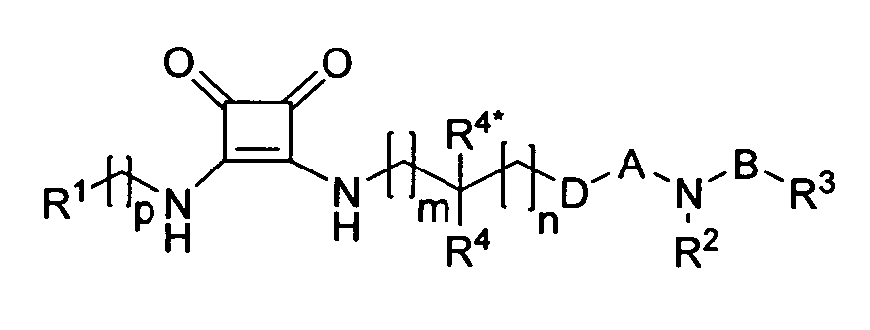
где
A выбирают из -C(=O)-, -S(=O)2-, -C(=S)- и -P(=O)(R5)-, где R5 выбирают из C1-6-алкила, C1-6-алкокси и гидрокси;
B выбирают из одинарной связи, -O-, -NR6- и -C(=O)-NR6-, где R6 выбирают из водорода, необязательно замещенного C1-12-алкила, необязательно замещенного C1-12-алкенила, необязательно замещенного арила, необязательно замещенного гетероциклила и необязательно замещенного гетероарила;
D выбирают из одинарной связи, -O-, -CR7R8- и -NR9, где R7, R8 и R9 независимо выбирают из водорода, необязательно замещенного C1-12-алкила, необязательно замещенного C1-12-алкенила, необязательно замещенного арила, необязательно замещенного гетероциклила и необязательно замещенного гетероарила;
m равно целому числу 0-12 и n равно целому числу 0-12, где сумма m+n равна 1-20;
p равно целому числу 0-2;
R1 выбирают из необязательно замещенного гетероарила и необязательно замещенного арила;
R2 выбирают из водорода, необязательно замещенного C1-12-алкила, необязательно замещенного C3-12-циклоалкила, -[CH2CH2O]1-10-(необязательно замещенного C1-6-алкила), необязательно замещенного C1-12-алкенила, необязательно замещенного арила, необязательно замещенного гетероциклила и необязательно замещенного гетероарила; и R3 выбирают из необязательно замещенного C1-12-алкила, необязательно замещенного C3-12-циклоалкила, -[CH2CH2O]1-10-(необязательно замещенного C1-6-алкила), необязательно замещенного C1-12-алкенила, необязательно замещенного арила, необязательно замещенного гетероциклила и необязательно замещенного гетероарила; или R2 и R3 вместе с промежуточными атомами (т.е. -N-B-) образуют необязательно замещенное N-содержащее гетероциклическое или гетероароматическое кольцо;
каждый из R4 и R4* независимо выбирают из водорода, необязательно замещенного C1-12-алкила и необязательно замещенного C1-12-алкенила;
и их фармацевтически приемлемые соли и их пролекарства.
Определения
В данном контексте термины "C1-12-алкил" и "C1-6-алкил" означают линейную, циклическую или разветвленную углеводородную группу, имеющую от 1 до 12 атомов углерода и от 1 до 6 атомов углерода, соответственно, такую как метил, этил, пропил, изопропил, циклопропил, бутил, изобутил, втор-бутил, циклобутил, пентил, циклопентил, гексил и циклогексил.
Хотя термин "C3-12-циклоалкил" включен в термин "C1-12-алкил", он относится конкретно к моно- и бициклическим соединениям, включая алкильные группы, имеющие экзоциклические атомы, например циклогексилметил.
Также, термины "C2-12-алкенил" и "C2-6-алкенил" включают линейные, циклические или разветвленные группы, имеющие от 2 до 12 атомов углерода и от 2 до 6 атомов углерода, соответственно, и содержащие (по крайней мере) одну ненасыщенную связь. Примеры алкенильных групп включают винил, аллил, бутенил, пентенил, гексенил, гептенил, октенил, гептадекаенил. Предпочтительными примерами алкенила являются винил, аллил, бутенил, особенно аллил.
Хотя термин "C3-12-циклоалкенил" включен в термин "C2-12-алкенил", он относится конкретно к моно- и бициклическим соединениям, включая алкенильные группы, имеющие экзоциклические атомы, например циклогексенилметил и циклогексилаллил.
В данном контексте, т.е. в сочетании с терминами "алкил", "циклоалкил", "алкокси", "алкенил", "циклоалкенил" и подобными, термин "необязательно замещенный" означает, что рассматриваемая группа может быть замещена один или несколько раз, предпочтительно, 1-3 раза, группой(ами), выбранными из гидрокси (которая, будучи связанной с ненасыщенным атомом углерода, может быть представлена в таутомерной кетоформе), C1-6-алкокси (т.е. C1-6-алкилокси), C2-6-алкенилокси, карбокси, оксо (образующей кето или альдегидную функциональность), C1-6-алкоксикарбонила, C1-6-алкилкарбонила, формила, арила, арилокси, ариламино, арилкарбонила, арилоксикарбонила, арилкарбонилоксила, ариламинокарбонила, арилкарбониламино, гетероарила, гетероарилокси, гетероариламино, гетероарилкарбонила, гетероарилоксикарбонила, гетероарилкарбонилокси, гетероариламинокарбонила, гетероарилкарбониламино, гетероциклила, гетероциклилокси, гетероциклиламино, гетероциклилкарбонила, гетероциклилоксикарбонила, гетероциклилкарбонилокси, гетероциклиламинокарбонила, гетероциклилкарбониламино, амино, моно- и ди(C1-6-алкил)амино, -N(C1-4-алкила)3 +, карбамоил, моно- и ди(C1-6-алкил)аминокарбонила, C1-6-алкилкарбониламино, циано, гуанидино, карбамидо, C1-6-алкилсульфониламино, арилсульфониламино, гетероарилсульфониламино, C1-6-алканоилокси, C1-6-алкилсульфонила, C1-6-алкилсульфинила, C1-6-алкилсульфонилокси, нитро, C1-6-алкилтио и галогена, где любой арил, гетероарил и гетероциклил могут быть замещены, как описано ниже для арила, гетероарила и гетероциклила, и любой алкил, алкокси и подобные, являющиеся заместителями, могут быть замещены гидрокси, C1-6-алкокси, амино, моно- и ди(C1-6-алкил)амино, карбокси, C1-6-алкилкарбониламино, C1-6-алкиламинокарбонилом или галогеном.
Обычно заместители выбирают из гидрокси (которая, будучи связанной с ненасыщенным атомом углерода, может быть представлена в таутомерной кетоформе), C1-6-алкокси (т.е. C1-6-алкилокси), C2-6-алкенилокси, карбокси, оксо (образующей кето или альдегидную функциональность), C1-6-алкилкарбонила, формила, арила, арилокси, ариламино, арилкарбонила, гетероарила, гетероарилокси, гетероариламино, гетероарилкарбонила, гетероциклила, гетероциклилокси, гетероциклиламино, гетероциклилкарбонила, амино, моно- и ди(C1-6-алкил)амино; карбамоила, моно- и ди(C1-6-алкил)аминокарбонила, амино-C1-6-алкиламинокарбонила, моно- и ди(C1-6-алкил)амино-C1-6-алкиламинокарбонила, C1-6-алкилкарбониламино, гуанидино, карбамидо, C1-6-алкилсульфониламино, C1-6-алкилсульфонила, C1-6-алкилсульфинила, C1-6-алкилтио, галогена, где любой арил, гетероарил и гетероциклил могут быть замещены, как описано ниже для арила, гетероарила и гетероциклила.
В некоторых вариантах заместители выбирают из гидрокси, C1-6-алкокси, амино, моно- и ди(C1-6-алкил)амино, карбокси, C1-6-алкилкарбониламино, C1-6-алкиламинокарбонила или галогена.
Термин "галоген" включает фтор, хлор, бром или йод.
В данном контексте термин "арил" означает полностью или частично ароматическое карбоциклическое кольцо или систему колец, такую как фенил, нафтил, 1,2,3,4-тетрагидронафтил, антрацил, фенантрацил, пиренил, бензопиренил, флуоренил и ксантенил, где предпочтительным примером является фенил.
Термин "гетероарил" означает полностью или частично ароматическое карбоциклическое кольцо или систему колец, где один или более атомов углерода замещены гетероатомами, например, азотом (=N- или -NH-), серой и/или кислородом. Примеры таких гетероарильных групп включают оксазолил, изоксазолил, тиазолил, изотиазолил, пирролил, имидазолил, пиразолил, пиридинил, пиримидинил, пиразинил, пиридазинил, триазинил, кумарил, фуранил, тиенил, хинолил, бензотиазолил, бензотриазолил, бензодиазолил, бензооксазолил, фталазинил, фталанил, триазолил, тетразолил, изохинолил, акридинил, карбазолил, дибензазепинил, индолил, бензопиразолил, феноксазонил. Особенно интересными гетероарильными группами являются бензимидазолил, оксазолил, изоксазолил, тиазолил, изотиазолил, пирролил, имидазолил, пиразолил, пиридинил, пиримидинил, пиразинил, пиридазинил, фурил, тиенил, хинолил, триазолил, тетразолил, изохинолил, индолил, в частности, бензимидазолил, пирролил, имидазолил, пиридинил, пиримидинил, фурил, тиенил, хинолил, тетразолил и изохинолил.
Термин "гетероциклил" означает не ароматическое карбоциклическое кольцо или систему колец, где один или более атомов углерода замещены гетероатомами, например, азотом (=N- или -NH-), серой и/или кислородом. Примеры таких гетероциклильных групп (поименованных согласно кольцам) включают имидазолидин, пиперазин, гексагидропиридазин, гексагидропиримидин, диазепан, диазокан, пирролидин, пиперидин, азепан, азокан, азиридин, азирин, азетидин, пирролин, тропан, оксазинан (морфолин), азепин, дигидроазепин, тетрагидроазепин и гексагидроазепин, оксазолан, оксазепан, оксазокан, тиазолан, тиазинан, тиазепан, тиазокан, оксазетан, диазетан, тиазетан, тетрагидрофуран, тетрагидропиран, оксепан, тетрагидротиофен, тетрагидротиопиран, тиепан, дитиан, дитиепан, диоксан, диоксепан, оксатиан, оксатиепан. Наиболее интересными примерами являются тетрагидрофуран, имидазолидин, пиперазин, гексагидропиридазин, гексагидропиримидин, диазепан, диазокан, пирролидин, пиперидин, азепан, азокан, азетидин, тропан, оксазинан (морфолин), оксазолан, оксазепан, тиазолан, тиазинан и тиазепан, в частности тетрагидрофуран имидазолидин, пиперазин, гексагидропиридазин, гексагидропиримидин, диазепан, пирролидин, пиперидин, азепан, оксазинан (морфолин) и тиазинан.
Термин "N-содержащее гетероциклическое или гетероароматическое кольцо" включает кольца, указанные как "гетероциклил" и "гетероарил", соответственно, которые включают один или более гетероатомов, по крайней мере, один из которых является атомом азота. Примеры включают пиперазин, изоксазол, изоксазолидин и морфолин, и т.д.
Термин "N,O-содержащее гетероциклическое или гетероароматическое кольцо" включает кольца, указанные как "гетероциклил" и "гетероарил", соответственно, которые включают два или более гетероатома, два из которых являются соседними атомами азота и кислорода. Примеры включают изоксазол, изоксазолидин, морфолин и т.д.
В данном контексте, т.е. в сочетании с терминами "арил", "гетероарил", "гетероциклил", "N,O-содержащее гетероциклическое или гетероароматическое кольцо" и подобные (например, "арилокси", "гетерарилкарбонил", и т.д.), термин "необязательно замещен" означает, что рассматриваемая группа может быть замещена один или несколько раз, предпочтительно, 1-5 раз, в частности, 1-3 раза, группой(ами), выбранными из гидрокси (которая, если присутствует в енольной системе, может быть представлена в таутомерной кетоформе), C1-6-алкила, C1-6-алкокси, C2-6-алкенилокси, оксо (которая может быть представлена в таутомерной енольной форме), оксида (актуальны только N-оксиды), карбокси, C1-6-алкоксикарбонила, C1-6-алкилкарбонила, формила, арила, арилокси, ариламино, арилоксикарбонила, арилкарбонила, гетероарила, гетероариламино, амино, моно- и ди(C1-6-алкил)амино; карбамоила, моно- и ди(C1-6-алкил)аминокарбонила, амино- C1-6-алкиламинокарбонила, моно- и ди(C1-6-алкил)амино-C1-6-алкиламинокарбонила, C1-6-алкилкарбониламино, циано, гуанидино, карбамидо, C1-6-алканоилокси, C1-6-алкилсульфониламино, арилсульфониламино, гетероарилсульфониламино, C1-6-алкилсульфонила, C1-6-алкилсульфинила, C1-6-алкилсульфонилокси, нитро, сульфанила, амино, аминосульфонила, моно- и ди(C1-6-алкил)аминосульфонила, дигалоген-C1-4-алкила, тригалоген-C1-4-алкила, галогена, где арил и гетероарил, являющиеся заместителями, могут быть замещены 1-3 раза C1-4-алкилом, C1-4-алкокси, нитро, циано, амино или галогеном, и любой алкил, алкокси и подобные, являющиеся заместителями, могут быть замещены гидрокси, C1-6-алкокси, C2-6-алкенилокси, амино, моно- и ди(C1-6-алкил)амино, карбокси, C1-6-алкилкарбониламино, галогеном, C1-6-алкилтио, C1-6-алкилсульфониламино или гуанидино.
Обычно заместители выбирают из гидрокси, C1-6-алкила, C1-6-алкокси, оксо (которая может быть представлена в таутомерной енольной форме), карбокси, C1-6-алкилкарбонила, формила, амино, моно- и ди(C1-6-алкил)амино; карбамоила, моно- и ди(C1-6-алкил)аминокарбонила, амино-C1-6-алкиламинокарбонила, C1-6-алкилкарбониламино, гуанидино, карбамидо, C1-6-алкилсульфониламино, арилсульфониламино, гетероарилсульфониламино, C1-6-алкилсульфонила, C1-6-алкилсульфинила, C1-6-алкилсульфонилокси, сульфанила, амино, аминосульфонила, моно- и ди(C1-6-алкил)аминосульфонила или галогена, где любой алкил, алкокси и подобные, являющиеся заместителями, могут быть замещены гидрокси, C1-6-алкокси, C2-6-алкенилокси, амино, моно- и ди(C1-6-алкил)амино, карбокси, C1-6-алкилкарбониламино, галогеном, C1-6-алкилтио, C1-6-алкилсульфониламино или гуанидино. В некоторых вариантах, заместители выбирают из C1-6-алкила, C1-6-алкокси, амино, моно- и ди(C1-6-алкил)амино, сульфанила, карбокси или галогена, где любой алкил, алкокси и подобные, являющиеся заместителями, могут быть замещены гидрокси, C1-6-алкокси, C2-6-алкенилокси, амино, моно- и ди(C1-6-алкил)амино, карбокси, C1-6-алкилкарбониламино, галогеном, C1-6-алкилтио, C1-6-алкилсульфониламино или гуанидино.
Группы (например, R2 и R3), включающие C3-12-циклоалкил, C3-12-циклоалкенил и/или арил в качестве, по крайней мере, части заместителя, обозначены как содержащие "карбоциклическое кольцо".
Группы (например, R2 и R3), включающие гетероциклил или гетероарил в качестве, по крайней мере, части заместителя, обозначены как содержащие "гетероциклическое кольцо" и "гетероароматическое кольцо", соответственно.
Термин "фармацевтически приемлемые соли" включает кислотно-аддитивные соли и основные соли. Иллюстративные примеры кислотно-аддитивных солей включают фармацевтически приемлемые соли, полученные с нетоксичными кислотами. Примеры таких органических солей включают соли малеиновой, фумаровой, бензойной, аскорбиновой, янтарной, щавелевой, бис-метиленсалициловой, метансульфоновой, этандисульфоновой, уксусной, пропионовой, винной, салициловой, лимонной, глюконовой, молочной, яблочной, миндальной, коричной, цитраконовой, аспартиновой, стеариновой, пальмитиновой, итаконовой, гликолевой, п-аминобензойной, глутаминовой бензолсульфоновой и теофиллинуксусной кислот, а также 8-галотеофиллины, например, 8-бромтеофиллин. Примеры таких неорганических солей включают соли с хлористоводородной, бромистоводородной, серной, сульфаминовой, фосфорной и азотной кислотами. Примеры основных солей включают соли, в которых (оставшийся) противоион выбирают из щелочных металлов, таких как натрий и калий, щелочноземельных металлов, таких как кальций и аммоний (+N(R)3R', где R и R' независимо обозначают необязательно замещенный C1-6-алкил, необязательно замещенный C2-6-алкенил, необязательно замещенный арил или необязательно замещенный гетероарил). Фармацевтически приемлемые соли описаны, например в Remington's Pharmaceutical Sciences, 17. Ed. Alfonso R. Gennaro (Ed.), Mack Publishing Company, Easton, PA, U.S.A., 1985 и более поздних изданиях, и в Encyclopedia of Pharmaceutical Technology. Таким образом, термин "его кислотно-аддитивная соль или щелочная соль" включает такие соли. Более того, соединения, а также любые промежуточные или исходные материалы, могут присутствовать в форме гидрата.
Термин "пролекарство" означает соединение, которое, при помещении в физиологические условия, освобождает производное такого соединения, которое способно оказывать желаемое биологическое действие. Типовые примеры включают нестабильные эфиры (т.е. скрытую гидроксильную группу или скрытую кислотную группу).
Более того, должно быть понятно, что соединения могут присутствовать в виде рацемических смесей или отдельных стереоизомеров, таких как энантиомеры или диастереомеры. Данное изобретение охватывает каждый и все такие возможные стереоизомеры (например, энантиомеры и диастереомеры) а также рацематы и смеси, обогащенные одним из возможных стереоизомеров.
Варианты осуществления
В одном важном варианте осуществления B выбирают из -O- и -NR5-, в частности, B является -O-. В одном из важных вариантов этого варианта осуществления, A является -S(=O)2- и B является -O-. В другом важном варианте этого варианта осуществления, A является-C(=O)- и B является -O-. В этих вариантах осуществления, D предпочтительно является одинарной связью.
В другом варианте осуществления, B является одинарной связью. В одном важном варианте этого варианта осуществления, A является -S(=O)2-.
В другом варианте осуществления, B является -C(=O)-NR5-. В этом варианте осуществления, D предпочтительно выбирают из одинарной связи, -O- и -NR9.
Что касается R1, этот заместитель предпочтительно является необязательно замещенным пиридинилом, в частности, необязательно замещенным пиридин-4-илом. В другом варианте осуществления, R1 является пиридин-3-илом.
Расстояние между R1 и 1,2-дигидроциклобутендионовой группой определяется p. p равно целому числу 0-2, но, предпочтительно, 0-1, в частности, 0.
В особенно интересном варианте осуществления, p равно 0 и R1 является пиридин-4-илом.
Длина разделяющего элемента определяется m и n. Предпочтительно, m равно целому числу 0-10 и n равно целому числу 0-10, где сумма m+n равна 1-12; в частности, m равно целому числу 1- 8 и n равно целому числу 0-3, где сумма m+n равна 3-8. В наиболее предпочтительном варианте, m равно целому числу 2-8 и n равно 0.
Очевидно, что - кроме D, A и B - R2 и R3 (и частично также R4 и R4*) играют важную роль в эффективности соединений в соответствии с данным изобретением. Следовательно, в одном особенно интересном варианте осуществления, по крайней мере, один из R2 и R3 включает карбоциклическое кольцо, гетероциклическое кольцо или гетероароматическое кольцо, или R2 и R3 вместе с промежуточными атомами образуют необязательно замещенное N-содержащее гетероциклическое или гетероароматическое кольцо.
В одном варианте, R2 и R3 вместе с промежуточными атомами образуют необязательно замещенное N,O-содержащее гетероциклическое или гетероароматическое кольцо.
Более того, R4 предпочтительно выбирают из водорода, C1-6-алкила и необязательно замещенного бензила, и R4* является водородом.
В одном особенно важном варианте осуществления,
A выбирают из -C(=O)- и -S(=O)2-;
B является -O-;
D выбирают из одинарной связи, -O- и -NR9
m равно целому числу 2-8 и n равно 0;
R2 выбирают из водорода, необязательно замещенного C3-12-циклоалкила, -[CH2CH2O]1-10-(необязательно замещенного C1-6-алкила), -(CH2)0-2-(необязательно замещенного арила), -(CH2)0-2-(необязательно замещенного гетероарила) и -(CH2)0-2-(необязательно замещенного гетероциклила);
R3 выбирают из необязательно замещенного C3-12-циклоалкила, -[CH2CH2O]1-10-(необязательно замещенного C1-6-алкила), необязательно замещенного C1-12-алкенила, необязательно замещенного арила, необязательно замещенного гетероциклила и необязательно замещенного гетероарила;
R4 выбирают из водорода, необязательно замещенного C3-12-циклоалкила, -(CH2)0-2-(необязательно замещенного арила), -(CH2)0-2-(необязательно замещенного гетероарила) и -(CH2)0-2-(необязательно замещенного гетероциклила); и
R4 является водородом.
Наиболее интересные соединения включают соединения, выбранные из соединений 1001-1181, описанных ниже:
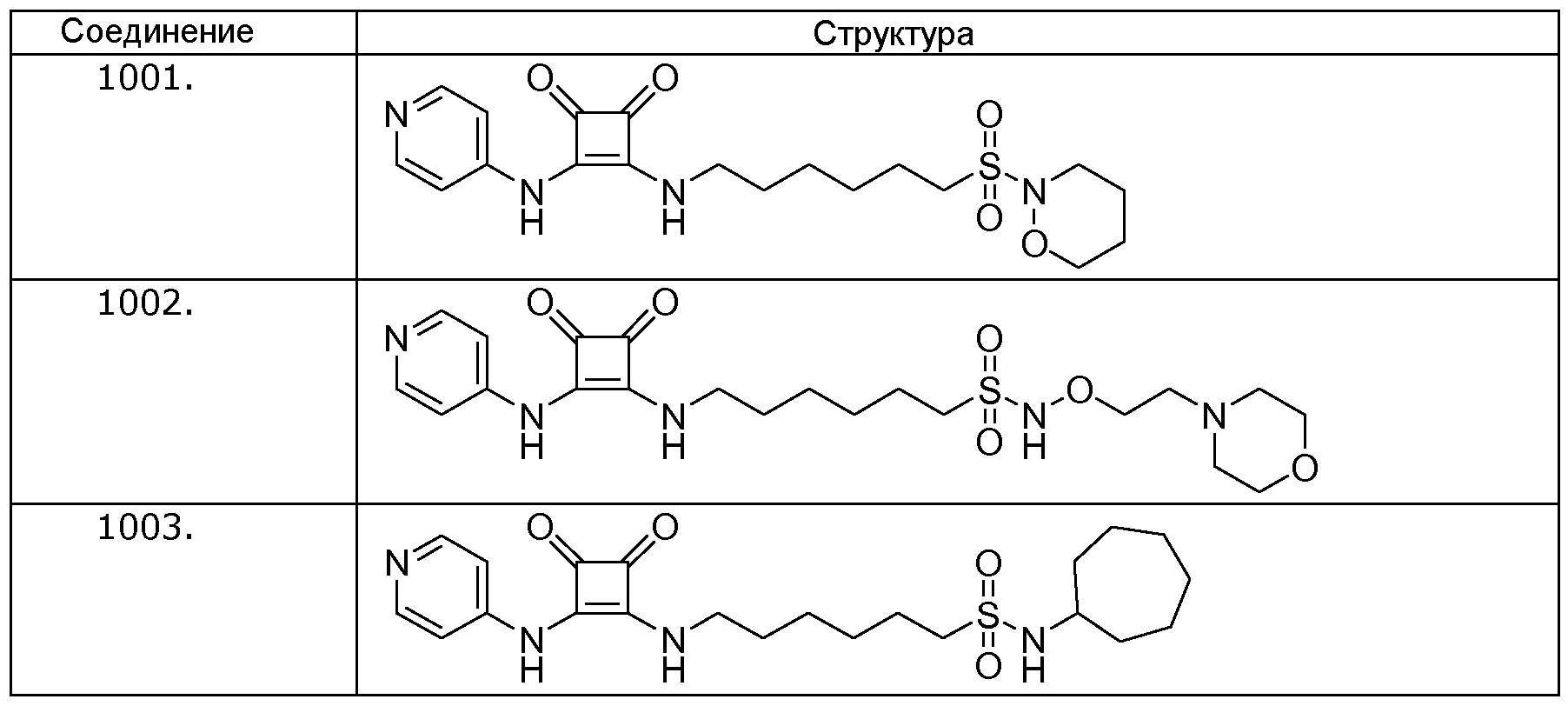
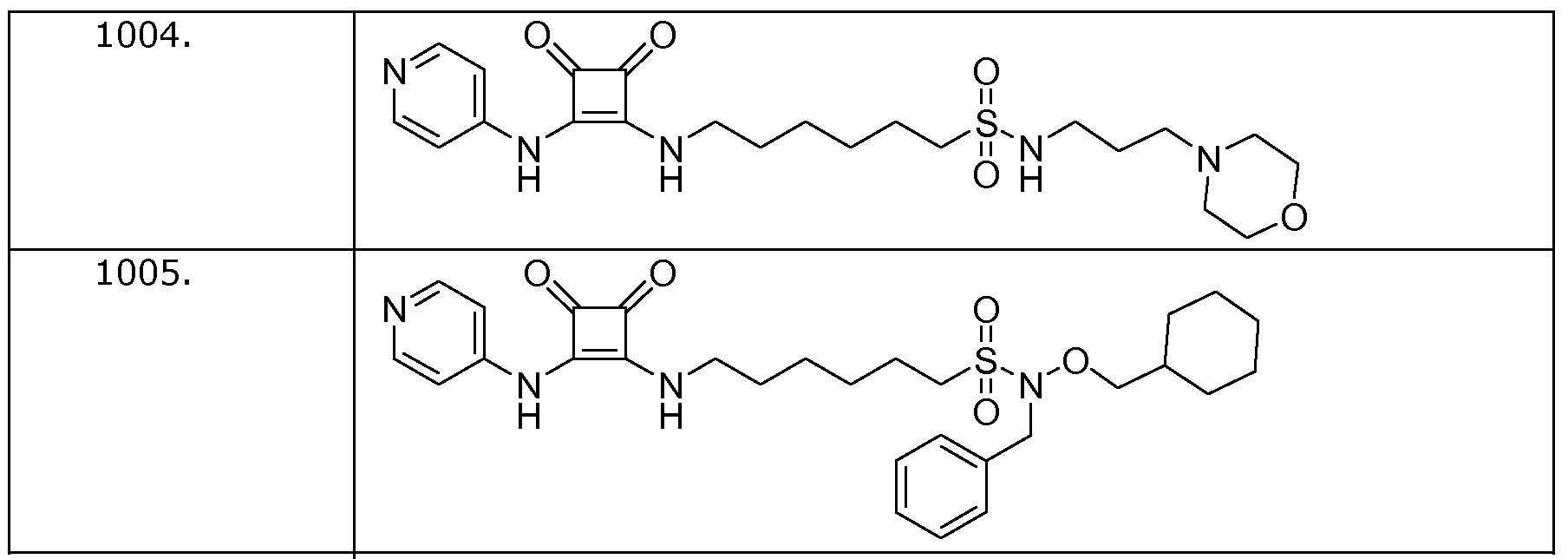
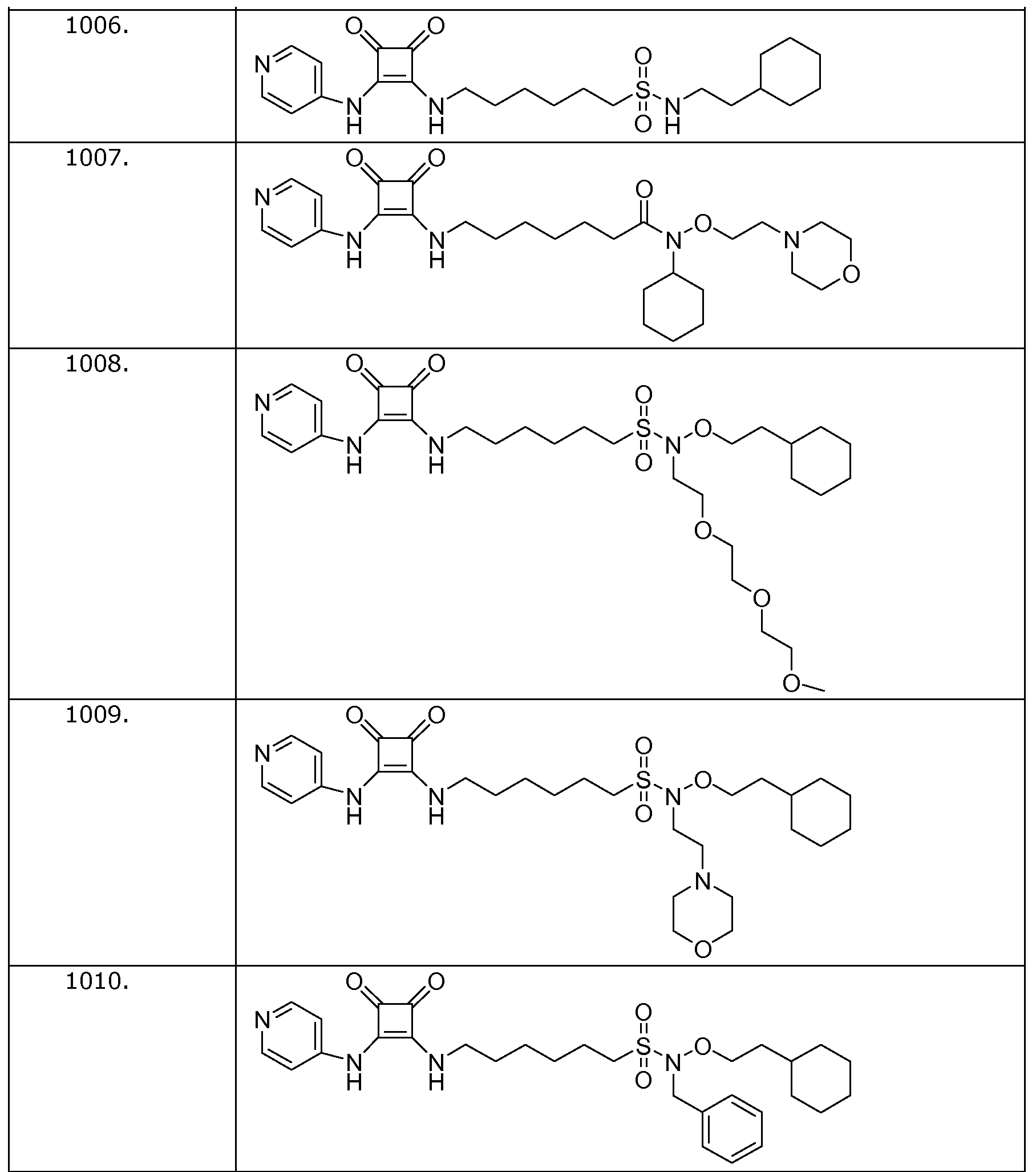
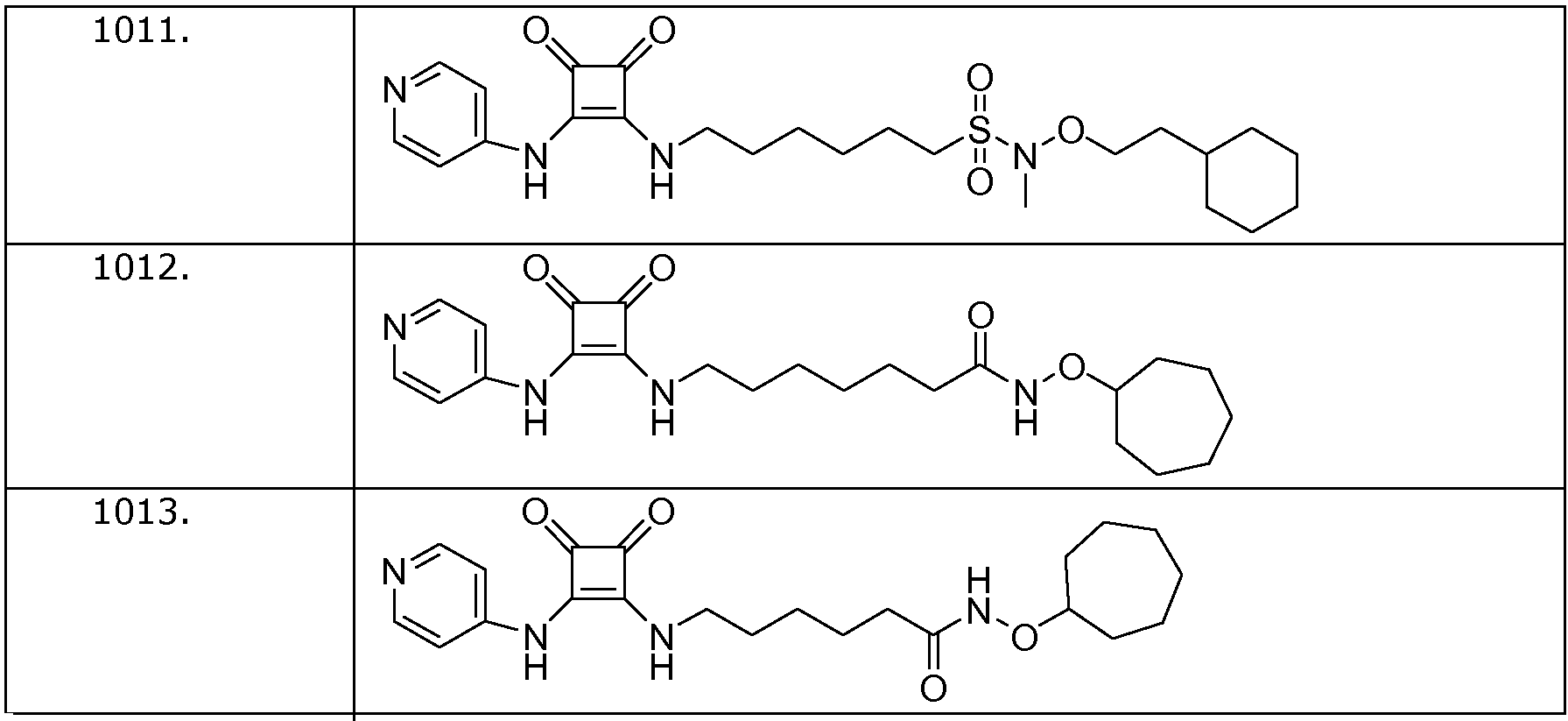
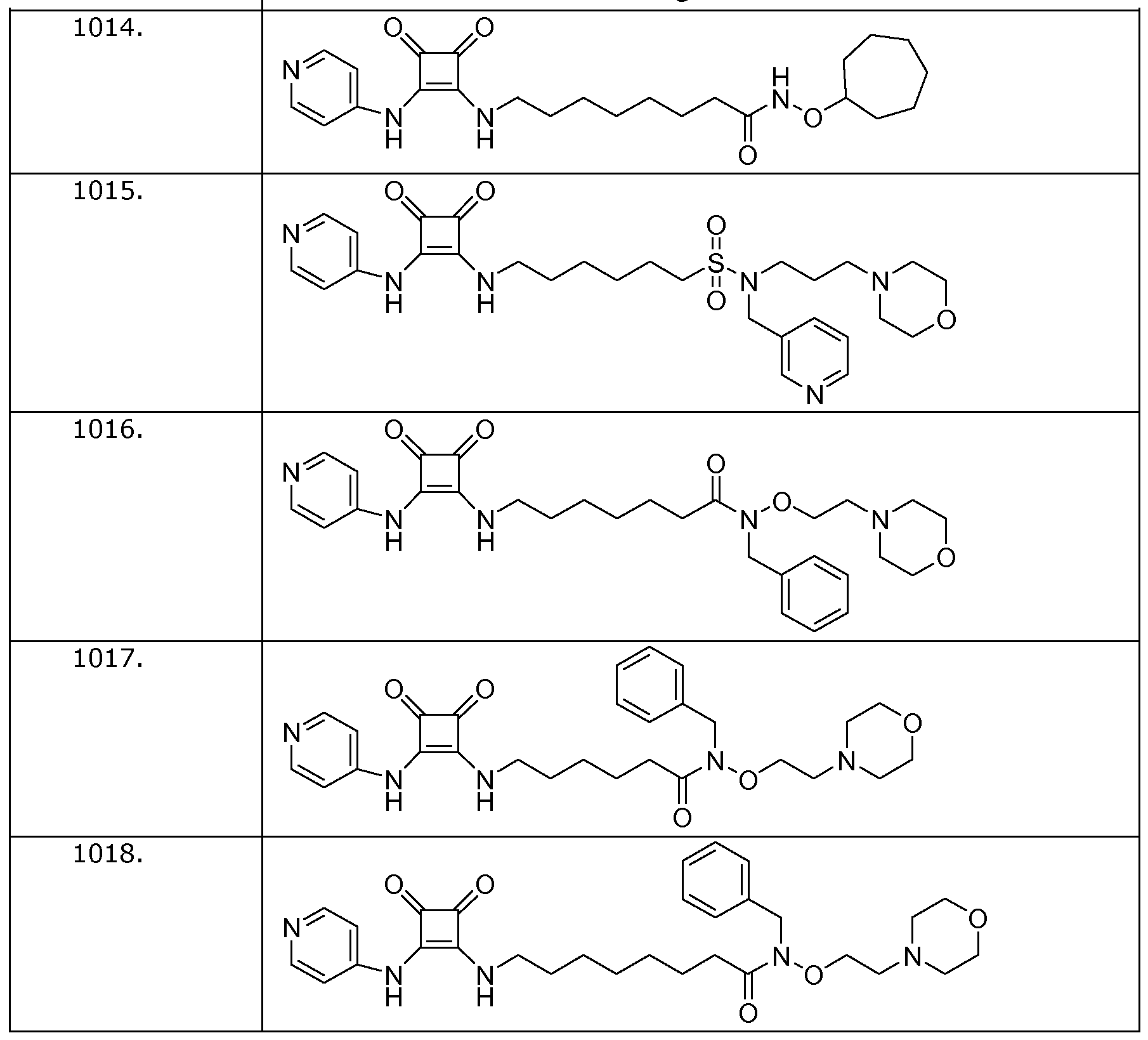
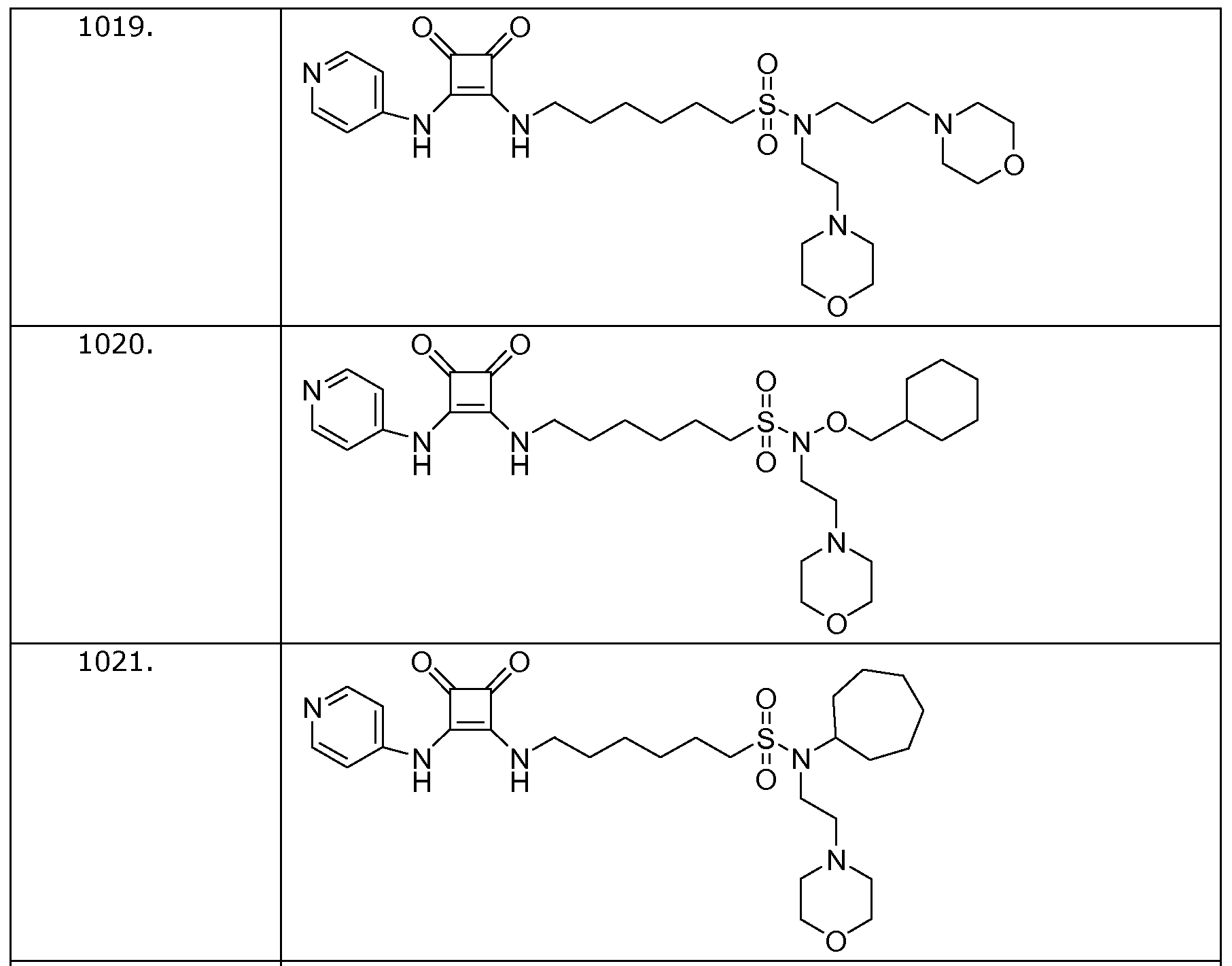
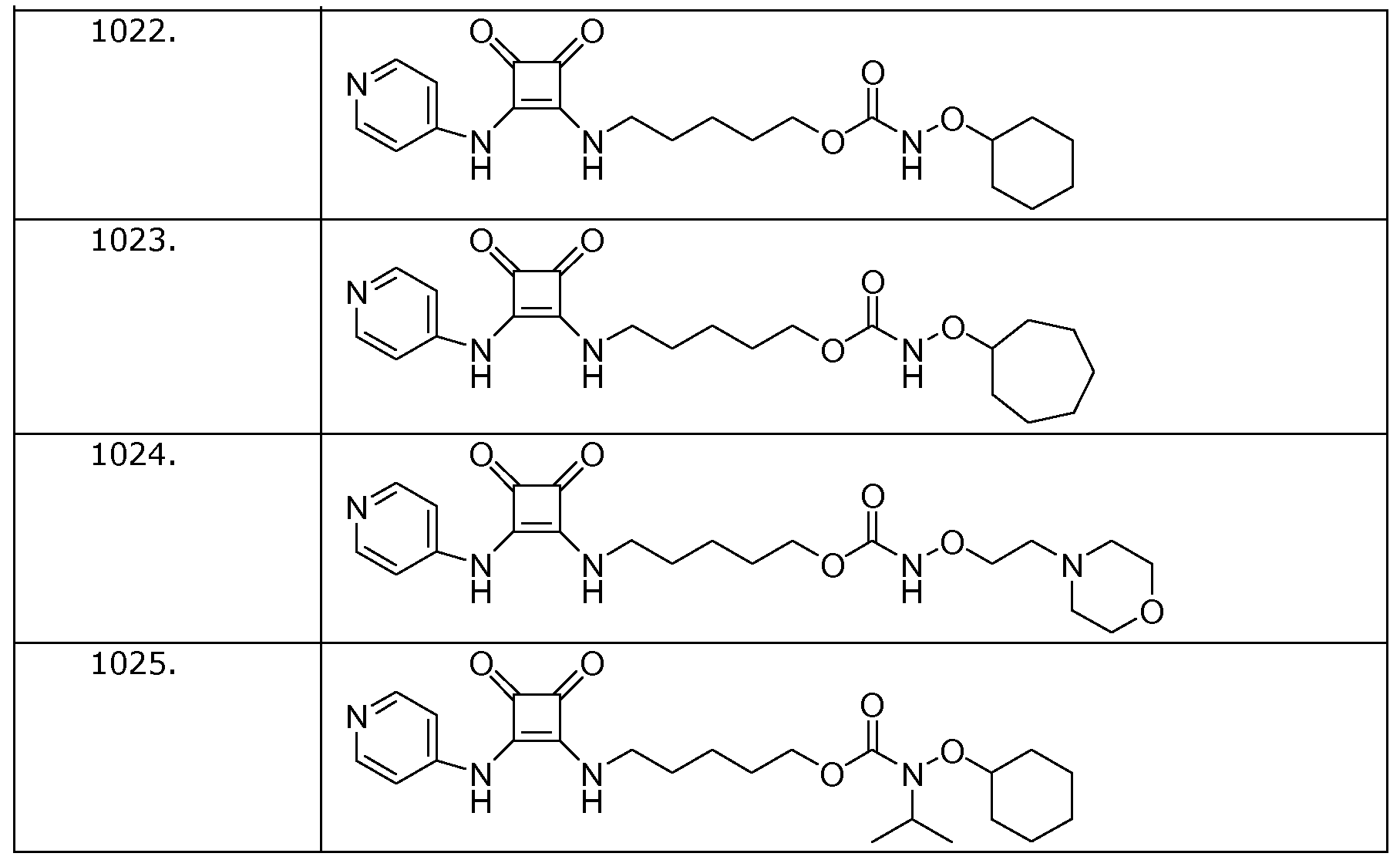
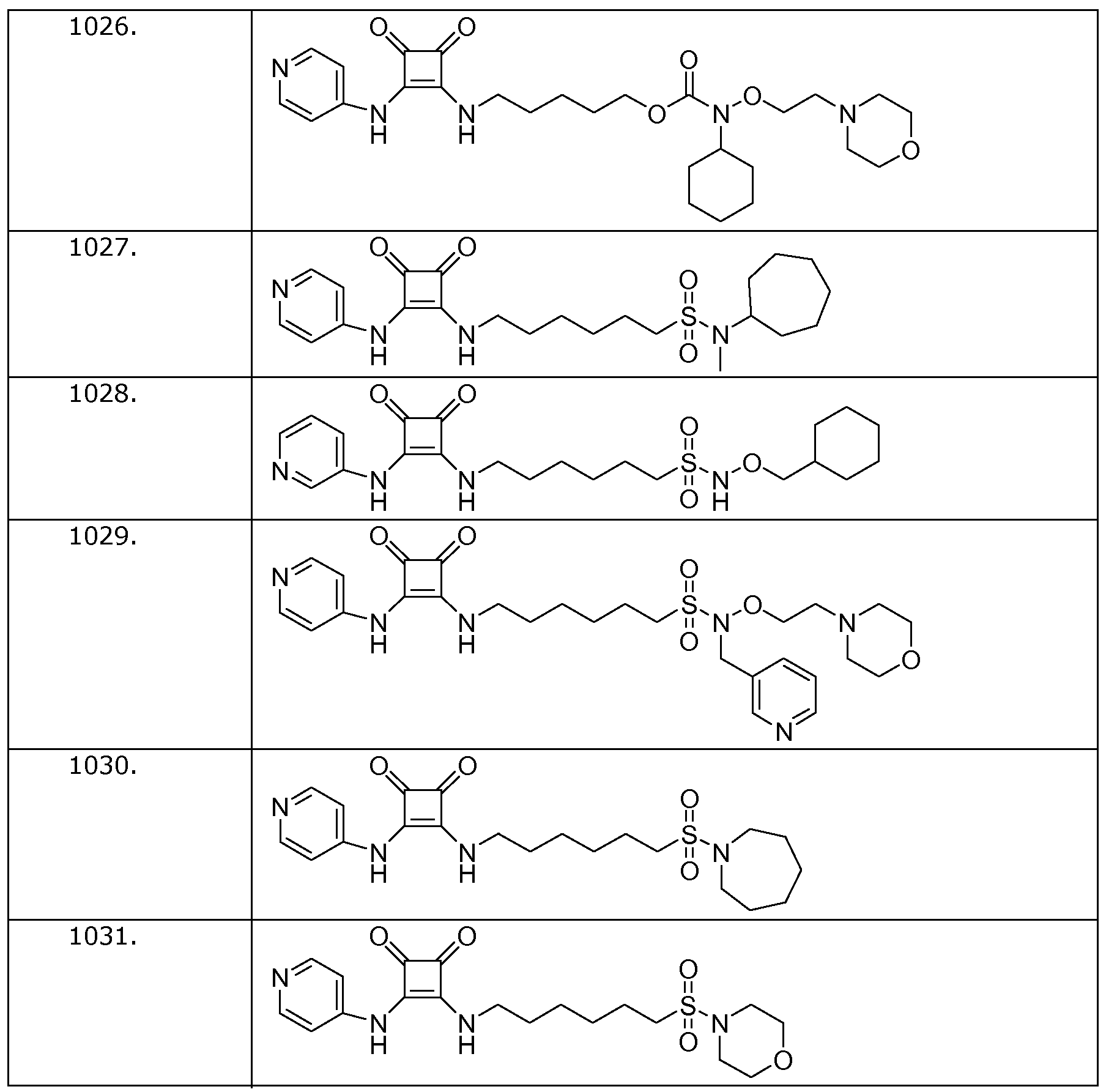
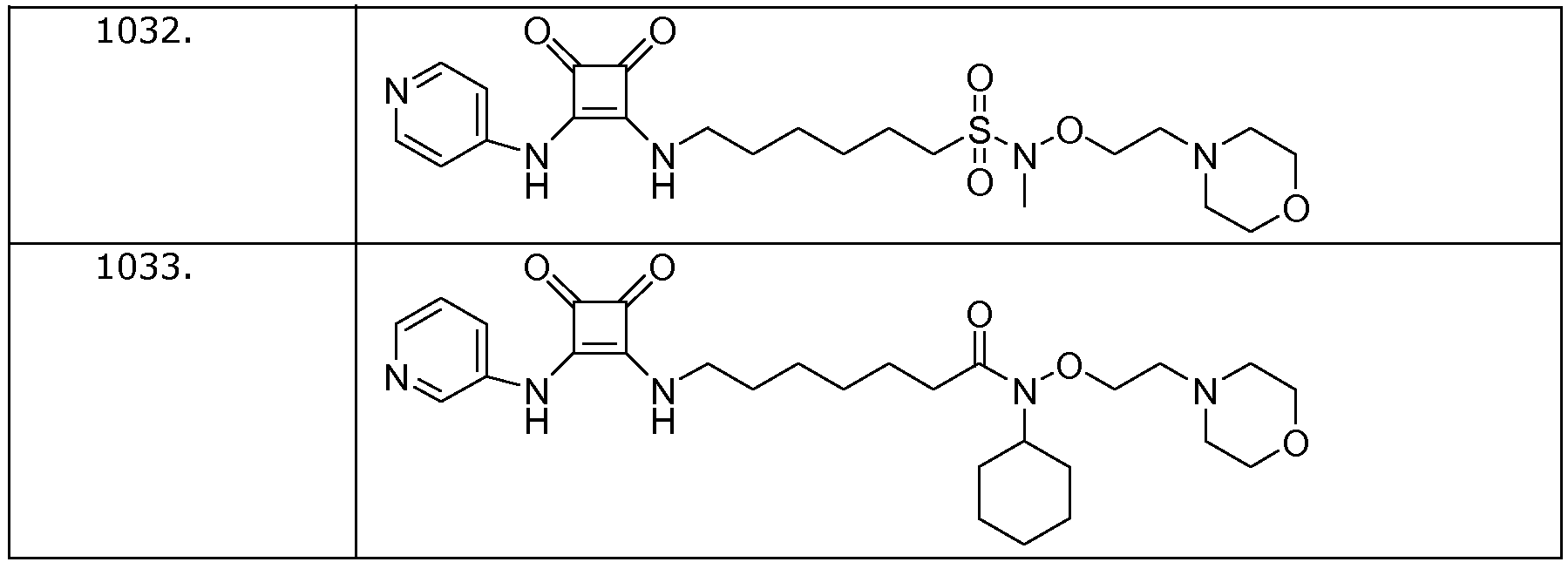
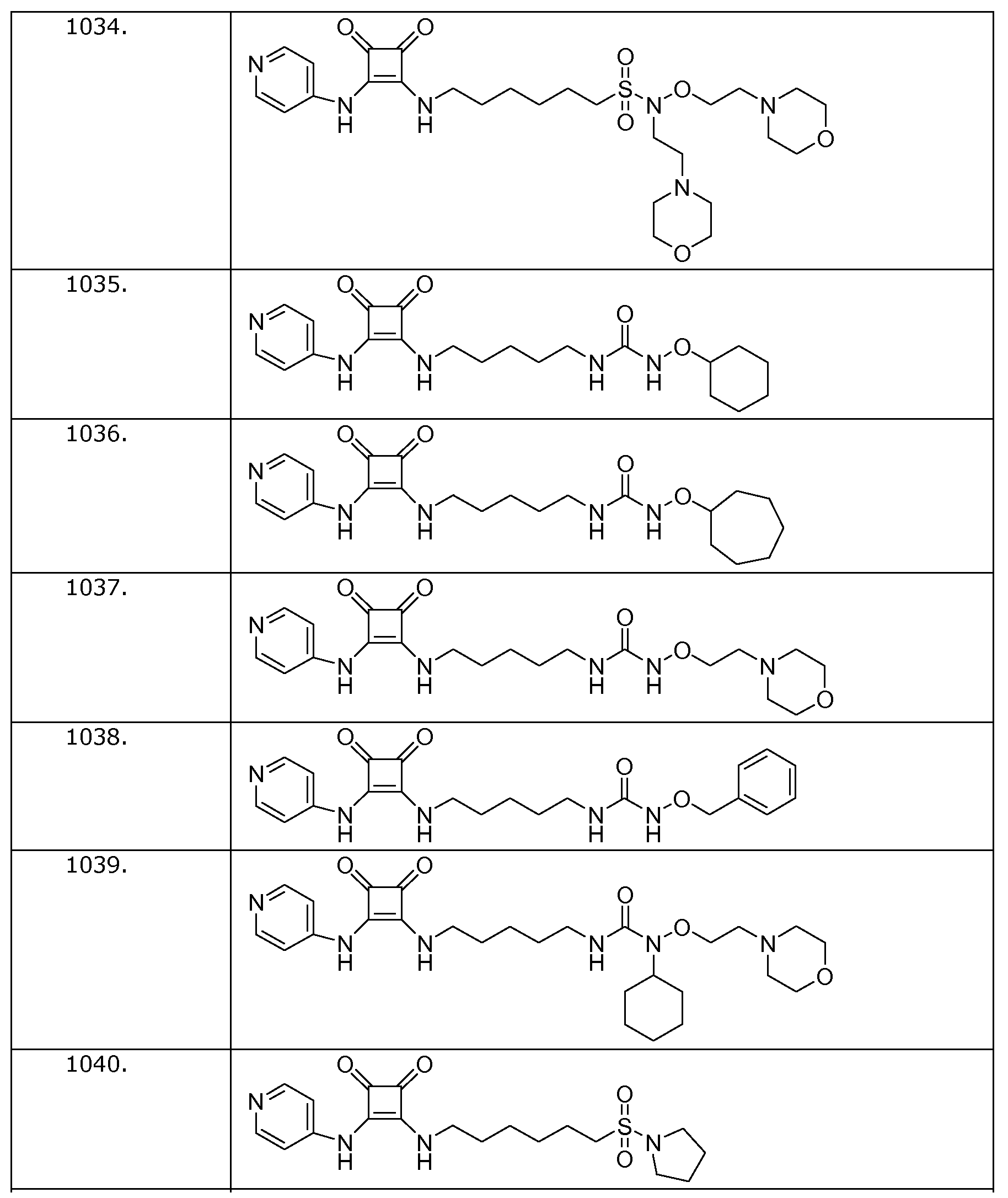
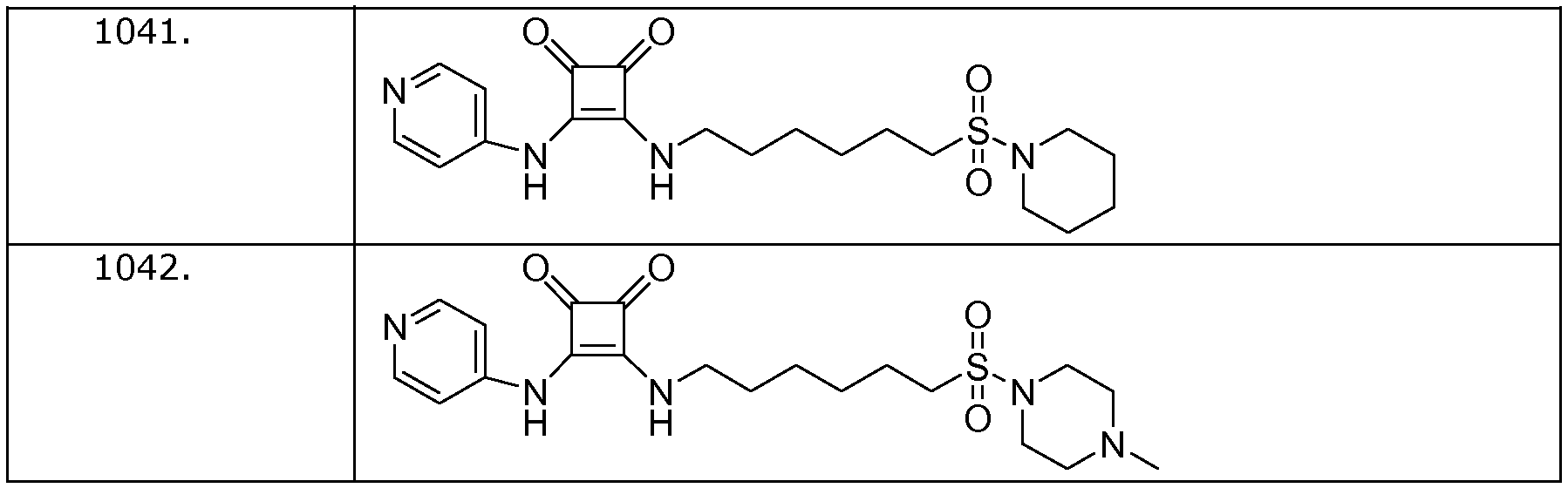
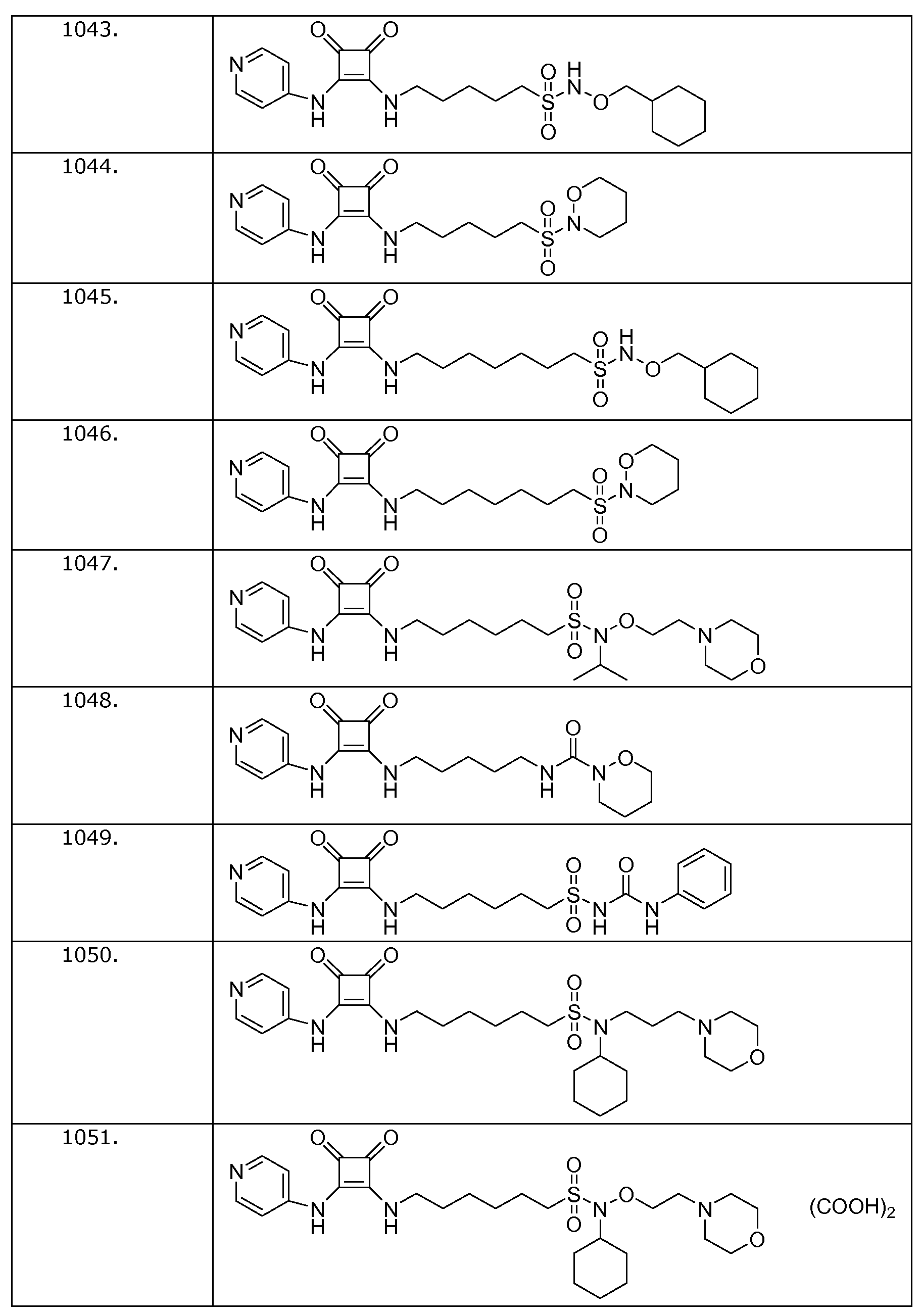
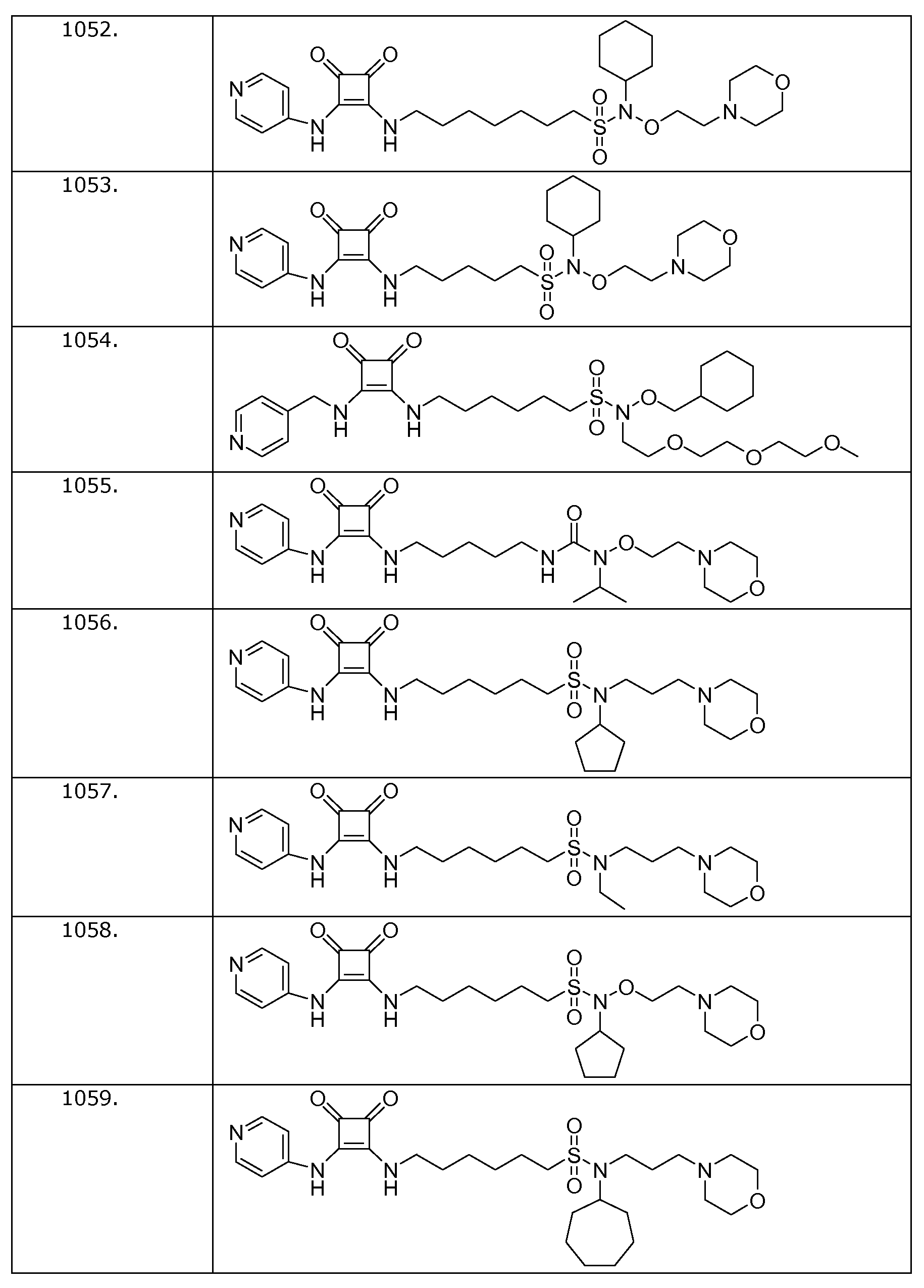
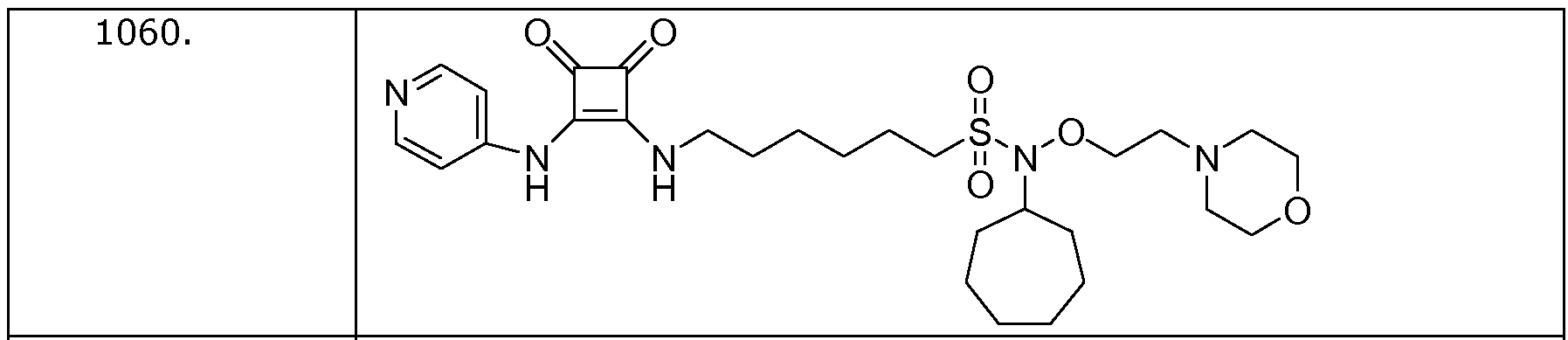
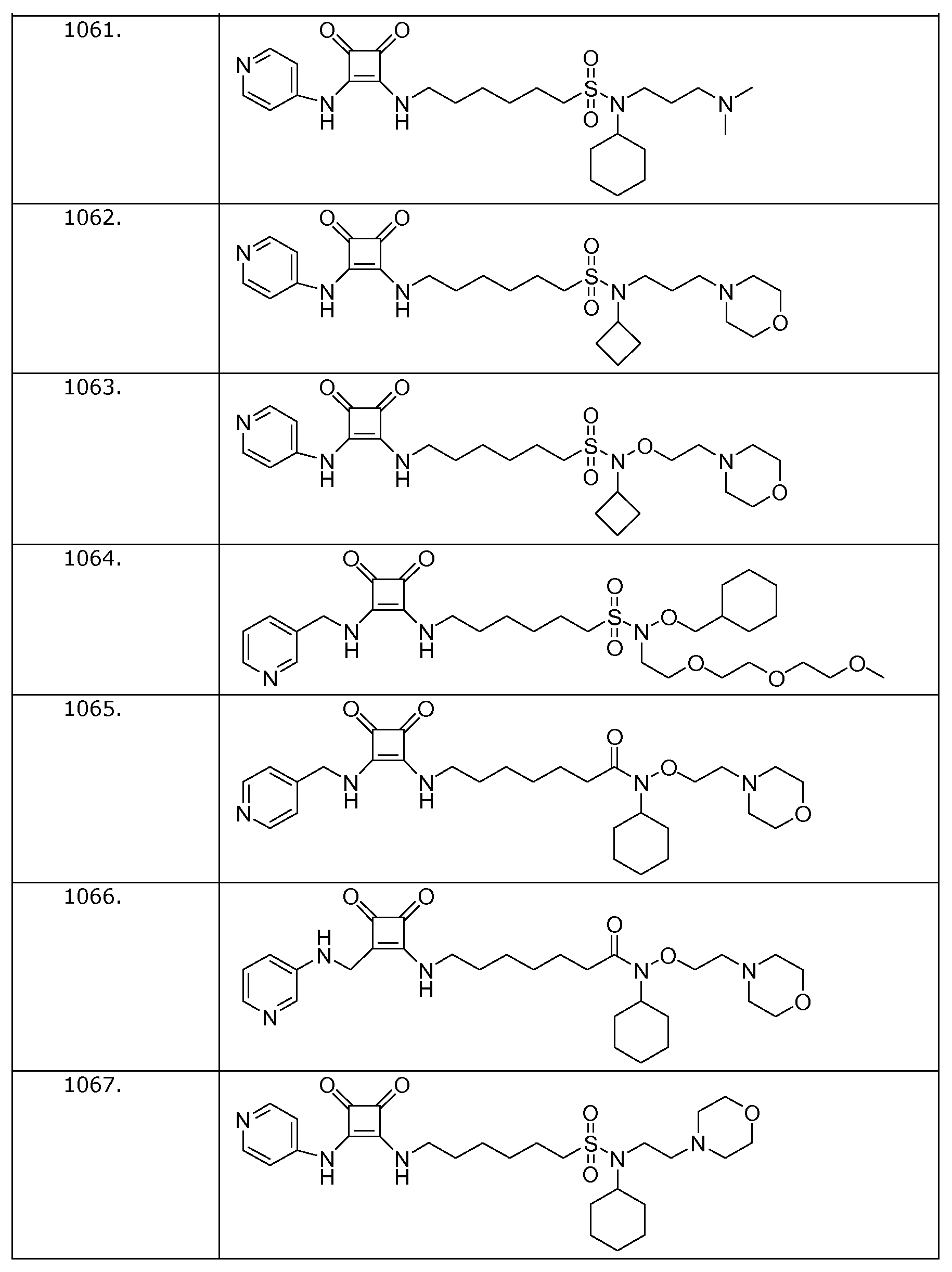
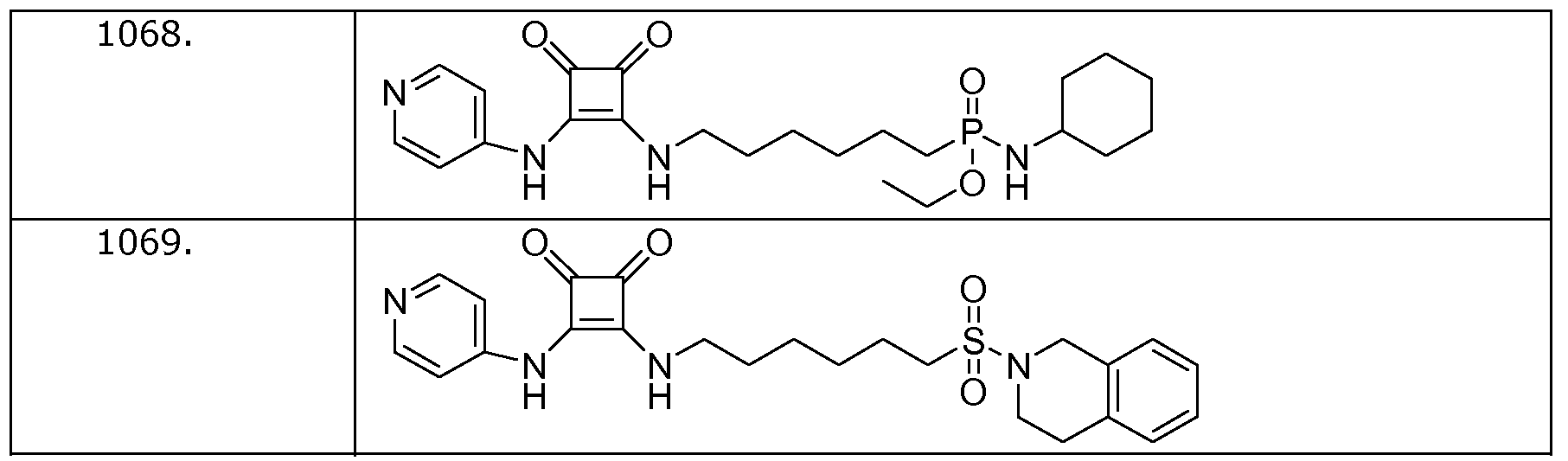
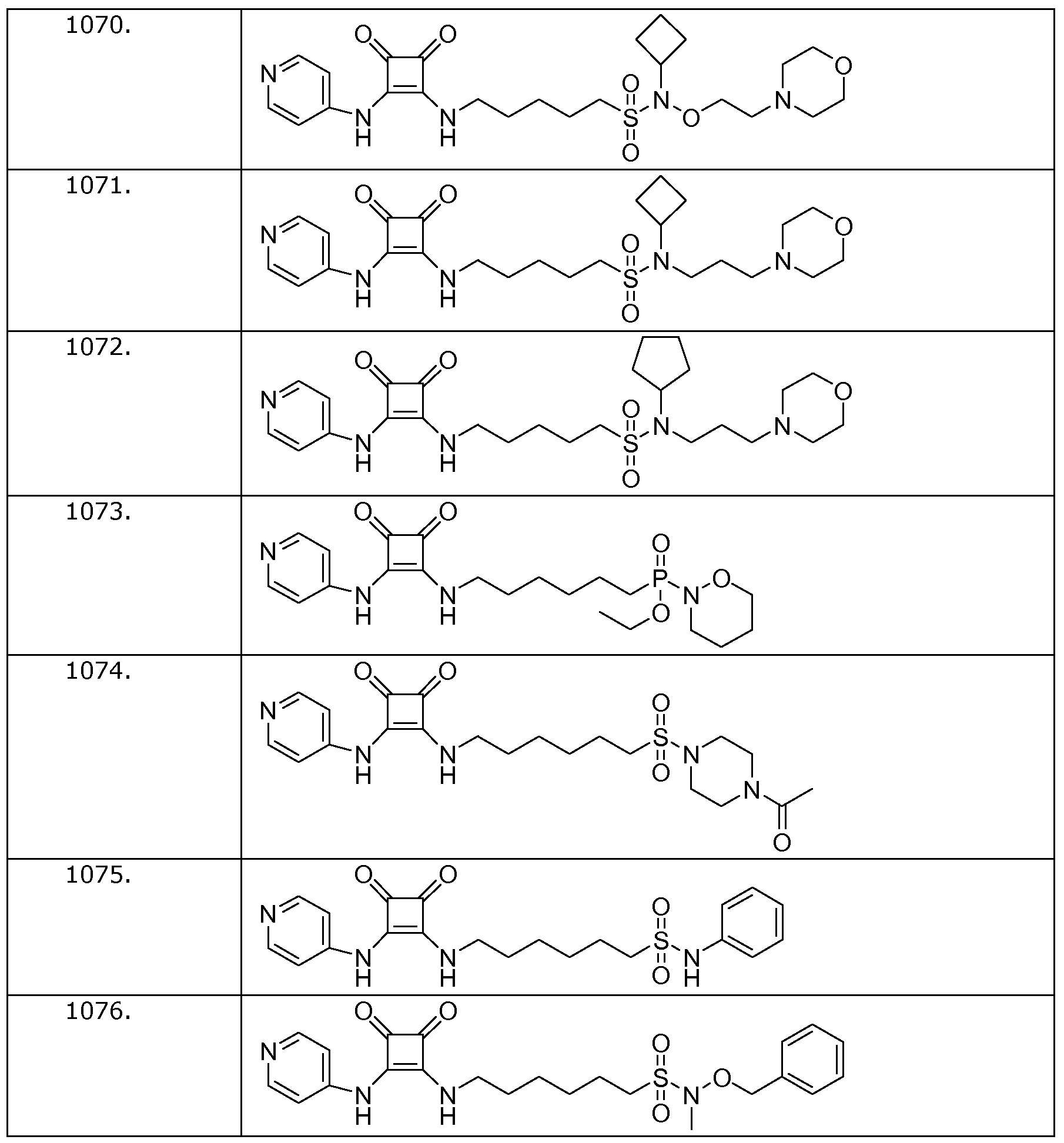
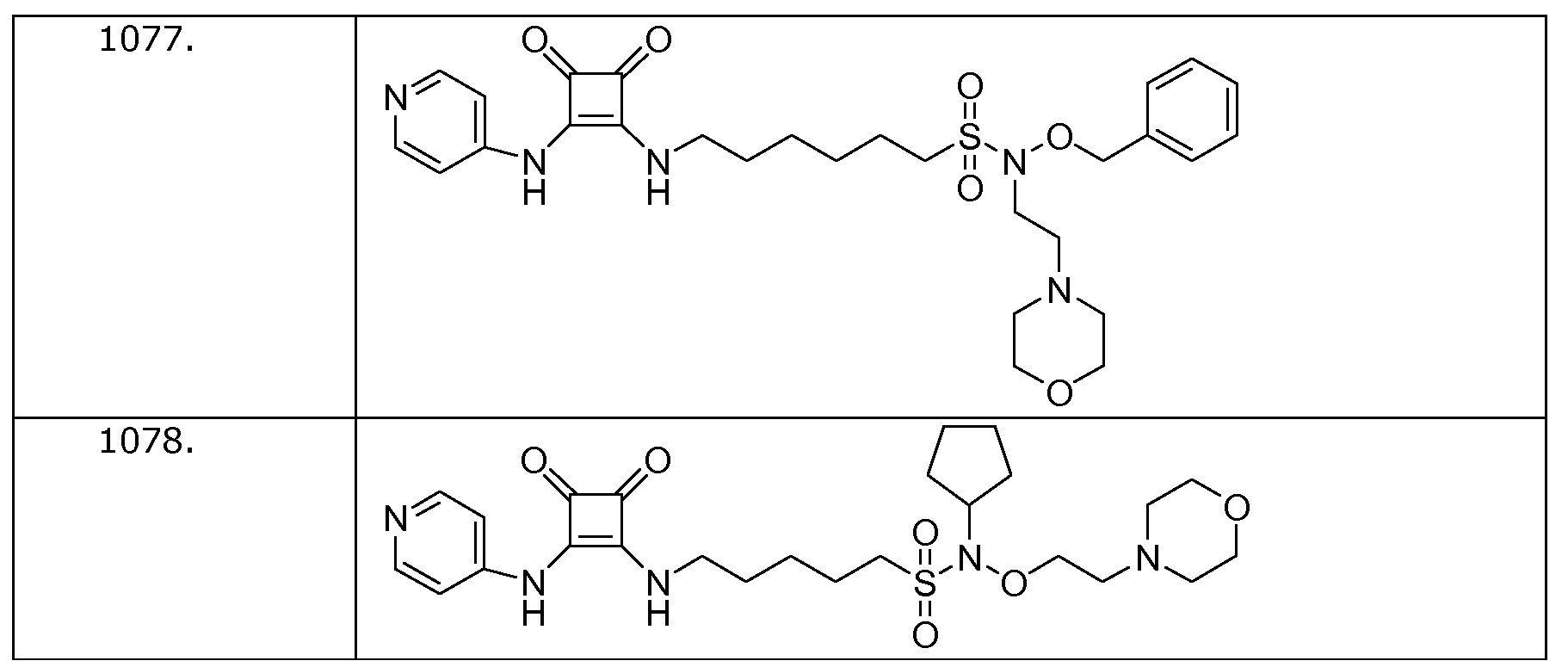
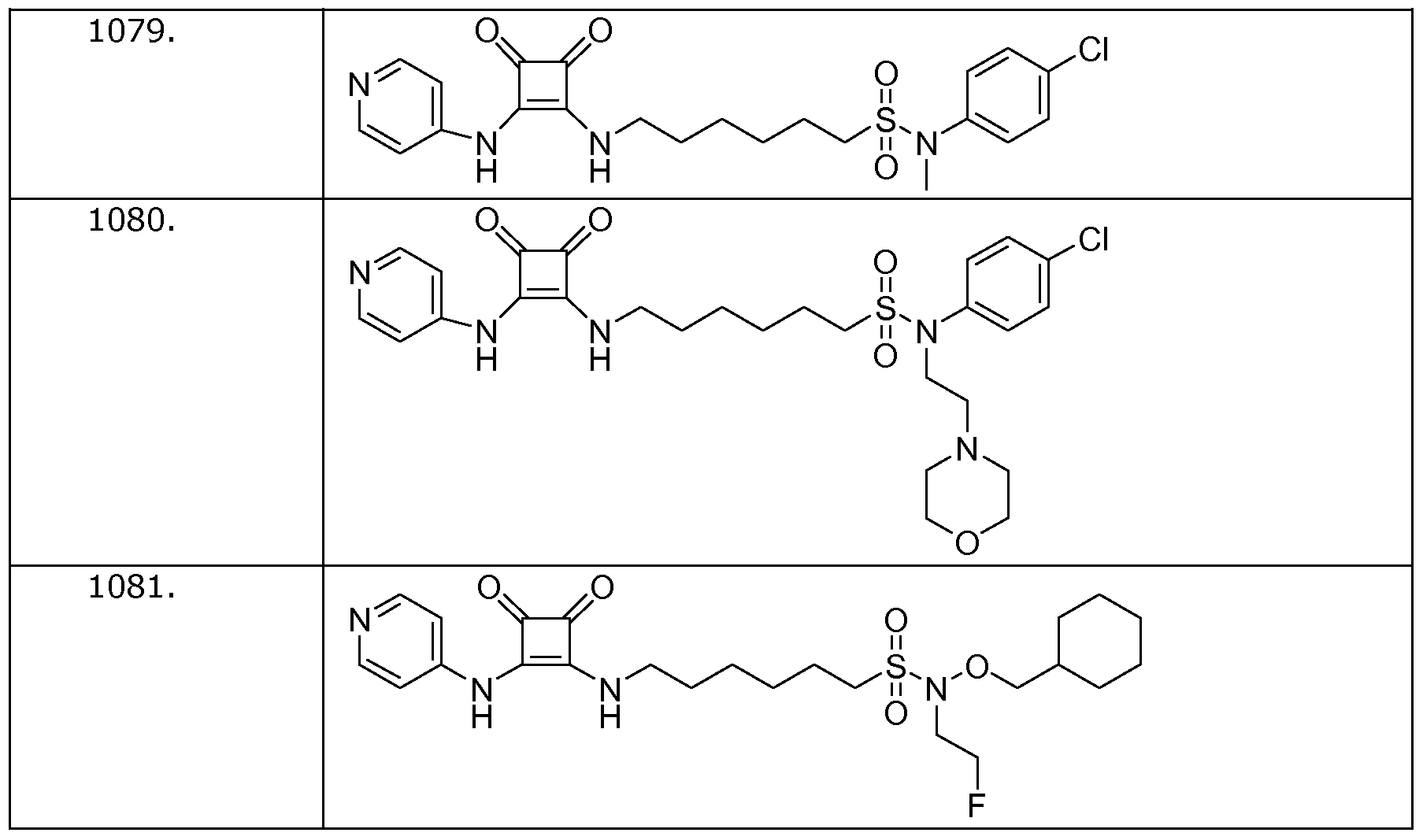
Получение соединений формулы (I)
Соединения в соответствии с данным изобретением могут быть синтезированы с применением указанных ниже методов вместе с методами, известными в области органического синтеза, или их вариантов, которые очевидны специалисту в данной области техники. Предпочтительные способы включают, но не ограничены ими, описанные ниже.
Новые соединение формулы (I) могут быть получены с применением реакций и методик, описанных в этом разделе. Реакции проводят в растворителях, подходящих для используемых реагентов и материалов и подходящих для проводимых превращений. Также в описанных ниже способах синтеза понятно, что все предложенные условия реакций, включая выбор растворителя, атмосферы реакции, температуры реакции, длительности эксперимента и обработки, выбраны так, чтобы быть стандартными для данной реакции, что легко распознается специалистом в данной области техники. Специалист в области органического синтеза поймет, что функциональность, присутствующая в различных частях полученной молекулы, должна быть совместима с предложенными реагентами и реакциями. Не все молекулы формулы (I), попадающие в указанный класс, могут быть совместимы с некоторыми условиями реакции, требуемыми в некоторых описанных способах. Такие ограничения заместителей, которые совместимы с условиями реакции, очевидны специалисту в данной области техники, и он может применять альтернативные способы.
Соединения общей формулы (I) могут быть получены реакцией аминов и 3,4-диэтоксициклобут-3-ен-1,2-диона с получением промежуточных соединений общей формулы (II), с последующей реакцией с аминами (III).
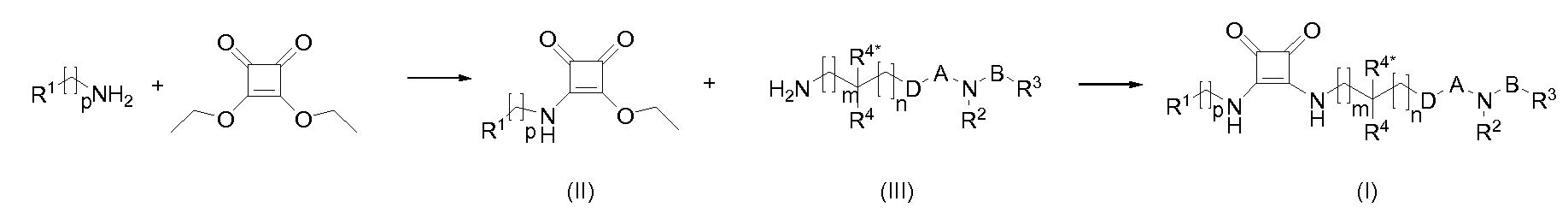
Соединения общей формулы (I), которые являются сложными эфирами гидроксаминовой кислоты, N-алкил- или N-арилгидразидами, N,N'-диалкил- или N,N'-диарилгидразидами (Ia), могут быть получены реакцией аминокислот общей формулы (IV) с промежуточными соединениями общей формулы (II) с получением кислот общей формулы (V), которые затем сочетают с гидроксиламинами или гидразинами общей формулы (VI) с применением пептидного сочетающего реагента (например, ЭДХ или ГАТУ).
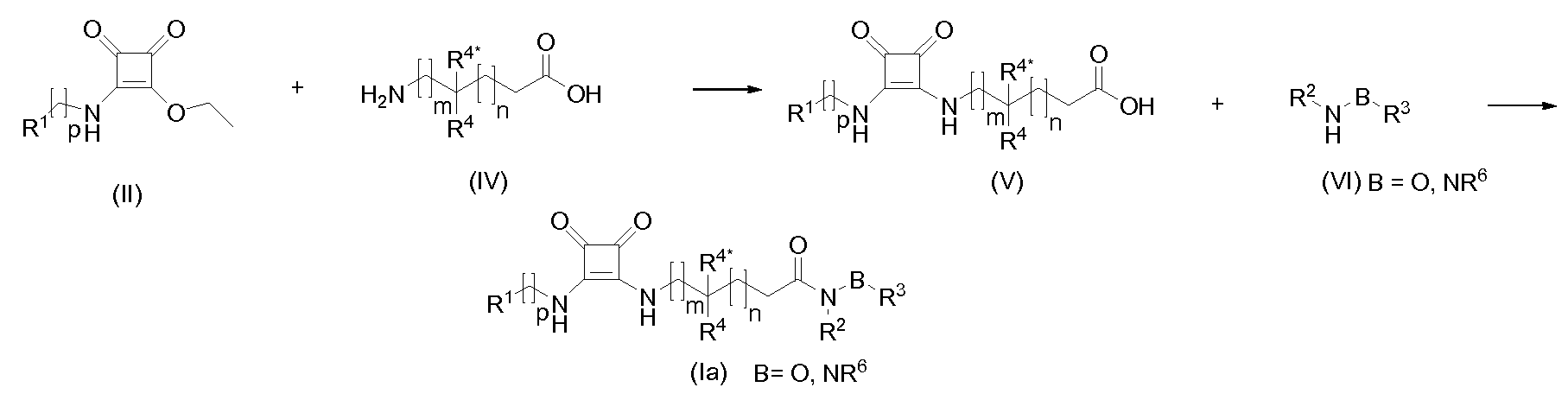
Аминокислоты (Va), содержащие заместитель α карбонильной группы, могут быть получены из аминокислот общей формулы (IVa) или их энантиомеров (полученных как описано в литературе, например, K. S. Orwig et al.: Tet.Lett. (2005) 46 7007-7009) сочетанием с соединениями общей формулы (II).
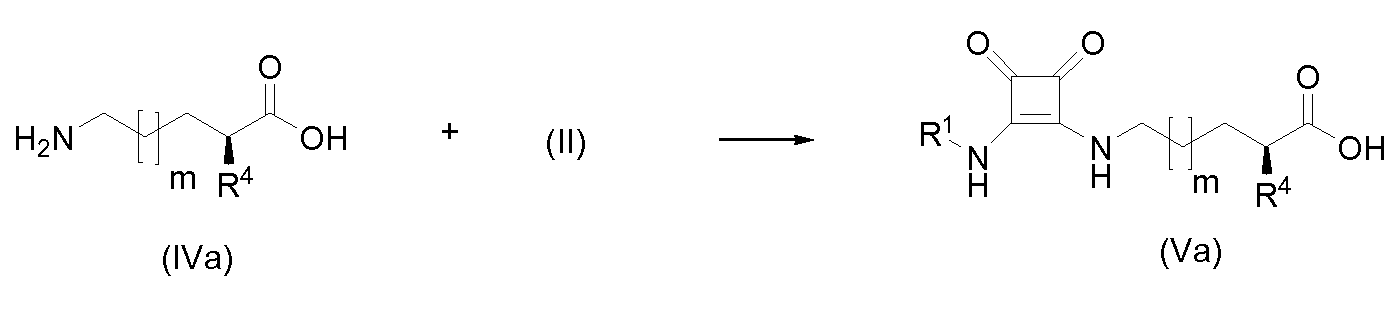
Альтернативно, амины общей формулы (III), которые являются сложными эфирами гидроксаминовой кислоты, N-алкил- или N-арилгидразидами, N,N'-диалкил- или N,N'-диарилгидразидами (IIIa), могут быть получены из защищенных аминокислот общей формулы (VII) (защитная группа Pg, например, Boc или фталимидо) сочетанием с гидроксиламинами или гидразинами общей формулы (VI) с применением пептидного сочетающего реагента (например, ЭДХ или ГАТУ), с последующим удалением защитной группы, с последующей реакцией полученного амина (IIIa) с промежуточными соединениями общей формулы (II).
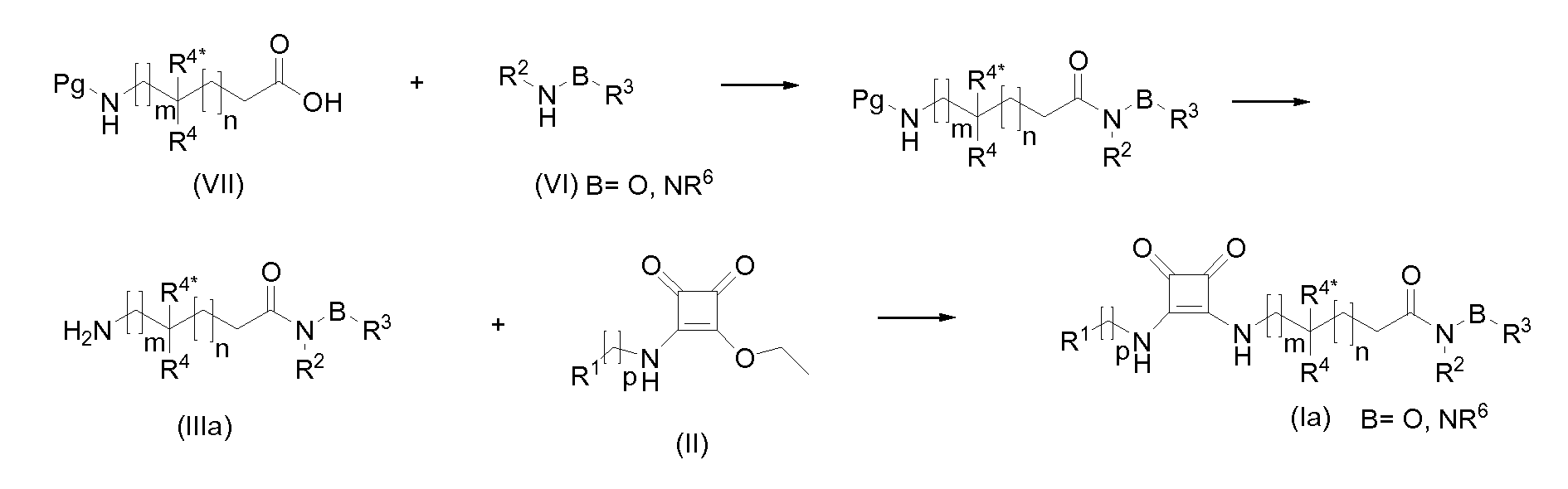
Гидроксиламины (VI) либо коммерчески доступны, либо могут быть получены из N-гидроксифталимида (или, альтернативно, втор-бутилгидроксикарбамата) алкилированием с галогенидом и основанием (например, ДБУ) или реакцией Мицунобу со спиртом (с применением, например, ДЭАД), с последующим снятием защиты гидразином или метилгидразином, с получением гидроксиламина (VIa).
Если R2 не является водородом, полученный гидроксиламин (VIa) может быть подвергнут восстановительному аминированию с альдегидом или кетоном с последующим восстановлением с, например, цианоборгидридом натрия, как описано в литературе (например, B.J. Mavunkel et al.: Eur.J.Med.Chem. (1994) 29, 659-666; T. Ishikawa et.al.: J.Antibiotics (2000), 53 (10), 1071-1085; J. Ishwara Bhat et al.: J.Chem.Soc, Perkin Trans. 2 (2000), 1435-1446). Альтернативно, алкилирование гидроксиламина (VIa) может быть достигнуто реакцией Мицунобу или алкилированием после защиты, например, 2-нитрофенилсульфонилхлоридом, и последующим удалением защитной группы (с применением, например, тиофенола и карбоната цезия).
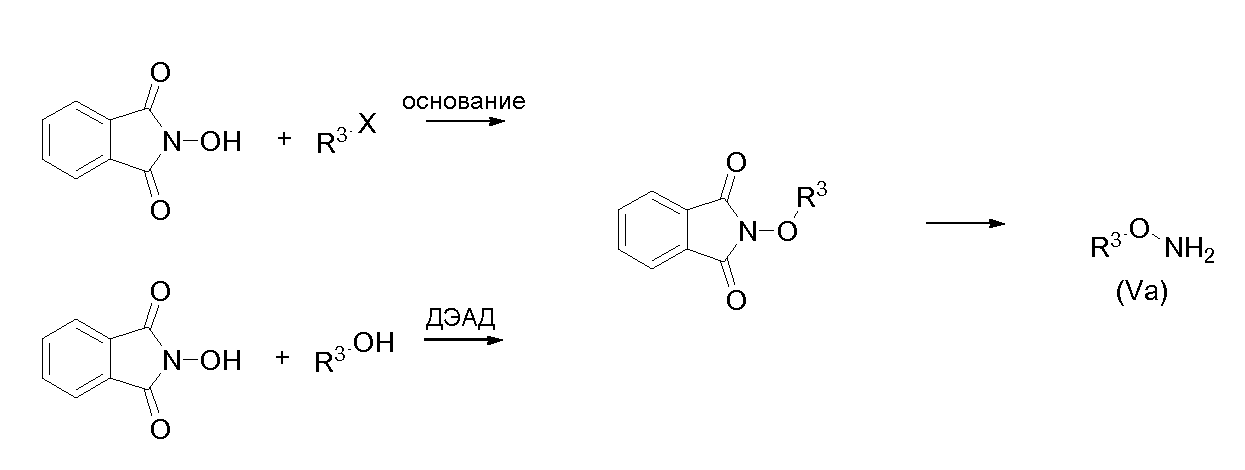
(где "Va" должно читаться как "VIa")
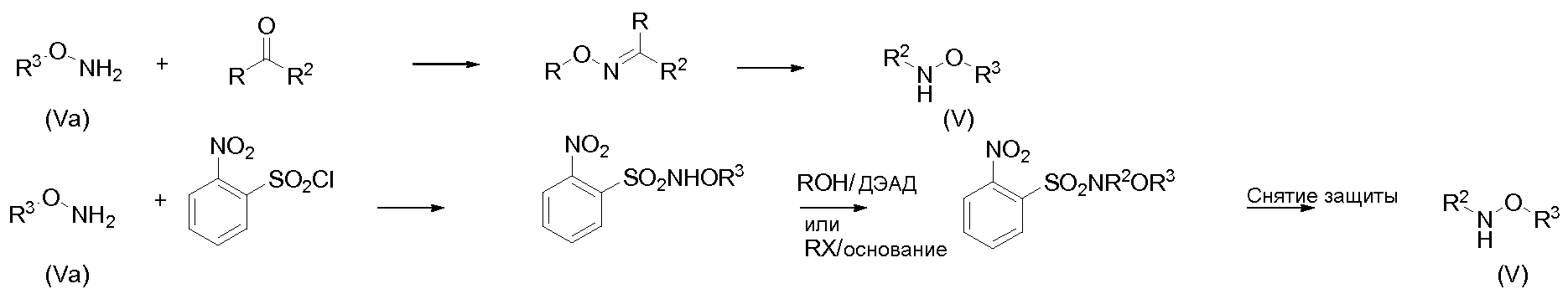
(где "Va" должно читаться как "VIa" и "V" должно читаться как "VI")
Гидразины (VI) либо коммерчески доступны, либо - если R2 является H - могут быть получены из гидразингидрата алкилированием в присутствии основания, согласно описанным в литературе методам (например, DJ. Drain et al.: J.Med.Chem. (1963) 6 63-9; G. B. Marini-Bettolo et al.: Rend.Ist.Super.Sanita (1960) 23 1110-27). N,N'-дизамещенные гидразины могут быть получены из монозамещенных гидразинов (VIa) реакцией с альдегидом или кетоном с последующим восстановлением с, например, водородом, LiAlH4, или бораном, согласно описанным в литературе методам (например, H. Dorn et.al.: Zeitschrift fur Chemie (1972) 12(4) 129-30; R.L. Hinman: JACS (1957) 79 414-417; J.A. Blair: JCS (Section) C: Organic (1970) (12) 1714-17) или, альтернативно, Boc-защитой гидразингидрата, алкилированием с алкилгалогенидом в присутствии гидрида натрия с последующим вторым алкилированием с другим алкилгалогенидом в присутствии гидрида натрия, и, наконец, удалением Boc-защитных групп (L.Ling et al.: Bioorg. Med. Chem. Lett. (2001) (11) 2715-2717).
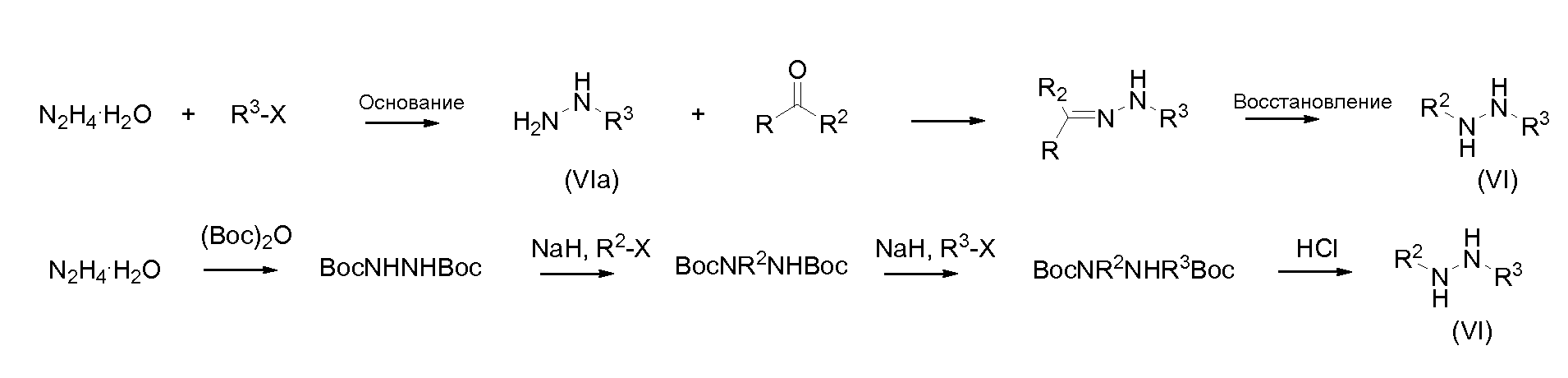
Соединения общей формулы (I) в соответствии с данным изобретением, которые являются N-алкокси- или N-арилокситиоамидами или тиогидразидами (Ib), могут быть получены из соответствующих соединений карбонила (Ia) обработкой с реагентом Ловессона согласно описанным в литературе методам (например, Thomsen et al.: Org. Synth. (1984) 62, 158, R.A. Cherkasov et al.: Tet. (1985) 41, 2567; M. P. Cava, MJ. Levinson Tet. (1985) 41, 5061).

Альтернативно, защищенные аминокислоты общей формулы (VII) (защитной группой является, например, Boc или фталимидо) могут быть превращены в активированные виды общей формулы (VIII) согласно описанным в литературе методам (M.A. Shalaby et al.: J.Org.Chem. (1996) 61 9045-48) и далее подвергнуты взаимодействию с гидроксиламинами или гидразинами (VI) с последующим снятием защиты и последующей реакцией амина (IIIb) с промежуточными соединениями общей формулы (II) как описано ниже.
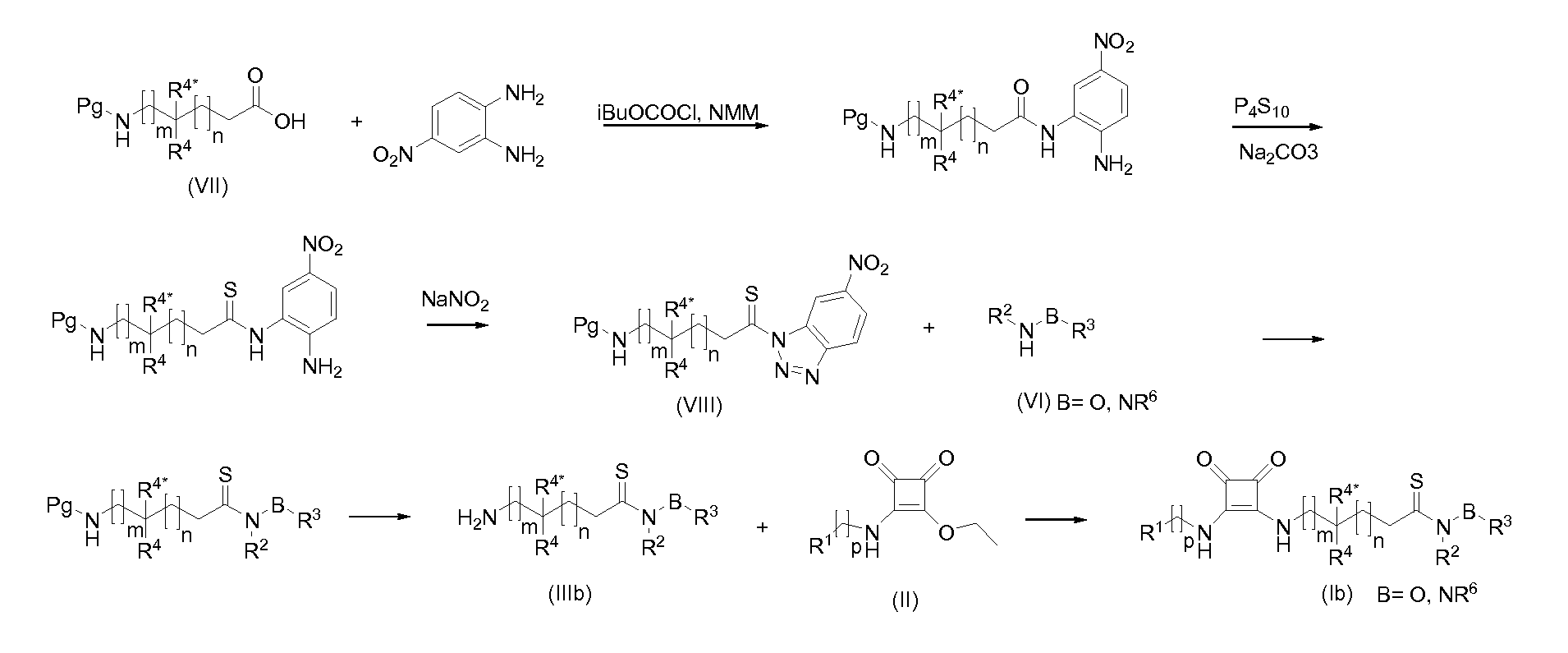
Соединения (I) в соответствии с данным изобретением, которые являются N-алкокси- или N-арилоксисульфонамидами, -сульфонамидами или сульфонилгидразидами (Ic), могут быть получены реакцией промежуточных соединений общей формулы (II) с аминами общей формулы (IIIc). Амины общей формулы (IIIc) могут быть получены, как описано в предварительной заявке на патент США 61/051130 (не опубликованной) и PCT/DK2009/000006.
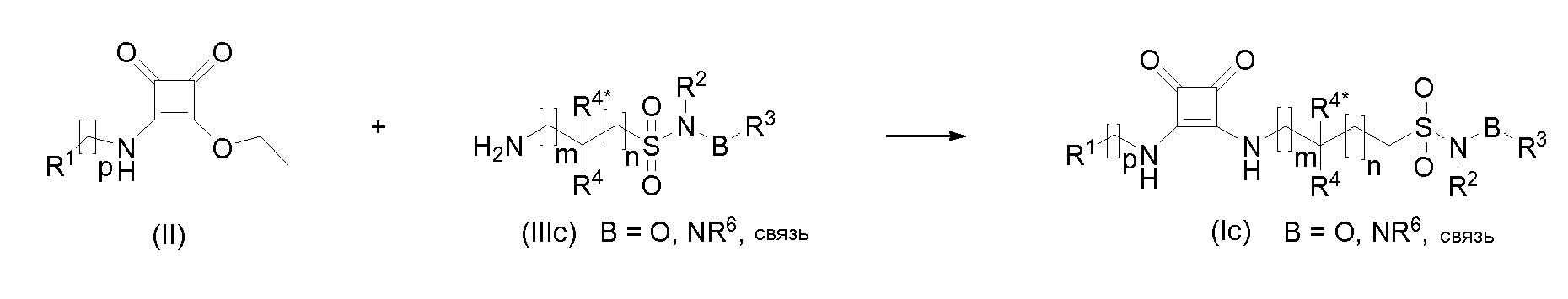
Соединения (I) в соответствии с данным изобретением, которые являются N-алкокси-P-алкилфосфонамидатами или N-арилокси-P-алкилфосфонамидатами, P-алкилфосфонамидатами или P-алкилфосфоногидразидатами (Id), могут быть получены реакцией защищенных фталимидо фосфонохлоридатов (IX) (полученных как описано в литературе, например, S. Gobecet at.al.: Tet.Lett. (2002) 43 167-170; U. Urleb et al.: Lett. In Peptide Science (1995) 2 193-197) с гидроксиламинами, аминами или гидразинами (VI), соответственно, в присутствии основания с последующим снятием защиты гидразингидратом. Полученный амин (IIId) затем подвергают взаимодействию с соединениями общей формулы (II) с получением соединений (Id). Могут применяться другие защитные группы, отличные от фталимидо.
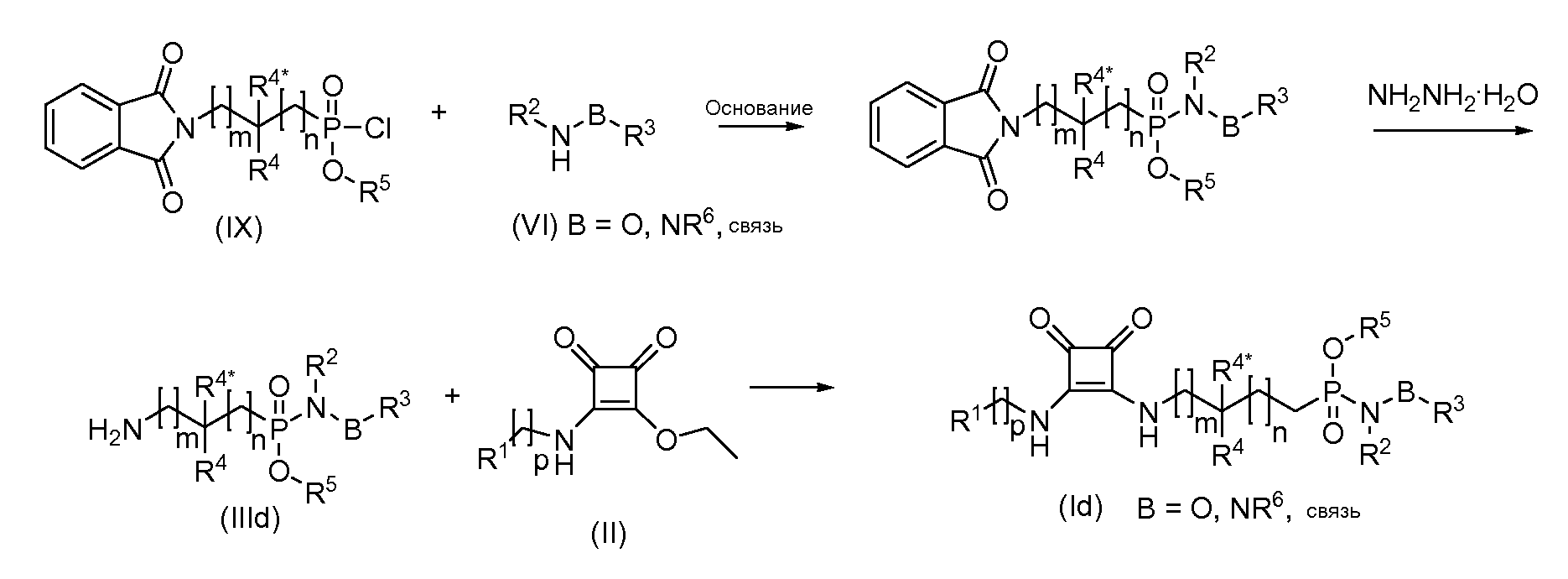
Соединения (I) в соответствии с данным изобретением, которые являются N-алкокси-P-алкилфосфиновыми амидами или N-арилокси-P-алкилфосфиновыми амидами, P-алкилфосфиновыми амидами или P-алкилфосфиновыми гидразидами (Ie), могут быть получены взаимодействием защищенных фталимидо алкилфосфиновых хлоридов (X) (например, S. Gobec et al.: Lett. In Peptide Science (1998) 5 109-114) с гидроксиламинами, аминами или гидразинами (VI), соответственно, в присутствии основания с последующим снятием защиты гидразингидратом. Полученный амин (IIIe) затем подвергают взаимодействию с соединениями общей формулы (II) с получением соединений формулы (Ie). Могут применяться другие защитные группы, отличные от фталимидо.
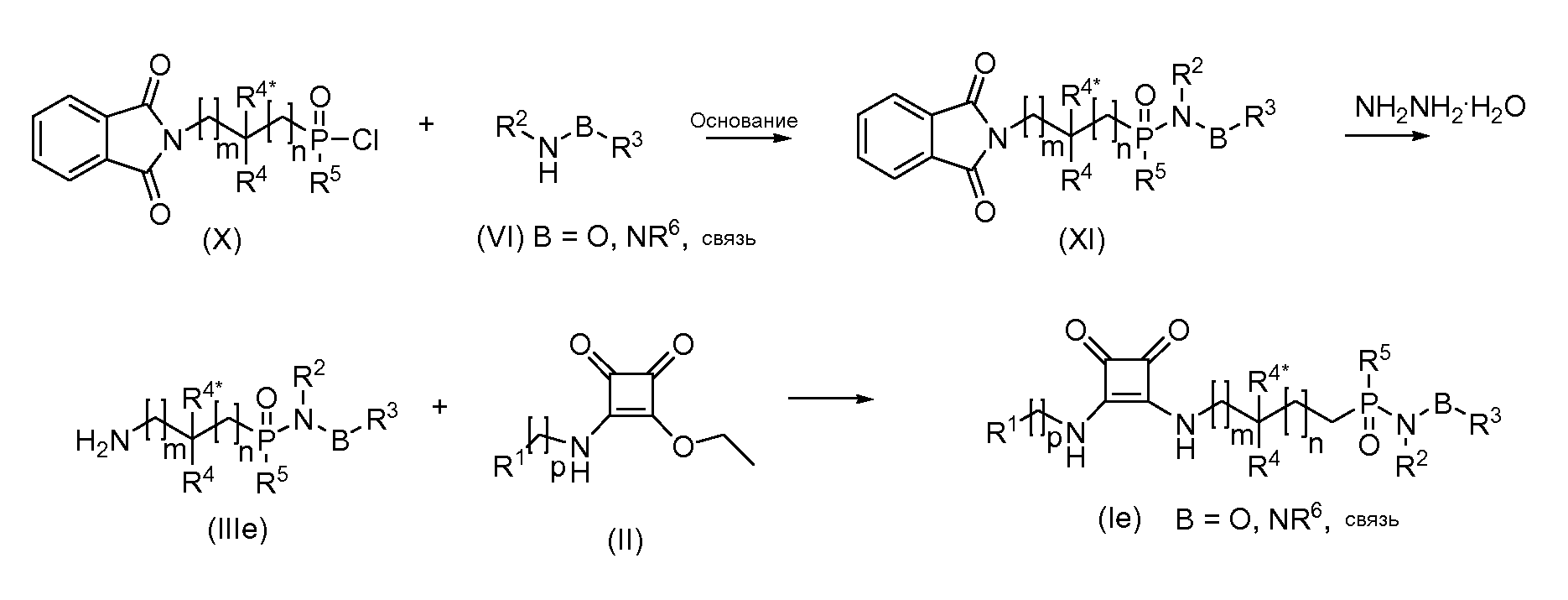
Соединения (I) в соответствии с данным изобретением, которые являются сульфонилмочевинами (If), могут быть получены известными в литературе способами (например, B. Hökfelt et al.: J.Med.&Pharm. Chem. (1962) 5 231-9; R. Tull et al. JCS Section C:Organic (1967) (8) 701-2;B. Loev: J. Med. Chem. (1963) 6(5) 506-8; D. R. Cassady et al.: J.Org.Chem. (1958) 23 923-6; D. Freitag : Tetrahedron (2005) 61 5615-21; Y. Kanbe et.al.: Bioorg. Med. Chem. Lett. (2006) 16 4090-94; I. Ubarretxena-Belandia et.al.: Eur.J.Biochem. (1999) 260 794-800; B. D. Roth et al.: Bioorg. Med. Chem. Lett. (1995) 5 (20) 2367-70), например, реакцией подходящим образом защищенных аминоалкансульфонилхлоридов (XII) (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006) с аммониевым эквивалентом или амином, с последующей реакцией с алкилхлорформиатом в присутствии основания с получением карбаматов общей формулы (XIV), которые затем подвергают взаимодействию с аминами R3R6NH2 с получением сульфонилмочевин (XV). Альтернативно, сульфонамиды общей формулы (XIII) могут быть подвергнуты взаимодействию непосредственно с изоцианатами с получением защищенных сульфонилмочевин (XVa).
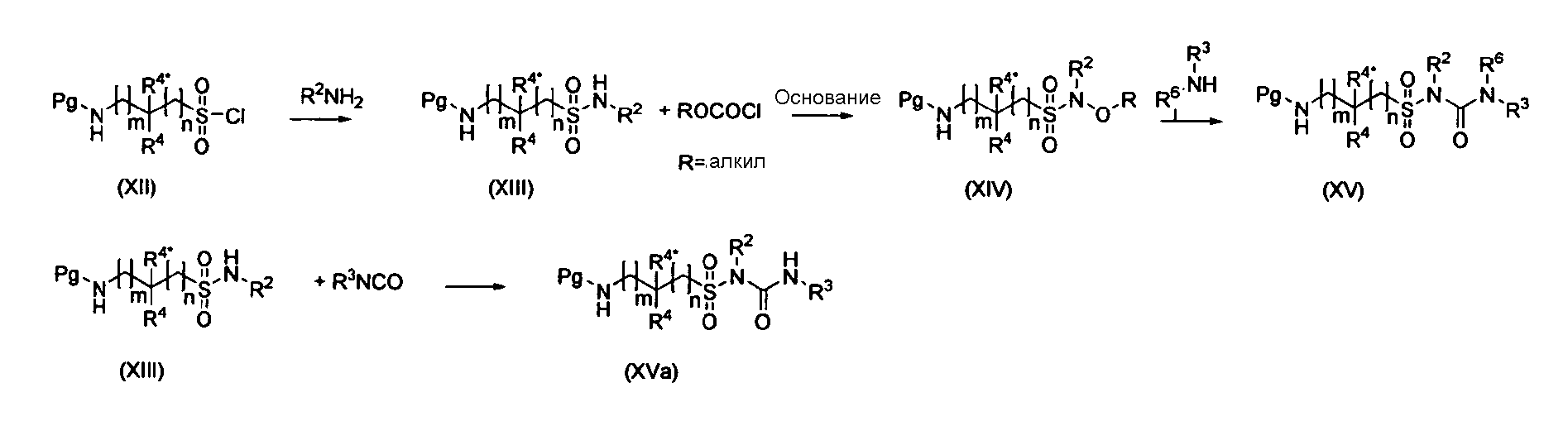
Защитная группа Pg (например, фталимидо, Boc или другая) затем может быть удалена и полученные амины (IIIf) подвергнуты взаимодействию с промежуточными соединениями общей формулы (II) с получением сульфонилмочевин общей формулы (If):
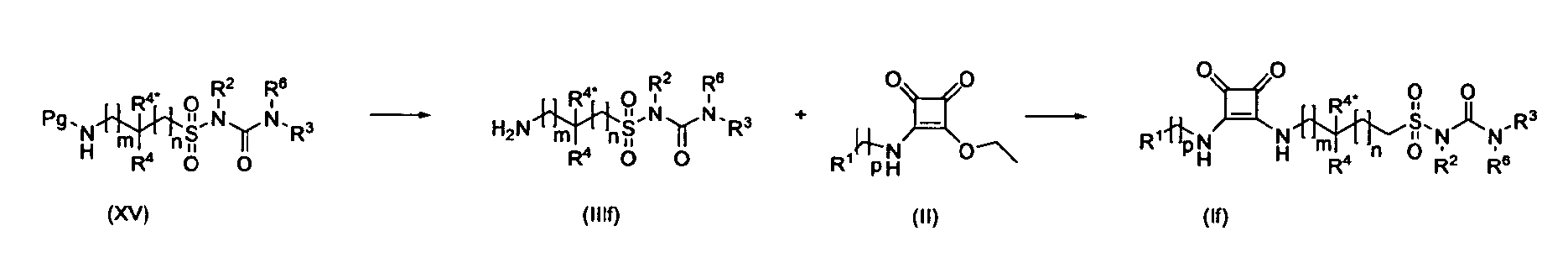
Соединения (I) в соответствии с данным изобретением, которые являются N-алкокси- или N-арилоксикарбаматами или алкил- или арилгидразинкарбоксилатами (Ig), могут быть получены взаимодействием защищенных аминоалкил 4-нитрофенилкарбонатов (XVI) (защитные группы, Boc или фталимидо) с гидроксиламинами или гидразинами (VI) с последующим снятием защиты и последующей реакцией аминов (IIIg) с промежуточными соединениями общей формулы (II) как изображено ниже.
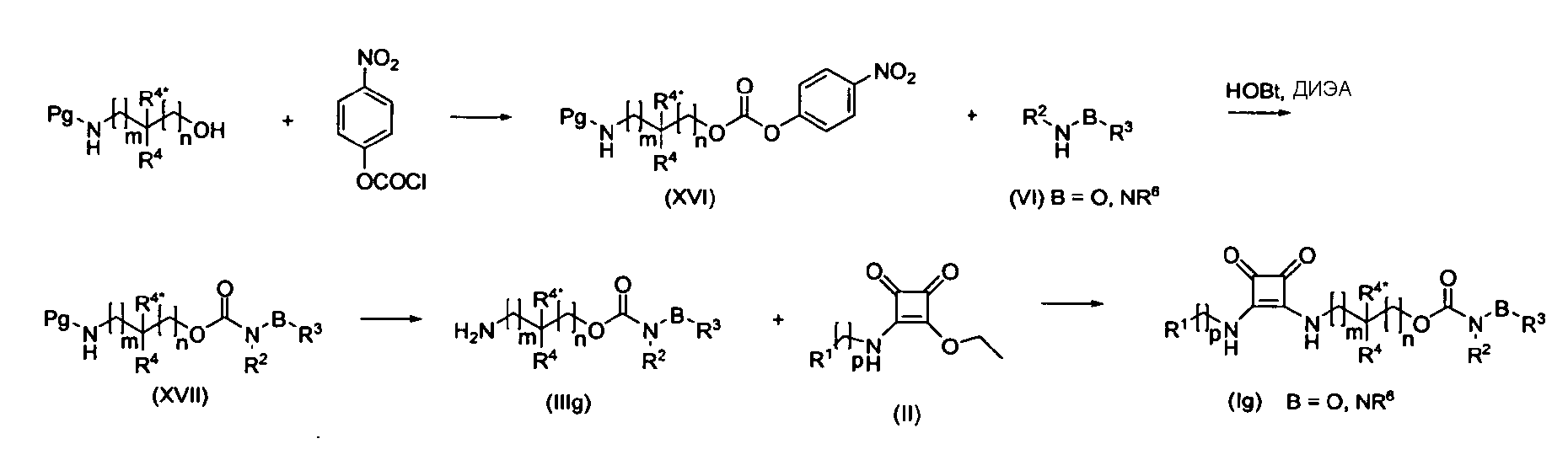
Соединения (I) в соответствии с данным изобретением, которые являются N-алкокси- или N-арилмочевинами или алкил- или арилгидразинкарбоксамидами (Ih), могут быть получены способами, известными специалистам в данной области техники для получения мочевин. Одним таким способом является реакция защищенных 4-нитрофениламиноалкилкарбаматов (XVIII) (защитная группа, например, Boc или фталимидо) с гидроксиламинами или гидразинами (VI) с последующим снятием защиты и последующей реакцией аминов (IIIg) с промежуточными соединениями общей формулы (II) как изображено ниже.
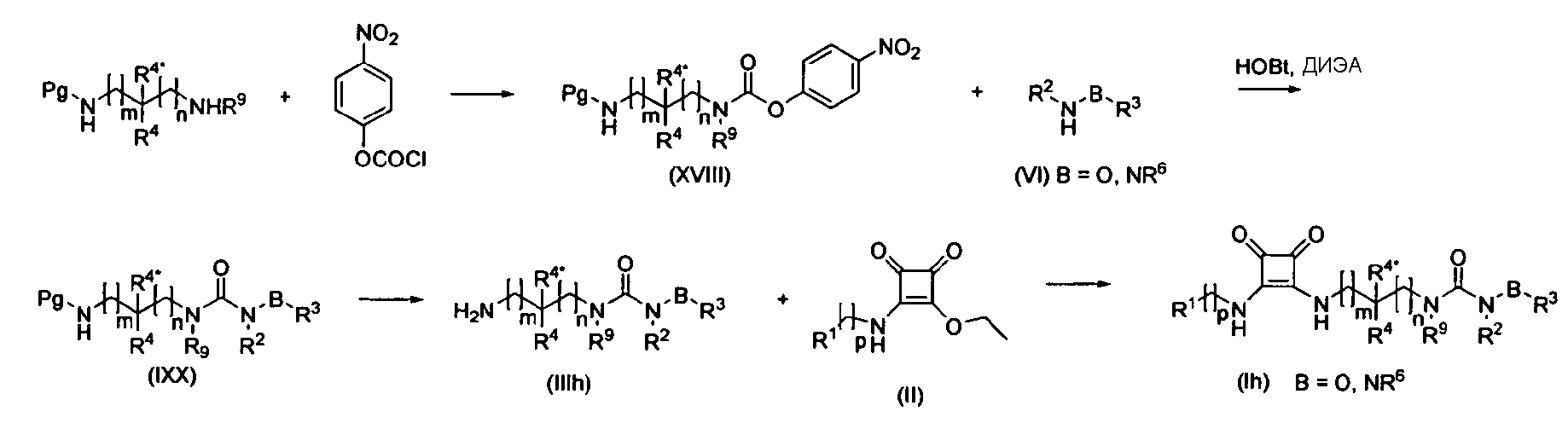
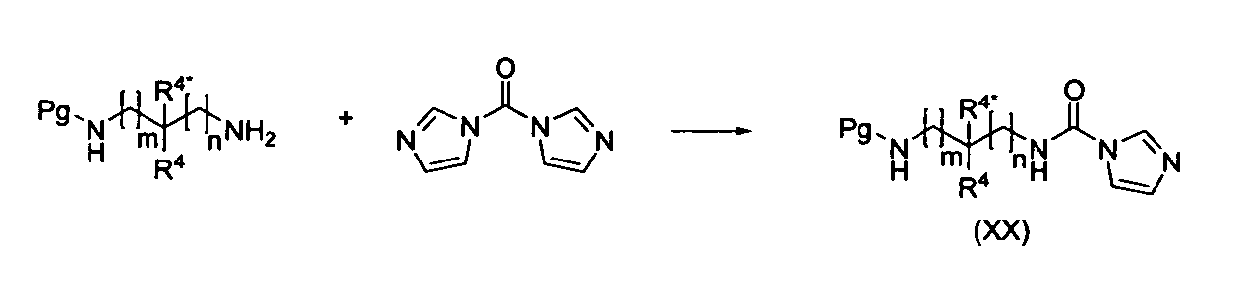
Альтернативно 4-нитрофениламиноалкилкарбаматам (XVIII) могут применяться N-(аминоалкил)-1H-имидазол-1-карбоксамиды (XX).
Применение в медицине
Полагают, что соединения в соответствии с данным изобретением особенно полезны для регулирования в сторону уменьшения НАД через ингибирование ФРТНАМ, и поэтому такие соединения особенно полезны для лечения заболеваний, в которые вовлечена активация NF-κB. Такие способы полезны для лечения различных заболеваний, включая воспалительные заболевания и расстройства восстановления тканей,; особенно ревматоидный артрит, воспалительную болезнь кишечника, астму и ХОЗЛ (хроническое обструктивное заболевание легких), остеоартрит, остеопороз и легочный фиброз; дерматоз, включая псориаз, атопический дерматит и повреждение кожи ультрафиолетом; аутоиммунные заболевания, включая системную красную волчанку, рассеянный склероз, псориазный артрит, анкилозирующий спондилит, отторжение тканей и органов, болезнь Альцгеймера, удар, атеросклероз, рестеноз, диабет, гломерулонефрит, рак, в частности, где рак выбирают из рака молочных желез, простаты, легких, толстой кишки, шейки матки, яичников, кожи, ЦНС, мочевого пузыря, поджелудочной железы, лимфомы, лейкемии или болезни Ходжкина, общее истощение, воспаление, связанное с инфекцией и определенными вирусными инфекциями, включая синдром приобретенного иммунодефицита (СПИД), респираторный дистресс-синдром у взрослых, атаксию-телеангеэктазию.
Следовательно, в данном изобретении представлено соединение формулы (I) для применения в качестве лекарственного средства; более конкретно, для применения в качестве лекарственного средства для лечения заболевания или состояния, вызванного повышенным уровнем фосфорибозилтрансферазы никотинамида (ФРТНАМ), особенно для лечения указанных выше заболеваний или состояний.
Более того, в данном изобретении также представлен способ ингибирования ферментной активности фосфорибозилтрансферазы никотинамида (ФРТНАМ) у млекопитающих, где указанный способ включает стадию введения указанному млекопитающему фармацевтически достаточного количества соединения общей формулы (I).
Далее, в данном изобретении представлен способ лечения заболевания или состояния (в частности, заболеваний и состояний, указанных выше), вызванного повышенным уровнем фосфорибозилтрансферазы никотинамида (ФРТНАМ) у млекопитающего, где указанный способ включает стадию введения указанному млекопитающему фармацевтически достаточного количества соединения общей формулы (I).
В таких способах соединение может вводиться в сочетании с агентом, выводящим из строя ДНК.
Составление фармацевтических композиций
Соединения общей формулы (I) подходящим образом составляют в фармацевтические композиции так, чтобы они подходили для желаемого способа введения.
Способ введения соединений может быть любым подходящим способом, который дает концентрацию в крови или ткани, соответствующую терапевтически эффективной концентрации. Таким образом, например, могут применяться следующие способы введения, хотя данное изобретение ими не ограничено: пероральное введение, парентеральное введение, кожное введение, назальное введение, ректальное введение, вагинальное введение и глазное введение. Специалисту в данной области техники должно быть очевидно, что способ введения зависит от конкретного соединения; в частности, выбор способа введения зависит от физико-химических свойств соединения, а также возраста и массы тела пациента и конкретного заболевания или состояния и его тяжести.
Соединения могут содержаться в любом подходящем количестве в фармацевтической композиции и обычно содержатся в количестве около 1-95%, например 1-10% массовых к общей массе композиции. Композиция может быть представлена в лекарственной форме, которая подходит для перорального, парентерального, ректального, кожного, назального, вагинального и/или глазного способа введения. Таким образом, композиция может быть в форме, например, таблеток, капсул, пилюль, порошков, гранул, суспензий, эмульсий, растворов, гелей, включая гидрогели, паст, мазей, кремов, пластырей, пропиток, устройств доставки, суппозиториев, клизм, инъекций, имплантатов, спреев, аэрозолей и в других подходящих формах.
Фармацевтические композиции могут быть составлены согласно обычно фармацевтической практике, см., например, "Remington's Pharmaceutical Sciences" и "Encyclopedia of Pharmaceutical Technology", под редакцией Swarbrick, J. & J. C. Boylan, Marcel Dekker, Inc., New York, 1988. Обычно определенные здесь соединения составляют с (по крайней мере) фармацевтически приемлемым носителем или наполнителем. Фармацевтически приемлемые носители или наполнители известны специалистам в данной области техники. Получение подходящих солей соединений формулы (I) также очевидно в свете написанного выше.
Таким образом, в данном изобретении, в другом аспекте, представлена фармацевтическая композиция, содержащая соединение общей формулы (I) в сочетании с фармацевтически приемлемым носителем.
Фармацевтические композиции в соответствии с данным изобретением могут быть составлены так, чтобы выделять активное соединение сразу же после введения или в любое заранее определенное время или период времени после введения. Последний тип композиций известен как композиции с контролируемым выделением.
В данном контексте термин "композиция с замедленным выделением" охватывает i) композиции, которые обеспечивают практически постоянную концентрацию лекарственного средства в теле в течение продолжительного периода времени, ii) композиции, которые после заранее определенного периода времени обеспечивают практически постоянную концентрацию лекарственного средства в теле в течение продолжительного периода времени, iii) композиции, которые замедляют действие лекарственного средства в течение определенного заранее периода времени через поддерживание относительно постоянного эффективного уровня лекарственного средства в теле при одновременной минимизации нежелательных побочных эффектов, связанных с колебаниями уровня активного лекарственного вещества в плазме (пилообразная кинетическая схема), iv) композиции, которые локализуют действие лекарственного средства, например, через помещение композиции с контролируемым выделением рядом или в самой болезненной ткани или органе, v) композиции с нацеленным действием лекарственного средства через носители или химические производные, доставляющие лекарственное средство к конкретным целевым клеткам.
Композиции с контролируемым выделением также могут обозначаться как композиции с "замедленным выделением", "пролонгированным выделением", "программируемым выделением", "в течение определенного периода времени", "с контролируемой скоростью" и/или "целевым выделением".
Фармацевтические композиции с контролируемым выделением могут быть представлены в любой подходящей лекарственной форме, особенно в лекарственной форме, предназначенной для перорального, парентерального, кожного, назального, ректального, вагинального и/или глазного введения. Пример включают одноразовые или многоразовые таблетированные или инкапсулированные композиции, масляные растворы, суспензии, эмульсии, микрокапсулы, микросферы, наночастицы, липосомы, устройства доставки, такие как устройства, предназначенные для перорального, парентерального, кожного, назального, вагинального или глазного введения.
Получение твердых лекарственных форм для перорального введения, пероральных лекарственных форм с контролируемым выделением, жидких композиций, парентеральных композиций, ректальных композиций, назальных композиций, чрезкожных и местных композиций, чрезкожных и местных композиций с контролируемым выделением и композиций для введения в глаз известно специалистам в области фармацевтических композиций. Конкретные композиции могут быть найдены в "Remington's Pharmaceutical Sciences".
Капсулы, таблетки и пилюли и т.д. могут содержать, например, следующие соединения: микрокристаллическую целлюлозу, камедь или желатин в качестве связующих агентов; крахмал или лактозу в качестве наполнителей; стеараты в качестве смазывающих агентов; различные подсластители или вкусовые добавки. В случае капсул лекарственная форма может содержать жидкий носитель, такой как жирные масла. Также часть лекарственной формы может составлять оболочка из сахара или энтеросолюбильных агентов. Фармацевтические композиции также могут быть эмульсиями соединения и жира с получением мицелльных эмульсий.
Для парентерального, подкожного, чрезкожного или местного введения, фармацевтическая композиция может включать стерильный разбавитель, буферы, регуляторы тоничности и антибактериальные агенты. Активное соединение может быть смешано с носителями, которые защищают от разложения или немедленного выведения из тела, включая имплантаты или микрокапсулы со свойствами контролируемого выделения. Для внутривенного введения предпочтительными носителями являются физиологический раствор или физиологический раствор с фосфатным буфером.
Дозы
В одном варианте фармацевтическая композиция имеет однократную лекарственную форму. В таких вариантах каждая однократная лекарственная форма обычно содержит 0,1-500 мг, например, 0,1-200 мг, например, 0,1-100 мг соединения.
В общем, соединение, предпочтительно, вводят в количестве около 0,1-250 мг на кг массы тела в сутки, например, около 0,5-100 мг на кг массы тела в сутки.
Для композиций, предназначенных для перорального введения для системного применения, доза обычно составляет от 0,5 мг до 1 г на дозу, вводимую 1-4 раза в сутки в течение от 1 недели до 12 месяцев, в зависимости от лечимого заболевания.
Доза для перорального введения композиции для профилактики заболеваний или состояний обычно составляет от 1 мг до 100 мг на кг массы тела в сутки. Доза может вводиться один или два раза в сутки в течение от 1 недели до воздействия заболевания до 4 недель после воздействия заболевания.
Для композиций, адаптированных для ректального введения, обычно предпочтительно более высокое количество соединения, т.е. от приблизительно 1 мг до 100 мг на кг массы тела в сутки.
Для парентерального введения обычна доза от около 0,1 мг до около 100 мг на кг массы тела в сутки. Для внутривенного введения обычна доза от около 0,1 мг до около 20 мг на кг массы тела в сутки, вводимая от 1 дня до 3 месяцев. Для интраартикулярного введения обычно предпочтительна доза от около 0,1 мг до около 50 мг на кг массы тела в сутки. Для парентерального введения в общем может применяться раствор в водной среде 0,5-2% или более активного ингредиента.
Для местного введения на кожу обычно предпочтительна доза от около 1 мг до около 5 г, вводимая 1-10 раз в сутки в течение от 1 недели до 12 месяцев.
ЭКСПЕРИМЕНТАЛЬНАЯ ЧАСТЬ
Общие методики, получение и примеры
Для ядерного магнитного резонанса приводятся 1H ЯМР спектр (300 МГц) и 13C ЯМР (75,6) значения химических сдвигов (δ) (в ч./млн), если не указано иначе, для растворов дейтериохлороформа по отношению к стандартам тетраметилсилану (δ=0,0) или хлороформу (δ=7,25) или дейтериохлороформу (δ=76,81 для 13C ЯМР). Значение мультиплета, либо определенного (дублет (д), триплет (т), двойной дублет (дд), двойной триплет (дт), квартет (кв)) или нет (м) в приблизительной средней точке дано, если не приведен интервал, (шс) означает широкий синглет.
МС проводят с применением Micromass LCT с пробой AP-ESI или ЖХ-МС с применением Bruker Esquire 3000+ ESI Iontrap с ВЭЖХ системой Agilent 1200 HPLC.
Очистку ВЭЖХ проводят с применением колонки X-Bridge Prep C18 OBD 19x150 мм, с применением градиентов буфера А (0,1% ТФК в H2O) и буфера В (0,1% ТФК в ацетонитриле).
Применяемые органические растворители являются безводными.
3-Этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 3-этокси-4-(пиридин-3-иламино)циклобут-3-ен-2,3-дион получают как описано в J.Med. Chem. (2000) 43 1187-1202.
Применяются следующие аббревиатуры:
|
|
Общая методика 1: реакция аминов общей формулы (III) с 3-этоксициклобут-3-ен-1,2-дионами общей формулы (II)
Амин общей формулы (III) (1,02 экв.) и 3-этоксициклобут-3-ен-1,2-дион общей формулы (II) (1,0 экв.) растворяют в ацетонитриле (если амин является солью, добавляют 1,0 экв. триэтиламина) и перемешивают при кт до полного расходования исходного материала, подтвержденного ТСХ. Продукт либо очищают кристаллизацией, либо хроматографией (хлороформ:метанол:NH3 (25% водн.) 95:5:1) с получением соединений общей формулы (I).
Соль оксалиновой кислоты соединения общей формулы (I) может быть получена растворением соединения общей формулы (I) (1 экв.) в MeCN и добавлением раствора оксалиновой кислоты (2 экв.) в MeCN. Осадок фильтруют и сушат с получением соли оксалиновой кислоты мочевины общей формулы (I).
Общая методика 2: Реакция 4-нитрофеноксикарбонатов общей формулы (XVI) с гидроксиламинами или гидразинами (VI) и последующее снятие защиты
4-Нитрофеноксикарбонат общей формулы (XVI) (1,0 экв.) растворяют в ДМФ, добавляют гидроксиламин или гидразин (VI) (2,0 экв.), HOBt (2 экв.) и ДИЭА (0,5 экв., или 2,5 экв. если гидроксиламин или гидразин является солью) и смесь нагревают до 50°C при перемешивании в течение 4 ч или до поглощения карбоната. Смесь концентрируют и очищают хроматографией (1-5% MeOH в ДХМ). Полученное Boc-защищенное соединение общей формулы (XVII) растворяют в MeOH и добавляют 3N HCl в MeOH при перемешивании. Через 2 ч смесь концентрируют и соединение используют напрямую как соль HCl или очищают хроматографией (хлороформ:метанол:NH3 (25% водн.) 95:5:1) с получением соединения общей формулы (III g).
Общая методика 3: Реакция 4-нитрофеноксикарбаматов общей формулы (XVIII) с гидроксиламинами или гидразинами (VI) и последующее снятие защиты
4-Нитрофеноксикарбамат общей формулы (XVII) (1,0 экв.) растворяют в ДМФ, добавляют гидроксиламин или гидразин (2,0 экв.), HOBt (2 экв.) и ДИЭА (0,5 экв., или 2,5 экв., если гидроксиламин или гидразин является солью) и смесь нагревают до 50°C при перемешивании в течение 4 ч или до поглощения карбамата. Смесь концентрируют и очищают хроматографией (1-5% MeOH в ДХМ). Полученное Boc-защищенное соединение общей формулы (IXX) растворяют в MeOH и добавляют 3N HCl в MeOH при перемешивании. Через 2 ч смесь концентрируют и соединение применяют в виде соли HCl или очищают хроматографией (хлороформ:метанол:NH3 (25% водн.) 95:5:1) с получением соединения общей формулы (IIIh).
Общая методика 4: Реакция аминов с 3,4-диэтоксициклобут-3-ен-1,2-дион с получением промежуточных соединений общей формулы (II)
Амин (1,0 экв.) и 3,4-диэтоксициклобут-3-ен-1,2-дион (1,0 экв.) растворяют в EtOH и нагревают до 80°C в течение ночи, концентрируют и очищают хроматографией (1-5% MeOH в ДХМ) с получением промежуточного соединения общей формулы (II).
Получение 1: трет-бутил 5-((4-нитрофенокси)карбонилокси)пентилкарбамата (соединение 1)
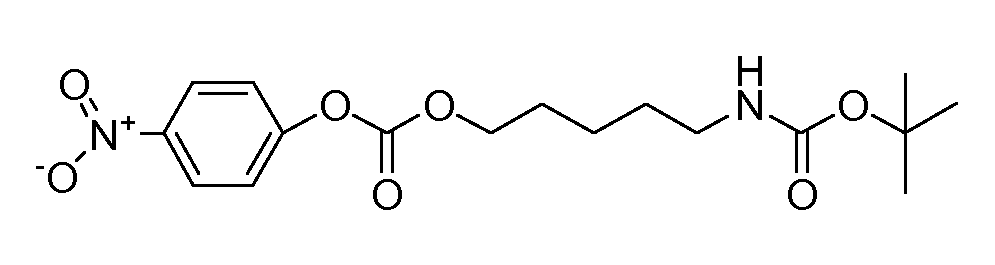
втор-Бутил 5-гидроксипентилкарбамат (950 мг, 4,67 ммоль) растворяют в EtOAc, добавляют 4-нитрофенилкарбонохлоридат (1,130 г, 5,14 ммоль), смесь охлаждают на ледяной бане, добавляют триэтиламин (0,85 мл, 6,07 ммоль) при перемешивании и смесь постепенно нагревают до кт и перемешивают в течение ночи. Смесь переносят в делительную воронку с EtOAc и H2O и встряхивают. Органическую фазу экстрагируют 1N HCl, H2O, NAHCO3 (водн., насыщ.), H2O (дважды), насыщенным раствором соли, сушат над Mg2SO4, фильтруют и концентрируют. Остаток очищают хроматографией (смеси петролейного эфира и EtOAc) с получением соединения 1.
1Н ЯМР (CDCl3): δ 8,28 (м, 2H), 7,39 (м, 2H), 4,52 (шс, 1H), 4,29 (т, 2H), 3,15 (м, 2H), 1,79 (м, 2H), 1,53 (м, 4H), 1,44 (с, 9H).
Получение 2: гидрохлорида 5-(бензилоксикарбамоилокси)пентан-
1-амино (соединение 2)
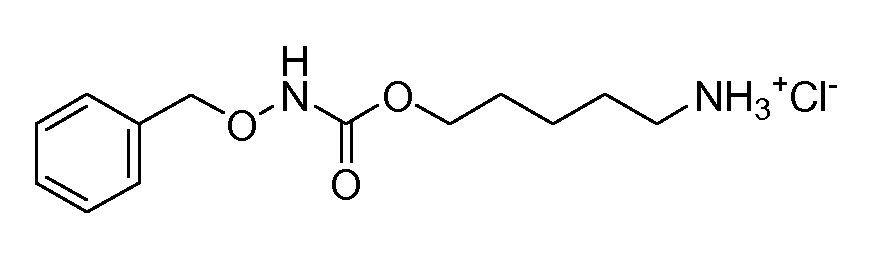
Общая методика 2. Исходные материалы: соединение 1 и гидрохлорид O-бензилгидроксиламин.
1Н ЯМР (CD3OD): δ 7,39 (м, 5H), 4,82 (с, 2H), 4,15 (т, 2H), 2,94 (м, 2H), 1,71 (м, 4H), 1,48 (м, 2H).
Получение 3: гидрохлорида 5-(циклогексилоксикарбамоилокси)пентан-1-амино (соединение 3)
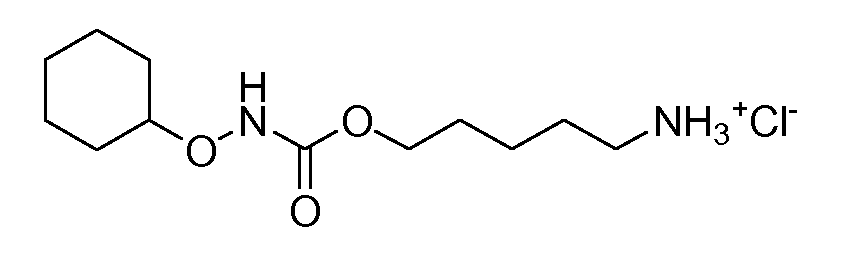
Общая методика 2. Исходные материалы: соединение 1 и O-циклогексилгидроксиламин.
1Н ЯМР (CD3OD): δ 4,14 (т, 2H), 3,70 (м, 1H), 2,95 (м, 2H), 1,91 (м, 2H), 1,85-1,2 (м, 14H).
Получение 4: 5-аминопентил циклогексилоксикарбамат
(соединение 4)
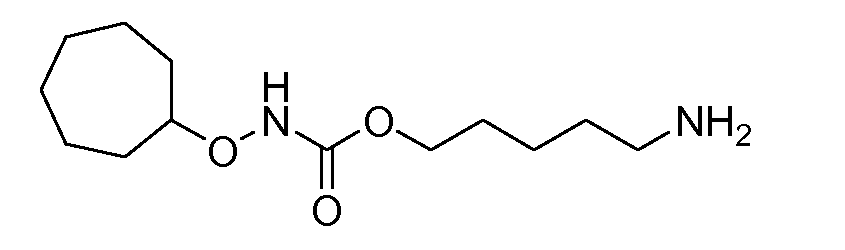
Общая методика 2. Исходные материалы: соединение 1 и O-циклогептилгидроксиламин.
1Н ЯМР (CDCl3): δ 4,14 (т, 2H), 3,91 (м, 1H), 2,71 (т, 2H), 2,08 (шс, 2H), 1,97 (м, 2H), 1,75-1,25 (м, 16H).
Получение 5: 5-аминопентил циклогексилокси(3-фенилпропил)карбамат (соединение 5)
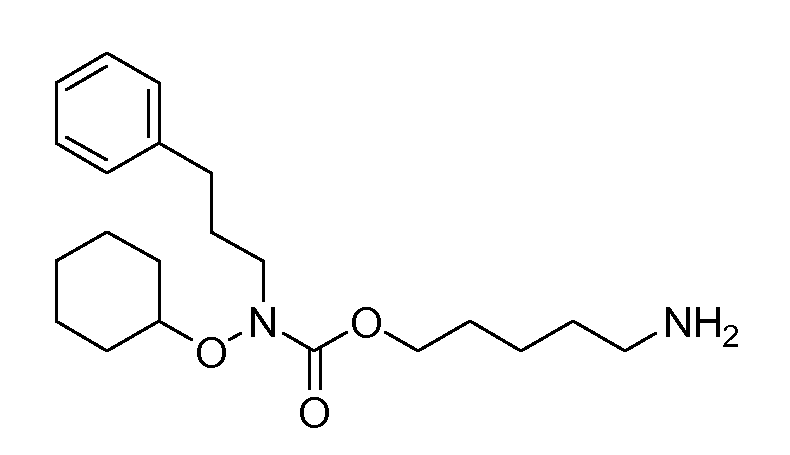
Общая методика 2. Исходные материалы: соединение 1 и O-циклогексил-N-(3-фенилпропил)гидроксиламин.
1Н ЯМР (CDCl3): δ 7,31-7,14 (м, 5H), 4,12 (т, 2H), 3,77 (м, 1H), 3,51 (т, 2H), 2,71 (т, 2H), 2,63 (т, 2H), 1,97 (м, 2H), 1,9 (шс, 2Н), 1,8-1,5 (м, 16H).
Получение 6: дигидрохлорид 5-аминопентилциклогексил(2-морфолиноэтокси)карбамата (соединение 6)
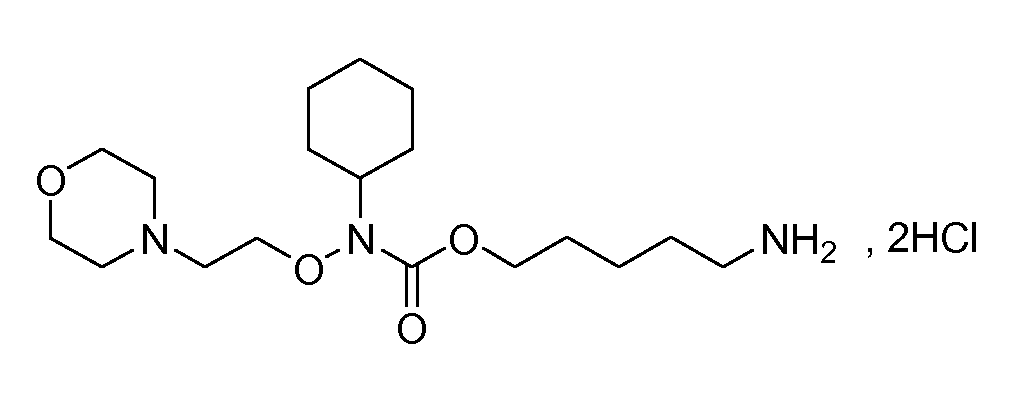
Общая методика 2. Исходные материалы: соединение 1 и N-циклогексил-O-(2-морфолиноэтил)гидроксиламин.
1Н ЯМР (ДМСО-d6): δ 11,44 (шс, 1H), 7,97 (шс, 3H), 4,22 (т, 2H), 4,09 (т, 2H), 3,97 (м, 2H), 3,83 (м, 2H), 3,72 (м, 1H), 3,40 (м, 4H), 3,14 (м, 2H), 2,77 (м, 2H), 1,8-1,0 (м, 16Н).
Получение 7: 5-аминопентил циклогексилокси(изопропил)карбамат (соединение 7)
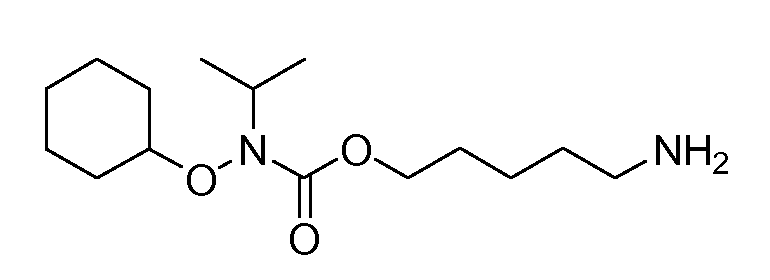
Общая методика 2. Исходные материалы: соединение 1 и O-циклогексил-N-изопропилгидроксиламин.
1Н ЯМР (CDCl3): δ 4,17 (м, 1H), 4,12 (т, 2H), 3,70 (м, 1H), 2,70 (т, 2H), 1,99 (м, 2H), 1,77 (м, 2H), 1,68 (м, 2H), 1,6-1,1 (м, 10H), 1,19 (д, 6H)
Получение 8: дигидрохлорид 5-аминопентил 2-морфолиноэтоксикарбамата (соединение 8)
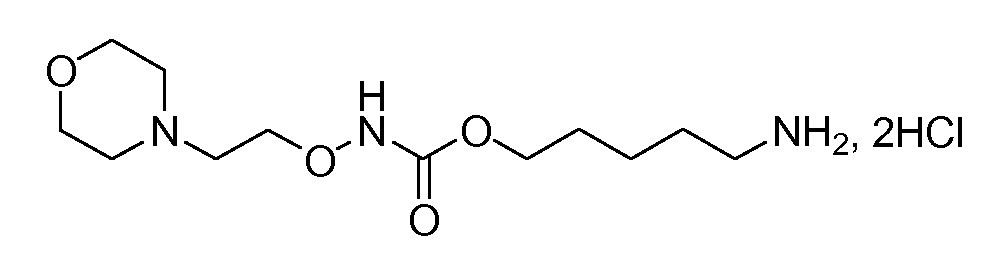
Общая методика 2. Исходные материалы: соединение 1 и O-(2-морфолиноэтил)гидроксиламин.
1Н ЯМР (ДМСО-d6): δ 11,14 (шс, 1H), 10,63 (шс, 1H), 7,92 (шс, 3H), 4,15 (т, 2H), 4,05 (т, 2H), 3,97 (м, 2H), 3,81 (м, 2H), 3,43 (м, 4H), 3,08 (м, 2H), 2,77 (м, 2H), 1,59 (м, 4H), 1,35 (м, 2H).
Получение 9: трет-бутил 5-((4-нитрофенокси)карбониламино)пентилкарбамат (соединение 9)
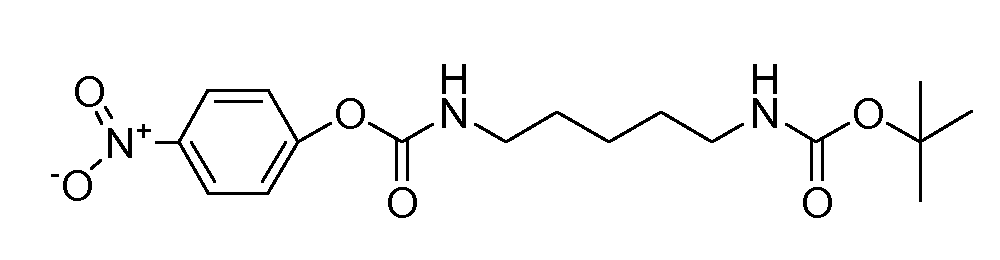
трет-Бутил 5-аминопентилкарбамат (2,02 г, 10 ммоль) растворяют в EtOAc, добавляют 4-нитрофенилкарбонохлоридат (2,22 г, 11 ммоль), смесь охлаждают на ледяной бане, добавляют ДИЭА (2,05 мл, 12 ммоль) при перемешивании и смесь постепенно нагревают до кт и перемешивают в течение 3 ч. Смесь переносят в делительную воронку с EtOAc и H2O и встряхивают. Органическую фазу экстрагируют 1N HCl, H2O, 5% NA2CO3, H2O (три раза), насыщенным раствором соли, сушат над Mg2SO4, фильтруют и концентрируют с получением соединения 9.
1Н ЯМР (CDCl3): δ 8,24 (м, 2H), 7,39 (м, 2H), 5,32 (шс, 1H), 4,56 (шс, 1H), 3,29 (кв, 2H), 3,14 (м, 2H), 1,7-1,3 (м, 6H), 1,44 (с, 9H).
Получение 10: 1-(5-аминопентил)-3-(циклогексилокси)мочевина (соединение 10)
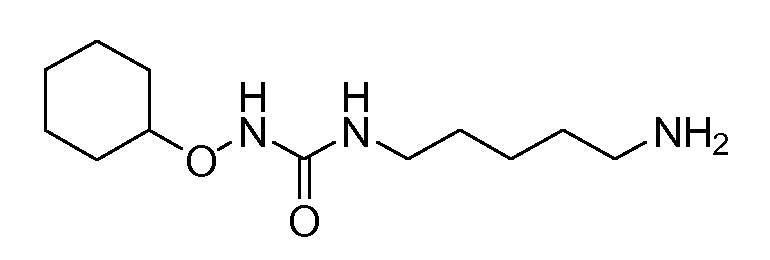
Общая методика 3. Исходные материалы: соединение 9 и O-циклогексилгидроксиламин.
1Н ЯМР (CDCl3): δ 6,89 (шс, 1H), 5,72 (т, 1H), 3,66 (м, 1H), 3,27 (кв, 2H), 2,70 (т, 2H), 1,96 (м, 2H), 1,74 (м, 2H), 1,65-1,15 (м, 14H).
Получение 11: 1-(5-аминопентил)-3-(циклогептилокси)мочевина (соединение 11)
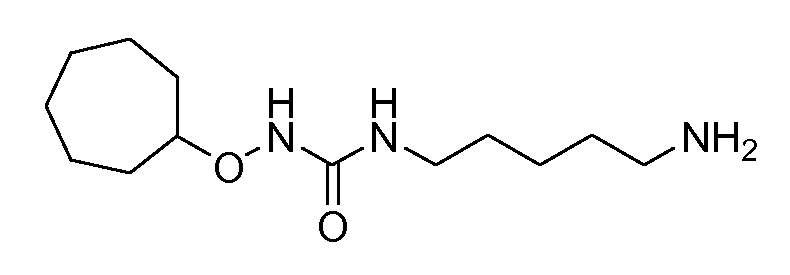
Общая методика 3. Исходные материалы: соединение 9 и O-циклогептилгидроксиламин.
1Н ЯМР (CDCl3): δ 5,72 (т, 1H), 4,87 (шс, 1H), 3,83 (м, 1H), 3,42 (шс, 2H), 3,24 (кв, 2H), 2,72 (т, 2H), 1,96 (м, 2H), 1,7-1,25 (м, 16H).
Получение 12: дигидрохлорид 1-(5-аминопентил)-3-(2-морфолиноэтокси)мочевины (соединение 12)
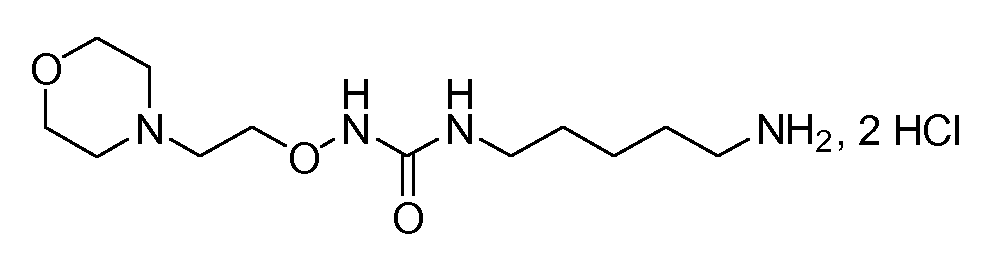
Общая методика 3. Исходные материалы: соединение 9 и O-(2-морфолиноэтил)гидроксиламин.
1Н ЯМР (ДМСО-d6): δ 11,38 (шс, 1H), 9,25 (шс, 1H), 7,92 (шс, 3H), 7,25 (т, 1H), 4,08 (м, 2H), 3,94 (м, 4H), 3,41 (м, 4H), 3,08 (м, 4H), 2,75 (м, 2H), 1,56 (м, 2H), 1,45 (м, 2H), 1,30 (м, 2H).
Получение 13: гидрохлорид 1-(5-аминопентил)-3-(бензилокси)мочевины (соединение 13)
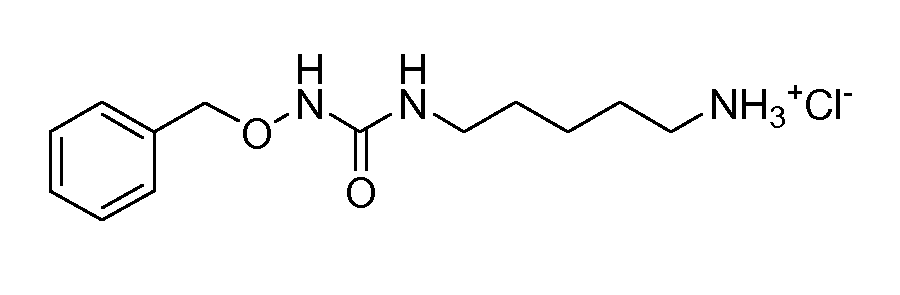
Общая методика 3. Исходные материалы: соединение 9 и гидрохлорид O-бензилгидроксиламина.
1Н ЯМР (ДМСО-d6): δ 9,05 (шс, 1H), 7,94 (шс, 3H), 7,37 (м, 5H), 6,76 (шс, 1H), 4,71 (с, 2H), 3,03 (т, 2H), 2,74 (м, 2H), 1,55 (м, 2H), 1,40 (м, 2H), 1,25 (м, 2H).
Получение 14: дигидрохлорид 3-(5-аминопентил)-1-циклогексил-1-(2-морфолиноэтокси)мочевины (соединение 14)
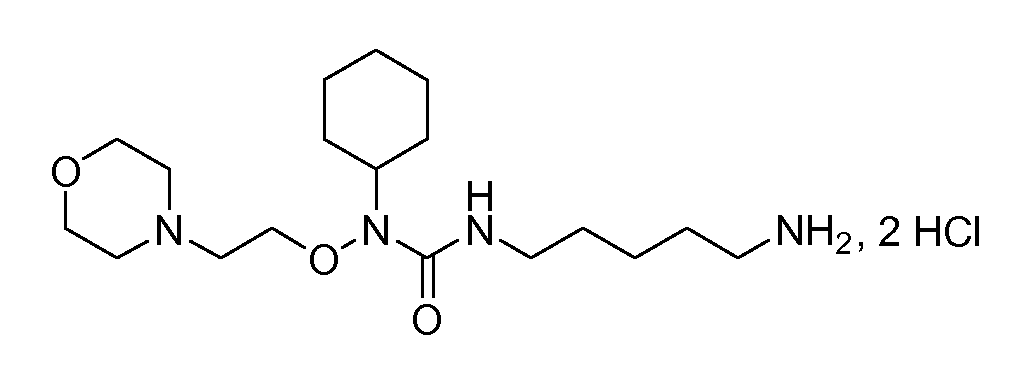
Общая методика 3. Исходные материалы: соединение 9 и N-циклогексил-O-(2-морфолиноэтилгидроксиламин.
1Н ЯМР (ДМСО-d6): δ 11,68 (шс, 1H), 7,88 (шс, 3H), 7,48 (т, 1H), 4,15 (т, 2H), 3,95 (м, 4H), 3, 3,72 (м, 1H), 3,44 (м, 4H), 3,10 (м, 4H), 2,75 (м, 2H), 1,85-0,95 (м, 16)
Получение 15: 3-Этокси-4-((пиридин-4-иламино)метил)циклобут-3-ен-1,2-дион (соединение 15)
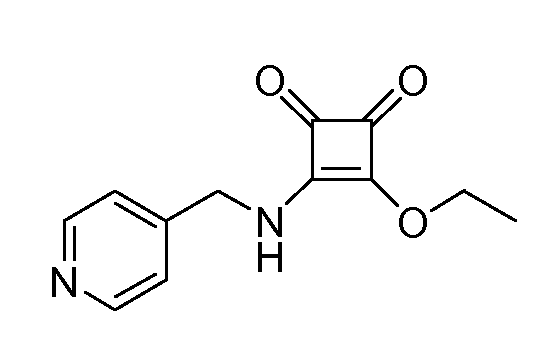
Общая методика 4. Исходный материал: 4-пиколиламин.
1Н ЯМР (ДМСО-d6): δ 9,21 (дт, 1H), 8,55 (м, 2H), 7,31 (м, 2H), 4,60 (м, 4H), 1,33 (дт, 3H).
Получение 16: 3-Этокси-4-((пиридин-3-иламино)метил)циклобут-3-ен-1,2-дион (соединение 16)
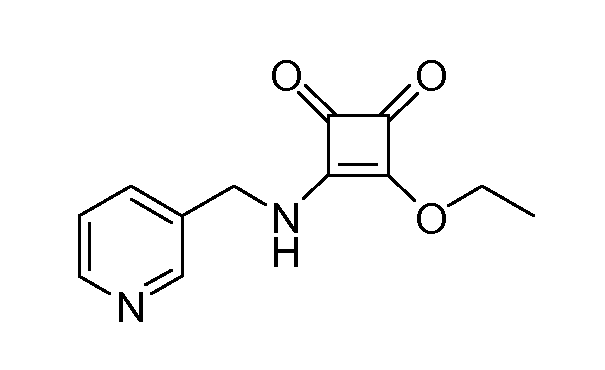
Общая методика 4. Исходный материал: 3-пиколиламин.
1Н ЯМР (ДМСО-d6): δ 9,20 (шс, 1H), 8,51 (м, 2H), 7,73 (м, 1H), 7,41 (м, 1H), 4,64 (м, 4H), 1,35 (м, 3H).
ПРИМЕРЫ
Пример 1: 3-(6-(Морфолиносульфонил)гексиламино)-4-(пиридин-
4-иламино)циклобут-3-ен-1,2-дион (соединение 1001)
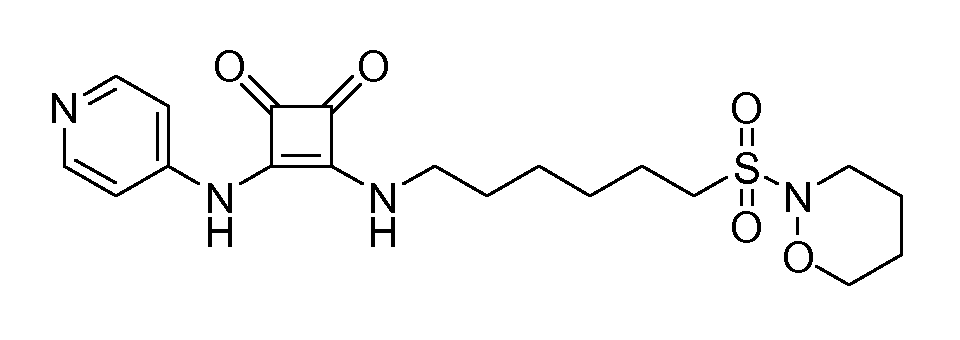
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(морфолиносульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,42-8,40 (м, 2H), 7,82 (шс, 1H), 7,44-7,42 (м, 2H), 4,03 (т, 2H), 3,64-3,58 (м, 2H), 3,03-3,18 (м, 4H), 1,82-1,33 (м, 12H).
Пример 2: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексан-1-сульфонамид (соединение 1002)
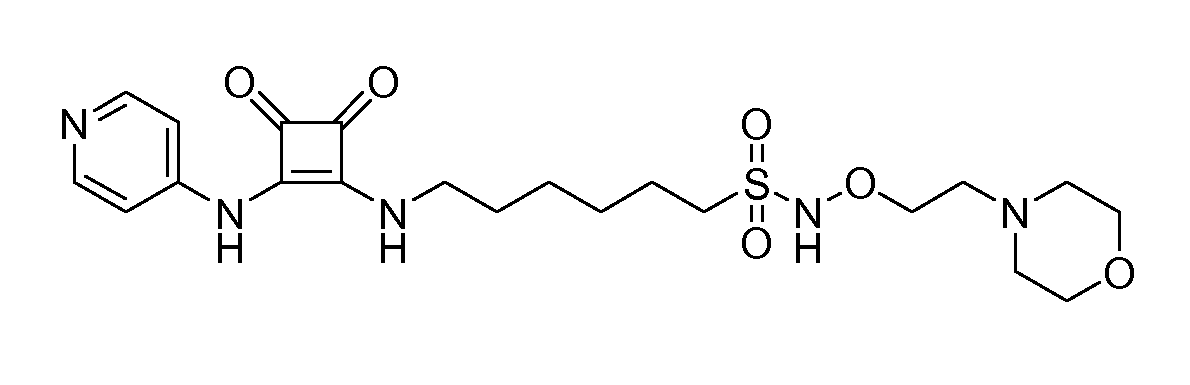
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-морфолиноэтокси)гексанe-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,61 (шс, 1H), 8,41-8,39 (м, 2H), 7,89 (шс, 1H), 7,44-7,42 (м, 2H), 6,92 (шс, 1H), 3,63-3,54 (м, 6H), 3,06-3,01 (м, 4H), 2,39-2,35 (м, 6H), 1,69-1,55 (м, 4H), 1,42-1,32 (м, 4H).
Пример 3: N-Циклогептил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексан-1-сульфонамид
(соединение 1003)
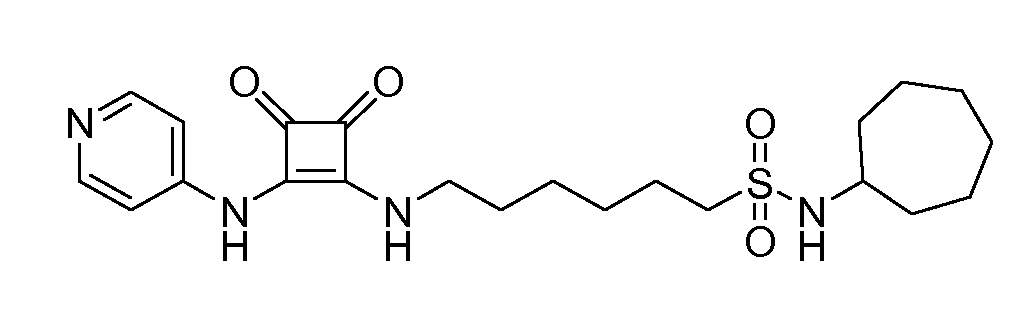
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогептилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39-8,37 (м, 2H), 7,56-7,54 (м, 2H), 3,74 (т, 2H), 3,44-3,36 (м, 3H), 3,06-3,01 (м, 2H), 2,02-1,93 (м, 2H), 1,86-1,42 (м, 16H).
Пример 4: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)гексан-1-сульфонамид
(соединение 1004)
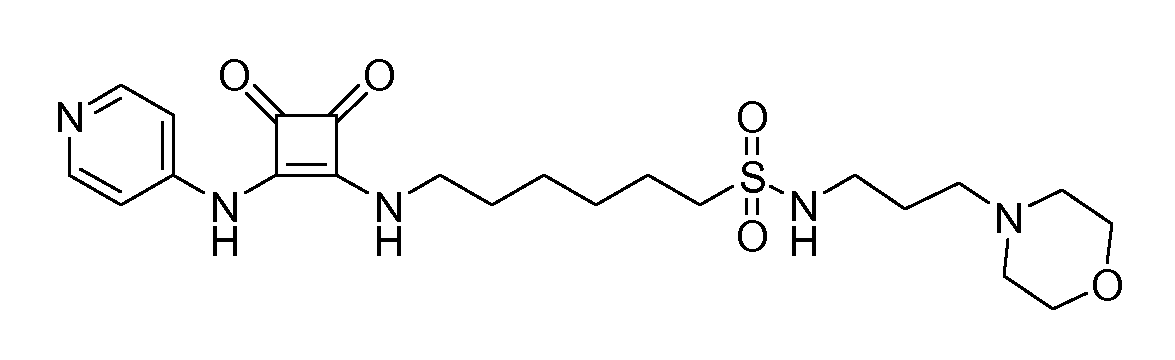
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,87 (шс, 1H), 8,42-8,40 (м, 2H), 7,84 (шс, 1H), 7,44-7,42 (м, 2H), 7,00 (шс, 1H), 3,63-3,53 (м, 6H), 2,99-2,91 (м, 4H), 2,33-2,27 (м, 6H), 1,67-1,54 (м, 6H), 1,45-1,34 (м, 4H).
Пример 5: N-Бензил-N-(циклогексилметокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексан-1-сульфонамид (соединение 1005)
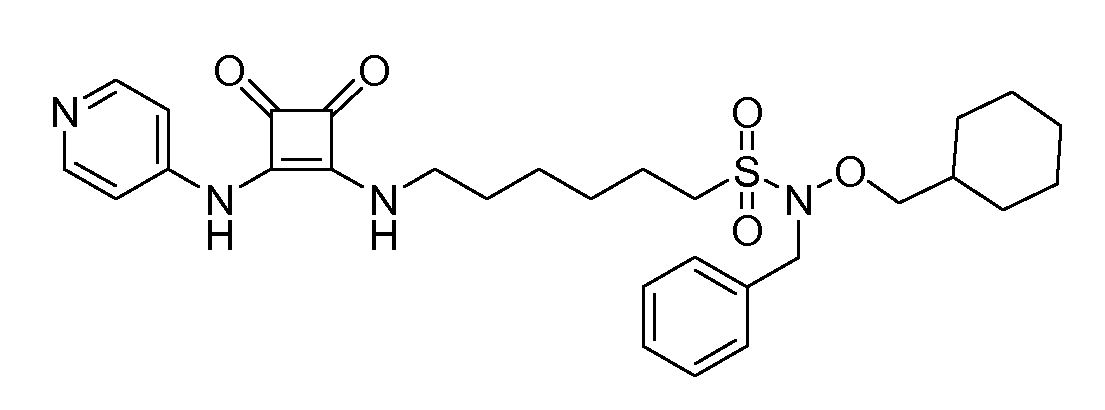
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-бензил-N-(циклогексилметокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 10,14 (шс, 1H), 8,40 (д, 2H), 8,09 (шс, 1H), 7,46-7,36 (м, 7H), 4,32 (с, 2H), 3,65-3,60 (м, 2H), 3,37-3,19 (м, 4H), 1,86-1,76 (м, 2H), 1,65-0,99 (м, 15H), 0,74-0,61 (м, 1H).
Пример 6: N-(2-циклогексилэтил)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексан-1-сульфонамид
(соединение 1006)
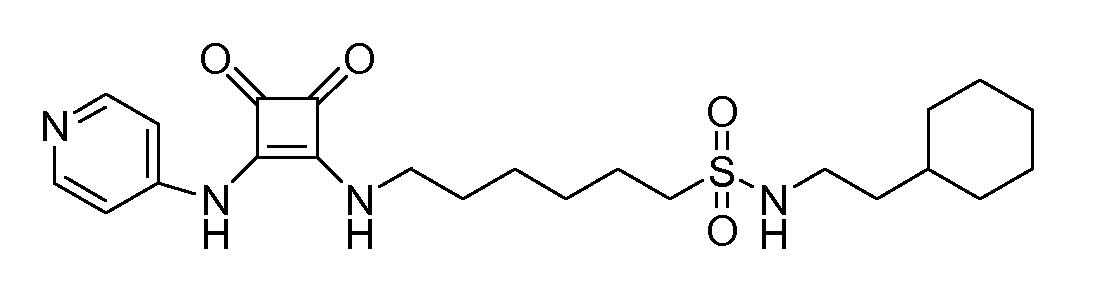
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-циклогексилэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,56 (м, 2H), 3,74 (т, 2H), 3,06 (м, 4H), 1,9-1,1 (м, 19H), 0,94 (м, 2H).
Пример 7: N-циклогексил-7-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гептанамид (соединение 1007)
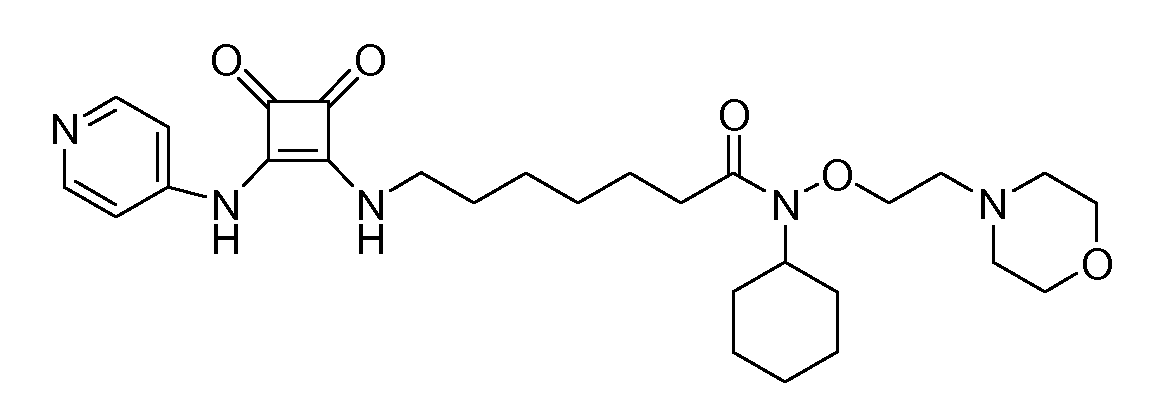
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-циклогексил-N-(2-морфолиноэтокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 4,08 (м, 3H), 3,71 (м, 6H), 2,67 (т, 2H), 2,56 (м, 4H), 2,51 (т, 2H), 1,9-1,1 (м, 19H).
Пример 8: N-(2-циклогексилэтокси)-6-(3,4-диоксо-2-
(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-(2-(2-метоксиэтокси)этокси)этил)гексан-1-сульфонамид
(соединение 1008)
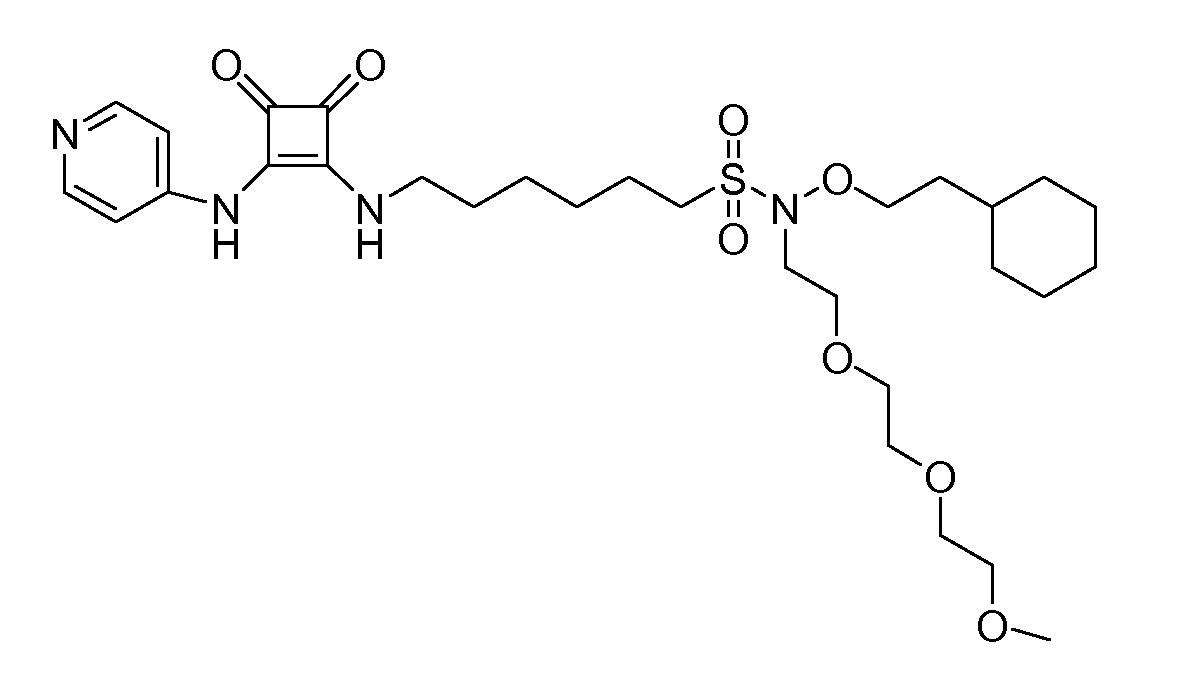
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-циклогексилэтокси)-N-(2-(2-(2-метоксиэтокси)этокси)этил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,40 (м, 2H), 7,62 (м, 2H), 4,08 (т, 2H), 3,8-3,6 (м, 10H), 3,55 (м, 2H), 3,44 (м, 4H), 3,38 (с, 3H), 3,20 (м, 2H), 1,91 (м, 2H), 1,85-1,1 (м, 17H), 0,95 (м, 2H).
Пример 9: N-(2-циклогексилэтокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1009)
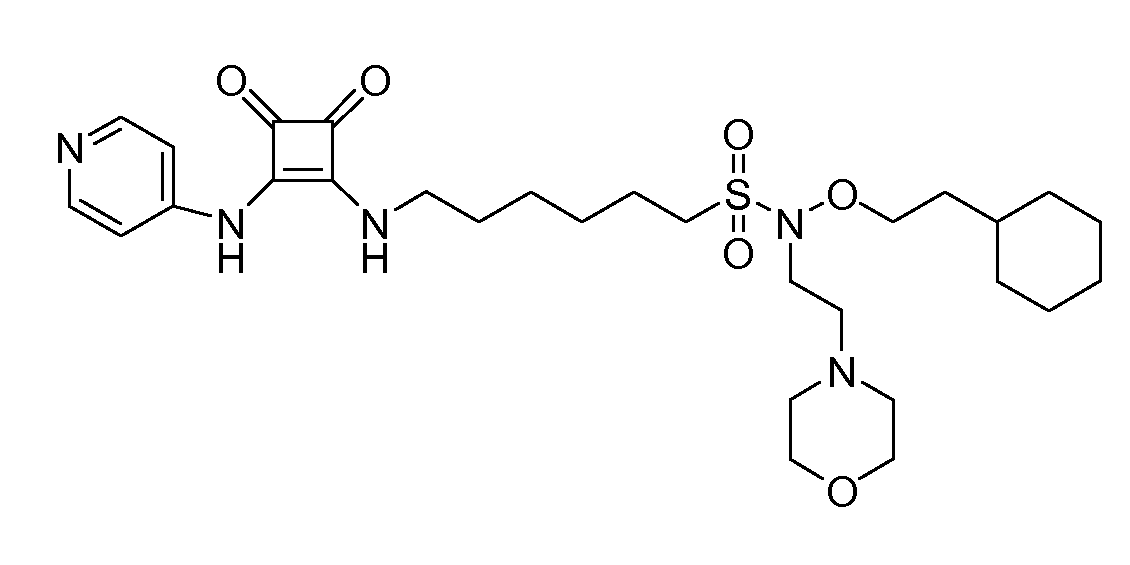
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-циклогексилэтокси)-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,58 (м, 2H), 4,10 (т, 2H), 3,75 (м, 2H), 3,71 (м, 4H), 3,41 (т, 2H), 3,21 (м, 2H), 2,67 (т, 2H), 2,53 (м, 4H), 1,91 (м, 2H), 1,8-1,1 (м, 17H), 0,93 (м, 2H).
Пример 10: N-бензил-N-(2-циклогексилэтокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексан-1-сульфонамид (соединение 1010)
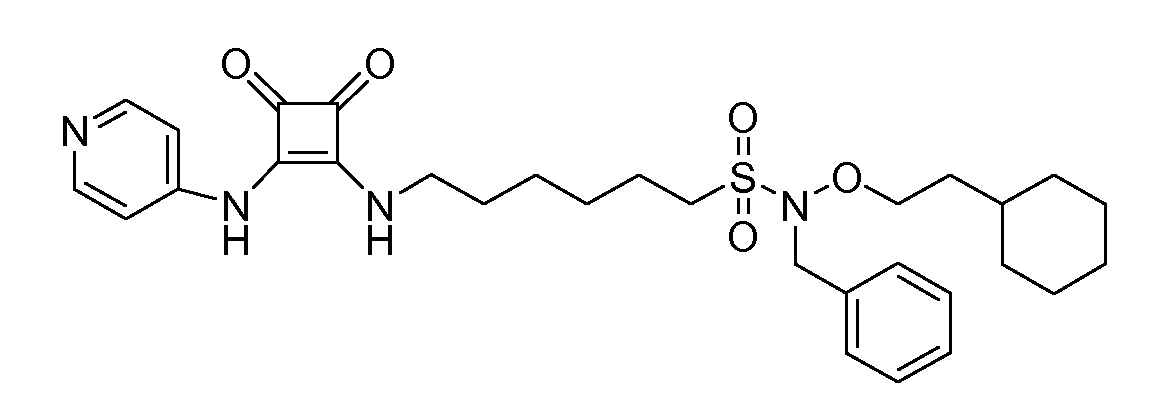
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-бензил-N-(2-циклогексилэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,95 (шс, 1H), 8,38 (м, 2H), 7,85 (шс, 1H), 7,39 (м, 7H), 4,32 (с, 2H), 3,63 (м, 2H), 3,56 (м, 2H), 3,27 (м, 2H), 1,82 (м, 2H), 1,65-0,95, 0,64 (м, 2H).
Пример 11: N-(2-циклогексилэтокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-метилгексан-1-сульфонамид (соединение 1011)
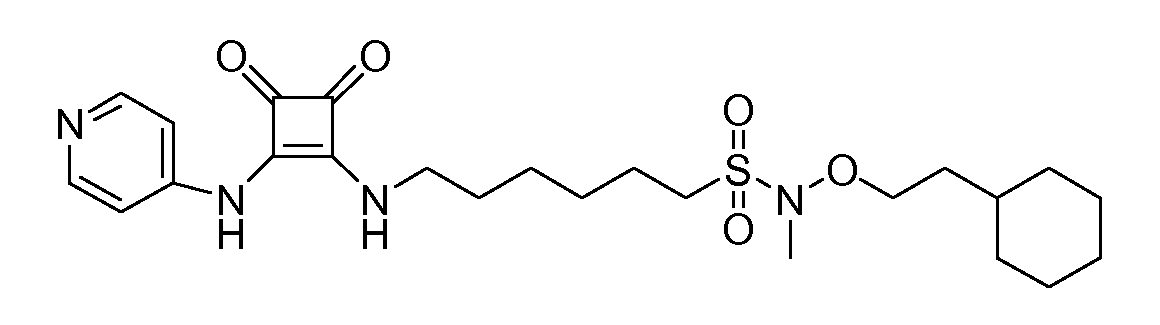
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-циклогексилэтокси)-N-метилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 4,00 (т, 2H), 3,75 (м, 2H), 3,17 (м, 2H), 3,01 (с, 3H), 1,89 (м, 2H), 1,8-1,1 (м, 17H), 0,94 (м, 2H).
Пример 12: N-(циклогептилокси)-7-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гептанамид (соединение 1012)
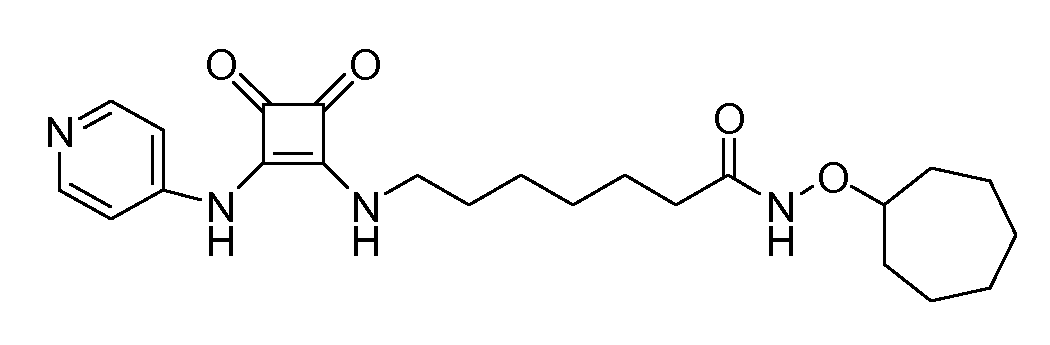
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-(2-циклогептилокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 3,94 (м, 1H), 3,74 (м, 2H), 2,12 (т, 2H), 1,98 (м, 2H), 1,75-1,25 (м, 18H).
Пример 13: N-(циклогептилокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексанамид (соединение 1013)
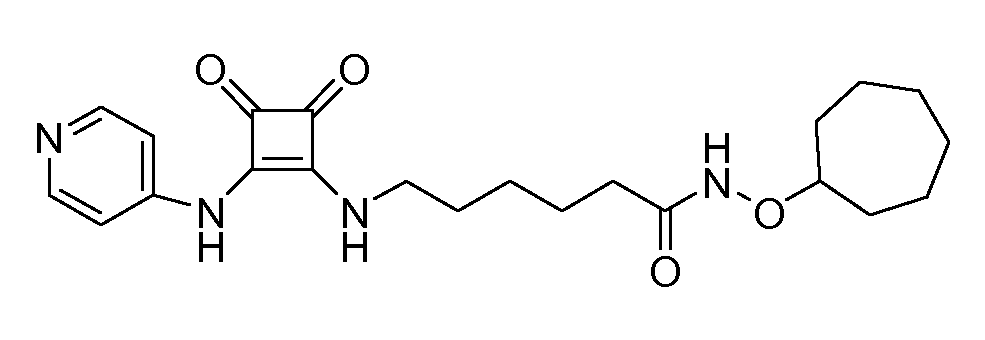
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-циклогептилокси)гексанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39 (м, 2H), 7,57 (м, 2H), 3,93 (м, 1H), 3,74 (т, 2H), 2,14 (т, 2H), 1,95 (м, 2H), 1,8-1,25 (м, 16H).
Пример 14: N-(циклогептилокси)-8-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)октанамид (соединение 1014)
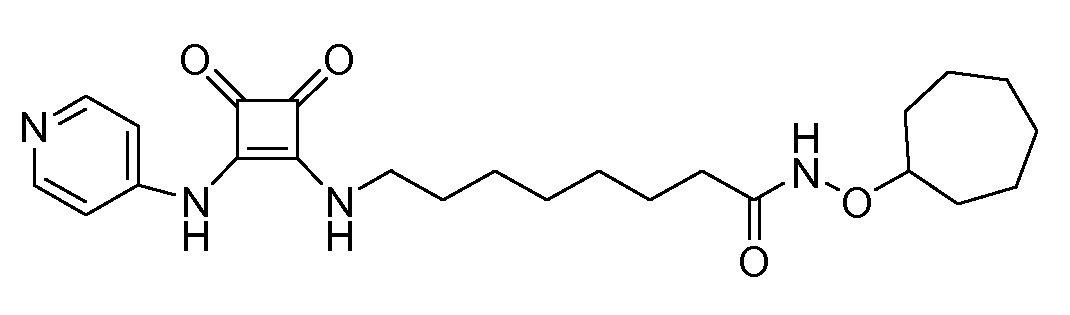
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 8-амино-N-(2-циклогептилокси)октанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,56 (м, 2H), 3,94 (м, 1H), 3,74 (м, 2H), 2,12 (т, 2H), 1,98 (м, 2H), 1,8-1,25 (м, 20H).
Пример 15: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)-N-(пиридин-3-илметил)гексан-1-сульфонамид (соединение 1015)
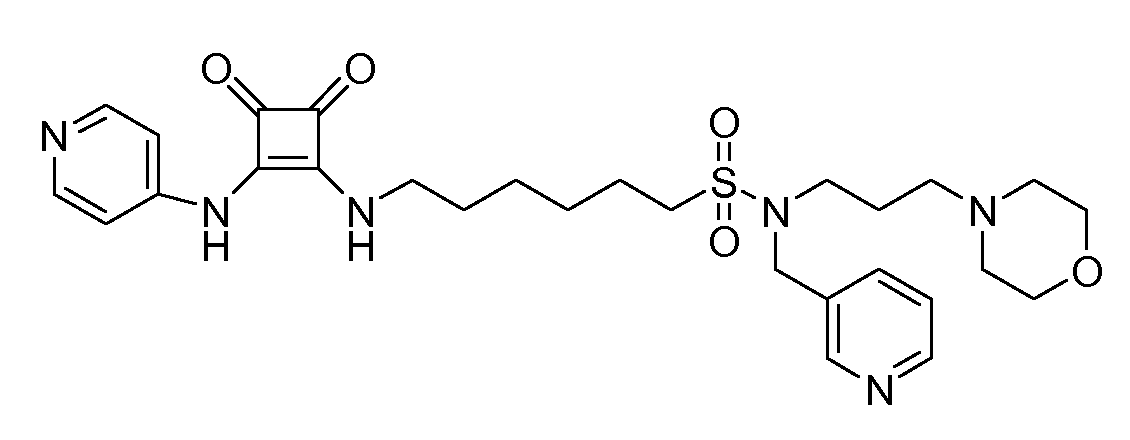
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(3-морфолинопропил)-N-(пиридин-3-илметил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,61 (д, 1H), 8,51 (м, 1H), 8,38 (м, 2H), 7,96 (м, 1H), 7,55 (м, 2H), 7,48 (м, 1H), 4,50 (с, 2H), 3,75 (м, 2H), 3,63 (м, 4H), 3,30 (м, 2H), 3,14 (м, 2H), 2,32 (м, 4H), 2,26 (м, 2H), 1,4-1,9 (м, 10H).
Пример 16: N-бензил-7-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гептанамид (соединение 1016)
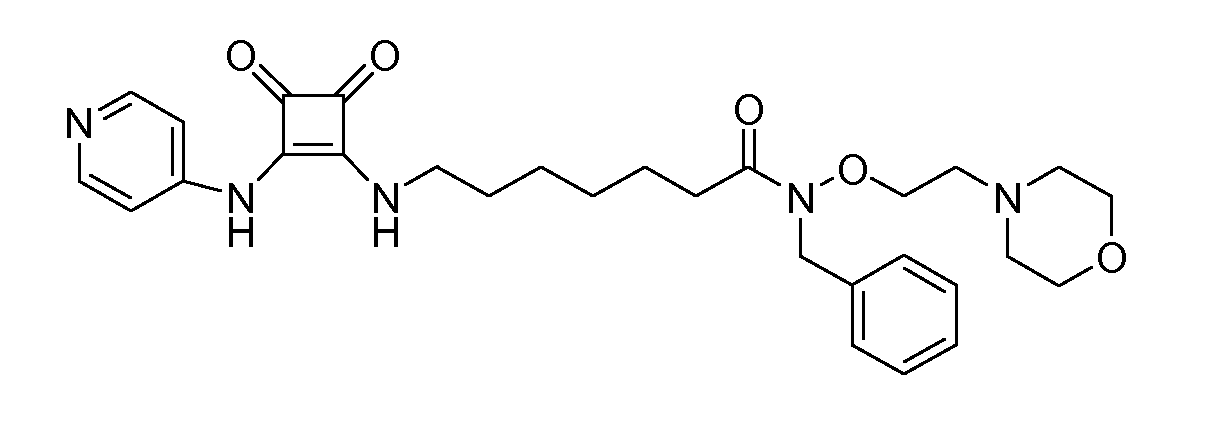
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-бензил-N-(2-морфолиноэтокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,54 (м, 2H), 7,33 (м, 5H), 4,86 (с, 2H), 4,03 (т, 2H), 3,72 (т, 2H), 3,64 (м, 4H), 2,59 (м, 4H), 2,44 (м, 4H), 1,68 (м, 4H), 1,44 (м, 4H).
Пример 17: N-бензил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексанамид (соединение 1017)
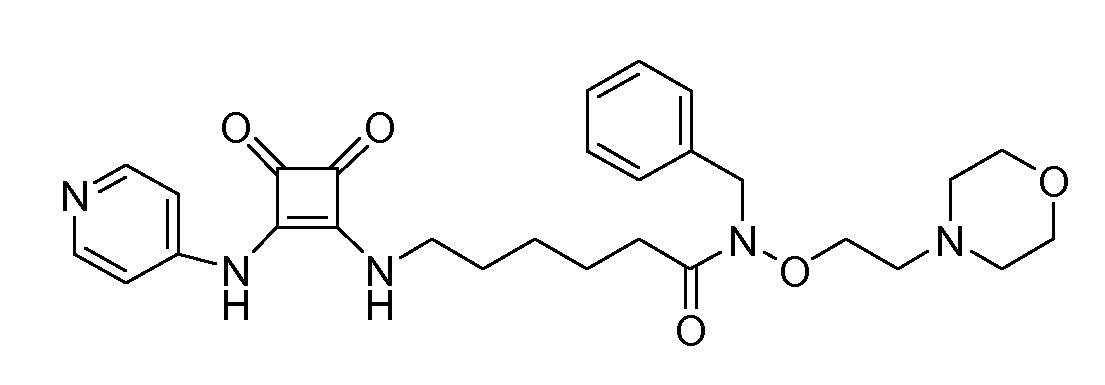
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-бензил-N-(2-морфолиноэтокси)гексанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,53 (м, 2H), 7,32 (м, 5H), 4,85 (с, 2H), 4,02 (т, 2H), 3,73 (т, 2H), 3,63 (м, 4H), 2,58 (м, 4H), 2,43 (м, 4H), 1,70 (м, 4H), 1,45 (м, 2H).
Пример 18: N-бензил-8-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)октанамид (соединение 1018)
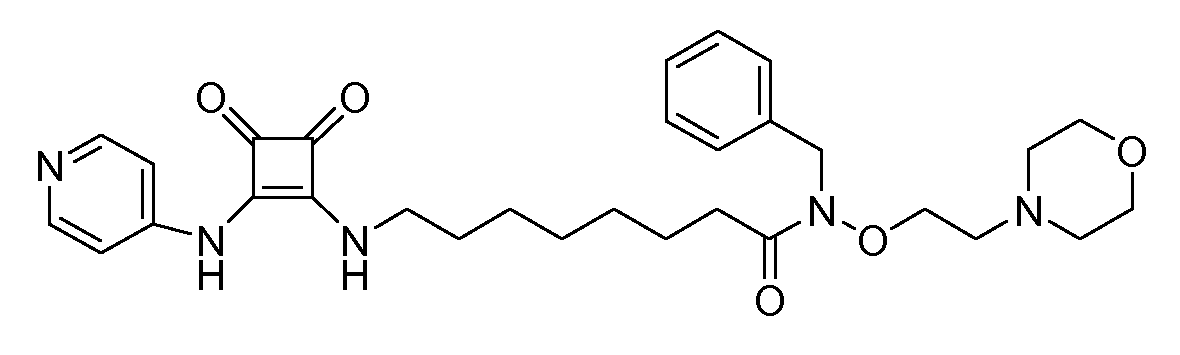
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 8-амино-N-бензил-N-(2-морфолиноэтокси)октанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,53 (м, 2H), 7,32 (м, 5H), 4,85 (с, 2H), 4,02 (т, 2H), 3,72 (т, 2H), 3,64 (м, 4H), 2,58 (м, 4H), 2,43 (м, 4H), 1,66 (м, 4H), 1,40 (м, 6H).
Пример 19: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)-N-(3-морфолинпропил)гексан-1-сульфонамид (соединение 1019)
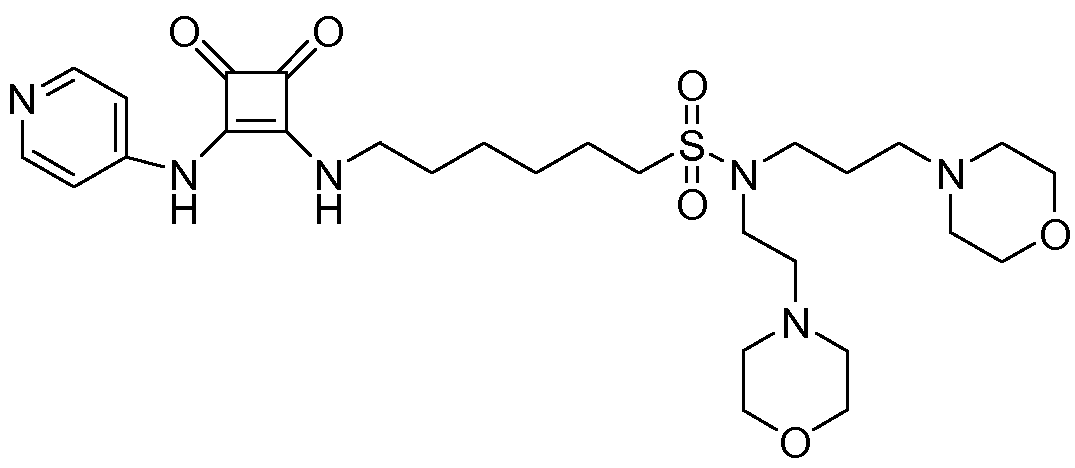
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-морфолиноэтил)-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 3,70 (м, 10H), 3,38 (т, 2H), 3,30 (м, 2H), 3,17 (м, 2H), 2,56 (м, 2H), 2,50 (м, 8H), 2,40 (м, 2H), 1,82 (м, 4H), 1,71 (м, 2H), 1,51 (м, 4H).
Пример 20: N-(циклогексилметокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1020)
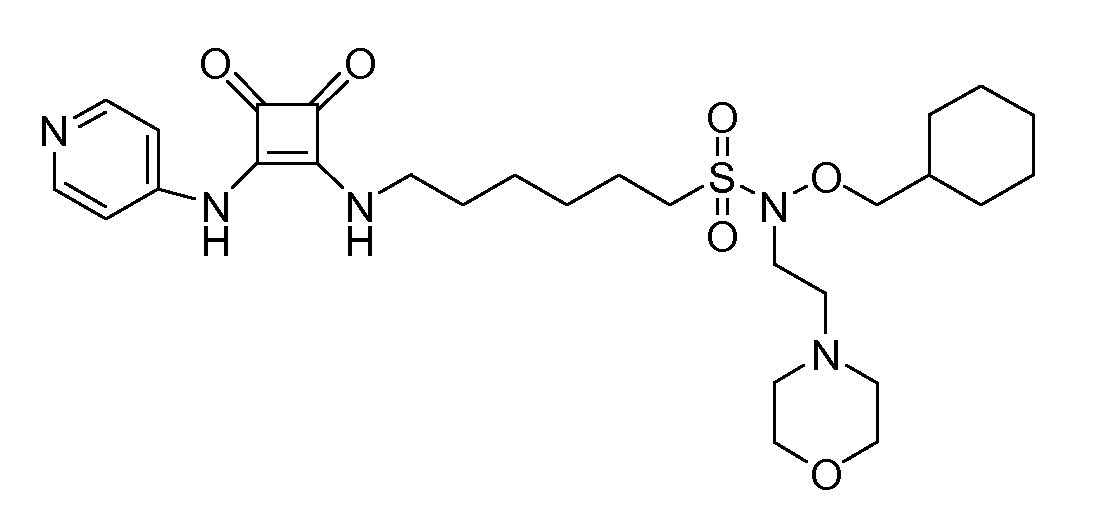
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(циклогексилметокси)-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 3,89 (д, 2H), 3,71 (м, 6H), 3,42 (т, 2H), 3,20 (м, 2H), 2,67 (т, 2H), 2,53 (м, 4H), 1,91 (м, 2H), 1,85-0,95 (м, 17H).
Пример 21: N-циклогептил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1021)
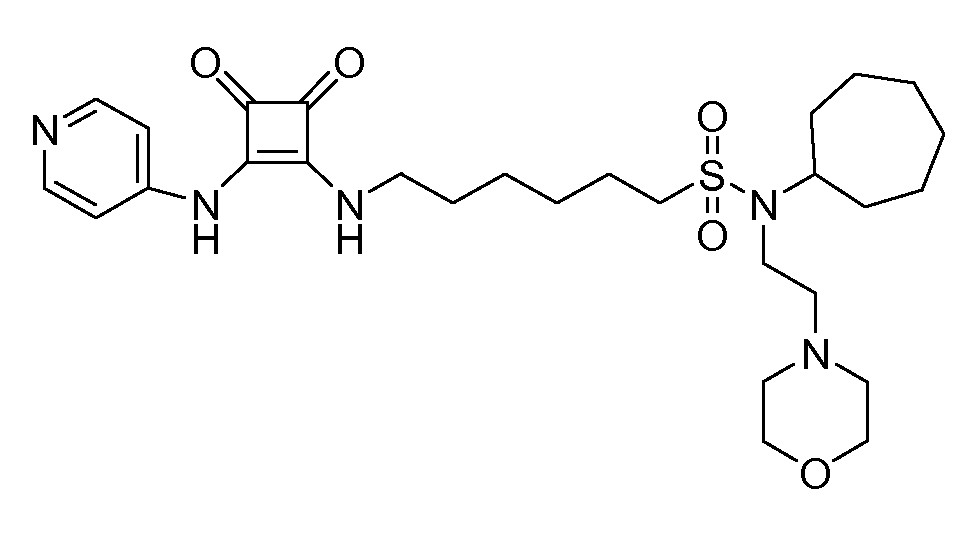
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогептил-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,54 (м, 2H), 3,71 (м, 9H), 3,10 (м, 2H), 2,58 (м, 2H), 2,52 (м, 4H), 1,95-1,4 (м, 16H).
Пример 22: 5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентилциклогексилоксикарбамат (соединение 1022)
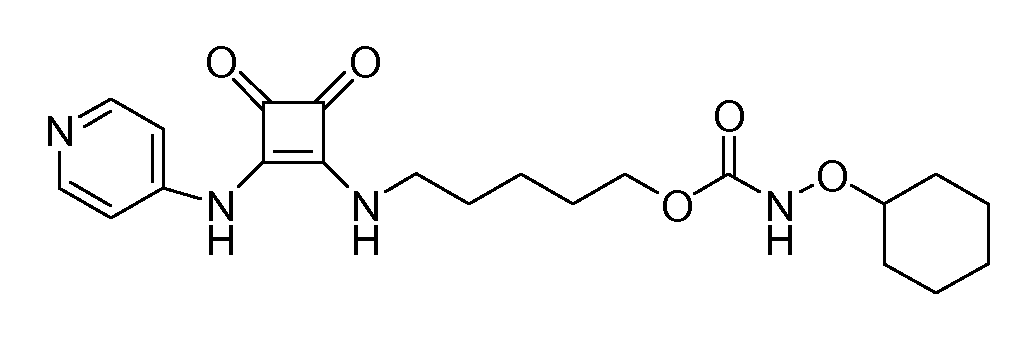
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 3.
1Н ЯМР (ДМСО-d6): δ 10,05 (шс, 2H), 8,41 (м, 2H), 7,42 (м, 2H), 4,58 (шс, 1H), 4,01 (м, 2H), 3,60 (м, 1H), 3,42 (м, 2H), 1,79 (м, 2H), 1,59 (м, 4H), 1,5-1,1 (м, 10H).
Пример 23: 5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентилциклогептилоксикарбамат (соединение 1023)
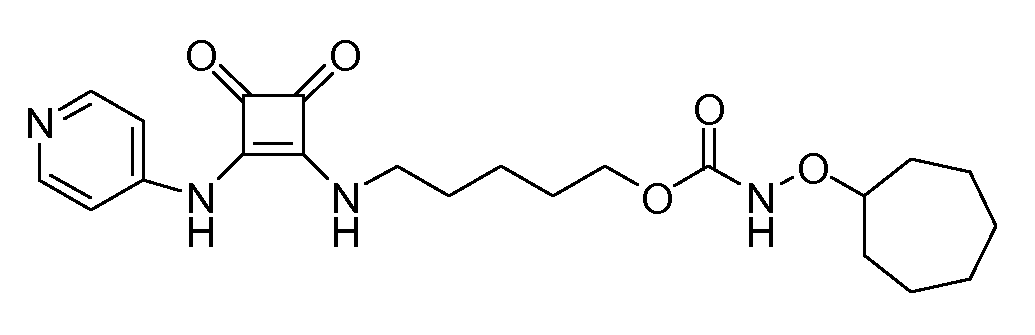
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 4.
1Н ЯМР (ДМСО-d6): δ 10,05 (шс, 1H), 9,99 (шс, 1H), 8,41 (м, 2H), 7,89 (т, 1H), 7,44 (м, 2H), 4,01 (м, 2H), 3,74 (м, 1H), 3,61 (м, 2H), 1,83 (м, 2H), 1,65-1,2 (м, 16H).
Пример 24: 5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил 2-морфолиноэтоксикарбамат (соединение 1024)
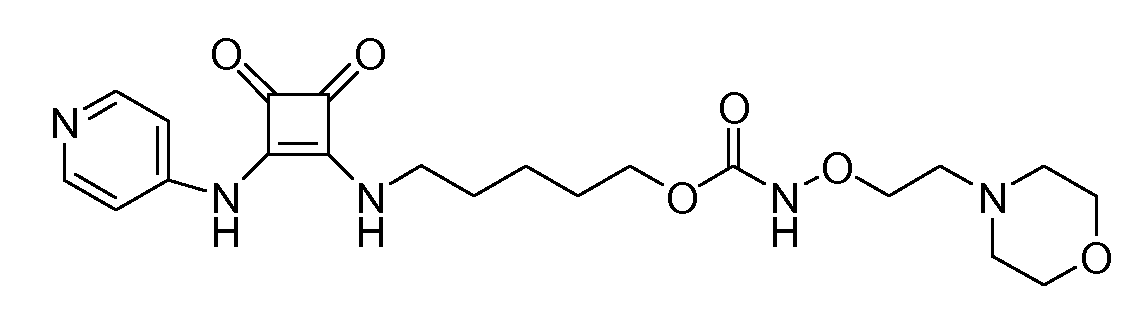
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 8.
1Н ЯМР (ДМСО-d6): δ 10,25 (шс, 2H), 8,39 (м, 2H), 7,85 (шс, 1H), 7,42 (м, 2H), 4,02 (м, 2H), 3,82 (м, 2H), 3,61 (м, 2H), 3,55 (м, 4H), 2,48 (м, 2H), 2,39 (м, 4H), 1,7-1,2 (м, 6H).
Пример 25: 5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентилциклогексилокси(изопропил)карбамат
(соединение 1025)
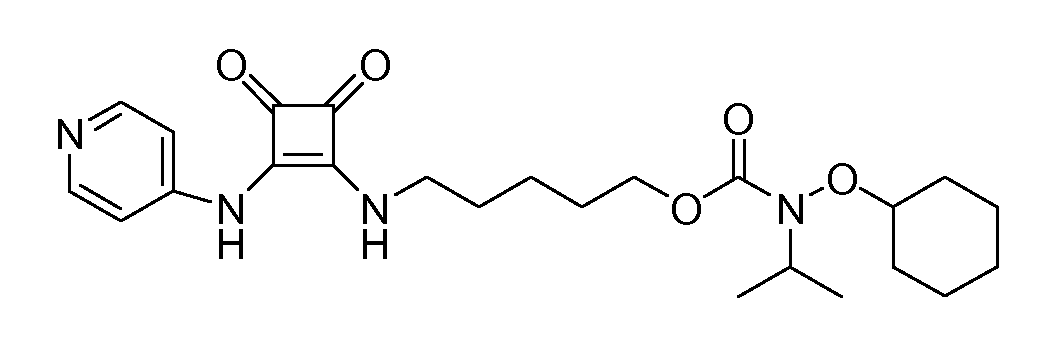
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 7.
1H ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,41 (м, 2H), 7,84 (шс, 1H), 7,42 (м, 2H), 4,06 (м, 3H), 3,64 (м, 3H), 1,84 (м, 2H), 1,64 (м, 6H), 1,55-1,1 (м, 8H), 1,09 (д, 3H).
Пример 26: 5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентилциклогексил(2-морфолиноэтокси)карбамат (соединение 1026
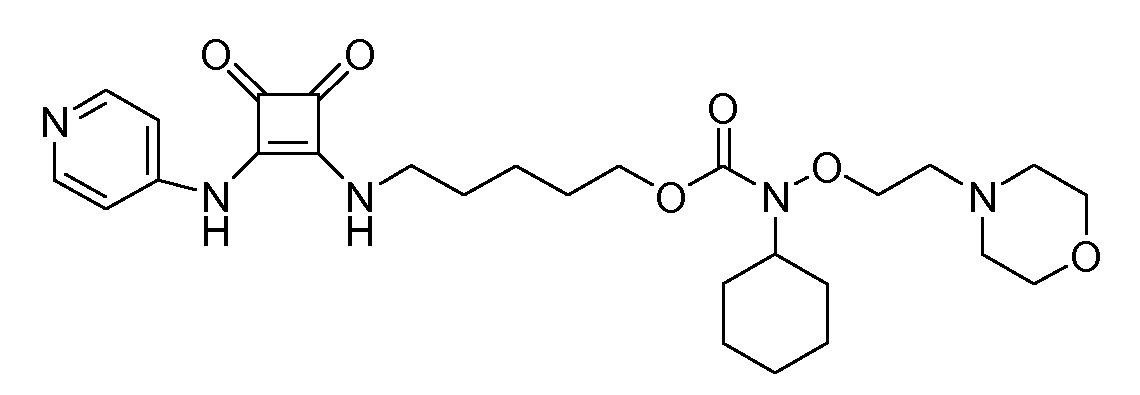
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 6.
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 4,18 (т, 2H), 4,02 (т, 2H), 3,72 (м, 7H), 2,65 (т, 2H), 2,56 (м, 4H), 1,9-1,45 (м, 13), 1,31 (м, 2H), 1,14 (м, 1H).
Пример 27: N-циклогептил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-метилгексан-1-сульфонамид (соединение 10127)
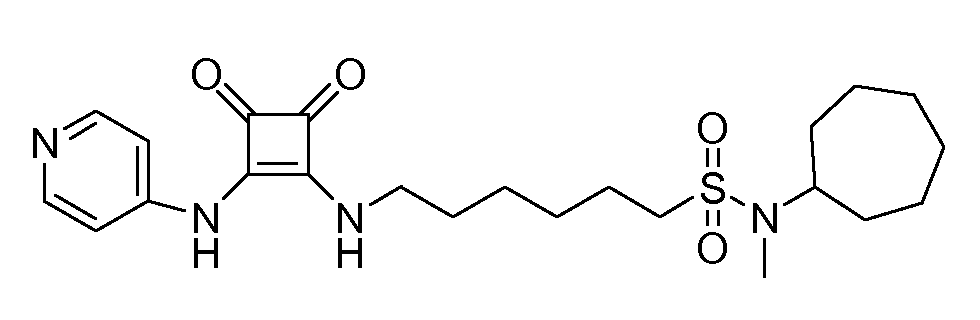
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогептил-N-метилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,41 (м, 2H), 7,82 (шс, 1H), 7,43 (м, 2H), 3,67 (м, 1H), 3,61 (м, 2H), 2,98 (м, 2H), 2,68 (с, 3H), 1,8-1,25 (м, 20H).
Пример 28: N-(циклогексилметокси)l-6-(3,4-диоксо-2-(пиридин-3-иламино)циклобут-1-ениламино)гексан-1-суфонамид
(соединение 1028)
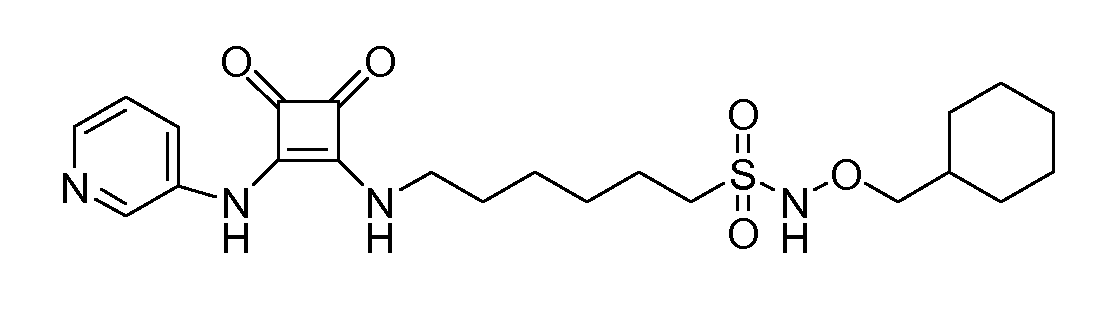
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-3-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(циклогексилметокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,95 (шс, 1H), 9,76 (шс, 1H), 8,56 (д, 1H), 8,23 (дд, 1H), 7,94 (м, 1H), 7,71 (шс, 1H), 7,38 (м, 1H), 3,65 (д, 2H), 3,60 (м, 2H), 3,12 (м, 2H), 1,8-1,5 (м, 10H), 1,40 (м, 4H), 1,16 (м, 3H), 0,91 (м, 2H).
Пример 29: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)-N-(пиридин-3-илметил)гексан-1-суфонамид (соединение 1029)
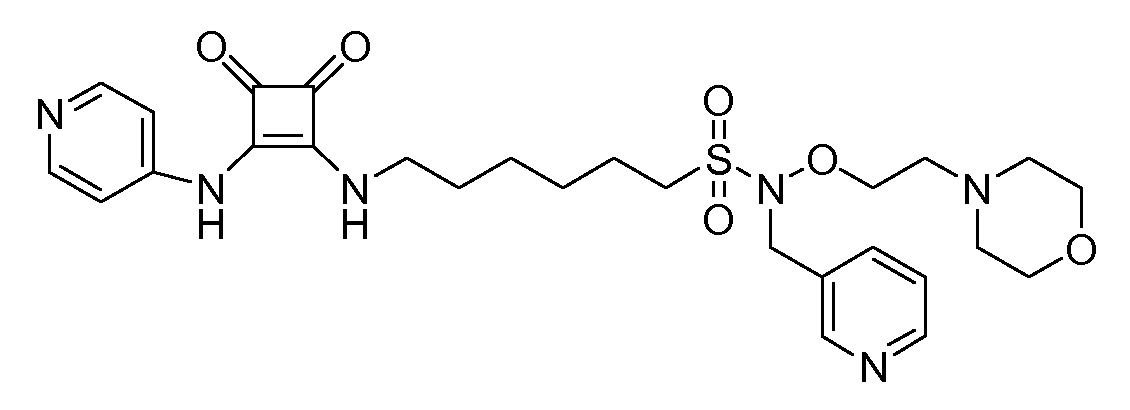
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-морфолиноэтокси)-N-(пиридин-3-илметил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,64 (дд, 1H), 8,56 (дд, 1H), 8,37 (м, 2H), 7,99 (м, 1H), 7,52 (м, 3H), 4,48 (с, 1H), 3,81 (м, 2H), 3,76 (м, 4H), 3,30 (м, 2H), 2,37 (м, 2H), 2,30 (м, 4H), 1,95 (м, 2H), 1,8-1,45 (м, 6H).
Пример 30: 3-(6-(азепан-1-илсульфонил)гексиламино)-4-
(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1030)
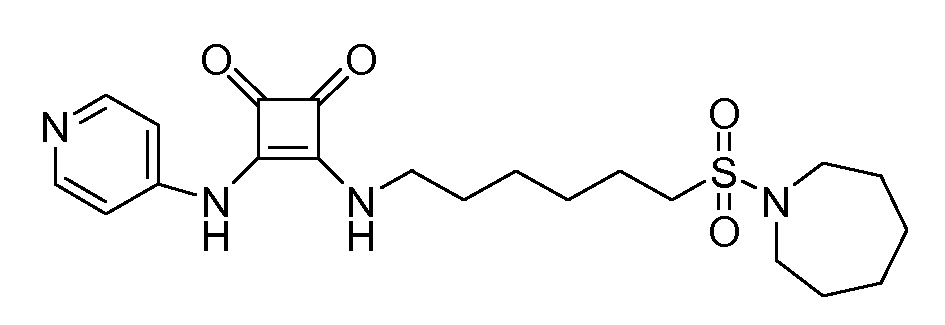
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(азепан-1-илсульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,89 (шс, 1H), 8,41 (м, 2H), 7,80 (т, 1H), 7,43 (м, 2H), 3,61 (м, 2H), 3,26 (м, 4H), 3,02 (м, 2H), 1,75-1,45 (м, 12H), 1,45-1,25 (м, 4H).
Пример 31: 3-(6-(морфолиносульфонил)гексиламино)-4-
(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1031)
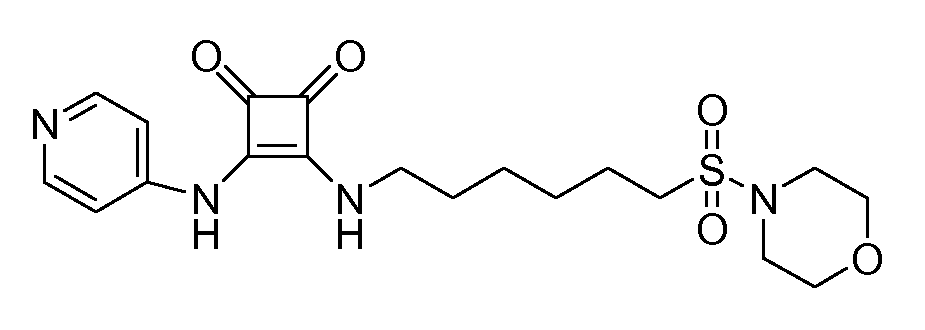
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(морфолиносульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,92 (шс, 1H), 8,41 (м, 2H), 7,85 (шс, 1H), 7,43 (м, 2H), 3,63 (м, 6H), 3,13 (м, 4H), 3,05 (м, 2H), 1,68 (м, 2H), 1,58 (м, 2H), 1,40 (м, 4H).
Пример 32: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-метил-N-(морфолиноэтокси)гексан-1-сульфонамид (соединение 1032)
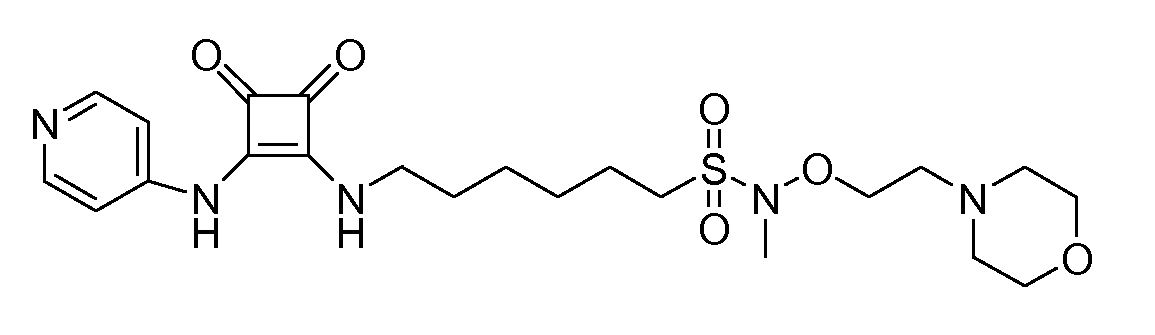
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-метил-N-(2-морфолиноетокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 10,03 (шс, 1H), 8,40 (м, 2H), 7,95 (шс, 1H), 7,44 (м, 2H), 4,00 (т, 2H), 3,61 (м, 2H), 3,55 (м, 4H), 3,21 (м, 2H), 2,98 (с, 3H), 2,52 (м, 2H), 2,39 (м, 2H), 1,76 (м, 2H), 1,59 (м, 2H), 1,42 (м, 4H).
Пример 33: N-циклогексил-7-(3,4-диоксо-2-(пиридин-3-иламино)циклобут-1-ениламино)-N- (морфолиноэтокси)гептанамид (соединение 1033)
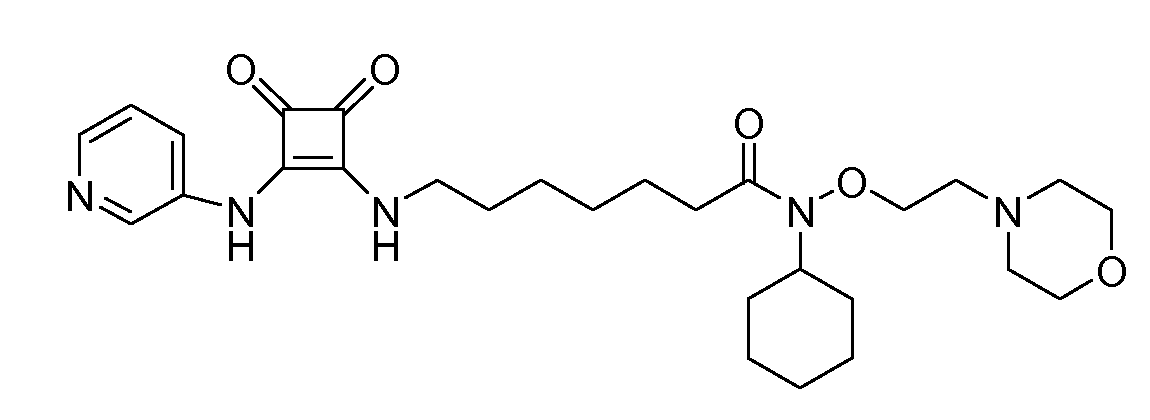
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-3-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-циклогексил-N-(2-морфолиноэтокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,59 (м, 1H), 8,24 (м, 1H), 8,09 (д, 1H), 7,42 (м, 1H), 4,13 (м, 1H), 4,08 (т, 2H), 3,73 (м, 2H), 3,71 (м, 4H), 2,67 (т, 2H), 2,56 (м, 4H), 2,51 (м, 2H), 1,9-1,6 (м, 10H), 1,55-1,25 (м, 7H), 1,20 (м, 1H).
Пример 34: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1034)
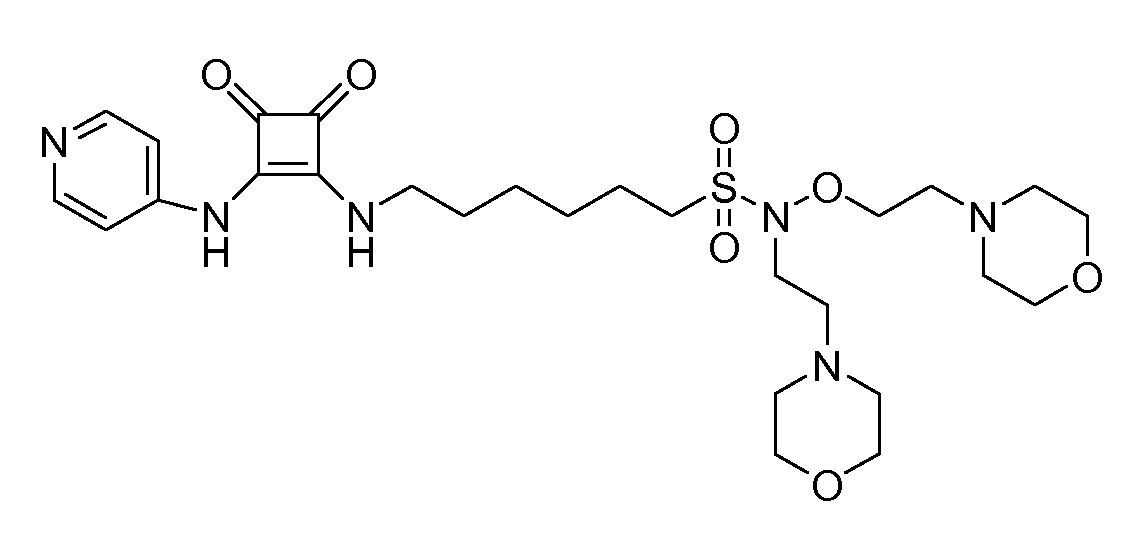
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(2-морфолиноэтокси)-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 4,23 (т, 2H), 3,75 (м, 2H), 3,70 (м, 8H), 3,43 (т, 3H), 3,26 (м, 2H), 2,70 (т, 2H), 2,64 (т, 2H), 2,53 (м, 8H), 1,91 (м, 2H), 1,73 (м, 2H), 1,54 (м, 4H).
Пример 35: 1-(циклогексилокси)-3-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил)мочевина (соединение 1035)
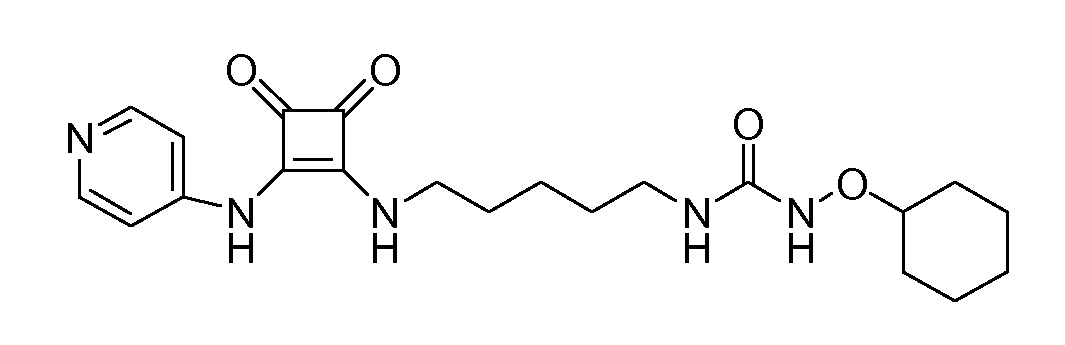
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 10.
1Н ЯМР (ДМСО-d6): δ 9,85 (шс, 1H), 8,81 (с, 1H), 8,41 (м, 2H), 7,83 (шс, 1H), 7,44 (м, 2H), 6,56 (т, 1H), 3,60 (м, 2H), 3,48 (м, 1H), 3,06 (м, 2H), 1,87 (м, 2H), 1,75-1,1 (м, 14H).
Пример 36: 1-(циклогептилокси)-3-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил)мочевина (соединение 1036)
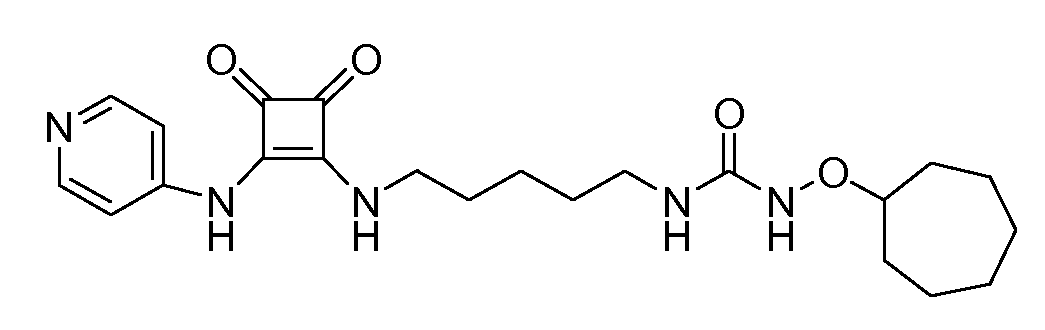
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 11.
1Н ЯМР (ДМСО-d6): δ 12,22 (шс, 1H), 9,03 (т, 1H), 8,80 (с, 1H), 8,60 (м, 2H), 7,89 (м, 2H), 6,49 (т, 1H), 3,63 (м, 3H), 3,05 (м, 2H), 1,90 (м, 2H), 1,75-1,1 (м, 16H).
Пример 37: 1-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-
1-ениламино)пентил)-3-(2-морофлиноэтокси)мочевина
(соединение 1037)
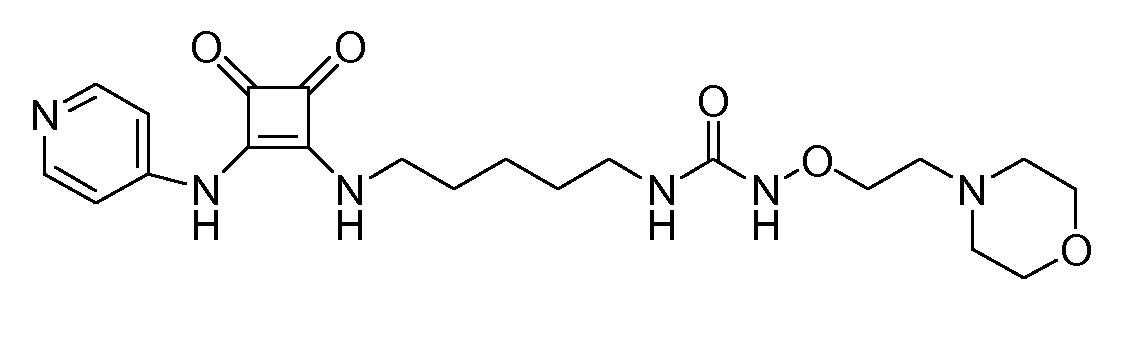
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 12.
1Н ЯМР (ДМСО-d6): δ 9,94 (шс, 1H), 8,96 (с, 1H), 8,40 (м, 2H), 7,85 (т, 1H), 7,44 (м, 2H), 7,32 (т, 1H), 3,76 (м, 2H), 3,62 (м, 2H), 3,58 (м, 4H), 3,09 (м, 2H), 2,48 (м, 2H), 2,40 (м, 4H), 1,60 (м, 2H), 1,47 (м, 2H), 1,33 (м, 3H), 0,85 (м, 1H).
Пример 38: 1-(бензилокси)-3-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил)мочевина (соединение 1038)
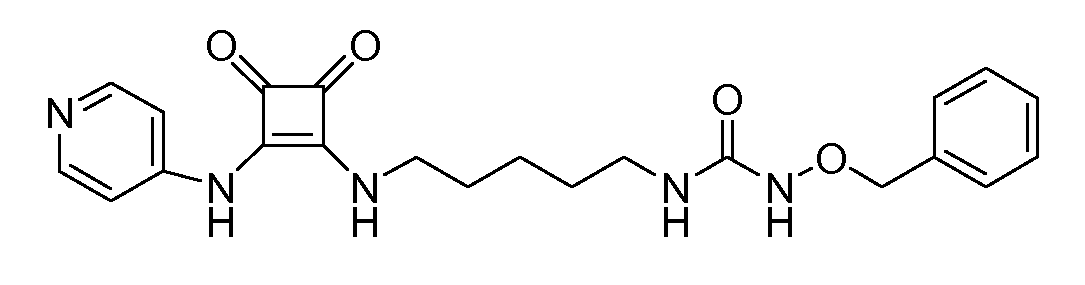
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 13.
1Н ЯМР (ДМСО-d6): δ 9,95 (шс, 1H), 9,02 (с, 1H), 8,40 (м, 2H), 7,87 (т, 1H), 7,38 (м, 7H), 6,75 (т, 1H), 4,70 (с, 2H), 3,61 (м, 2H), 3,05 (м, 2H), 1,7-0,7 (м, 2H).
Пример 39: 1-циклогексил-3-(5-(3,4-диоксо-2-
(пиридин-4-иламино)циклобут-1-ениламино)пентил)-1-
(2-морфолиноэтокси)мочевина (соединение 1039)
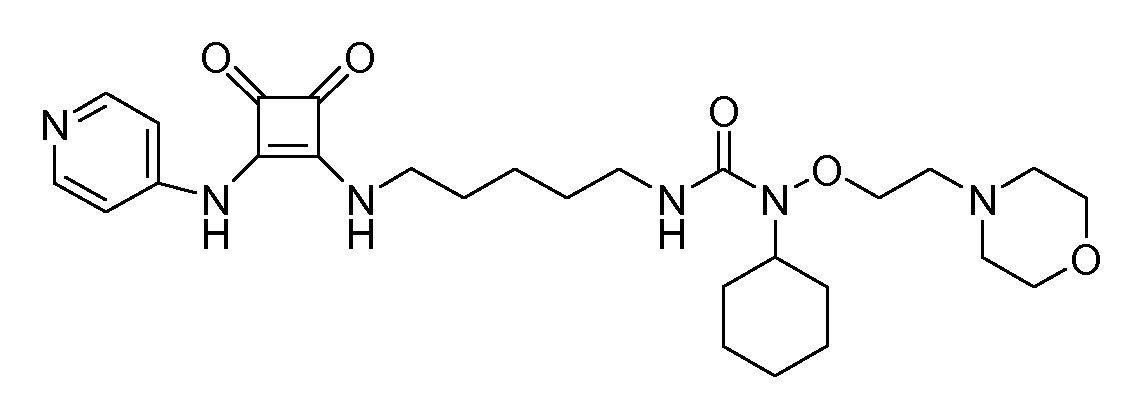
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и соединение 14.
1Н ЯМР (ДМСО-d6): δ 9,89 (шс, 1H), 8,41 (м, 2H), 7,81 (т, 1H), 7,65 (т, 1H), 7,43 (м, 2H), 3,82 (м, 2H), 3,72 (м, 1H), 3,62 (м, 2H), 3,58 (м, 4H), 3,11 (м, 2H), 2,46 (м, 2H), 2,42 (м, 4H), 1,75-0,9 (м, 16H).
Пример 40: 3-(пиридин-4-иламино)-4-(6-(пирролидин-1-илсульфонил)гексиламино)циклобут-3-ен-1,2-дион
(соединение 1040)
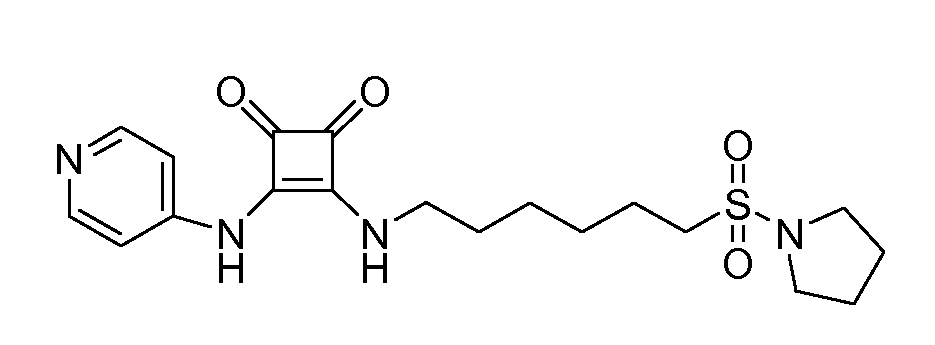
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(пирролидин-1-илсульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,89 (шс, 1H), 8,41 (м, 2H), 7,81 (т, 1H), 7,43 (м, 2H), 3,61 (м, 2H), 3,22 (м, 4H), 3,04 (м, 2H), 1,83 (м, 4H), 1,67 (м, 2H) 1,58 (м, 2H), 1,37 (м, 4H).
Пример 41: 3-(6-(пиперидин-1-илсульфонил)гексиламино)-4-(пиридин-4-иламино)-циклобут-3-ен-1,2-дион (соединение 1041)
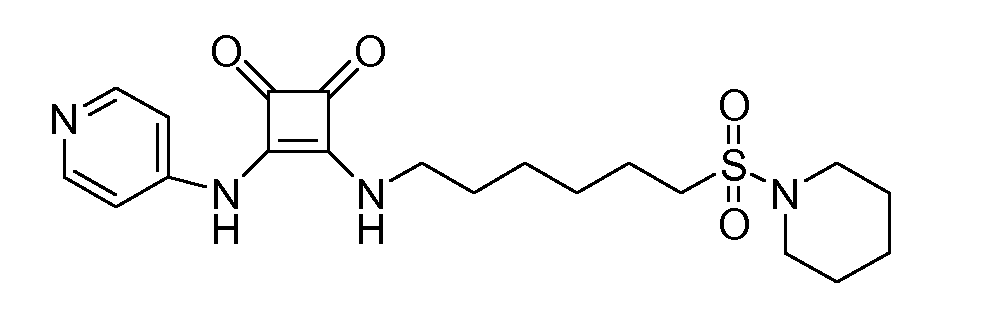
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(пиперидин-1-илсульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,89 (шс, 1H), 8,41 (м, 2H), 7,80 (т 1H), 7,43 (м, 2H), 3,61 (м, 2H), 3,12 (м, 4H), 2,98 (м, 2H), 1,75-1,3 (м, 14H).
Пример 42: 3-(6-(4-метилпиперазин-1-илсульфонил)гексиламино)-4-(пиридин-4-иламино)-циклобут-3-ен-1,2-дион (соединение 1042)
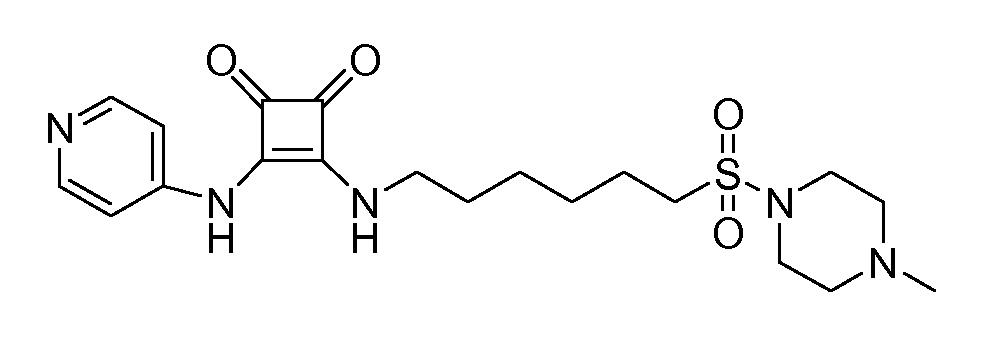
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(4-метилпиперазин-1-илсульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,87 (шс, 1H), 8,41 (м, 2H), 7,81 (шс, 1H), 7,43 (м, 2H), 3,60 (м, 2H), 3,14 (м, 4H), 3,03 (м, 2H), 2,35 (м, 4H), 1,68 (м, 2H), 1,58 (м, 2H), 1,40 (м, 4H).
Пример 43: N-(циклогексилметокси)-5-(3,4-диоксо-2-
(пиридин-4-иламино)циклобут-1-ениламино)пентансульфонамид
(соединение 1043)
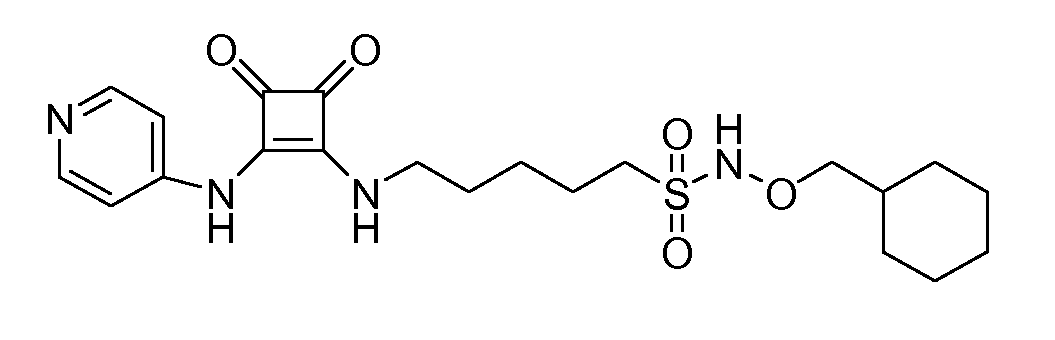
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-(циклогексилметокси)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,40 (м, 2H), 7,54 (м, 2H), 3,75 (м, 4H), 3,22 (м, 2H), 1,88 (м, 2H), 1,85-1,5 (м, 9H), 1,30 (м, 4H), 0,98 (м, 2H).
Пример 44: 3-(5-(морфолиносульфонил)пентиламино)-4-
(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1044)
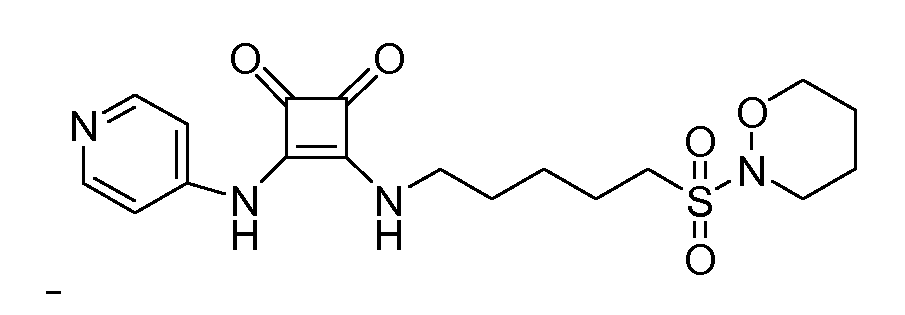
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-(морфолиносульфонил)пентан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
МС [M+H]+ = 409,2, [M-H]- = 407,2
Пример 45 N-(циклогексилметокси)-7-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гептансульфонамид (соединение 1045)
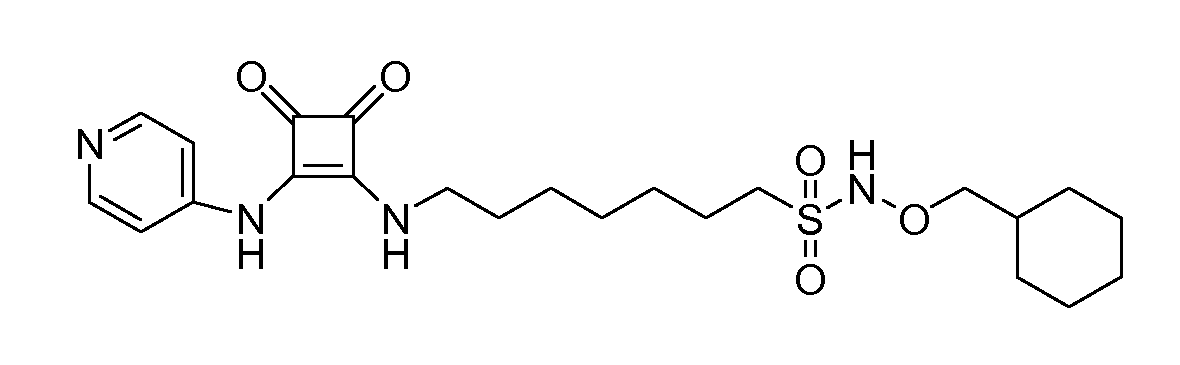
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-(циклогексилметокси)гептан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,40 (м, 2H), 7,54 (м, 2H), 3,76 (м, 4H), 3,22 (м, 2H), 1,88 (м, 2H), 1,85-1,5 (м, 13H), 1,30 (м, 4H), 1,08 (м, 2H).
Пример 46: 3-(7-(морфолиносульфонил)гептиламино)-4-
(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1046)
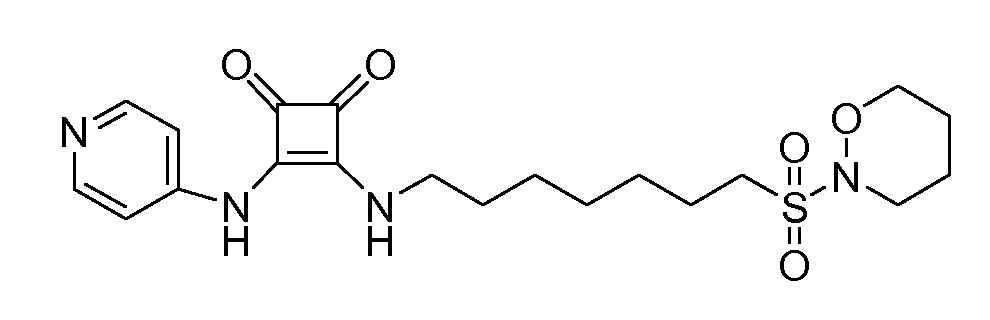
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-(морфолиносульфонил)гептан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 4,11 (т, 2H), 3,74 (т, 2H), 3,36 (м, 2H), 3,20 (т, 2H), 1,87 (м, 4H), 1,71 (м, 4H), 1,49 (м, 6H).
Пример 47: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-изопропил-N-(2-морфолиноэтокси)гексан-
1-сульфонамид (соединение 1047)
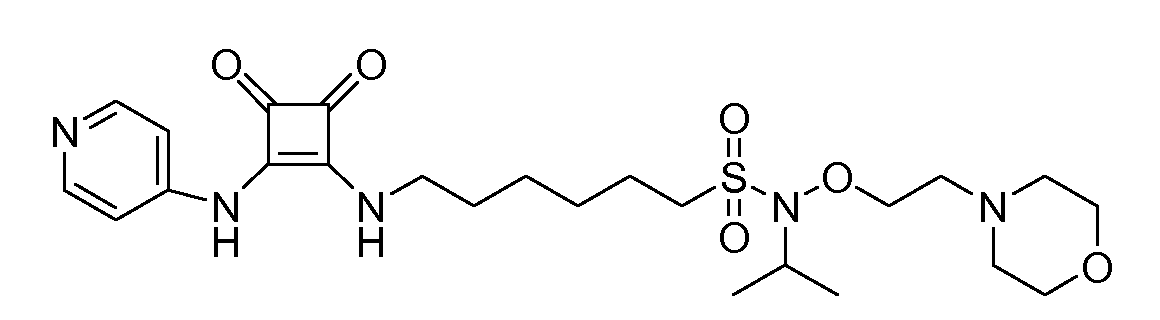
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-изопропил-N-(2-морфолиноэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 4,17 (т, 2H), 3,98 (м, 1H), 3,74 (т, 2H), 3,70 (м, 4H), 3,23 (м, 2H), 2,65 (т, 2H), 2,54 (м, 4H), 1,90 (м, 2H), 1,72 (м, 2H), 1,53 (м, 4H), 1,28 (д, 6H).
Пример 48: N-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил)морфолин-2-карбоксамид (соединение 1048)
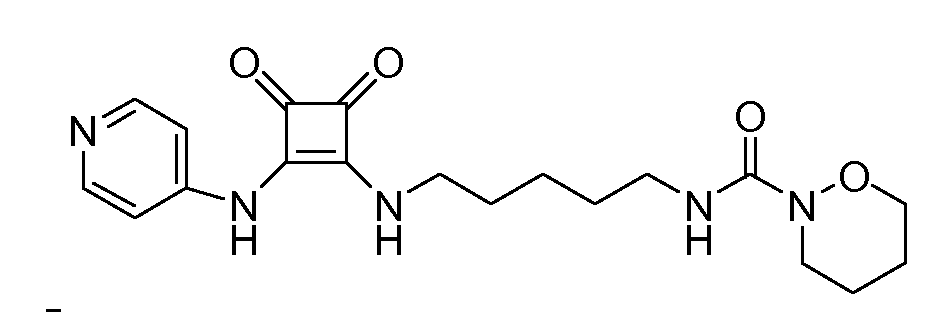
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и N-(5-аминопентил)морфолин-2-карбоксамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,88 (шс, 1H), 8,39 (м, 2H), 7,80 (шс 1H), 7,43 (м, 2H), 6,96 (шс, 1H), 3,82 (м, 2H), 3,50 (м, 2H), 3,40 (м, 2H), 3,06 (м, 2H), 1,75-1,15 (м, 10H).
Пример 49: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(фенилкарбамоил)гексан-1-сульфонамид
(соединение 1049)
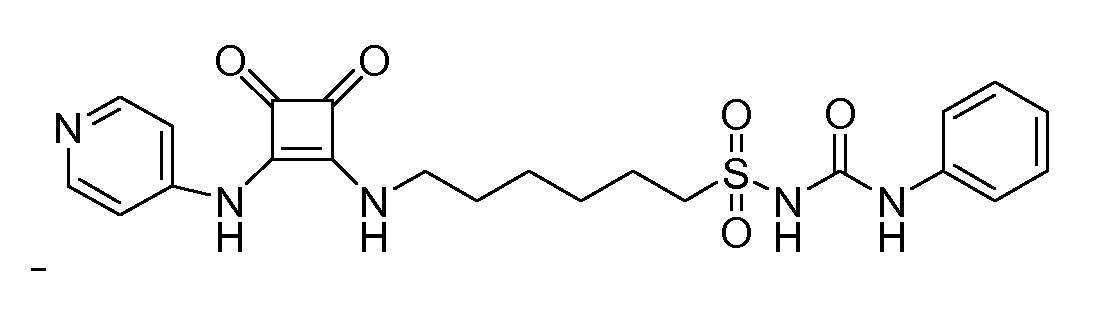
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(фенилкарбамоил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
MS [M+H]+ = 472,2, [M-H]- = 470,2
Пример 50: N-Циклогексил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)гексан-
1-сульфонамид (соединение 1050)
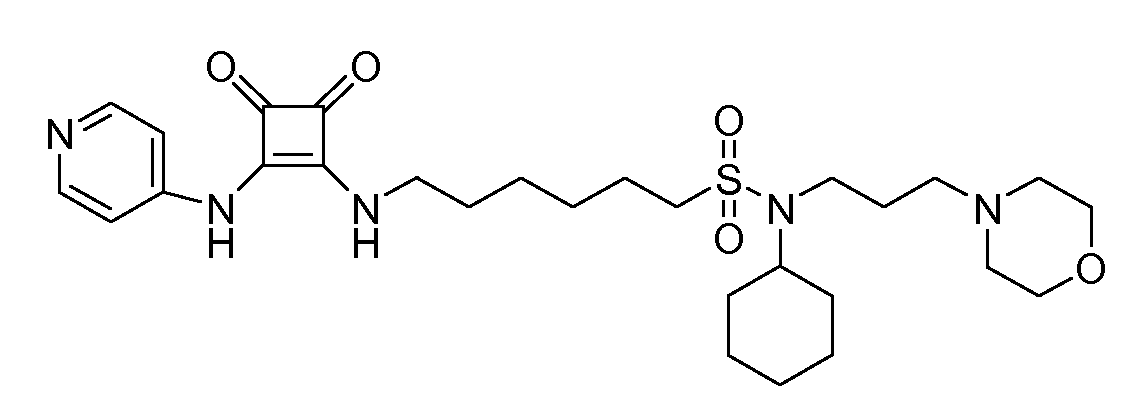
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогексил-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,87 (шс, 1H), 8,41 (м, 2H), 7,79 (т, 1H), 7,43 (м, 2H), 3,57 (м, 6H), 3,41 (м, 1H), 3,11 (т, 2H), 2,99 (т, 2H), 2,31 (м, 4H), 2,24 (т, 2H), 1,8-1,1 (м, 19H), 1,05 (м, 1H).
Пример 51: оксалат N-циклогексил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексан-1-сульфонамида (соединение 1051)
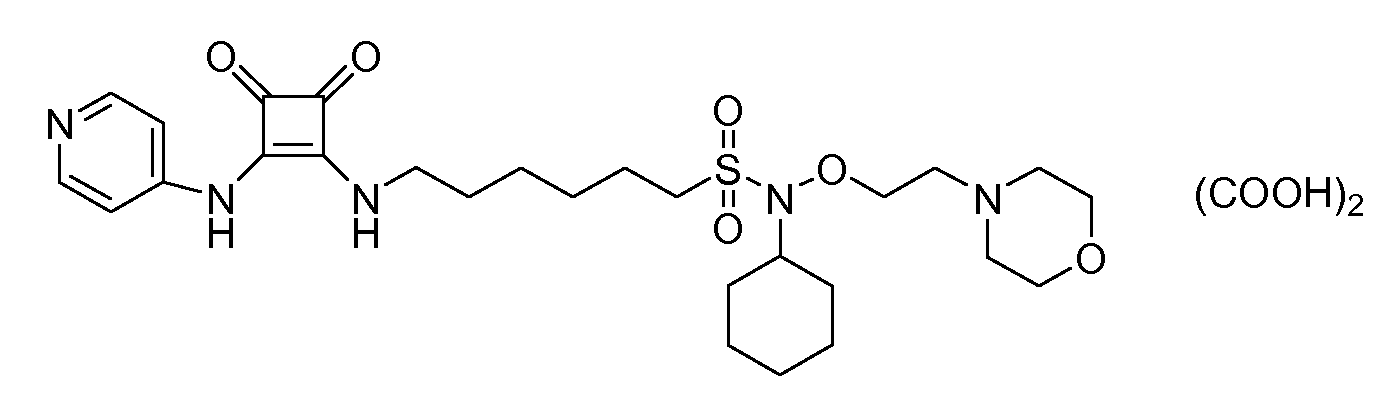
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогексил-N-(2-морфолиноэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР 400 МГц (ДМСО-d6): δ 9,28 (шс, 1H), 8,42 (д, 2H), 7,41 (д, 2H), 7,32 (шс, 1H), 4,11 (м, 2H), 3,76 (т, 2H), 3,68 (м, 4H), 3,57 (м, 1H), 3,13 (м, 2H), 2,59 (т, 2H), 2,49 (м, 4H), 1,95-1,76 (м, 6H), 1,71-1,35 (м, 9H), 1,35-1,20 (м, 2H), 1,17-1,03 (м, 1H).
Пример 52: N-Циклогексил-7-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гептан-1-сульфонамид (соединение 1052)
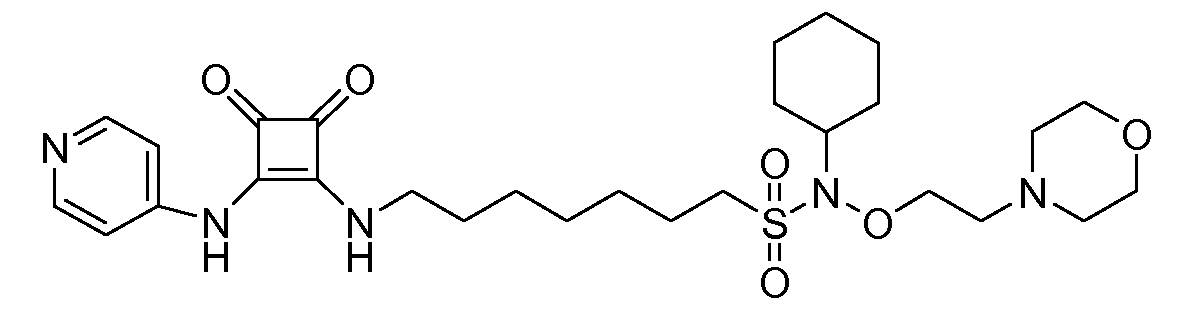
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 7-амино-N-циклогексил-N-(2-морфолиноэтокси)гептан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 4,15 (т, 2H), 3,75 (т, 2H), 3,71 (м, 4H), 3,58 (м, 1H), 3,22 (м, 2H), 2,65 (т, 2H), 2,55 (м, 4H), 2,0-1,25 (м, 19H), 1,19 (м, 1H).
Пример 53: N-Циклогексил-5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)пентан-
1-сульфонамид (соединение 1053)
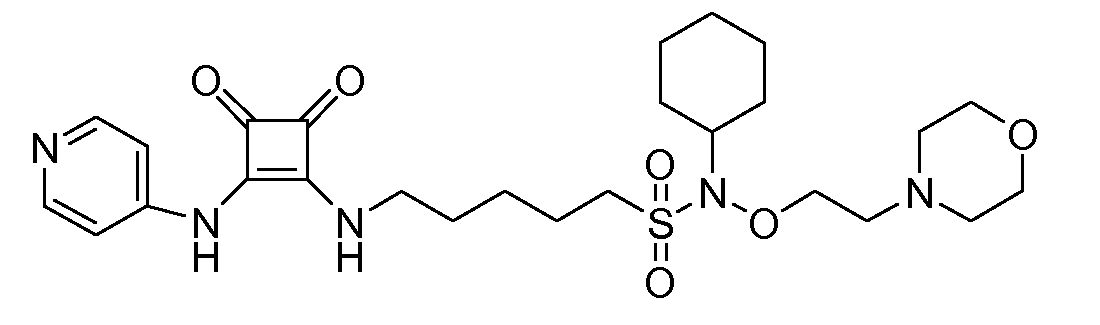
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-циклогексил-N-(2-морфолиноэтокси)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,54 (м, 2H), 4,15 (т, 2H), 3,76 (т, 2H), 3,70 (м, 4H), 3,58 (м, 1H), 3,27 (м, 2H), 2,65 (т, 2H), 2,54 (м, 4H), 2,0-1,55 (м, 13H), 1,35 (м, 2H), 1,19 (м, 1H).
Пример 54: N-(Циклогексилметокси)-6-(3,4-диоксо-2-
(пиридин-4-илметиламино)циклобут-1-ениламино)-N-(2-(2-(2-метоксиэтокси)этокси)этил)гексан-1-сульфонамид
(соединение 1054)
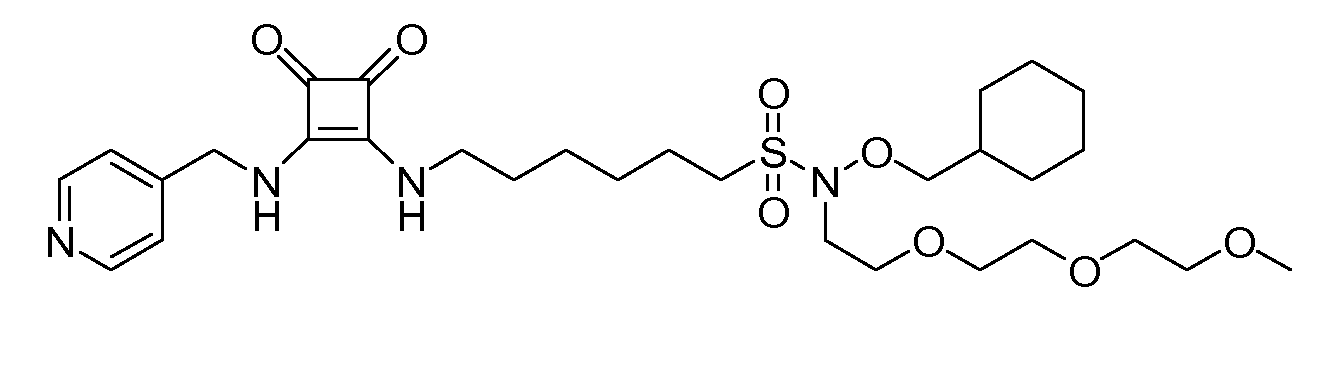
Общая методика 1. Исходные материалы: соединение 15 и 6-амино-N-(циклогексилметокси)-N-(2-(2-(2-метилоксиэтокси)этокси)этил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
МС [M+H]+ = 625,4, [M-H]- = 623,5
Пример 55: 3-(5-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)пентил)-1-изопропил-1-(2-морфолиноэтокси)мочевина (соединение 1055)
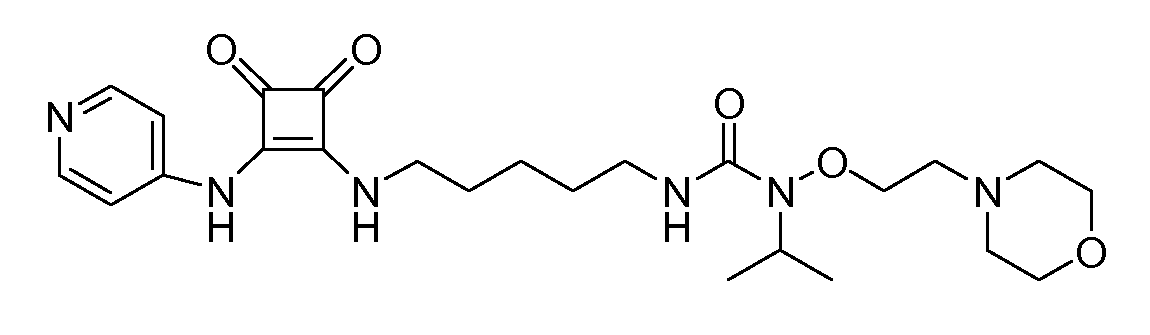
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 3-(5-аминопентил)-1-изопропил-1-(2-морфолиноэтокси)мочевина (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (с, 1H), 8,41 (д, 2H), 7,82 (т, 1H), 7,70 (т, 1H), 7,42 (д, 2H), 4,12 (м, 1H), 3,87 (м, 2H), 3,59 (м, 6H), 3,11 (м, 2H), 2,48 (м, 2H), 2,41 (м, 4H), 1,59 (м, 2H), 1,48 (м, 2H), 1,32 (м, 2H), 1,02 (м, 6H).
Пример 56: N-циклопентил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)гексан-
1-сульфонамид (соединение 1056)
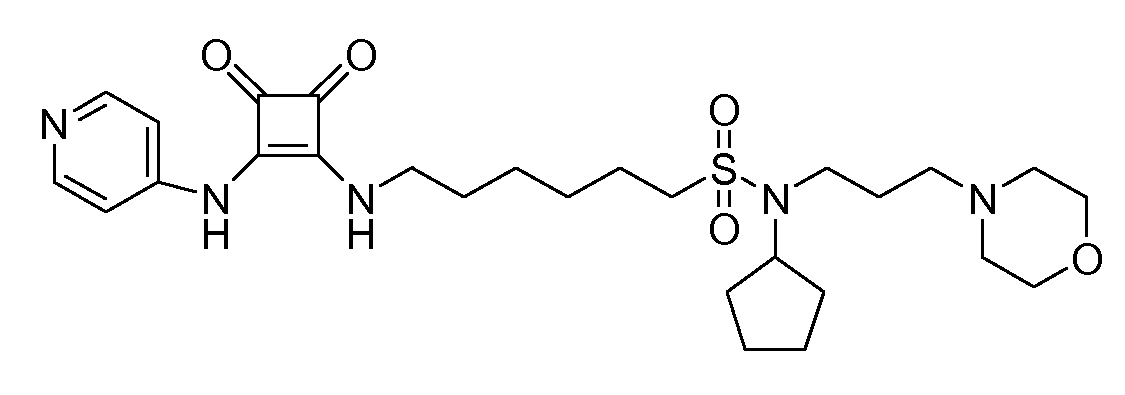
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклопентил-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39 (д, 2H), 7,55 (д, 2H), 4,06 (м, 1H), 3,75 (т, 2H), 3,70 (м, 4H), 3,17 (т, 2H), 3,04 (т, 2H), 2,49 (м, 4H), 2,40 (т, 2H), 2,0-1,35 (м, 18H).
Пример 57: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-этил-N-(3-морфолинопропил)гексан-1-сульфонамид (соединение 1057)
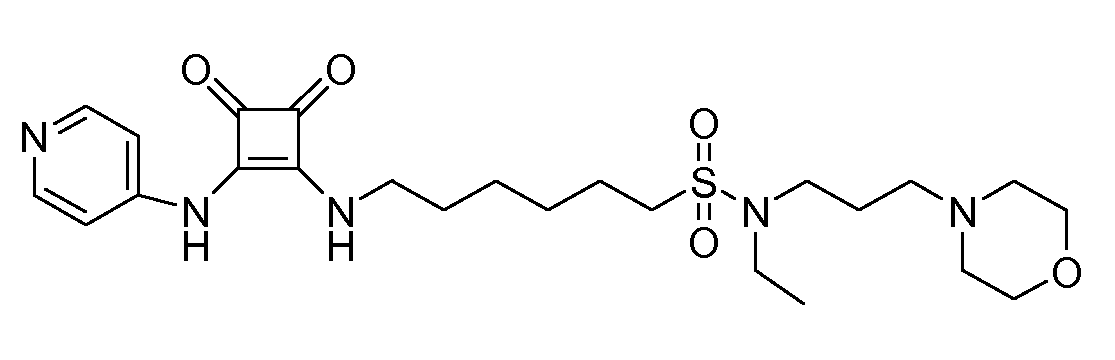
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-этил-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
МС [M+H]+ = 508,3, [M-H]- = 506,4
Пример 58: N-циклопентил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексан-
1-сульфонамид (соединение 1058)
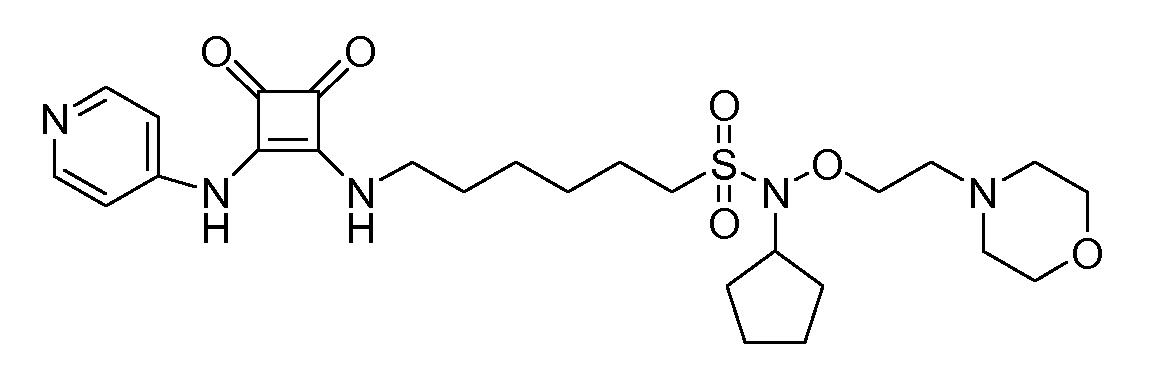
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклопентил-N-(2-морфолиноэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 10,0 (шс, 1H), 8,40 (д, 2H), 8,0 (шс, 1H), 7,44 (д, 2H), 4,05 (т, 2H), 3,94 (м, 1H), 3,61 (т, 2H), 3,54 (т, 4H), 3,16 (т, 2H), 2,48 (м, 2H), 2,38 (т, 4H), 1,95-1,25 (м, 16H).
Пример 59: N-циклогептил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)гексан-1-
сульфонамид (соединение 1059)
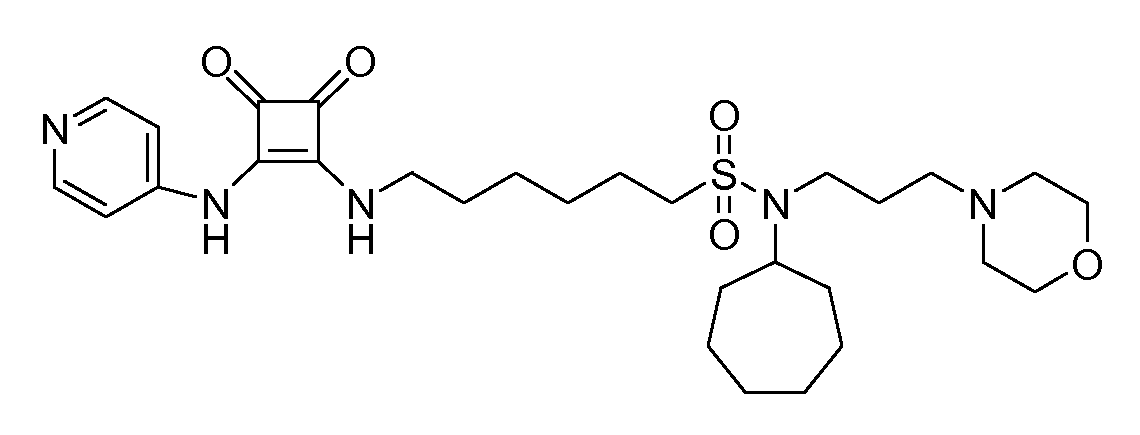
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогептил-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,40 (д, 2H), 7,81 (т, 1H), 7,43 (д, 2H), 3,60 (м, 7H), 3,09 (т, 2H), 2,97 (т, 2H), 2,31 (м, 4H), 2,23 (т, 2H), 1,85-1,25 (м, 22H).
Пример 60: N-циклогептил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексан-1-сульфонамид (соединение 1060)
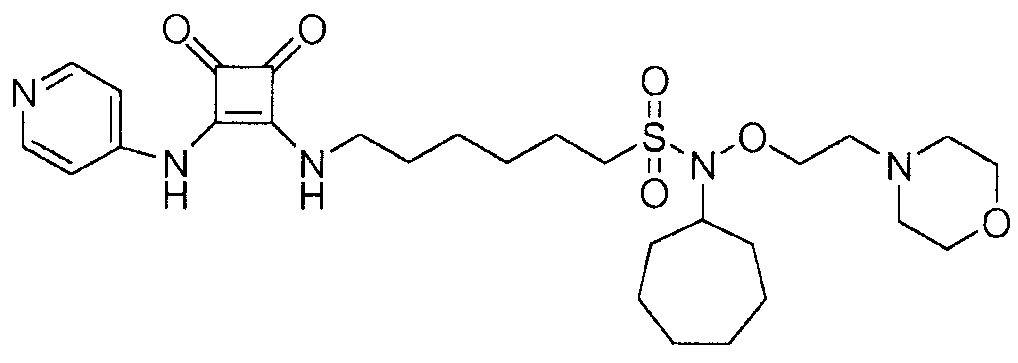
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогептил-N-(2-морфолиноэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,90 (шс, 1H), 8,40 (д, 2H), 7,80 (т, 1H), 7,43 (д, 2H), 4,03 (т, 2H), 3,71 (м, 1H), 3,58 (м, 8H), 3,17 (т, 2H), 2,39 (м, 4H), 1,95-1,25 (м, 20H).
Пример 61: N-циклогексил-N-(3-(диметиламино)пропил)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексан-1-сульфонамид (соединение 1061)
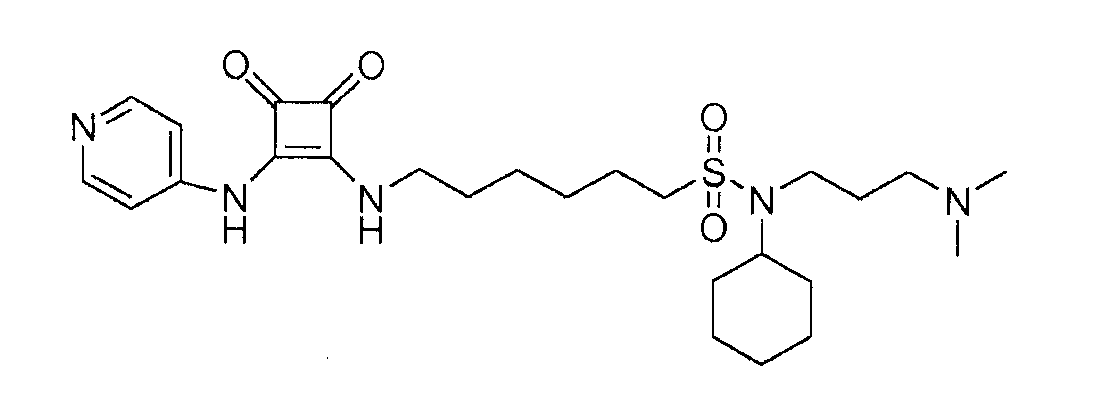
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогексил-N-(3-(диметиламино)пропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,38 (м, 2H), 7,55 (м, 2H), 3,75 (т, 2H), 3,51 (м, 1H), 3,21 (т, 2H), 3,04 (т, 2H), 2,37 (т, 2H), 2,28 (с, 6H), 1,9-1,25 (м, 19H), 1,17 (м, 1H).
Пример 62: N-циклобутил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)гексан-
1-сульфонамид (соединение 1062)
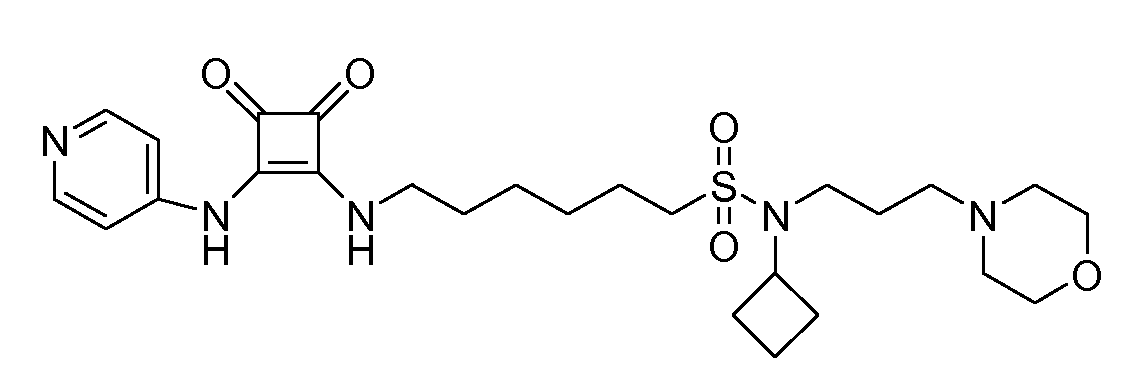
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклобутил-N-(3-морфолинопропил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39 (д, 2H), 7,55 (д, 2H), 4,20 (м, 1H), 3,75 (т, 2H), 3,71 (т, 4H), 3,29 (т, 2H), 2,98 (м, 2H), 2,48 (м, 4H), 2,41 (т, 2H), 2,21 (м, 4H), 1,73 (м, 8H), 1,49 (м, 4H).
Пример 63: N-циклобутил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)гексан-
1-сульфонамид (соединение 1063)
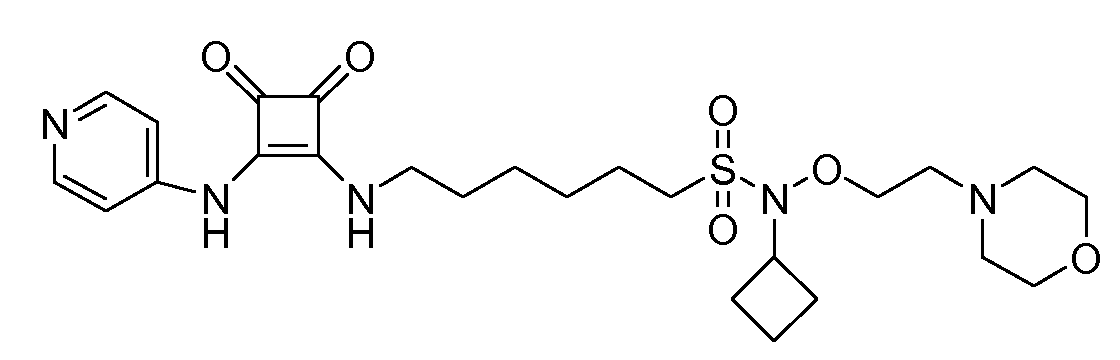
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклобутил-N-(2-морфолиноэтокси)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39 (м, 2H), 7,55 (м, 2H), 4,24 (м, 1H), 4,19 (т, 2H), 3,75 (т, 2H), 3,71 (м, 4H), 3,08 (т, 2H), 2,69 (т, 2H), 2,56 (м, 4H), 2,41 (м, 2H), 2,13 (м, 2H), 1,88 (м, 2H), 1,72 (м, 4H), 1,52 (м, 4H).
Пример 64: N-(Циклогексилметокси)-6-(3,4-диоксо-2-
(пиридин-3-илметиламино)циклобут-1-ениламино)-N-(2-(2-
(2-метоксиэтокси)этокси)этил)гексан-1-сульфонамид
(соединение 1064)
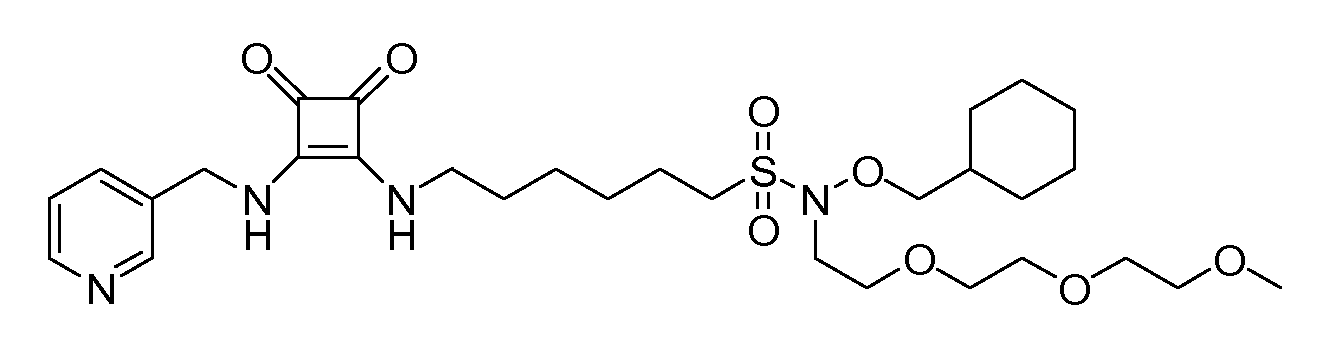
Общая методика 1. Исходные материалы: соединение 16 и 6-амино-N-(циклогексилметокси)-N-(2-(2-(2-метилоксиэтокси)этокси)этил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,60 (шс, 1H), 8,52 (д, 1H), 7,91 (м, 1H), 7,49 (м, 1H), 4,89 (с, 2H), 3,87 (д, 2H), 3,73 (т, 2H), 3,66 (м, 11H), 3,57 (м, 2H), 3,44 (т, 2H), 3,18 (т, 2H), 1,95-1,15 (м, 17H), 1,05 (м, 2H).
Пример 65: N-Циклогексил-7-(3,4-диоксо-2-
(пиридин-4-илметиламино)циклобут-1-ениламино)-N-
(2-морфолиноэтокси)гептанамид (соединение 1065)
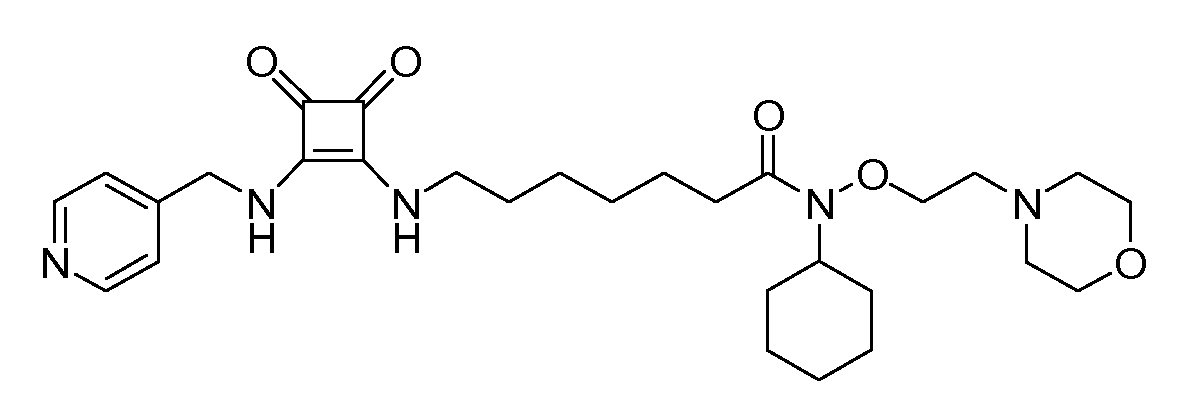
Общая методика 1. Исходные материалы: соединение 15 и 7-амино-N-циклогексил-N-(2-морфолиноэтокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,54 (м, 2H), 7,44 (м, 2H), 4,89 (с, 2H), 4,15 (м, 1H), 4,08 (т, 2H), 3,71 (м, 4H), 3,63 (м, 2H), 2,67 (т, 2H), 2,56 (м, 4H), 2,50 (м, 2H), 1,9-1,25 (м, 17H), 1,20 (м, 1H).
Пример 66: N-Циклогексил-7-(3,4-диоксо-2-
(пиридин-3-илметиламино)циклобут-1-ениламино)-N-
(2-морфолиноэтокси)гептанамид (соединение 1066)
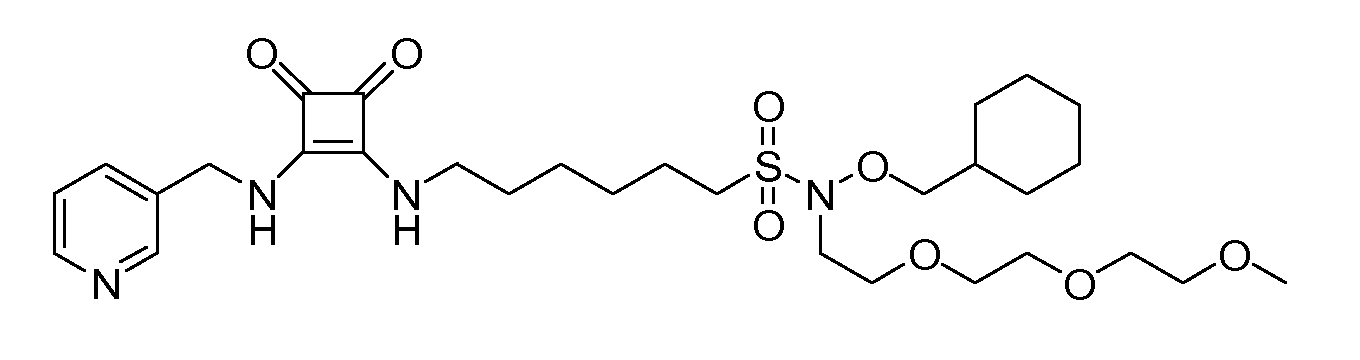
Общая методика 1. Исходные материалы: соединение 16 и 7-амино-N-циклогексил-N-(2-морфолиноэтокси)гептанамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,59 (шс, 1H), 8,51 (д, 1H), 7,90 (м, 1H), 7,48 (м, 1H), 4,88 (с, 2H), 4,15 (м, 1H), 4,08 (т, 2H), 3,71 (м, 4H), 3,63 (м, 2H), 2,67 (т, 2H), 2,56 (м, 4H), 2,49 (м, 2H), 1,9-1,25 (м, 17H), 1,19 (м, 1H).
Пример 67: N-циклогексил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-
1-сульфонамид (соединение 1067)
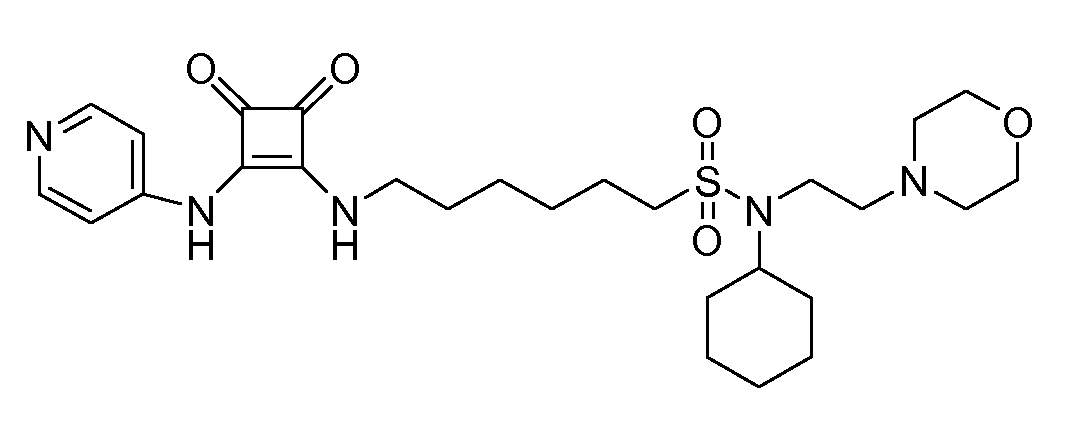
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-циклогексил-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,36 (м, 2H), 7,54 (м, 2H), 3,73 (т, 2H), 3,69 (м, 4H), 3,51 (м, 1H), 3,34 (м, 2H), 3,13 (м, 2H), 2,53 (м, 6H), 1,9-1,25 (м, 17H), 1,16 (м, 1H).
Пример 68: Этил N-циклогексил-P-(6-(3,4-диоксо-2-
(пиридин-4-иламино)циклобут-1-ениламино)гексил)фосфонимидат (соединение 1068)
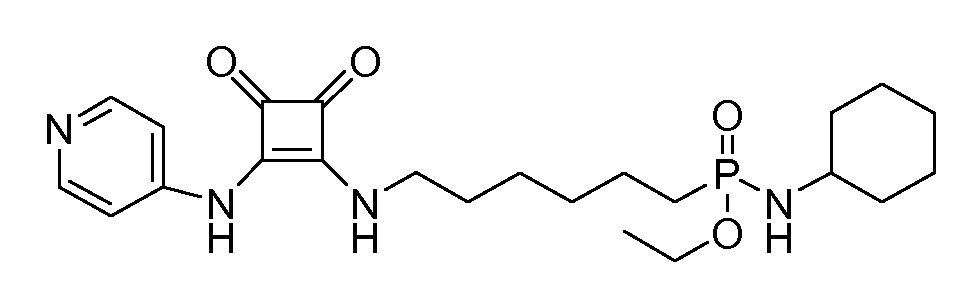
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и этил P-6-аминогексил-N-циклогексилфосфонамидат (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 4,00 (м, 2H), 3,73 (т, 2H), 2,95 (м, 1H), 1,88 (м, 2H), 1,8-1,05 (м, 21H).
Пример 69: 3-(6-(3,4-дигидроизохинолин-2(1Н)-илсульфонил)
гексиламино)-4-(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1069)
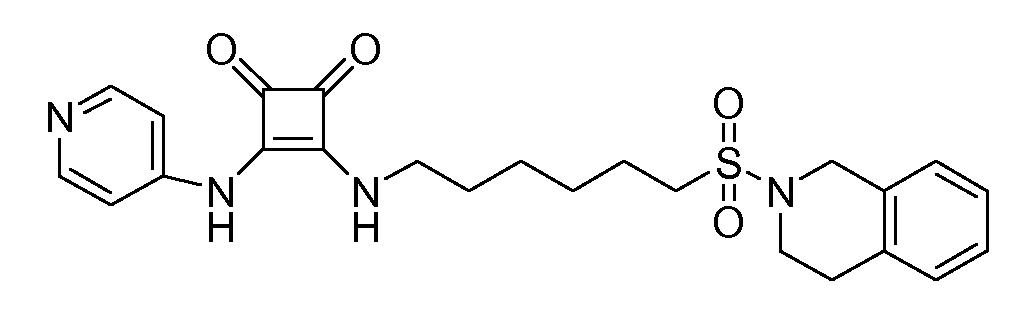
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-(3,4-дигидроизохинолин-2(1Н)-илсульфонил)гексан-1-амин (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,40 (м, 2H), 7,80 (шс, 1H), 7,43 (м, 2H), 7,17 (м, 4H), 4,39 (с, 2H), 3,59 (м, 2H), 3,47 (т, 2H), 3,10 (м, 2H), 2,86 (т, 2H), 1,67 (м, 2H), 1,54 (м, 2H), 1,36 (м, 4H).
Пример 70: N-циклобутил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)пентан-
1-сульфонамид (соединение 1070)
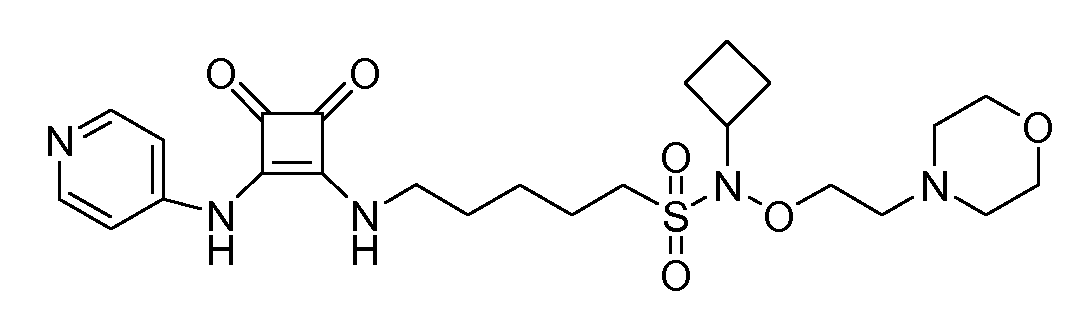
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-циклобутил-N-(2-морфолиноэтокси)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 4,24 (м, 1H), 4,18 (т, 2H), 3,74 (т, 2H), 3,70 (м, 4H), 3,11 (т, 2H), 2,69 (т, 2H), 2,56 (м, 4H), 2,41 (м, 2H), 2,13 (м, 2H), 1,92 (м, 2H), 1,74 (м, 4H), 1,61 (м, 2H).
Пример 71: N-циклобутил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)пентан-1-сульфонамид (соединение 1071)
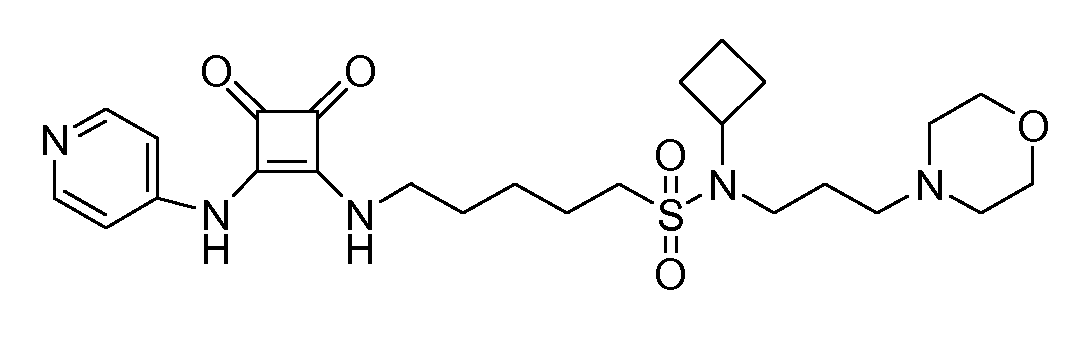
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-циклобутил-N-(3-морфолинопропил)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,40 (м, 2H), 7,83 (шс, 1H), 7,43 (м, 2H), 4,09 (м, 1H), 3,61 (т, 2H), 3,55 (м, 4H), 3,17 (м, 2H), 2,96 (м, 2H), 2,30 (м, 4H), 2,25 (т, 2H), 2,07 (м, 4H), 1,7-1,3 (м, 10H).
Пример 72: N-циклопентил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(3-морфолинопропил)пентан-
1-сульфонамид (соединение 1072)
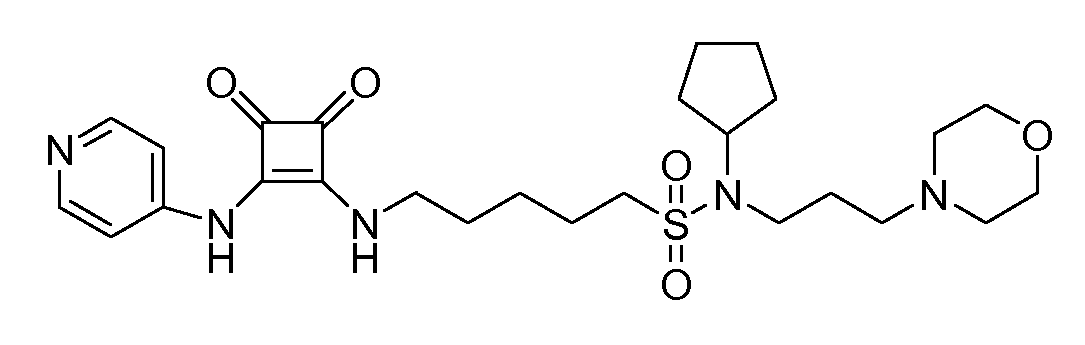
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-циклопентил-N-(3-морфолинопропил)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (CD3OD): δ 8,39 (м, 2H), 7,55 (м, 2H), 4,07 (м, 1H), 4,18 (т, 2H), 3,76 (т, 2H), 3,71 (м, 4H), 3,18 (м, 2H), 3,07 (т, 2H), 2,47 (м, 4H), 2,38 (т, 2H), 1,87 (м, 8H), 1,74 (м, 4H), 1,60 (м, 4H).
Пример 73: Этил 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)гексил(морфолино)фосфинат (соединение 1073)
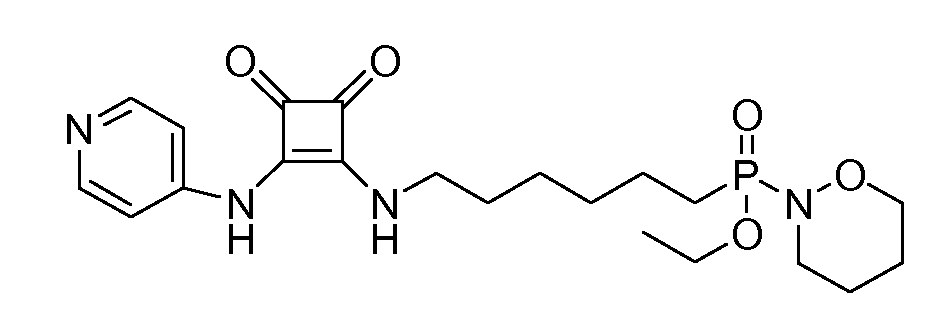
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и этил 6-аминогексил(морфолино)фосфинат (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 4,11 (м, 2H), 3,91 (т, 2H), 3,73 (т, 2H), 1,88 (м, 2H), 1,8-1,4 (м, 14H), 1,32 (т, 3H).
Пример 74: 3-(6-(4-ацетилпиперазин-1-илсульфонил)гексиламино)-4-(пиридин-4-иламино)циклобут-3-ен-1,2-дион (соединение 1074)
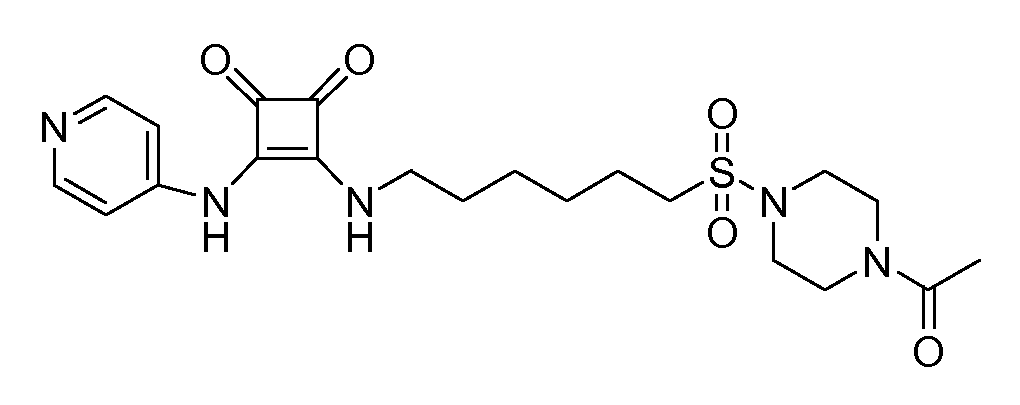
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 1-(4-(6-аминогексилсульфонил)пиперазин-1-ил)этанон (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,94 (шс, 1H), 8,40 (м, 2H), 7,82 (т, 1H), 7,43 (м, 2H), 3,59 (м, 6H), 3,17 (м, 2H), 3,09 (м, 2H), 3,02 (т, 2H), 1,67 (м, 2H), 1,56 (м, 2H), 1,37 (м, 4H).
Пример 75: 6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-фенилгексан-1-сульфонамид (соединение 1075)
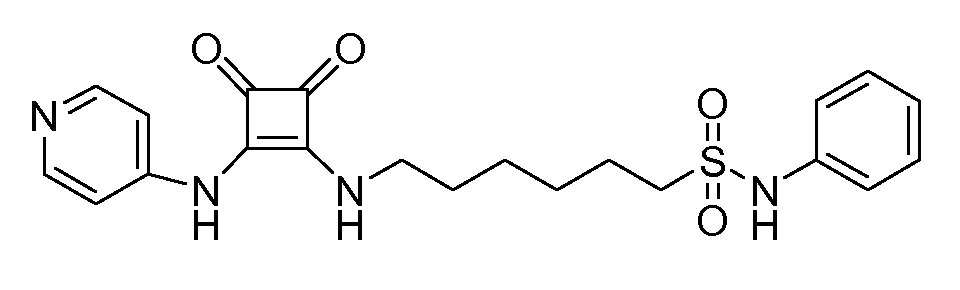
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-фенилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (ДМСО-d6): δ 9,88 (шс, 1H), 9,79 (с, 1H), 8,40 (м, 2H), 7,78 (т, 1H), 7,42 (м, 2H), 7,31 (м, 2H), 7,20 (м, 2H), 7,06 (м, 1H), 3,57 (кв, 2H), 3,06 (м, 2H), 1,67 (м, 2H), 1,51 (м, 2H), 1,32 (м, 4H).
Пример 76: N-(бензилокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-метилгексан-1-сульфонамид (соединение 1076)
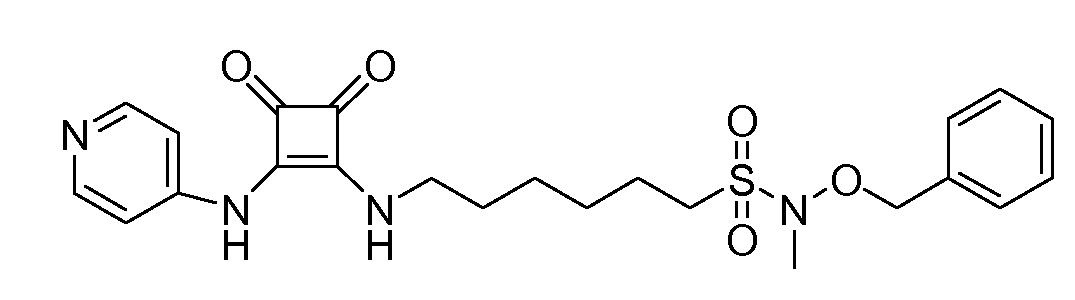
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(бензилокси)-N-метилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,40 (м, 2H), 7,81 (т, 1H), 7,43 (м, 2H), 7,38 (м, 5H), 4,90 (с, 2H), 3,60 (кв, 2H), 3,20 (м, 2H), 2,89 (с, 3H), 1,75 (м, 2H), 1,56 (м, 2H), 1,39 (м, 4H).
Пример 77: N-(бензилокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1077)
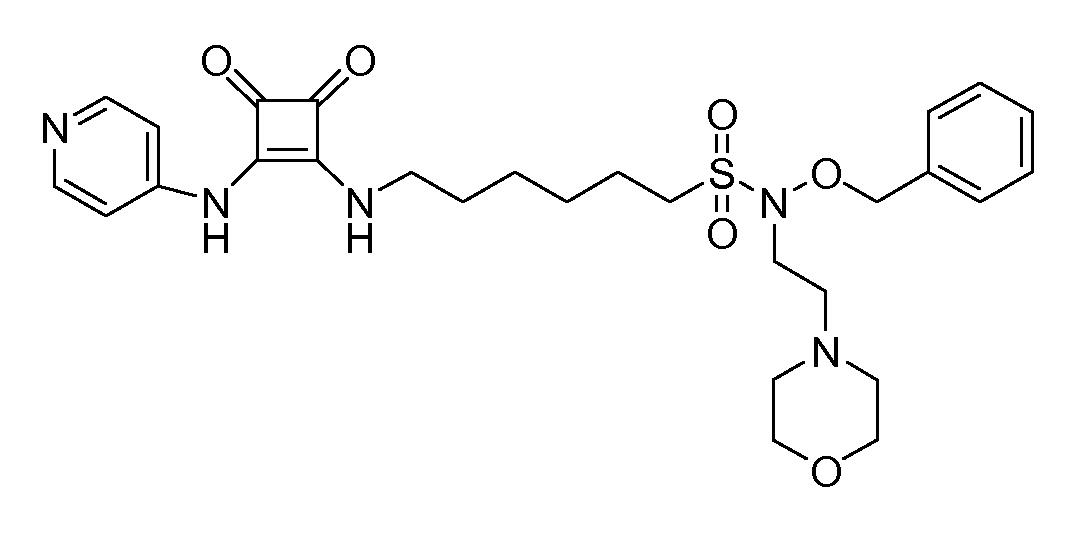
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(бензилокси)-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,37 (м, 2H), 7,54 (м, 2H), 7,39 (м, 5H), 5,05 (с, 2H), 3,68 (м, 6H), 3,40 (м, 2H), 3,23 (т, 2H), 2,53 (т, 2H), 2,47 (м, 4H), 1,92 (м, 2H), 1,70 (м, 2H), 1,52 (м, 4H).
Пример 78: N-циклопентил-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтокси)пентан-1-сульфонамид (соединение 1078)
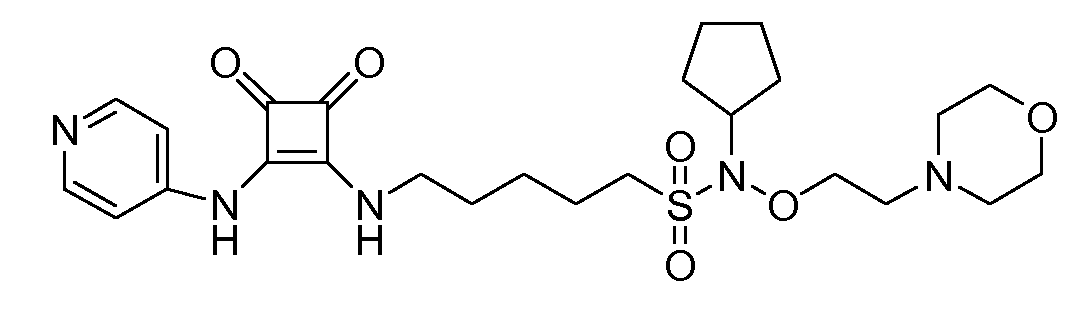
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 5-амино-N-циклопентил-N-(2-морфолиноэтокси)пентан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (CD3OD): δ 8,39 (м, 2H), 7,55 (м, 2H), 4,20 (м, 2H), 4,04 (м, 1H), 3,77 (т, 2H), 3,70 (м, 4H), 3,26 (т, 2H), 2,64 (т, 2H), 2,54 (м, 4H), 2,0-1,5 (м, 14H).
Пример 79: N-(4-хлорфенил)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-метилгексан-1-сульфонамид (соединение 1079)
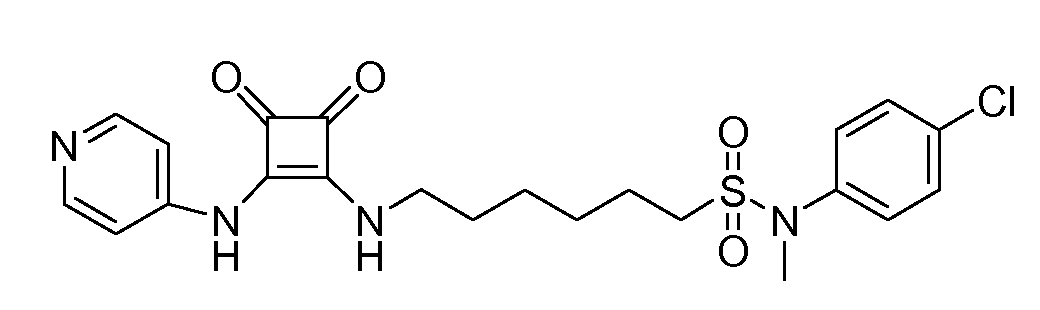
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(4-хлорфенил)-N-метилгексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (ДМСО-d6): δ 9,85 (шс, 1H), 8,39 (м, 2H), 7,5 (шс, 1H), 7,43 (м, 6H), 3,57 (т, 2H), 3,23 (с, 3H), 3,12 (м, 2H), 1,63 (м, 2H), 1,53 (м, 2H), 1,33 (м, 4H).
Пример 80: N-(4-хлорфенил)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-морфолиноэтил)гексан-1-сульфонамид (соединение 1080)
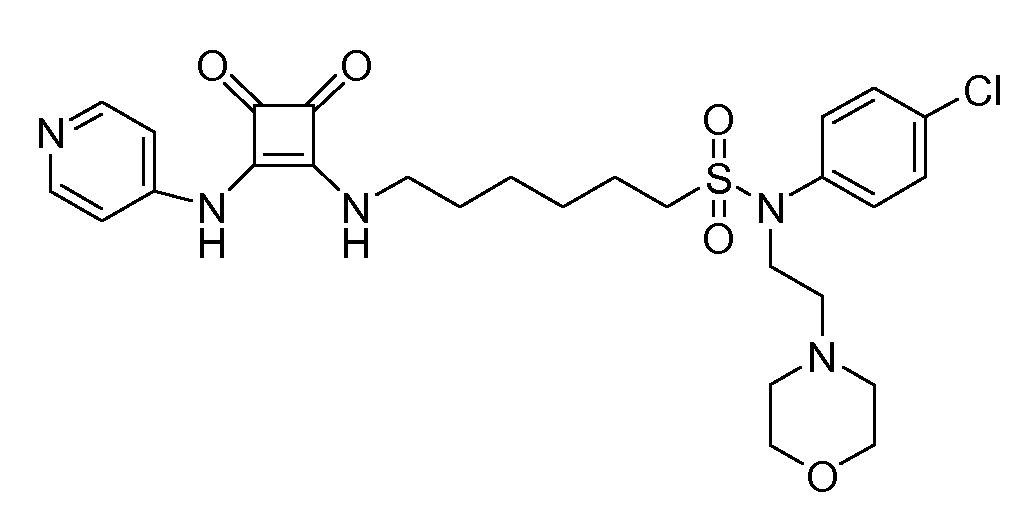
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(4-хлорфенил)-N-(2-морфолиноэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006)
1Н ЯМР (ДМСО-d6): δ 9,91 (шс, 1H), 8,40 (м, 2H), 7,78 (т, 1H), 7,43 (м, 6H), 3,72 (т, 2H), 3,54 (м, 6H), 3,15 (м, 2H), 2,29 (м, 6H), 1,68 (м, 2H), 1,75 (м, 2H), 1,35 (м, 4H).
Пример 81: N-(циклогексилметокси)-6-(3,4-диоксо-2-(пиридин-4-иламино)циклобут-1-ениламино)-N-(2-фторэтил)гексан-1-сульфонамид (соединение 1081)
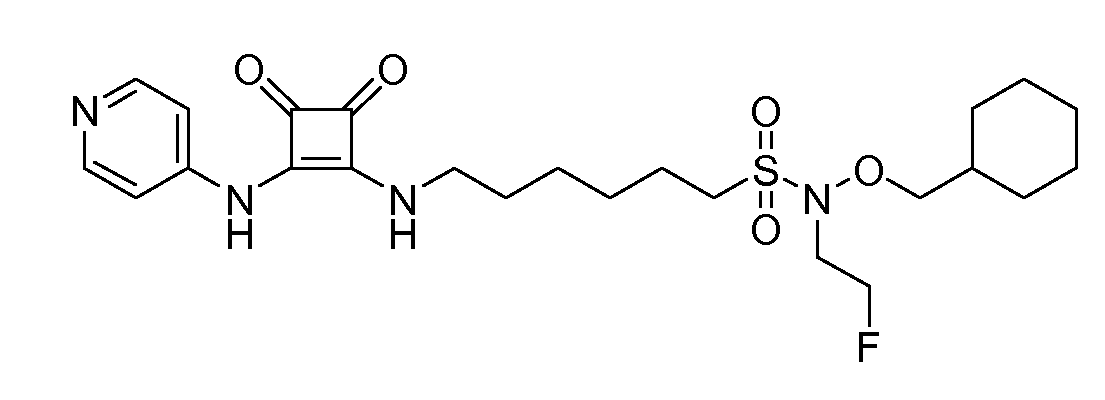
Общая методика 1. Исходные материалы: 3-этокси-4-(пиридин-4-иламино)циклобут-3-ен-2,3-дион и 6-амино-N-(циклогексилметокси)-N-(2-фторэтил)гексан-1-сульфонамид (см., например, предварительную заявку на патент США № 61/051130 (не опубликована) и PCT/DK2009/000006).
1Н ЯМР (ДМСО-d6): δ 9,90 (шс, 1H), 8,40 (м, 2H), 7,79 (шс, 1H), 7,42 (м, 2H), 4,60 (дт, 2H), 3,77 (д, 2H), 3,59 (м, 2H), 3,53 (м, 2H), 3,21 (м, 2H), 1,85-0,85 (м, 19H).
Пример 82: In vitro анализ пролиферации клеток (WST-I анализ)
Клетки A2780 высевают в 96-луночные планшеты в количестве 3x103 клеток/лунку в 100 мкл культуральной среды, 8 лунок оставляют пустыми для контроля только среды.
Через 24 ч проводят титрацию, в отдельной чашке Петри, серийным разведением соединения общей формулы (I) в культуральной среде. 100 мкл каждого разведения добавляют в посеянные клетки, это делают трижды, и включают контроли (например, ДМСО и пустые). Планшеты инкубируют в течение 24 ч при 37°C в CO2 инкубаторе. Титрование соединения повторяют в отдельной чашке Петри через 24 ч. Затем из анализируемых планшетов отсасывают среду и соединение. 100 мкл среды затем добавляют во все лунки, затем 100 мкл каждого разведения соединения. Планшеты инкубируют в течение еще 48 ч при 37°C в CO2 инкубаторе (общее время инкубирования 72 ч). Затем оценивают количество жизнеспособных клеток с применением реагента для пролиферации клеток WST-1. 10 мкл реагента WST-I добавляют в каждую лунку и инкубируют в течение от одного до четырех часов при 37°C в CO2 инкубаторе. Измеряют абсорбцию (450 нм/690 нм).
Активность соединений общей формулы (I) для снижения количества жизнеспособных клеток рассчитывают следующим образом:
% активности = [(Sc-B)/(S°-B)]x100,
где Sc означает сигнал, измеренный в присутствии тестируемого соединения, Sо означает сигнал, определенный в отсутствие соединения, и B означает фоновый сигнал, измеренный в пустых ячейках, содержащих только среду. Данные анализируют с применением GraphPad Prism.
Результаты показаны в таблице 1, где IC50 означает концентрацию, дающую 50% активность.
Пример 83: In vitro анализ пролиферации клеток (SRB анализ)
A2780 клетки высевают в 96-луночные планшеты в количестве 2000 клеток/лунку в 100 мкл культуральной среды, 4 лунки оставляют пустыми для контроля только среды.
Через 24 ч проводят титрацию, в отдельной чашке Петри, серийным разведением соединения общей формулы (I) в культуральной среде. 100 мкл каждого разведения добавляют в посеянные клетки, это делают четырежды, и включают контроли (например, ДМСО и пустые). Планшеты инкубируют в течение 72 ч при 37°C в CO2 инкубаторе. Затем добавляют 50 мкл холодной 50% трихлоруксусной кислоты в каждую лунку. Через 1 час надосадочную жидкость отбрасывают и лунки промывают 5 раз водопроводной водой и сушат при комнатной температуре. В каждую лунку добавляют 50 мкл 0,4% раствора Сульфо-Родамина B (SRB) в 1% уксусной кислоте и через 30 минут надосадочную жидкость удаляют и лунки промывают 4 раза 1% уксусной кислотой и сушат при комнатной температуре. Связанные пятна затем солюбилизируют добавлением 200 мкл 10 мМ Tris pH 10,5 в каждую лунку и планшеты встряхивают в течение, по крайней мере, 30 минут, и абсорбцию считывают на автоматическом планшетном ридере при 515 нм. Используя девять измерений абсорбции [время ноль, (Tz), контрольный рост, (C), и тестируемый рост в присутствии лекарственного средства в семи концентрациях (Ti)], процент роста рассчитывают для каждой из концентраций лекарственного средства после получения среднего для четырех лунок. Ингибирование процента роста рассчитывают следующим образом:
[(Ti-Tz)/(C-Tz)]x100 для концентраций, для которых Ti>/=Tz
[(Ti-Tz)/Tz]x100 для концентраций, для которых Ti<Tz.
Ингибирование роста на 50% (IC50) рассчитывают из [(Ti-Tz)/(C-Tz)]x100=50, что дает концентрацию лекарственного средства, дающую 50% снижение чистого увеличения белка (измеренного SRB окрашиванием) в контрольных лунках во время инкубирования лекарственного средства.
Результаты представлены в таблице 1.
|