Результат интеллектуальной деятельности: СПОСОБ ПОЛУЧЕНИЯ (2R,4R)-2-АЛКИЛ-3-(2-МЕРКАПТОБЕНЗОИЛ)-1,3-ТИАЗОЛИДИН-4-КАРБОНОВЫХ КИСЛОТ
Вид РИД
Изобретение
Изобретение относится к способу получения производных (2R,4R)-2-алкил-3-(2-меркаптобензоил)-1,3-тиазолидин-4-карбоновых кислот - потенциальных антигипертензивных веществ, ингибиторов ангиотензинпревращающего фермента (АПФ).
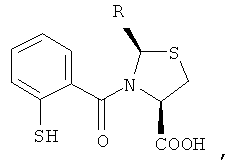
Анализ патентных данных показал, что из числа серусодержащих ингибиторов АПФ наиболее активными являются соединения, отвечающие общей формуле (I):

где R1=H или COAlk(Ar), R2=H или Alk, A - остаток циклической альфа-аминокислоты (или ее эфира), n=1 или 2.
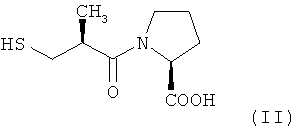
Первым среди препаратов такой серии был каптоприл - (S)-1-(3-меркапто-2-метил-1-оксопропил)-L-пролин (US 4,046,899; US 4,105,766; BE 861,454) (формула II):
Последующие исследования в поиске антигипертензивных веществ, ингибиторов АПФ были направлены на замену природной аминокислоты L-пролина в формуле (I) на синтетические циклические аминокислоты гетероциклического ряда. В ряду производных 1,3-тиазолидина пример ингибирующей активности по отношению к АПФ известен для разработанного фирмой Сантэн Фармацевтикал Ко (Япония) антигипертензивного препарата фентиаприла (III) - (2R,4R)-2-(2-гидроксифенил)-3-(3-меркаптопропионил)-1,3-тиазолидин-4-карбоновой кислоты (US 4,423,054), а также ряда других соединений, содержащих алкильный или арильный заместитель в положении 2 1,3-тиазолинового цикла (US 4,282,235):

Наиболее близким к заявляемым соединениям по своей структуре является S-3-(2-меркаптобензоил)-5,5-диметил-1,3-тиазолидин-4-карбоновая кислота (X=H) или ее S-ацетильное производное (X=COCH3) (IV) (US 6,211,212):

Соединение (IV) является производным синтетической аминокислоты (S-5,5-диметил-1,3-тиазолидин-4-карбоновой) и имеет иную конфигурацию карбоксильной группы в молекуле, чем большинство известных ингибиторов АПФ.
Технической задачей заявляемого способа является поиск новых и доступных в синтетическом отношении потенциальных антигипертензивных веществ, ингибиторов АПФ, соединений общей формулы (I), где в качестве фрагмента A используется 4R-2-алкил-1,3-тиазолидин-4-карбоновая кислота, а в качестве серусодержащего фрагмента - 2-меркаптобензоильная группировка:


Найдено, что взаимодействие L-цистеина с серией альдегидов RCH=O (где R - насыщенные алифатические или жирно-ароматические заместители, содержащие от 2 до 8 атомов углерода) проходит при 25°C в течение 10-15 ч при смешении исходных реагентов в воде или в водно-метанольном растворе и приводит к образованию 2-алкил-1,3-тиазолидин-4-карбоновой кислоты (V) в виде смеси 2R,S-стереоизомеров с выходами 80-95%.
Ацилирование соединений (V) дихлорангидридом дитиосалициловой кислоты (VI) проходит в тетрагидрофуране (ТГФ) в присутствии эквивалентного количества пиридина при 0-5°C в течение 1 ч и завершается через 5-10 ч при 25°С образованием бис-(2R,4R)-2,2'-диалкил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновых кислот (VII) с выходами 45-60%:

Восстановление дисульфидной группы соединений (VII) проходит в водном растворе при 25°C в присутствии сульфита натрия в течение 20-30 мин и приводит к образованию целевых продуктов - (2R,4R)-2-алкил-3-(2-меркаптобензоил)-1,3-тиазолидин-4-карбоновых кислот (VIII) с выходами 85-90%:

где R=C2H5, изо-C4H9, СН2СН2С6Н5, указанные в формуле заместители означают: С2Н5 - этил, изо-С4Н9 - изобутил, СН2СН2С6Н5 - фенилэтил. Положительным результатом предлагаемого способа является то, что конечный продукт получается оптически чистым, а в основе его синтеза используются природные или коммерчески доступные соединения.
Более подробно предлагаемый способ раскрывается на следующих примерах:
Пример 1. Смесь 1.32 г L-цистеина, 0.8 г пропионового альдегида в 50 мл метанола и 10 мл воды выдерживают при 25°C в течение 1-2 ч. После удаления растворителя выпавшую кристаллическую массу отфильтровывают, промывают эфиром, сушат и перекристаллизовывают из смеси этанол-вода, 2:1. Выход (2RS,4S)-2-этил-1,3-тиазолидин-4-карбоновой кислоты 80-55%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: (2R,4R)-форма (55%): 0.91 т (J=7.2 Гц, CH3); 1.54 м (CH2); 2.73 д. д (JAB=10.1 Гц, JAX=9.0 Гц, Н-5); 3.18 д. д (JAB=10.1 Гц, JBX=7.0 Гц, Н-5); 3.69 д. д (JAX=9.0 Гц, JBX=7.0 Гц, Н-4); 4.36 т (J=7.0 Гц, Н-2); (2S,4R)-форма (45%): 0.96 т (J=7.2 Гц, СН3); 1.71 м (СН2); 2.90 д. д (JAB=10.0 Гц, JAX=5.5 Гц, Н-5); 3.08 д. д (JAB=10.0 Гц, JBX=7.0 Гц, Н-5); 4.03 д. д (JAX=5.5 Гц, JBX=7.0 Гц, Н-4); 4.50 т (J=6.8 Гц, Н-2); Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: (2R,4R)-форма: 12.14 (СН3); 28.14 (СН2); 36.79 (С-5); 65.57 (С-4); 72.70 (С-2); 172.54 (С=0); (2S,4R)-форма: 12.31 (СН3); 30.07 (СН2); 37.11 (С-5); 64.38 (С-4); 72.00 (С-2); 172.99 (С=O).
Пример 2. Аналогичен примеру 1, только вместо пропионового альдегида используют 0.90 г изовалерианового альдегида. Выход (2RS,4S)-2-изобутил-1,3-тиазолидин-4-карбоновой кислоты 70%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: (2R,4R)-форма (60%): 0.89 д (J=6.4 Гц, 2СН3); 1.65 м (СН2); 1.79 м (СН); 2.75 д. д (JAB=10.0 Гц, JAX=9.0 Гц, Н-5); 3.19 д. д (JAB=10.0 Гц, JBX=7.0 Гц, Н-5); 3.70 д. д (JAX=9-0 Гц, JBX=7.0 Гц, Н-4); 4.46 т (J=7.0 Гц, Н-2); (2S,4R)-форма (40%): 0.90 д (J=6.4 Гц, 2СН3); 1.65 м (СН2); 1.76 м (СН); 2.94 д. д (JAB=10.3 Гц, JAX=5.0 Гц, Н-5); 3.08 д. д (JAB=10.3 Гц, JBX=7.0 Гц, Н-5); 4.08 д. д (JAX=5.0 Гц, JBX=7.0 Гц, Н-4); 4.61 т (J=7.2 Гц, Н-2); Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: (2R,4R)-форма: 22.26 (2СН3); 27.10 (СН); 37.15 (С-5); 44.02 (СН2); 65.27 (С-4); 69.62 (С-2); 172.04 (С=O); (2S,4R)-форма: 22.26 (2СН3); 26.76 (СН); 36.76 (С-5); 45.64 (СН2); 64.20 (С-4); 68.84 (С-2); 173.45 (С=O).
Пример 3. Аналогичен примеру 2, только вместо изовалерианового альдегида используют 1.35 г гидрокоричного альдегида, а в качестве растворителя используют 50 мл смеси вода-метанол, 4:1. Выход (2RS,4S)-2-(2-фенилэтил)-1,3-тиазолидин-4-карбоновой кислоты 85%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: (2R,4R)-форма (50%): 2.02 м (СН2); 2.67 м (СН2); 2.79 д. д (JAB=10.0 Гц, JAX=9.1 Гц, Н-5); 3.19 д. д (JAB=10.0 Гц, JBX=7.0 Гц, Н-5); 3.71 д. д (JAX=9.1 Гц, JBX=7.0 Гц, Н-4); 4.37 т (J=6.7 Гц, Н-2); (2S,4R)-форма (50%): 2.19 м (СН2); 2.67 м (СН2); 2.93 д. д (JAB=10.1 Гц, JAX=5.4 Гц, Н-5); 3.19 д. д (JAB=10.1 Гц, JBX=7.0 Гц, Н-5); 4.09 д. д (JAX=5.4 Гц, JBX=7.0 Гц, Н-4); 4.54 т (J=6.7 Гц, Н-2); Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: (2R,4R)-форма: 33.53 (СН2); 37.12 (С-5); 38.76 (СН2); 65.36 (С-4); 70.48 (С-2); 125.96-141.41 (Аr); 172.40 (С=O); (2S,4R)-форма: 33.74 (СН2); 36.87 (С-5); 38.74 (СН2); 64.23 (С-4); 69.66 (С-2); 125.96-141.41 (Аr); 172.90 (С=O)
Пример 4. К раствору 1.8 г (2S,4S)-2-этил-1,3-тиазолидин-4-карбоновой кислоты, полученной по примеру в смеси 30 мл ТГФ, 10 мл ДМФА и 1 мл пиридина при температуре 0-5°С добавляют 1.7 г дихлорангидрида дитиосалициловой кислоты. Смесь выдерживают при температуре 0-5°С в течение 1 ч, а затем при 20°С в течение 5 ч, удаляют растворитель в вакууме, а остаток нейтрализуют до pH 7 добавлением 0.1 М раствором НС1. Выпавшие кристаллы фильтруют, промывают водой и сушат. Выход бис-(2R,4R)-2,2'-диэтил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты 60%. Спектр ЯМР 1Н, ДМСО-d6, δ, м. д.: 0.97 м (6Н, 2СН3); 1.75 м (4Н, 2СН2); 3.21-3.47 м (4Н, 2Н-5); 4.63 м (2Н, 2Н-4); 5.20 м (2Н, 2Н-2); 7.39-7.56 м (8Н, Аr).
Пример 5. Аналогичен примеру 4, только вместо 1.7 г добавляется 2.5 г дихлорангидрида дитиосалициловой кислоты. Выход бис-(2R,4R)-2,2'-дипропил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты 65%. Добавление большего количества хлорангидрида не влияет на увеличение выхода целевого продукта.
Пример 6. Аналогичен примеру 4, только используется раствор в ТГФ (2RS,4S)-2-изобутил-1,3-тиазолидин-4-карбоновой кислоты, полученной по примеру 2. Выход бис-(2R,4R)-2,2'-диизобутил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты 60%. Спектр ЯМР 1Н, ДМСО-d6, δ, м. д.: 0.95 м (12Н, 4СН3); 1.75 м (4Н, 2СН2); 2.06 м (2Н, 2СН); 3.24-3.43 м (4Н, 2Н-5); 4.59 м (2Н, 2Н-4); 5.21 м (2Н, 2Н-2); 7.37-7.63 м (8Н, Аr).
Пример 7. Аналогичен примеру 6, только используется раствор в ТГФ (2RS,4S)-2-(2-фенилэтил)-1,3-тиазолидин-4-карбоновой кислоты, полученной по примеру 3. Выход бис-(2R,4R)-2,2'-(2,2'-дифенилэтил)-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты 75%. Спектр ЯМР 1Н, ДМСО-d6, δ м.д.: 2.01 м (4Н, 2СН2); 2.73 м (4Н, 2СН2); 3.14-3.38 м (4Н, Н-5); 4.60 м (2Н, 2Н-4); 5.29 м (2Н, 2Н-2); 7.14-7.47 м (18Н, Аr).
Пример 8. К суспензии 6 г бис-(2R,4R)-2,2'-диэтил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты в 50 мл воды при 25°С добавляют 5 г сульфита натрия. Образовавшийся через 5 мин гомогенный раствор выдерживают в течение 1 ч, а затем подкисляют до pH 5 добавлением разбавленной НСl. Выпавшие кристаллы фильтруют, сушат и перекристаллизовывают из смеси этанол-вода, 1:2. Выход (2R,4R)-2-этил-3-(2-меркапто-бензоил)-1,3-тиазолидин-4-карбоновой кислоты - 85%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: 0.98 т (3Н, J=7.2 Гц, СН3); 1.69 м (СН2); 3.15-3.48 м (2Н, Н-5); 4.52 т (1H, J=8.2 Гц, Н-4); 5.46 т (1Н, J=5.4 Гц, Н-2); 7.34-7.67 м (4Н, Аr). Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: 11.30 (СН3); 29.66 (СН2); 32.89 (С-5); 62.06 (С-4); 65.08 (С-2); 126.97-139.93 (Аr); 167.78 (С=O); 171.31 (С=O).
Пример 9. Аналогичен примеру 6, только используется суспензия 6 г бис-(2R,4R)-2,2'-диизобутил-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты. Выход (2R,4R)-2-изобутил-3-(2-меркаптобензоил)-1,3-тиазолидин-4-карбоновой кислоты - 80%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: 0.94 д (6Н, J=6.3 Гц, 2СН3); 1.63 м (2Н, СН2); 2.08 м (1H, СН); 3.21-3.56 м (2Н, Н-5); 4.53 т (1Н, J=8.2 Гц, Н-4); 5.52 т (1H, J=5.5 Гц, Н-2); 7.37-7.73 м (4Н, Аr). Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: 23.20 (2СН3); 26.10 (СН); 31.61 (С-5); 45.26 (СН2); 61.66 (С-4); 64.57 (С-2); 127.10-139.50 (Аr); 165.79 (С=O); 171.27 (С=O).
Пример 10. Аналогичен примеру 6, только используется суспензия 6 г бис-(2R,4R)-2,2'-(2,2'-дифенилэтил)-3,3'-(2,2'-дитиобензоил)-1,3-дитиазолидин-4,4'-дикарбоновой кислоты. Выход (2R,4R)-2-(2-фенилэтил)-3-(2-меркаптобензоил)-1,3-тиазолидин-4-карбоновой кислоты - 85%. Спектр ЯМР 1Н, ДМСО-d6, δ, м.д.: 2.00 м (2Н, СН2); 2.70 м (2Н, СН2); 3.17-3.39 м (2Н, Н-5); 4.47 т (1Н, J=8.0 Гц, Н-4); 5.48 т (1Н, J=5.3 Гц, Н-2); 7.07-7.83 м (9Н, Аr). Спектр ЯМР 13С, ДМСО-d6, δ, м.д.: 32.27 (С-5); 32.80 (СН2); 36.44 (СН2); 63.93 (С-4); 64.96 (С-2); 126.03-141.04 (Аr); 167.18 (С=O); 171.19 (С=O).
Таким образом, положительный результат данного способа заключается в том, что конечные продукты являются оптически чистыми, а в основе их синтеза используются природные или коммерчески доступные соединения.
Способ получения (2R,4R)-2-алкил-3-(2-меркаптобензоил)-1,3-тиазолидин-4-карбоновых кислот, включающий ацилирование дихлорангидридом дитиосалициловой кислоты 2-алкил-1,3-тиазолидин-4-карбоновых кислот, отличающийся тем, что в основе синтеза целевого продукта используют природную аминокислоту L-цистеин и алифатические или жирноароматические альдегиды, содержащие от 2 до 8 атомов углерода, при этом получают соединения формулы: где R=CH, изо-СН, CHCHCH, указанные в формуле заместители означают: СН - этил, изо-СН - изобутил, CHCHCH - фенилэтил.