Результат интеллектуальной деятельности: МИКРОФЛЮИДНАЯ СИСТЕМА ДЛЯ ПРОВЕДЕНИЯ ИММУНОАНАЛИЗА
Вид РИД
Изобретение
Изобретение относится к устройствам для проведения иммуноанализов и может использоваться для лабораторной диагностики вирусных инфекций.
Для лабораторной диагностики вирусных инфекций чаще всего используют методы иммуноферментного, или иммунофлуоресцентного анализа.
Метод иммуноферментного анализа предназначен для выявления антител и основан на использовании специфических вирусных белков - антигенов, выделенных из зараженных клеток, или полученных методами генной инженерии. Вирусные антигены сорбируют на стенках пластиковой ячейки и инкубируют с исследуемой сывороткой крови, содержащей определяемые антитела. После отмывания неспецифично связанных вязавшихся антител в ячейки добавляют вторые по отношению к определяемым антитела, ковалентно связанные с ферментом, обычно пероксидазой или щелочной фосфатазой. Избыток вторых антител отмывают, а количество связавшихся, зависящее от количества противовирусных антител в сыворотке, оценивают по интенсивности ферментативной реакции.
Метод иммунофлуоресцентного анализа применяют для выявления, как антигенов, так и антител. Этот метод основан на использовании реагентов, меченных флюоресцентным красителем. Антитела чаще всего метят флюоресцеин изотиоцианатом. Меченые антитела связываются с антигеном, образуя комплексы, которые можно выявить с помощью флюоресцентной микроскопии. Существуют три модификации иммунофлюоресцентного анализа:
- Метод прямой иммунофлюоресценции применяют для выявления антигенов. Он основан на непосредственном определении антигена, связанного с твердой подложкой, при помощи флюоресцентно меченых антител. Реакцию оценивают с помощью флюоресцентного микроскопа.
- Метод непрямой иммунофлюоресценции позволяет выявить антитела к известному антигену. Антиген, сорбированный на твердой подложке, связывается с определяемыми антителами. Комплексы антиген-антитело выявляются с помощью меченых антител к иммуноглобулинам.
- Метод конкурентной иммунофлюоресценции основан на добавлении к исследуемой пробе известной концентрации меченого антигена и проведении реакции с антителами, сорбированными на твердой подложке. Поскольку меченый и немеченый антигены конкурируют за связывание с антителами, по количеству связанного меченого антигена можно определить концентрацию антигена в исследуемой пробе.
Микрофлюидные технологии - одна из новых, быстро развивающихся областей конвергенции наук и технологий, основанная на интеграции высокотехнологичных и наукоемких методов микросистемотехники, электроники, физики, химии, оптики и гидравлики, молекулярной и клеточной биологии, информатики и других наук.
Основное достоинство микрофлюидных технологий состоит в том, что они позволяют работать с предельно малыми объемами реагентов - 10-9-10-15 литров и пикограммами веществ. Рассматриваемые рабочие среды могут представлять собой жидкости различной природы, содержащие нерастворимые микро- и наночастицы, полимерные молекулы, клеточные суспензии, эмульсии, состоящие из мицелл, капель неперемешивающихся жидкостей или воздушных пузырьков и др.
Для микрофлюидных систем характерны экстремально большие соотношения «поверхность/объем» и высокие скорости массо- и теплопереноса, что делает их исключительно эффективными для интенсификации протекания целевых процессов.
Ряд базовых характеристик микрофлюидных технологий делают их исключительно ценными и перспективными для решения широкого круга фундаментальных и прикладных задач:
- микрофлюидные технологии оперируют микро/фемто объемами анализируемых жидкостей;
- течение жидкости в микрофлюидных каналах является ламинарным, в силу этого возможен точный расчет транспортируемых масс веществ к различным точкам микрофлюидной системы в зависимости от геометрии каналов, распределения давления, свойств жидкости;
- в силу ламинарности смешивание потоков жидкостей осуществляется в результате диффузии;
- ламинарность потоков и диффузия в комбинации могут обеспечивать создание градиентов веществ в микрофлюидных системах;
- в микрофлюидной системе увеличивается отношение поверхности к объему, что создает оптимальные условия для диффузии и теплового обмена;
- капиллярные системы позволяют реализовать на микроуровне важнейшие транспортные методы современной аналитической химии: проточно-инжекционный анализ, основанный на разнице в давлениях, и высокоэффективный капиллярный электрофорез;
- уникальные возможности создания микроканалов сложной конфигурации, встраивания различных типов микрореакторов, управления микропотоками позволяют реализовать сложные многостадийные аналитические реакции;
- высокочувствительные системы детектирования результатов анализа например, флуоресцентные микроскопия и спектроскопия дают возможность обнаружения искомых компонентов на уровне следовых количеств (вплоть до единичных молекул);
- объемы жидкостей, которыми способны оперировать микрофлюидные устройства, сопоставимы с размерами клеток или на порядки меньше их.
Микрофлюидные системы представляют собой интегрированные устройства - лаборатории на чипах, образованные системой каналов с ламинарным течением жидкостей, что создает оптимальные и легко контролируемые условия для протекания транспортных и диффузионных процессов; функционирования бактериальных и эукариотических клеток; протекания молекулярно-биологических, молекулярно-генетических, биохимических, химических реакций.
Реакция свободной иммунодиффузии в микрофлюидных системах предназначена для выявления в исследуемых жидкостях антител или антигенов и основана на том, что в процессе взаимодействия антигена с антителом происходит образование комплекса антиген-антитело, в результате чего происходит существенное изменение размеров анализируемых частиц. Размеры конъюгатов антигена и флуоресцентного красителя значительно меньше размеров образующегося комплекса антиген - антитело. Увеличение размеров частицы приводит к изменению скорости диффузии. Изменение скорости диффузии меченых частиц в каналах микрофлюидной системы можно оценить по расстоянию, пройденному красителем в канале. Современные методы детекции позволяют определять характеристики процесса диффузии флуоресцентно-меченых частиц. Метод ограничен по способности определять антигены в силу сравнимости размеров образуемых комплексов и антител.
Известна микрофлюидная система в форме микрофлюидного чипа для быстрого множественного иммуноферментного твердофазного анализа, который представляет собой иммобилизованные антигены в одном или множестве каналов [Заявка США №20090123336, МПК: B01J 19/00, B01J 019/00; G01N 33/00]. Каждый канал включает секцию извилистого пути или множество секций извилистого пути. Рецептор для детектирования анализируемого вещества может быть закреплен в различных секциях извилистого пути, например с помощью адсорбции. Различные рецепторы могут быть иммобилизованы в различных секциях извилистого пути каждого канала или в различных каналах для одновременного детектирования множества анализируемых веществ. Этот чип является особенно полезным для проведения иммуноферментного твердофазного анализа.
Известна также микрофлюидная система в форме микрофлюидного чипа для детектирования присутствия анализируемого вещества в пробе жидкости, представляющий собой монолит и канал в этом монолите. Проток в канале имеет направление между входом и выходом и включает по крайней мере одну секцию извилистого пути [Патент США №8075854 МПК G01N 30/00]. У этого чипа секция извилистого пути включает рецептор, который комплементарен веществу, наличие которого будет тестироваться.
Эта микрофлюидная система принята за прототип изобретения.
Ее недостатком является необходимость проводить отмывку - удалять из канала несвязавшееся с рецептором анализируемое вещество.
Изобретение решает задачу создания системы для определения субстрата, способной осуществлять и тестировать реакцию между субстратом и рецептором, без иммобилизации рецептора и последующей отмывки.
Поставленная задача решается тем, что предлагается микрофлюидная система, включающая канал для анализируемой жидкости, отличающаяся тем, что она также содержит четыре канала, расположенных перпендикулярно к каналу для анализируемой жидкости, и одним концом соединяющихся с ним, при этом один из этих каналов является измерительным и в него помещены рецепторы в жидкой среде, другой канал является опорным и содержит жидкую среду, а в два других канала помещены флуоресцентные метки с иммобилизованным на них субстратом в жидкой среде.
Каналы системы выполнены в монолите.
Каналы закрыты со второго конца, который не соединяется с каналом для анализируемой жидкости.
Каналы, перпендикулярные каналу с анализируемой жидкостью, имеют одинаковые размеры.
Измерительный и опорный каналы содержат одинаковую жидкую среду.
Жидкой средой, как правило, является буферный раствор.
Флуоресцентные метки могут иметь форму квантовых точек.
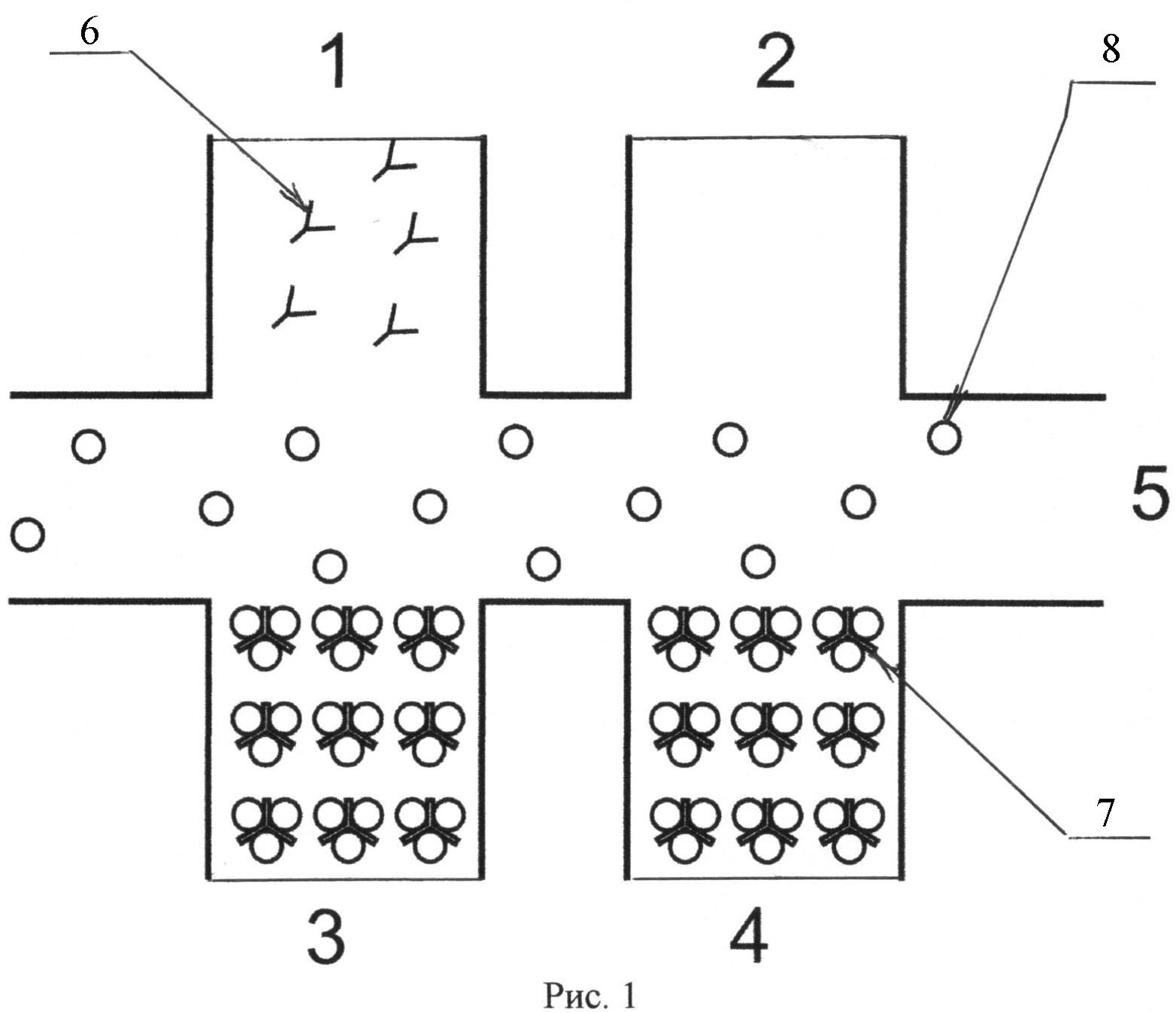
На рис.1 приведена схема предлагаемой микрофлюидной системы в исходном положении до начала анализа, где: 1 - измерительный канал, 2 - опорный канал, 3 - канал с флуоресцентными метками, 4 канал с канал с флуоресцентными метками, 5 - канал с анализируемой жидкостью, 6 - рецепторы, 7 - флуоресцентная метка, 8 - субстрат.
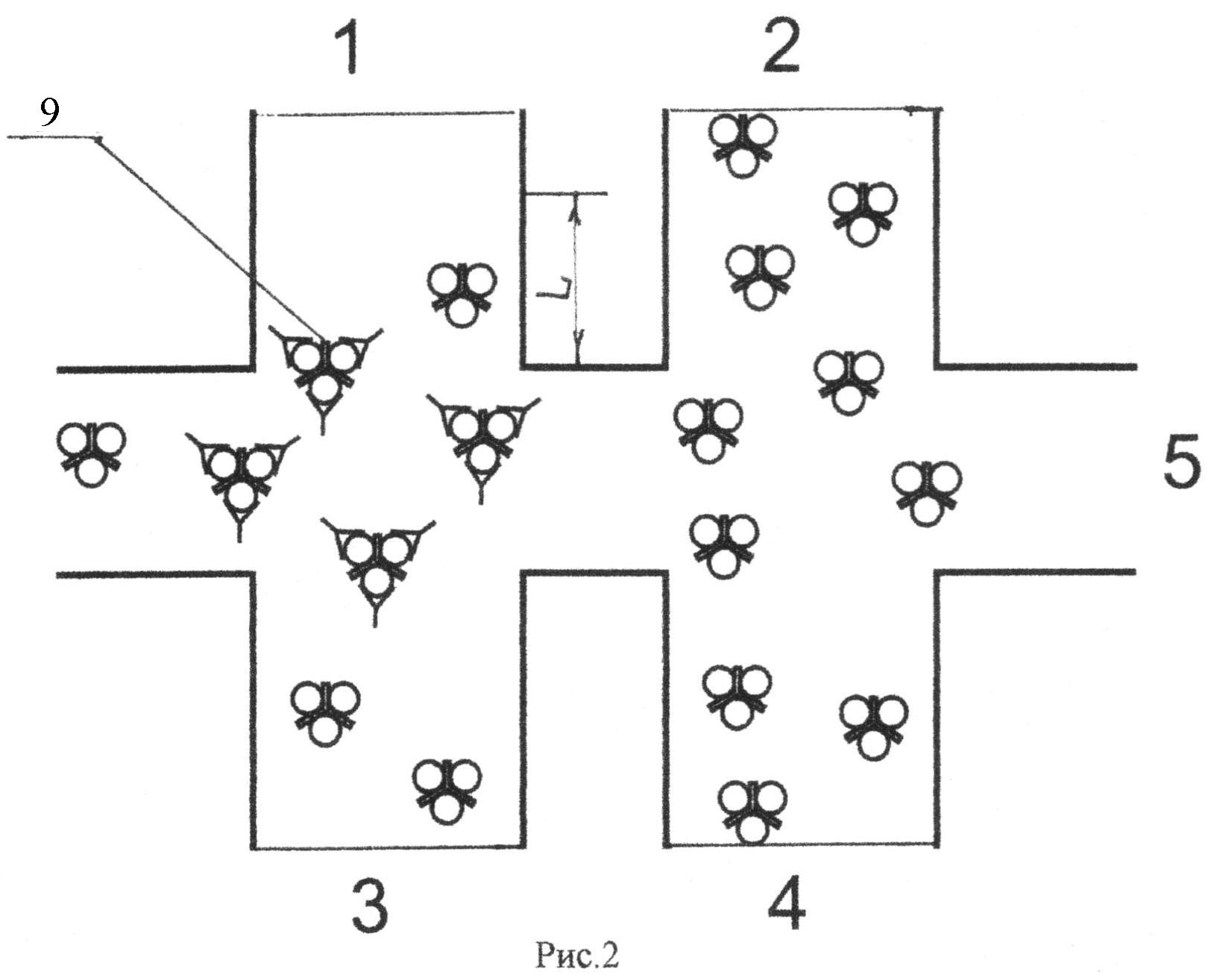
На рис.2 приведена схема предлагаемой микрофлюидной системы в конечном положении после проведения анализа, где: 9 - комплексы субстрата с рецепторами, L - расстояние от канала 5, где измеряется интенствность флуоресценции.
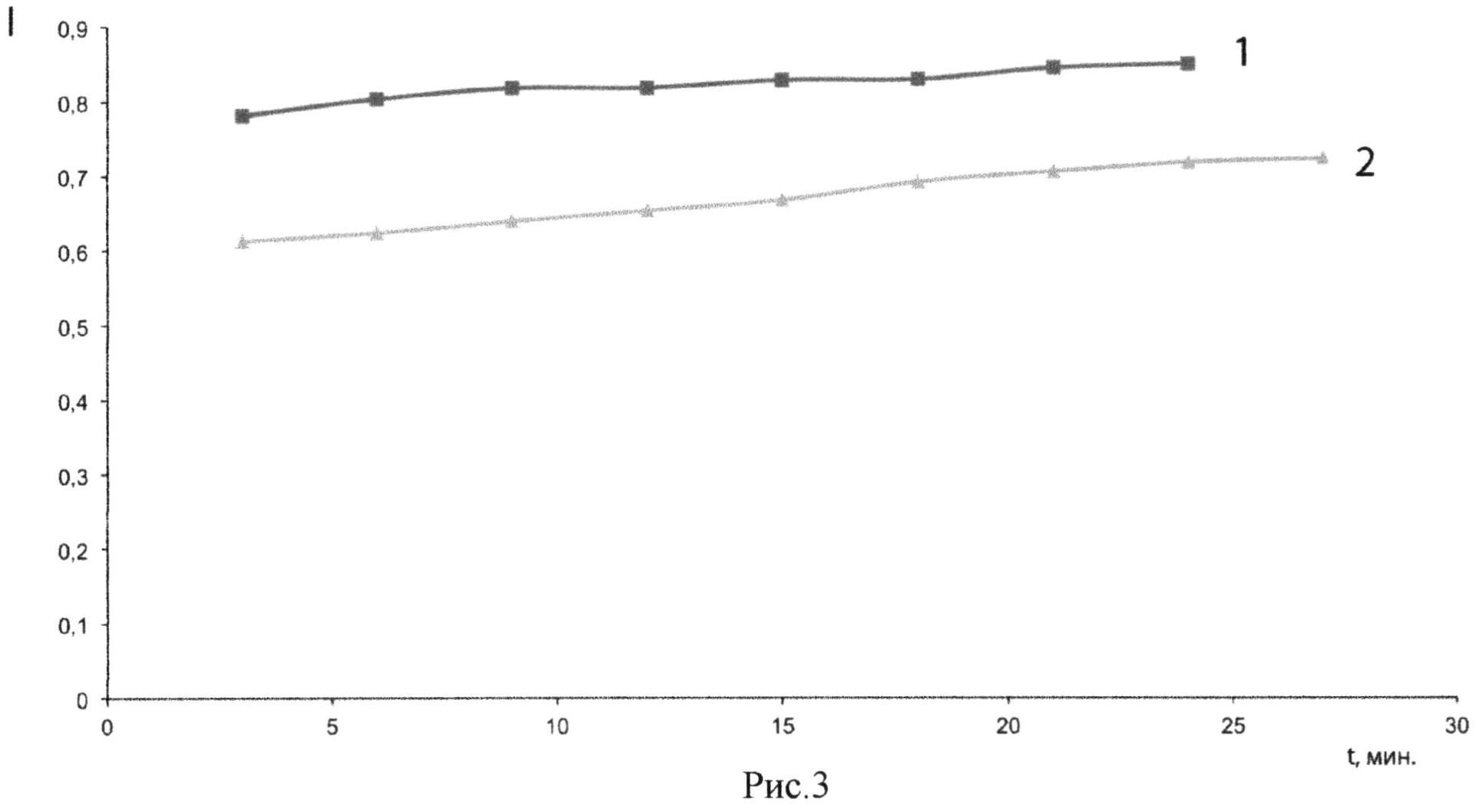
На рис.3 приведены кривые роста интенсивности флуоресценции в системе при проведении анализа, описанного в примере.
Как показано на рис.1 и 2, предлагаемая система имеет 5 каналов. Канал 1 является измерительным и в исходном состоянии, в него помещены рецепторы 6 в жидкой среде. Соседний с ним канал 2 является опорным и он заполнен такой же жидкой средой, как канал 1, но в исходном состоянии он не содержит никаких частиц, в том числе, рецепторов. Два других канала 3 и 4 расположены напротив измерительного и опорного каналов. Эти каналы в исходном состоянии содержат флуоресцентные метки 7 с иммобилизованным на них субстратом 8. Их размер больше, чем размер субстрата и размера рецептора. Центральный канал 5 расположен перпендикулярно каналам 1, 2, 3, и 4 и сообщается с каждым из них. Канал 5 предназначен для анализируемой жидкости.
Анализ осуществляют в следующем порядке.
Каналы 1, 2, 3, 4 заполняют жидкостью, например буферным раствором, при этом в канал 1 помещают рецепторы 6, а в каналы 3 и 4 помещают флуоресцентные метки 7 с иммобилизованным на них субстратом. Флуоресцентные метки представляют собой, например, квантовые точки с иммобилизованными на их поверхности антигенами. Размеры антигенов существенно меньше размеров специфических к ним антител и размеров флуоресцентных меток. В канал 5 подают анализируемую жидкость, которая содержит субстрат 8. Ширина и глубина каналов может варьировать от 10 мкм до 1 мм, наиболее предпочтительные размеры - менее 500 мкм по ширине. Подача реагентов осуществляется стандартными шприцами или другим способом, для продвижения жидкости может быть использован любой способ: давление, гравитация, капиллярные силы или другие.
После того, как канал 5 заполнен анализируемой жидкостью, ее подачу прекращают. В стационарных условиях начинается процесс диффузии из канала 5 субстрата 8 в каналы 1, 2, 3 и 4 и процесс диффузии меток 7 из каналов 3 и 4 через канал 5 в каналы 1 и 2 соответственно. При этом коэффициент диффузии субстрата в каналах существенно больше коэффициента диффузии меток. В канале 1 образуются комплексы субстрата 8 и рецепторов 6, в результате чего количество свободных рецепторов в канале 1 уменьшается.
Флуоресцентные метки 7 в процессе диффузии попадают в канал 5, а затем в канал 1 и 2 и часть из них образуют комплексы с оставшимися свободными рецепторами 6, т.к. метки представляют собой комплекс флуоресцентной частицы с иммобилизованным на поверхности субстратом. При этом коэффициент диффузии образующихся комплексов существенно меньше коэффициента диффузии меток. Наличие в канале 5 субстрата определяется по разности интенсивности флюоресценции на расстоянии L в каналах 1 и 2. Скорость нарастания интенсивности зависит от соотношения количества флуоресцентных меток и образовавшихся комплексов меток с рецепторами. Нарастание интенсивности в канале 2 на расстоянии L дает нормировочный коэффициент для определения наличия антигенов при условии одинаковой концентрации меток в каналах 3 и 4.
В основе работы этой системы лежит изменение скорости диффузии флуоресцентных нанокомплексов по сравнению со скоростью диффузии флуоресцентных меток в каналах микрофлюидной системы. Как известно из источников информации, реакция свободной иммунодиффузии предназначена для определения наличия в анализируемой жидкости только частиц, размеры которых существенно больше используемых флуоресцентных меток. Изменение скорости диффузии основано на увеличении стоксова радиуса при образовании флуоресцентных нанокомплексов при взаимодействии больших анализируемых частиц с маленькими метками. Это ограничивает возможность определения наличия в анализируемой жидкости частиц маленького размера из-за практически неизменного стоксового радиуса при взаимодействии больших меток с маленькими анализируемыми частицами.
Работа предлагаемой системы основана на связывании стандартного меченого (иммобилизованного на поверхности флуоресцентной метки) и присутствующего в исследуемой пробе жидкости немеченого субстрата с рецептором в канале 1. Поскольку меченый и немеченый субстрат конкурируют за связывание с рецептором, по скорости диффузии флуоресцентного комплекса в канале 1 можно определить наличие в канале 5 конкурирующего субстрата. В случае отсутствия в канале 5 конкурирующего субстрата интенсивность флуоресценции, формирующаяся в каналах 1 и 2 на расстоянии L от пересечения с каналом 5 за счет диффузии флуоресцентных комплексов, будет различаться через время t. Это различие обусловлено увеличением стоксова радиуса флуоресцентного комплекса за счет связывания с рецептором, находящимся в канале 1. В случае, когда в канале 5 присутствует субстрат (немеченые частицы маленького размера) весь (или частично) рецептор из канала 1 связывается с ним до того как в канал 1 диффундируют флуоресцентные комплексы из канала 3. Таким образом, для связывания с флуоресцентным комплексом свободных рецепторов не остается, а скорость диффузии флуоресцентных комплексов в каналах 1 и 2 становится одинаковой. В результате интенсивность флуоресценции, формирующаяся в каналах 1 и 2 на расстоянии L от пересечения с каналом 5 за счет диффузии флуоресцентных комплексов, будет одинакова через время t.
Измеряя интенсивность флуоресценции в каналах 1 и 2 на расстоянии L за время t и нормируя интенсивность флюоресценции в канале 1 на интенсивность флюоресценции в канале 2 можно определить наличие субстрата в исследуемой жидкости.
Измерение интенсивности флюоресценции осуществляют в отсутствие движения жидкости в системе.
Возможна нормировка системы для количественного определения субстрата в анализируемой жидкости, однако, на практике достаточно провести качественный анализ, чтобы определить наличие или отсутствие заболевания.
Таким образом, предлагаемая микрофлюидная система для определения субстрата, способна осуществлять и тестировать реакцию между субстратом и рецептором без иммобилизации рецептора и последующей отмывки, что существенно облегчает проведение анализов.
Кроме прочего, система позволяет проводить анализы, когда размеры антигенов существенно меньше размеров специфических к ним антител и размеров флуоресцентных меток.
Пример
Флуоресцентные метки представляют собой квантовые точки Qdots 625 с иммобилизованным на их поверхности белком p24 HIV - антигена вируса иммунодифицита человека. В каналы 3 и 4 микрофлюидной системы помещают флуоресцентные метки.
В канал 1 помещают антитела к белку р24 HIV, канал 2 оставляют заполненным буферным раствором TBS (50 мМ ТРИС, 0,9% NaCl, pН 7.2). В канал 5 подают анализируемую жидкость - белок р24 HIV в концентрации 0,08 мг/мл в буферном растворе.
Для регистрации сигнала систему позиционируют на предметном столике инвертированного флуоресцентного микроскопа и осуществляют покадровую съемку процесса диффузии в каналах 1 и 2 на расстоянии 3 мм от пересечения каналов 1 и 2 с каналом 5.
На рис.3 показан график интенсивности флуоресцентного сигнала по результатам покадровой съемки в зависимости от времени после подачи в систему анализируемой жидкости. Кривая 1 показывает рост интенсивности сигнала в опорном канале 2, а кривая 2 показывает рост интенсивности сигнала в измерительном канале 1. Рост интенсивности флуоресценции свидетельствует о наличи в тестируемом образце жидкости белка р24 HIV.