Результат интеллектуальной деятельности: СПОСОБЫ И КОМПОЗИЦИИ ДЛЯ ЛЕЧЕНИЯ ШИЗОФРЕНИИ С ИСПОЛЬЗОВАНИЕМ НЕЙРОЛЕПТИЧЕСКОЙ КОМБИНИРОВАННОЙ ТЕРАПИИ
Вид РИД
Изобретение
ПРЕДПОСЫЛКИ К СОЗДАНИЮ ИЗОБРЕТЕНИЯ
Краткий Обзор по Шизофрении
Шизофрения резко ухудшает здоровье и благосостояние людей, которые страдают этим расстройством психики, являющимся одним из самых тяжелых и трудных для лечения. Лица, страдающие шизофренией ("шизофреники"), могут страдать несметным числом симптомов и могут требовать тщательной опеки и непрерывной лекарственной и/или режимной терапии, что приводит к существенным социально-экономическим затратам, даже в отсутствии госпитализации или институционализации. Шизофрения затрагивает приблизительно 2 миллиона американцев. Болезнь обычно развивается между пубертатным периодом и возрастом 30 лет и характеризуется одним или более положительными симптомами (например, иллюзиями и галлюцинациями) и/или отрицательными симптомами (например, замедленными эмоциями и отсутствием интереса) и/или дезорганизованными симптомами (например, спутанное сознание и речь, или дезорганизованное поведение и восприятие). Во многих исследованиях показано, что шизофреники имеют сниженные способности в решении задач, требующих кратковременной устной рабочей памяти, быстро ассоциируемого когнитивного "прогноза" или "ожидания" или продолжительного контроля внимания/бдительности. Шизофреники, которые имеют слуховые галлюцинации (которые описаны для большинства пораженных лиц), также имеют сильно коррелирующее снижение их способностях восприятия речи. Шизофреники также имеют социальные и функциональные дефициты, например, дефициты и спутанность в идентификации настроения или реакций других людей, в определении, что для них является социально правильным курсом действия и в идентификации причин настоящих и прошлых действий или событий. Шизофрения представляет собой хроническое нарушение, и большинство пациентов требует постоянного лечения для облегчения или уменьшения частоты психотических эпизодов. Причины шизофрении в значительной степени неизвестны. Хотя она, как считается, имеет генетический компонент, факторы окружающей среды, по-видимому, влияют на возникновение и серьезность заболевания.
Краткий Обзор Механистических Соображений в Патогенезе Шизофрении
До недавнего времени внимание исследователей, работающих в области биохимии психозов, было главным образом сконцентрировано на двух системах медиаторов: система допамина и система серотонина. Гипотеза допамина происходила от общей способности традиционных (типичных) нейролептических лекарственных средств вызывать неврологические побочные эффекты, подобные симптомам Болезни Паркинсона. Это самое свойство также дало препаратам общепринятое название нейролептиков. Нейробиохимия паркинсонизма связана с нарушением баланса между допамином и холинергическими системами в nigrostriatum, в котором активность допаминовых структур снижается, в то время как активность холинергических структур увеличивается. Способность типичных нейролептиков контролировать продуктивную семиологию у пациентов, страдающих шизофреническим нарушением (иллюзии, галлюцинации, спутанность поведения) коррелирует со способностью вызывать паркинсонизм и происходит от свойств подавления активности системы допамина. Таким образом, было сделано заключение, что положительная семиология психоза является следствием чрезмерной активности допаминергической системы. Еще одним аргументом в пользу этого результата был результат исследования метаболитов допамина в спинальной жидкости. Более высокое уровни гомованильной кислоты (продукт метаболизма допамина) были найдены у пациентов с психозом по сравнению со здоровыми людьми. В настоящее время эта гипотеза была развита далее под влиянием новых данных, включающих результаты посмертного исследования мозга и позитронной эмиссионной томографии живых пациентов. Важная роль регулятора рецепторов допамина была показана тщательным исследованием изменений функции допаминергической системы под влиянием нейролептических лекарственных средств. Были описаны несколько типов рецепторов допамина, каждый из которых имеет свои собственные особенности локализации и функции.
Допаминергические агенты, прежде всего блокаторы рецептора допамина подтипа D2, в частности, галоперидол и хлорпромазин и многие другие, широко используются для лечения пациентов с шизофренией в соответствии с допаминовой теорией шизофрении. Они эффективно уменьшают фазу острого психоза у пациентов с шизофренией, но часто намного менее эффективны в лечении других фаз этого заболевания. По этой причине в последние годы было проведено интенсивное исследование по изучению механизма патогенеза шизофрении и разработке новых лекарственных средств для ее эффективного лечения.
Вторая гипотеза предполагает, что фундаментальной причиной является нарушение соотношения между системами допамин и серотонина. Серотонинэргические структуры оказывает сложный корректирующий эффект на функцию допаминергической системы, увеличивая ее активность в мезолимбической и мезостриатальной структурах и уменьшая ее в префронтальной области, что обусловливает клинические феномены гипофронтальной функции. Весомым аргументом в пользу этой гипотезы, как обычно считается, является введение прототипа атипичных нейролептиков, клозапина, в клиническую практику. Нейрохимический спектр активности клозапина отличает его от всех нейролептических средств, известных на тот момент, поскольку клозапин блокирует серотонинергические рецепторы в основном сильнее, чем допаминергические рецепторы. Кроме того, оказалось, что он является эффективным в отношении заболеваний, в которых преобладают первичные нарушения, связанные с дефицитами, и также в большинстве случаев, которые демонстрируют резистентность к традиционным нейролептическим средствам. Кроме того, клозапин значительно реже вызывает нейролептические побочные эффекты J.M. Kane, "The new antipsychotics,"J. Pract. Psychiatry Behav. Health, 1997, 3:343-354.
Данные, полученные в ходе клинического исследования нейролептиков второго поколения (блокаторы серотонина-допамина, так называемые атипичные нейролептики "AН"), показали превосходство этих лекарственных средств над нейролептическими средствами первого поколения (блокаторы допамина "БД") в отношении их эффекта на отрицательные симптомы шизофрении, на устойчивые продуктивные симптомы и нейрокогнитивные нарушения. Сегодня существует множество гипотез, в рамках которых делаются попытки объяснить фармакодинамические механизмы, которые приводят к превосходству АН над нейролептическими средствами первого поколения (гипотеза преобладающего эффекта на серотониновые структуры шовных ядер, гипотеза быстрой неадгезивной блокады допаминовых рецепторов, гипотеза глутаматных эффектов клозапина). Биоклинические исследования в области шизофрении, включая успехи психофармакологии, находят все более убедительные факты, свидетельствующие о зависимости между развитием и сохранением клинических симптомов и нейрокогнитивных нарушений в случаях шизофрении и множеством нейрохимических, нейроиммунологических, биохимических, генетических и морфологических характеристик.
Гипотезы, описанные выше, имеют достаточную объяснительную ценность относительно большого тела фактов. Однако, не все данные вписываются в них. Известно, что блокада допаминергических рецепторов происходит намного быстрее, чем развивается клинический эффект. Кроме того, степень блокады этих рецепторов является такой же у пациентов, которые хорошо реагируют на нейролептическую терапию, как и у пациентов, которые являются устойчивыми к ней (S. Heckers, "Neural models of schizophrenia," Dialogues in Clinical Neuroscience, 2000,2(3): 267-280). С другой стороны, попытки психофармакологов разработать лекарственное средство с нейролептическими эффектами, которое не затрагивало бы допаминергическую систему, не приводили к успеху (S. Kapur, G. Remington, "Dopamine D(2) receptors and their role in atypical antipsychotic action: still necessary and may even be sufficient," Biol. Psychiatry, 2001, 50 (11):873-83).
В то же самое время, не все практики одинаково смотрят на смену поколений нейролептических лекарственных средств. Кроме того, некоторые скептически смотрят на идею, что препараты второго поколения имеют более широкий спектр эффективности. Действительно, исследования, в которых терапевтическая реакция на лекарственное средство первого поколения сравнивается с реакцией на лекарственное средство второго поколения, не показывают значительного преимущества в отношении контроля над продуктивными симптомами психоза. Именно этот эффект в особенности является традиционным индикатором терапевтической активности нейролептического средства. Расширение понятия фармакодинамики нейролептических средств и возможного резерва, скрытого в ремиссии, которая достигается благодаря типичной терапии, может быть очень важным для пересмотра отношения практикующих психиатров к новым препаратам.
Помимо широко признанной важности допаминовой и серотониновой активности нейролептиков для осуществления их клинической активности, привлекает к себе внимание еще одна нейромедиаторная система. Это глутаматергическая нейромедиаторная система центральной нервной системы (ЦНС). Поскольку многие исследователи в последние годы склонялись к мнению, что когнитивные нарушения играют фундаментальную роль в формировании шизофреничного нарушения (N.C. Andreasen, "Schizophrenia: the fundamental questions," Brain Res. Rev., 2000, 31 (2-3): 106-12), глутаматергическая система притягивает все возрастающий интерес, не только теоретически, но также и практически (K. Hashimoto, M. Iyo, "Glutamate hypothesis of schizophrenia and targets for new antipsychotic drugs," Nihon Shinkei Seishin Yakurigaku Zasshi, 2002, 22 (1):3-13). Стимуляция глутаматергической передачи может приводить к стимуляции активности центральной нервной системы, но в некоторый момент это может также привести к токсическим эффектам в отношении мозга. С другой стороны, подавление глутаматергической системы может привести к нейропротективным эффектам, но наряду с ними, к дефициту когнитивной функции (S. Heckers, C. Konradi, "Hippocampal neurons in schizophrenia," J. Neural Transm., 2002,109(5-6):891-905). Некоторые исследователи полагают способность оказывать глутаматергический эффект единственным возможным нейрохимическим механизмом антидефицитной активности клозапина (L. Chen, CR. Yang, "Interaction of dopamine Dl and NMDA receptors mediates acute clozapine potentiation of glutamate EPSPs in rat prefrontal cortex," J. Neurophysiol, 2002, 87 (5):2324-36). Кроме того, глутаматергической системе приписывают роль в координации функционирования других проводящих структур мозга. Эта функция может быть осуществлена, в частности, вследствие гипотетической способности мозжечка (в функционировании которого глутаматергическая система играет важную роль) формировать временную организацию умственных процессов (N.C. Andreasen, "Schizophrenia: the fundamental questions," Brain Res. Rev. 2000, 31 (2-3): 106-12). Контроль этой функции с трудом достижим для традиционных нейролептических лекарственных средств. Однако, глутаматная активность клозапина в этой связи влечет за собой возможность формирования новых гипотез, которые объясняют его необычную клиническую активность в ходе длительного курса лечения (L. Chen, CR. Yang, "Interaction of dopamine Dl and NMDA receptors mediates acute clozapine potentiation of glutamate EPSPs in rat prefrontal cortex," J. Neurophysiol, 2002; 87(5): 2324-36) и формирование новых гомеостатических связей, требующих длительного периода времени. Несмотря на мгновенную блокаду рецепторов допамина, первые симптомы клинического эффекта нейролептиков (контроль продуктивных симптомов) проявляются постепенно, в течение более чем нескольких недель, и выздоровление пациента длится много месяцев.
Таким образом, наряду с теорией патогенеза шизофрении, которая была разработана относительно давно и широко принята, где главная роль отдается гиперфункционированию допаминергической нейромедиаторной системы ЦНС и также дисбаллансу в серотонинергической медиаторной системе, совсем недавно произошло интенсивное развитие теории патогенеза, где главную роль в развитии этого заболевания играют нарушения в глутаматергической нейромедиаторной системе ЦНС. Предположено, что многие элементы психического нарушения, которые наблюдаются у пациентов с шизофренией, связаны с гипофукционированием глутаматергической системы. Поддержка глутаматной теории шизофрении включает факт, что фенциклидин, блокатор ионного канала рецептора NMDA, одного из основных подтипов глутаматных рецепторов, вызывает у здоровых добровольцев комплекс поведенческих симптомов, которые являются очень схожими с поведением пациентов, страдающих шизофренией: они демонстрируют психоз, аутизм, плохое настроение; они становятся неспособными решать задачи (тесты); они становятся эксцентричными и их речь и мышление ухудшаются. В настоящее время фенциклидиновая модель шизофрении, как полагают, является самой близкой и самой адекватной поведению пациентов, страдающих шизофренией (R. M. Allen, S. J. Young, "Phencyclidine-induced psychosis," Amer. J. Psychiatry, 1976, 33:1425-8). Подобные эффекты также вызываются другими блокаторами ионного канала рецептора NMDA, такими как кетамин, и блокаторами AMPA, такими как МК-801. Показано, что пациенты, страдающие шизофренией, демонстрируют более низкий уровень глутаминовой кислоты в цереброспинальной жидкости, чем нормальные люди. Также показано в последующих исследованиях, что в мозге пациентов, страдающих шизофренией, наблюдается увеличение большого диаметра глутаматергических волокон, который на 30% больше, чем в мозге пациентов, не страдающих шизофренией, и что наблюдается одновременное уменьшение малого диаметра глутаматергических волокон на 78%. Кроме того, в коре головного мозга пациентов, страдающих шизофренией, наблюдается увеличение числа рецепторов NMDA, но также наблюдается уменьшение обратного захвата глутамата в базальных ганглиях.
Краткое описание Гидрированных Производных Пиридо[4,3-b]Индола
Известные соединения класса производных тетра- и гексагидро-1H-пиридо[4,3-b]индола проявляют широкий спектр биологической активности. В ряду 2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индолов были обнаружены следующие типы активности: антигистаминовая активность (DE 1 813 229, подана 6 декабря 1968; DE 1 952 800, подана 20 октября 1969), центральная депрессивная и противовоспалительная активность (US 3 718 657, подана 3 декабря 1970), нейролептическая активность (Herbert C A., Plattner S.S., Welch W.M., Mol. Pharm. 1980, v.17, N 1, p. 38-42) и другие. Производные 2,3,4,4a,5,9b-гексагидро-1H-пиридо[4,3-b]индола показывают психотропную (Welch W.M., Harbert CA., Weissman А., Кое B.K., J.Med.Chem.,1986, vol.29, No. 10, p. 2093-2099), антиагрессивную, антиаритмическую и другие типы активности.
Известно, что некоторые лекарственные средства, такие как диазолин (мебгидролин), димебон, дорастин, карбидин (дикарбин), стобадин и гевотролин, были получены на основе производных тетра- или гексагидро-1H-пиридо[4,3-b]индола. Диазолин (2-метил-5-бензил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид) (Klyuev M.A., Drugs, used in "Medical Pract.", USSR, Moscow, "Meditzina" Publishers, 1991, p.512) и димебон (2,8-диметил-5-(2-(6-метил-3-пиридил)этил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид) (M. D. Mashkovsky, "Medicinal Drugs" in 2 vol. Vol. 1,12th Edition, Moscow, "Meditzina" Publishers, 1993, p.383), а также дорастин (2-метил-8-хлор-5-[2-(6-метил-3-пиридил)этил]-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид) (USAN and USP dictionary of drugs names (United States Adopted Names, 1961-1988, current US Pharmacopoeia and National Formula for Drugs and other nonproprietary drug names), 1989, 26th Edition., p. 196), известны как антигистаминные препараты; карбидин (дикарбин) (цис(±)-2,8-диметил-2,3,4,4a,5,9b-гексагидро-1H-пиридо[4,3-b]индол дигидрохлорид) представляет собой нейролептическое средство, имеющее антидепрессивный эффект (L. N. Yakhontov, R. G. Glushkov, Synthetic Drugs, ed. by A. G. Natradze, Moscow, "Meditzina" Publishers, 1983, p.234-237), и его (-)-изомер, стобадин, известен как противоаритмическое средство (Kitlova M., Gibela P., Drimal J., Bratisl. Lek. Listy, 1985, vol.84, No.5, p.542-549); гевотролин, 8-фтор-2-(3-(3-пиридил)пропил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид, представляет собой нейролептик и транквилизатор (Abou-Gharbi M., Patel U.R., Webb M.B., Moyer J.A., Ardnee Т.Н., J. Med. Chem., 1987, vol.30, p.l818-1823). Димебон использовался в медицине как противоаллергическое средство (Авторское Свидетельство Номер 1138164, IP Класс A61K 31/47,5, C07 D 209/52, опубликовано 7 февраля 1985) в России в течение более 20 лет.
Как описано в Патенте США 6187785 и 7021206, гидрированные производные пиридо[4,3-b]индола, такие как димебон, имеют свойства антагониста NMDA, которые делают их пригодными для лечения нейродегенеративных заболеваний, таких как Болезнь Альцгеймера. Как описано в WO 2005/055951, гидрированные производные пиридо[4,3-b]индола, такие как димебон, пригодны в медицине или ветеринарии в качестве геропротекторов, например, задерживая начало и/или развитие связанного с возрастом или относящегося к возрасту проявления и/или патологии или состояния, включая расстройство в кожно-волосяном наружном покрове, расстройство зрительного восприятия и снижение массы тела. В заявках на патенты США 11/543529 (Публикация США Номер 20070117835) и 11/543341 (Публикация США Номер 20070117834) раскрыты гидрированные производные пиридо[4,3-b]индола, такие как димебон, в качестве нейропротекторов для использования в лечении и/или профилактике и/или замедлении прогрессии или начала и/или развития болезни Гентингтона. Димебон и/или его свойства также обсуждаются в: Yu. Ya. Ivanov et al., 2001; N.N. Lermontova et al., 2001 ; S.O. Bachurin et al, 2003and V.V. Grigor'ev et al., 2003.
Значительная Медицинская Потребность
Сохраняется значительный интерес и потребность в дополнительных или альтернативных терапиях для лечения, профилактики и/или задержки начала и/или развития шизофрении. Предпочтительно, новые терапии должны улучшать качество жизни для пациентов с шизофренией и/или сопровождаться меньшим числом побочных эффектов или менее тяжелыми побочными эффектами по сравнению с доступными в настоящее время терапиями.
КРАТКОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
Описываются способы, комбинированные терапии, фармацевтические композиции и наборы для лечения и/или профилактики и/или задержки начала и/или развития шизофрении с использованием гидрированного [4,3-b]индола и нейролептика или фармацевтически приемлемой соли любого из них. Изобретение охватывает комбинированные терапии, имеющие первое соединение и второе средство, где первое соединение представляет собой гидрированный [4,3-b]индол, подробно описанный здесь, и второе средство представляет собой нейролептик. Второе средство может быть типичным нейролептиком или атипичным нейролептиком или комбинацией атипичного и типичного нейролептика (когда второе средство может содержать по меньшей мере два различных соединения). Изобретение, в частности, охватывает комбинированную терапию, в которой первое соединение представляет собой димебон (2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид), и второе средство представляет собой атипичный нейролептик, особенно рисперидон (3-[2-[4-(6-фтор-1,2-бензоксазол-3-ил)пиперидин-1-ил]этил]-2-метил-6,7,8,9-тетрагидропиридо[2,1-b]пиримидин-4-он) и/или типичный нейролептик, в особенности перфеназин, или фармацевтически приемлемую соль любого из них. В одном варианте, нейролептический компонент комбинированной терапии не является атипичным нейролептиком.
В одном варианте изобретение охватывает способ: (a) лечения шизофрении у человека; (b) замедление прогрессии шизофрении у человека, у которого была диагностирована шизофрения; или (c) профилактика или задержка развития шизофрении у человека, который подвергается риску развития шизофрении, включающий введение человеку эффективного количества комбинированной терапии. В одном варианте способ представляет собой способ облегчения одного или более положительных симптомов шизофрении путем введения человеку эффективного количества комбинированной терапии. В одном варианте способ представляет собой способ облегчения одного или более отрицательных симптомов шизофрении путем введения человеку эффективного количества комбинированной терапии. В одном варианте способ представляет собой способ облегчения одного или более дезорганизованных симптомов шизофрении путем введения человеку эффективного количества комбинированной терапии. В одном варианте способ представляет собой способ облегчения одного или более симптомов шизофрении путем введения человеку эффективного количества комбинированной терапии. В одном варианте способ представляет собой способ облегчения положительного и отрицательного симптома шизофрении путем введения человеку эффективного количества комбинированной терапии. В другом варианте способ представляет собой способ облегчения положительного и дезорганизованного симптома шизофрении. В еще одном варианте способ представляет собой способ облегчения отрицательного и дезорганизованного симптома шизофрении путем введения человеку эффективного количества комбинированной терапии. В одном варианте нейролептик комбинированной терапии вводят в дозе, которая является меньшей, чем требуемое для той же самой нейролептической монотерапии (или двойной терапии, где атипичный нейролептик вводят в комбинации с типичным нейролептиком) получая сопоставимый терапевтический эффект. Также в рамки изобретения входят способы усиления реакции человека на нейролептик, включающие введение первого соединения, такого как димебон, в комбинации с нейролептиком. Изобретение далее включает способы лечения шизофрении путем введения комбинированной терапии, включающей димебон и нейролептик, причем комбинированную терапию вводят в количестве, эффективном для улучшения когнитивного симптома шизофрении. Особенно изобретение охватывает комбинированные терапии, которые приводят к улучшению когнитивных функций у человека. Изобретение охватывает способы, которые усиливают когнитивную способность человека (улучшают познание/запоминание чисел и/или серьезность когнитивных симптомов, связанных с шизофренией) в большей степени, чем использование нейролептика в качестве индивидуальной/монотерапии (и в отсутствие первого соединения, такого как димебон) у тех же самых или подобных пациентов. Изобретение также охватывает фармацевтические композиции для комбинированной терапии, включая их разовые формы. Применительно к любому из описанных здесь вариантов осуществления, такому как любой из способов, описанных здесь, в одном варианте в комбинированной терапии используют нейролептик, который не является атипичным нейролептиком.
ПОДРОБНОЕ ОПИСАНИЕ ИЗОБРЕТЕНИЯ
В рамках настоящего описания, если не указано иное, использование единственного числа подразумевает «один или более».
Ссылка на «приблизительно» относительно величины или параметра включает (и описывает) варианты осуществления, которые направлены на эту величину или параметр per se. Например, описание, относящееся к "приблизительно X" включает описание "X".
В рамках изобретения под "комбинированной терапией" имеется в виду терапия, включающая первое соединение и второе средство, причем первое соединение представляет собой гидрированный пиридо[4,3-b]индол, как описано здесь, и второе средство представляет собой нейролептик, и где первое соединение используется в сочетании со вторым средством. Терапия, включающая димебон, используемый в сочетании с рисперидоном, представляет собой пример комбинированной терапии согласно изобретению. Введение первого соединения "в сочетании со" вторым средством включает введение соединений в составе той же самой или другой композиции, последовательно, одновременно или непрерывно. Введение в сочетании охватывает любое обстоятельство, в котором первое соединение и второе средство вводят человеку в эффективном количестве. Как обсуждается далее, понимается, что первое соединение и второе средство могут вводиться с разной частотой и/или интервалами введения и могут вводиться с использованием одного и того же пути введения или разных путей введения. Например, введение "в сочетании с" включает режим введения, в соответствии с которым первое соединение комбинированной терапии вводится три раза в день, а второе средство комбинированной терапии вводится один раз в день, и причем первая суточная доза первого соединения вводится одновременно со вторым средством, и где вторая и третья суточные дозы первого соединения вводятся индивидуально (в отсутствие второго средства). Далее понимается, что различные режимы введения могут меняться в ходе курса введения. Например, в комбинированной терапии, включающей димебон и рисперидон, димебон может вводиться раз в день, а рисперидон может вводиться раз в неделю или реже чем раз в день. В некоторых вариантах комбинированная терапия в случае необходимости включает один или более фармацевтически приемлемых носителей или эксципиентов, фармацевтически неактивных соединений и/или инертных веществ. Таким образом, соединения в комбинированной терапии по изобретению могут вводиться последовательно, одновременно или непрерывно с использованием одних и тех же или разных путей введения для каждого соединения.
Также понято и ясно следует из настоящего описания, что ссылка на "первое соединение" включает и относится к любому гидрированному пиридо[4,3-b]индолу или его фармацевтически приемлемой соли или другой форме, как описано здесь, такой как соединение димебон.
Также понято и ясно следует из настоящего описания, что ссылка на "второе средство" комбинированной терапии включает и относится к нейролептику или его фармацевтически приемлемой соли. Второе средство может быть атипичным и/или типичным нейролептиком.
В рамках изобретения термин "шизофрения" включает все формы и классификации шизофрении, известные в уровне техники, включая, но не ограничиваясь ими, кататонический тип, гебефренический тип, дезорганизованный тип, параноидальный тип, остаточный тип или недифференцированный тип шизофрении и дефицитного синдрома и/или описанные в American Psychiatric Association: Diagnostic and Statistical Manual of Mental Disorders, Fourth Edition, Washington D.C, 2000 или в Международной Статистической Классификации Заболеваний и Смежных Проблем Здоровья, или иначе известные специалистам.
В рамках изобретения термин "нейролептик" относится к и охватывает атипичный и/или типичный нейролептик. В одном варианте в комбинированной терапии используют атипичный нейролептик. В одном варианте в комбинированной терапии используют типичный нейролептик. В одном варианте в комбинированной терапии использует атипичный нейролептик и типичный нейролептик. В частном варианте в комбинированной терапии используют нейролептик, отличный от атипичного нейролептика (в одном варианте атипичный нейролептик исключается).
В рамках изобретения термин "атипичный нейролептик" обозначает нейролептик, который снижает или исключает активность рецептора 5-HT2A и рецептора D2. В некоторых вариантах осуществления атипичный нейролептик снижает активность рецептора серотонина-2A (5-HT2A) и рецептора допамина-2 (D2) по меньшей мере на или приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 100% по сравнению с соответствующей активностью у того же самого пациента до лечения атипичным нейролептиком или по сравнению с соответствующей активностью у других пациентов, не получающих атипичный нейролептик. В некоторых вариантах осуществления атипичный нейролептик способен к связыванию с активным центром по меньшей мере одного из рецептора 5-HT2A и рецептора D2 (например, сайте связывания лиганда). В некоторых вариантах осуществления атипичный нейролептик способен к связыванию с аллостерическим сайтом по меньшей мере одного из рецептора 5-HT2A и рецептора D2. Взаимодействие между атипичным нейролептиком и рецептором 5-HT2A и рецептором D2 может быть обратимым или необратимым. В некоторых вариантах осуществления атипичный нейролептик уменьшает число или степень моторных побочных эффектов, таких как EPS и поздние дискинезии, по сравнению с типичными нейролептиками, вводимыми тому же самому или другим пациентам в стандартных дозах. Примеры атипичных нейролептиков включают рисперидон (3-[2-[4-(6-фтор-1,2-бензоксазол-3-ил)пиперидин-1-ил]этил]-2-метил-6,7,8,9-тетрагидропиридо[2,1-b]пиримидин-4-он); клозапин (3-хлор-6-(4-метилпиперазин-1-ил)-5H-бензо[c][1,5]бензодиазепин); оланзапин (2-метил-4-(4-метилпиперазин-1-ил)-5H-тиено[3,2-c][1,5]бензодиазепин); кветиапин (2-[2-(4-бензо[b][1,5]бензотиазепин-6-илпиперазин-1-ил)этокси]этанол) и ципразидон (5-[2-[4-(1,2-бензотиазол-3-ил)пиперазин-1-ил]этил]-6-хлор-1,3-дигидроиндол-2-он); оланзапин/флуоксетин (выпускаемый как Symbyax); арипипразол (7-[4-[4-(2,3-дихлорфенил)пиперазин-1-ил]бутокси]-3,4-дигидро-1H-хинолин-2-он; палиперидон (3-[2-[4-(6-фторбензо[d]изоксазол-3-ил)-1-пиперидил]этил]-7-гидрокси-4-метил-1,5-диазабицикло[4.4.0]дека-3,5-диен-2-он); сертиндол (1-[2-[4-[5-хлор-1-(4-фторфенил)-индол-3-ил]-1-пиперидил]этил]имидазолидин-2-он); зотепин (2-((8-хлордибензо(b,f)тиепин-10-ил)окси)-N,N-диметилэтиламин); амисульприд (4-амино-N-[(1-этилпирролидин-2-ил)метил]-5-этилсульфонил-2-метокси-бензамид); бифепрунокс (7-[4-[(3-Фенилфенил)метил]пиперазин-1-ил]-3H-бензоксазол-2-он); и мельперон (1-(4-фторфенил)-4-(4-метил-1-пиперидил)бутан-1-он).
В рамках изобретения термин «типичный нейролептик» обозначает нейролептик, который снижает или исключает прежде всего активность рецептора допамина-2 (D2) обратимым или необратимым образом. В некоторых вариантах осуществления типичный нейролептик снижает активность рецептора D2 по меньшей мере на или приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 100% по сравнению с соответствующей активностью у того же самого пациента до лечения типичным нейролептиком или по сравнению с соответствующей активностью у других пациентов, не получающих типичный нейролептик. В некоторых вариантах осуществления типичный нейролептик способен к связыванию с активным центром рецептора D2 (например, сайтом связывания лиганда). В некоторых вариантах осуществления типичный нейролептик способен к связыванию с аллостерическим сайтом рецептора D2.
В рамках изобретения "лечение" представляет собой подход к получению полезного или желательного результата, включая клинические результаты (например, уменьшение серьезности или продолжительности, стабилизация серьезности или устранение одного или более симптомов (биохимического, гистологического и/или поведенческого) шизофрении). В целях этого изобретения полезные или желательные результаты включают, но не ограничены ими, облегчение симптомов, связанных с шизофренией, уменьшение степени проявления симптомов, связанных с шизофренией, предотвращение ухудшения симптомов, связанных с шизофренией, включая положительные и/или отрицательные и/или дезорганизованные симптомы. Лечение охватывает повышение качества жизни людей, которые страдают шизофренией, снижение дозы других лекарственных средств, необходимых для лечения шизофрении, задержку прогрессии шизофрении и/или продление выживания пациентов, страдающих шизофренией. Предпочтительно, лечение комбинированной терапией, раскрытой здесь, не вызывает или вызывает меньше побочных эффектов, чем обычно связано с введением нейролептических лекарственных средств, таких как экстрапирамидальные побочные эффекты (EPS), острая дистония, острая дискинезия и поздняя дискинезия. В одном варианте лечение комбинированной терапией по изобретению уменьшает или устраняет число или степень когнитивных симптомов шизофрении (облегчает когнитивную дисфункцию) в большей степени, чем терапии, которые не включают введение первого соединения, такого как димебон (например, по сравнению с теми же самыми или подобными пациентами, которые следуют нейролептической индивидуальной/монотерапии или двойной терапии, где атипичный нейролептик вводят в сочетании с типичным нейролептиком или где вводят два или более атипичных или типичных нейролептика).
В описании, если не указано иное, "лицо" в рамках изобретения обозначает млекопитающее, включая, но не ограничиваясь им, человека. Лицо может быть человеком, у которого была диагностирована или подозревается, или имеется риск ее развития, шизофрения. Лицо может быть человеком, который демонстрирует один или более симптомов, связанных с шизофренией. Лицо может быть человеком, который в силу наследственности или по иным причинам предрасположен к развитию шизофрении.
В рамках изобретения, если не указано иное, комбинированная терапия может вводиться пациенту в любой доступной лекарственной форме. Первое соединение и второе средство комбинированной терапии может вводиться в одних и тех же или разных лекарственных формах, и изобретение включает эти различные лекарственные формы. В одном варианте первое соединение или второе средство, или как первое соединение, так и второе средство комбинированной терапии вводят пациенту как обычную лекарственную форму немедленного высвобождения. В одном варианте первое соединение или второе средство, или как первое соединение, так и второе средство комбинированной терапии вводят пациенту в форме замедленного высвобождения или как часть системы замедленного высвобождения, такой как система, способная поддерживать скорость высвобождения соединения в организм пациента в течение желаемого периода, который может быть иметь увеличенную продолжительностью, такую как продолжительность, превышающая время, требуемое для высвобождения соответствующей лекарственной формой непосредственного высвобождения того же самого количества (например, в весовом или молярном выражении) соединения, и может составлять часы или дни. Желаемая продолжительность может составлять по меньшей мере период полувыведения вводимого соединения и может быть равна, например, по меньшей мере приблизительно 6 часам или по меньшей мере приблизительно 12 часам, или по меньшей мере приблизительно 24 часам, или по меньшей мере приблизительно 30 часам, или по меньшей мере приблизительно 48 часам, или по меньшей мере приблизительно 72 часам, или по меньшей мере приблизительно 96 часам, или по меньшей мере приблизительно 120 часам, или по меньшей мере приблизительно 144 или более часам, и может быть равна по меньшей мере приблизительно одной недели, по меньшей мере приблизительно 2 неделям, по меньшей мере приблизительно 3 неделям, по меньшей мере приблизительно 4 неделям, по меньшей мере приблизительно 8 неделям или по меньшей мере приблизительно 16 неделям или более.
Термин "эффективное количество" обозначает такое количество соединения (например, компонента комбинированной терапии по изобретению) или комбинированной терапии, которое в комбинации с его(ее) параметрами эффективности и токсичности, а так же на основании знаний практикующего специалиста должно быть эффективным в данной терапевтической форме. Как понимают в уровне техники, эффективное количество может находиться в одной или более дозах, то есть, для достижения желаемого результата лечения может понадобиться единственная доза или множество доз. В некоторых вариантах осуществления эффективное количество соединения или комбинированной терапии представляет собой количество, достаточное, чтобы снизить активность рецептора 5HT2A и рецептора D2, например, привести к снижению этих активностей по меньшей мере на или приблизительно на 10%, 20%, 30%, 40%, 50%, 60%, 70%, 80%, 90%, 95% или 100% по сравнению с соответствующей активностью у того же самого пациента до лечения или по сравнению с соответствующей активностью у других пациентов, не получающих комбинированную терапию. Для измерения величины этого эффекта могут использоваться стандартные методы, такие как анализ in vitro с очищенным ферментом, клеточный тест, модели животных или исследование на человеке. Эффективное количество комбинированной терапии включает количество первого соединения и количества второго средства, которые при последовательном, одновременном или непрерывном введении производят желаемый результат.
В различных вариантах осуществления лечение комбинированной терапией может привести к аддитивному или даже синергическому (например, превышающему аддитивный) результату по сравнению с индивидуальным введением первого соединения или второго средства. В некоторых вариантах осуществления как часть комбинированной терапии используется более низкое количество каждого из первого соединения и второго средства, по сравнению с количеством каждого компонента, обычно используемым для индивидуальной (некомбинированной) терапии. Предпочтительно, при использовании комбинированной терапии получают тот же самый или больший терапевтический эффект, чем при использовании любого индивидуального соединения (компонентов комбинации) по отдельности. В некоторых вариантах осуществления тот же самый или больший терапевтический эффект получают, используя меньшее количество (например, более низкую дозу или менее частое введение) фармацевтически активного соединения в комбинированной терапии, чем количество, обычно используемое для индивидуальной терапии. Предпочтительно, использование меньшего количества нейролептика приводит к сокращению числа, серьезности, частоты или продолжительности одного или более побочных эффектов, связанных с этим соединением. Подходящие дозы любого из соединений, которые вводят в сочетании друг с другом как часть комбинированной терапии, могут в случае необходимости быть уменьшены вследствие совместного действия (например, аддитивные или синергические эффекты) соединений.
Термин "одновременное введение" в рамках изобретения, означает, что первое соединение и второе средство в комбинированной терапии вводят с разделением по времени не больше, чем приблизительно 15 минут, например, не больше, чем приблизительно 10, 5 или 1 минуту. Когда соединения вводят одновременно, первое соединение и второе средство могут содержаться в одной и той же композиции (например, композиции, включающей как гидрированный пиридо[4,3-b]индол, такой как димебон, так и нейролептик, такой как атипичный нейролептик рисперидон и/или типичный нейролептик, такой как перфеназин) или в отдельных композициях (например, гидрированный пиридо[4,3-b]индол, такой как димебон, содержится в одной композиции, а нейролептик, такой как атипичный нейролептик рисперидон, содержится в другой композиции).
В рамках изобретения термин "последовательное введение" означает, что первое соединение и второе средство в комбинированной терапии вводят с разделением по времени более чем приблизительно 15 минут, например, более чем приблизительно 20, 30, 40, 50, 60 или более минут. Сначала может быть введено или первое соединение, или второе средство. Первое соединение и второе средство для последовательного введения содержатся в отдельных композициях, которые могут содержаться в одной и той же или разных упаковках или наборах.
Соединение/компонент комбинированной терапии может быть составлено с подходящими носителями для любого доступного пути доставки, будь то в форме немедленного высвобождения или в форме замедленного высвобождения, включая пероральный, через слизистую оболочку (например, назальный, подъязычный, влагалищный, щечный или ректальный), парентеральный (например, внутримышечный, подкожный или внутривенный), топический или чрескожный путь доставки. Соединение может быть составлено с подходящими носителями для получения форм доставки, которые могут быть, но не обязательно, формами замедленного высвобождения, которые включают, но не ограничены ими: таблетки, каплетки, капсулы (такие как твердые желатиновые капсулы и мягкие эластичные желатиновые капсулы), облатки, пастилки, лепешки, жевательные резинки, дисперсии, суппозитории, мази, катаплазмы (припарки), пасты, порошки, перевязочные материалы, кремы, растворы, пластыри, аэрозоли (например, спреи и ингаляции для носа), гели, суспензии (например, водные или неводные жидкие суспензии, эмульсии типа "масло в воде" или жидкие эмульсии типа «вода в масле»), растворы и эликсиры. Первое соединение и второе средство комбинированной терапии могут быть составлены с подходящими носителями для одних и тех же или разных путей введения и могут быть составлены для одновременного введения через один и тот же путь введения.
Первое соединение и второе средство комбинированной терапии могут использоваться отдельно или вместе в получении состава, такого как фармацевтический состав, путем комбинации соединения или соединений в качестве активных ингредиентов с фармакологически приемлемым носителем, которые известны в уровне техники. В зависимости от терапевтической формы системы (например, чрескожный пластырь или пероральная таблетка), носитель может быть в различных формах. Кроме того, фармацевтические препараты могут содержать консерванты, солюбилизаторы, стабилизаторы, смачивающие вещества, эмульгаторы, подсластители, красители, регуляторы, соли для регулирования осмотического давления, буферы, агенты покрытия или антиоксиданты. Препараты, содержащие активный ингредиент, могут также содержать другие вещества, которые имеют ценные терапевтические свойства. Терапевтические формы могут быть представлены обычной стандартной дозой и могут быть получены известным фармацевтическим способом. Подходящие составы могут быть найдены, например, в Remington's Pharmaceutical Sciences, Mack Publishing Company, Philadelphia, PA, 20th ed. (2000), который включен в настоящее описание путем ссылки.
Количество соединения/компонента комбинированной терапии в форме доставки может быть любым эффективным количеством. В одном варианте комбинированная терапия включает первое соединение (такое как димебон) в лекарственной форме в количестве от приблизительно 10 нг до приблизительно 1500 мг или более. В одном варианте комбинированная терапия включает второе средство в лекарственной форме в количестве от приблизительно 10 нг до приблизительно 1500 мг или более. В одном варианте комбинированная терапия включает димебон как первое соединение в форме для доставки, такой как система замедленного высвобождения, в количестве, которое составляет меньше чем приблизительно 30 мг димебона. В одном варианте комбинированная терапия включает димебон как первое соединение в форме для доставки, такой как отдельная система замедленного высвобождения, пригодная для введения димебона в течение нескольких дней, где эта форма включает такое количество димебона, что суточная доза димебона составляет меньше чем приблизительно 30 мг.
Режим лечения, включающий лекарственную форму первого соединения и/или второго средства комбинированной терапии, будь то в форме немедленного высвобождения или в виде системы замедленного высвобождения, может включать введение первого соединения и/или второго средства пациенту в дозе от приблизительно 0,1 до приблизительно 10 мг/кг массы тела, по меньшей мере один раз в день и в течение промежутка времени, необходимого для достижения терапевтического эффекта. В других вариантах суточная доза (или другая частота введения) первого соединения и/или второго средства составляет от приблизительно 0,1 до приблизительно 8 мг/кг; или от приблизительно 0,1 до приблизительно 6 мг/кг; или от приблизительно 0,1 до приблизительно 4 мг/кг; или от приблизительно 0,1 до приблизительно 2 мг/кг; или от приблизительно 0,1 до приблизительно 1 мг/кг; или от приблизительно 0,5 до приблизительно 10 мг/кг; или от приблизительно 1 до приблизительно 10 мг/кг; или от приблизительно 2 до приблизительно 10 мг/кг; или от приблизительно 4 до приблизительно 10 мг/кг; или от приблизительно 6 до приблизительно 10 мг/кг; или от приблизительно 8 до приблизительно 10 мг/кг; или от приблизительно 0,1 до приблизительно 5 мг/кг; или от приблизительно 0,1 до приблизительно 4 мг/кг; или от приблизительно 0,5 до приблизительно 5 мг/кг; или от приблизительно 1 до приблизительно 5 мг/кг; или от приблизительно 1 до приблизительно 4 мг/кг; или от приблизительно 2 до приблизительно 4 мг/кг; или от приблизительно 1 до приблизительно 3 мг/кг; или от приблизительно 1,5 до приблизительно 3 мг/кг; или от приблизительно 2 до приблизительно 3 мг/кг; или от приблизительно 0,01 до приблизительно 10 мг/кг; или приблизительно от 0,01 до 4 мг/кг; или приблизительно от 0,01 мг/кг до 2 мг/кг; или приблизительно от 0,05 до 10 мг/кг; или приблизительно от 0,05 до 8 мг/кг; или приблизительно от 0,05 до 4 мг/кг; или приблизительно от 0,05 до 4 мг/кг; или от приблизительно 0,05 до приблизительно 3 мг/кг; или от приблизительно 10 кг до приблизительно 50 кг; или от приблизительно 10 до приблизительно 100 мг/кг или от приблизительно 10 до приблизительно 250 мг/кг; или от приблизительно 50 до приблизительно 100 мг/кг или приблизительно от 50 до 200 мг/кг; или от приблизительно 100 до приблизительно 200 мг/кг или от приблизительно 200 до приблизительно 500 мг/кг; или более приблизительно 100 мг/кг; или более приблизительно 500 мг/кг. В некоторых вариантах осуществления вводят такую суточную дозу димебона в качестве первого соединения комбинированной терапии, как суточная доза димебона меньше чем приблизительно 0,1 мг/кг, которая может включать, но не ограничена ими, суточную дозу приблизительно 0,05 мг/кг. В одном варианте суточная доза (по весу) первого соединения (такого как димебон) приблизительно в 10 раз превышает суточную дозу (по весу) второго средства. Например, в одном варианте комбинированная терапия включает введение димебона в суточной дозе приблизительно 60 мг и рисперидона в суточной дозе приблизительно 6 мг.
Комбинированная терапия может вводиться пациенту в соответствии с эффективным режимом введения в течение желаемого периода или промежутка времени, такого как по меньшей мере приблизительно один месяц, по меньшей мере приблизительно 2 месяца, по меньшей мере приблизительно 3 месяца, по меньшей мере приблизительно 6 месяцев или по меньшей мере приблизительно 12 месяцев или дольше. В одном варианте комбинированная терапия вводится по ежедневной или нечеткой схеме в течение жизни пациента.
Частота введения первого соединения и/или второго средства в комбинированной терапии может составлять один раз в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может составлять один раз в день. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть больше чем один раз в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть меньше чем три раза в день. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть меньше чем приблизительно три раза в день. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть приблизительно три раза в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть приблизительно четыре раза в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть приблизительно два раза в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть больше чем один раз в неделю, но меньше чем приблизительно один раз в день. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть приблизительно один раз в месяц. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть приблизительно два раза в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть больше чем приблизительно один раз в месяц, но меньше чем приблизительно один раз в неделю. Частота введения первого соединения и/или второго средства в комбинированной терапии может быть вариативной (например, один раз в день в течение 7 дней, затем без введения в течение 7 дней, с повтором цикла каждые 14 дней, например, в течение приблизительно 2 месяцев, приблизительно 4 месяцев, приблизительно 6 месяцев или больше). Частота введения первого соединения и/или второго средства в комбинированной терапии может быть постоянной (например, один раз в неделю в течение многих недель). При любой из частот введения может использоваться любое из соединений, описанных здесь, вместе с любой из доз, описанных здесь, например, частота введения первого соединения в комбинированной терапии может быть ежедневной в дозе менее чем 0,1 мг/кг или менее чем приблизительно 0,05 мг/кг димебона. В одном варианте введение первого соединения осуществляют три раза в день, а введение второго средства - один раз в день. В частном варианте комбинированная терапия включает введение димебона три раза в день (например, приблизительно 20 мг 3 раза в день) и введение рисперидона один раз в день (например, приблизительно 6 мг один раз в день).
Способы Лечения Шизофрении
Гидрированные пиридо[4,3-b]индолы и нейролептики, описанные здесь, могут использоваться в комбинированной терапии для лечения и/или профилактики и/или задержки начала и/или развития шизофрении. Как показано в Примере 1, представитель гидрированных пиридо[4,3-b]индолов димебон способен уменьшать блокирующий эффект МК-801 на NMDA-индуцированные токи в культивируемых нейронах гиппокампа крысы. Примеры способов определения способности гидрированных пиридо[4,3-b]индолов лечить и/или предотвращать и/или задерживать начало и/или развития шизофрении описаны в Примерах 2 и 3. Продолжающееся клиническое исследование, включающее комбинированную терапию, описано в Примере 4.
Было неожиданно обнаружено, что димебон, хотя и является блокатором рецептора NMDA, может также снижать блокирующую активность МК-801 на рецепторах NMDA. Поскольку было обнаружено, что фенциклидин и МК-801 действуют в соответствии с одним и тем же механизмом, конкурируя за тот же самый сегмент внутри канала рецептора NMDA, следует ожидать, что первые соединения, описанные здесь, такие как димебон, будут снижать блокирующий эффект фенциклидина на рецепторе NMDA точно таким же способом. Так как психотомиметические свойства фенциклидина являются следствием его способности стабильно связываться с определенным сегментом в ионном канале рецептора NMDA и блокировать ионные токи, проходящие через его ионный канал, ослабление этого блокирующего эффекта соединениями, описанными здесь, такими как соединения Формулы (1), (2), (A) или (B), должно привести к уменьшению психотомиметических свойств фенциклидина.
Атипичные и типичные нейролептики нашли использование в лечении шизофрении. Например, рисперидон представляет собой атипичный нейролептик, который был одобрен в Соединенных Штатах для лечения шизофрении. Рисперидон доступен в форме таблеток в дозах в пределах от 0,25 мг до 4 мг, перорального раствора, например, в дозе 1 мг/мл, и в форме расщепляемых таблеток, например, в дозах в пределах от 0,5 до 4 мг. Однако, использование атипичных нейролептиков не лишено побочных эффектов, таких как потенциальное развитие поздней дискинезии и экстрапирамидальных симптомов (ESP). Некоторые атипичные нейролептики, также могут иметь ограниченное использование в некоторых группах пациентов.
Комбинированные терапии, которые включают первое соединение и второе средство, где первое соединение представляет собой гидрированный пиридо[4,3-b]индол, особенно соединение димебон, и второе средство представляет собой нейролептик, могут иметь увеличенную активность в отношении лечения, профилактики и/или задержки начала и/или развития шизофрении. В частности комбинированные терапии по изобретению включают гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль в сочетании с нейролептиком, полезным для лечения, профилактики и/или задержки начала и/или развития шизофрении. Способы, в которых используют такие комбинированные терапии, могут привести к аддитивному или даже синергическому (например, превышающему аддитивный) результату по сравнению с индивидуальным введением любого соединения комбинированной терапии.
В одном варианте комбинированная терапия, включающая первое соединение и второе средство, требует более низких доз индивидуальных соединений, чем было бы необходимо, если бы индивидуальные соединения вводили индивидуально. Эта сниженная дозировка может уменьшить побочные эффекты, связанные с терапиями, и в лучшей степени привести к согласию со стороны пациента, что является очень желательным для популяции пациентов с шизофренией. Таким образом, в некоторых вариантах осуществления используется более низкое количество каждого фармацевтически активного соединения как часть комбинированной терапии по сравнению с количеством, обычно используемым для индивидуальной терапии. В некоторых вариантах осуществления такой же или больший терапевтический эффект достигается при использовании меньшего количества (например, более низкая доза или менее частое введение) фармацевтически активного соединения в комбинированной терапии, чем количество, обычно используемое для индивидуальной терапии. Предпочтительно, использование малого количества фармацевтически активного соединения приводит к сокращению числа, серьезности, частоты или продолжительности одного или более побочных эффектов, связанных с соединением.
Таким образом, настоящее изобретение относится к различным способам, в которых используют комбинированную терапию, таким как описанные в "Кратком Описании Изобретения" и в других местах настоящего описания. Например, в одном варианте осуществления настоящее изобретение относится к способу лечения шизофрении у пациента, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу задержки начала и/или развития шизофрении у пациента, для которого установлен риск развития шизофрении (например, пациента, один или более членов семьи которого имели шизофрению, или пациента, у которого была диагностирована генетическая мутация, связанная с шизофренией, или пациента, который демонстрирует поведение, характерное для начала шизофрении), включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу задержки начала и/или развития шизофрении у пациента, который генетически предрасположен к развитию шизофрении, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу задержки начала и/или развития шизофрении у пациента, имеющего мутантный или аномальный ген, связанный с шизофренией (такой как ген NRG1 или DTNBP1), но у которого не была диагностирована шизофрения, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу профилактики шизофрении у пациента, который генетически предрасположен к развитию шизофрении или который имеет мутантный или аномальный ген, связанный с шизофренией, но у которого не была диагностирована шизофрения, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу предотвращения начала и/или развития шизофрении у пациента, который не идентифицирован как генетически предрасположенный к развитию шизофрении, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу уменьшения интенсивности или серьезности симптомов шизофрении у пациента, у которого диагностирована шизофрения, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте осуществления настоящее изобретение относится к способу улучшения качества жизни пациента, у которого диагностирована шизофрения, включающему введение пациенту эффективного количества комбинированной терапии, включающей гидрированный пиридо[4,3-b]индол или его фармацевтически приемлемую соль (такую как димебон) и нейролептик. В одном варианте способ включает получение лекарственного средства для комбинированной терапии для использования в любом из описанных способов, например, лечения и/или профилактики и/или задержки начала или развития шизофрении. В одном варианте в способах по изобретению используют комбинированную терапию, в которой нейролептик отличается от атипичного нейролептика.
Таким образом, изобретение относится к способам лечения шизофрении, включающим введение гидрированного пиридо[4,3-b]индола или его фармацевтически приемлемой соли (такого как димебон) и нейролептика (такого как рисперидон и/или перфеназин), в которых пациент имеет (или у него подозревается ее наличие) шизофрению. Способы введения нейролептика, такого как рисперидон и/или перфеназин, известны в уровне техники. Уменьшение дозы нейролептика (что уменьшает зависимость от введения этих лекарственных средств и в действительности задерживает введение этих лекарственных средств), может быть оценено, например, путем сравнения с известными и/или установленными средними дозами (в отношении количества и/или интервалов) которые известны в уровне техники.
В другом аспекте изобретение относится к способам усиления лечения шизофрении нейролептиком, включающим введение эффективного количества гидрированного пиридо[4,3-b]индола или его фармацевтически приемлемой соли (такого как димебон) в сочетании с нейролептиком. Усиление лечения может быть установлено путем оценки известных параметров и/или индикаторов (таких как число и/или серьезность симптомов и/или клинические и/или психометрические и/или нейрокогнитивные и/или биологических маркеры или оценки) у пациента, который получает комбинированную терапию, по сравнению с теми же самыми параметрами и/или индикаторами у тех же самых или подобных пациентах, которые получают нейролептическую монотерапию или которые не получают комбинированной терапии, включающей первое соединение, как описано здесь.
Гидрированные пиридо[4,3-b]индолы для Использования в Способах, Составах, Наборах и Изобретениях, Раскрытых Здесь
Когда дается ссылка на органические остатки или группы, имеющие определенное число атомов углерода, если не указано иное, она относится ко всем геометрическим и другим изомерам. Например, "бутил" включает н-бутил, втор.-бутил, изобутил и трет.-бутил; "пропил" включает н-пропил и изопропил.
Термин "алкил" включает линейные, разветвленные или циклические углеводородные структуры и их комбинации. Предпочтительными алкильными группами являются такие, которые имеют 20 атомов углерода (C20) или меньше. Более предпочтительными алкильными группами являются такие, которые имеют меньше чем 15 или меньше чем 10 или меньше чем 8 атомов углерода.
Термин "низший алкил" относится к алкильным группам, содержащим от 1 до 5 атомов углерода. Примеры низших алкилов включают метил, этил, пропил, изопропил, бутил, втор.- и трет.-бутил и т.п. Низший алкил представляет собой субпопуляцию алкила.
Термин "арил" или ("Ar") относится к ненасыщенной ароматической карбоциклической группе, содержащей от 6 до 14 атомов углерода, имеющей единственное кольцо (например, фенил) или множество конденсированных колец (например, нафтил или антрил), которые могут быть или не быть ароматическими (например, 2-бензоксазолинон, 2H-1,4-бензоксаин-3(4H)-он-7-ил) и т.п. Предпочтительные арилы включают фенил и нафтил.
Термин "гетероарил" относится к ароматической карбоциклической группе, содержащей в кольце от 2 до 10 атомов углерода и от 1 до 4 гетероатомов, выбранных из кислорода, азота и серы. Такие гетероарильные группы могут иметь единственное кольцо (например, пиридил или фурил) или множество конденсированных колец (например, индолизинил или бензотиенил). Примеры гетероарильных остатков включают, например, имидазолил, пиридинил, индолил, тиофенил, тиазолил, фуранил, бензимидазолил, хинолинил, изохинолинил, пиримидинил, пиразинил, тетразолил и пиразолил.
Термин "аралкил" относится к остатку, в котором арильная группа присоединена к материнской структуре через алкильный остаток. Примерами являются бензил, фенетил и т.п.
Термин "гетероаралкил" относится к остатку, в котором гетероарильная группа присоединена к материнской структуре через алкильный остаток. Примеры включают фуранилметил, пиридинилметил, пиримидинилэтил и т.п.
Термин "замещенный гетероаралкил" относится к гетероарильным группам, которые замещены заместителями числом от 1 до 3, таким как остатки, выбранные из группы, состоящей из гидрокси, алкил, алкокси, алкенила, алкинила, амино, арила, карбоксила, галогена, нитро и амино.
Термин "гало" или "галоген" относится к фтору, хлору, брому и йоду.
Гидрированные пиридо[4,3-b]индолы или их фармацевтически приемлемые соли, такие как из соли с кислотой или основанием, являются первым соединением комбинированной терапии, содержащей гидрированный пиридо[4,3-b]индол и нейролептик. Гидрированный пиридо[4,3-b]индол может быть тетрагидро пиридо[4,3-b]индолом или его фармацевтически приемлемой солью. Гидрированный пиридо[4,3-b]индол может также быть гексагидро пиридо[4,3-b]индолом или его фармацевтически приемлемой солью. Гидрированные пиридо[4,3-b]индолы могут быть замещены 1 - 3 заместителями, хотя могут рассматриваться также незамещенные гидрированные пиридо[4,3-b]индолы или гидрированные пиридо[4,3-b]индолы с больше чем 3 заместителями. Подходящие заместители включают, но не ограничены ими, алкил, низший алкил, аралкил, гетероаралкил, замещенный гетероаралкил и галоген.
Частные примеры гидрированных пиридо[4,3-b]индолов иллюстрируются Формулами A и B:
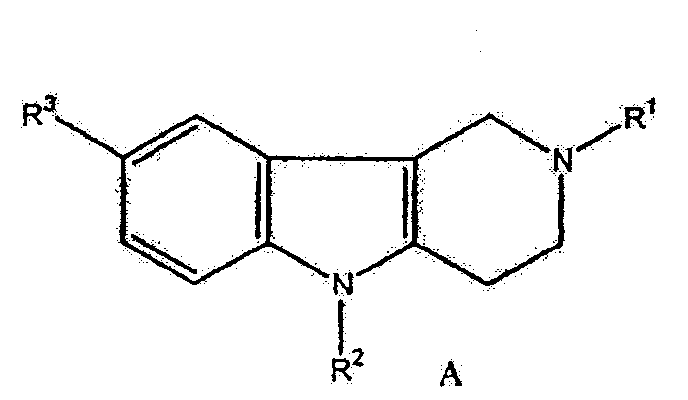 или
или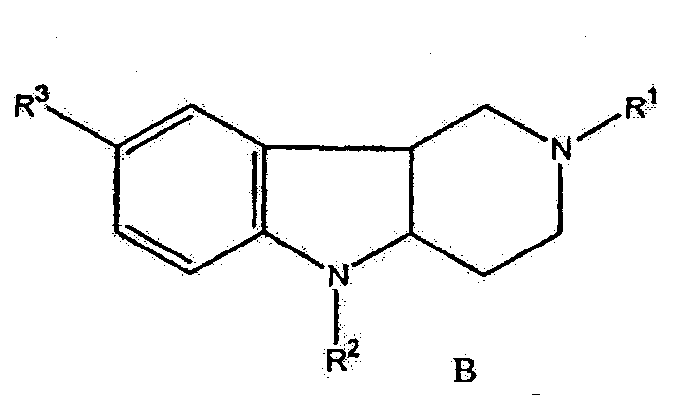
где R1 выбран из группы, состоящей из алкила, низшего алкила и аралкила, R2 выбран из группы, состоящей из водорода, аралкила и замещенного гетероаралкила; и R3 выбран из группы, состоящей из водорода, алкила, низшего алкила и галогена.
В одном варианте R1 обозначает алкил, такой как алкил, выбранный из группы, состоящей из C1-C15алкила, C10-C15алкила, C1-C10алкила, C2-C15алкила, C2-C10алкила, C2-C8алкила, C4-C8алкила, C6-C8алкила, C6-C15алкила, C15-C20алкила; C1-C8алкила и C1-C6алкила. В одном варианте R1 обозначает аралкил. В одном варианте R1 обозначает низший алкил, такой как низший алкил, выбранный из группы, состоящей из C1-C2алкила, C1-C4алкила, C1-C15алкила, C2-C4алкила, C1-C5алкила и C2-C5алкила.
В одном варианте R1 обозначает алкильную группу с прямой цепью. В одном варианте R1 обозначает разветвленную алкильную группу. В одном варианте R1 обозначает циклическую алкильную группу.
В одном варианте R1 обозначает метил. В одном варианте R1 обозначает этил. В одном варианте R1 обозначает метил или этил. В одном варианте R1 обозначает метил или аралкил, такой как бензил. В одном варианте R1 обозначает этил или аралкил, такой как бензил.
В одном варианте R1 обозначает аралкил. В одном варианте R1 обозначает аралкил, где любой из алкильных или низших алкильных заместителей, перечисленных в предыдущих параграфах, дополнительно замещен арилом (например, Ar-C1-C6алкил, Аr-C1-C3алкил или Ar-C1-C15алкил). В одном варианте R1 обозначает аралкил, где любой из алкильных или низших алкильных заместителей, перечисленных в предыдущих параграфах, замещен единственным кольцевым арильным остатком. В одном варианте R1 обозначает аралкил, где любой из алкильных или низших алкильных заместителей, перечисленных в предыдущих параграфах, дополнительно замещен фенилом (например, Ph-C1-C6алкил или Ph-C1-C3алкил, Ph-C1-C15алкил). В одном варианте R1 обозначает бензил.
Все варианты для R1 могут комбинироваться с любым из вариантов, заявленных ниже для R2 и R3, как если бы каждая комбинация R1, R2 и R3 была специфически и индивидуально перечислена.
В одном варианте R2 обозначает Н. В одном варианте R2 обозначает аралкил. В одном варианте R2 обозначает замещенную гетероаралкильную группу. В одном варианте R2 обозначает водород или аралкил. В одном варианте R2 обозначает водород или замещенную гетероаралкильную группу. В одном варианте R2 обозначает аралкильную группу или замещенную гетероаралкильную группу. В одном варианте R2 выбран из группы, состоящей из водорода, аралкильной группы и замещенной гетероаралкильной группы.
В одном варианте R2 обозначает аралкил, где R2 может быть любой из аралкильных групп, отмеченных выше для R1, как если бы каждый вариант аралкила, перечисленный для R1, был отдельно и индивидуально перечислен для R2.
В одном варианте R2 обозначает замещенную гетероаралкильную группу, где алкильная часть гетероаралкила может быть любым алкилом или низшим алкилом, таким как упомянутые выше для R1. В одном варианте R2 обозначает замещенный гетероаралкил, где гетероарил замещен 1-3 C1-C3алкильными заместителями (например, 6-метил-3-пиридилэтил). В одном варианте R2 обозначает замещенную гетероаралкильную группу, причем гетероарил замещен 1-3 метильными группами. В одном варианте R2 обозначает замещенную гетероаралкильную группу, причем гетероарил замещен одним низшим алкильным заместителем. В одном варианте R2 обозначает замещенную гетероаралкильную группу, причем гетероарил замещен одним C1-C3 алкильным заместителем. В одном варианте R2 обозначает замещенную гетероаралкильную группу, причем гетероарил замещен одной или двумя метильными группами. В одном варианте R2 обозначает замещенную гетероаралкильную группу, причем гетероарил замещен одной метильной группой.
В других вариантах R2 обозначает любую из замещенных гетероаралкильных групп, указанных в предыдущем параграфе, где гетероарильная часть гетероаралкильной группы является единственной кольцевой гетероарильной группой. В других вариантах R2 обозначает любую из замещенных гетероаралкильных групп, указанных в предыдущем параграфе, где гетероарильная часть гетероаралкильной группы является множественной конденсированной кольцевой гетероарильной группой. В других вариантах R2 обозначает любую из замещенных гетероаралкильных групп, указанных в предыдущем параграфе, где гетероаралкильная часть представляет собой пиридил (Py).
В одном варианте R2 обозначает 6-CH3-3-Py-(CH2)2-.
В одном варианте R3 обозначает водород. В других вариантах R3 обозначает любую из алкильных групп, отмеченных выше для R1, как если бы каждый вариант алкила, перечисленный для R1, был отдельно и индивидуально перечислен для R3. В другом варианте R3 обозначает галоген. В одном варианте R3 обозначает водород или алкил. В одном варианте R3 обозначает галоген или алкил. В одном варианте R3 обозначает водород или галоген. В одном варианте R3 выбран из группы, состоящей из водорода, алкила и галогена. В одном варианте R3 обозначает Br. В одном варианте R3 обозначает I. В одном варианте R3 обозначает F. В одном варианте R3 обозначает Cl.
В частном варианте гидрированный пиридо[4,3-b]индол представляет собой 2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол или его фармацевтически приемлемую соль.
Гидрированные пиридо[4,3-b]индолы могут быть в форме фармацевтически приемлемых солей, которые известны специалистам. Фармацевтически приемлемые соли включают фармацевтически приемлемые соли с кислотой. Примеры фармацевтически приемлемых солей включают гидрохлориды или дигидрохлориды. В частном варианте гидрированный пиридо[4,3-b]индол представляет собой фармацевтически приемлемую соль 2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола, такую как 2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид (димебон).
Частные представители гидрированных пиридо-([4,3-b])индолов могут также быть описаны Формулой (1) или Формулой (2):
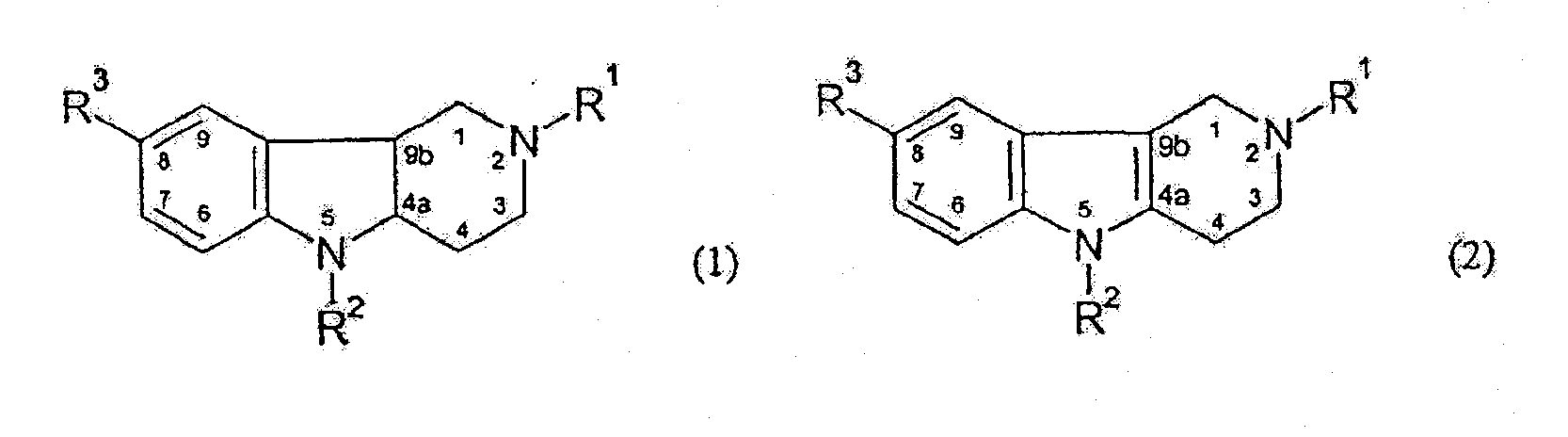
Для соединений общей Формулы (1) или (2),
R1 обозначает -CH3, CH3CH2- или PhCH2-(бензил);
R2 обозначает -H, PhCH2- или 6-CH3-3-Py-(CH2)2-;
R3 обозначает -H, -CH3 или -Br,
с любой комбинацией вышеупомянутых заместителей. Все возможные комбинации заместителей Формул (1) и (2) рассматриваются как определенные и индивидуальные соединения, как если бы каждое отдельное и индивидуальное соединение было перечислено под химическим названием. Также рассматриваются соединения Формулы (1) или (2), из которых удалены одна или более возможных групп из упомянутых выше групп заместителей: например, где R1 обозначает -CH3; R2 обозначает -H, PhCH2- или 6-CH3-3-Py-(CH2)2-; и R3 обозначает -H, -CH3 или -Br, или где R1 обозначает -CH3; R2 обозначает 6-CH3-3-Py-(CH2)2-; и R3 обозначает -H, -CH3 или -Br.
Вышеупомянутое и любое соединение могут быть в форме солей с фармацевтически приемлемыми кислотами и в форме кватернизованных производных.
Соединение может быть соединением Формулы (1), где R1 обозначает -CH3, R2 обозначает -H и R3 обозначает -CH3. В одном варианте соединение имеет Формулу (1), при условии, что заместители отличаются от случая, где R1 обозначает -CH3, R2 обозначает -H и R3 обозначает -CH3. Соединение может быть соединением Формулы (2), где R1 обозначает -CH3, CH3CH2- или PhCH2-; R2 обозначает -H, PhCH2- или 6-CH3-3-Py-(CH2)2-; R3 обозначает -H, -CH3 или -Br. Соединение может быть соединением Формулы (2), где R1 обозначает CH3CH2- или PhCH2-, R2 обозначает -H и R3 обозначает -H; или соединением, где R1 обозначает -CH3, R2 обозначает PhCH2-, R3 обозначает -CH3; или соединением, где R1 обозначает -CH3, R2 обозначает 6-CH3-3-Py-(CH2)2-, и R3 обозначает -CH3; или соединением, где R1 обозначает -CH3, R2 обозначает -H, R3 обозначает -H или -CH3; или соединением, где R1 обозначает -CH3, R2 обозначает -H, R3 обозначает -Br.
Соединения, известные из литературы, которые могут использоваться в способах, раскрытых здесь, включают следующие соединения:
1. цис(±) 2,8-диметил-2,3,4,4a,5,9b-гексагидро-1H-пиридо[4,3-b]индол и его дигидрохлорид;
2. 2-этил-2,3,4,5-тетрагидро-1Н-пиридо[4,3-b]индол;
3. 2-бензил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол;
4. 2,8-диметил-5-бензил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол и его дигидрохлорид;
5. 2-метил-5-(2-метил-3-пиридил)этил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол и его сесквисульфат;
6. 2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол и его дигидрохлорид (димебон);
7. 2-метил-2,3,4,5-тетрагидро-1Н-пиридо[4,3-b]индол;
8. 2,8-диметил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол и его метилйодид;
9. 2-метил-8-бром-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол и его гидрохлорид.
В одном варианте соединение является соединением Формулы A или B, и R1 выбран из низшего алкила или бензила; R2 выбран из водорода, бензила или 6-CH3-3-Py-(CH2)2-, и R3 выбран из водорода, низшего алкила или галогена, или любой его фармацевтически приемлемой солью. В другом варианте R1 выбран из -CH3, CH3CH2- или бензила; R2 выбран из -H, бензила, или 6-CH3-3-Py-(CH2)2-; и R3 выбран из -H, -CH3 или -Br, или любая его фармацевтически приемлемая соль. В другом варианте соединение выбрано из группы, состоящей из: цис(±) 2,8-диметил-2,3,4,4a,5,9b-гексагидро-1H-пиридо[4,3-b]индола в форме рацемической смеси или в в основном чистой (+) или в основном чистой (-) форме; 2-этил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; 2-бензил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; 2,8-диметил-5-бензил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; 2-метил-5-(2-метил-3-пиридил)этил-2,3,4,5-тетрагидро-1Н-пиридо[4,3-b]индола; 2,8-диметил-5-(2-(6-метил-3-пиридил)этил)-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; 2-метил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; 2,8-диметил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола; или 2-метил-8-бром-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индола или любой фармацевтически приемлемой соли любого из этих соединений. В одном варианте соединение является соединением Формулы A или B, в которых R1 обозначает -CH3, R2 обозначает -H и R3 обозначает -CH3, или любой его фармацевтически приемлемой солью. Соединение может иметь Формулу A или B, где R1 обозначает CH3CH2- или бензил, R2 обозначает -H, и R3 обозначает -CH3 или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R1 обозначает -CH3, R2 обозначает бензил и R3 обозначает -CH3 или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R1 обозначает -CH3, R2 обозначает 6-CH3-3-Py-(CH2)2- и R3 обозначает -H, или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R2 обозначает 6-CH3-3-Py-(CH2)2-, или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R1 обозначает -CH3, R2 обозначает -Н и R3 обозначает -H или -CH3, или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R1 обозначает -CH3, R2 обозначает -Н и R3 обозначает -Br, или представлять собой любую его фармацевтически приемлемую соль. Соединение может иметь Формулу A или B, где R1 выбран из низшего алкила или аралкила, R2 выбран из водорода, аралкила или замещенного гетероаралкила и R3 выбран из водорода, низшего алкила или галогена.
Соединение для использования в композициях, наборах и способах может представлять собой 2,8-диметил-5-(2-(6-метил-3-пиридил)этил-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол или любую его фармацевтически приемлемую соль, такую как кислая соль, гидрохлорид или дигидрохлорид.
Любое из раскрытых здесь соединений, имеющих два стереоцентра в кольцевой структуре пиридо[4,3-b]индола (например, углерод 4a и 9b соединения (I)) включает соединения, стереоцентры которых находятся в цис или транс форме. Композиция может включать такое соединение в основном чистой форме, такой как композиция в основном чистого S,S или R,R или S,R или R,S соединения. Композиция в основном чистого соединения означает, что композиция содержит не больше, чем 15% или не больше, чем 10%, или не больше, чем 5%, или не больше, чем 3%, или не больше, чем 1% примеси соединения в другой стереохимической форме. Например, композиция в основном чистого S,S соединения означает, что композиция содержит не больше, чем 15% или не больше, чем 10%, или не больше, чем 5%, или не больше, чем 3%, или не больше, чем 1% R,R или S,R или R,S формы соединения. Композиция может содержать соединение как смеси таких стереоизомеров, где смесь может быть смесью энантиомеров (например, S,S и R,R) или диастереомеров (например, S,S и R,S или S,R) в равных или неравных количествах. Композиция может содержать соединение как смесь 2 или 3 или 4 таких стереоизомеров в любом отношении стереоизомеров. Соединения, раскрытые здесь, имеющие стереоцентры помимо таковых в кольцевой структуре пиридо[4,3-b]индола, включают все стереохимические варианты таких соединений, включая, но не ограничиваясь ими, энантиомеры и диастереомеры в любом отношении, и включают рацемические и энантиомерно обогащенный и другие возможные смеси. Если стереохимия явно не обозначена в структуре, структура охватывает все возможные стереоизомеры изображенного соединения.
Синтез и исследования нейролептических свойств для цис(±) 2,8-диметил-2,3,4,4a,5,9b-гексагидро-1H-пиридо[4,3-b]индола и его дигидрохлорида описаны, например, в следующей публикации: Yakhontov, L.N., Glushkov, R.G., Synthetic therapeutic drugs. A.G. Natradze, the editor, Moscow Medicina, 1983, p. 234-237. Синтез соединений 2, 8 и 9, отмеченных выше как известные из литературы, и данных относительно их свойств как антагонистов серотонина описаны, например, в C.J. Cattanach, A. Cohen & B.H. Brown in J. Chem. Soc. (Ser.C) 1968, p. 1235-1243. Синтез соединения 3, отмеченного выше как известное из литературы, описан, например, в статье N.P.Buu-Hoi, O.Roussel, P.Jacquignon, J. Chem. Soc, 1964, N 2, p. 708-711. N.F. Kucherova and N.K. Kochetkov (General chemistry (russ.), 1956, v. 26, p. 3149-3154), описывают синтез соединения 4, отмеченного выше как известное из литературы. Синтез соединений 5 и 6, отмеченных выше как известные из литературы, описан в статье A.N. Kost, M.A. Yurovskaya, T.V. Mel'nikova, Chemistry of heterocyclic compounds, 1973, N 2, p. 207-212. Синтез соединения 7, отмеченного выше как известное из литературы, описан U,Horlein in Chem. Ber., 1954, Bd. 87, hft 4,463-p. 472. M.Yurovskaya and LL. Rodionov в Chemistry of heterocyclic compounds (1981, N 8, p. 1072-1078), описывают синтез метилйодида соединения 8.
Первое соединение и вторые средства комбинированной терапии могут быть скомбинированы с фармацевтически приемлемым носителем, и фармацевтические композиции, включающие комбинированную терапию, входят в рамки изобретения.
Изобретение также охватывает комбинированные лекарственные формы для терапии, где первое соединение и второе средство комбинированной терапии присутствуют в виде лекарственной формы. В рамках изобретения, термин "лекарственная форма" относится к составу для комбинированной терапии, который содержит определенную дозу первого соединения (такого как димебон) и определенную дозу второго средства (такого как рисперидон). Первое соединение и вторые средства комбинированной лекарственной формы для терапии присутствуют в количествах, эффективных для лечения шизофрении.
Изобретение далее относится к наборам, включающим комбинированную терапию, как описано здесь. Наборы могут содержать первое соединение и вторые средства комбинированной терапии в виде лекарственной формы (например, лекарственная форма содержит и димебон, и нейролептик, такой как рисперидон и/или перфеназин) или как отдельные лекарственные формы (например, димебон содержится в одной лекарственной форме, а нейролептик, такой как рисперидон и/или перфеназин, содержится в другой лекарственной форме). Наборы также содержат инструкции по использованию. В одном варианте в наборе используются димебон и рисперидон. Наборы могут использоваться для любого одного или более применений, описанных здесь, и, соответственно, могут содержать инструкции в отношении любого одного или более заявленных применений (например, лечения и/или профилактики и/или задержки начала и/или развития шизофрении).
Наборы обычно включают подходящую упаковку. Наборы могут включать один или более контейнеров, содержащих любое соединение или комбинированную терапию, описанную здесь. Каждый компонент (если имеется более одного компонента), может быть упакован в отдельные контейнеры, или некоторые компоненты могут быть объединены в одном контейнере, если перекрестная реактивность и срок годности это позволяют.
Наборы могут включать ряд инструкций, обычно письменных инструкций, хотя электронные носители данных (например, магнитная дискета или оптический диск), содержащие инструкции, также приемлемы, относительно использования компонента(ов) в способе согласно настоящему изобретению (например, лечения, профилактики и/или задержки начала и/или развития шизофрении. Инструкции, включенные в набор, обычно содержат информацию относительно компонентов и их введения пациенту.
Следующие Примеры представлены для иллюстрации, но не ограничения изобретения.
Все ссылки, приведенные здесь, полностью включены в настоящее описание путем ссылки.
ПРИМЕРЫ
Пример 1. Способ оценки свойств соединений в отношении блокировки NMDA-индуцированного тока
Лекарственное средство "димебон", 2,8-диметил-5-[2-(6-метилпиридил-3)этил]-2,3,4,5-тетрагидро-1H-пиридо[4,3-b]индол дигидрохлорид Формулы:
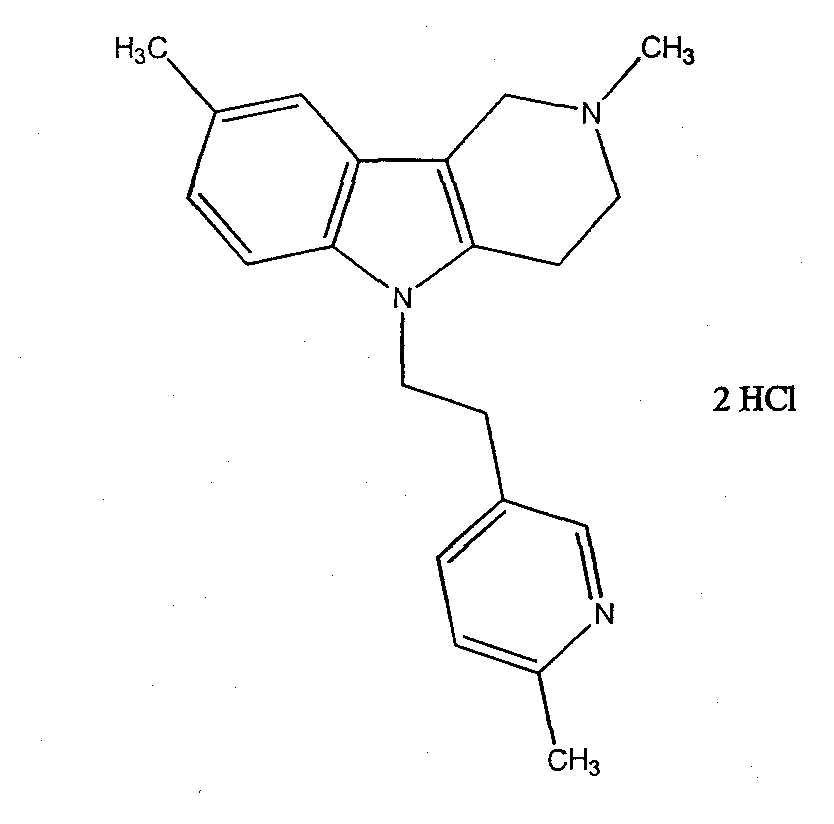
был использован как представитель описанных здесь соединений.
Эксперименты были выполнены способом фиксации потенциала на свежеизолированных нейронах коры головного мозга крысы или на культивируемых нейронах гиппокампа крысы. Нейроны для культивирования были получены из гиппокампа новорожденных крыс (1-2 дня) способом трипсинизации с последующим пипетированием. Клетки, суспендированные в культуральной среде, были помещены в количестве 3 мл в лунки планшета с 6 лунками (Nunc) или в Чашки Петри, в которые были сначала помещены стекла, покрытые поли-L-лизином. Концентрация клеток как правило составляла 2,5 Ч 10-6 - 5 Ч 10-6 клеток/мл. Культуральная среда состояла из минимальной среды Игла и среды DME/F12 (1:1), дополненной 10%-ой телячьей сывороткой, глутамином (2 мM), гентамицином (50 мкг/мл), глюкозой (15 мM) и 20 мM KCl, с рН, доведенным до 7-7,4 с использованием NaHCO3. Планшеты, содержащие культуры, были помещены в CO2-инкубатор при 37°C и 100%-ой влажности. На второй-третий день культивирования добавляли 10-20 мкл цитозинарабинозида. Через 6-7 дней культивирования к среде добавляли1 мг/мл глюкозы или среду заменяли, в зависимости от следующего эксперимента. Культивируемые нейроны гиппокампа были помещены в рабочую камеру объемом 0,4 мл. Рабочий раствор имел следующий состав (мМ): NaCl 150,0, KCl 5,0, CaCl2 2,6, MgSO4 Ч 7H2O 2,0, HEPES 10,0, глюкоза 15,0, рН 7,36.
Трансмембранные токи, продуцируемые нанесением NMDA, были измерены электрофизиологическим способом фиксации потенциала в полноклеточной конфигурации. Нанесение веществ осуществляли способом быстрого суперслияния. Токи были измерены при помощи боросиликатных микроэлектродов (сопротивление 3,0-4,5 мОм), заполненных следующей композицией (мМ): KCl 100,0, EGTA 11,0, CaCl2 1,0, MgC12 1,0, HEPES 10,0, АТФ 5,0, pH 7,2. Для регистрации использовали инструмент EPC-9 (HEKA, Германия). Токи регистрировали на жестком диске ПК Pentium IV, используя импульсную программу, также приобретенную у HEKA. Результаты были проанализированы при помощи программы Pulsefit (HEKA).
Нанесение NMDA вызвало входящие токи в культивируемых нейронах гиппокампа. Димебон оказывал блокирующий эффект на токи, вызванные нанесением NMDA. IC50 димебона варьировала от 6,0 до 10 мкМ и составляла среднее 7,7 ± 1,9 мкМ. МК-801 также вызвал блокаду NMDA-индуцированных токов. Эта блокада имела ясную "зависимость использования", другими словами величина эффекта блокирования, вызванного МК-801, зависела от предыдущего эффекта агониста, то есть, NMDA: эффект блокирования увеличивается в серии последовательных нанесений агониста до некоторой конечной величины, которая зависит от концентрации МК-801. 1 мкМ МК-801 приводит к блокаде NMDA-индуцированных токов на 70 ± 15%. Предварительная перфузия нейронов с раствором, содержащим димебон в концентрации 10 мкМ вызвала уменьшение эффекта блокирования МК-801 до 40 ± 18%. Для сравнения был исследован эффект конкурентного антагониста рецептора NMDA D-AP5 (D-2-амино-5-фосфоновалериановая кислота - селективный антагонист рецептора NMDA). D-AP5 непосредственно в дозе 5 мкМ блокировал NMDA-индуцированные токи на 60-80%. Предварительное нанесение D-AP5 не снижало блокирующий эффект МК-801.
Результаты, которые были получены, приведены в Таблице 1.
|
Результаты показывают, что димебон, несмотря на то, что он, как полагают, сам является антагонистом рецепторов NMDA, способен уменьшать блокирующий эффект МК-801 на NMDA-индуцированные токи в культивируемых нейронах гиппокампа крысы. Хотя механизм блокирующего эффекта димебона на рецепторы NMDA еще не установлен, он не имеет нейротоксичного эффекта, который является характерным для неконкурентных блокаторов ионных каналов рецептора NMDA - фенциклидина, МК-801 и кетамина. На основании этих новых результатов можно предположить, что сокращение блокирующего канал эффекта МК-801 (и аналогично фенциклидина) на рецепторах NMDA может привести к уменьшению их психотомиметического эффекта и, поэтому, к устранению симптомов, характерных для шизофрении.
Эти результаты показывают, что димебон, наряду с его ранее описанными свойствами, может использоваться для эффективного лечения шизофрении.
Пример 2. Использование модели in vivo для определения способности соединений по изобретению лечить, предотвращать и/или задерживать начало и/или развитие шизофрении
In vivo модели шизофрении могут использоваться для определения способности любого из гидрированных пиридо[4,3-b]индолов, описанных здесь (например, димебона) лечить и/или предотвращать и/или задерживать начало и/или развитие шизофрении.
В одной модели для проверки активности одного или более гидрированных пиридо[4,3-b]индолов, описанных здесь, лечить и/или предотвращать и/или задерживать начало и/или развитие шизофрении используют фенциклидин, который долгое время вводят животному (например, не являющемуся приматом (крыса) или примату (обезьяна)), что приводит к дисфункциям, подобным наблюдаемым у людей с шизофренией. См. Jentsch et al., 1997, Science 277:953-955 and Piercey et al., 1988, Life Sei. 43(4):375-385). В этой или в других моделях животных могут использоваться стандартные экспериментальные протоколы.
Пример 3. Использование клинических испытаний на людях для определения способности соединений по изобретению лечить, предотвращать и/или задерживать начало и/или развитие шизофрении
Если желательно, любой из гидрированных пиридо[4,3-b]индолов, описанных здесь (например, димебон) могут также быть проверены на людях, чтобы определить способность соединения лечить, предотвращать и/или задерживать начало и/или развитие шизофрении. Для этих клинических испытаний могут использоваться стандартные методы.
В одном примере способа пациентов с шизофренией регистрируют в исследовании фазы I в отношении толерантности, фармакокинетики и фармакодинамики гидрированного пиридо[4,3-b]индола, используя стандартные протоколы. Затем проводят фазу II, двойное слепое рандомизированное контролируемое испытание, чтобы определить эффективность гидрированного пиридо[4,3-b]индола.
Пример 4. Использование клинических испытаний на людях для определения способность комбинированных терапий по изобретению лечить, предотвращать и/или задерживать начало и/или развитие шизофрении
В настоящее время проводится клиническое психофармакологическое исследование для оценки клинических и нейрокогнитивных характеристик и динамики биологических маркеров в течение времени, на фоне переключения пациентов с лекарственных средств первого поколения на второе поколение атипичных нейролептических средств и с добавлением димебона. В этом исследовании оценивают эффект переключения пациентов с хронической шизофренией с традиционной терапии на монотерапию с рисполептом (блокатор серотонина-допамина) в соответствии с клиническими индикаторами, результаты нейрокогнитивных тестов, нейрохимические, нейроиммунологические, биохимические, генетические и морфологические маркеры. Рисполепт - другой термин для обозначения рисперидона, также продающегося в Соединенных Штатах под маркой Risperdal, и обозначает соединение 3-[2-[4-(6-фтор-1,2-бензоксазол-3-ил)пиперидин-1-ил]этил]-2-метил-6,7,8,9-тетрагидропиридо[2,1-b]пиримидин-4-он. В исследовании также оценивают возможное увеличение клинического эффекта нейролептической терапии, когда к монотерапии с блокатором серотонина-допамина добавляют лекарственное средство димебон, который имеет глутаматную активность.
Исследование включает 60 пациентов с диагнозом непрерывной параноидальной и эпизодической-прогрессивной шизофрении с текущим состоянием лекарственной ремиссии или с развитием лекарственной ремиссии, безотносительно синдрома, определяющего текущий психический статус. Таким образом, исследование не включает пациентов, которые являются полностью резистентными к психотропной терапии. Согласно DSM-IV, эти пациенты отвечают критериям 295.30, шизофрения, параноидальный тип, хроническое течение.
На первой стадии исследования пациенты, которые дают согласие на основе полной информации на участие в исследовании и которые отвечают критериям включения/исключения, переключаются на монотерапию с атипичным нейролептиком (рисполепт), и клиническую стабильность пациентов оценивают на протяжении более двух недель. На второй стадии пациенты, которые оказываются восприимчивыми (отвечающими) к новому лечению, продолжают терапию в фиксированных дозах (приблизительно 6 мг рисполепта, один раз в день), а те, кто оказался нечувствителен к новому лечению (неотвечающие), исключаются из программы и переводятся на обычную терапию. На третьей стадии, после 4 недель монотерапии с атипичным нейролептиком, пациентов разделяют на две группы на основе рандомизации 1:1 и им вводят противоаллергическое лекарственное средство с гипотетической глутаматной нейропротективной активностью (димебон, приблизительно 20 мг три раза в день) или плацебо в дополнение к основной нейролептической терапии. Третья стадия длится 8 недель. На четвертой стадии (дополнительный период), спустя 6 месяцев после завершения терапии в рамках описанного протокола, оценивают стабильность характеристик, достигнутых в ходе исследования.
|
Исследование проводят, выбирая пациентов согласно следующим критериям включения/исключения: 1. мужчины, возраст от 18 до 65 лет; 2. пациенты, которые дали согласие на основе полной информации, на участие в исследовании; 3. пациент отвечает критериям DSM-IV 295.30 шизофрения, параноидальный тип, хроническое течение; 4. психическое состояние соответствует категории лекарственной ремиссии или развития лекарственной ремиссии, безотносительно синдрома, определяющего текущий психический статус; 5. Показатели PANSS для "дезорганизации мышления", "подозрительности", "галлюцинаторного поведения", "возбуждения" не должны превышать "4"; 6. клинические симптомы острого психотического возбуждения не должны присутствовать - CGI - психотическое возбуждение не должно превышать "умеренного"; 7. пациент не демонстрирует симптомов полной резистентности к нейролептической терапии (отсутствие положительной динамики в двух курсах нейролептической терапии с различными нейролептиками); и 8. психотическое состояние не является следствием органического заболевания мозга.
В исследовании используют способы, детализированные ниже.
1. Клинический/психопатологический (описательный) способ используется при каждом посещении.
2. Психометрический способ используется в конце первого периода, в конце второго периода, через 4 недели третьего периода и в конце третьего периода.
• Шкала PANSS
• Шкала Калгари для оценки депрессии во время шизофрении
CGI-S
CGI-I
Исследование Отрицательных Симптомов-16 (NSA-16)
AIMS
BARS
SARS
3. Способы нейрокогнитивного функционирования используются в конце второго периода, через 4 недели третьего периода и в конце третьего периода. Некоторых пациентов оценивают, используя следующее:
ШКАЛА ПАМЯТИ WECHSLER_ПОДТЕСТ V: ПРЯМОЕ И ОБРАТНОЕ ВОСПРОИЗВЕДЕНИЕ ЛИНИЙ ШИФРА
ШКАЛА ПАМЯТИ WECHSLER_ПОДТЕСТ IV: ЛОГИЧЕСКАЯ ПАМЯТЬ (ЧАСТЬ ОДИН, ЧАСТЬ ДВА.)
ТЕСТ WECHSLER, ПОДТЕСТ VII: ЗАШИФРОВЫВАНИЕ
ШКАЛА ПАМЯТИ WECHSLER_ПОДТЕСТ VII: ВОСПРОИЗВЕДЕНИЕ ПАРНЫХ АССОЦИАЦИЙ
ВИЗУАЛЬНЫЙ ТЕСТ НАМЕРЕНИЯ БЕНТОНА
ЛОНДОНСКИЙ ТАУЭР
ТЕСТ STROOP
ТАБЛИЦЫ SHULTE
ЗАДАЧА НА ПОСТОЯННОЕ ВНИМАНИЕ
ТЕСТ WISKONSIN НА СОРТИРОВКУ КАРТ
МОДИФИЦИРОВАННЫЙ ТЕСТ BOURDOHN
4. Контроль биологических маркеров. Могут быть оценены следующие маркеры:
• Нейрохимические характеристики:
• Белок, подобный глютаминсинтетазе
• Цитохром C оксидаза
• Нейроморфология:
• Исследования ультраструктуры лимфоцитов и моноцитов
• Нейроиммунология:
• Цитокины реакции воспаления (IL-1 бета, IL-2, IF гамма, фактор некроза опухоли)
• Клиническая генетика
• Полиморфные изменения генов нейротрофического фактора мозга
• Полиморфные варианты генов рецептора серотонина типа 2a
• Лаборатория молекулярной биохимии
• Активность эластазы лейкоцитов
• активность ингибитора протеиназы a-1
• Содержание C-реактивного белка
• Уровень антител к нейроантигенам - факторам роста нервов и основного белка миелина
• Клиническая лаборатория биохимии
• Уровень тромбоцитарного серотонина
• Адгезия тромбоцитов на колонке и пик времени задержки тромбоцитов
• Определение периода полужизни инфузории Tetrahymena piriformis при инкубации с сывороткой крови от пациентов ("полная токсичность крови")
• Основные параметры пероксидирования липидов в крови пациентов
Хотя изобретение было описано выше в подробностях посредством иллюстрации и примера для ясности понимания, специалисту очевидно, что могут быть осуществлены некоторые незначительные изменения и модификации. Поэтому описание и примеры не должны рассматриваться как ограничение объема изобретения.
Все приведенные ссылки, публикации, патенты и заявки на патент тем самым полностью включены в настоящее описание путем ссылки.

