КОНСОРЦИУМ БИФИДОБАКТЕРИЙ И ЛАКТОБАЦИЛЛ, ИСПОЛЬЗУЕМЫЙ ДЛЯ ПРИГОТОВЛЕНИЯ БАКТЕРИЙНЫХ ПРЕПАРАТОВ И БИОЛОГИЧЕСКИ АКТИВНЫХ ДОБАВОК К ПИЩЕ, ПРЕДНАЗНАЧЕННЫХ ДЛЯ КОРРЕКЦИИ МИКРОФЛОРЫ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ДЕТЕЙ В ВОЗРАСТЕ ДО 3-Х ЛЕТ, И СПОСОБ ЕГО ПОЛУЧЕНИЯ, БИОЛОГИЧЕСКИ АКТИВНАЯ ДОБАВКА К ПИЩЕ И БАКТЕРИАЛЬНЫЙ ПРЕПАРАТ ДЛЯ ЛЕЧЕНИЯ ДИСБИОТИЧЕСКИХ СОСТОЯНИЙ ЖЕЛУДОЧНО-КИШЕЧНОГО ТРАКТА ДЕТЕЙ В ВОЗРАСТЕ ДО 3-Х ЛЕТ
Вид РИД
Изобретение
Изобретение относится к медицине и биотехнологии и может быть использовано для приготовления лечебно-профилактических средств пробиотической направленности, предназначенных для коррекции дисбиотических нарушений микрофлоры желудочно-кишечного тракта и поддержания ее колонизационной резистентности у детей в возрасте от рождения до 3-х лет. Средства для профилактики и лечения конструируются преимущественно на основе двух групп микроорганизмов - бифидобактерий и лактобацилл. Бифидобактерий являются наиболее значимыми представителями микрофлоры человеческого организма - как по удельному весу в составе микробиоценоза, так и по их многофункциональной роли в поддержании гомеостаза организма. У детей на грудном вскармливании они составляют практически 100% микрофлоры толстой кишки. Бифидобактерий оказывают положительное воздействие на становление систем пищеварения, иммунитета, кроветворения ребенка [1, 2, 3]. Бифидобактерий обеспечивают колонизационную резистентность в отношении патогенных и условно-патогенных микроорганизмов; обладают иммуномодулирующим действием; синтезируют аминокислоты, витамины, летучие жирные кислоты, ферменты, участвующие в процессах пищеварения и обмена веществ; способствуют усвоению железа, кальция, поддержанию водно-солевого баланса [4, 5]. Частичная или полная элиминация бифидобактерий приводит к угнетению иммунных сил организма, развитию дисбиоза.
Многофакторное позитивное воздействие на организм ребенка позволяет рассматривать бифидобактерий как эффективный биокорректор и основу для создания препаратов, обладающих регулирующим и стимулирующим воздействием на организм.
В России традиционным подходом к бактериотерапии является назначение больным препаратов на основе культур штаммов бифидобактерий с доказанным пробиотическим действием преимущественно в виде монокультур штаммов Bifidobacterium bifidum 1, В. bifidum 791, B.bifidum ЛВА-3, B.longum В379М, B.adolescentis MC-42. Это, прежде всего, широко применяющийся лечебный препарат "Бифидумбактерин" [6].
При этом следует отметить, что в микробиоценозе кишечника человека бифидобактерий представлены одновременно многими видами - как отдельными, так и в ассоциациях [7]. Это позволяет предположить, что введение в состав пробиотических препаратов сразу нескольких видов бифидобактерий будет способствовать повышению их лечебной и профилактической эффективности.
Подобный подход предлагается в Российском патенте [8], касающемся консорциума на основе 9 штаммов бифидобактерий B.bifidum 791, B.bifidum ЛВА-3, B.longum В379М, B.longum Я-3, В.breve 79-119, В.breve 79-88, B.infantis 73-15, B.infantis 79-43, B.adolescentis Г7513.
Вместе с тем, указанный консорциум не учитывает, что рациональный подход к конструированию и применению новых средств коррекции микрофлоры должен основываться на таком явлении, как аутогенная сукцессия - последовательность смены биоценозов в определенной экологической нише [9, 10]. В ходе этого процесса в видовом сообществе происходит последовательное вытеснение одних видов другими вследствие их биоэкологических преимуществ в определенных условиях. При этом образуется так называемый сукцессионный ряд с образованием конечного -устойчивого биоценоза. Все биоценозы в живой природе развиваются по законам сукцессии. Что касается микроэкологии человеческого организма, данная закономерность прослеживается в смене видового состава бифидофлоры в процессе онтогенеза, совпадающей с критическими периодами развития в детском и подростковом возрасте: становлением иммунной и ферментативной систем, изменением гормонального фона, сменой пищевого рациона. В то же время, видовой состав бифидофлоры взрослых людей относительно стабилен [11, 12].
Таким образом, препараты должны представлять собой ассоциации доминирующих микроорганизмов, которые максимально приближены по составу к естественному микробиоценозу желудочно-кишечного тракта человека в определенный возрастной период. Это является обоснованным подходом, обеспечивающим индивидуализацию бактериотерапии и повышение ее эффективности, способствуя устойчивой локализации или новому заселению биотопа теми видами бифидобактерий, которые преобладают в микробиоценозе конкретного человека.
Помимо бифидобактерий, в биопрепаратах-пробиотиках широко используются лактобациллы. Эти микроорганизмы обладают высокой антагонистической активностью против широкого спектра патогенных и условно-патогенных микробов, стимулируют неспецифическую резистентность организма человека, обладают выраженным воздействием на ферментативную систему. Обладая бета-галактозидазной активностью, нивелируют лактазную недостаточность, которая особенно часто встречается у детей первого года жизни. Применение метода совместного культивирования требует анализа межштаммовых взаимодействий микроорганизмов в условиях in vitro [13]. Пригодными для совместного культивирования считают биосовместимые штаммы, т.е. штаммы, взаимоотношения которых расцениваются как симбиоз.
Совместное культивирование двух и более видов лактобацилл повышает их технологичность и расширяет спектр функциональной активности.
Проведенные эксперименты по изучению биосовместимости различных штаммов, позволили выделить группу лактобацилл, наиболее перспективных в отношении совместного культивирования. Наибольший интерес из этой группы лактобактерий представляют штаммы L. helveticus К3ш24, L. helveticus NK-1 и L.casei KHM-I2. Они обладают выраженным антагонизмом по отношению к условно-патогенным микроорганизмам и устойчивостью к спектру антибактериальных средств. Кроме того, установлена высокая степень биосовместимости этих штаммов, что определило целесообразность их совместного культивирования.
Известен Патент РФ №2180915 [14]. В данном патенте предлагается консорциум бифидобактерий и лактобацилл следующего состава: Bifidobacterium bifidum 1, B.bifidum 791, B.breve 79-88, B.breve 79-119, В.infantis 79-43, В. infantis 75-13, L. plantarum 8-PA-3, L.fermentum 90-TC-4. Характеризуя Патент РФ [14], следует отметить, что недостатком способа получения консорциума, заявленного в нем, является то, что консорциум получают путем объединения инокулятов культур отдельных штаммов бифидобактерий в равных долях, совместным культивированием в питательной среде в течение 10-12 часов в ферментере или 18-20 часов в стационарных условиях при темперуре 37-38° и последующим добавлением к нему культур лактобацилл в соотношении 10:1.
В настоящее время для изучения таксономии представителей микробиоты, в том числе бифидобактерий и лактобацилл, разработаны и широко применяются различные молекулярно-генетические методы, включая секвенирование, мультилокусное генотипирование и другие, что существенно пополнило наши представления о видовом многообразии этих бактерий, позволило реклассифицировать известные и выявить новые виды [15, 16]. Это тесным образом связано с разработкой новых пробиотических препаратов, обладающих иммуномодулирующим действием, широким набором свойств, определяющих метаболическую и антагонистическую активность.
Так, изучение вышеперечисленных штаммов молекулярно-генетическими методами показало несоответствие в видовой принадлежности некоторых штаммов, идентифицированных ранее с помощью биохимических тестов. Так, штамм L.fermentum 90-ТС-4 показал себя, как L.plantarum. Штамм B.bifidum 1, широко используемый в производстве пробиотиков, оказался природным рекомбинантом, состоящим из двух клонов: B.bifidum и B.breve. Данная информация говорит о необходимости новых подходов к конструированию мультипробиотических препаратов.
Изучение видового состава бифидофлоры детей в возрасте до 3 лет на основе амплификации и секвенирования фрагментов двух генов: 16S рибосомальной РНК (16S) и трансальдолазы (tal) показало, что виды B.infantis и B.breve, которые ранее считались постоянными обитателями желудочно-кишечного тракта ребенка, в численном отношении уступают такому виду, как B.pseudocatenulatum (10% и 17%) [17]. Вид B.bifidum остается преобладающим в микробиоценозе ребенка. Постоянно и в высоком процентном соотношении к другим видам в последние годы присутствует вид B.longum [18]. Вместе с тем, вид B.pseudocatenulatum, по мнению ряда авторов [19], ассоциируется с атопической экземой у детей. Это касается также вида B.animalis [20]. Reiter [21] причисляет их к подвидам B.adolescentis, который нехарактерен для микробиоценоза детей. Такие виды нефизиологичны для детей и не могут быть использованы в составе средств коррекции микрофлоры данной возрастной группы.
Представленные данные убедительно показывают, что для эффективной коррекции дисбиотических нарушений микробиоценоза детей данной возрастной группы в состав препарата должны входить штаммы с доказанным пробиотическим эффектом и в видовом отношении комплементарных бифидофлоре детей до 3-х лет. Важное значение имеет включение в состав средств коррекции микрофлоры штаммов, выделенных от современных детей.
Это относится к всесторонне изученным и запатентованным штаммам бифидобактерий, выделенным от здоровых детей на грудном вскармливании: штамм В. breve OV-12 [22], штамм В. bifidum OV-19 [23]. Штамм В. breve OV-12 обладает более высокой антагонистической активностью к патогенным и условно-патогенным микроорганизмам, чем штамм В. breve 79-88. Патент РФ №2373274 на штамм В. breve OV-12 отмечен дипломом, как вошедший в 100 лучших изобретений 2011 года под №39.
Штамм В. bifidum 0V-19, помимо, помимо пробиотических свойств, обладает устойчивым генотипом, в отличие от штамма В.Bifidum1.
Задачей настоящего изобретения является создание консорциума бифидобактерий и лактобацилл, по составу максимально приближенного к микробиоценозу детей в возрасте до 3-х лет, а также разработкой способа его получения, учитывающего биосовместимость штаммов в процессе культивирования и при дальнейшем хранении.
Техническим результатом настоящего изобретения является тот факт, что заявляемый консорциум является высокотехнологичным, накапливает биомассу на питательных средах в короткие сроки с высокой концентрацией пробиотических микроорганизмов, обладает кислотообразующими и антагонистическими свойствами в отношении патогенной и условно-патогенной микрофлоры. Синергидный эффект совместного использования штаммов в консорциуме проявляется в повышении всех перечисленных свойств по сравнению с отдельными штаммами.
Консорциум бифидобактерий и лактобацилл для препаратов и БАД, предназначенный для для детей в возрасте до 3-х лет
1. Bifidobacterium bifidum OV-19 - ГКНМ МНИИЭМ им. Г.Н.Габричевского
№216, выделен из содержимого кишечника здорового ребенка, RU 2375444.
2. Bifidobacterium B.bifidum 791 - ВНИИгенетика в ЦМГТМ №В-3300, ГКНМ МНИИЭМ им. Г.Н.Габричевского №80, выделен из содержимого кишечника здорового ребенка.
3. Bifidobacterium longum В379М - ВНИИгенетика в ЦМПМ №В-2000, ГКНМ МНИИЭМ им. Г.Н.Габричевского №79, выделен из содержимого кишечника здорового человека.
4. Bifidobacterium breve OV-12 - ГКНМ МНИИЭМ им. Г.Н.Габричевского №217, выделен из содержимого кишечника здорового ребенка, RU 2373274.
5. Bifidobacterium infantis 73-15 - ГКНМ МНИИЭМ им. Г.Н.Габричевского №155, выделен из содержимого кишечника здорового ребенка, RU 2112034.
6. Lactobacillus helveticus К3ш24 - выделен из содержимого кишечника здорового человека, ВНИИгенетика №ЦМПМ В-3190, ГКНМ МНИИЭМ им. Г.Н.Габричевского №42.
7. Lactobacillus helveticus NK-1 - выделен из содержимого кишечника здорового человека ВНИМИ ЦЛМ №22/10, ГКНМ МНИИЭМ им. Г.Н.Габричевского №54,
8. Lactobacillus casei КНМ-12 - ГКНМ МНИИЭМ им. Г.Н.Габричевского №12, выделен из молочного продукта.
Задачей настоящего изобретения является также разработка определенной схемы совместного культивирования отдельных культур для получения консорциума.
Техническим результатом предлагаемой схемы культивирования отдельных штаммов для получения консорциума является отсутствие взаимного ингибирования штаммов и расширение спектра ферментативной и антагонистической активности.
Способ получения консорциума основан на предварительном изучении и подборе для совместного культивирования штаммов по принципу биосовместимости и с учетом кинетики роста каждого из них.
Алгоритмом к созданию консорциума бифидобактерий и лактобацилл является совместное культивирование определенных штаммов с учетом длительности экспоненциальной фазы роста каждого из них и численного соотношения в микробиоценоза кишечника бифидобактерий и лактобацилл, на основании чего определяется временная точка засева питательной среды при поэтапном внесении инокулятов монокультур.
По оптическому стандарту мутности устанавливают концентрацию ОЕ/мл, соответствующую 1 млрд клеток бифидобактерий. Лактобациллы, являясь микроаэрофиллами, поглощая остаточный кислород из среды, создают благоприятные условия для развития бифидобактерий. По оптическому стандарту мутности устанавливают концентрацию ОЕ/мл, соответствующую 1 млрд клеток. При подборе дозы инокулята необходимо учитывать также соотношение бифидобактерий и лактобацилл в микробиоценозе человека (100:1) и более высокую кинетику роста лактобацилл.
Посев каждой из культур бифидобактерий в ферментер, по 2% к объему среды культивирования, проводят поэтапно, с периодичностью в 30 минут, коррегируя рН культуральной жидкости 20% NaOH перед засевом нового штамма до 6,8. При засеве лактобацилл % инокулята составляет 0,1%; рН среды перед засевом должен быть более кислым - 6,0.
Очередность внесения инокулята для получения данного консорциума является следующей:
1) Bifidobacterium infantis 73-15 - 2%;
2) Bifidobacterium bifidum 791 - 2%;
3) Bifidobacterium breve OV-2 - 2%;
4) 5) Bifidobacterium bifidum OV-19 - 2%;
6) Bifidobacterium longum B379M - 2%;
7) L.casei KHM-12-0,1%;
8) L. helveticus К3ш24 - 0,1%
9) L.helveticus NK-1 - 0,1%.
Консорциум культивируют при 37°C при периодическом перемешивании в течение 8-10 часов; рН культуральной жидкости после окончания процесса составляет 3,9-4,3.
Культурально-морфологические признаки консорциума.
Клетки представляют Грам+ полиморфные палочки: бифидобактерий расположенны преимущественно в виде скоплений; в стационарной фазе роста часто отмечаются клетки с раздвоениями на концах или булавовидными утолщениями. Лактобациллы - цепочками из крупных клеток с закругленными концами.
При выращивании в ферментере в экспоненциальной фазе роста при микроскопии культура имеет вид ровных палочек разной величины, расположенных цепочками или скоплениями.
В полужидких питательных средах биомасса консорциума бифидобактерий и лактобацилл растет по всему объему питательной среды, кроме зоны аэробиоза. Морфология колоний неоднородна и зависит от входящих в консорциум штаммов, сохраняя признаки каждого из них в совокупной культуре.
Физиолого-биохимические признаки микроорганизмов, входящих в консорциум.
Бифидобактерий - облигатные анаэробы, лактобациллы - микроаэрофиллы. На агаризованной поверхности образуют прозрачные колонии. Оптимальная температура выращивания составляет 37,5-38°С, рН питательных сред 7,2-7,4. Каталазу не образуют, желатин не разжижают, газообразование отсутствует. Сбраживают глюкозу с образованием кислоты без образования газа, закисляя среду выращивания до рН 4,3-5,1.
Результаты культивирования монокультур бифидобактерий и лактобацилл и их совместного культивирования представлены в таблице 1.

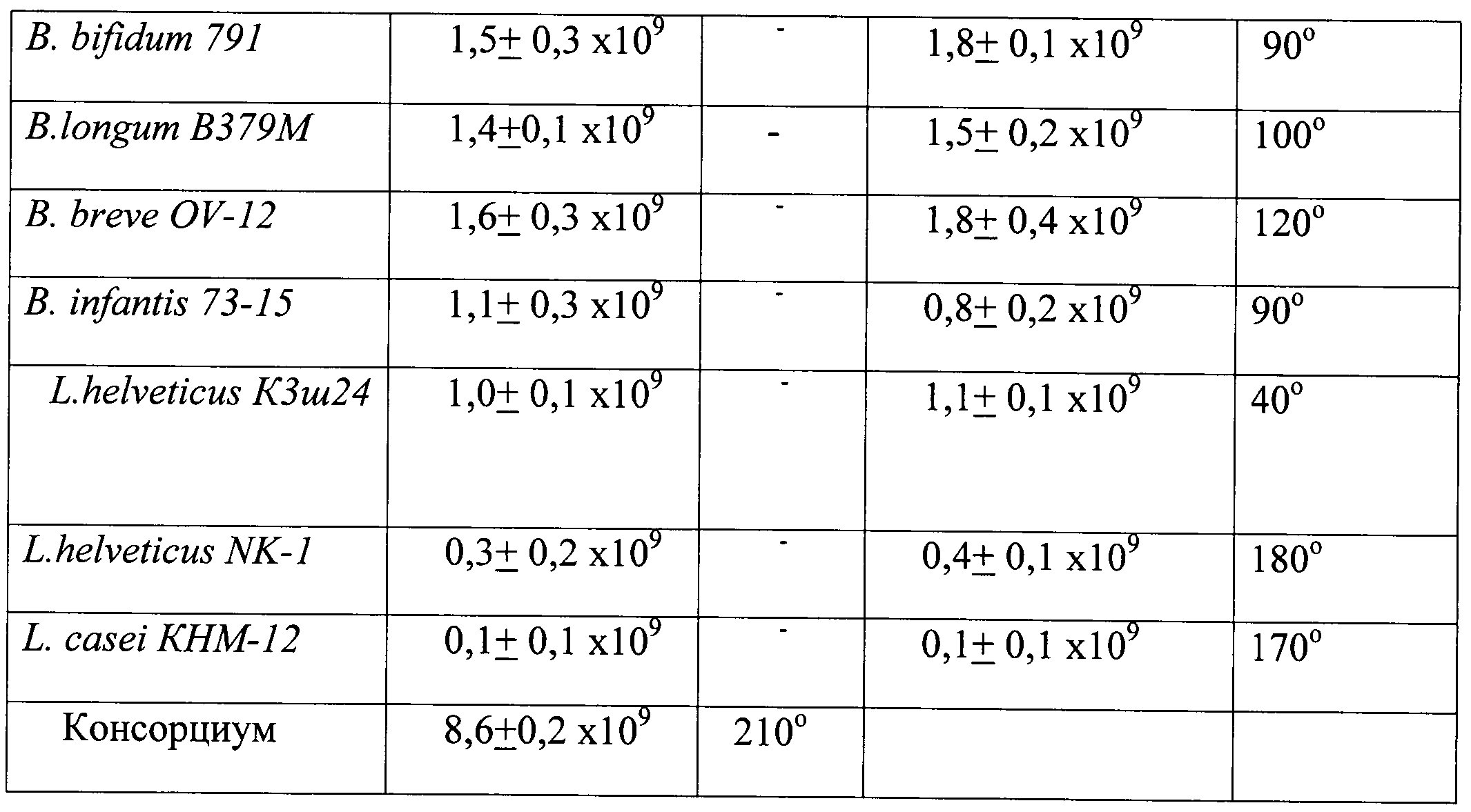
Консорциум активно размножается как на средах, принятых в производстве, со стабильно высокими показателями КОЕ/мл пробиотических микроорганизмов и продуцируемых органических кислот (таблица 2).
|
Как видно из результатов, представленных в таблицах 1 и 2, не происходит взаимного ингибирования культур. При этом отмечается тенденция к синергидному эффекту.
Наиболее перспективной в производстве препаратов и БАД для детей младшего возраста является гидролизатно-молочная среда. В настоящее время среди детей широко распространена непереносимость коровьего молока. Данная среда гипоаллергенна, так как ее основой является гидролизат молока, состоящий из низкомолекулярных пептидов и аминокислот, которые легко усваиваются детским организмом. Среда, изготовленная на основе гидролизата молока, имеет следующий состав (в расчете на 100 л):
|
Среда проста в приготовлении, экономически выгодна; вместе с тем, как видно из результатов, представленных в таблице 2, по ростовым свойствам уступает остальным средам.
Для устранения данного недостатка в нее были дополнительно включены добавки, стимулирующие рост пробиотических микроорганизмов - пребиотики инулин и олигофруктоза и дрожжевой аутолизат, содержащий витамины группы В, необходимые для их развития и аскорбиновая кислота, как антиоксидант. Состав усовершенствованной таким образом среды представлен в таблице 4.
|
При изучении ростовых свойств заявляемой среды было показано, что они превосходят ростовые свойства гидролизатно-молочной среды, т.е. желаемый результат был достигнут.Результаты представлены в таблице 5.
|
Таким образом, заявляемая среда является перспективной в производстве препаратов и БАД для детей младшего возраста.
Синергидный эффект, который был отмечен при культивировании консорциума, проявляется также при определении спектра биохимической активности.
В качестве иллюстрации в таблице 6 представлено, как расширяется спектр ферментативной активности штаммов при совместном культивировании - увеличивается число усвоенных субстратов.
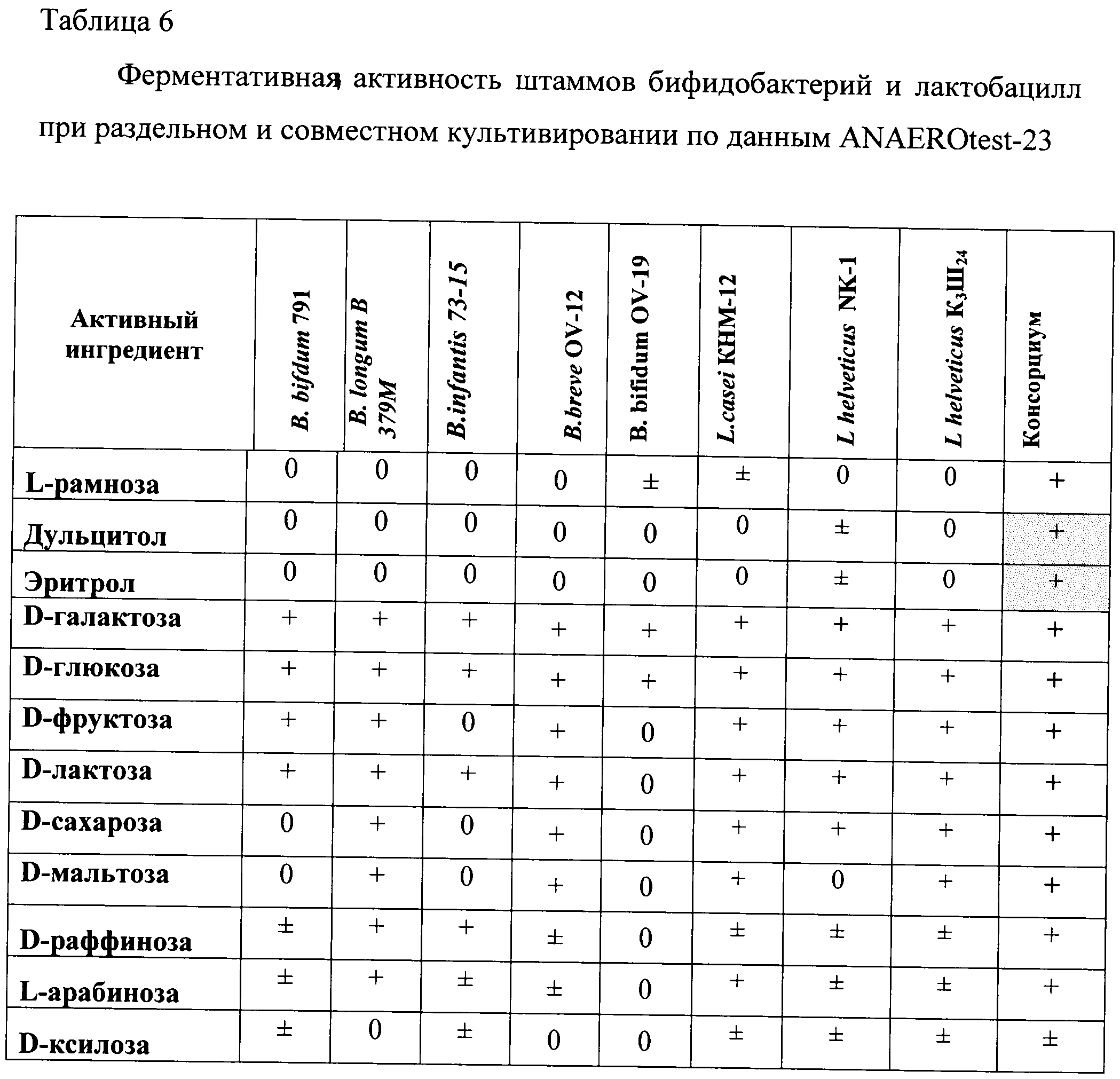
Синергидный эффект консорциума проявляется также в большей антагонистической активности консорциума по сравнению с монокультурами, что повышает пробиотическую значимость препарата. Данный эффект можно наблюдать по зонам задержки роста тест-культур (табл.7).
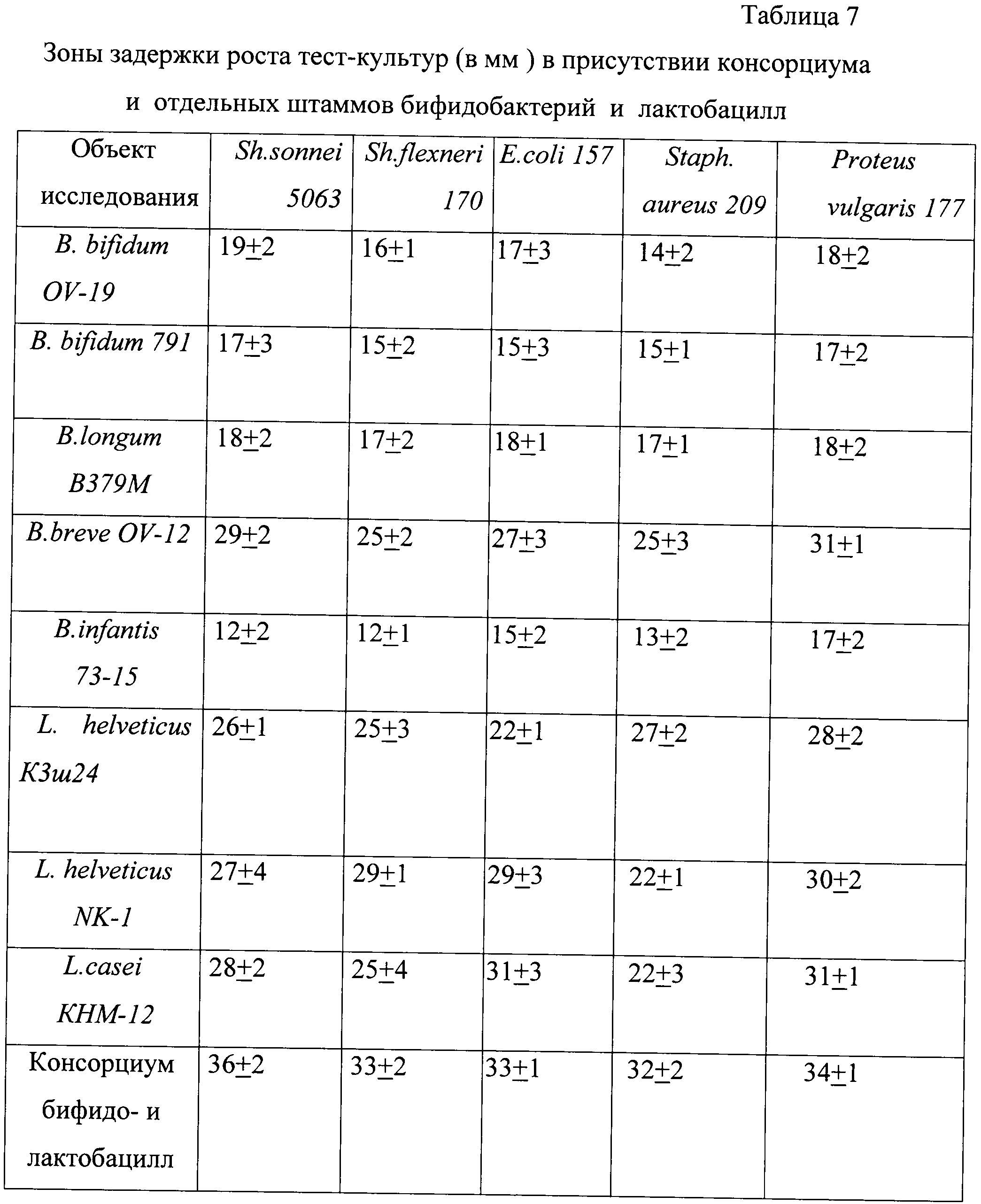
Как показывают данные, представленные в таблице 7, по антагонистической активности в отношении тест-штаммов патогенных микроорганизмов консорциум превосходит отдельные штаммы, входящие в его состав.
Таким образом, полученные результаты говорят не только о возможности совместного культивирования различных видов бифидобактерий и лактобацилл, но и синергидном эффекте консорциума штаммов, что позволяет решить сложную биотехнологическую задачу получения многокомпонентных пробиотических препаратов, имеющих определенный состав и назначение.
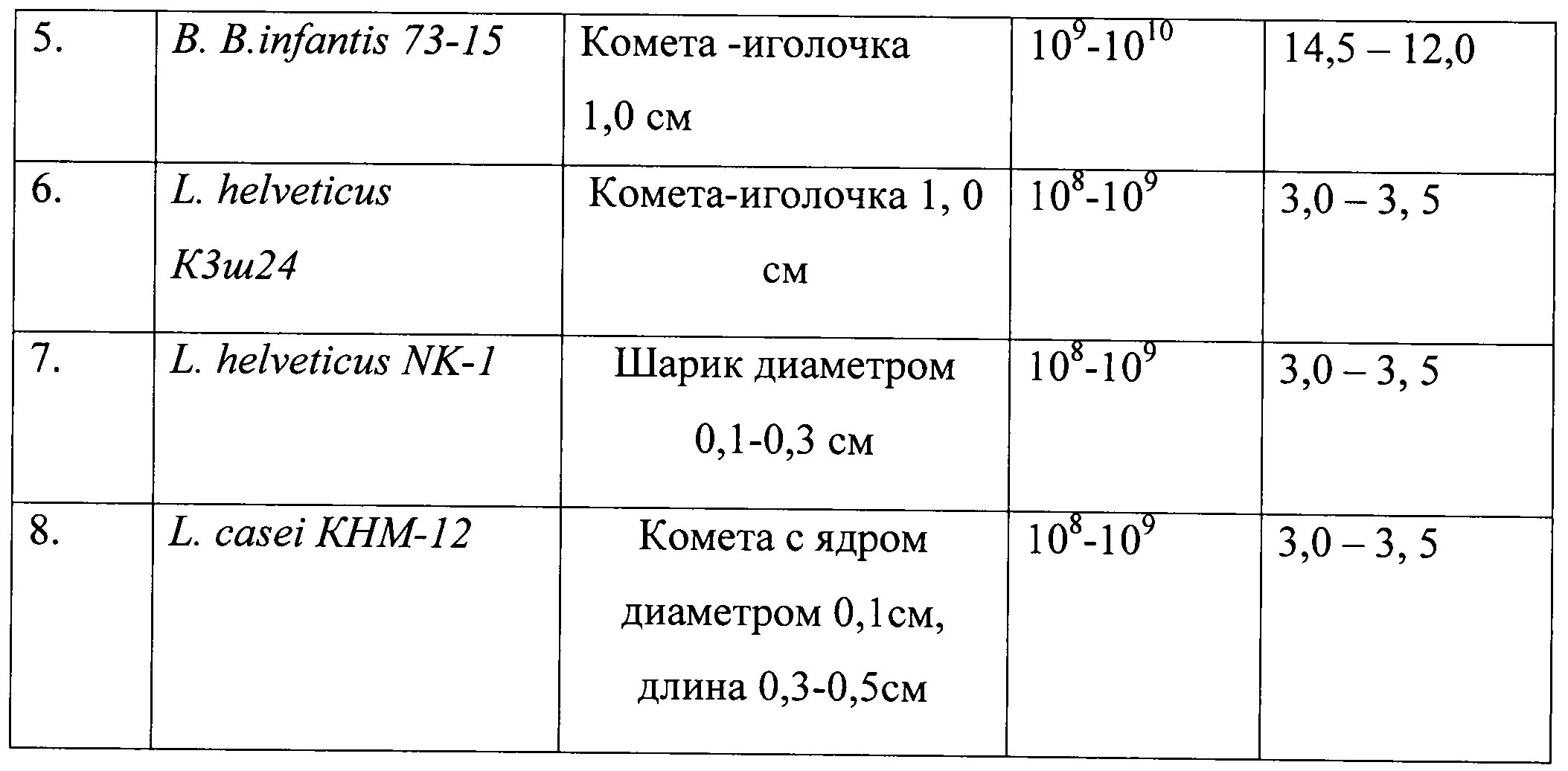
В предлагаемом консорциуме помимо определенного видового состава бифидобактерий и лактобацилл, отмечается определенное количественное соотношение микробных культур после культивирования. Количественный учет долевого участия отдельных штаммов производится путем подсчета числа колоний, выросших в полужидкой среде. Культура каждого штамма имеет колонии определенной морфологии и размера, что позволяет их различать. Соотношение отдельных видов бифидобактерий и лактобацилл в консорциуме представлено в таблице 8.
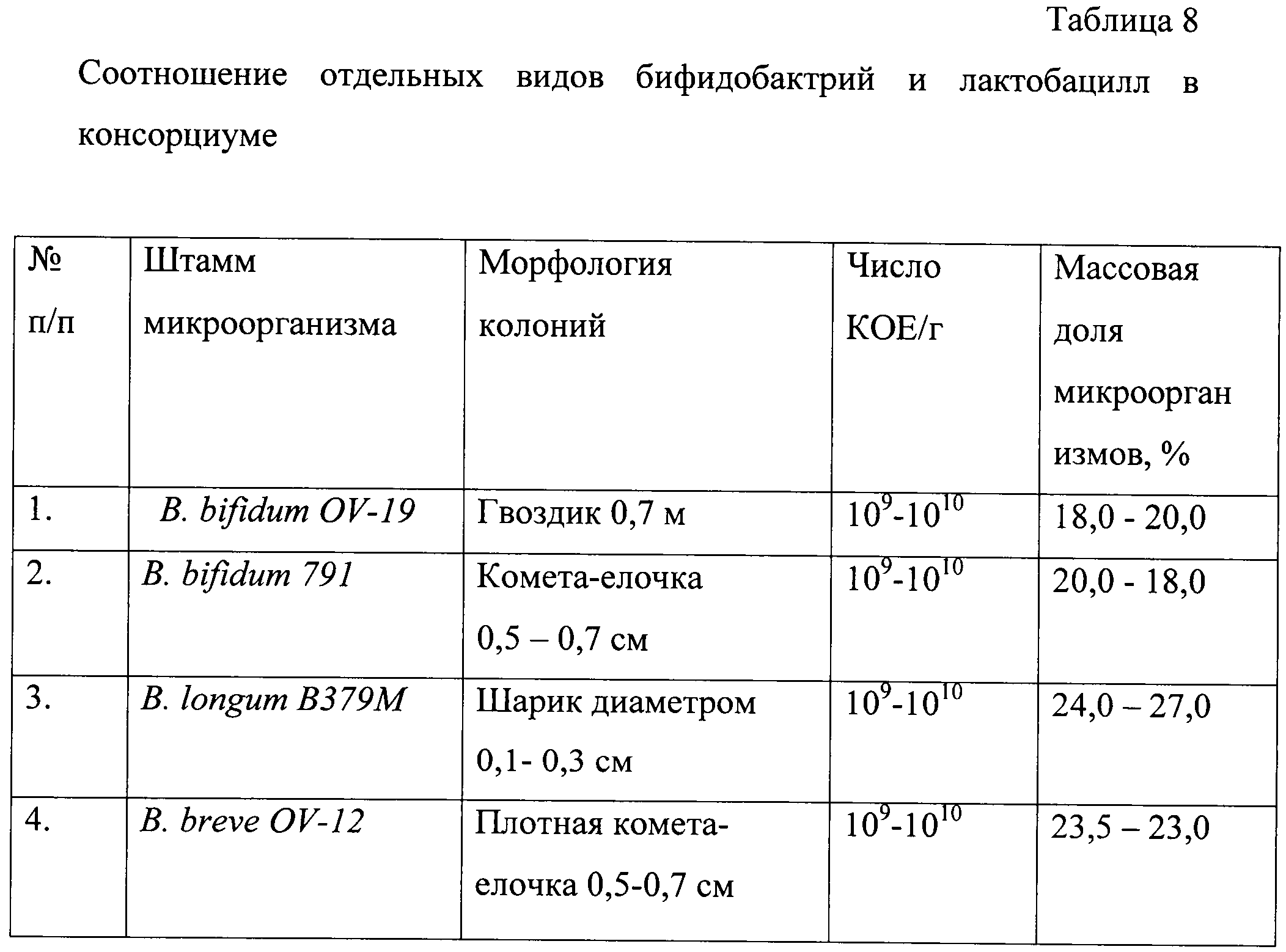
Примеры
1. Консорциум бифидобактерий и лактобацилл для нормализации микрофлоры желудочно-кишечного тракта детей от рождения до 3-х лет и способ его получения
1-й пассаж - лиофилизированный материал штаммов В. bifidum OV-19, В. bifidum 791, В. longum В379М, В. breve OV-12, В. infantis 73-15, L. L. helveticus К3ш24, L.casei КНМ-12, L.helveticus NK-1 по отдельности регидратируют физиологическим раствором в объеме 1 мл и титруют методом десятикратных разведений в питательной среде до 107-8. Инкубируют при температуре 37-38°С в течение 36 ч.
2-й пассаж.- каждую из выросших культур из разведения 106-8 в объеме 3% вводят в заявляемую среду (30 мл) и культивируют 7 ч при 37-38°С.
3-й пассаж- каждую из выросших культур засевают в питательную полужидкую среду заявляемого состава и выращивают в течение 17 ч при 37-38°С.
Выращивание консорциума.
Консорциум бифидобактерий и лактобацилл получают путем совместного культивирования вышеперечисленных штаммов. Для этого подбирают строго количественное соотношение посевного материала каждого из штаммов согласно разработанной схеме. По оптическому стандарту мутности устанавливают концентрацию ОЕ/мл, соответствующую 1 млрд клеток бифидобактерий.
Процесс культивирования ведут 9 ч при при 37-38°С.
Состав среды выращивания (в расчете на 100):
|
2. Биологически активная добавка к пище для детей до 3-х лет и способ ее получения
БАД изготавливается на основе консорциума сухой биомассы бифидобактерий и лактобацилл с добавлением функционально значимых ингредиентов.
Выращивание консорциума.
1-й пассаж - лиофилизированный материал штаммов В.bifidum OV-19, В.bifidum 791, В.breve 79-119, В. breve OV-12, В.infantis 73-15, L.helveticus К3ш24, L.casei KHM-12, L.acidophilus NK-1 по отдельности регидратируют физиологическим раствором в объеме 1 мл и титруют методом десятикратных разведений в питательной среде до 107-8. Инкубируют при температуре 37-38°С в течение 36 ч.
2-й пассаж.- каждую из выросших культур из разведения 106-8 в объеме 3% вводят в среду накопления (30 мл) и культивируют 7 ч при 37-38°С.
3-й пассаж - каждую из выросших культур засевают в питательную полужидкую среду и выращивают в течение 17 ч при 37-38°С.
Консорциум бифидобактерий и лактобацилл получают путем совместного культивирования вышеперечисленных штаммов. Для этого подбирают строго количественное соотношение посевного материала каждого из штаммов в соответствии. По оптическому стандарту мутности устанавливают концентрацию ОЕ/мл, соответствующую 1 млрд клеток бифидобактерий. Посев культур в ферментер проводят поэтапно, с периодичностью в 30 минут по разработанной схеме, коррегируя рН культуральной жидкости 20% NaOH перед засевом нового штамма до 6,0. Процесс культивирования ведут 8 ч при при 37-38°С.
К выращенной биомассе добавляют защитную сахарозо-желатиновую среду и обезжиренное 10%-ное молоко по 10% к объему биомассы бифидобактерий и лиофильно высушивают.
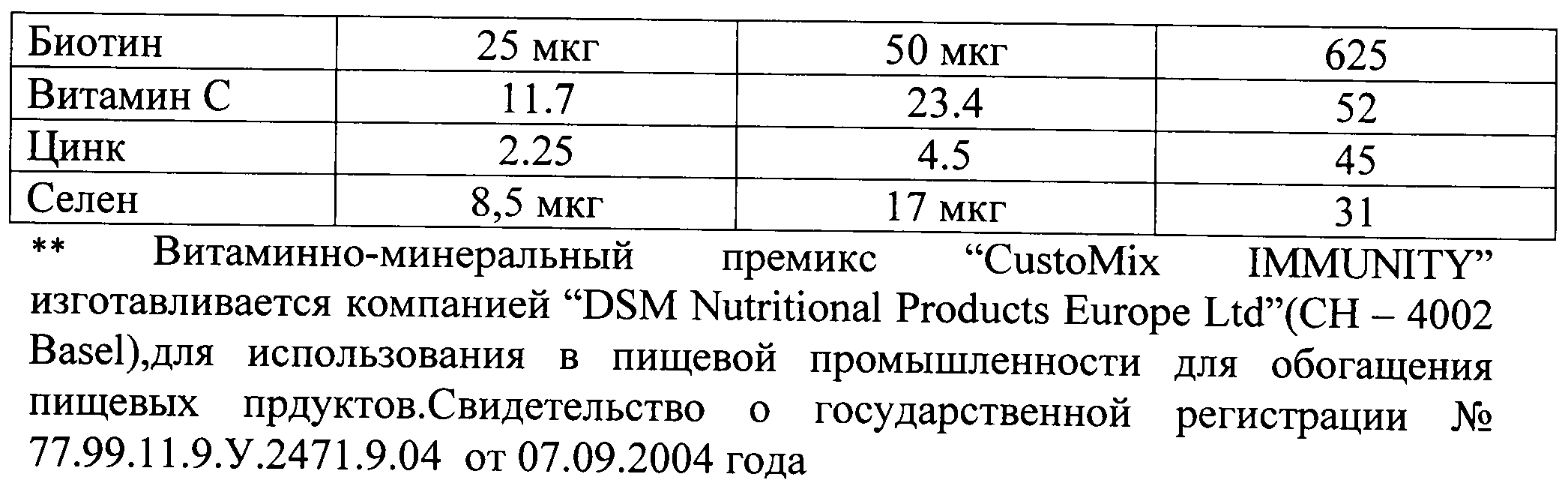
Техническим результатом, достигаемым при получении биологически активной добавки с использованием заявляемого консорциума, является более эффективная и быстрая коррекция микрофлоры и функционального состояния ЖКТ детей в возрасте до 3-х лет, а также источником витаминов, цинка и селена.
После помола биомассу смешивают с витаминно-минеральным премиксом, инулином, олигофруктозой и фасуют по 25 г в стерильные пластиковые баночки с герметично закрывающимися крышками, к которым прилагается мерная ложечка.
Рецептура биологически активной добавки представлена в таблице 9 (а, б).


3. Бактериальный препарат для лечения дисбиотических состояний ЖКТ у детей от рождения до 3 лет и способ его производства
1-й пассаж - лиофилизированный материал штаммов В.bifidum OV-19, В.bifidum 791, В.longum В379М, В. breve OV-12, В.infantis 73-15, L..helveticus К3ш24, L.casei КНМ-12, L.helveticus NK-1 по отдельности регидратируют физиологическим раствором в объеме 1 мл и титруют методом десятикратных разведений в питательной среде до 107-8. Инкубируют при температуре 37-38°С в течение 24 ч.
2-й пассаж.- каждую из выросших культур из разведения 106-8 в объеме 3% вводят в среду накопления (30 мл) и культивируют 7 ч при 37-38°С.
3-й пассаж- каждую из выросших культур засевают в питательную полужидкую среду и выращивают в течение 17 ч при 37-38°С. Выращивание консорциума. Консорциум бифидобактерий и лактобацилл получается путем совместного культивирования вышеперечисленных штаммов. Для этого подбирают строго количественное соотношение посевного материала каждого из штаммов согласно разработанной схеме. По оптическому стандарту мутности устанавливают концентрацию ОЕ/мл, соответствующую 1 млрд клеток бифидобактерий.
Процесс культивирования ведут 10 ч при при 37-38°С.
Состав среды выращивания (в расчете на 100):
|
Процесс культивирования ведут 10 ч при при 37-38°С. К выращенной комплексной биомассе бифидобактерий и лактобацилл добавляют защитную сахарозо-желатиновую среду и обезжиренное 10%-ное молоко по 10% к объему биомассы, разливают в асептических условиях по 5 мл в стеклянные пенициллиновые флаконы и лиофильно высушивают.
Техническим результатом, достигаемым при получении бактериального препарата с использованием заявляемого консорциума в качестве активного вещества, является более эффективная и быстрая коррекция дисбиотических нарушений ЖКТ детей в возрасте от рождения до 3-х лет.
* Содержание КОЕ/г бифидобактерий и лактобацилл в готовом препарате не менее 108.
Список цитируемой литературы
L.Mitsuoka Т. Intestinal Flora and Host.//Asian.Med.J.-1989-V.31.-N7.-P.400-409.
2. Гончарова Г.И., Лянная A.M., Козлова Э.Л., Семенова Л.П. Роль бифидофлоры в повышении устойчивости организма к инфекции. // В сб. материалов международной конференции «Гнотобиология в теоретической и практической медицине». - М. - 1987. - С.62.
3. Шендеров Б.А. Микрофлора пищеварительного тракта - важнейший фактор поддержания микроэкологического гомеостаза хозяина. // Клиническое питание. - 2005. - №2. - С.2-5.
4. Гончарова Г.И. Бифидофлора человека, ее защитная роль в организме и обоснование сфер применения препарата бифидумбактерин // Автореф.дис… д-ра биол..наук. - М. - 1982. -48 С.
5. Шендеров Б.А. Функциональное питание и его роль в профилактике метаболического синдрома // Москва: Дели принт. - 2008. - С.317.
6. Гончарова В.В. Изучение бифидобактерий, разработка препарата «сухой бифидумбактерин» и его эффективность при кишечных заболеваниях детей первого года жизни. // Автореф.дисс… канд.биол.наук. - Москва. 1970. - С.15.
7. Mitsuoka Т., Hayakawa К., Kimura N.. The fecal flora of man. II. Communication: the composition of bifidobacterium flora of different age groups. // Zentralbl. Bakteriol. Mikrobiol. Hyg. 1 Abt. Orig. - A 1974. - V.226/ - P.469-478.
8. Патент РФ №2196174.
9. Сукачев B.H., Дылиса Н.В. Лесной биогеоценоз // М.:Наука. - 1964. - С.574.
10. Рыбальченко О.В., В.М.Бондаренко, Добрица В.П. Атлас ультраструктуры микробиоты кишечника человека. // С-Петербург. - 2008. - С.109.
11. Бифидобактерий и их использование в клинике, медицинской промышленности и сельском хозяйстве. // Сб.научных трудов. - М. - 1986. - С.208.
12. Леванова Л.Л., Алешкин В.А., Воробьев А.Л., и др. Возрастные особенности микробиоценоза кишечника у жителей г.Кемерово. // Журн. Микробиол. - 2001. - №3. - С.72-75.
12. Глушанова Н.А., Шендеров Б.А. Взаимоотношения пробиотических и индигенных лактобацилл в условиях совместного культививрования in vitro. // Журнал микроб., эпидемиол., и иммунобиол. - 2005. - №2. - С.56-61.
14. Патент РФ №2180915 «Консорциум бифидобактерий и лактобацилл, используемый для приготовления бактериальных препаратов, заквасок для кисломолочных продуктов, ферментированных и неферментированных пищевых продуктов, биологически активных добавок, предназначенных для коррекции микрофлоры детей в возрасте до 3-х лет»; Заявка №2001111553 от 28.04.2001 г. Опубл. 27.03.2002 г.
15. Карзанова М.В., Воронина О.Л., Лунин В.Г., Жиленкова О.Г., Амерханова A.M. Определение видовой принадлежности штаммов бифидобактерий на основе секвенирования фрагментов генов 16S рРНК и трансальдолазы. // Сборник докладов Россельхозакадемии. - М. - 2006. - №5. - С.9-12.
16. Namba К., Hatano М. at all. Method of detecting Bifidobacterium infantis // United States Patent.- Prior Publication data 14.12.2006. - 22 P.
17. Жиленкова О.Г.Селекция производственно перспективных штаммов бифидобактерий, выделенных от детей // Автореф. дисс.канд.биол.наук, Москва, 2011, С.16.
18. Шкопоров А.Н., Кафарская Л.И., Афанасьев С.С. и др. Молекулярно-генетический анализ видового и штаммового разнообразия бифидобактерий у детей раннего возраста. // Вестник Российской АМН. - 2006, - №1. - С.45-50.
19. Smehilova М., Vilkova Е., Nevoral J. Comparison of intestinal microflora in healthy infants and infants with allergic colitis. Folia Microbiol (Praha) 2008. - 53(3). - P.255-258
20. Ezendam J., de Klerk A., Gremmer E.R., van Loveren H. Effects of Bifidobacterium animalis administered during lactaion on allergic and autoimmune responses in rodents. // Clinical and Experimental Immunology. - 2008. - V.154. - P.424-155.
21. Reiter [24] причисляет их к подвидам B.adolescentis, который нехарактерен для микробиоценоза детей. Такие виды нефизиологичны для детей и не могут быть использованы в составе средств коррекции микрофлоры данной возрастной группы.
22. Патент РФ №2373274 от 20.11.2009 Штамм Bifidobacterium breve OV-12, используемый для получения бактерийных препаратов, биологически активных добавок к пище, ферментированных и неферментированных пищевых продуктов, гигиенических и косметических средств.
23. Патент РФ №2375444 от 10.12.2009 Штамм Bifidobacterium bifidum OV-19, используемый для получения бактерийных препаратов, биологически активных добавок к пище, ферментированных и неферментированных пищевых продуктов, гигиенических и косметических средств.

