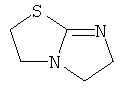Результат интеллектуальной деятельности: ОТВЕРЖДАЕМАЯ КОМПОЗИЦИЯ, СОДЕРЖАЩАЯ ТЕРМОЛАТЕНТНОЕ ОСНОВАНИЕ
Вид РИД
Изобретение
Данное изобретение относится к отверждаемым композициям, содержащим термолатентное амидиновое основание и органический материал, который способен к полимеризации или поперечному сшиванию с основным или нуклеофильным катализатором. В частности, данное изобретение относится к отверждаемым композициям покрытий, особенно композициям порошковых покрытий, и отверждаемым адгезивным композициям, а также к применению термолатентного амидинового основания в качестве катализатора отверждения для термически индуцируемых, катализируемых основанием реакций полимеризации или поперечного сшивания.
Соединения, из которых основания выделяются при нагревании, называют термолатентными основаниями. Термолатентные основания применяют в различных системах, созданных таким образом, чтобы основания, выделяемые при нагревании, могли функционировать в них. Примеры таких систем включают термопроявляемые фотографические материалы, теплочувствительные регистрирующие материалы, полимеризуемые по анионному механизму адгезивы, пленкообразование при нанесении покрытия, герметики, уплотнители и тому подобное.
Типичные термолатентные основания для применения в различных типах формирующих изображение материалов, для которых используется теплота, включают соли карбоновых кислот и органические основания, как описывается, например, в GB 998949 (соли трихлоруксусной кислоты), US-В-6699651 (соли α-сульфонилуксусной кислоты), DE-A-3530252, где описаны соли, содержащие, в качестве термолатентного основания, протежированный гуанидин, его амидиновую или циклическую производную. Применение этих солей основано на том, что декарбоксилирование карбоновых кислот при нагревании приводит к выделению органических оснований. Другие термолатентные основания включают производные 2-карбоксикарбоксамида, описанные в US-A-4088496, карбаматы гидроксамовой кислоты, описанные в EP-A-0120661, и карбаматы альдоксима, описанные в EP-A-0118078.
В WO 98/04531 описываются отверждаемые смеси на основе эпоксидных смол, содержащие N-алкоксикарбонилимидазол в качестве катализатора отверждения, которые выделяет производную имидазола при декарбоксилировании. В US-A-4189543 также описано применение таких соединений при получении полиуретановых пен.
Отверждаемые композиции, содержащие термолатентное основание в качестве катализатора отверждения, могут быть предварительно смешаны. Для ингибирования нежелательного преждевременного отверждения во время хранения предварительно смешанных композиций, содержащих катализатор отверждения, существует постоянная потребность в термолатентных основаниях, обладающих хорошей стабильностью во время хранения в отверждаемых композициях, но также быстро превращающихся в активные основания при нагревании до температуры применения.
Было обнаружено, что определенные низкоосновные замещенные амидины выделяют циклический и значительно более основный или нуклеофильный амидин при повышенных температурах. Эти циклические амидины являются достаточно основными или нуклеофильными для того, чтобы инициировать большое число катализируемых основанием реакций полимеризации и поперечного сшивания.
Следовательно, данное изобретение относится к отверждаемой композиции, содержащей
(A) органический материал, который способен к полимеризации или поперечному сшиванию с основным или нуклеофильным катализатором и
(B) соединение формулы
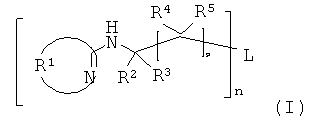
где заместитель R1 образует, вместе с атомам углерода и атомом азота, с которыми он связан, моно- или пол и циклическую С2-C20 кольцевую систему, которая может также содержать один или более гетероатомов O, S и/или N и/или может быть не замещена или замещена C1-C18алкилом; C1-C18алкилом, который замещен E и/или прерывается D; C5-C12циклоалкилом, который замещен Е и/или прерывается D; С5-С12циклоалкенилом; C2-C18алкенилом; C2-C18алкинилом; C6-C18арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C18алкокси; C1-C18алкокси, который замещен Е и/или прерывается D; C1-C18алкилтио; C1-C18алкилтио, который замещен Е и/или прерывается D; C7-C18аралкилом; C7-C18аралкилом, который замещен G; галогеном; оксо; ОН; SH; CN; NH2; NO2; COOH; NHR6; NR7R8; CONH2; CONR9R10; COR11; C(O)OR12; SO2R13; SO3R14; SO2NHR15; SO2NR16R17;
или указанная кольцевая система замещена одной или более группами формулы
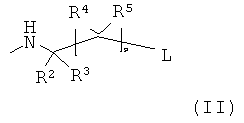
R2, R3, R4 и R5 независимо друг от друга и в каждом случае являются Н; C1-C18алкилом; C1-C18алкилом, который замещен Е и/или прерывается D; C5-C12циклоалкилом; C5-C12циклоалкилом, который замещен Е; C6-C12арилом; C8-C18арилом который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C18алкокси; C1-C18алкокси, который замещен Е и/или прерывается D; C7-C18аралкилом; C7-C18аралкилом, который замещен G; NHR18, NR19R20, COOH;
или R2 и R3, R4 и R5 или R2 и R4 образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому они присоединены, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 12 атомов в общем; или два R5, которые связаны с соседними атомами углерода, образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому они присоединены, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 12 атомов в общем;
D представляет собой -CO-; -COO-; -S-; -SO-; -SO2-; -O-; -NR21-; -SiR22R23-; -POR24-; -CR25=CR26-; или -C≡C-;
E представляет собой OR27; SR28; SOR29; SO2R30; NR31R32; COR33; COOR34; CONR35R36; PO(R37)2; Si(R38)3; CN; или галоген; и
G представляет собой Е или C1-C18алкил;
R6, R7, R8 , R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, R19, R20, R21, R22, R23, R24, R25, R26, R27, R28, R29, R30, R31, R32, R33, R34, R35, R36, R37 и R38 независимо друг от друга являются C1-C18алкилом; C1-C18алкилом, который прерывается группой -O-; C6-C18арилом; C6-C18арилом, который замещен C1-C18алкилом или C1-C18алкокси; C7-C18аралкилом; C7-C18аралкилом, который замещен G; C2-C18гетероарилом;
или R7 и R8, R9 и R10, R16 и R17, R19 и R20, R31 и R32 или R35 и R36 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 кольцевых атомов в общем;
L является n-валентной уходящей группой,
n равно целому числу 1, 2, 3 или 4; и
p равно целому числу 1, 2, 3 или 4.
Соединения формулы (I) являются практически неактивными при комнатной температуре или при слегка повышенной температуре и не способствуют полимеризации до тех пор, пока композиция в соответствии с данным изобретением не будет нагрета. При повышенных температурах они выделяют соединение формулы (V) согласно следующей схеме реакции:
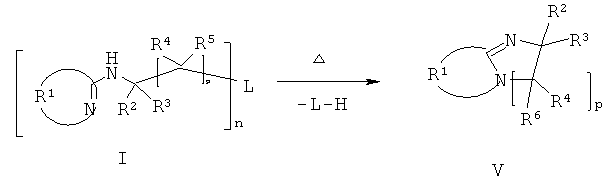
Соединения формулы (V) содержат структуру циклического амидина и, поэтому, являются достаточно основными или нуклеофильными для инициации большого числа катализируемых основанием реакций полимеризации или поперечного сшивания. Интервал температур, при которых данные основания выделяются и при которых они являются активными, может варьироваться в широком интервале в зависимости от выбора типа замещения.
Поэтому, соединения формулы (I) способны формировать так называемые однореакторные системы с полимеризуемыми в присутствии основания олигомерами или мономерами, имеющими очень длительный срок хранения без специальных мер предосторожностей. Кроме того, такие системы обладают преимуществом в плане сокращенной подготовки непосредственно перед применением и низких количеств отходов благодаря лучшему предельному сроку хранения. Системы могут быть получены с незначительным количеством растворителя или без растворителя, так как соединения могут быть растворены в мономерах или олигомерах без воздействия на эти соединения. Эти системы могут применяться для множества целей, особенно для покрытий, более предпочтительно, для порошковых покрытий.
При повышенных температурах термолатентное основание катализирует реакцию в форме его выделенных оснований. Как правило, температуры реакции, требуемые для активации катализатора, могут быть от около 50°C до около 250°. Предпочтительный интервал температуры составляет от около 80°C до около 150°, более предпочтительно, от около 110°C до около 130°C.
Термин "термолатентное основание", также указанный как "термочувствительный предшественник основания", относится к нейтральному или слабоосновному, или слабонуклеофильному соединению, которое выделяет основное или нуклеофильное соединение при нагревании.
В предпочтительном варианте данное изобретение относится к отверждаемой композиции, содержащей, в качестве компонента (В), соединение формулы (I), где, если n равно 1, L является галогеном, OH, OR40, SR40, OCOR40, OCOOR41, OCONR42R43, OCSNR42R43, OSO2R40, OSO3R40, NR42R43, S+R42R43X-, N+R42R43R44X-, P+R42R43R44X-, NHCOR40, N(COR45)2, NHSO2R40, NHSO3R40, SO2R40, OP(NR42R43)2, OPO(NR42R43)2, OP(OR40)2, OPO(OR40)2, OPO(R46)(OR47), OSi(R40)3;
где
R40, R42, R43, R44, R45, R46 и R47 независимо друг от друга является Н, C1-C18алкилом или C1-C18алкилом, который замещен Е и/или прерывается D; C5-C12циклоалкилом, C5-C12циклоалкилом, который замещен Е и/или прерывается D; C6-C18арилом; C6-C18арилом, который замещен G; C7-C18аралкилом; C7-C18аралкилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; или R42 и R43 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 кольцевых атомов в общем; или два R45 образуют органическую мостиковую группу, составляющую, вместе с -OC-N-CO-группой, к которой они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 атомов всего;
R41 является C1-C18алкилом или C1-C18алкилом, который замещен Е и/или прерывается D;
C5-C12гциклоалкилом, C5-C12циклоалкилом, который замещен Е и/или прерывается D;
C6-C18арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G;
X- является галогенидом, гидроксидом, C1-C18алкилсульфонатом, C6-C18арилсульфонатом, R48COO-, HSO4 - или 1/2 SO4 2-, где R48 является Н, C1-C18алкилом или C1-C18алкилом, который замещен Е и/или прерывается D; C5-C12циклоалкилом, C5-C12циклоалкилом, который замещен Е и/или прерывается D; C6-C18арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G;
если n равно 2, L является -ОСО-О,
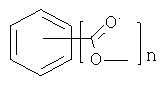 ,
, 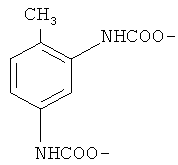 ,
, 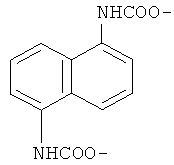 ,
,
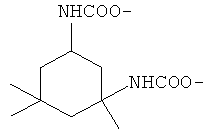 , -OSO2O-, OCO-(CH2)q-COO-, OSi(CH3)2O-, OCONH(CH2)q, где q равно 0 или целому числу от 1 до 10; или
, -OSO2O-, OCO-(CH2)q-COO-, OSi(CH3)2O-, OCONH(CH2)q, где q равно 0 или целому числу от 1 до 10; или
если n равно 3 или 4, L является 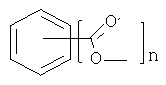
Согласно определениям, кольцевая система, образованная R1 вместе с атомом углерода и азота, с которыми он связан, соответствующая 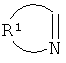 , является моно- или полициклической С2-С20 кольцевой системой, которая, в дополнение к N, может содержать один или более гетероатомов O, S и/или N и/или может быть не замещена или замещена, как указано в п.1.
, является моно- или полициклической С2-С20 кольцевой системой, которая, в дополнение к N, может содержать один или более гетероатомов O, S и/или N и/или может быть не замещена или замещена, как указано в п.1.
Кольцевая система может быть ароматической или неароматической гетероциклической системой.
Предпочтительно, С2-С20 кольцевая система содержит от 1 до 4 конденсированных колец и вплоть до 5 гетероатомов, выбранных из О, N и/или S. Более предпочтительно, С2-С20 кольцевая система содержит от 1 до 3, например, 1 или 2 конденсированных колец, и от 1 до 3, например, 1 или 2, гетероатома, выбранных из N и/или S.
Алкильные группы могут быть в указанных пределах атомов углерода линейными или разветвленными, если возможно. Примеры включают метил, этил, н-пропил, изопропил, н-бутил, втор-бутил, изобутил, трет-бутил, н-пентил, 2-пентил, 3-пентил, 2,2-диметилпропил, 1,1,3,3-тетраметилпентил, н-гексил, 1-метилгексил, 1,1,3,3,5,5-гексаметилгексил, н-гептил, изогептил, 1,1,3,3-тетраметилбутил, 1-метил гептил, 3-метилгептил, н-октил, 1,1,3,3-тетраметилбутил и 2-этилгексил, н-нонил, децил, ундецил, додецил, тридецил, тетрадецил, пентадецил, гексадецил, гептадецил, октадецил.
Циклоалкильные группы могут включать в данных пределах, например, циклопентил, циклогексил, циклогептил, циклооктил, метилциклопентил, диметилциклопентил, метилциклогексил и диметилциклогексил, предпочтительно, циклогексил. Циклоалкильная группа, в частности, циклогексильная группа, может быть конденсирована одиножды или дважды с фенилом, который может быть замещен от одного до трех раз С1-С4алкилом и галогеном.
Циклоалкенильные группы могут включать в данных пределах, например, циклопентенил, циклогексенил, метилциклопентенил, диметилциклопентенил и метилциклогексенил. Циклоалкенил может содержать более одной двойной связи, которые могут быть конъюгированы или не конъюгированы, например, может содержать одну двойную связь.
Алкенильные группы могут быть в данных пределах атомов углерода прямыми или разветвленными, если возможно. Примеры включают винил, аллил, металлил, изопропенил, 2-бутенил, 3-бутенил, изобутенил, н-пента-2,4-диенил, 3-метилбут-2-енил, н-окт-2-енил, н-додец-2-енил, изододеценил, олеил, н-додец-2-енил или н-октадец-4-енил. Термин алкенил также включает остатки с более чем одной двойной связью, которые могут быть конъюгированы или не конъюгированы, например, могут включать одну двойную связь.
Алкинильные группы могут быть в данных пределах атомов углерода прямыми или разветвленными, если возможно. Примеры включают этинил, 1-пропин-3бутин, 1-бутин-4-ил, 1-пентин-5-ил, 2-метил-3-бутин-2-ил, 1,4-пентадиин-3-ил, 1,3-пентадиин-5-ил, 1-гексин-6-ил, цис-3-метил-2-пентен-4-ин-1-ил, транс-3-метил-2-пентен-4-ин-1-ил, 1,3-гексадиин-5-ил, 1-октин-8-ил, 1-нонин-9-ил или 1-децин-10-ил. Термин алкинил также включает остатки с более чем одной тройной связью и остатки с тройной связью и двойной связью, которые могут быть конъюгированы или не конъюгированы. Например, алкинил включает одну тройную связь.
Термин "арильная группа" обычно означает С6-C18арил, такой как фенил, инденил, азуленил, нафтил, бифенил или терфенилил, as-индаценил, s-индаценил, аценафтиленил, фенантрил, флуорантренил, трифениленил, кризенил, нафтацен, пиценил, периленил, пентафенил, гексаценил, пиренил или антраценил, предпочтительно, фенил, 1-нафтил, 2-нафтил, 9-фенантрил, 2- или 9-флуоренил, 3- или 4-бифенил.
Алкоксигруппы могут быть в данных пределах атомов углерода прямыми или разветвленными алкоксигруппами, например, метокси, этокси, н-пропокси, изопропокси, н-бутокси, втор-бутокси, изобутокси, трет-бутокси, амилокси, изоамилокси или трет-амилокси, гептилокси, октилокси, изооктилокси, нонилокси, децилокси, ундецилокси, додецилокси, тетрадецилокси, пентадецилокси, гексадецилокси, гептадецилокси и октадецилокси.
Термин "алкилтиогруппа" включает такие же группы, как алкоксигруппы, за исключением того, что атом кислорода простоэфирной связи заменен атомом серы.
Аралкильные группы могут включать в указанных пределах атомов углерода, например, бензил, 2-бензил-2-пропил, β-фенилэтил (фенэтил), α,α-диметилбензил, ω-фенилбутил, ω,ω-диметил-ω-фенилбутил, ω-фенилдодецил, в которых алифатические и ароматические углеводородные группы могут быть не замещены или замещены. Предпочтительные примеры включают бензил, фенэтил и α,α-диметилбензил.
Термин "гетероарильная группа", особенно C2-C18гетероарил, означает кольцо, где азот, кислород или сера являются возможными гетероатомами, и, как правило, означает ненасыщенный гетероциклический радикал, содержащий от пяти до 18 атомов, имеющих, по меньшей мере, шесть конъюгированных тт-электронов, такой как тиенил, бензо[b]тиенил, дибензо[b,d]тиенил, тиантренил, фурил, фурфурил, 2Н-пиранил, бензофуранил, изобензофуранил, 2Н-хроменил, ксантенил, дибензофуранил, фенокситиенил, пирролил, имидазолил, пиразолил, пиридил, бипиридил, триазинил, пиримидинил, пиразинил, 1Н-пирролизинил, изоиндолил, пиридазинил, индолизинил, изоиндолил, индолил, 3Н-индолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, индазолил, пуринил, хинолизинил, хинолил, изохинолил, фталазинил, нафтиридинил, хиноксалинил, хиназолинил, циннолинил, птеридинил, карбазолил, 4аН-карбазолил, карболинил, бензотриазолил, бензоксазолил, фенантридинил, акридинил, перимидинил, фенантролинил, феназинил, изотиазолил, фенотиазинил, изоксазолил, фуразанил или феноксазинил.
Галоген означает I, Br, Cl, F, особенно, Br или Cl.
Примеры 5-12-членного кольца, образованного R2 и R3, R4 и R5, R2 и R4 или двумя R5, включают циклоалканы, которые могут иметь один дополнительный гетероатом, выбранный из NR', О и S, где R' является C1-C18алкилом или фенилом, и/или указанное кольцо может быть замещено Е и/или прерывается D. Предпочтительными являются 5-7-членные циклоалканы.
Примеры 5-7-членного кольца, образованного R7 и R8, R9 и R10, R16 и R17, R19 и R20, R31 и R32, R35 и R36 или R42 и R43, включают гетероциклоалканы или гетероциклоалкены, имеющие от 3 до 6 атомов углерода и, необязательно, один дополнительный гетероатом, выбранный из NR', О и S, где R' является C1-C18алкилом или фенилом, и/или указанное кольцо может быть замещено Е и/или прерывается D.
Примерами являются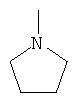 ,
, 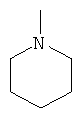 ,
, 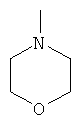 , или
, или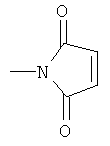 , которые могут быть частью бициклической системы, например,
, которые могут быть частью бициклической системы, например, 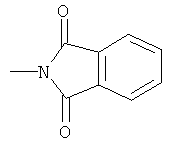 и
и 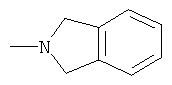 .
.
Примеры 5-7-членного кольца, образованного двумя R45, включают гетероциклоалканы или гетероциклоалкены, имеющие от 3 до 6 атомов углерода, например,  , которые могут быть частью бициклической системы, например
, которые могут быть частью бициклической системы, например  .
.
Термин "в каждом случае" для R4 и R5 означает, что радикалы R4 и R5 могут иметь, независимо друг от друга, различные значения, если p равно 2, 3 или 4.
Как описано выше, указанные радикалы могут быть замещены Е и/или, при желании, прерываются D. Прерывания, конечно, возможны только в случае радикалов, содержащих, по меньшей мере, 2 атома углерода, связанных друг с другом одинарными связями; С6-С18арил не прерывается; прерывающиеся арилалкил или алкиларил содержат составляющую D в алкильной группе. С1-С18алкил замещен одной или более составляющими E и/или прерывается одной или более составляющими D и является, например, (CH2CH2O)5-Rx, где s равно числу из интервала 1-9, и Rx является Н или C1-C10алкилом или C2-C10алканоилом (например, CO-CH(C2H5)C4H9), CH2-CH(ORy')-CH2-O-Ry, где Ry является C1-C18алкилом, C5-C12циклоалкилом, фенилом, C7-C15фенилалкилом, и Ry' имеет те же определения, что Ry или является Н); C1-C8алкилен-COO-Rz, например, CH2COORz, CH(CH3)COORz, C(CH3)2COORz, где Rz является Н, C1-C18алкилом, (CH2CH2O)1-9-Rx, и Rx имеет те же определения, которые указаны выше; CH2CH2-O-CO-CH=СН2; CH2CH(OH)CH2-O-CO-C(CH3)=CH2.
Термин "замещенный G" означает, что могут присутствовать один или более, особенно от одного до трех заместителей G.
Термин "по меньшей мере" означает один или более, например, один или два или три, предпочтительно, один или два.
В другом предпочтительном варианте отверждаемая композиция содержит, в качестве компонента (В), соединение формулы (I), где R2, R3, R4 и R5 независимо друг от друга являются Н; C1-C8алкилом; C5-C8циклоалкилом; C6-C18арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C4алкокси; C7-C10аралкил; NHR6, NR7R8, где R6, R7 и R8 независимо друг от друга являются C1-C4алкилом; C6-C12арилом; C6-C12арилом, который замещен C1-C4алкилом или C1-C4алкокси; C7-C10аралкилом; или R7 и R8 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 атомов всего;
или R2 и R3, R4 и R5 или R2 и R4 образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому они присоединены, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 7 атомов всего;
или два R5, которые связаны с соседними атомами углерода, образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому она присоединена, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 7 атомов в целом;
Предпочтительно, композиция содержит, в качестве компонента (В), соединение формулы (I), где R2, R3, R4 и R5 независимо друг от друга являются Н или C1-C4алкил, и p равно целому числу 1 или 2.
В другом предпочтительном варианте данное изобретение относится к композициям, содержащим, в качестве компонента (B), соединение формулы (I), где R1 является моно- или полициклической C2-C20кольцевой системой, выбранной из группы, включающей имидазол, бензимидазол, тиазол, бензотиазол, пиразол, оксазол, бензоксазол, изоксазол, изотиазол, 1,2,3-триазол, 1,2,4-триазол, тетразол, 1,2,4-оксадиазол, 1,2,4-тиадиазол, 1,3,4-оксадизаол, 1,3,4-тиадиазол, пиридин, хинолин, изохинолин, фенантридин, пиридазин, пиримидин, пиразин, циннолин, фталазин, хиназолин, хиноксалин, хиназолинон, 1,3,5-триазин, 1,2,4,5-тетразин, пурин, ксантин, гипоксантин, гуанин, аденин, птеридин, птерин, 1,10-фенантролин, 2,2'-бипиридин, 4,4'-бипиридин,
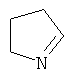 ,
, 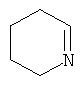 ,
, 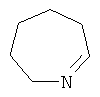 ,
, 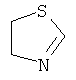 ,
, 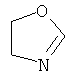 ,
, 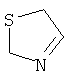 ,
,  ,
, 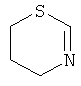 ,
, 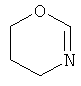 ,
, 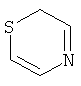 ,
,
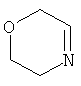
указанная кольцевая система не замещена или замещена C1-C8алкилом; C5-C7циклоалкилом; C6-C12арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C8алкокси; C1-C8алкокси, который замещен Е и/или прерывается D; C7-C11аралкилом; C7-C11аралкилом, который замещен G;
галогеном, OH, оксо, CN, NH2, NHR6, NR7R8, CONH2, CONR9R10, COR11, C(O)OR12, где R6, R7, R8, R9, R10, R11 и R12 независимо друг от друга являются C1-C8алкилом; C1-C8алкилом, который прерывается группой -О-; C6-C12арилом; C6-C12арилом, который замещен C1-C8алкилом или C1-C8алкокси; C7-C11аралкилом; C7-C11аралкилом, который замещен G;
или R7 и R8 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 атомов в целом;
или указанная кольцевая система далее конденсирована с одним или более бензольными кольцами.
Более предпочтительными являются композиции, содержащие, в качестве компонента (В), соединение формулы (I), где R1 является моно- или полициклической C1-C20 кольцевой системой, выбранной из группы, включающей имидазол, бензимидазол, тиазол, бензотиазол, оксазол, бензоксазол, изотиазол, пиридин, хинолин, изохинолин, фенантридин, пиридазин, пиримидин, пиразин, циннолин, фталазин, хиназолин, хиноксалин, пурин, 1,10-фенантролин, 2,2'-бипиридин и 4,4'-бипиридин;



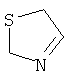

указанная кольцевая система не замещена или замещена C1-C4алкилом; фенилом; фенилом, который замещен C1-C4алкилом, C1-C4алкокси или галогеном; C1-C4алкокси; бензилом; фенэтилом; галогеном, ОН, NH2, NHR6, NR7R8, CONH2, CONR9R10, COR11, C(O)OR12, где R6, R7, R8, R9, R10, R11 и R12 независимо друг от друга являются C1-C4алкилом; фенилом; бензилом; фенэтилом;
или R7 и R8 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 6 атомов в целом;
или указанная кольцевая система далее конденсирована с одним или более бензольными кольцами.
В другом предпочтительном варианте данное изобретение относится к композициям, содержащим, в качестве компонента (В), соединение формулы (I), где n равно 1, и L является галогеном, OH, OR40, SR40, OCOR40, OCOOR41, OCONR42R43, OCSNR42R43, NR42R43, где R40, R42, R43 независимо друг от друга являются Н, C1-C8алкилом; фенилом; или бензилом.
Особенно предпочтительные композиции включают, в качестве компонента (В), соединение формулы (I), где n равно 1, и L является галогеном, ОН, OMe, SMe, NH2, NMe2, ОСОМе, OCOPh, OCOtBu, OCSNMe2, OCONMe2, OCONHMe, OCONHEt, OCONHPh, OCOOMe, OCOOtBu, OCOOPh, OCOOCH2Ph.
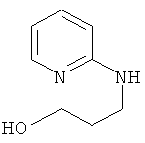
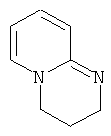
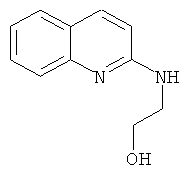
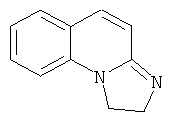
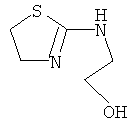
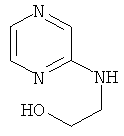
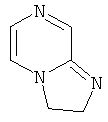
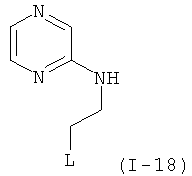
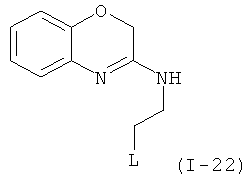
Примеры особенно подходящего термолатентного основания включают
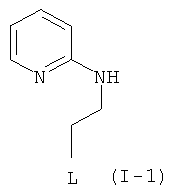 ,
, 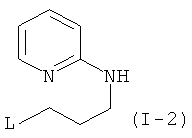 ,
,
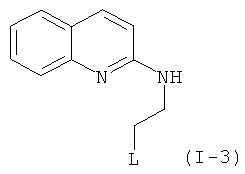 ,
, 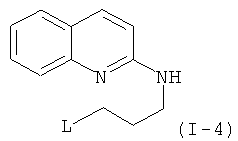 ,
, 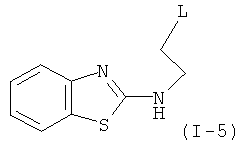 ,
, 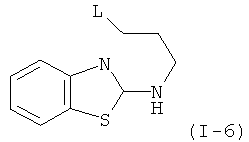 ,
,
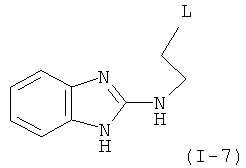 ,
, 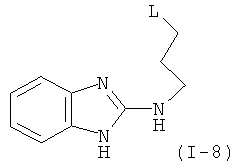 ,
, 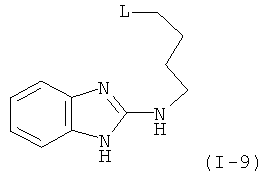 ,
, 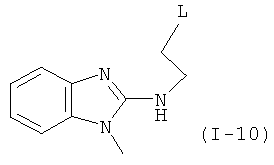 ,
,
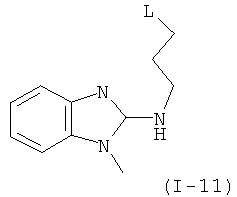 ,
, 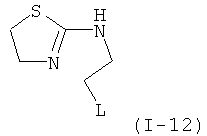 ,
, 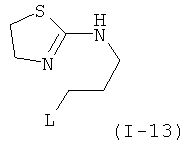 ,
, 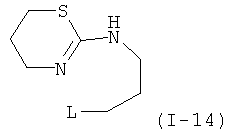 ,
,
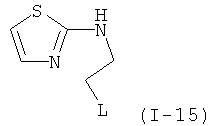 ,
, 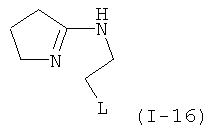 ,
, 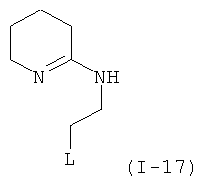 ,
, 
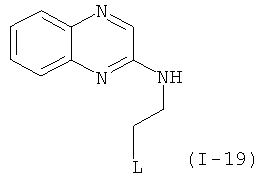 ,
, 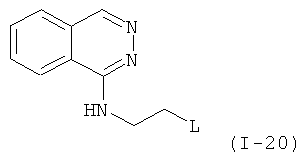 ,
, 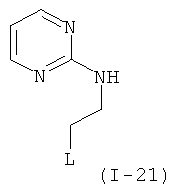 ,
, 
и
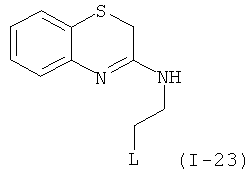 , где L является таким, как определен выше, предпочтительно, галогеном, OH, OMe, SMe, NH2, NMe2, ОСОМе, OCOPh, OCOtBu, OCSNMe2, OCONMe2, OCONHMe, OCONHEt, OCONHPh, OCOOMe, OCOOtBu, OCOOPh, OCOOCH2Ph.
, где L является таким, как определен выше, предпочтительно, галогеном, OH, OMe, SMe, NH2, NMe2, ОСОМе, OCOPh, OCOtBu, OCSNMe2, OCONMe2, OCONHMe, OCONHEt, OCONHPh, OCOOMe, OCOOtBu, OCOOPh, OCOOCH2Ph.
Примеры термолатентных оснований, где моно- или полициклическая C2-C20 кольцевая система замещена одной или более группами формулы
 , где R2, R3, R4, R5, L и p такие, как определены
, где R2, R3, R4, R5, L и p такие, как определены
выше, включают 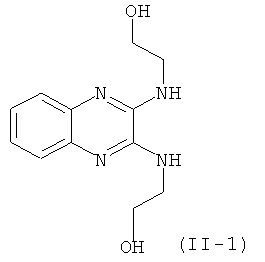 и
и 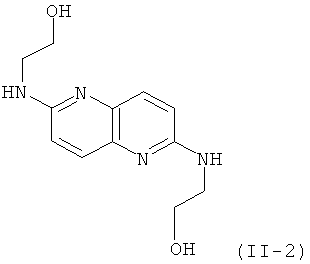
Превращение слабого термолатентного основания, соединения формулы (I), в выделенное или активированное основание, соединение формулы (V), согласно указанной выше схеме реакции, сопровождается повышением основности. В общем, соединения формулы (V) имеют значение рКа от 6 до 15, предпочтительно, от 8 до 15, и изменение рКа во время превращения составляет от около 2 до 8.
Например, повышение основновности может быть продемонстрировано данными рКа, рассчитанными с применением программного обеспечения Advanced Chemistry Development (ACD/Labs) Software V8.14 для Solaris, как показано в таблице 1.
|
Компонент (А), т.е. органический материал, который способен к полимеризации или поперечному сшиванию с основным или нуклеофильным катализатором, может, как правило, быть в виде моно- или полифункциональных мономеров, олигомеров или полимеров. Особенно предпочтительные олигомерные/полимерные системы являются связующими агентами или система для нанесения покрытий, обычно применяемыми в области покрытий.
Следовательно, в другом предпочтительном варианте, данное изобретение относится к отверждаемой композиции, где компонент (А) является одной из следующих систем:
a) акрилатные сополимеры, имеющие алкоксисилановые или алкоксисилоксановые боковые группы, например, полимеры, описанные в US-A-4772672 или US-A-4444974;
b) двухкомпонентные системы, включающие содержащие гидроксильные группы полиакрилаты, сложные полиэфиры и/или простые полиэфиры, и алифатические или ароматические полиизоцианаты;
c) двухкомпонентные системы, содержащие функциональные полиакрилаты и/или сложные полиэфиры и полиэпоксид, где полиакрилат и/или сложный полиэфир содержит карбоксильные или ангидридные группы;
d) двухкомпонентные системы, содержащие фтор-модифицированные или силикон-модифицированные, полиакрилаты, сложные полиэфиры и/или простые полиэфиры, имеющие гидроксильные группы, и алифатические или ароматические полиизоцианаты;
e) двухкомпонентные системы, содержащие (поли)кетимины и алифатические или ароматические полиизоцианаты;
f) двухкомпонентные системы, содержащие (поли)кетимины и ненасыщенные акрилатные смолы или ацетоацетатные смолы или метил а-акриламидометилгликолят;
h) двухкомпонентные системы, содержащие (поли)оксазолидины и полиакрилаты, содержащие ангидридные группы, или ненасыщенные акрилатные смолы или полиизоцианаты;
i) двухкомпонентные системы, содержащие эпоксисодержащие полиакрилаты и содержащие карбоксильные группы полиакрилаты или дикарбоновую кислоту, например, додекандикарбоновую кислоту;
l) полимеры на основе аллилглицидилового простого эфира;
m) двухкомпонентные системы, содержащие (поли)спирт и (поли)изоцианат;
n) двухкомпонентные системы, содержащие α,β-этиленненасыщеное карбонильное соединение и полимер, который содержит активированные СН2 группы, где активированные СН2 группы могут присутствовать либо в основной цепи, либо в боковой цепи, либо в обеих, как описано, например, в EP-В-O 161697 для (поли)малонатных групп. Другие соединение, имеющие активированные СН2 группы, включают (поли)ацетоацетаты и (поли)цианоацетаты.
Среди этих катализируемых основанием связующих агентов особенное предпочтение отдается следующим:
b) двухкомпонентные системы, содержащие полиакрилаты, сложные полиэфиры и/или простые полиэфиры, имеющие гидроксильные группы, и алифатические или ароматические полиизоцианаты;
c) двухкомпонентные системы, содержащие функциональные полиакрилаты и/или сложные полиэфиры и полиэпоксид, где полиакрилат и/или сложный полиэфир содержит карбоксильные или ангидридные группы;
i) двухкомпонентные системы, содержащие эпоксисодержащие полиакрилаты и содержащие карбоксильные группы полиакрилаты или дикарбоновую кислоту, например, додекандикарбоновую кислоту;
m) двухкомпонентные системы, содержащие (поли)спирт и (поли)изоцианат;
n) двухкомпонентные системы, содержащие α,β-этиленненасыщеное карбонильное соединение и полимер, который содержит активированные СН2 группы, где активированные СН2 группы могут присутствовать либо в основной цепи, либо в боковой цепи, либо в обеих, как описано, например, в EP-В-O 161697 для (поли)малонатных групп. Другие соединение, имеющие активированные СН2 группы, включают (поли)ацетоацетаты и (поли)цианоацетаты.
Двухкомпонентные системы, содержащие α,β-этиленненасыщенное карбонильное соединение и (поли)малонат, и их получение, описаны в ЕР-В-О 161697. Малонатная группа может быть присоединена в полиуретане, сложном полиэфире, полиакрилате, эпоксидной смоле, полиамиде или поливиниловом полимере, либо в основной цепи, либо в боковой цепи. Применяемое α,β-этиленненасыщенное карбонильное соединение может быть любой двойной связью, активированное карбонильной группой. Примеры включают сложные эфиры или амиды акриловой кислоты или метакриловой кислоты. В сложноэфирных группах также возможно присутствие дополнительных гидроксильных групп. Также возможны сложные диэфиры и сложные триэфиры.
Типичные примеры включают диакрилат гександиола или триакрилат триметилолпропана. Вместо акриловой кислоты также возможно применять другие кислоты и их сложные эфиры или амиды, такие как кротоновая или коричная кислота.
При основном катализе компоненты системы реагируют друг с другом с получением поперечно-сшитой системы для покрытия, которая подходит для множества применений. Благодаря хорошей характерной атмосферостойкости она подходит, например, для внешних применений, а также, при необходимости, может быть дополнительно стабилизирована поглотителями УФ излучения и другими светостабилизаторами.
Смеси указанных выше систем также возможны.
Другие системы, подходящие в качестве компонента (А) в новых композициях, включают эпоксидные системы. Эпоксидные смолы, подходящие для получения новых отверждаемых смесей, содержащих эпоксидные смолы в качестве компонента (А), включают смолы, обычно применяемые в технологии эпоксидных смол, где примеры таких эпоксидных смол включают:
I) Полиглицидиловые и поли(β-метилглицидиловые) сложные эфиры, получаемые взаимодействием соединения, имеющего, по меньшей мере, две карбоксильные группы в молекуле, с эпихлоргидрином или 3-метилэпихлоргидрином. Реакцию проводят в присутствии оснований. В качестве соединения, имеющего, по меньшей мере, две карбоксильные группы в молекуле, могут применяться алифатические поликарбоновые кислоты. Примеры таких поликарбоновых кислот включают щавелевую, янтарную, глутаровую, адипиновую, пимелиновую, пробковую, азелаиновую или димеризованную или тримеризованную линолевую кислоту. Однако также возможно применять циклоалифатические поликарбоновые кислоты, такие как тетрагидрофталевая, 4-метилтетрагидрофталевая, гексагидрофталевая или 4-метилгексагидрофталевая кислота. Также могут применяться поликарбоновые кислоты, такие как фталевая, изофталевая или терефталевая кислота.
II) Полиглицидиловые или поли(β-метилглицидиловые) простые эфиры, получаемые взаимодействием соединения, имеющего, по меньшей мере, две свободные спиртовые гидроксильные группы и/или фенольные гидроксильные группы, с эпихлоргидрином или β-метилэпихлоргидрином, в щелочных условиях или в присутствии кислотного катализатора, с последующей щелочной обработкой.
Глицидиловые простые эфиры такого типа получают, например, из ациклических спиртов, таких как этиленгликоль, диэтиленгликоль и высшие поли(оксиэтилен)гликоли, пропан-1,2-диол или
поли(оксипропилен) гликоли, пропан-1,3-диол, бутан-1,4-диол, поли(окситетраметилен)гликоли, петан-1,5-диол, гексан-1,6-диол, гексан-2,4,6-триол, глицерин, 1,1,1-триметилолпропан, пентаэритритол, сорбит, и из полиэпихлоргидринов. Их также получают из, например, циклоалифатических спиртов, таких как 1,4-циклогександиметанол, бис(4-гидроксициклогексил)метан или 2,2-бис(4-гидроксициклогексил)пропан, или обладающих ароматическим ядром, таких как N,N-бис(2-гидроксиэтил)анилин или р,р'-бис(2-гидроксиэтиламино)дифенилметан. Простые глицидиловые эфиры также могут быть получены из одноядерных фенолов, таких как резорцин или гидрохинон, или могут быть основаны на многоядерных фенолах, таких как бис(4-гидроксифенил)метан, 4,4'-дигидроксибифенил, бис(4-гидроксифенил)сульфон, 1,1,2,2-тетракис(4-гидроксифенил)этан, 2,2-бис(4-гидроксифенил)пропан, 2,2-бис(3,5-дибром-4-гидроксифенил)пропан и из новолаков, получаемых конденсацией альдегидов, таких как формальдегид, ацетальдегид, хлорал или фурфуральдегид, с фенолами, такими как фенол, или с фенолами, ядро которых замещено атомами хлора или C1-С9алкильными группами, где примеры включают 4-хлорфенол, 2-метилфенол или 4-трет-бутилфенол, или конденсацией с бисфенолами определенного выше типа.
III) Поли(N-глицидиловые) соединения, получаемые дегидрохлорированием продуктов реакции эпихлоргидрина с аминами, содержащими, по меньшей мере, две активные водородные связи с атомами азота амина. Эти амины включают, например, анилин, н-бутиламин, бис(4-аминофенил)метан, м-ксилилендиамин или бис(4-метиламинофенил)метан.
Поли(N-глицидиловые) соединения также включают изоцианурат триглицидила, N,N'-диглицидильные производные циклоалкиленмочевин, таких как этиленмочевина или 1,3-пропиленмочевина, и диглицидильные производные гидантоинов, таких как 5,5-диметилгидантоин.
IV) Поли(3-глицидильные) соединения, например ди-S-глицидильные производные, полученные из дитиолов, таких как этан-1,2-дитиол или бис(4-меркаптометилфениловый) простой эфир.
V) Циклоалифатические эпоксидные смолы, например, бис(2,3-эпоксициклопентиловый) простой эфир, 2,3-эпоксициклопентилглицидиловый простой эфир, 1,2-бис(2,3-эпоксициклопентилокси)этан или 3,4-эпоксициклогексилметил 3',4'-эпоксициклогексанкарбоксилат.
Однако также возможно применять эпоксидные смолы, в которых 1,2-эпоксидные группы присоединены к различным гетероатомам и/или функциональным группам; эти соединения включают, например, N,N,O-триглицидильную производную 4-аминофенола, простой глицидиловый эфир сложного глицидилового эфира салициловой кислоты, N-глицидил-N'-(2-глицидилоксипропил)-5,5-диметилгидантоин или 2-глицидилокси-1,3-бис(5,5-диметил-1-глицидилгидантоин-3-ил)пропан.
Смеси эпоксидных смол также применяют в качестве компонента (А).
Следовательно, в другом предпочтительном варианте, данное изобретение относится к композиции, где компонентом (А) является эпоксидная смола или смесь различных эпоксидных смол.
Обычно термолатентное основание может применяться в отверждаемой композиции в соответствии с данным изобретением в количестве от 0,01 до 15 мас.%, предпочтительно, от 0,1 до 10 мас.%, и более предпочтительно, от 0,1 до 2 мас.%, по отношению к массе компонента (А).
Компонент (В), т.е. термолатентное основание, может применяться отдельно или в виде комбинации двух или более. Также оно может применяться вместе с известными термолатентными основаниями в виде композиции. Примеры известных термолатентных оснований описаны в документах известного уровня техники.
Подходящие примеры термолатентных оснований могут включать N-алкоксикарбонилимидазолы, как описано в WO 98/04531, такие как 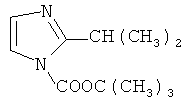 ,
, 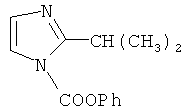 ,
, 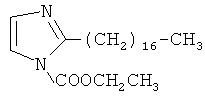 или производные имидазола, описанные в US-A-5623023.
или производные имидазола, описанные в US-A-5623023.
Также фотолатентное основание может быть добавлено в отверждаемую композицию в соответствии с данным изобретением. Примеры фотолатентных оснований включают блокированные аминосоединения например, соединения классов: о-нитробензилоксикарбониламинов, 3,5-диметокси-α,α-диметилбензилоксикарбониламинов, бензоинкарбаматов, производных анилидов, фотолатентных гуанидинов, в основном фотолатентных третичных аминов, например аммониевых солей кетокарбоновых кислот, или других карбоксилатов, бензгидриламмониевых солей, трифенилалкилборатов N-(бензофенонилметил)-три-N-алкиламмония, фотолатентных оснований на основе комплексов металлов, например, аминовых комплексов кобальта, комплексов вольфрама и пентакарбонила хрома пиридиния, образующих анион фотоинициаторов на основе металлов, таких как комплексы хрома и кобальта "соли Рейнеке", или металлопорфиринов. Примеры опубликованы в J.V.Crivello, K.Dietliker "Photoinitiators for Free Radical, Cationic & Anionic Photopolymerisation", Vol.III of "Chemistry & Technology of UV & EB Formulation for Coatings, Inks & Paints", 2nd Ed., J. Wiley and Sons/SITA Technology (London), 1998 или в WO 98/32756, WO 98/38195, WO 98/41524 и WO 00/10964.
Также, в качестве катализатора на основе фотолатентного основания для композиций в соответствии с данным изобретением, подходят основания, описанные в WO 97/31033. Особенно латентные основания на основе вторичных аминов, гуанидинов или амидинов. Также в качестве доноров фотолатентного основания подходят α-аминокетоновые соединения, описанные в EP-А-O 898202, например (4-морфолинобензоил)-1-бензил-1-диметиламинопропан или (4-метилтиобензоил)-1-метил-1-морфолиноэтан. Также представляющие интерес фотолатентные основные соединения включают соединения следующей структуры 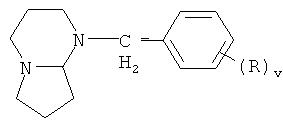 , например, описанные в WO 03/33500.
, например, описанные в WO 03/33500.
Фотолатентные основания обычно присутствуют в количестве от около 0 до 10 мас.%, предпочтительно, от 0,01 до 10 мас.%, и более предпочтительно, от 0,01 до 2 мас.%, по отношению к массе компонента (А).
Необязательно, термолатентное основание может применяться в сочетании с другим катализатором, обозначенным как компонент (С), например, другим основанием. Подходящие примеры включают ароматические амины, такие как имидазол или замещенные имидазолы, например, 2-метилимидазол, или пиридин, алифатические амины, такие как 2,2,6,6-тетраметилпиперидин, морфолин, пиперазин или пиперидин, или амидины, такие как 1,5-диазабицикло[4.3.0]нон-5-ен (ДБН), 1,8-диазабицикло[5.4.0]ундец-7-ен (ДБУ) или 1,4-диазабицикло[2.2.2]октан (ДАБЦО), или их смеси.
Дополнительный катализатор отверждения может присутствовать в отверждаемой композиции в соответствии с данным изобретением в количестве от 0 до 1 мас.%, предпочтительно, от 0,5 до 1 мас.%, по отношению к массе компонента (А).
В общем, отверждаемая композиция в соответствии с данным изобретением может включать, в качестве дополнительных добавок, т.е., компонента (D), одно или более соединений из группы, состоящей из пигментов, красителей, наполнителей, восков, выравнивателей, дегазаторов, агентов контроля заряда, оптических осветлителей, промоторов адгезии, антиоксидантов, светостабилизаторов, пластификаторов, реологических и тиксотропных агентов или фотоинициаторов. Композиция также может содержать ингибиторы коррозии, например, антикоррозийные пигменты, такие как фосфат- или боратсодержащие пигменты или пигменты на основе оксидов металлов, или другие органические или неорганические ингибиторы коррозии, например, соли нитроизофталевой кислоты, сложные эфиры фосфорной кислоты, технические амины или замещенные бензотриазолы. Дополнительные добавки обычно добавляют в количестве от 0 до 20 мас.%, предпочтительно, от 0,1 до 15 мас.%, по отношению к массе компонента (A).
Следовательно, в предпочтительном варианте данное изобретение относится к отверждаемой композиции, также содержащей
(C) катализатор отверждения, отличный от компонента (В) и
(D) по меньшей мере, одну добавку.
В более предпочтительном варианте данное изобретение относится к отверждаемой композиции, также содержащей
(C) катализатор отверждения, отличный от компонента (В) и
(D) по меньшей мере, одну добавку, выбранную из группы, включающей пигменты, красители, наполнители, воски, стабилизаторы, выравниватели, реологические и тиксотропные агенты, дегазаторы, агенты контроля заряда, оптические осветлители, промоторы адгезии, огнестойкие агенты и пластификаторы.
Примеры дополнительных добавок приведены ниже. 1. Антиоксиданты
1.1. Алкилированные монофенолы, например 2,6-ди-трет-бутил-4-метилфенол, 2-трет-бутил-4,6-ди-метилфенол, 2,6-ди-трет-бутил-4-этилфенол, 2,6-ди-трет-бутил-4-н-бутилфенол, 2,6-ди-трет-бутил-4-изобутилфенол, 2,6-дициклопентил-4-метилфенол, 2-(α-метил-циклогексил)-4,6-диметилфенол, 2,6-диоктадецил-4-метилфенол, 2,4,6-трициклогексилфенол, 2,6-ди-трет-бутил-4-метоксиметилфенол, нонилфенолы, которые являются линейными или разветвленными в боковых цепях, например 2,6-динонил-4-метилфенол, 2,4-диметил-6-(1'-метилундец-1'-ил)фенол, 2,4-диметил-6-(1'-метилгептадец-1'-ил)фенол, 2,4-диметил-6-(1'-метилтридец-1'-ил)фенол и их смеси.
1.2. Алкилтиометилфенолы, например 2,4-диоктилтиометил-6-трет-бутилфенол, 2,4-диоктилтиометил-6-метилфенол, 2,4-диоктилтиометил-6-этилфенол, 2,6-ди-додецилтиометил-4-нонилфенол.
1.3. Гидрохиноны и алкилированные гидрохиноны, например 2,6-ди-трет-бутил-4-метоксифенол, 2,5-ди-трет-бутилгидрохинон, 2,5-ди-трет-амилгидрохинон, 2,6-дифенил-4-октадецилоксифенол, 2,6-ди-трет-бутилгидрохинон, 2,5-ди-трет-бутил-4-гидроксианизол, 3,5-ди-трет-бутил-4-гидроксианизол, стеарат 3,5-ди-трет-бутил-4-гидроксифенила, адипат бис-(3,5-ди-трет-бутил-4-гидроксифенила).
1.4. Токоферолы, например α-токоферол, β-токоферол, γ-токоферол, δ-токоферол и их смеси (витамин E).
1.5. Гидроксилированные простые эфиры тиодифенила, например 2,2'-тиобис(6-трет-бутил-4-метилфенол), 2,2'-тиобис(4-октилфенол), 4,4'-тиобис(6-трет-бутил-3-метилфенол), 4,4'-тиобис(6-трет-бутил-2-метилфенол), 4,4'-тиобис-(3,6-ди-втор-амилфенол), 4,4'-бис(2,6-диметил-4-гидроксифенил)дисульфид.
1.6. Алкилиденбисфенолы, например 2,2-метиленбис(6-трет-бутил-4-метилфенол), 2,2-метиленбис(6-трет-бутил-4-этилфенол), 2,2'-метиленбис[4-метил-6-(α-метилциклогексил)фенол], 2,2'-метиленбис(4-метил-6-циклогексилфенол), 2,2'-метиленбис(6-нонил-4-метилфенол), 2,2'-метиленбис(4,6-ди-трет-бутилфенол), 2,2'-этилиденбис(4,6-ди-трет-бутилфенол), 2,2'-этилиденбис(6-трет-бутил-4-изобутилфенол), 2,2'-метиленбис[6-(α-метилбензил)-4-нонилфенол], 2,2'-метиленбис[6-(α,α-диметилбензил)-4-нонилфенол], 4,4-метиленбис(2,6-ди-трет-бутилфенол), 4,4-метиленбис(6-трет-бутил-2-метилфенол), 1,1-бис(5-трет-бутил-4-гидрокси-2-метилфенил)бутан, 2,6-бис(3-трет-бутил-5-метил-2-гидрокси-бензил)-4-метилфенол, 1,1,3-трис(5-трет-бутил-4-гидрокси-2-метилфенил)-бутан, 1,1-бис(5-трет-бутил-4-гидрокси-2-метилфенил)-3-н-додецилмер-каптобутан, бис[3,3-бис(3'-трет-бутил-4'-гидроксифенил)бутират]этилен-гликоля, бис(3-трет-бутил-4-гидрокси-5-метилфенил)дициклопентадиен, бис[2-(3'-трет-бутил-2'-гидрокси-5'-метилбензил)-6-трет-бутил-4-метилфенил]терефталат, 1,1-бис-(3,5-диметил-2-гидроксифенил)бутан, 2,2-бис-(3,5-ди-трет-бутил-4-гидроксифенил)пропан, 2,2-бис-(5-трет-бутил-4-гидрокси-2-метилфенил)-4-н-додецилмеркаптобутан, 1,1,5,5-тетра(5-трет-бутил-4-гидрокси-2-метилфенил)пентан.
1.7. O-, H- и S-бензильные соединения, например 3,5,3',5'-тетра-трет-бутил-4,4'-дигидроксидибензиловый простой эфир, октадецил-4-гидрокси-3,5-диметилбензилмеркаптоацетат, тридецил-4-гидрокси-3,5-ди-трет-бутилбензилмеркаптоацетат, трис(3,5-ди-трет-бутил-4-гидроксибензил)-амин, бис(4-трет-бутил-3-гидрокси-2,6-диметилбензил)дитиотерефталат, бис(3,5-ди-трет-бутил-4-гидроксибензил)сульфид, изооктил-3,5-ди-трет-бутил-4-гидроксибензилмеркаптоацетат.
1.8. Гидроксибензилированные малонаты, например диоктадецил-2,2-бис-(3,5-ди-трет-бутил-2-гидроксибензил)малонат, диоктадецил-2-(3-трет-бутил-4-гидрокси-5-метилбензил)малонат, дидодецилмеркаптоэтил-2,2-бис-(3,5-ди-трет-бутил-4-гидроксибензил)малонат, бис[4-(1,1,3,3-тетра-метилбутил)фенил]-2,2-бис(3,5-ди-трет-бутил-4-гидроксибензил)малонат.
1.9. Ароматические гидроксибензильные соединения, например 1,3,5-трис-(3,5-ди-трет-бутил-4-гидроксибензил)-2,4,6-триметилбензол, 1,4-бис(3,5-ди-трет-бутил-4-гидроксибензил)-2,3,5,6-тетраметилбензол, 2,4,6-трис(3,5-ди-трет-бутил-4-гидроксибензил)фенол.
1.10. Соединения триазина, например 2,4-бис(октилмеркапто)-6-(3,5-ди-трет-бутил-4-гидроксианилино)-1,3,5-триазин, 2-октилмеркапто-4,6-бис(3,5-ди-трет-бутил-4-гидроксианилино)-1,3,5-триазин, 2-октилмеркапто-4,6-бис(3,5-ди-трет-бутил-4-гидроксифенокси)-1,3,5-триазин, 2,4,6-трис-(3,5-ди-трет-бутил-4-гидроксифенокси)-1,2,3-триазин, 1,3,5-трис-(3,5-ди-трет-бутил-4-гидроксибензил)изоцианурат, 1,3,5-трис(4-трет-бутил-3-гидрокси-2,6-диметилбензил)изоцианурат, 2,4,6-трис-(3,5-ди-трет-бутил-4-гидроксифенилэтил)-1,3,5-триазин, 1,3,5-трис(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гексагидро-1,3,5-триазин, 1,3,5-трис(3,5-дициклогексил-4-гидроксибензил)изоцианурат.
1.11. Бензил Фосфонаты, например диметил-2,5-ди-трет-бутил-4-гидроксибензилфосфонат, диэтил-3,5-ди-трет-бутил-4-гидроксибензилфосфонат, диоктадецил-3,5-ди-трет-бутил-4-гидроксибензилфосфонат, диоктадецил-5-трет-бутил-4-гидрокси-3-метилбензилфосфонат, кальциевая соль моноэтилового сложного эфира 3,5-ди-трет-бутил-4-гидроксибензилфосфоновой кислоты.
1.12. Ациламинофенолы, например 4-гидроксилауранилид, 4-гидроксистеаранилид, октил N-(3,5-ди-трет-бутил-4-гидроксифенил)карбамат.
1.13. Сложные эфиры β-(3,5-ди-трет-бутил-4-гидроксифенил)пропионовой кислоты с моно- или многоядерными спиртами, например, с метанолом, этанолом, н-октанолом, изо-октанолом, октадеканолом, 1,6-гександиолом, 1,9-нонандиолом, этиленгликолем, 1,2-пропандиолом, неопентилгликолем, тиодиэтиленгликолем, диэтиленгликолем, триэтиленгликолем, пентаэритритолом, трис(гидроксиэтил)изоциануратом, N,N'-бис(гидрокси-этил)оксамидом, 3-тиаундеканолом, 3-тиапентадеканолом, триметил-гександиолом, триметилолпропаном, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октаном.
1.14. Сложные эфиры β-(5-трет-бутил-4-гидрокси-3-метилфенил)пропионовой кислоты с моно- или многоядерными спиртами, например, с метанолом, этанолом, н-октанолом, изо-октанолом, октадеканолом, 1,6-гександиолом, 1,9-нонандиолом, этиленгликолем, 1,2-пропандиолом, неопентилгликолем, тиодиэтиленгликолем, диэтиленгликолем, триэтиленгликолем, пентаэритритолом, трис(гидроксиэтил) изоциануратом, N,N'-бис-(гидроксиэтил)оксамидом, 3-тиаундеканолом, 3-тиапентадеканолом, триметилгександиолом, триметилолпропаном, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октаном; 3,9-бис[2-{3-(3-трет-бутил-4-гидрокси-5-метилфенил)пропионилокси}-1,1-диметилэтил]-2,4,8,10-тетраоксаспиро[5.5]-ундеканом.
1.15. Сложные эфиры β-(3,5-дициклогексил-4-гидроксиФенил)пропионовой кислоты с моно- или многоядерными спиртами, например, с метанолом, этанолом, октанолом, октадеканолом, 1,6-гександиолом, 1,9-нонандиолом, этиленгликолем, 1,2-пропандиолом, неопентилгликолем, тиодиэтиленгликолем, диэтиленгликолем, триэтиленгликолем, пентаэритритолом, трис(гидроксиэтил)изоциануратом, N,N'-бис(гидроксиэтил)оксамидом, 3-тиаундеканолом, 3-тиапентадеканолом, триметилгександиолом, триметилолпропаном, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октаном.
1.16. Сложные эфиры 3,5-ди-трет-бутил-4-гидроксифенилуксуной кислоты с моно- или многоядерными спиртами, например, с метанолом, этанолом, октанолом, октадеканолом, 1,6-гександиолом, 1,9-нонандиолом, этиленгликолем, 1,2-пропандиолом, неопентилгликолем, тиодиэтилен-гликолем, диэтиленгликолем, триэтиленгликолем, пентаэритритолом, трис(гидроксиэтил)изоциануратом, N,N'-бис(гидроксиэтил)оксамидом, 3-тиаундеканолом, 3-тиапентадеканолом, триметилгександиолом, триметилолпропаном, 4-гидроксиметил-1-фосфа-2,6,7-триоксабицикло[2.2.2]октаном.
1.17. Амиды 3-(3,5-ди-трет-бутил-4-гидроксифенил)пропионовой кислоты, например, N,N'-бис(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гексаметилендиамид, N,N'-бис(3,5-ди-трет-бутил-4-гидроксифенилпропионил)триметилендиамид, N,N'-бис(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гидразид, N,N'-бис[2-(3-[3,5-ди-трет-бутил-4-гидроксифенил]пропионилокси)этил]оксамид (Naugard®XL-1, поставляется Uniroyal).
1.18. Аскорбиновая кислота (витамин С)
1.19. Аминные антиоксиданты, например N,N'-ди-изопропил-п-фенилендиамин, N,N'-ди-втор-бутил-п-фенилендиамин, N,N'-бис(1,4-диметилпентил)-п-фенилендиамин, N,N'-бис(1-этил-3-метилпентил)-п-фенилендиамин, N,N'-бис(1-метилгептил)-п-фенилендиамин, N,N'-дициклогексил-п-фенилендиамин, N,N'-дифенил-п-фенилендиамин, N,N'-бис(2-нафтил)-п-фенилендиамин, N-изопропил-N'-фенил-п-фенилендиамин, N-(1,3-диметилбутил)-N'-фенил-п-фенилендиамин, N-(1-метил гептил)-N'-фенил-п-фенилендиамин, N-циклогексил-N'-фенил-п-фенилен-диамин, 4-(п-толуолсульфамоил)дифениламин, N,N'-диметил-N,N'-ди-втор-бутил-п-фенилендиамин, дифениламин, N-аллилдифениламин, 4-изопропоксидифениламин, N-фенил-1-нафтиламин, N-(4-трет-октилфенил)-1-нафтиламин, N-фенил-2-натиламин, октилированный дифениламин, например р,р'-ди-трет-октилдифениламин, 4-н-бутил-аминофенол, 4-бутуриламинофенол, 4-нонаноиламинофенол, 4-додеканоиламинофенол, 4-октадеканоиламинофенол, бис(4-метокси-фенил)амин, 2,6-ди-трет-бутил-4-диметиламинометилфенол, 2,4'-диаминодифенилметан, 4,4'-диаминодифенилметан, N,N,N',N'-тетра-метил-4,4'-диаминодифенилметан, 1,2-бис[(2-метилфенил)амино]этан, 1,2-бис(фениламино)пропан, (о-толил)бигуанид, бис[4-(1',3'-диметилбутил)-фенил]амин, трет-октилированный N-фенил-1-нафтиламин, смесь моно- и диалкилированных трет-бутил/трет-октилдифениламинов, смесь моно- и диалкилированных нонилдифениламинов, смесь моно- и диалкилированных додецилдифениламинов, смесь моно- и диалкилированных изопропил/изогексилдифениламинов, смесь моно- и диалкилированных трет-бутилдифениламинов, 2,3-дигидро-3,3-диметил-4Н-1,4-бензотиазин, фенотиазин, смесь моно- и диалкилированных трет-бутил/трет-октилфенотиазинов, смесь моно- и диалкилированных трет-октилфенотиазинов, N-аллилфенотиазин, N,N,N',N'-тетрафенил-1,4-диаминобут-2-ен, N,N-бис(2,2,6,6-тетраметилпиперид-4-илгексаметилен-диамин, бис(2,2,6,6-тетраметилпиперид-4-ил)себакат, 2,2,6,6-тетраметил-пиперидин-4-он, 2,2,6,6-тетраметилпиперидин-4-ол.
2. Поглотители УФ излучения и светостабилизаторы
2.1. 2-(2'-Гидроксифенил)бензотриазолы, например 2-(2'-гидрокси-5'-метилфенил)бензотриазол, 2-(3',5'-ди-трет-бутил-2,-гидроксифенил)бензотриазол, 2-(5'-трет-бутил-2'-гидроксифенил)бензотриазол, 2-(2'-гидрокси-5'-(1,1,3,3-тетраметилбутил)фенил)бензотриазол, 2-(3,,5,-ди-трет-бутил-2'-гидроксифенил)-5-хлорбензотриазол, 2-(3'-трет-бутил-2'-гидрокси-5,-метил-фенил)-5-хлор-бензотриазол, 2-(3'-втор-бутил-5,-трет-бутил-2,-гидроксифе-нил)бензотриазол, 2-(2'-гидрокси-4'-октилоксифенил)бензотриазол, 2-(3',5'-ди-трет-амил-2'-гидроксифенил)бензотриазол, 2-(3',5'-бис-(α,α-диметилбензил)-2'-гидроксифенил)бензотриазол, 2-(3'-трет-бутил-2'-гидрокси-5,-(2-октилоксикарбонилэтил)фенил)-5-хлорбензотриазол, 2-(3'-трет-бутил-5'-[2-(2-этилгексилокси)карбонилэтил]-2'-гидроксифенил)-5-хлорбензотриазол, 2-(3'-трет-бутил-2'-гидрокси-5,-(2-метоксикарбонилэтил)фенил)-5-хлорбен-зотриазол, 2-(3'-трет-бутил-2'-гидрокси-5'-(2-метоксикарбонилэтил)фенил)-бензотриазол, 2-(3'-трет-бутил-2,-гидрокси-5'-(2-октилоксикарбонилэтил)-фенил)бензотриазол, 2-(3'-трет-бутил-5'-[2-(2-этилгексилокси)карбонил-этил]-2'-гидроксифенил)бензотриазол, 2-(3'-додецил-2'-гидрокси-5'-метилфенил)бензотриазол, 2-(3'-трет-бутил-2,-гидрокси-5'-(2-изооктилокси-карбонилэтил)фенилбензотриазол, 2,2'-метилен-бис[4-(1,1,3,3-тетраме-тилбутил)-6-бензотриазол-2-илфенол]; продукт трансэстерификации 2-[3'-трет-бутил-5'-(2-метоксикарбонилэтил)-2,-гидроксифенил]-2Н- бензотриазола с полиэтиленгликолем 300; 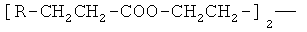 , где R=3'-трет-бутил-4'-гидрокси-5'-2H-бензотриазол-2-илфенил, 2-[2'-гидрокси-3'-(α,α-диметилбензил)-5'-(1,1,3,3-тетраметилбутил)фенил]бензо-триазол; 2-[2'-гидрокси-3'-(1,1,3,3-тетраметилбутил)-5'-(α,α-диметилбензил)фенил]бензотриазол.
, где R=3'-трет-бутил-4'-гидрокси-5'-2H-бензотриазол-2-илфенил, 2-[2'-гидрокси-3'-(α,α-диметилбензил)-5'-(1,1,3,3-тетраметилбутил)фенил]бензо-триазол; 2-[2'-гидрокси-3'-(1,1,3,3-тетраметилбутил)-5'-(α,α-диметилбензил)фенил]бензотриазол.
2.2. 2-Гидроксибензофеноны, например производные 4-гидрокси, 4-метокси, 4-октилокси, 4-децилокси, 4-додецилокси, 4-бензилокси, 4,2',4'-тригидрокси и 2'-гидрокси-4,4'-диметокси.
2.3. Сложные эфиры замещенных и незамещенных бензойных кислот, например салицилат 4-трет-бутилфенила, салицилат фенила, салицилат октилфенила, дибензоилрезорцин, бис(4-трет-бутилбензоил)резорцин, бензоилрезорцин, 2,4-ди-трет-бутилфенил 3,5-ди-трет-бутил-4-гидроксибензоат, гексадецил 3,5-ди-трет-бутил-4-гидроксибензоат, октадецил 3,5-ди-трет-бутил-4-гидроксибензоат, 2-метил-4,6-ди-трет-бутилфенил 3,5-ди-трет-бутил-4-гидроксибензоат.
2.4. Акрилаты, например этил α-циано-β,β-дифенилакрилат, изооктил α-циано-β,β-дифенилакрилат, метил α-карбометоксициннамат, метил α-циано-β-метил-п-метоксициннамат, бутил α-циано-β-метил-п-метоксициннамат, метил α-карбометокси-п-метоксициннамат и N-(β-карбометокси-β-циановинил)-2-метилиндолин.
2.5. Соединения никеля, например комплексы никеля с 2,2'-тио-бис-[4-(1,1,3,3-тетраметилбутил)фенолом], такие как 1:1 или 1:2 комплекс, с или без дополнительных лигандов, таких как н-бутиламин, триэтаноламин или N-циклогексилдиэтаноламин, дибутилдитиокарбамат никеля, никелевая соль сложных эфиров моноалкила, например, метиловый или этиловый эфир 4-гидрокси-3,5-ди-трет-бутилбензилфосфоновой кислоты, комплексы никеля с кетоксимами, например, 2-гидрокси-4-метилфенилун-децилкетоксимом, комплексы никеля с 1-фенил-4-лауроил-5-гидроксипиразолом, с или без дополнительных лигандов.
2.6. Пространственно затрудненные амины, например бис(2,2,6,6-тетраметил-4-пиперидил)себакат, бис(2,2,6,6-тетраметил-4-пиперидил)сукцинат, бис(1,2,2,6,6-пентаметил-4-пиперидил)себакат, бис(1-октилокси-2,2,6,6-тетраметил-4-пиперидил)себакат, бис(1,2,2,6,6-пентаметил-4-пиперидил)н-бутил-3,5-ди-трет-бутил-4-гидроксибензилма-лонат, конденсат 1-(2-гидроксиэтил)-2,2,6,6-тетраметил-4-гидрокси-пиперидина и янтарной кислоты, линейные или циклические конденсаты N,N'-бис(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамина и 4-трет-октиламино-2,6-дихлор-1,3,5-триазина, трис(2,2,6,6-тетраметил-4-пиперидил)нитрилотриацетат, тетракис(2,2,6,6-тетраметил-4-пиперидил)-1,2,3,4-бутантетракарбоксилат, 1,1'-(1,2-этандиил)бис(3,3,5,5-тетраметилпи-перазинон), 4-бензоил-2,2,6,6-тетраметилпиперидин, 4-стеарилокси-2,2,6,6-тетраметилпиперидин, бис(1,2,2,6,6-пентаметилпиперидил)-2-н-бутил-2-(2-гидрокси-3,5-ди-трет-бутилбензил)малонат, 3-н-октил-7,7,9,9-тетраметил-1,3,8-триазаспиро[4.5]декан-2,4-дион, бис(1-октилокси-2,2,6,6-тетраметилпиперидил)себакат, бис(1-октилокси-2,2,6,6-тетраметилпи-перидил)сукцинат, линейные или циклические конденсаты N,N'-бис-(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамин и 4-мрфолино-2,6-дихлор-1,3,5-триазин, конденсат 2-хлор-4,6-бис(4-н-бутиламино-2,2,6,6-тетраметилпиперидил)-1,3,5-триазина и 1,2-бис(3-аминопропил-амино)этана, конденсат 2-хлор-4,6-ди-(4-н-бутиламино-1,2,2,6,6-пентаметилпиперидил)-1,3,5-триазина и 1,2-бис-(3-аминопропиламино)этана, 8-ацетил-3-додецил-7,7,9,9-тетраметил-1,3,8-триазаспиро[4.5]декан-2,4-дион, 3-додецил-1-(2,2,6,6-тетраметил-4-пиперидил)пирролидин-2,5-дион, 3-додецил-1-(1,2,2,6,6-пентаметил-4-пиперидил)пирролидин-2,5-дион, смесь 4-гексадецилокси- и 4-стеарилокси-2,2,6,6-тетраметилпиперидин, конденсат N,N'-бис(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамина и 4-циклогексиламино-2,6-дихлор-1,3,5-триазина, конденсат 1,2-бис(3-аминопропиламино)этана и 2,4,6-трихлор-1,3,5-триазина, а также 4-бутиламино-2,2,6,6-тетраметилпиперидин (CAS Reg. No. [136504-96-6]); конденсат 1,6-гександиамина и 2,4,6-трихлор-1,3,5-триазина, а также N,N-дибутиламина и 4-бутиламино-2,2,6,6-тетраметилпиперидина (CAS Reg. No. [192268-64-7]); N-(2,2,6,6-тетраметил-4-пиперидил)-н-додецилсукцинимид, N-(1,2,2,6,6-пентаметил-4-пиперидил)-н-додецилсукцинимид, 2-ундецил-7,7,9,9-тетраметил-1-окса-3,8-диаза-4-оксоспиро[4,5]декан, продукт реакции 7,7,9,9-тетраметил-2-циклоундецил-1-окса-3,8-диаза-4-оксоспиро-[4,5]декана и эпихлоргидрина, 1,1-бис(1,2,2,6,6-пентаметил-4-пиперидилоксикарбонил)-2-(4-метоксифенил)этен, N,N'-бисформил-N,N'-бис(2,2,6,6-тетраметил-4-пиперидил)гексаметилендиамин, сложный диэфир 4-метоксиметиленмалоновой кислоты с 1,2,2,6,6-пентаметил-4-гидроксипиперидином, поли[метилпропил-3-окси-4-(2,2,6,6-тетраметил-4-пиперидил)]силоксан, продукт реакции сополимера α-олефин - ангидрид малеиновой кислоты с 2,2,6,6-тетраметил-4-аминопиперидином или 1,2,2,6,6-пентаметил-4-аминопиперидином.
2.7. Оксамиды, например 4,4'-диоктилоксиоксанилид, 2,2'-диэтоксиоксанилид, 2,2'-диоктилокси-5,5'-ди-трет-бутоксанилид, 2,2'-дидодецилокси-5,5'-ди-трет-бутоксанилид, 2-этокси-2'-этилоксанилид, N,N'-бис(3-диметиламинопропил)оксамид, 2-этокси-5-трет-бутил-2'-этоксанилид и его смесь с 2-этокси-2'-этил-5,4'-ди-трет-бутоксанилидом, смеси о- и п-метоксидизамещенных оксанилидов и смеси о- и п-этоксидизамещенных оксанилидов.
2.8. 2-(2-ГидроксиФенил)-1,3.5-триазины. например 2,4,6-трис(2-гидрокси-4-октилоксифенил)-1,3,5-триазин, 2-(2-гидрокси-4-октилоксифенил)-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-(2,4-дигидроксифенил)-4,6-бис(2,4-диметилфенил)-1,3,5-триазин, 2,4-бис(2-гидрокси-4-пропилоксифенил)-6-(2,4-диметилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-октилоксифенил)-4,6-бис(4-метилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-додецилоксифенил)-4)6-бис(2,4-диметилфенил)-1,3,5-триазин, 2-(2-гидрокси-4-триде-цилоксифенил)-4)6-бис(2,4-диметилфенил)-1,315-триазин, 2-[2-гидрокси-4-(2-гидрокси-3-бутилоксипропокси)фенил]-4,6-бис(2,4-диметил)-1,3,5-триазин, 2-[2-гидрокси-4-(2-гидрокси-3-октилоксипропилокси)фенил]-4,6-бис(2,4-диметил)-1,3,5-триазин, 2-[4-(додецилокси/тридецилокси-2-гидроксипропокси)-2-гидроксифенил]-4,б-бис(2,4-диметилфенил)-1,3,5-триазин, 2-[2-гидрокси-4-(2-гидрокси-3-додецилоксипропокси)фенил]-4,6-бис(2,4-диметилфенил)-,3,5-триазин, 2-(2-гидрокси-4-гексилокси)фенил-4,6-дифенил-1,3,5-триазин, 2-(2-гидрокси-4-метоксифенил)-4,6-дифенил-1,3,5-триазин, 2,4,6-трис[2-гидрокси-4-(3-бутокси-2-гидроксипропокси)фенил]-1,3,5-триазин, 2-(2-гидроксифенил)-4-(4-метоксифенил)-6-фенил-1,3,5-триазин, 2-{2-гидрокси-4-[3-(2-этилгексил-1-окси)-2-гидроксипропилокси]фенил}-4,6-бис(2,4-диметилфенил)-1,3,5-триазин.
3. Деактиваторы металлов, например N,N'-дифенилоксамид, N-салицилаль-N'-салицилоилгидразин, N,N'-бис(салицилоил)гидразин, N,N'-бис(3,5-ди-трет-бутил-4-гидроксифенилпропионил)гидразин, 3-сали-цилоиламино-1,2,4-триазол, бис(бензилиден)оксалилдигидразид, оксанилид, изофталоилдигидразид, себакоилбисфенилгидразид, N,N'-диацетиладипоилдигидразид, N,N'-бис(салицилоил)оксалилдигидразид, N,N'-бис(салицилоил)тиопропионилдигидразид.
4. Фосфиты и фосфониты, например трифенилфосфит, дифенилалкилфосфиты, фенилдиалкилфосфиты, трис(нонилфенил)-фосфит, трилаурилфосфит, триоктадецилфосфит, дистеарилпентаэритритолдифосфит, трис(2,4-ди-трет-бутилфенил)фосфит, диизодецилпентаэритритолдифосфит, бис(2,4-ди-трет-бутилфенил)пентаэритритолдифосфит, бис(2,4-ди-кумилфенил)пентаэритритолдифосфит, бис(2,6-ди-трет-бутил-4-метилфенил)пентаэритритолдифосфит, диизодецилоксипентаэритритолдифосфит, бис(2,4-ди-трет-бутил-6-метилфенил)пента-эритритолдифосфит, бис(2,4,6-трис(трет-бутилфенил)пентаэритритол-дифосфит, тристеарилсорбиттрифосфит, тетракис(2,4-ди-трет-бутилфенил) 4,4'-бифенилен дифосфонит, 6-изооктилокси-2,4,8,10-тетра-трет-бутил-12Н-дибенз[d,g]-1,3,2-диоксафосфоцин, бис(2,4-ди-трет-бутил-6-метилфенил)метилфосфит, бис(2,4-ди-трет-бутил-6-метилфенил)этил-фосфит, 6-фтор-2,4,8,10-тетра-трет-бутил-12-метилдибенз[d,g]-1,3,2-диоксафосфоцин, 2,2',2''-нитрило[триэтилтрис(3,3',5,5'-тетра-трет-бутил-1,1,-бифенил-2,2'-диил)фосфит], 2-этилгексил(3,3',5,5'-тетра-трет-бутил-1,1'-бифенил-2,2'-диил)фосфит, 5-бутил-5-этил-2-(2,4,6-три-трет-бутил-фенокси)-1,3,2-диоксафосфиран.
Особенно предпочтительны следующие фосфиты:
Трис(2,4-ди-трет-бутилфенил) фосфит (Irgafos®168, Ciba-Geigy), трис(нонилфенил)фосфит,
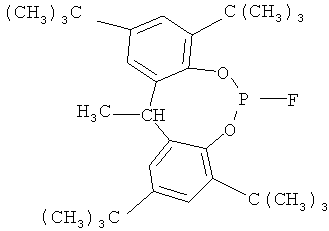 ,
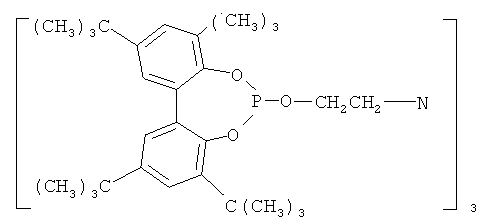
, 
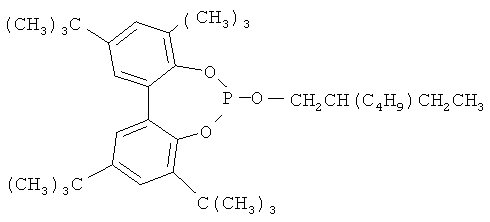 ,
,
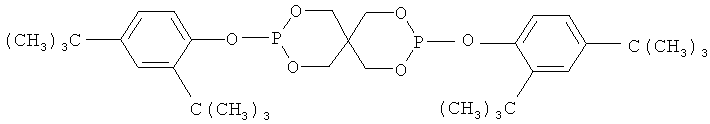 ,
,
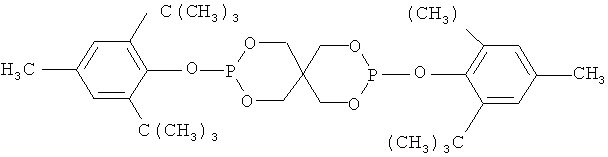 ,
,
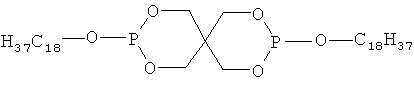 и
и 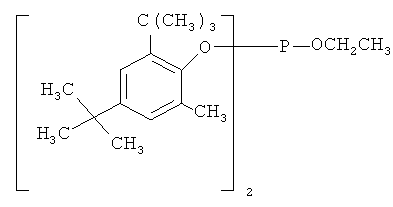 .
.
5. Гидроксиламины, например N,N-дибензилгидроксиламин, N,N-дизтилгидроксиламин, N,N-диоктилгидроксиламин, N,N-дилаурилгидроксиламин, N,N-дитетрадецилгидроксиламин, N,N-дигексадецилгидроксиламин, N,N-диоктадецилгидроксиламин, N-гексадецил-N-октадецилгидроксиламин, N-гептадецил-N-октадецил-гидроксиламин, N,N-диалкилгидроксиламин, полученный из гидрированного таллового амина.
6. Нитроны, например N-бензил-альфа-фенилнитрон, N-этил-альфа-метилнитрон, N-октил-альфа-гептилнитрон, N-лаурил-альфа-ундецилнитрон, N-тетрадецил-альфа-тридецилнитрон, N-гексадецил-альфа-пентадецилнитрон, N-октадецил-альфа-гептадецилнитрон, N-гексадецил-альфа-гептадецилнитрон, N-октадецил-альфа-пентадецилнитрон, N-гептадецил-альфа-гептадецилнитрон, N-октадецил-альфа-гексадецилнитрон, нитрон, полученный из N,N-диалкилгидроксиламина, полученного из гидрированного таллового амин.
7. Тиосинергетики, например дилаурилтиодипропионат или дистеарилтиодипропионат.
8. Акцепторы перекиси, например сложные эфиры β-тиодипропионовой кислоты, например, лауриловый, стеариловый, миристиловый или тридециловый сложные, меркаптобензимидазол или цинковая соль 2-меркаптобензимидазола, дибутилдитиокарбамат цинка, дисульфид диоктадецила, тетракис(β-додецилмеркапто)пропионат пентаэритритола.
9. Полиамидные стабилизаторы, например соли меди в комбинации с йодидами и/или соединениями фосфора и соли двухвалентного марганца.
10. Основные co-стабилизаторы, например меламин, поливинилпирролидон, дициандиамид, триаллилцианурат, производные мочевины, производные гидразина, амины, полиамиды, полиуретаны, соли щелочных металлов и соли щелочноземельных металлов и высших жирных кислот, например, стеарат кальция, стеарат цинка, бегенат магния, стеарат магния, рицинолеат натрия и пальмитат калия, пирокатехолат сурьмы или пирокатехолат цинка.
11. Зародыши кристаллизации, например, неорганические вещества, такие как тальк, оксиды металлов, такие как двуокись титана или оксид магния, фосфаты, карбонаты или сульфаты, предпочтительно, щелочноземельных металлов; органические соединения, такие как моно- или поликарбоновые кислоты и их соли, например, 4-трет-бутилбензойная кислота, адипиновая кислота, дифенилуксусная кислота, сукцинат натрия или бензоат натрия; полимерные соединения, такие как ионные сополимеры (иономеры). Особенно предпочтительными являются 1,3:2,4-бис(3',4'-диметилбензилиден)сорбит, 1,3:2,4-ди(параметилдибензилиден)сорбит и 1,3:2,4-ди(бензилиден)сорбит.
12. Наполнители и усиливающие агенты, например карбонат кальция, силикаты, стекловолокно, стеклянная бульба, асбест, тальк, каолин, слюда, сульфат бария, оксиды и гидроксиды металлов, сажа, графит, древесная мука или волокна других природных продуктов, синтетические волокна.
13. Другие добавки, например, пластификаторы, смазывающие агенты, выравниватели крашения, эмульгаторы, пигменты, реологические и тиксотропные агенты, регуляторы потока, оптические отбеливатели, огнезащитные агенты, антистатические агенты и пенообразователи.
14. Бензофураноны и индолиноны, например такие, как описаны в патентах U.S. 4325863; U.S. 4338244; U.S. 5175312; U.S. 5216052; U.S. 5252643; DE-A-4316611; DE-A-4316622; DE-A-4316876; EP-A-0589839 или EP-A-0591102 или 3-[4-(2-ацетоксиэтокси)фенил]-5,7-ди-трет-бутилбензофуран-2-он, 5,7-ди-трет-бутил-3-[4-(2-стеароилоксиэтокси)фенил]бензофуран-2-он, 3,3'-бис[5,7-ди-трет-бутил-3-(4-[2-гидроксиэтокси]фенил)бензофуран-2-он], 5,7-ди-трет-бутил-3-(4-этоксифенил)бензофуран-2-он, 3-(4-ацетокси-3,5-диметилфенил)-5,7-ди-трет-бутилбензофуран-2-он, 3-(3,5-диметил-4-пивалоилоксифенил)-5,7-ди-трет-бутилбензофуран-2-он, 3-(3,4-диметилфенил)-5,7-ди-трет-бутилбензофуран-2-он, 3-(2,3-диметил-фенил)-5,7-ди-трет-бутилбензофуран-2-он.
В дополнение к указанным выше связующим агентам, полимеризуемым или поперечно-сшиваемым с применением основания, компонента (А), композиция также может включать другие связующие агенты. Например, возможно применять другие олефинненасыщенные соединения. Ненасыщенные соединения могут включать одну или более олефиновые двойные связи. Они могут иметь низкую молекулярную массу (мономеры) или более высокую молекулярную массу (олигомеры). Примеры мономеров, имеющих двойную связь, включают алкилакрилаты или гидроксиалкилакрилаты или алкилметакрилаты или гидроксиалкилметакрилаты, такие как метил, этил, бутил, 2-этилгексил или 2-гидроксиэтилакрилат, изоборнилакрилат, метилметакрилат или этилметакрилат. Силиконакрилаты также представляют интерес. Другие примеры включают акрилонитрил, акриламид, метакриламид, N-замещенные (мет)акриламиды, сложные эфиры винила, такие как винилацетат, простые эфиры винила, такие как изобутилвиниловый эфир, стирол, алкил- и галогенстиролы, N-винилпирролидон, винилхлорид или винилиденхлорид.
Примеры мономеров, имеющих несколько двойных связей, включают диакрилаты этилен гликоля, пропилен гликоля, неопентил гликоля, гексаметиленгликоля или бисфенола А, 4,4'-бис(2-акрилоилоксиэтокси)дифенилпропан, триакрилат триметилолпропана, триакрилат пентаэритритола или тетраакрилат пентаэритритола, винилакрилат, дивинилбензол, сукцинат дивинила, фталат диаллила, фосфат триаллила, изоцианурат триалилла или трис(2-окрилоилэтил)изоцианурат.
Примеры полиненасыщенных соединений с высокой молекулярной массой (олигомеров) включают акрилированные эпоксидные смолы, акрилированные сложные полиэфиры или простые полиэфиры, содержащие группы простого винилового эфира или эпоксидные группы, полиуретаны и простые полиэфиры. Другие примеры ненасыщенных олигомеров включают ненасыщенные полиэфирные смолы, которые в основном получают из малеиновой кислоты, фталевой кислоты и одного или боле диолов, и которые имеют молекулярную массу от около 500 до 3000. Кроме того, также возможно применять мономеры и олигомеры простого винилового эфира, а также олигомеры с концевым малеатом с основным цепями сложного полиэфира, полиуретана, простого полиэфира, поливинилового эфира и эпоксида. В частности, сочетания олигомеров, содержащих простой виниловый эфир, и полимеров, которые описаны в WO 90/01512, являются очень подходящими. Также подходят сополимеры простого виниловго эфира и мономеров с функциональной группой малеиновой кислоты. Ненасыщенные олигомеры этого типа также предпочтительны в качестве форполимеров.
Особенно подходящие примеры включают сложные эфиры этиленненасыщенных карбоновых кислот и многоатомных спиртов или полиэпоксидов, и полимеры, содержащие этиленненасыщенные группы в цепи или в боковых группах, такие как ненасыщенные сложные полиэфиры, полиамиды и полиуретаны, и их сополимеры, алкидные смолы, полибутадиеновые и бутадиеновые сополимеры, полиизопреновые и изопреновые сополимеры, полимеры и сополимеры, имеющие (мет)акриловые группы в боковых цепях, и смеси одного или более таких полимеров.
Кроме того, если применяются такие радикально отверждаемые мономеры, олигомеры/полимеры, то целесообразно добавлять дополнительный фотоинициатор или теплочувствительный инициатор радикалов, которые разлагаются на радикалы. Такие фотоинициаторы известны и производятся промышленно. Примеры включают бензофенон, производные бензофенона, ацетофенон, производные ацетофенона, например α-гидроксициклоалкилфенилкетоны, диалкоксиацетофеноны, α-гидрокси- или α-аминоацетофеноны, 4-ароил-1,3-диоксоланы, бензоиналкиловые простые эфиры и бензилкетали, оксиды моноацилфосфина, оксиды бисацилфосфина, соединения ферроцения или титаноцены.
Примеры указаны в EP-А-284561. Полимерные системы такого типа, в которых отверждение/поперечное сшивание проходит с применением различных механизмов, также названы гибридными системами.
Также возможно добавлять нереакционноспособные связующие агенты в новые композиции, что особенно целесообразно, если полимеризуемый по анионному механизму или поперечно сшиваемый органический материал, компонент (A), является жидким или вязким веществом. Количество нереакционноспособного связующего агента может составлять, например, 5-95%, предпочтительно 10-90% и, в частности, 40-90 мас.%, по отношению к массе компонента (A). Выбор нереакционноспособного связующего агента делают в зависимости от области применения и свойств, требуемых для такого применения, таких как возможность проявления в системах водных и органических растворителей, адгезия к субстратам и чувствительность к кислороду.
Примеры подходящих связующих агентов включают полимеры, имеющие молекулярную массу около 5000-2000000, предпочтительно 10000-1000000. Примеры включают гомо- и сополимерные акрилаты и метакрилаты, например, сополимеры метилметакрилата/этилакрилата/метакриловой кислоты, поли(алкилметакрилаты), поли(алкилакрилаты); сложные и простые эфиры целлюлозы, такие как ацетат целлюлозы, ацетатбутират целлюлозы, метилцеллюлоза, этилцеллюлоза; поливинилбутираль, поливинилформаль, циклизованный каучук, простые полиэфиры, такие как полиэтиленоксид, полипропиленоксид, политетрагидрофуран; полистирол, поликарбонат, полиуретан, хлорированные полиолефины, поливинилхлорид, сополимеры винилхлорида/винилиденхлорида, сополимеры винилиденхлорида с акрилонитрилом, метилметакрилат и винилацетат, поливинилацетат, сополи(этилен/винилацетат), полимеры, такие как поликапролактам и поли(гексаметиленадиамид) и сложные полиэфиры, такие как поли(терефталат этилен гликоля) и поли(сукцинат гексаметиленгликоля).
Отверждаемые композиции в соответствии с данным изобретением получают методами, известными в данной области техники. Компонент (В), т.е. термолатентное основание, представленное формулой (I), и необязательные другие добавки могут быть добавлены к компоненту (A), т.е. анионно полимеризуемому или поперечно сшиваемому органическому материалу, и необязательным дополнительным связующим агентам, отдельно или в смеси друг с другом.
Введение компонента (B) и необязательных добавок в компонент (A) и необязательных связующих агентов проводят известными методами, такими как сухое смешивание, в виде порошка, или влажное смешивание, в виде растворов или суспензий. Подходящие растворители включают, например, диметилформамид, тетрагидрофуран, метилэтилкетон или этилацетат. Обычные аппараты для смешивания включают, например, мешалки, месильные машины, валки, или для твердых веществ, сухие мешалки.
Новые отверждаемые композиции могут применяться для разных целей, предпочтительно в качестве покрытий. Новые отверждаемые композиции подходят, например, в качестве покрытий для субстратов всех типов, например, дерева, текстиля, бумаги, керамики, стекла, пластика, такого как сложные полиэфиры, полиэтилентерефталат, полиолефины или ацетат целлюлозы, особенно в виде пленок, а также металла, такого как Al, Cu, Ni, Fe, Zn, Mg или Co и GaAs, Si или SiO2.
Композиции для моментального покрытия особенно подходят для финишных покрытий для металла и тонировки автомобиля, особенно для ретуширования, а также для различных типов рулонного покрытия. Покрытия в соответствии с данным изобретением предпочтительно применяют обычным путем с применением двух способов, либо способом однослойного нанесения, либо способом двухслойного нанесения. В последнем способе содержащее пигмент основание наносят первым, и затем на него наносят конечное покрытие из прозрачного лака.
Если желательны растворимые в воде, смешиваемые с водой или диспергируемые в воде покрытия, формируют аммониевые соли кислотных групп, присутствующих в полимере.
Термолатентные основания, компонент (B), особенно полезны, если органический растворитель или вода не присутствуют в композиции покрытия. Это является обычным для порошковых покрытий.
Порошковые покрытия представляют собой известную технологию и описаны, например, в "Ullmann's Encyclopedia of Industrial Chemistry, Fifth, Completely Revised Edition, Volume A 18", страницы 438-444 (1991). В процессе нанесения порошкового покрытия порошок обычно ожижают с применением воздуха, электростатически заряжают и наносят на заземленный, предпочтительно, металлический субстрат. Субстрат затем нагревают, в процессе чего прилипший порошок плавится, коалесцируется и образует когерентную пленку на металлической поверхности. Так как порошковое покрытие не требует растворителя, эта технология особенно благоприятна для окружающей среды.
Способ, при применении которого порошок контактирует с рабочей поверхностью, на которую наносят покрытие, характеризует различные способы нанесения, например, электростатическое распыление порошка с применением коронного пистолета или трибоэлектрического пистолета, электростатического спекания в псевдоожиженном слое или с применением методики нанесения магнитной щеткой.
Новые отверждаемые композиции также могут применяться в качестве адгезивов, включая чувствительные к давлению адгезивы, в качестве ламинирующих смол, для покрытия или инкапсулирования электрических или электронных компонентов, или в качестве покрытия для оптических волокон.
Также возможно наносить отверждаемые композиции в соответствии с данным изобретением в виде жидкой композиции, раствора или суспензии на субстрат. Выбор растворителя и концентрации зависит от, преимущественно, типа композиции и процесса нанесения покрытия. Растворитель должен быть инертным: другими словами, он не должен вступать в химические реакции с компонентами, и должен обладать способностью удаляться после нанесения покрытия, в процессе сушки. Примеры подходящих растворителей включают кетоны, простые эфиры и сложные эфиры, такие как метилэтилкетон, изобутилметилкетон, циклопентанон, циклогексанон, N-метилпирролидон, диоксан, тетрагидрофуран, 2-метоксиэтанол, 2-этоксиэтанол, 1-метокси-2-пропанол, 1,2-диметоксиэтан, этилацетат, н-бутилацетат и этил 3-этоксипропионат.
При применении известных процессов нанесения покрытий, раствор наносят равномерно на субстрат, например, центрифугированием, погружением, шабером, наливом, брашингом, распылением, особенно электростатическим распылением и обратным валком, и электрофорезным нанесением.
Наносимое количество (толщина слоя) и природа субстрата (подложка слоя) зависят от желаемой области применения. Интервал толщины слоя обычно составляет от около 0,1 мкм до более 100 мкм.
Отверждение отверждаемой композиции в соответствии с данным изобретением для получения покрытий или подобного проводят способом, обычно применяемым в области нанесения покрытий. Тепловое отверждение обычно означает нагревание композиции при температуре от 60°C до 250°C, предпочтительно, от 80°C до 150°C. В случае термоусаживаемых порошковых покрытий, предпочтительная температура составляет от 120°C до 200°C.
Если фотолатентные основания присутствуют в композиции, композиция может быть отверждена облучением композиции светом, имеющим длину волны от 200 нм до 650 нм, предпочтительно, от 250 нм до 400 нм.
В некоторых случаях может быть предпочтительно проводить нагревание во время или после облучения светом. Таким образом, во многих случаях возможно усилить реакцию поперечного сшивания.
Время отверждения может составлять, например, от 1 до 60 минут для термоусаживаемых покрытий.
Это изобретение также относится к применению соединения формулы (I)
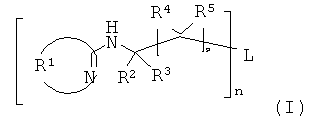
в качестве катализатора отверждения для вызванных нагреванием катализируемых основанием реакций полимеризации или поперечного сшивания, в частности, для отверждения композиций, содержащих компонент (А), где R1, R2, R3, R4, R5, L, p и n имеют значения и предпочтительные значения, указанные выше.
Далее, данное изобретение относится к применению соединения формулы (I) для получения композиций покрытия, особенно композиций порошкового покрытия, или адгезивных композиций.
Согласно другому объекту, данное изобретение относится к полимеризуемым или поперечно-сшиваемым новым композициям, например, покрытиям или связанным материалам, поученным отверждением отверждаемой композиции в соответствии с данным изобретением, как описано выше.
Согласно другому объекту, данное изобретение относится к изделию с покрытием или связанному изделию, где изделие с покрытием или связанное изделие содержит соединение формулы V 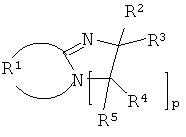 , где the R1, R2, R3, R4, R5 и p такие, как определены выше, и полимеризованный или поперечно-сшитый органический материал.
, где the R1, R2, R3, R4, R5 и p такие, как определены выше, и полимеризованный или поперечно-сшитый органический материал.
Некоторые соединения формулы (I) являются известными соединениями. Множество соединений формулы (I), где L является определенной уходящей группой, являются новыми соединениями. Данное изобретение также относится к соединению формулы (III),
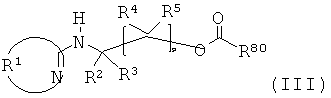 ,
,
где,
R1 является С2-C20 кольцевой системой, либо моноциклической кольцевой системой, которая содержит вплоть до двух гетероатомов S или N, или полициклической кольцевой системой, которая содержит один или более гетероатомов S или N,
где указанная кольцевая система не замещена или замещена
C1-C18алкилом; C1-C18алкилом, который замещен Е и/или прерывается D; C5-C12циклоалкилом, C5-C12циклоалкилом, который замещен Е и/или прерывается D; C2-C18алкенилом; C2-C18алкинилом; C6-C18арилом; C6-C18арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C18алкокси; C1-C18алкокси, который замещен Е и/или прерывается D; C1-C18алкилтио; C1-C18алкилтио, который замещен Е и/или прерывается D; C7-C18аралкилом; C7-C18аралкилом, который замещен G; галогеном; оксо; OH; SH; CN; NH2; СООН; NHR6; NR7R8; CONH2; CONR9R10; COR11; C(O)OR12; SO2R13; SO3R14; SO2NHR15; SO2NR16R17;
или указанная кольцевая система замещена одной или более группами формулы
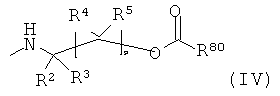
R2, R3, R4 и R5 независимо друг от друга, и каждый R4 или R5 независимо от других R4 или R5 являются Н; C1-C18алкилом; C1-C18алкилом, который замещен Е и/или прерывается D; C5-C12циклоалкилом; C5-C12гциклоалкилом, который замещен Е; C6-C12; C6-C12арилом, который замещен G; C2-C18гетероарилом; C2-C18гетероарилом, который замещен G; C1-C18алкокси; C1-C18алкокси, который замещен Е и/или прерывается D; C7-C18аралкилом; C7-C18аралкилом, который замещен G; NHR18, NR19R20, СООН;
или R2 и R3, R4 и R5, или R2 и R4 образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому они присоединены, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 12 кольцевых атомов в общем;
или два R5, которые связаны с соседними атомами углерода, образуют органическую мостиковую группу, составляющую, вместе с атомом углерода, к которому они присоединены, карбоциклическое или гетероциклическое кольцо, содержащее от 5 до 12 атомов всего;
D является -CO-; -COO-; -S-; -SO-; -SO2-; -O-; -NR21-; -SiR22R23-; -POR24-; -CR25=CR26-; или -C≡C-; E является OR27; SR28; SOR29; SO2R30; NR31R32; COR33; COOR34; CONR35R36; PO(R37)2; Si(R38)3; CN; Cl, Br или I; и
G является E или C1-C18алкилом;
R6, R7, R8, R9, R10, R11, R12, R13, R14, R15, R16, R17, R18, R19, R20, R21, R22, R23, R24, R25, R26, R27, R29, R30, R31, R32, R33, R34, R35, R36, R37 и R38 независимо друг от друга являются C1-C18алкилом; C1-C18алкилом, который прерывается группой -O-; C6-C18арилом; C1-C18арилом, который замещен C1-C18алкилом или C1-C18алкокси; C4-C18аралкилом; C7-C18аралкилом, который замещен G; C2-C18гетероарилом;
или R7 и R8, R9 и R10, R16 и R17, R19 и R20, R29 и R30 или R33 и R34 образуют органическую мостиковую группу, составляющую, вместе с атомом азота, к которому они присоединены, гетероциклическое кольцо, содержащее от 5 до 7 атомов в целом;
R80 является C1-C18валкокси, ОC6-C18арилом, NHC6-C18арилом, NH C1-C18алкилом;
p равно целому числу 1 или 2,
при условии, что если p равно 1 и кольцевая система является пиридином или пиримидином, R3 и R4 не являются фенилом, или
если p равно 1 и кольцевая система является пиримидином, указанное пиримидиновое кольцо незамещено галогеном.
Предпочтительными являются соединения формулы (III), где
R1 является моно- или полициклической C2-C20кольцевой системой, которая содержит вплоть до 2 гетероатомов S или N, и/или незамещенным или замещенным C1-C18алкилом;
R2, R3, R4 и R5 независимо друг от друга, и каждые R4 или R5 независимо от других R4 или R5 являются Н или C1-C18алкилом,
R80 является C1-C18алкокси, ОC6-C18арилом, NНС6-С18арилом, NH C1-C18 C1-C18алкилом; и
p равно целому числу 1 или 2.
Более предпочтительными являются соединения формул (I-1)-(1-21) и (I-23), где L является OCONHMe, OCONHEt, OCONHPh, ОСООМе, OCOOtBu, OCOOPh, OCOOCH2Ph.
Соединения компонента (В) могут быть получены различными известными способами. Например, один способ получения включает взаимодействие галоген-замещенного гетероцикла с подходящим амином, как описано у D.-H.Yang et al., J. Chem. Res. 9, 2006, 600-601, V.Birman et al., Org. Lett. 9(1), 2007, 37-40 или MJ. Weiss, CR. Hauser, J. Am. Chem. Soc. 72, 1950, 1858-1859. Другой способ получения включает взаимодействие амино-замещенного гетероцикла с подходящим эпоксидом или алкилирующим агентом, как описано у А.Р.Gray et al., J. Am. Chem. Soc, 81, 1959, 4351-4355 или W.H.Yanko et al., J. Am. Chem. Soc. 67, 1945, 664-668 или F.C.Whitmore et al., J. Am. Chem. Soc. 67, 1945, 393.
Гидрокси или аминогруппа компонента (B), соответствующая уходящей группе L в формуле (I), может быть далее модифицирована с получением лучшей нуклеофильной группы L.
Отверждаемые композиции в соответствии с данным изобретением обладают превосходной устойчивостью при хранении благодаря применению термолатентных амидиновых оснований, описанных выше. Так называемые однореакторные системы с полимеризуемыми основанием олигомерами или мономерами имеют очень длительный срок хранения без применения особых мер предосторожности, что является преимуществом с точки зрения сокращения подготовительной обработки перед применением и уменьшения количества побочных продуктов благодаря большему сроку хранения. Время докторабильности, т.е. период до отверждения композиции, которое необходимо для обработки композиции, увеличивается.
Далее, отверждаемые композиции могут быть получены при повышенной температуре, например, экструзией, что особенно интересно для получения порошковых покрытий. Обычно порошковые покрытия могут быть получены при температурах ниже температур, которые могут активировать термолатентное основание. Подходящие температуры для производства порошковых покрытий составляют от 80 до 120°C. Таким образом, интервал температур получения отверждаемой композиции, а также применения, увеличивается.
Покрытия, полученные отверждение композиции в соответствии с данным изобретением, в меньшей степени желтеют после получения, а также в течение определенного времени. Более того, выравнивание покрытий, предпочтительно, полученных нанесением порошкового покрытия в соответствии сданным изобретением, улучшается.
Определения и предпочтения, указанные выше для отверждаемой композиции, применяются во многих комбинациях, а также в любых комбинациях других объектов данного изобретения.
Представленные ниже примеры приведены в иллюстративных целях и не ограничивают данное изобретение никоим образом. Если не указано иное, части и проценты, указанные в описании или формуле изобретения, являются массовыми, и комнатная температура означает температуру в интервале 20-25°C. Реакции проводят в атмосфере азота и при отсутствии света, если не указано иное.
Аппараты и т.д., применяемые для измерения:
1Н ЯМР: Bruker 300 МГц спектрометр
ИК спектроскопия: Nicolet 380 FT-IR спектрометр
Примеры
Пример 1 (Ссылочный пример)
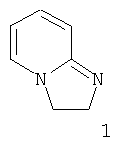
Соединение получают в соответствии с V.Birman et al., J. Am. Chem. Soc. 126, 2004, 12226-12227.
Пример 2
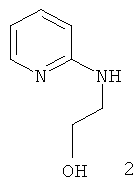
Соединение получают в соответствии с V.Birman et al., J. Am. Chem. Soc. 126, 2004, 12226-12227.
Пример 3
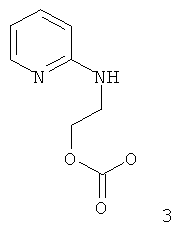
0,5 г 4-диметиламинопиридина и 28 мл (0,2 моль) триэтиламина добавляют к раствору 13,8 г (0,1 моль) 2-(пиридин-2-иламино)этанола (2) в 50 мл тетрагидрофурана. Затем добавляют раствор 26,2 г (0,12 моль) ди-трет-бутилдикарбоната в 50 мл тетрагидрофурана в течение 10 минут, и полученную смесь перемешивают при комнатной температуре в течение 20 часов. Растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (9:1 к 5:1) с получением 17,3 г соединения 3 в виде светло-желтого масла.
1Н ЯМР (300 МГц, CDCl3): 8,08 (д, 1Н, J=5,1 Гц), 7,40 (м, 1Н), 6,57 (м, 1Н), 6,41 (д, 1Н, J=8,4 Гц), 4,8 (уш. с, NH), 4,26 (т, 2Н, J=5,4 Гц), 3,64 (м, 2Н), 1,49 (с, трет-Bu).
Пример 4
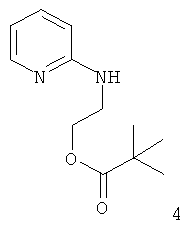
0,05 г 4-диметиламинопиридина и 1,6 мл (0,011 моль) триэтиламина добавляют к раствору 1,38 г (0,01 моль) 2-(пиридин-2-иламино)этанола (2) в 10 мл тетрагидрофуран. Затем добавляют 1,32 г (0,011 моль) пивалоилхлорида в течение 10 минут, и полученную смесь перемешивают при комнатной температуре в течение 20 часов. Смесь выливают в 100 мл ледяной воды, и осевшее масло экстрагируют 4х 20 мл дихлорметана. Объединенные экстракты промывают водой и сушат над MgSO4. Затем растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (8:1 к 8:2) с получением 1,39 г соединения 4 в виде светло-желтого масла.
1Н ЯМР (300 МГц, CDCl3): 8,08 (д, 1Н, J=5,1 Гц), 7,40 (м, 1Н), 6,58 (м, 1Н), 6,43 (д, 1Н, J=8,4 Гц), 4,8 (уш.с, NH), 4,26 (т, 2Н, J=5,4 Гц), 3,60 (м, 2Н), 1,19 (с, трет-Bu).
Пример 5
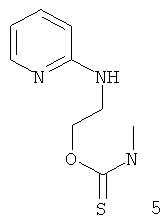
0,58 г (0,0132 моль) гидрида натрия (55% в минеральном масле) добавляют к раствору 1,66 г (0,012 моль) 2-(пиридин-2-иламино)этанола (2) в 6 мл диметилформамида, и полученную смесь перемешивают в течение 30 минут. Смесь затем охлаждают до 3°C, и добавляют 1,65 г (0,0132 моль) хлорида диметилтиокарбамоила в течение 10 минут. Полученную смесь перемешивают в течение 2 часов и затем выливают в 20 мл ледяной воды. Осевшее масло экстрагируют 3х 25 мл дихлорметана, и объединенные экстракты промывают водой и сушат над MgSO4. Затем растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (7:3) с получением 1,95 г соединения 5 в виде желтого масла.
1Н ЯМР (300 МГц, CDCl3): 8,08 (д, 1Н, J=5,1 Гц), 7,41 (м, 1Н), 6,58 (м, 1Н), 6,43 (д, 1Н, J=8,4 Гц), 4,8 (уш.с, NH), 4,70 (т, 2Н, J=5,4 Гц), 3,70 (м, 2Н), 3,36 (с, CH3), 3,08 (с, СН3).
Пример 6
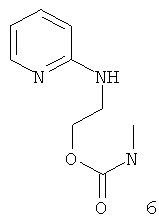
0,58 г (0,0132 моль) гидрида натрия (55% в минеральном масле) добавляют к раствору 1,66 г (0,012 моль) 2-(пиридин-2-иламино)этанола (2) в 6 мл диметилформамида, и полученную смесь перемешивают в течение 30 минут. Смесь затем охлаждают до 3°C, и добавляют 1,42 г (0,0132 моль) хлорида диметилкарбамоила в течение 10 минут. Полученную смесь перемешивают в течение 2 часов и затем выливают в 100 мл ледяной воды. Осевшее масло экстрагируют 5×20 мл дихлорметана, и объединенные экстракты промывают водой и сушат над MgSO4. Затем растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (3:7) с получением 1,95 г соединения 6 в виде белого твердого вещества (т.пл. 49-52°C).
1Н ЯМР (300 МГц, CDCl3): 8,08 (д, 1Н, J=4,8 Гц), 7,40 (м, 1Н), 6,58 (м, 1Н), 6,43 (д, 1Н, J=8,4 Гц), 4,8 (уш.с, NH), 4,29 (т, 2Н, J=5,4 Гц), 3,58 (м, 2Н), 2,91 (с, СН3), 2,88 (с, СН3).
Пример 7
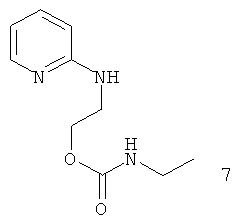
160 мг 4-диметиламинопиридина и 5,05 мл (0,064 моль) этилизоцианата добавляют к раствору 7,6 г (0,055 моль) 2-(пиридин-2-иламино)этанола (2) в 35 мл дихлорметана, и полученную смесь перемешивают при комнатной температуре в течение 20 часов. Растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (1:1 к 3:7). Чистые фракции перекристаллизовывают из дихлорметана-гексана с получением 12,9 г соединения 7 в виде белого твердого вещества (т.пл. 80-83°C).
1Н ЯМР (300 МГц, CDCl3): 8,07 (д, 1Н, J=5,1 Гц), 7,39 (м, 1Н), 6,55 (м, 1Н), 6,41 (д, 1Н, J=8,4 Гц), 5,04 (уш.с, 2NH), 4,26 (м, 2Н), 3,55 (м, 2Н), 3,20 (м, 2Н), 1,12 (м, 3Н).
Пример 8
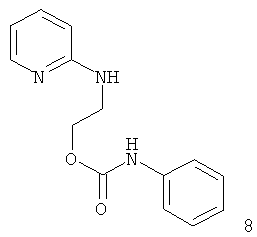
60 мг 4-диметиламинопиридина и 1,31 г (0,011 моль) фенилизоцианата добавляют к раствору 1,38 г (0,01 моль) 2-(пиридин-2-иламино)этанола (2) в 10 мл дихлорметана, и полученную смесь перемешивают при комнатной температуре в течение 75 часов. Растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (3:7). Чистые фракции перекристаллизовывают из дихлорметана-гексана с получением 1,84 г соединения 8 в виде белого твердого вещества (т.пл. 80-81°C).
1Н ЯМР (300 МГц, CDCl3): 8,09 (д, 1Н, J=4,2 Гц), 7,46-7,26 (м, С6Н5), 7,09 (м, 1Н), 6,75 (уш.с, NH), 6,60 (м, 1Н), 6,45 (д, 1Н, J=8,4 Гц), 4,90 (уш.с, NH), 4,38 (т, 2Н, J=5,4 Гц), 3,66 (м, 2Н).
Пример 9
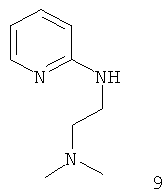
Соединение получают, как описано у К.Kovacs, Т.Vajda, Chemistry & Industry, 1959, 259.
Пример 10
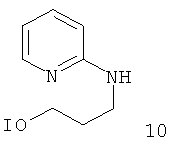
Соединение получают, как описано у D.Heckmann et al., Angew. Chem., Internat. Ed. 46 (19), 2007, 3571-3574.
Пример 11

Раствор 2,62 г (0,012 моль) ди-трет-бутилдикарбоната в 4 мл тетрагидрофурана добавляют раствору 1,52 г (0,01 моль) 3-(пиридин-2-иламино)пропан-1-ола (10), 0,055 г 4-диметиламинопиридина и 2,8 мл (0,02 моль) триэтиламина в 2 мл тетрагидрофуран, и полученную смесь перемешивают при комнатной температуре в течение 24 часов. Затем растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (9:1) с получением 1,02 г соединения 11 в виде бесцветного твердого вещества, которое отверждается при выстаивании (т.пл. 55-57°С)
1Н ЯМР (300 МГц, CDCl3): 8,07 (д, 1Н, J=4,2 Гц), 7,41 (м, 1Н), 6,56 (м, 1Н), 6,39 (д, 1Н, J=8,4 Гц), 4,7 (уш.с, NH), 4,19 (т, 2Н, J=5,7 Гц), 3,41 (м, 2Н), 1,98 (м, 2Н), 1,49 (с, трет-Bu).
Пример 12
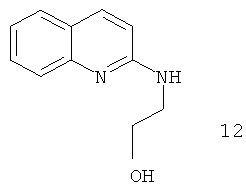
Смесь 16,3 г (0,1 моль) 2-хлорхинолина и 24,5 г (0,4 моль) 2-аминоэтанола нагревают до 170°C в течение 21 часа. Затем смесь охлаждают до комнатной температуры и туда добавляют 180 мл ледяной воды. Осевшее твердое вещество растворяют в 120 мл дихлорметана, полученный раствор промывают 2х 15 мл воды, сушат над MgSO4 и выпаривают. Остаток перекристаллизовывают из дихлорметана-этилацетата с получением 13,04 г соединения 12 в виде светло-желтого твердого вещества (т.пл. 119-122°C).
1Н ЯМР (300 МГц, CDCl3): 7,79-7,49 (м, 4Н), 7,26-7,19 (м, 1Н), 6,63 (д, 1Н, J=9 Гц), 6,0 (уш.с, NH), 5,34 (уш.с, NH), 3,86 (м, 2Н), 3,66 (м, 2Н).
Пример 13
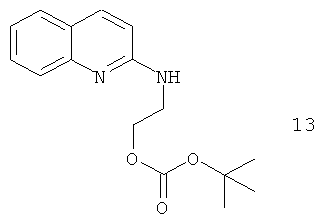
Раствор 2,62 г (0,012 моль) ди-трет-бутилдикарбоната в 5 мл тетрагидрофурана добавляют к раствору 1,88 г (0,01 моль) 2-(хинолин-2-иламино)этанола (12), 0,055 г 4-диметиламинопиридина и 2,8 мл (0,02 моль) триэтиламина в 7 мл тетрагидрофурана, и полученную смесь перемешивают при 40°C в течение 1 часа. Затем растворитель выпаривают, и остаток подвергают хроматографии на силикагеле с дихлорметаном-этилацетатом (9:1). Чистые фракции перекристаллизовывают из гексана-этилацетата с получением 1,37 г соединения 13 в виде бесцветного твердого вещества (т.пл. 113-116°C).
1Н ЯМР (300 МГц, CDCl3): 7,83-7,50 (м, 4Н), 7,26-7,19 (м, 1Н), 6,56 (м, 1Н), 6,63 (д, 1Н, J=8,7 Гц), 5,1 (уш.с, NH), 4,34 (т, 2Н, J=5,7 Гц), 3,86 (м, 2Н), 1,49 (с, трет-Bu).
Пример 14 (Ссылочный пример)
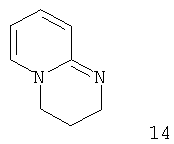
Соединение получают, как описано у Т.Yamazaki et al., Yakugaku Zasshi, 88(2), 1968, 212-215.
Пример 15
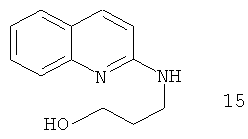
Соединение получают, как описано у М.Nagata et al., Yakugaku Zasshi, 83, 1963, 682-689.
Пример 16
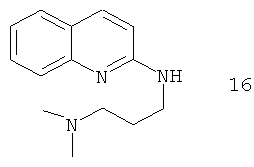
Смесь 8,15 г (0,05 моль) 2-хлорхинолина и 15,3 г (0,15 моль) 3-диметиламинопропиламина нагревают до 170°C в течение 17 часов. Затем полученную смесь охлаждают до комнатной температуры и добавляют 80 мл ледяной воды. Осевшее масло экстрагируют 10 мл дихлорметана, полученный раствор промывают 40 мл воды и 25 мл 2М Na2CO3, отделенную органическую фазу сушат над MgSO4 и выпаривают получением 9,5 г соединения 16 в виде светло-желтого масла.
1Н ЯМР (300 МГц, CDCl3): 7,80-7,40 (м, 4Н), 7,20-7,10 (м, 1Н), 6,61 (д, 1Н, J=9ГЦ), 5,65 (уш.с, NH), 3,56 (м, 2Н), 2,42 (т, 2Н, J=6,6 Гц), 2,25 (с, 2×СН3); 1,81 (м, 2Н).
Пример 17
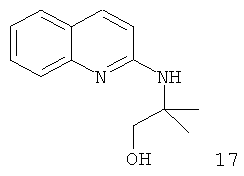
Смесь 16,3 г (0,1 моль) 2-хлорхинолина и 26,8 г (0,3 моль) 2-амино-2-метилпропанола нагревают до 170°С в течение 48 часов. Затем полученную смесь охлаждают до комнатной температуры и добавляют 270 мл ледяной воды. Продукт отфильтровывают и сушат с получением 16,15 г твердого вещества, которое дважды перекристаллизовывают из этанола с получением 7,9 г соединения 17 в виде серого твердого вещества.
1Н ЯМР (300 МГц, CDCl3): 7,8-6,6 (м, 6Н), 5,0 (уш.с, NH), 3,71 (с, 2Н), 1,43 (с, 6Н).
Пример 18
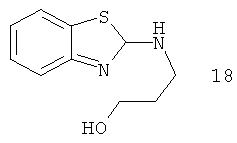
Соединение получают, как описано у V.Birman et al., Org. Lett. 9 (1), 2007, 37-40.
Пример 19
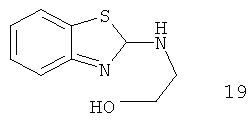
Соединение получают, как описано у М.Kobayashi et al., Tetrahedron Lett., 47 (26), 2006, 4347-4350.
Пример 20
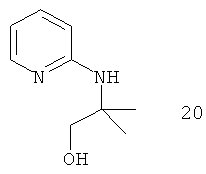
Смесь 16,6 г (0,105 моль) 2-бромпиридина и 29 г (0,325 моль) 2-амино-2-метилпропанола (29 г, 0,325 моль) нагревают до 170°C в течение 84 часов. Полученную смесь затем охлаждают до комнатной температуры, и добавляют 200 мл ледяной воды. Продукт экстрагируют 4х 30 мл дихлорметана, объединенные экстракты сушат над MgSO4 и выпаривают с получением 12,7 г коричневого масла, которое подвергают хроматографии на силикагеле с этилацетатом-гексаном (1:1) с получением 7,15 г соединения 20 в виде светло-желтого твердого вещества (т.пл. 90-94°C).
1Н ЯМР (300 МГц, CDCl3): 7,97 (д, 1Н, и=7,8 Гц), 7,45-7,35 (м, 1Н), 6,58-6,53 (м, 1Н), 6,42 (д, 1Н, и=8,4 Гц), 4,5 (уш.с, NH), 3,62 (с, 2Н), 1,34 (с, 6Н).
Пример 21
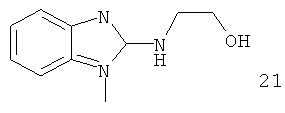
Соединение получают, как описано у A.M.Simonov et al., Khimiya Geterotsiklicheskikh Soedinenii, 6, 1975, 826-828.
Пример 22
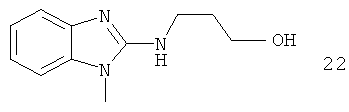
Соединение получают, как описано у V.A.Anisimova et al., Pharm. Chem. J. 36 (9), 2002, 468-473.
Пример 23
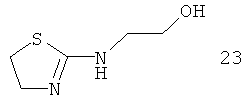
Соединение получают как описано у R.С.Clapp et al., J. Org. Chem., 28 (8), 1964, 2172-2174.
Пример 24
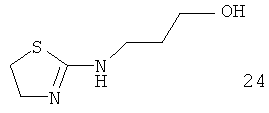
Соединение получают, как описано у R.С.Clapp et al., J. Heterocycl. Chem., 7 (6), 1970, 1357-1361.
Пример 25
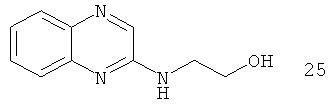
Соединение получают, как описано у Н.Otomasu et al., Yakugaku Zasshi, 90 (11), 1970, 1391-1395.
Пример 26
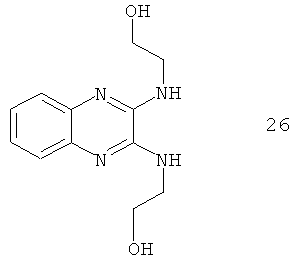
Соединение получают, как описано у I.N. Goncharov et al., Zhurnal Obshchei Khimii 32, 1962, 3332-3339.
Пример 27
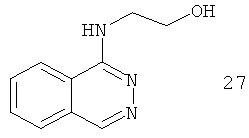
Соединение получают, как описано у R.N.Castle et al., J. Heterocycl. Chem., 3 (3), 1966, 381-383.
Пример 28
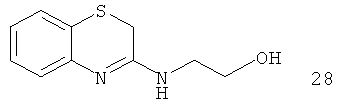
Соединение получают, как описано у K.Bhandari et al., Indian. J. Chem., Sect. B, 17B (2), 1979, 107-110.
Пример 29
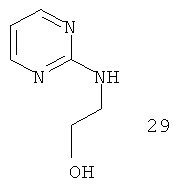
Соединение получают, как описано у J.N.Singh et al., J. Indian Chem. Soc, 40, 1963, 195-198.
Пример 30
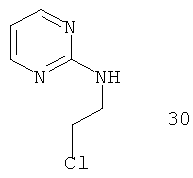
Соединение получают, как описано у J.N.Singh et al., J. Indian Chem. Soc. 43 (5), 1966, 308-310.
Пример 31
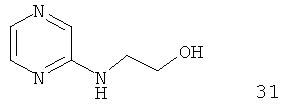
Соединение получают, как описано у G. Cignarella et al., J. Med. Chem. 8(3), 1965, 326-331.
Примеры применения
Примеряют порошковое покрытие, содержащее сложный полиэфир с кислотной функциональной группой и полимер с эпоксидной функциональной группой, которое отверждают без катализатора при 200°С в течение 20 минут.
Твердое покрытие растворяют до 50% твердых веществ в метил-изо-бутилкетоне для простоты применения. Отверждающий катализатор добавляют в различных количествах от 0,5 до 1,5 мас.%, по отношению к твердому веществу. Термолатентные соединения сравнивают с имидазолом или соединением 1 в качестве контрольного основания. Композицию наносят на толщину во влажном состоянии 250 мкм с применением проволоки. Растворитель выпаривают при комнатной температуре в течение 30 минут, и покрытие отверждают в течение указанного времени и при указанной температуре (см. таблицы 2-4). Прогресс отверждения оценивают с применением инфракрасной (ИК) спектроскопии нарушенного полного внутреннего отражения. Затенение относящегося к эпоксиду пика при 899-921 см-1 по сравнению со стабильным контрольным пиком при 814-841 см-1 применяют для расчета превращения эпоксигрупп.
|
Изменение цвета или желтение, соответственно, в ΔЕ, определяют по системе е CIELAB. Было обнаружено, что при превращении через 15 минут при 120°C АЕ композиции, содержащей соединение 1, была на 30% лучше, чем соответствующее значение для композиции, содержащей имидазол.
|
|
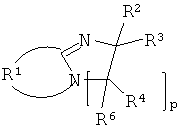
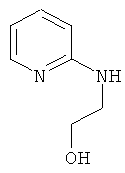 рКа=5,93±0,19
рКа=5,93±0,19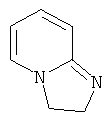 рКа=12,5±0,50
рКа=12,5±0,50