Результат интеллектуальной деятельности: СПОСОБ ОПРЕДЕЛЕНИЯ КОНЦЕНТРАЦИИ ВАРФАРИНОВОГО СПИРТА В ПЛАЗМЕ КРОВИ
Вид РИД
Изобретение
Изобретение относится к области биохимии и касается способа определения концентрации варфаринового спирта - продукта метаболизма варфарина, антикоагулянта, используемого при профилактике и в лечении тромбозов.
Острые артериальные и венозные тромбозы являются жизненно опасной патологией, угрожающей развитием тромбоэмболии легочной артерии и внезапной гибелью пациента. В России распространенность верифицированных тромбозов достигает 30%. Низкая эффективность проводимых лечебных мероприятий приводит к инвалидизации 40-70% больных в течение трех лет после манифестации заболеваний, а через 10 лет стойкая утрата трудоспособности отмечается у 80-100% пациентов. Базовой терапией тромбозов является антикоагулянтная терапия (в России в основном варфарином), нередко пожизненная. Однако количество осложнений приема варфарина, в первую очередь геморрагии различной степени тяжести, остается достаточно высоким - до 16%, при этом фатальные (жизнеугрожающие) кровотечения отмечаются у 2% пациентов. Одной из основных причин развития осложнений при приеме варфарина являются генетически обусловленные изменения скорости биотрансформации лекарственного агента и отсутствие данных о фармакокинетике препарата у людей с различными особенностями метаболизма.
В настоящее время продолжается разработка новых способов определения параметров метаболизма варфарина, в том числе с применением масс-спектрометрического анализа (Zuo Z. et al. Journal of pharmaceutical and biomedical analysis. Elsevier B.V., 2010. Vol.52, №2. P.305-310), позволяющего определять концентрацию варфарина, его R-, S-изомеров, и продуктов его метаболизма - гидроксиварфаринов, окисленных по различным положениям.
Наряду с 7-гидроксиварфарином, варфариновый спирт является одним из главных метаболитов варфарина, поэтому определение концентрации последнего в плазме крови и использование ее для характеризации метаболизма варфарина является актуальной задачей.
Известен способ определения концентрации варфаринового спирта флуометрическим методом (Lewis RJ. et al. Warfarin. The Journal of clinical investigation. American Society for Clinical Investigation, 1974. Vol.53, №6. Pp.1607-1617.), включающим разделение исходной смеси, содержащей варфарин и его метаболиты, методом многократной тонкослойной хроматографии. При этом качественно варфариновый спирт детектируют в ультрафиолетовом свете, а количественно концентрацию варфаринового спирта рассчитывают по отношению флуоресценции образца к флуоресценции стандарта с известной концентрацией.
Известен способ определения концентрации метаболитов варфарина путем флуометрического определения варфарина и его гидроксиварфаринов с использованием жидкостной хроматографии (Locatelli I. et al. Journal of chromatography. B, Analytical technologies in the biomedical and life sciences. 2005. Vol.818, №2. P.191-198.). В этом способе используют внутренние стандарты, которые добавляют к образцам плазмы крови перед извлечением варфарина. Смесь определяемых веществ разделяют обращено-фазовой хроматографией на последовательно подключенных колонках. Детекцию образцов проводят в ультрафиолетовом свете на разных длинах волн в диапазоне 299-312 нм. Расчет концентрации проводят по соотношению площади пика флуоресценции вещества к площади пика флуоресценции внутреннего стандарта с известной концентрацией.
Недостатками известных способов являются необходимость проведения многократной тонкослойной или жидкостной хроматографии, низкая воспроизводимость измерения, а также длительность и трудоемкость способов, связанная с флуориметрическим определением концентрации вещества.
Наиболее ближайшим к заявленному способу - прототипом, является способ определения концентрации варфарина и 7-гидроксиварфарина (Kwon M.-J. et al. The Korean journal of laboratory medicine. 2009. Vol.29, №6. P.515-523.), состоящий из следующих стадий. Для определения варфарина в плазме крови используют образец крови, полученный не менее чем через 12 ч после приема последней дозы варфарина. Белки плазмы крови отделяют путем их соосаждения с ZnSO4. Для этого 10 мкл плазмы крови добавляют к 40 мкл 0,1 М ZnSO4 и перемешивают в течение 30 сек. К смеси добавляют 100 мкл раствора внутреннего стандарта (10 нг/мл хлороварфарина в ацетонитриле). После встряхивая в течение 30 с, смесь центрифугируют в течение 3 мин при 20817 × g (14000 оборотов в минуту), затем 10 мкл супернатанта наносят непосредственно на аналитическую колонку.
Разделение образцов проводят на ВЭЖХ системе 2795 Alliance фирмы Waters. После прохождения колонки мобильная фаза, содержащая определяемое вещество, подается на масс-спектрометр для проведения анализа.
Анализ проводят на масс-спектрометре Quattro Mikro API (Waters, Manchester, UK) в режиме обнаружения положительных ионов. Количественный масс-спектроскопический анализ проводят в режиме мониторинга множественных реакций (MRM) с разрушением исходных молекул на осколки: m/z 307,0 → 160.9 для варфарина, 322,9 → 176.8 для 7-гидроксиварфарина и 340.9 → 283.8 для внутреннего стандарта. Время проведения масс-спектрометрического анализа зависит от времени проведения хроматографического разделения и составляет, как минимум, 4 минуты.
Количественное определение варфарина и 7-гидроксиварфарина производят по отношению площадей пиков ионной плотности, соответствующих варфарину и 7-гидроксиварфарину, к площади пика ионной плотности внутреннего стандарта. Расчеты проводят в программе Masslynx (Waters, Manchester, UK).
Точность измерения зависит от границ диапазона линейной зависимости концентрации образца от площади пика ионной плотности, полученной в процессе выполнения масс-спектрометрического анализа. Для этого отдельно готовят калибровочные растворы различной концентрации. По вышеописанному способу определяют концентрацию и находят линейный диапазон зависимости. Прототип обеспечивает линейность концентрации варфарина и 7-гидроксиварфарина в диапазоне 75-7500 нг/мл (r2>0.99).
Недостатками прототипа являются длительность способа из-за проведения хроматографического разделения образцов и недостаточная точность анализа из-за высокой нижней границы линейного диапазона зависимости концентрации от площади пика ионной плотности.
Задачей изобретения является разработка более быстрого, точного и достоверного способа определения концентрации варфаринового спирта.
Техническим результатом является повышение точности и сокращение длительности способа.
Поставленная задача достигается заявляемым способом, заключающимся в следующем.
Предварительно готовят калибровочные растворы варфаринового спирта с концентрацией 0, 10, 25, 50, 75, 100 нг/мл.
Для определения варфаринового спирта в образце используют плазму крови, полученную в период 1-96 ч после приема последней дозы варфарина.
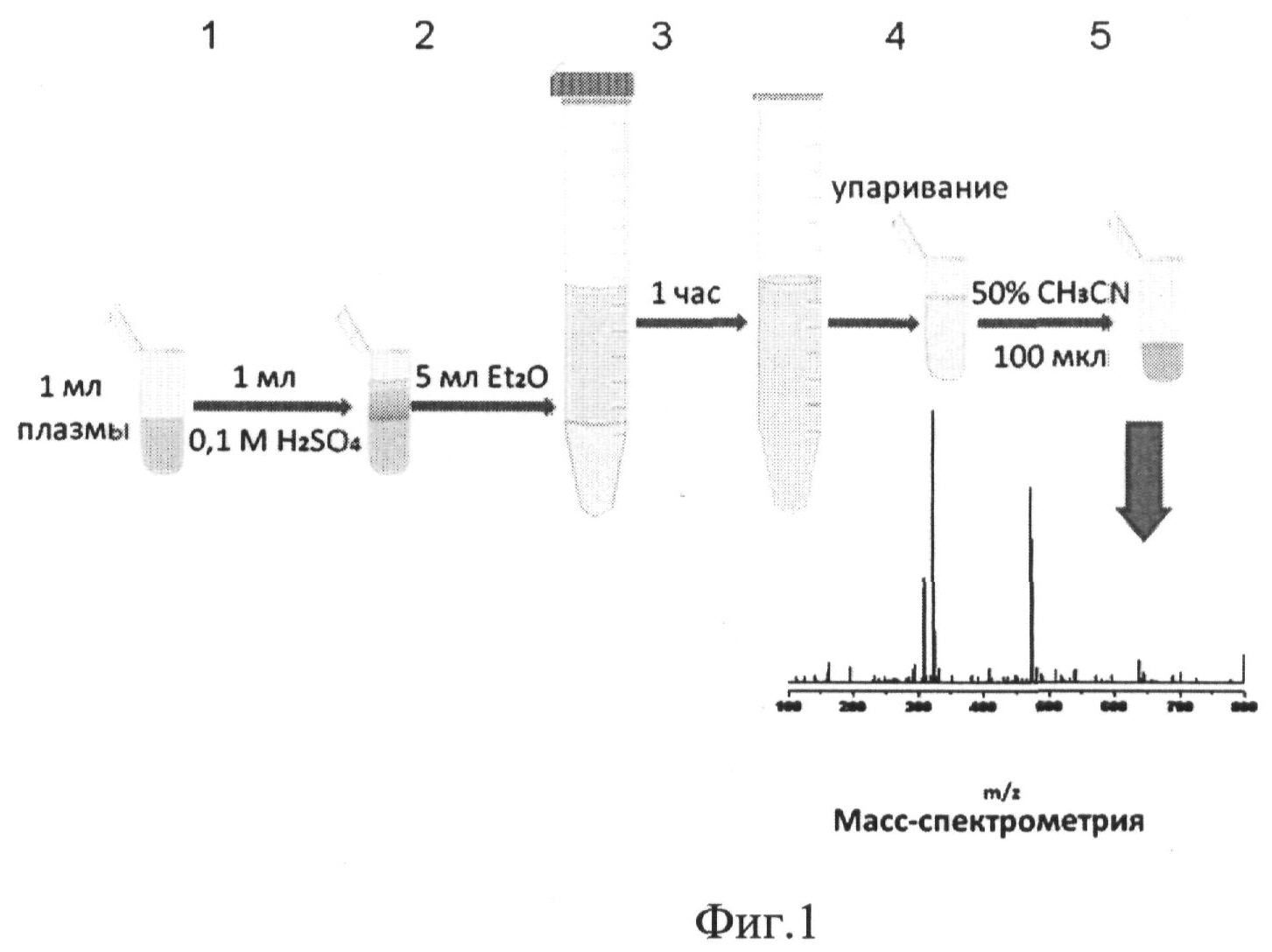
Готовят пробы исследуемых образцов к анализу путем экстракции варфаринового спирта из образца с последующим упариванием и перерастворением стандартным методом. На фиг.1 представлен процесс извлечения варфарина из плазмы крови в ходе пробоподготовки для проведения количественного анализа, где: берут 1 мл плазмы крови человека (1), добавляют 1 мл 1 М H2SO4 до рН 1 (2), добавляют 5 мл диэтилового эфира и экстрагируют варфариновый спирт в течение 1 часа при перемешивании со скоростью 250 оборотов в минуту при 25°С (3), диэтиловый эфир, содержащий варфариновый спирт, переносят в чистые пробирки и упаривают органическую фазу досуха в водяной бане при температуре при 45-50°С и токе воздуха (4), полученный варфариновый спирт растворяют путем поэтапного добавления к сухому остатку по 150 мкл 50% ацетонитрила (5).
Далее из полученного образца или калибровочного раствора отбирают аликвоту объемом 50 мкл и добавляют 250 мкл 50% ацетонитрила. Полученный раствор используют для масс-спектрометрического анализа.
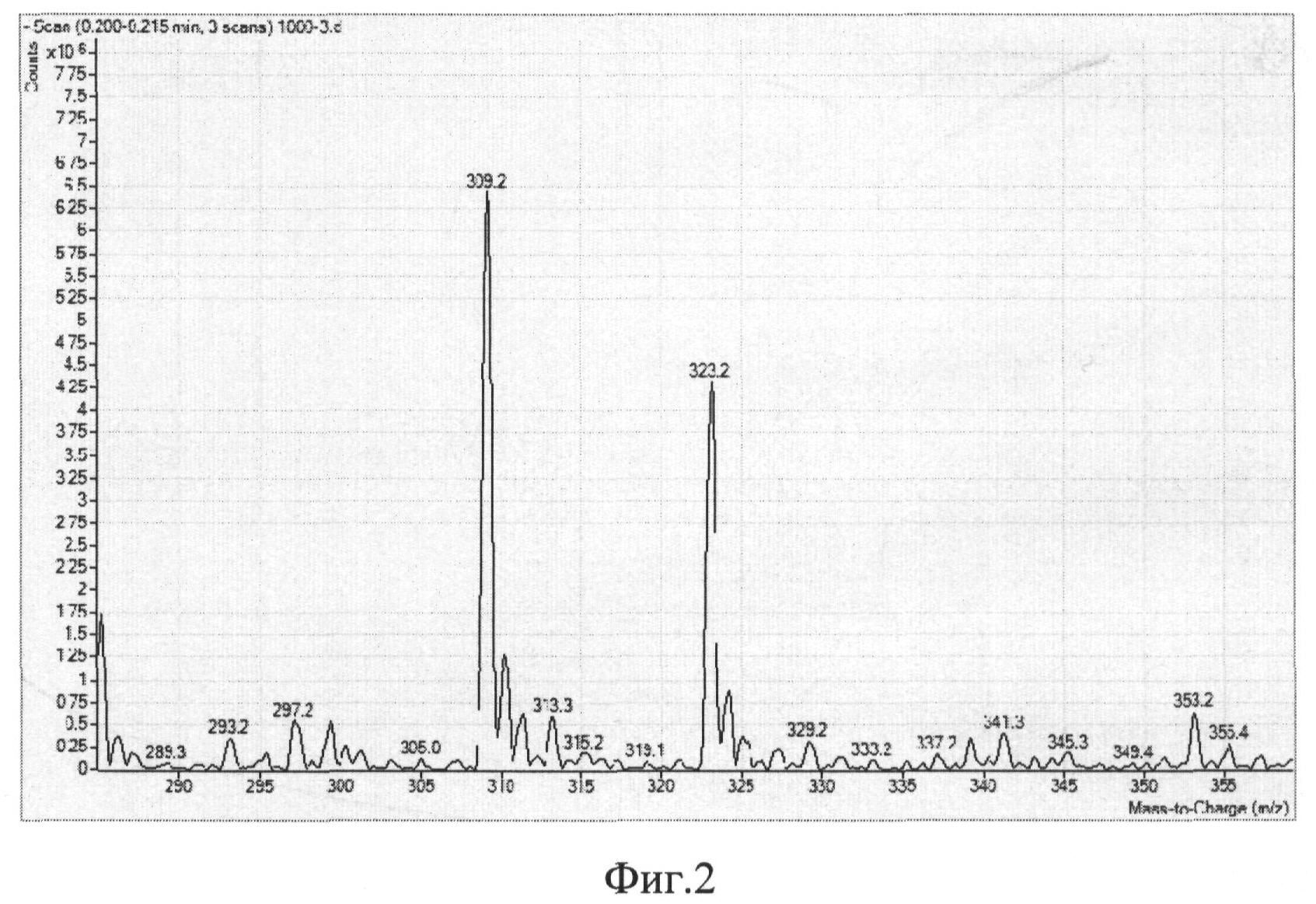
Анализ проводят на масс-спектрометре Agilent 6410 QQQ (Agilent Technologies) в режиме обнаружения отрицательных ионов. Количественный масс-спектроскопический анализ проводят в режиме сканирования MS2 без разрушения исходных молекул на осколки: стандартный масс-спектр, получаемый в ходе определения варфаринового спирта в плазме крови, представлен на фиг.2, из которой видно, что варфариновому спирту соответствует первый пик с 309,2 m/z.
С помощью программного комплекса Masshunter фирмы Agilent Technologies задают положение флакона образца (для серии до 56 образов) и калибровочных растворов в планшете и параметры анализа: объем аликвоты 50 мкл, скорость потока элюента 0,8-1 мл/мин, подвижную фазу 50% ацетонитрил, время анализа 1-2 мин, диапазон измерения 100-1000 m/z.
После проведения масс-спектрометрического анализа, производят количественное определение концентрации варфаринового спирта. Для этого по калибровочным растворам строят калибровочную зависимость: отношение площади пика ионной плотности варфаринового спирта к концентрации калибровочного раствора. Используя калибровочную зависимость, по определенной в образце площади пика ионной плотности с 309,2 m/z находят концентрацию варфаринового спирта в образце. Все расчеты производят в автоматическом режиме в программном комплексе Masshunter фирмы Agilent Technologies.
Определение точности измерения проводят в ходе выполнения анализа по использованным калибровочным растворам. При построении калибровочной зависимости автоматически проводят сопоставление определяемой концентрации варфаринового спирта в калибровочном растворе с заданной концентрацией. Способ обеспечивает линейность концентрации варфаринового спирта в диапазоне 1-100 нг/мл (r2>0.99).
Определяющими отличиями заявленного способа от прототипа являются:
1. Предварительно готовят калибровочные растворы варфаринового спирта, что позволяет уменьшить время анализа за счет определения точности измерения в ходе анализа и возможности использования калибровочных растворов для серии образцов.
2. Пробы исследуемых образцов анализируют на масс-спектрометре в режиме обнаружения отрицательных ионов со следующими параметрами анализа: объем аликвоты 50 мкл, скорость потока элюента 0,8-1,0 мл/мин, подвижная фаза 50% ацетонитрил, время анализа 1-2 мин, диапазон измерения 100-1000 m/z, что позволяет существенно сократить время анализа без разрушения исходной молекулы на осколки за счет отсутствия хроматографического разделения.
3. По калибровочным растворам строят калибровочную зависимость по отношению площади пика ионной плотности варфаринового спирта к концентрации калибровочного раствора и, используя калибровочную зависимость, по определенной в образце площади пика ионной плотности с 309,2 m/z находят концентрацию варфаринового спирта в образце, что позволяет более точно определять концентрацию варфаринового спирта
Таким образом, существенные отличительные признаки заявляемого способа, вкупе с известными, позволяют сократить длительность способа в 2 раза за счет исключения стадии предварительного хроматографического разделения образцов на обращено-фазовой колонке, а также проведения масс-спектрометрического анализа в экспериментально подобранном оптимальном режиме, и повысить точность анализа за счет использования предварительно построенной калибровочной зависимости, изменения линейного диапазона измерения концентрации, использования программы Masshunter для расчета концентрации варфаринового спирта и расширения диапазона времени, прошедшего после приема варфарина.
Изобретение иллюстрируется следующими примерами конкретного выполнения.
Пример 1.
Определение концентрации варфаринового спирта в образце плазмы крови человека, полученном через 2 часа после приема 5 мг варфарина, с использованием заявленного способа
Готовят калибровочные растворы варфаринового спирта, путем добавления к 0,8 мл плазмы здоровых доноров, не принимающих варфарин, аликвот исходного раствора варфаринового спирта с концентрацией 1 мг/мл, так, чтобы конечная концентрация составляла 0, 10, 25, 50, 75, 100 нг/мл.
Готовят пробы исследуемых образцов. Для чего к 0,8 мл плазмы крови образца или калибровочного раствора добавляют 0,8 мл 1 М H2SO4 (pH 1), смесь перемешивают путем вращения пробирки вокруг ее вертикальной оси в течение 30 секунд и добавляют 4 мл диэтилового эфира. Варфариновый спирт экстрагируют в течение 1 часа при перемешивании со скоростью 250 оборотов в минуту при 25°С. После перемешивания диэтиловый эфир, содержащий варфариновый спирт, переносят в чистые пробирки. Органическую фазу упаривают досуха в водяной бане при V температуре при 45°С и токе воздуха (для повышения скорости упаривания) в течение 30 минут. Полученный варфариновый спирт растворяют путем поэтапного добавления к сухому остатку по 150 мкл 50% ацетонитрила. После этого пробирку омывают 150 мкл 100% ацетонитрила и растворы объединяют. Из образца или калибровочного раствора отбирают аликвоту объемом 50 мкл и добавляют 250 мкл 50% ацетонитрила. Полученный раствор используют для масс-спектрометрического анализа.
Анализ проводят на масс-спектрометре Agilent 6410 QQQ (Agilent Technologies) в режиме обнаружения отрицательных ионов. В качестве десольватирующего газа используется азот (3,5 л/мин). Температура источника ионов и десольватирующего газа составляла 200 и 325°С соответственно. Диссоциацию, индуцированной столкновением, не производят. Напряжение на капилляре составляло 2500 В. Количественный масс-спектроскопический анализ проводят в режиме сканирования MS2 без разрушения исходных молекул на осколки.
С помощью программного комплекса Masshunter фирмы Agilent Technologies задают положение флакона образца и калибровочных растворов в планшете и параметры анализа: объем аликвоты 50 мкл, скорость потока элюента 0,8 мл/мин, подвижную фазу 50% ацетонитрил, время анализа 2 мин, диапазон измерения 100-1000 m/z.
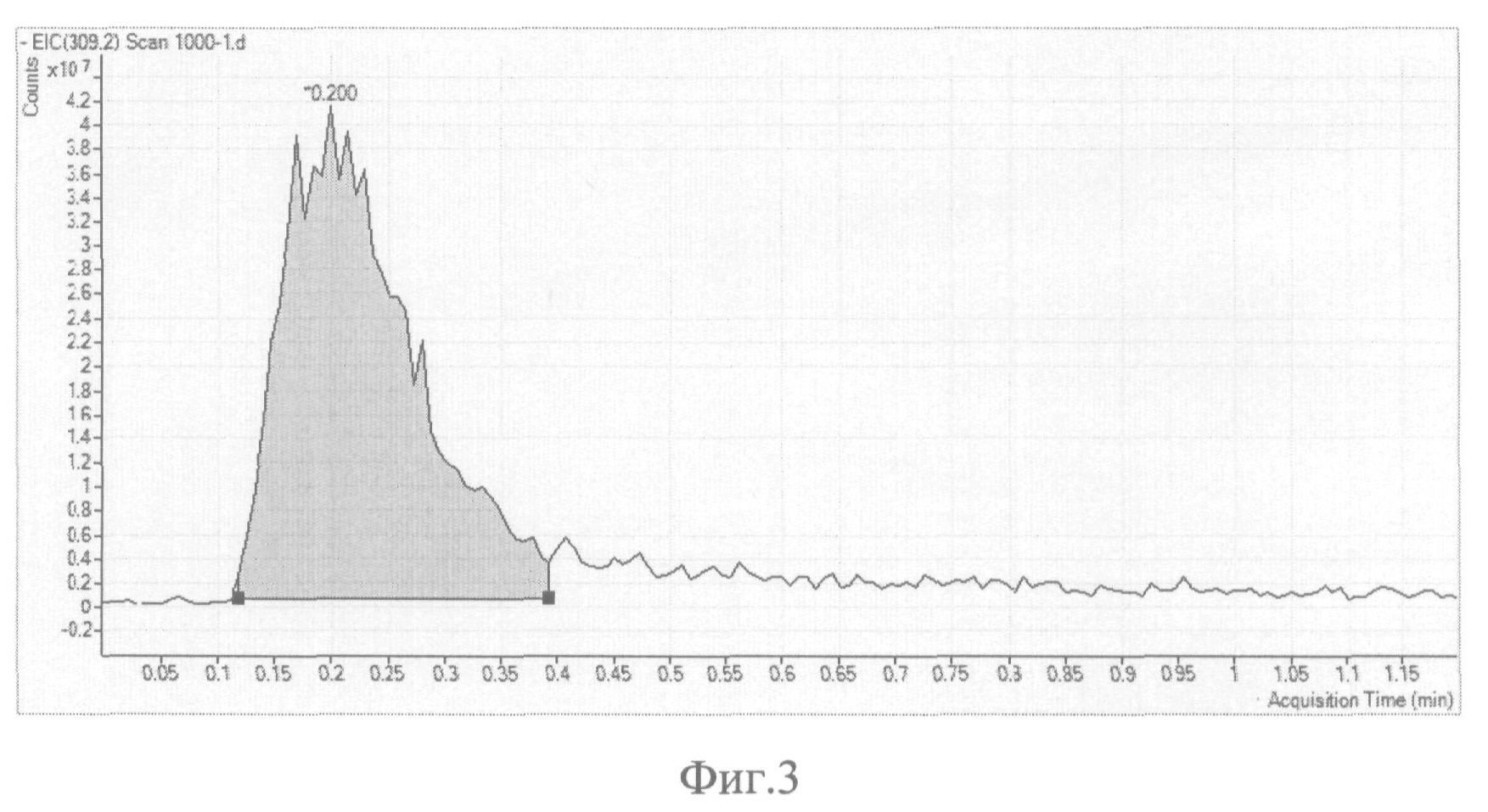
На фиг.3 представлен пример пика ионной плотности, соответствующий отношению массы к заряду 309,2 m/z. Из фиг.3 видно, что время масс-спектрометрического анализа образца варфаринового спирта составляет 0,4 мин.
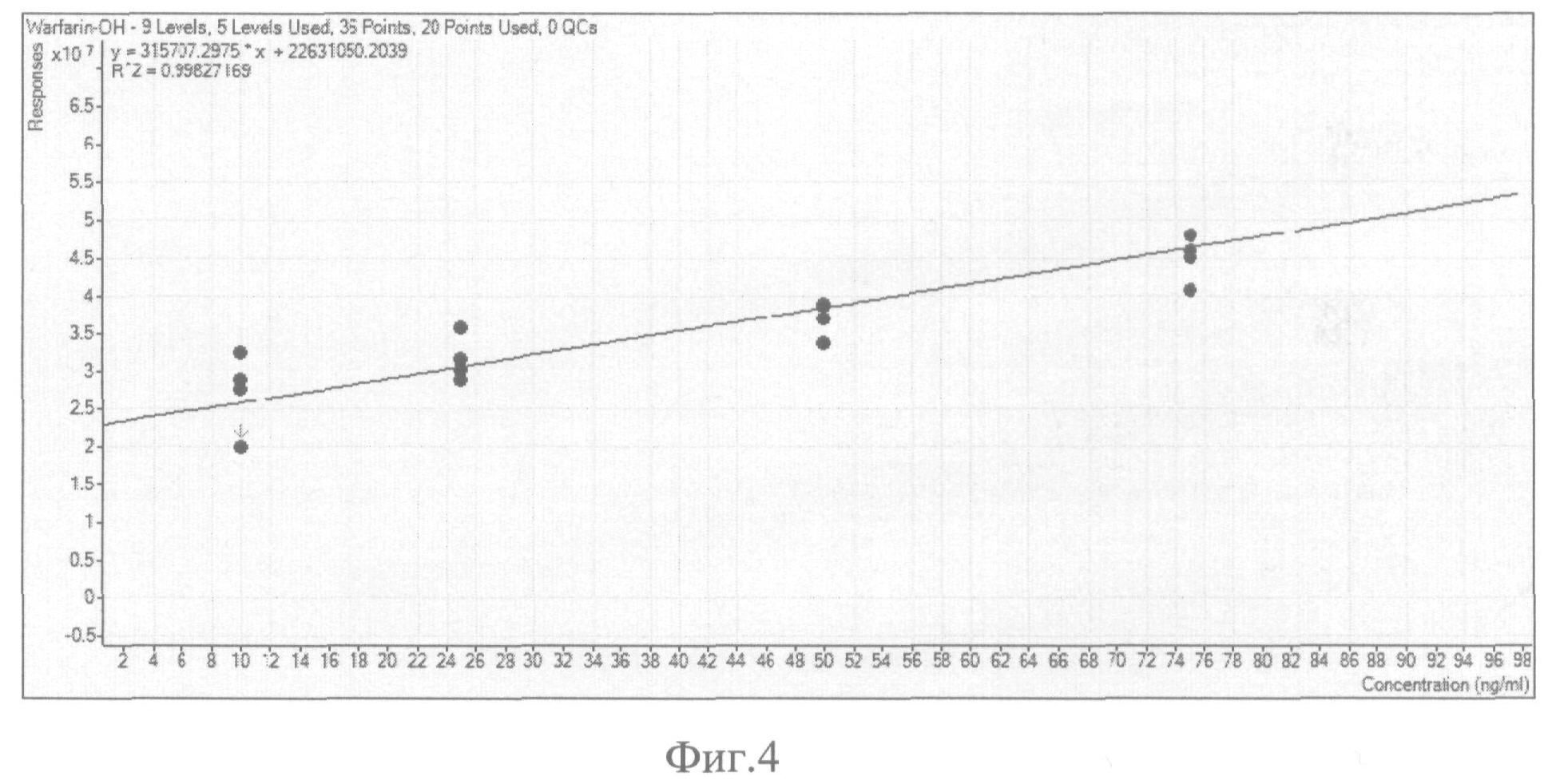
После проведения масс-спектрометрического анализа, производят количественное определение варфаринового спирта. Для этого по калибровочным растворам строят калибровочную зависимость: отношение площади пика ионной плотности варфаринового спирта к концентрации калибровочного раствора. На фиг.4. представлена калибровочная зависимость площади ионной плотности от концентрации варфаринового спирта в диапазоне 0-100 нг/мл. Используя калибровочную зависимость, по определенной в образце площади пика ионной плотности с 309,2 m/z находят концентрацию варфаринового спирта в образце. Все расчеты производят в автоматическом режиме в программном комплексе Masshunter фирмы Agilent Technologies.
В результате определяют концентрацию варфаринового спирта - 32 нг/мл.
Пример 2.
Определение концентрации варфаринового спирта в серии образцов плазмы крови человека, полученных через 0-74 часа после приема 5 мг варфарина, с использованием заявляемого способа
Готовят калибровочные растворы варфаринового спирта, путем добавления к 1 мл плазмы здоровых доноров, не принимающих варфарин, аликвот исходного раствора варфаринового спирта, так, чтобы конечная концентрация составляла 0, 10, 25, 50, 75, 100 нг/мл.
К 1 мл плазмы крови образца или калибровочного раствора добавляют 1 мл 1 М H2SO4 (pH 1), смесь перемешивают путем вращения пробирки вокруг ее вертикальной оси в течение 30 секунд и добавляют 5 мл диэтилового эфира. Варфариновый спирт экстрагируют в течение 1 часа при перемешивании со скоростью 250 оборотов в минуту при 25°С. После перемешивания диэтиловый эфир, содержащий варфариновый спирт, переносят в чистые пробирки. Органическую фазу упаривают досуха в водяной бане при температуре при 50°С и токе воздуха (для повышения скорости упаривания) в течение 25 минут. Для каждого образца полученный варфариновый спирт растворяют путем поэтапного добавления к сухому остатку по 150 мкл 50% ацетонитрила. После этого пробирку омывают 150 мкл 100% ацетонитрила и растворы объединяют. Из образца или калибровочного раствора отбирают аликвоту объемом 50 мкл и добавляют 250 мкл 50% ацетонитрила. Полученный раствор используют для масс-спектрометрического анализа.
Анализ проводят на масс-спектрометре Agilent 6410 QQQ (Agilent Technologies) в режиме обнаружения отрицательных ионов аналогично примеру 1.
С помощью программного комплекса Masshunter фирмы Agilent Technologies задают положение флакона образца (до 112 образов) и калибровочных растворов в планшете и параметры анализа: объем аликвоты 50 мкл, скорость потока элюента 1,0 мл/мин, подвижную фазу 50% ацетонитрил, время анализа 1 мин, диапазон измерения 100-1000 m/z. Проводят масс-спектрометрический анализ.
После проведения масс-спектрометрического анализа, по калибровочным растворам строят калибровочную зависимость и находят концентрацию варфаринового спирта в образце аналогично примеру 1.
В таблице представлены полученные значения концентрации варфаринового спирта.
|
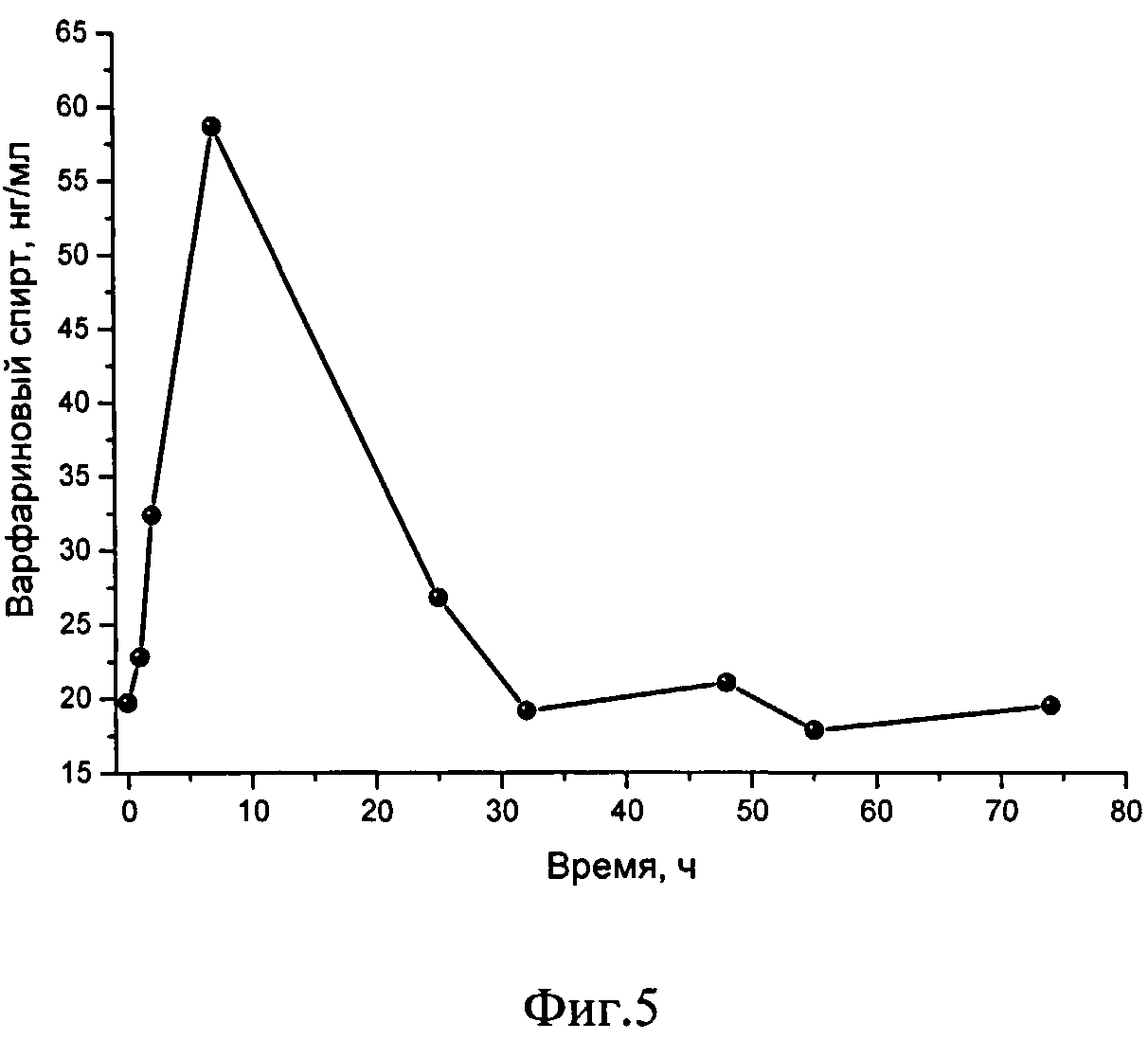
На фиг.5. представлен график изменения концентрации варфаринового спирта в процессе его метаболизма в организме человека.
Использование способа позволит повысить скорость, точность и достоверность определения концентрации варфаринового спирта в плазме крови, а также исключить наиболее часто встречающиеся ошибки определения. Полученные с помощью данного способа данные могут быть использованы в фармакокинетике для определения параметров метаболизма как варфаринового спирта, так и варфарина.