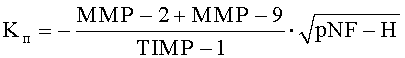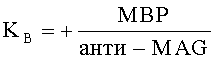Результат интеллектуальной деятельности: СПОСОБ ЛЕЧЕНИЯ БОЛЬНЫХ С ОСЛОЖНЕННОЙ ТРАВМОЙ ШЕЙНОГО ОТДЕЛА ПОЗВОНОЧНИКА
Вид РИД
Изобретение
Изобретение относится к медицине, в частности к нейрохирургии и клинической лабораторной диагностике, и может быть использовано с целью оптимизации тактики лечения больных с осложненной травмой шейного отдела позвоночника путем выбора рациональных средств и методов лечения, направленных на уменьшение вторичных альтерирующих факторов, а также увеличение регенераторного потенциала в поврежденной нервной ткани спинного мозга.
Несмотря на большой прогресс в технике операций на позвоночнике и спинном мозге, развитие анестезиологии и реанимации, до сих пор отсутствуют эффективные методы хирургического или терапевтического воздействия на поврежденный спинной мозг.
Основными направлениями современных исследований являются поиск возможностей предотвращения вторичного повреждения спинного мозга, а также выявление условий регенерации и восстановления функции поврежденных клеток. Общепризнанным является положение о вторичном повреждении нервной ткани, которое начинается с момента травмы и продолжается длительное время, захватывая неповрежденную ткань вещества спинного мозга.
На современном этапе патогенез травматической болезни спинного мозга связан с концепцией первичного и вторичного повреждения нервной ткани. Травматический агент (смещенные фрагменты позвонков, межпозвонковых дисков, инородное тело) приводят к локальному механическому повреждению, нарушению кровообращения и ишемии ткани спинного мозга. В результате этого формируется локальный некротический очаг первичного повреждения спинного мозга. Некрозу подвергаются как тела нервных, глиальных клеток, так и проводящие волокна спинного мозга. Некротическая гибель клеток связана с чрезмерным механическим или ишемическим повреждением, выдержать которое клеточные мембраны не способны. Это приводит к нарушению энергообеспечения, набуханию и распаду клетки. Наблюдается сдвиг ионных потенциалов, массивный выход протеолитических ферментов и нейромедиаторов. Накапливаются продукты распада клеток, биологически активные вещества (цитокины), которые активируют универсальную реакцию тканей на травму - синдром системного воспалительного ответа. Повреждение мозга не останавливается на этом этапе, а продолжается длительное время после первичной травмы, захватывая новые, изначально неповрежденные участки спинного мозга. Процесс вторичного повреждения развивается в ранние сроки (1-14 сутки) с момента получения травмы и вызывает каскад реакций, приводящих к стойким морфологическим и функциональным изменениям в нервной ткани.
Одним из эффективных методов воздействия на поврежденную нервную ткань является проведение электростимуляции в послеоперационном периоде, позволяющей улучшить процесс проведения нервного импульса и увеличить регенераторный потенциал в нервной ткани. Однако сроки проведения электростимуляции требуют уточнения.
Известны способы лечения повреждений и заболеваний спинного мозга и его корешков, основанные на применении электростимуляции спинного мозга в ранние сроки после проведения хирургического вмешательства [авторское свидетельство SU на изобретение №1333341, патент RU на изобретение №2140798].
Однако проведение электростимуляции в сроки менее 7 дней после хирургического вмешательства на фоне развития второй волны апоптоза может негативно сказываться на результатах лечения вследствие усиления активности метаболических процессов в поврежденной нервной ткани, усиления микроциркуляции, увеличение степени выраженности отека, что приводит к нарастанию альтерирующих влияний.
Наиболее близким аналогом к заявляемому изобретению является способ лечения поражений шейного отдела позвоночника [патент RU на изобретение №2333017]. Способ включает проведение декомпрессии спинного мозга, электростимуляции и электрофореза с нейропротекторами на шейный отдел позвоночника в послеоперационном периоде. При этом электрофорез начинают с первого дня после операции и осуществляют его в течение 15-22 дней, причем в течение первых 1-3 дней его проводят с нейропротекторными препаратами или с биогенными стимуляторами, затем в течение 10-14 дней - с глюкокортикоидными, после чего - со спазмолитическими средствами. Это позволяет перекрыть клинически и экспериментально второй пик процесса апоптоза (7-14 сутки). Проведение же электрофореза в течение первых 1-3 дней его с нейропротекторными препаратами или с биогенными стимуляторами позволяет затормозить развитие патологического процесса апоптоза нервных клеток, что способствует сохранению изначально неповрежденных клеток и улучшению выживаемости нейронов, глин, их связей. Введение нейропротекторов электрофоретически на шейный отдел позвоночника обеспечивает локальное воздействие на заинтересованный участок спинного мозга без системного влияния на организм. Начинают электростимуляцию с 3-4 дня и проводят в течение 10-14 дней, осуществляя при этом электростимуляцию стволов плечевого сплетения в надключичной области и по ходу пораженного корешка в области предплечья. Это способствует восстановлению проводимости эфферентных и афферентных путей спинного мозга, но и направленно перемещает накапливаемые лекарственные средства по спинно-мозговым корешкам и периферическим нервам.
Однако применение вышеуказанного способа, основанного на применении электростимуляции с 3-4 дня после хирургического вмешательства, может приводить к усилению степени выраженности отека нервной ткани за счет увеличения интенсивности метаболических процессов вследствие развития артериальной гиперемии. Персонализированный подход, основанный на тестировании маркеров апоптоза в течение 7 суток с момента хирургического вмешательства, позволяет считать, что процесс вторичной альтерации длится более чем 4 дня, следовательно, применение электростимуляции в сроки до 7 дней может неблагоприятно сказываться на результатах лечения.
Задачей заявляемого изобретения является разработка способа лечения больных с осложненной травмой шейного отдела позвоночника, позволяющего повысить эффективность проводимого комплексного лечения при уменьшении риска возникновения послеоперационных осложнений и сокращении сроков начала реабилитационно-восстановительных мероприятий.
Сущность заявляемого изобретения характеризуется тем, что в способе лечения больных с осложненной травмой шейного отдела проводят хирургическое вмешательство путем выполнения декомпрессии спинного мозга, стабилизации поврежденных позвоночно-двигательных сегментов и установки в эпидуральное пространство катетеров для последующего выполнения локальной гипотермии спинного мозга, с первого дня после хирургического вмешательства осуществляют противоотечную терапию путем проведения локальной гипотермии спинного мозга, на каждые 7-е сутки с момента хирургического вмешательства производят забор крови, готовят образцы сыворотки крови, осуществляют исследование сыворотки крови с помощью иммуноферментного анализа, при этом определяют количественные значения уровня содержания матриксных металлопротеиназ ММР-2 и ММР-9, антинейронального иммуноглобулина анти-MAG, фосфорилированного нейрофиламента pNF-H, основного белка миелина МВР, тканевого ингибитора металлопротеиназ TIMP-1, считают коэффициенты повреждения нервной ткани 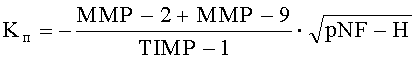 и восстановления нервной ткани
и восстановления нервной ткани 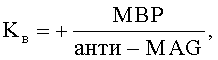 оценивают полученные значения коэффициентов и в зависимости от их суммарного значения ∑Kп+Kв:
оценивают полученные значения коэффициентов и в зависимости от их суммарного значения ∑Kп+Kв:
- при отрицательных значениях продолжают проведение локальной гипотермии спинного мозга;
- при положительных значениях заканчивают проведение локальной гипотермии спинного мозга, удаляют катетеры, пункционно через межостистые промежутки устанавливают электроды в эпидуральное пространство выше и ниже уровня поврежденного позвонка и начинают сеансы электростимуляции спинного мозга. Кроме того, заявляется способ лечения больных с осложненной травмой шейного отдела позвоночника с вышеописанными признаками, в котором электростимуляцию осуществляют в течение 30 дней.
Технический результат заявляемого изобретения.
Заявляемый способ позволяет повысить эффективность лечения больных с осложненной травмой шейного отдела позвоночника путем выбора персонализированной тактики, основанной на начале проведения эпидуральной стимуляции спинного мозга по достижению регресса явлений восходящего отека спинного мозга, определяемого по описанному в данной заявке способу оценки соотношения показателей повреждения и восстановления нервной ткани. Отрицательные показатели маркеров ремоделирования позволяют судить о доминировании процесса дегенерации нервной ткани и служит критерием для продолжения проведения противоотечной терапии. Одним из таких методов является локальная гипотермия спинного мозга, создающая лечебный эффект гибернации в условиях травматической болезни спинного мозга, восстанавливая тканевой гомеостаз. В свою очередь, применение гипотермии позволяет ограничить зону первичного очага повреждения и предупредить развитие каскада вторичных альтерирующих факторов, а также начать комплекс реабилитационно-восстановительных мероприятий, включающих методы прямой электростимуляции.
Метод эпидуральной электростимуляции, выполненный после регресса явлений вторичного повреждения, позволяет увеличить регенераторный потенциал в поврежденной нервной ткани спинного мозга за счет улучшения проводимости нервных импульсов и восстановления органной микроциркуляции, не вызывая при этом развития восходящего отека спинного мозга. Это способствует повышению устойчивости нейрональных структур к повреждающему воздействию биологически активных веществ и аутоантител. В результате облегчается реализация аксонального транспорта и синаптической передачи, что создает предпосылки для улучшения условий проведения импульса по восстанавливающимся нервным проводникам. Это позволяет считать метод прямой электростимуляции как один из наиболее перспективных и эффективных способов лечения позвоночно-спинно-мозговой травмы. Но сроки начала проведения электростимуляции, основанные только на эмпирическом подходе, могут не оказать должного эффективного влияния, либо повлиять негативно за счет усиления микроциркуляции в поврежденной нервной ткани, возникновения артериальной гиперемии, увеличения степени выраженности восходящего отека спинного мозга. Поэтому установление оптимальных и достоверных сроков регресса каскада альтерирующих факторов позволяет уменьшить риск возникновения осложнений, сократить сроки начала реабилитационно-восстановительных мероприятий и улучшить ближайшие и отдаленные результаты хирургического лечения больных с осложненной травмой шейного отдела позвоночника.
Способ лечения больных с осложненной травмой шейного отдела позвоночника осуществляют следующим образом.
Первоначально осуществляют клиническое обследование больных с помощью стандартных методов, т.е. с оценкой жалоб и соматического статуса, детальным сбором анамнеза с выявлением факторов, влияющих на иммунный статус.
После клинического обследования больных и подтверждения наличия осложненной травмы шейного отдела позвоночника осуществляют декомпрессивно-стабилизирующее хирургическое вмешательство, во время проведения которого в эпидуральное пространство устанавливают катетеры для осуществления локальной гипотермии, охлажденным физиологическим раствором. С первого дня после хирургического вмешательства проводят стандартное медикаментозное лечение, направленное на улучшение метаболических процессов в нервной ткани, противоотечную терапию путем выполнения локальной гипотермии спинного мозга и профилактику гнойно-воспалительных осложнений. На каждые 7-е сутки с момента получения травмы в асептических условиях производят забор крови из периферической вены в пробирку 5 мл. С помощью центрифугирования получают сыворотку крови. Полученные образцы сыворотки крови тестируют методом иммуноферментного анализа. При этом определяют в полученной сыворотке крови количественные значения содержания уровней, матриксных металлопротеиназ ММР-2 и ММР-9, антинейронального иммуноглобулина анти-MAG, фосфорилированного нейрофиламента pNF-H, основного белка миелина МВР, тканевого ингибитора металлопротеиназ TIMP-1. На основании полученных фактических значений исследуемых биологических маркеров считают коэффициенты повреждения Kп и восстановления Kв нервной ткани по формулам:
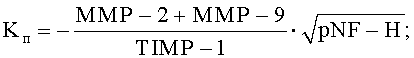
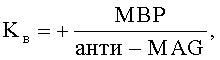
где Kп - коэффициент повреждения нервной ткани,
«-» - отрицательное значение, отражающее потерю основной массы ткани и внеклеточного матрикса,
ММР-2 - уровень матриксной металлопротеиназы 2,
ММР-9 - уровень матриксной металлопротеиназы 9,
TIМР-1 - уровень тканевого ингибитора металлопротеиназ 1,
pNF-H - уровень фосфорилированного нейрофиламента,
Kв - коэффициент восстановления нервной ткани,
«+» - положительное значение, отражающее увеличение основной массы ткани и внеклеточного матрикса,
МВР - уровень основного белка миелина,
n - титр антинейрональных антител,
анти-MAG - уровень антинейронального иммуноглобулина.
Затем оценивают полученные значения коэффициентов. В зависимости от их суммарного значения:
- при отрицательных значениях продолжают проведение локальной гипотермии спинного мозга;
- при положительных значениях заканчивают проведение локальной гипотермии спинного мозга, удаляют катетеры, пункционно через межостистые промежутки устанавливают электроды в эпидуральное пространство выше и ниже уровня поврежденного позвонка и начинают сеансы электростимуляции спинного мозга в большинстве случаев в течение 30 дней.
Пример.
Пациент П., 32 лет, поступил в отделение нейрохирургии на 2-м часу с момента получения травмы с диагнозом: «Закрытая осложненная травма шейного отдела позвоночника. Компрессионно-оскольчатый нестабильный перелом тела С3 позвонка с дислокацией костных фрагментов в просвет позвоночного канала. Ушиб и сдавление спинного мозга на этом уровне. Тетраплегия. Нарушение функций тазовых органов по центральном типу». В неврологическом статусе был выявлен синдром поражения каудальных отделов ствола головного мозга в виде дисфонии, снижения глоточных рефлексов с обеих сторон; вялая тетраплегия 0 баллов, с отсутствием всех видов чувствительности с уровня С2 - сегмента с двух сторон; нарушение функций тазовых органов по типу задержки. По экстренным показаниям пациенту была выполнена декомпрессивно-стабилизирующая операция на шейном отделе позвоночника: «Резекция С3 позвонка, передняя декомпрессия дурального мешка, вентральный бисегментарный корригирующий спондилодез эндопротезом «Mesh». фирмы «Medtronic». Накостная бисегментарная фиксация С2-С4 позвонков пластиной «Atlantis». фирмы «Medtronic». В эпидуральное пространство установлены катетеры для проведения локальной гипотермии спинного мозга». Для дальнейшего лечения пациент переведен в отделение реанимации.
С первого дня после хирургического вмешательства производили стандартное медикаментозное лечение, направленное на улучшение метаболических процессов в нервной ткани, противоотечную терапию путем проведения локальной гипотермии спинного мозга и профилактику гнойно-воспалительных осложнений.
На 7-е сутки с момента проведения хирургического вмешательства пациенту осуществили забор крови из периферической вены для выполнения иммуноферментного анализа. При этом определили количественные значения уровней содержания отдельных биологических маркеров: ММР-2 - 182.2 пг/мл; ММР-9 - 160.3 пг/мл; TIMP-1 - 172.1 пг/мл: МВР - 345.4 нг/мл; анти-MAG - 1:80; pNF-H - 3212. Были рассчитаны коэффициенты Kп и Kв.
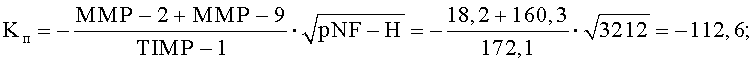
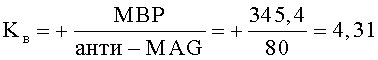
Рассчитали суммарное значение полученных коэффициентов: ∑Kп+Kв=-112,6+4,31=-108,29. Таким образом, по полученным данным было принято решение о продолжении противоотечной терапии восходящего отека спинного мозга путем проведения сеансов локальной гипотермии охлажденным до +5°С раствором натрия хлорида 1 раз в сутки со скоростью 40 кап/мин в течение 60 минут. На 14-е сутки с момента проведения хирургического вмешательства пациенту повторно осуществили забор крови из периферической вены для выполнения иммуноферментного анализа. Получили сыворотку крови и определили количественные значения уровней содержания отдельных биологических маркеров: ММР-2 - 37,4 пг/мл; ММР-9 - 32,1 пг/мл; TIMP-1 - 398,9 пг/мл; МВР - 236,4 нг/мл: анти-MAG - 10: pNF-H - 134,2 пг/мл. Были рассчитаны коэффициенты Kп и Kв.
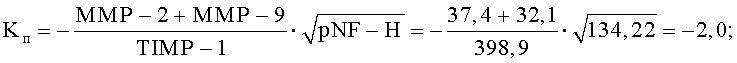
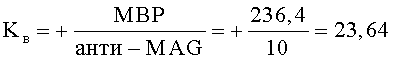
Рассчитали суммарное значение полученных коэффициентов:
∑Kп+Kв=-2,0+23,64=21,64. Учитывая полученные результаты, было принято решение о начале проведения эпидуральной электростимуляции по стандартной методике в течение 30 дней по 3 раза в день. По окончанию сеансов электростимуляции у больного отмечали положительную динамику в виде: появления минимальных движений в обеих кистях, возникновения мышечно-суставного чувства в нижних конечностях и формирования спинального автоматизма к физиологическим отправлениям.