СПОСОБ ПОВЫШЕНИЯ ПРОНИЦАЕМОСТИ ЭПИТЕЛИАЛЬНОГО БАРЬЕРА
Вид РИД
Изобретение
Перекрестная ссылка на родственные заявки
Настоящая заявка заявляет приоритет по временной заявке США №61/328,723 с датой подачи 28 апреля 2010, по временной заявке США №61/411,085 с датой подачи 8 ноября 2010 и по временной заявке США №61/435,963 с датой подачи 25 января 2011, все из которых включены в настоящий документ в полном объеме посредством ссылки.
Уровень техники
Долгожданной целью является нацеленная доставка лекарственного средства, при которой агент (например, лекарственное средство или терапевтическое средство) доставляется в активном состоянии в конкретный тип клеток или тканей в эффективных концентрациях. Для достижения этой цели необходимо преодолеть множество трудностей. Например, прежде всего, агент должен успешно доставляться в желательную мишень. Основные способы доставки, применяемые в настоящее время, включают пероральную доставку и инъекции. Однако инъекции являются болезненными, и оба способа склонны обеспечивать скорее выброс агентов, нежели предпочтительную постоянную доставку. Кроме того, человеческий организм разработал множество систем, чтобы предотвращать приток чужеродных веществ, причем одной из наиболее успешных является разнообразие структурных компонентов, которые предотвращают свободное перемещение соединений через барьеры, сформированные эпителиальной тканью, например, кожей.
Материалы для трансдермальной доставки были разработаны в целях попытки обеспечить безболезненный способ доставки активных агентов в течение продолжительного периода. Для того чтобы быть успешной схема трансдермальной доставки должна доставлять агент через эпидермис, первичной функцией которого является защита от чужеродных веществ. Самый внешний слой эпидермиса, роговой слой, обладает структурной стабильностью, обеспеченной перекрывающимися корнеоцитами и сшитыми кератиновыми волокнами, удерживаемыми вместе десмосомами и находящимися внутри липидного матрикса, все из которых обеспечивают отличную барьерную функцию. Под роговым слоем лежит зернистый слой, внутри которого между кератиноцитами формируются плотные контакты. Плотные контакты представляют собой барьерные структуры, которые включают сетку из трансмембранных белков, погруженных в соседние плазматические мембраны (например, клаудины, окклюдин и синаптические адгезионные молекулы), а также множество белков бляшки (например, ZO-1, ZO-2, ZO-3, цингулин, симплекин). Плотные контакты обнаруживаются во внутреннем эпителии (например, эпителий тонкой кишки, гемоэнцефалический барьер), а также в зернистом слое кожи. Под роговым слоем и зернистым слоем лежит шиповатый слой. Шиповатый слой включает клетки Лангерганса, которые представляют собой дендритные клетки, которые могут стать полностью функционирующими антиген-презентирующими клетками и могут создавать иммунный ответ и/или ответ на чужеродное тело в отношении проникающего агента.
Не смотря на сложности преодоления естественных границ, был достигнут прогресс в достижении доставки активных агентов через эпителиальные барьеры. К сожалению, способы трансдермальной доставки, существующие в настоящее время, ограничены до доставки низкомолекулярных агентов, которые имеют умеренную липофильность и не имеют заряда. Даже при успешном преодолении естественных границ, все еще остаются проблемы, связанные с поддержанием уровня активности доставленных агентов и отторжением чужеродного тела, и иммунным ответом.
Применение дополнительных способов, чтобы повысить трансдермальную доставку активных агентов, улучшило этот способ доставки. Например, устройства на основе микроигл, как было обнаружено, полезны при переносе материала в или через кожу. В общем, устройство на основе микроигл включает множество игл, которые могут проникать через роговой слой кожи и достигать нижележащего слоя. Примеры устройств на основе микроигл были описаны в патенте США №6,334,856, принадлежащем Allen, et al., и в патенте США №.7,226,439, принадлежащем Prausnitz, et al., оба из которых включены в настоящий документ посредством ссылки.
Исследователи поняли молекулярный мир, в котором осуществляются функции доставки, при попытке улучшить трансдермальную доставку. Например, хитозан, как было обнаружено, эффективен при открытии плотных контактов в эпителии тонкой кишки (смотрите, например, Sapra, et al., AAPS Pharm. Sci. Tech., 10(1), March, 2009; Kaushal, et al., Sci. Pharm., 2009; 77; 877-897). Кроме того, нанотопография поверхности, соседней с клеткой, как было обнаружено, влияет на адгезивные характеристики между обеими, а также влияет на поведение клетки, включая морфологию, подвижность, цитоскелет структуру, пролиферацию и дифференциацию (смотрите, например, Hart. et al., European Cells and Materials, Vol.10, Suppl. 2, 2005; Lim, et al., J R Soc Interface, March 22, 2005, 2(2), 97-108; Yim, et al., Biomaterials, September, 2005, 26(26), 5405-5413). В качестве расширения этого первоначального исследования была изучена нанотопография поддерживающих субстратов с точки зрения применения в тканевой инженерии (смотрите, например, публикацию заявки на патент США №2008/0026464, принадлежащей Borenstein, et al., публикацию заявки на патент США №2008/0311172, принадлежащей Schapira, et al.).
Несмотря на то, что выше описываются улучшения в данной области техники, все еще сохраняется потребность в усовершенствованиях. Например, были бы предпочтительны устройства и способы, которые обеспечивают эффективную доставку активных агентов через клеточный барьер, включая эпителиальную ткань.
Сущность изобретения
Согласно одному варианту выполнения настоящего изобретения раскрывается способ повышения проницаемости клеточного слоя. Способ может включать контакт клеточного слоя с поверхностью устройства, причем клеточный слой содержит эпителиальные клетки. Поверхность содержит множество наноструктур, образованных на поверхности. Более конкретно, наноструктуры могут располагаться предопределенным образом. После контакта между клеточным слоем и поверхность в отношении лекарственного, клеточный слой может проявлять повышенную проницаемость в отношении лекарственного соединения.
Краткое описание чертежей
Полное и достаточное раскрытие объекта изобретения, включая наилучший вариант его выполнения, направленное на специалистов в данной области техники, излагается более конкретно в следующей части описания изобретения, в которой делаются ссылки на приложенные фигуры, где:
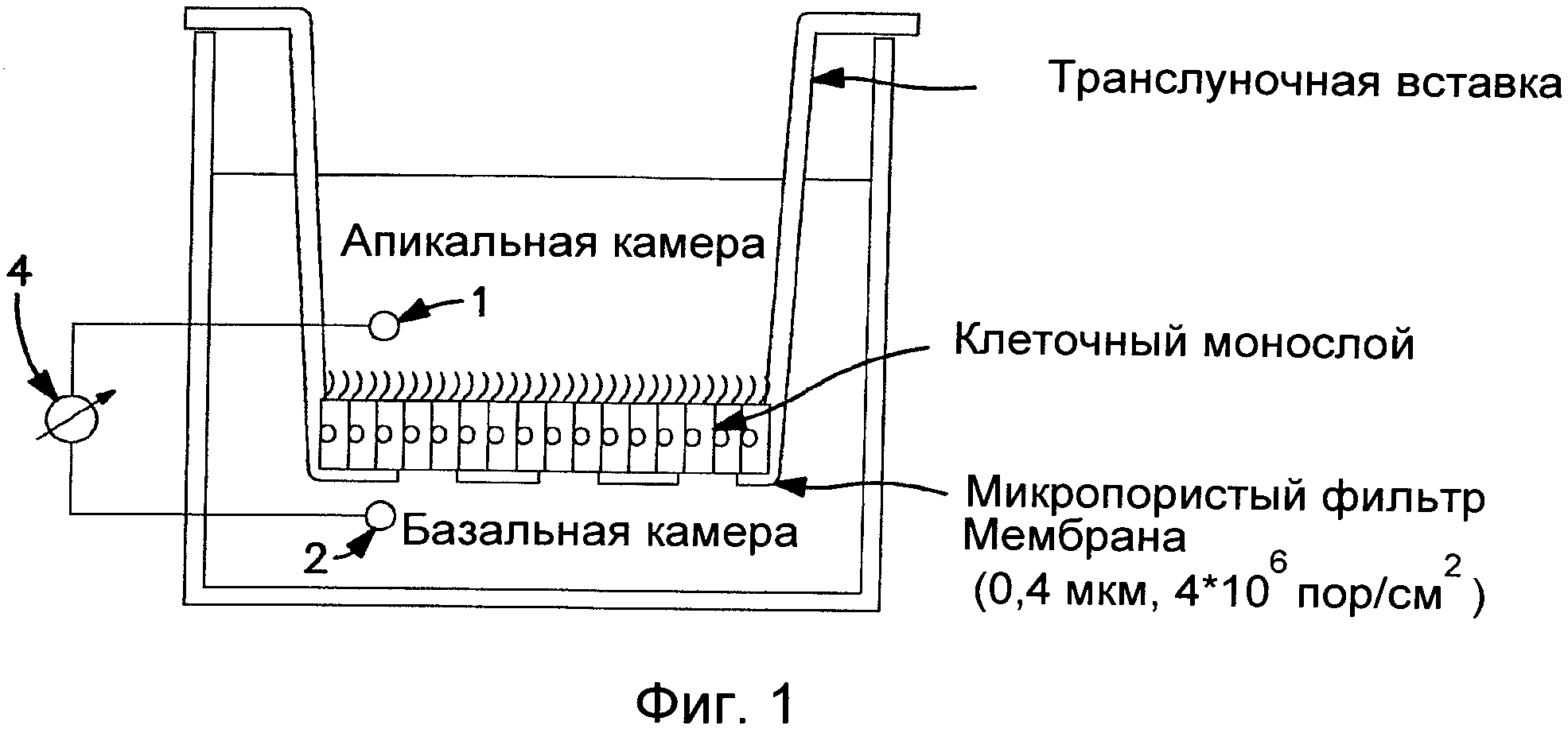
Фиг.1 иллюстрирует способ определения TEER клеточного слоя.
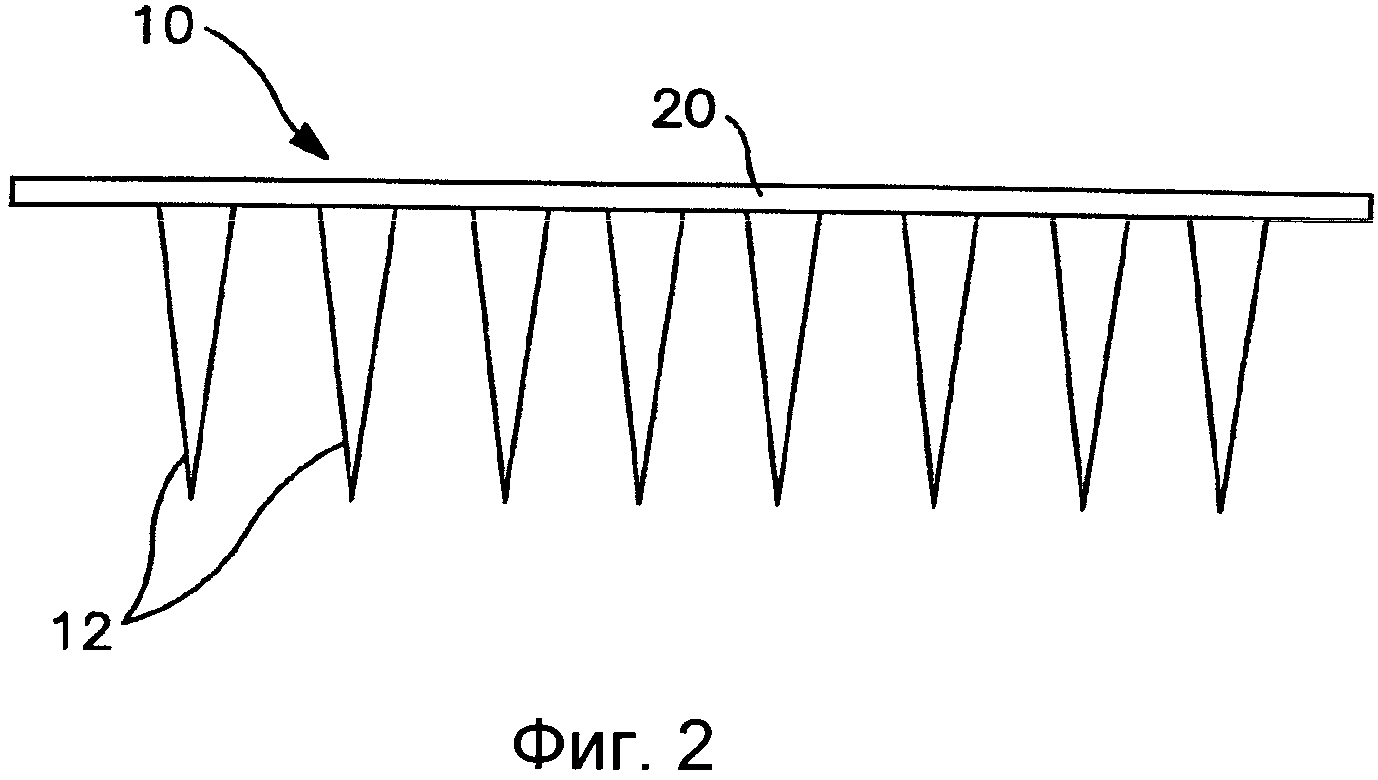
Фиг.2 иллюстрирует один вариант выполнения устройства на основе ми крои гл.
Фиг.3 иллюстрирует другой вариант выполнения устройства на основе ми крои гл.
Фиг.4 иллюстрирует один вариант выполнения микроиглы, включая поверхность, которая определяет нанотопографию.
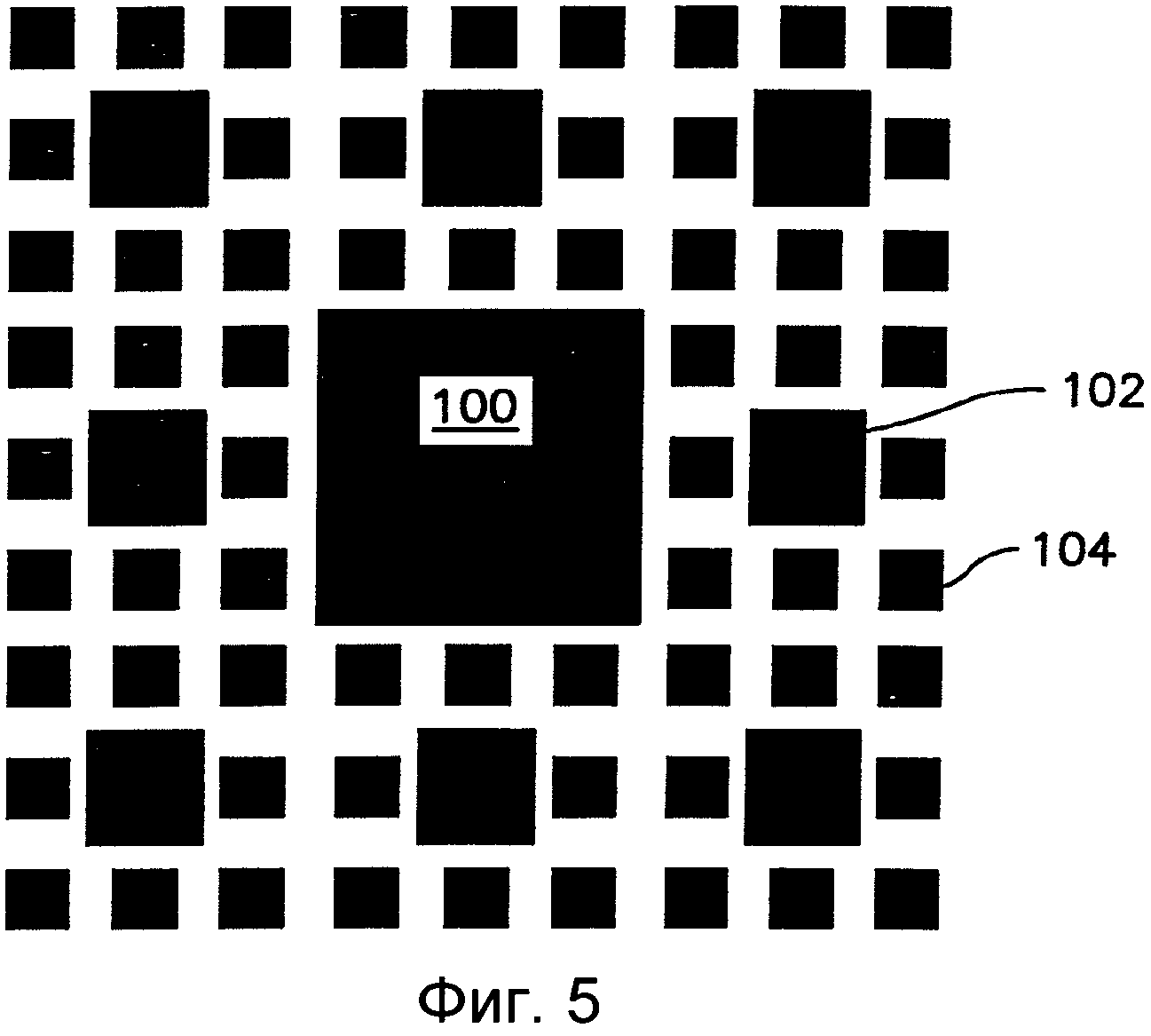
Фиг.5 иллюстрирует один вариант выполнения сложного рисунка, который может быть сформирован на поверхности устройства.
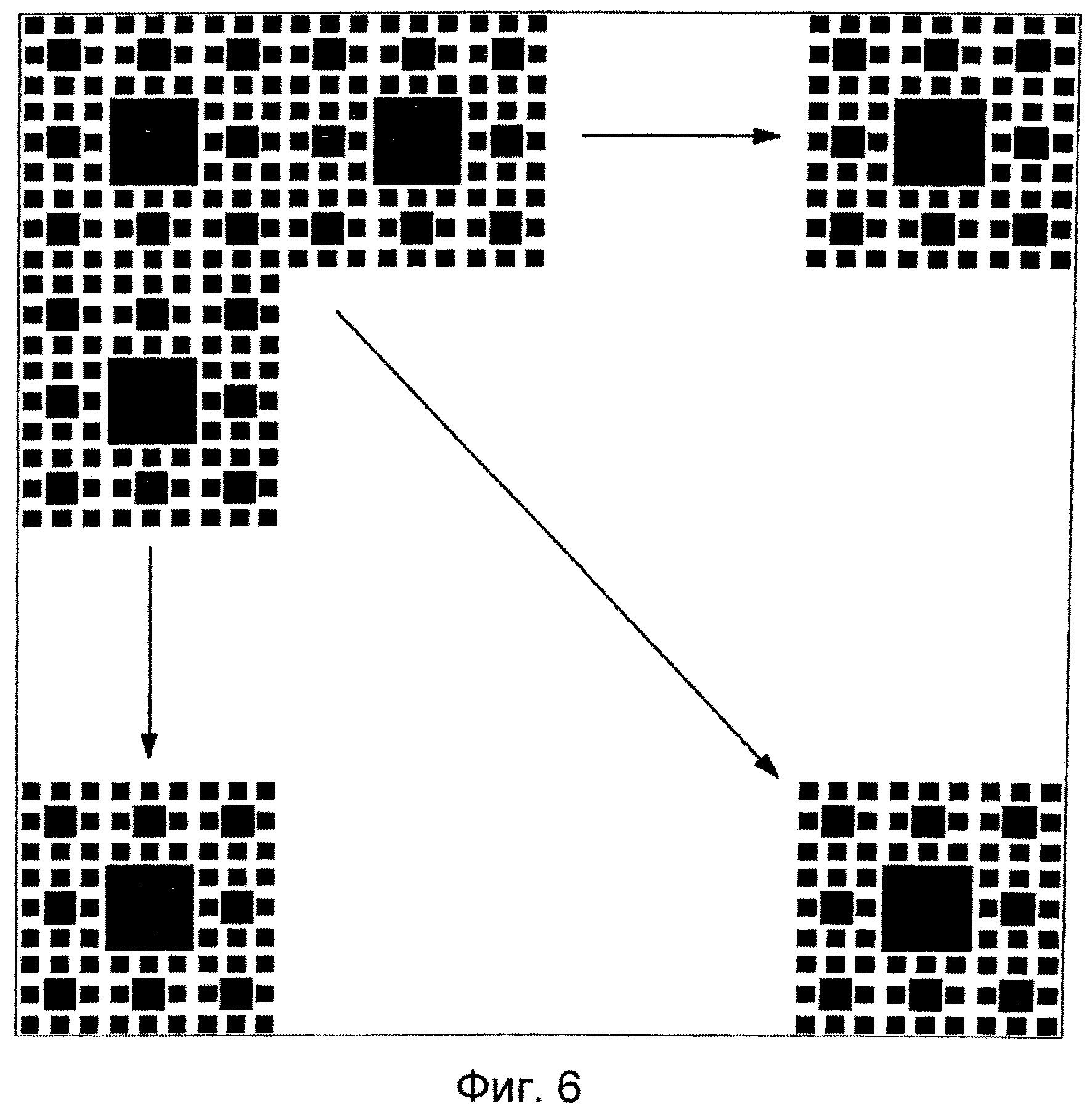
Фиг.6 иллюстрирует рисунок, включающий множество повторений сложного рисунка согласно Фиг.5.
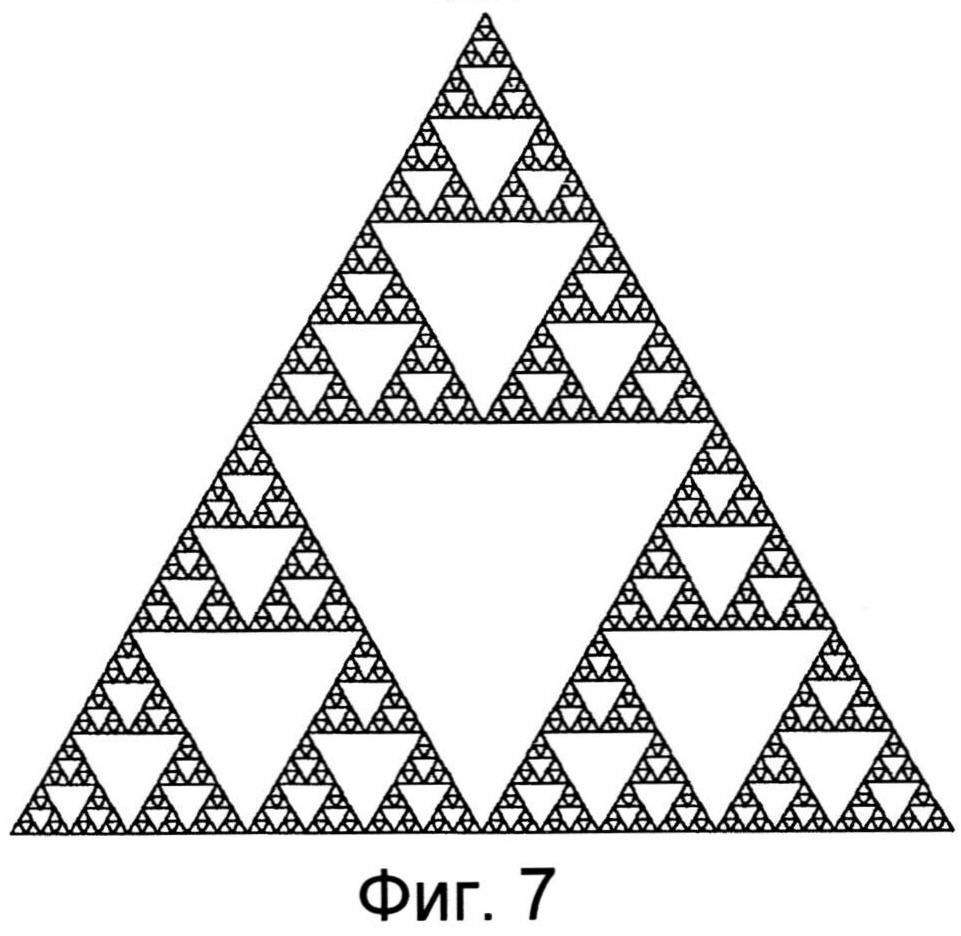
Фиг.7 иллюстрирует фрактальный треугольник Серпинского.
Фиг.8A-8D иллюстрируют сложные фрактальные и фрактал-подобные нанотопографии.
Фиг.9 иллюстрирует другой сложный рисунок, который может быть образован на поверхности устройства.
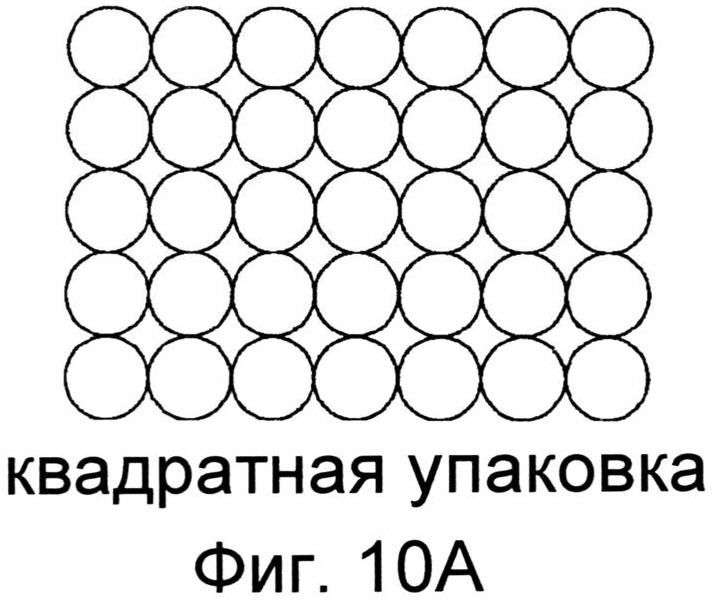
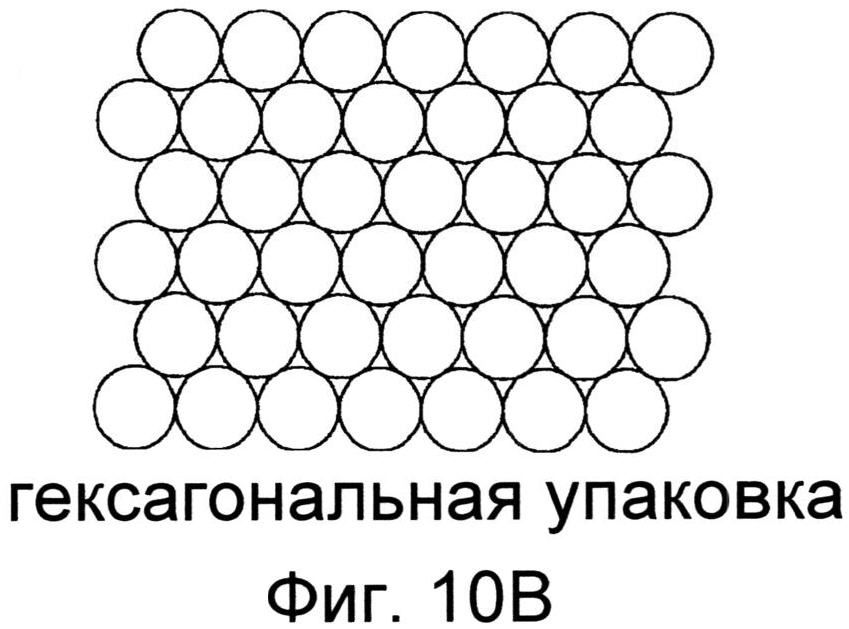
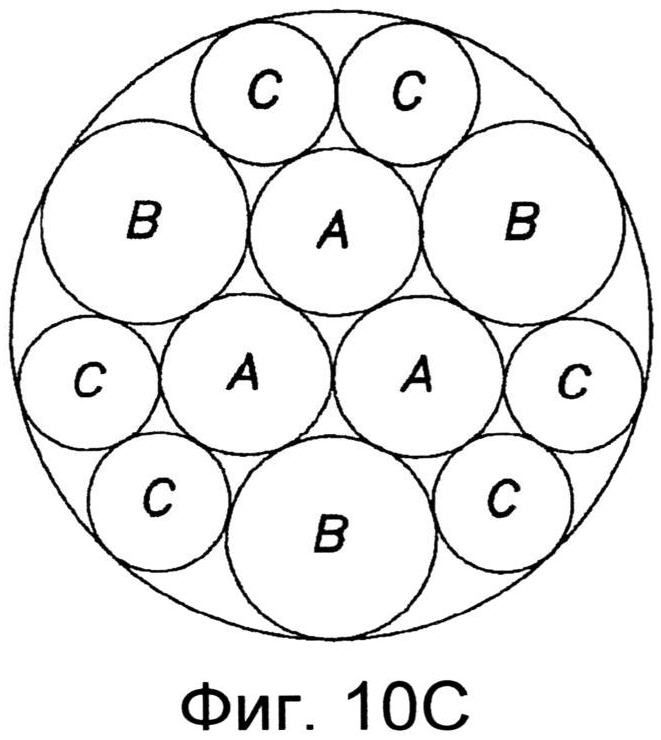
Фиг.10 иллюстрирует примерные плотности расположения, как может применяться для наноразмерных структур, как описано в настоящей заявке, включая квадратную модель размещения (Фиг.10А), гексагональную модель размещения (Фиг.10В) и круговую модель размещения (Фиг.10С).
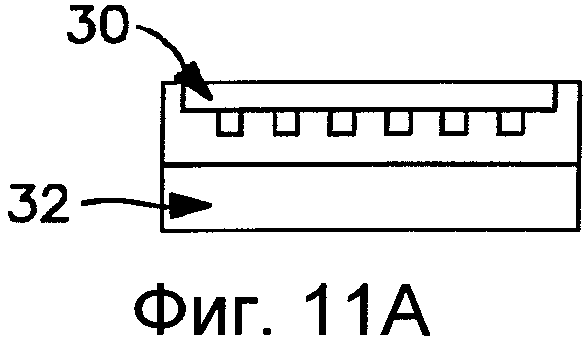
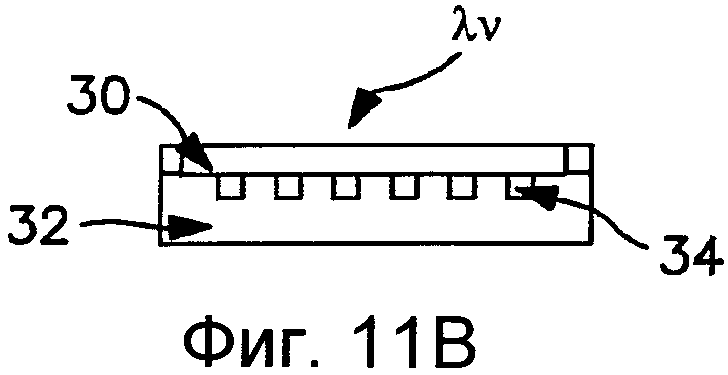
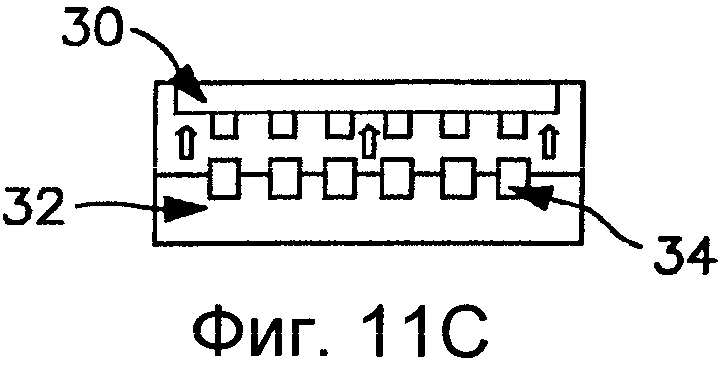
Фиг.11А-11С схематически иллюстрируют способ наноимпринтинга, как может применяться в одном варианте выполнения настоящего изобретения при формировании устройства.
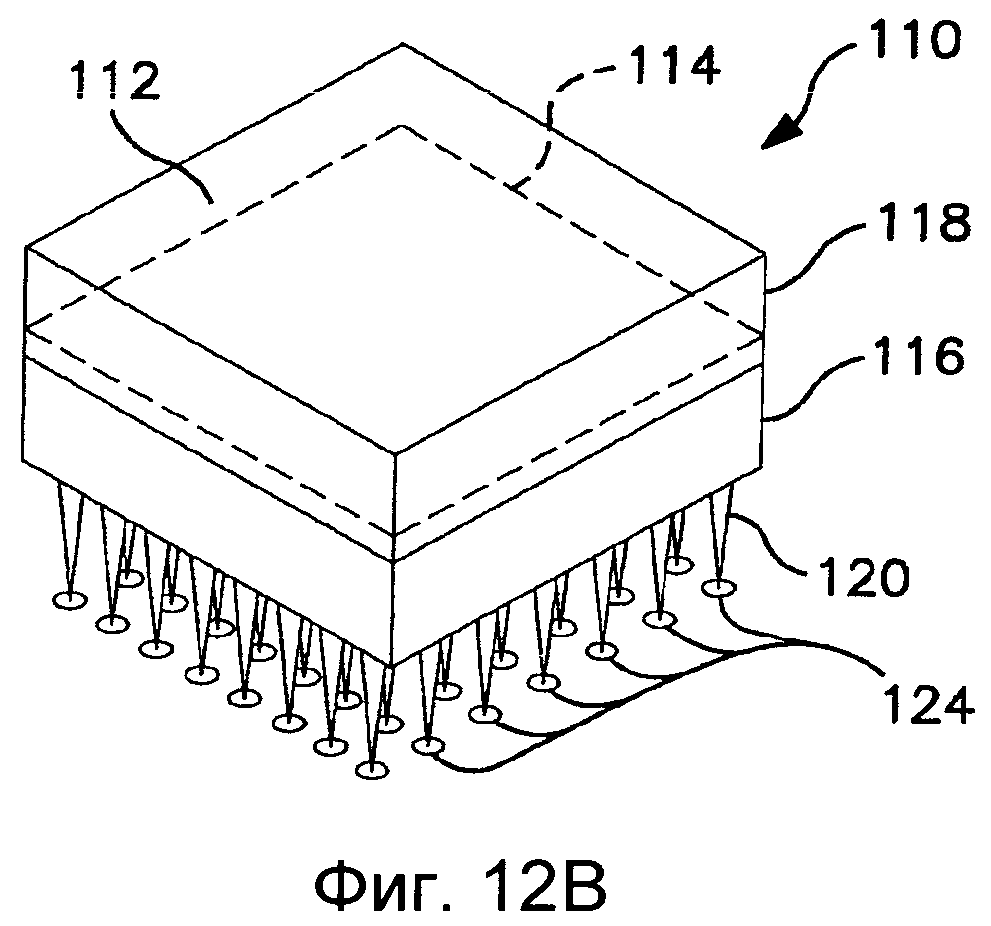
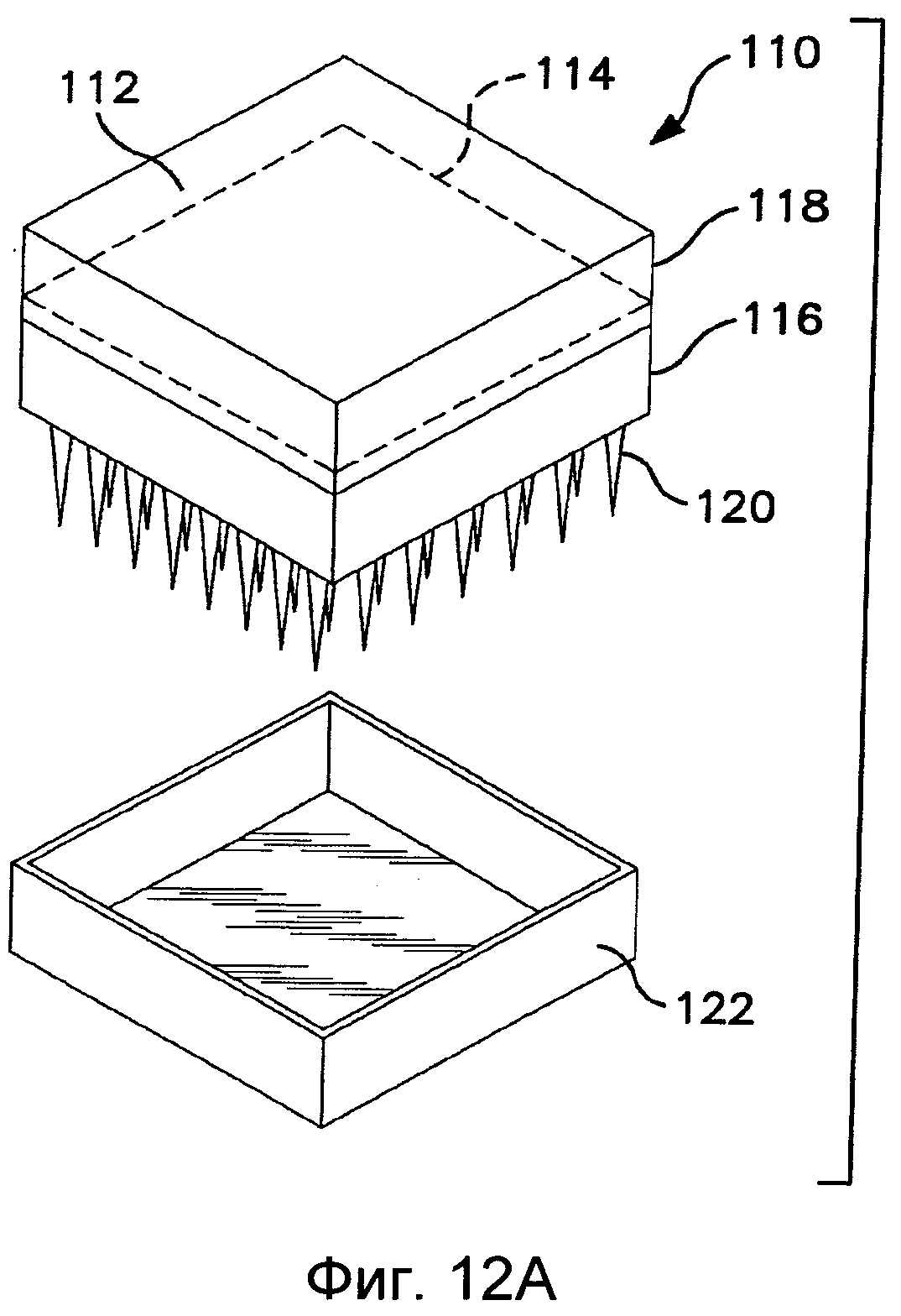
Фиг.12 схематически иллюстрирует один вариант выполнения устройства.
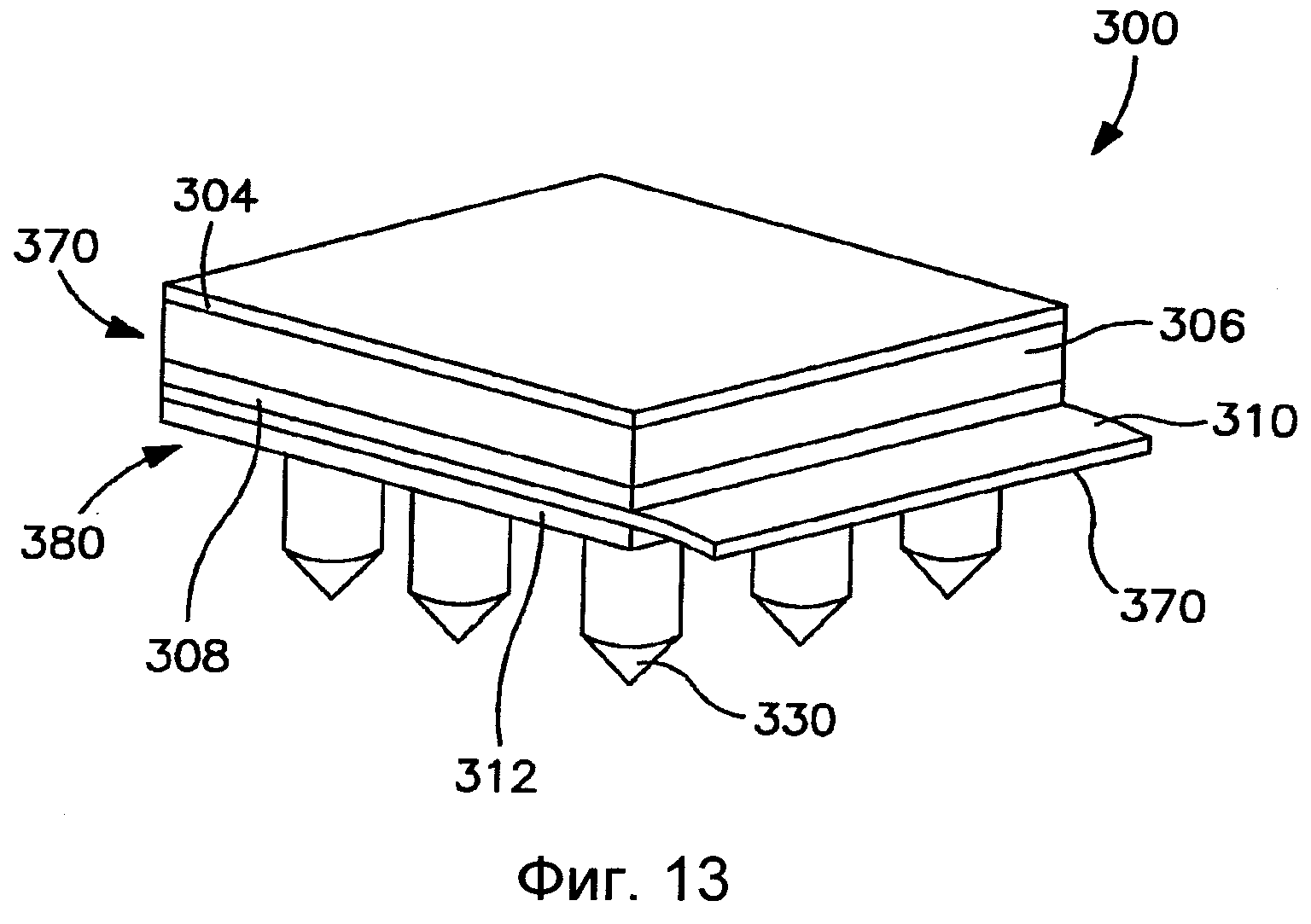
На Фиг.13 показан вид в перспективе одного варианта выполнения трансдермального пластыря до доставки лекарственного соединения.
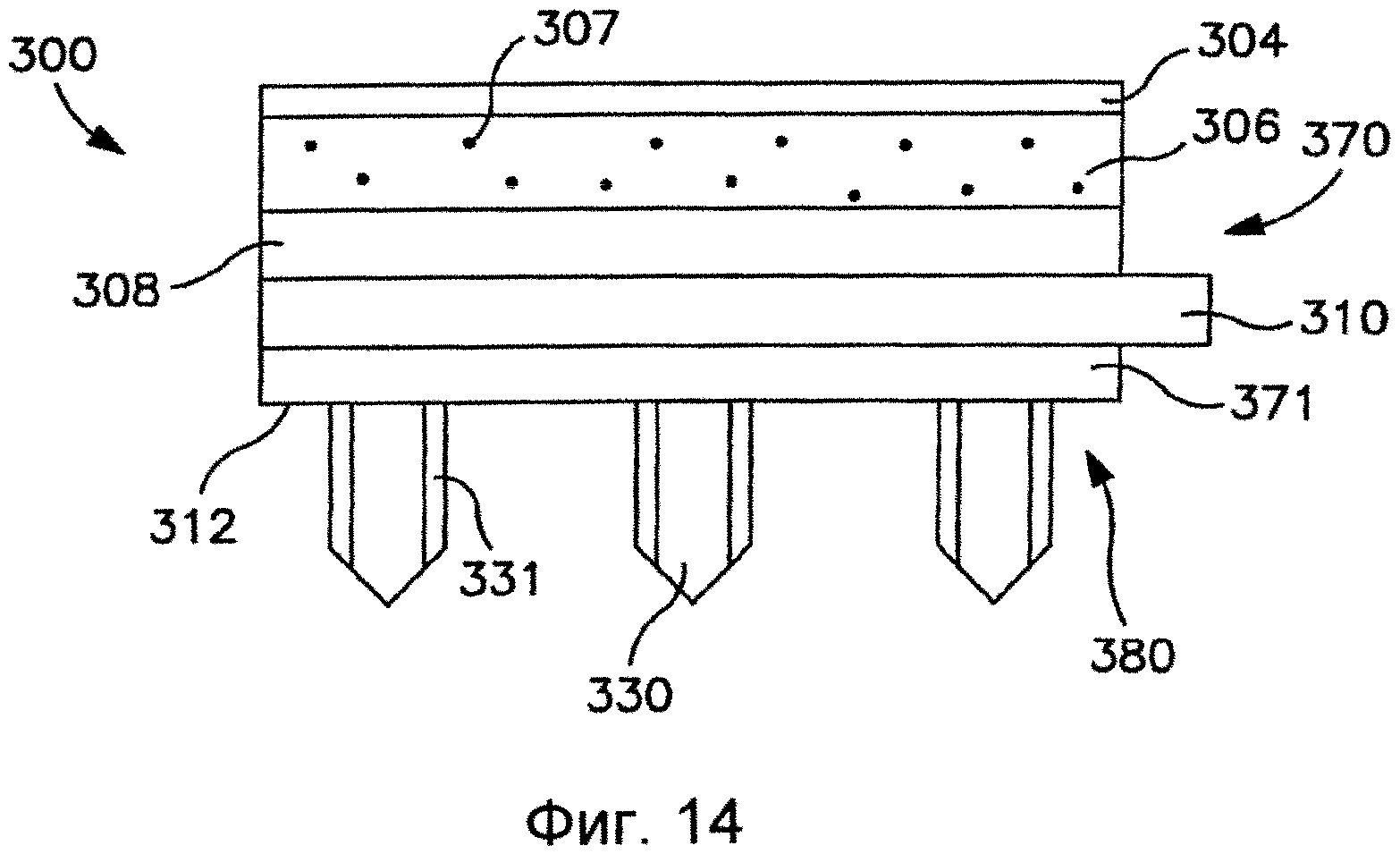
На Фиг.14 показан вид спереди пластыря согласно Фиг.13.
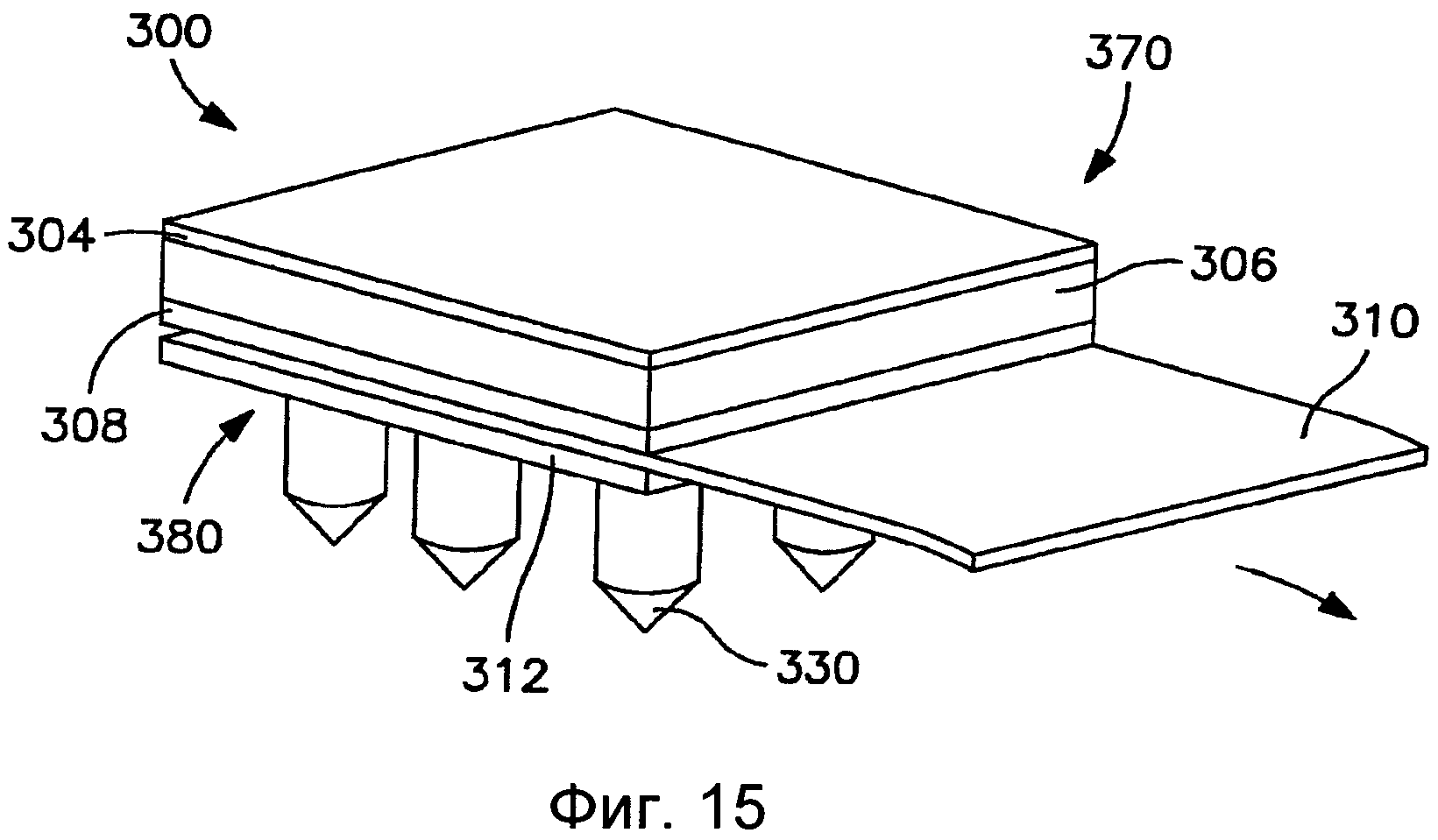
На Фиг.15 показан вид в перспективе пластыря согласно Фиг.13, на котором высвобождаемый компонент частично выдвинут из пластыря.
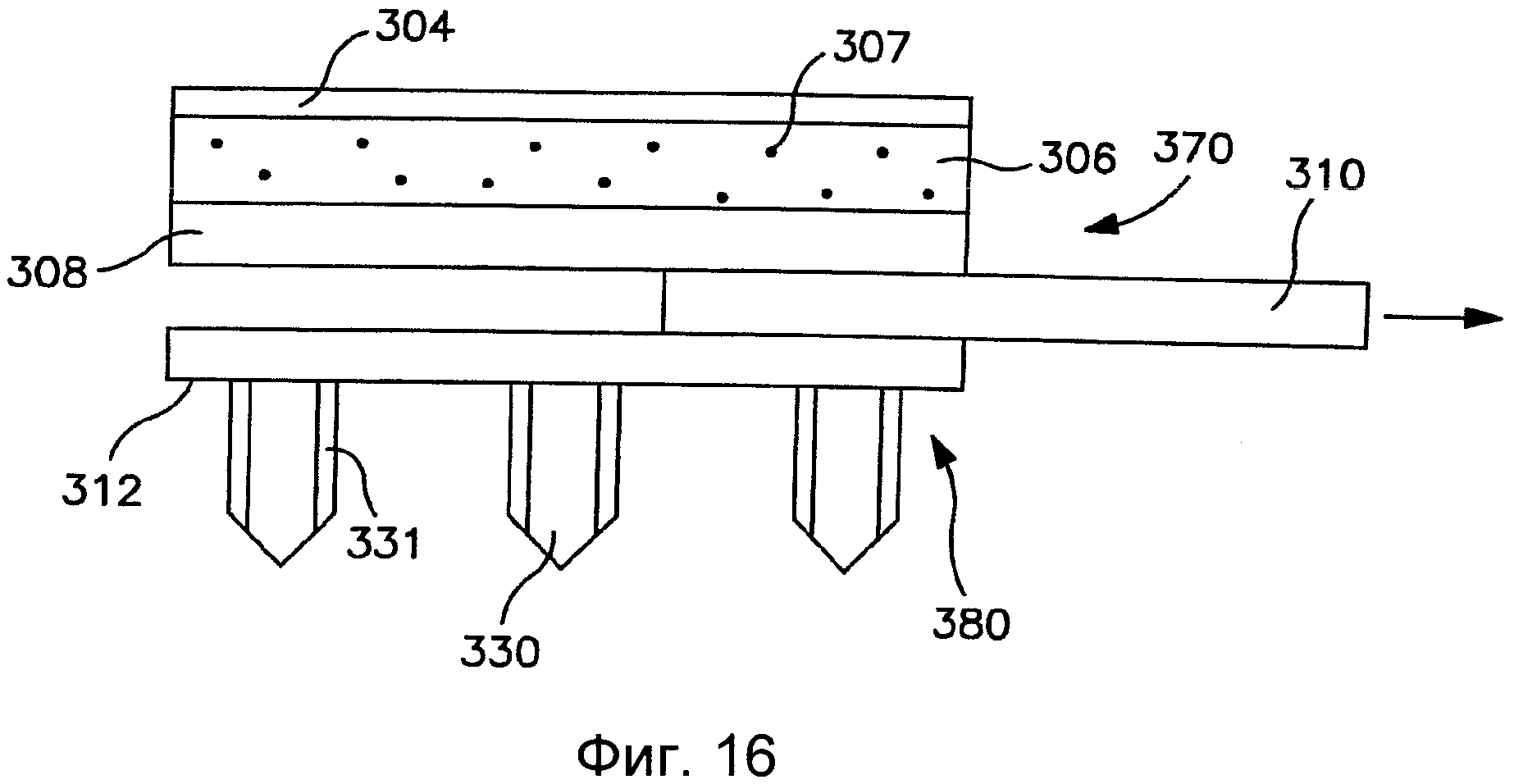
На Фиг.16 показан вид спереди пластыря согласно Фиг.15.
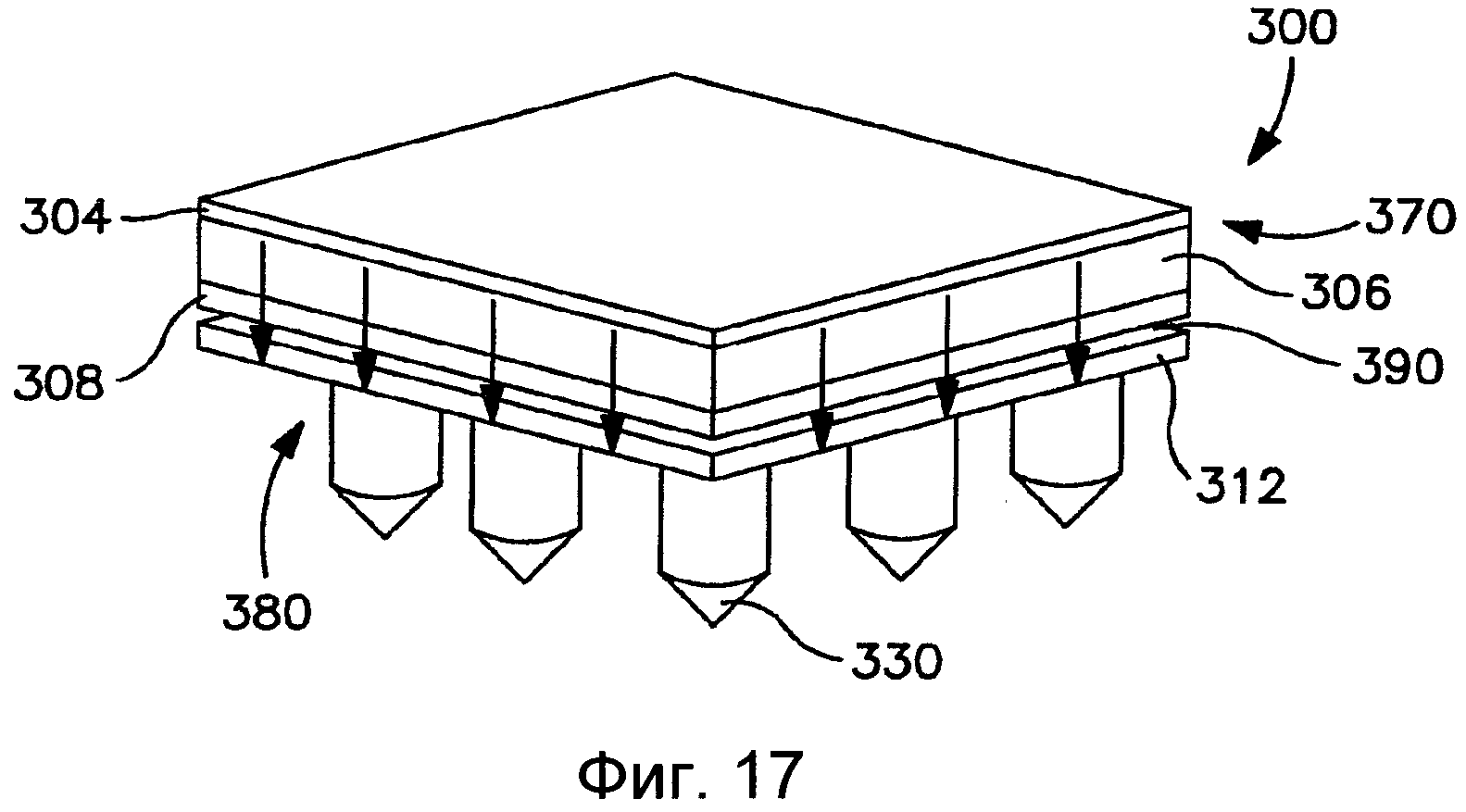
На Фиг.17 показан вид в перспективе пластыря согласно Фиг.13 после удаления высвобождаемого компонента и в ходе применения.
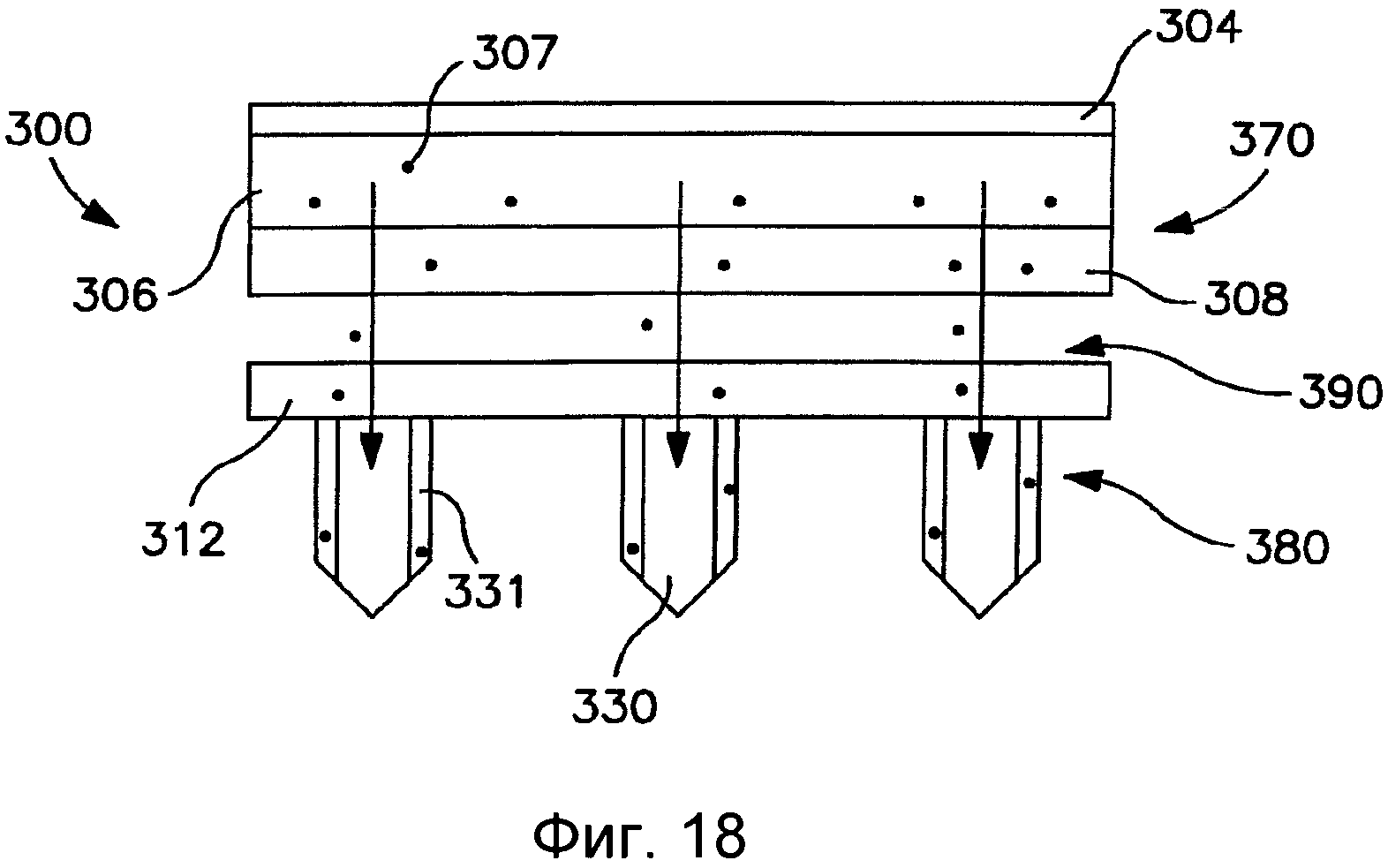
На Фиг.18 показан вид спереди пластыря согласно Фиг.17.
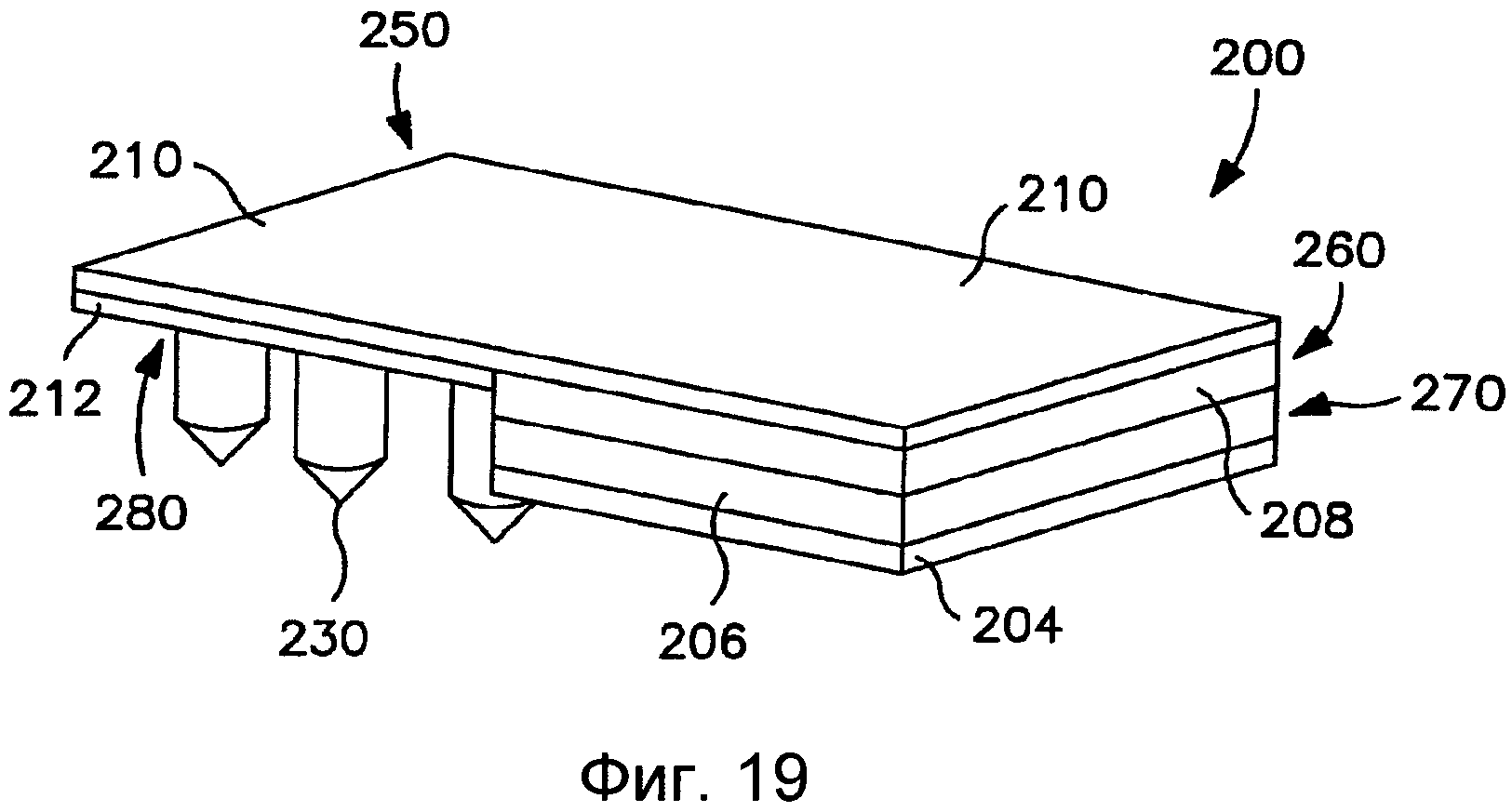
На Фиг.19 показан вид в перспективе другого варианта выполнения трансдермального пластыря до доставки лекарственного соединения.
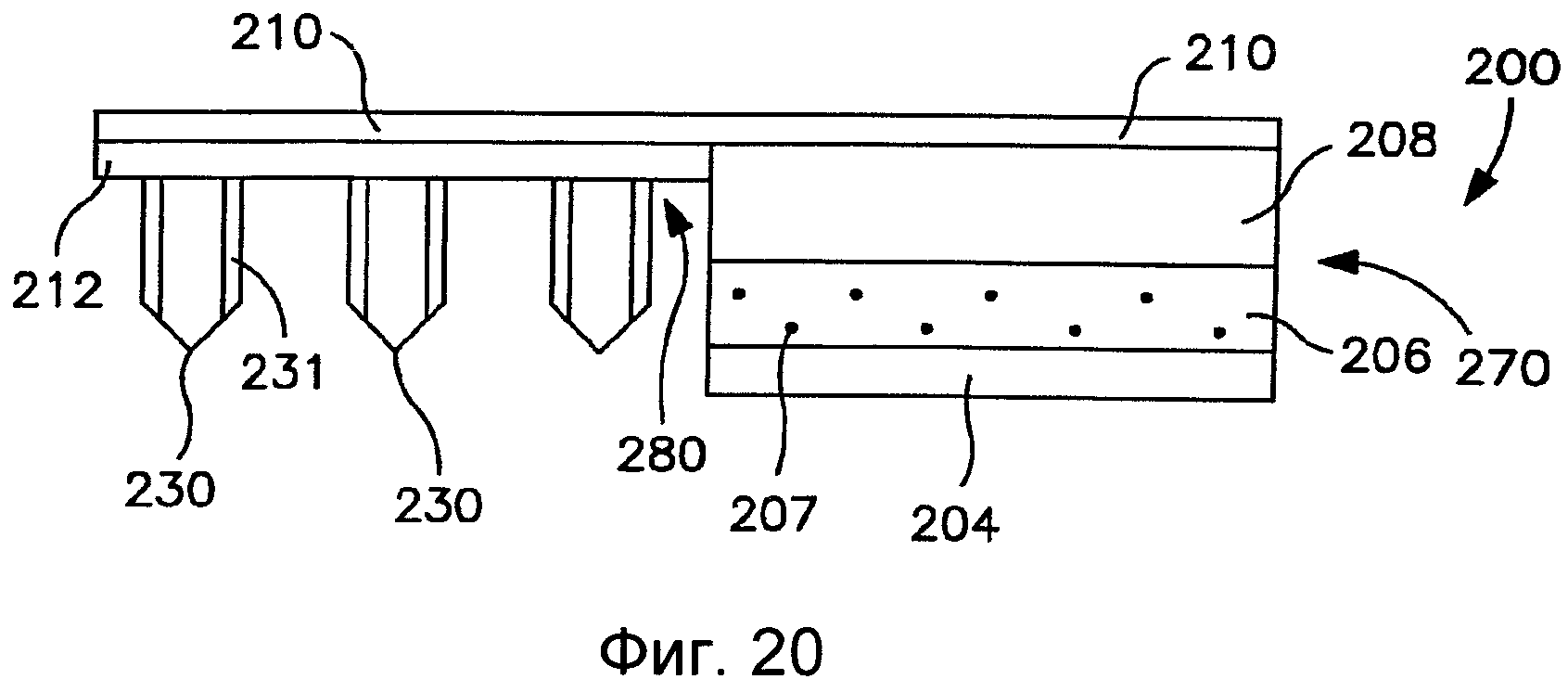
На Фиг.20 показан вид спереди пластыря согласно Фиг.19.
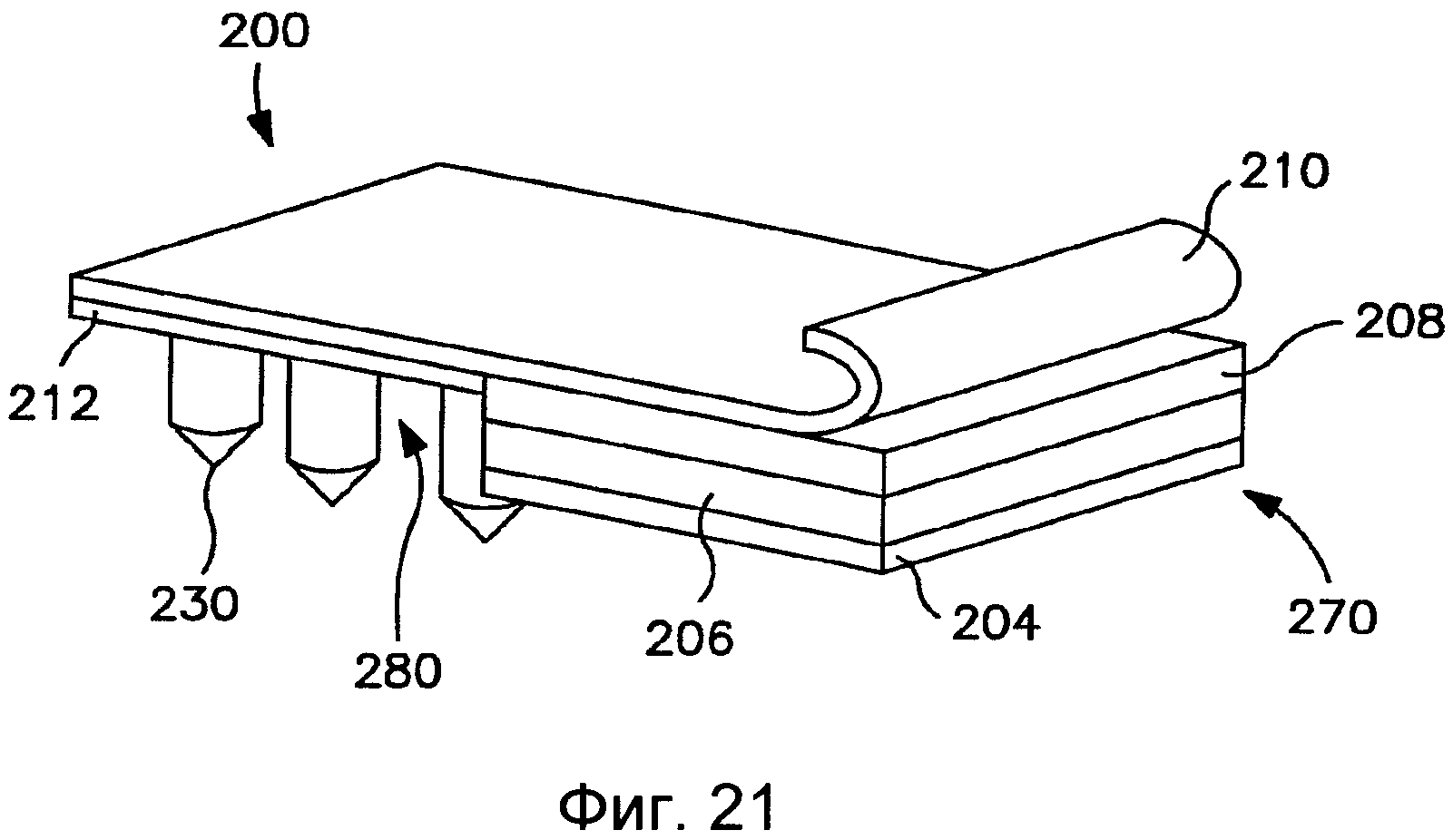
На Фиг.21 показан вид в перспективе трансдермального пластыря согласно Фиг.19, в котором высвобождаемый компонент частично высвободился из пластыря.
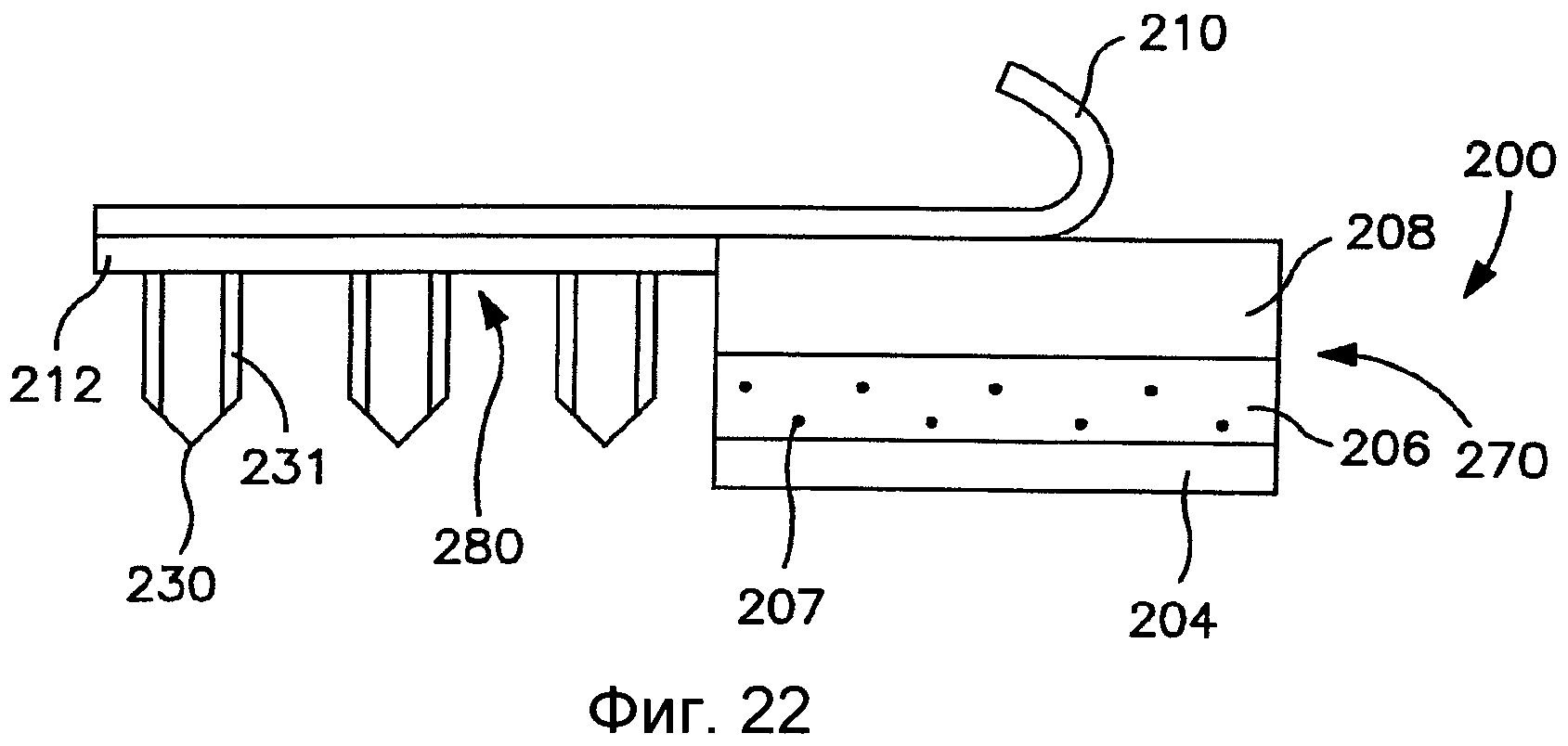
На Фиг.22 показан вид спереди трансдермального пластыря согласно Фиг.21.
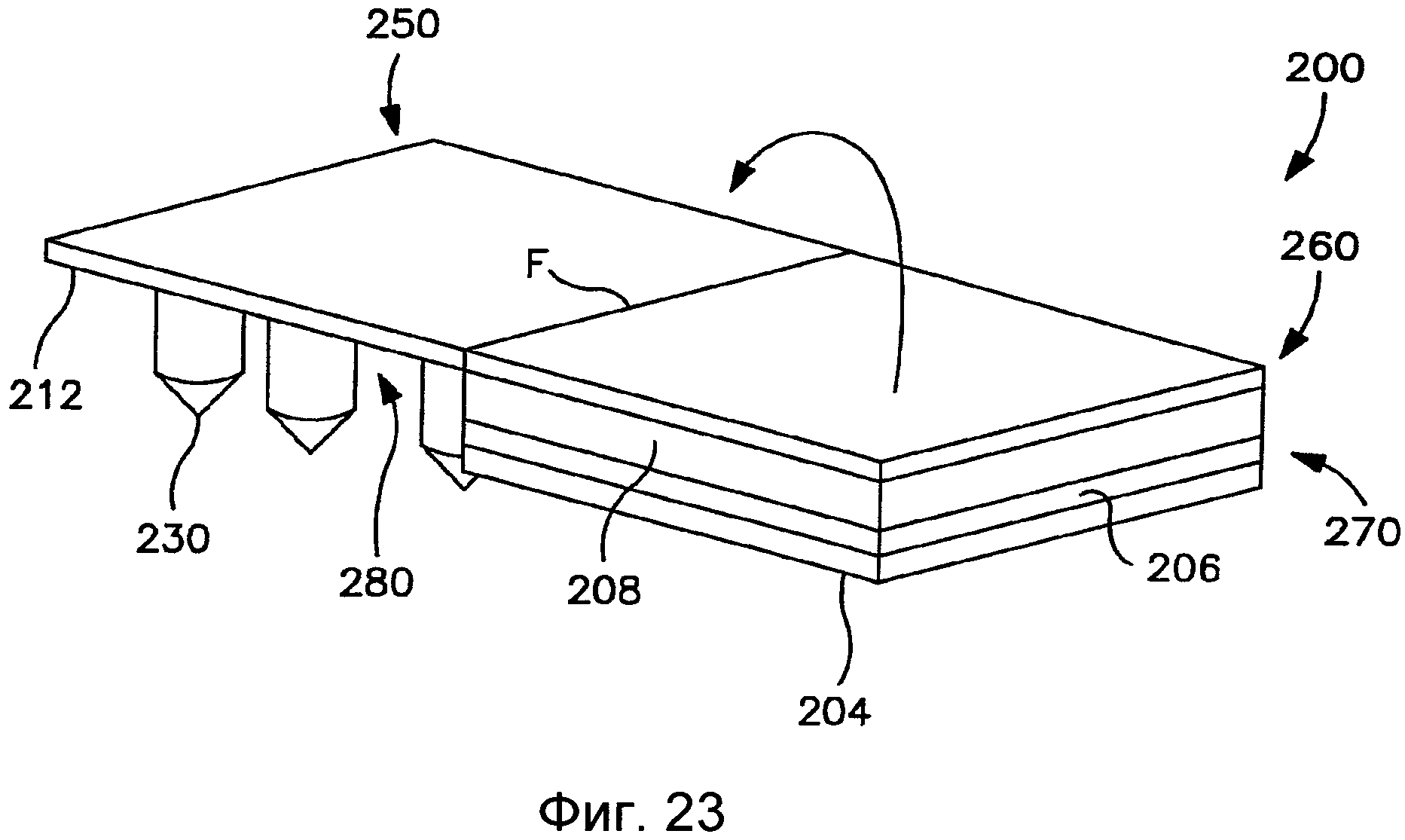
На Фиг.23 показан вид в перспективе трансдермального пластыря согласно Фиг.19, в котором высвобождаемый компонент полностью высвободился из пластыря.
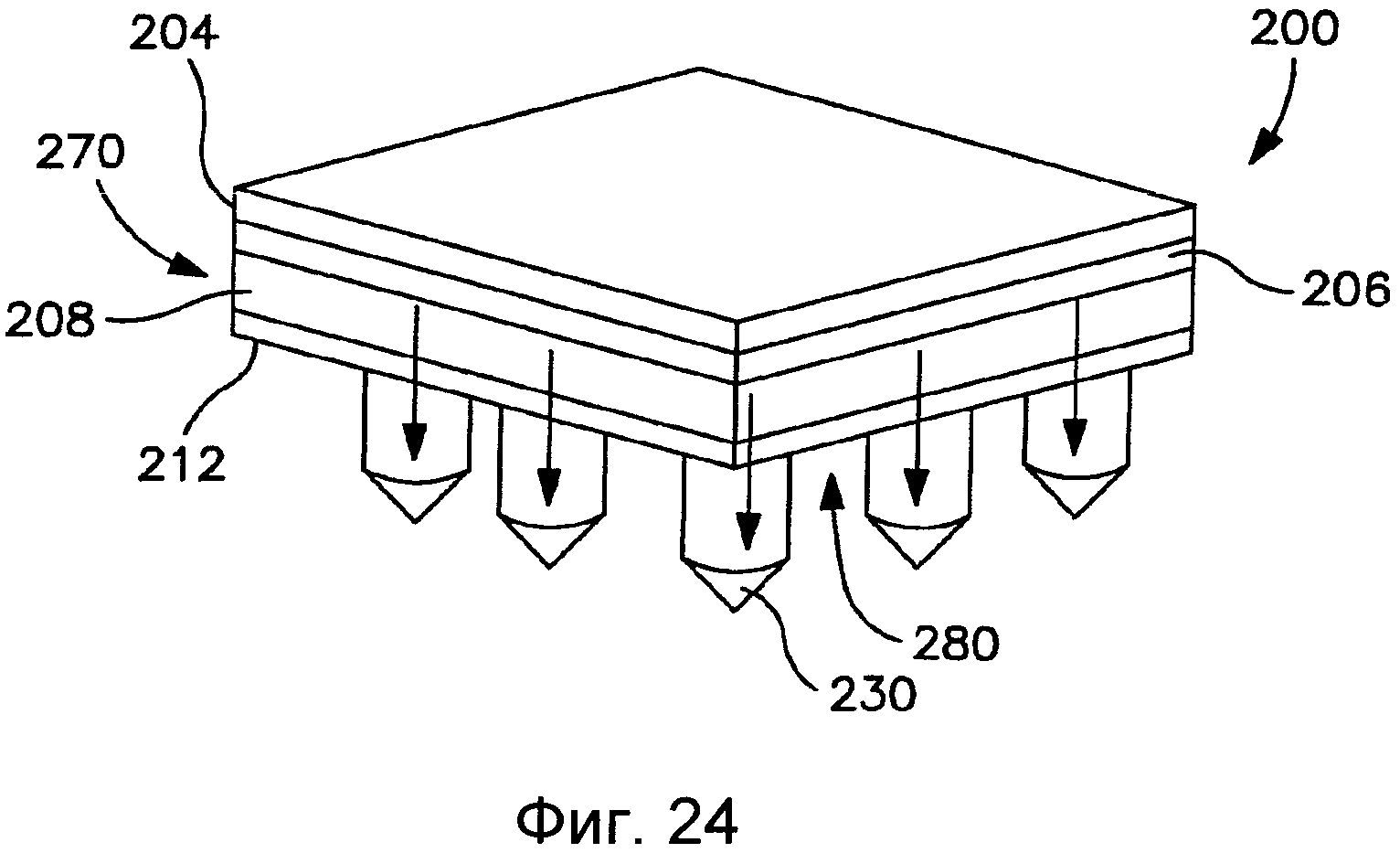
На Фиг.24 показан вид в перспективе трансдермального пластыря согласно Фиг.19 после высвобождения высвобождаемого компонента и в ходе применения.
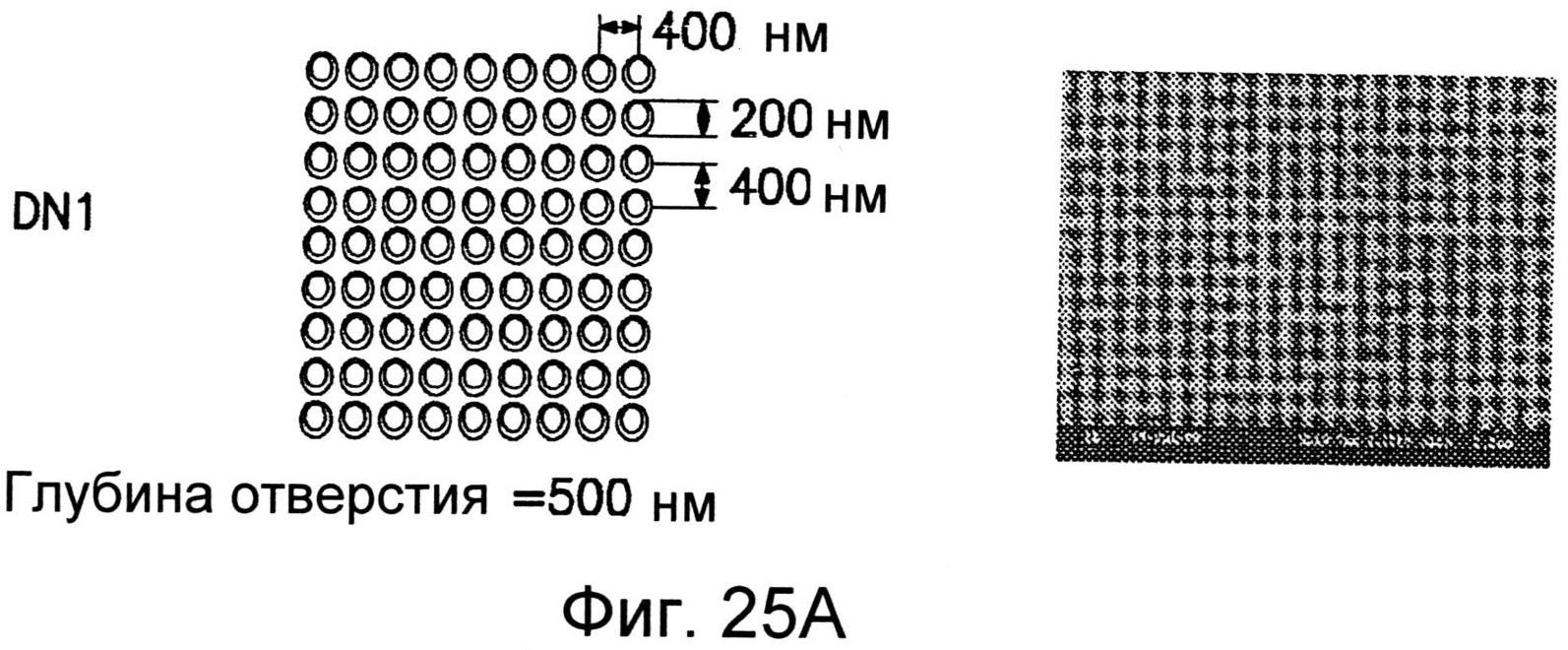
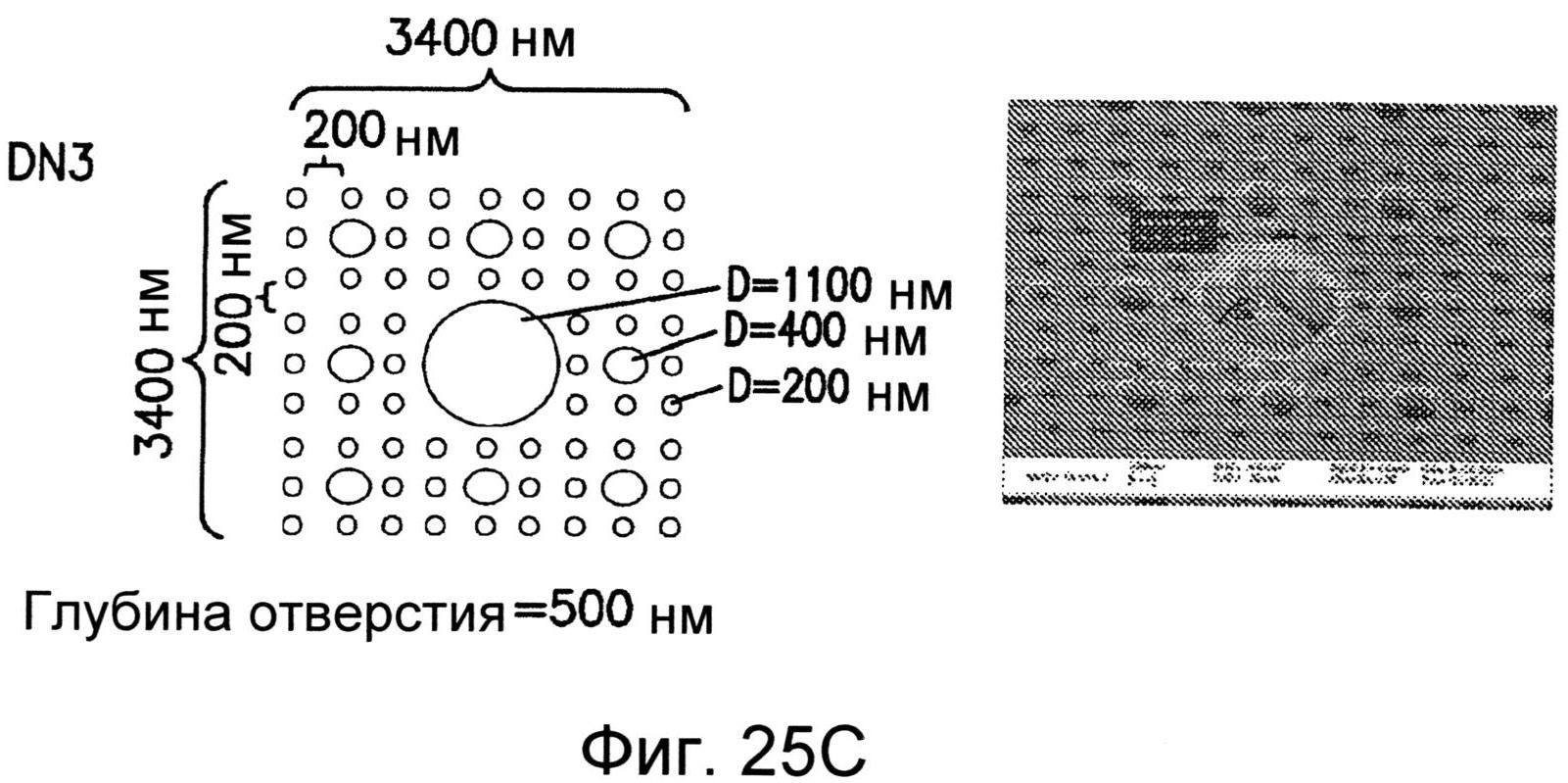
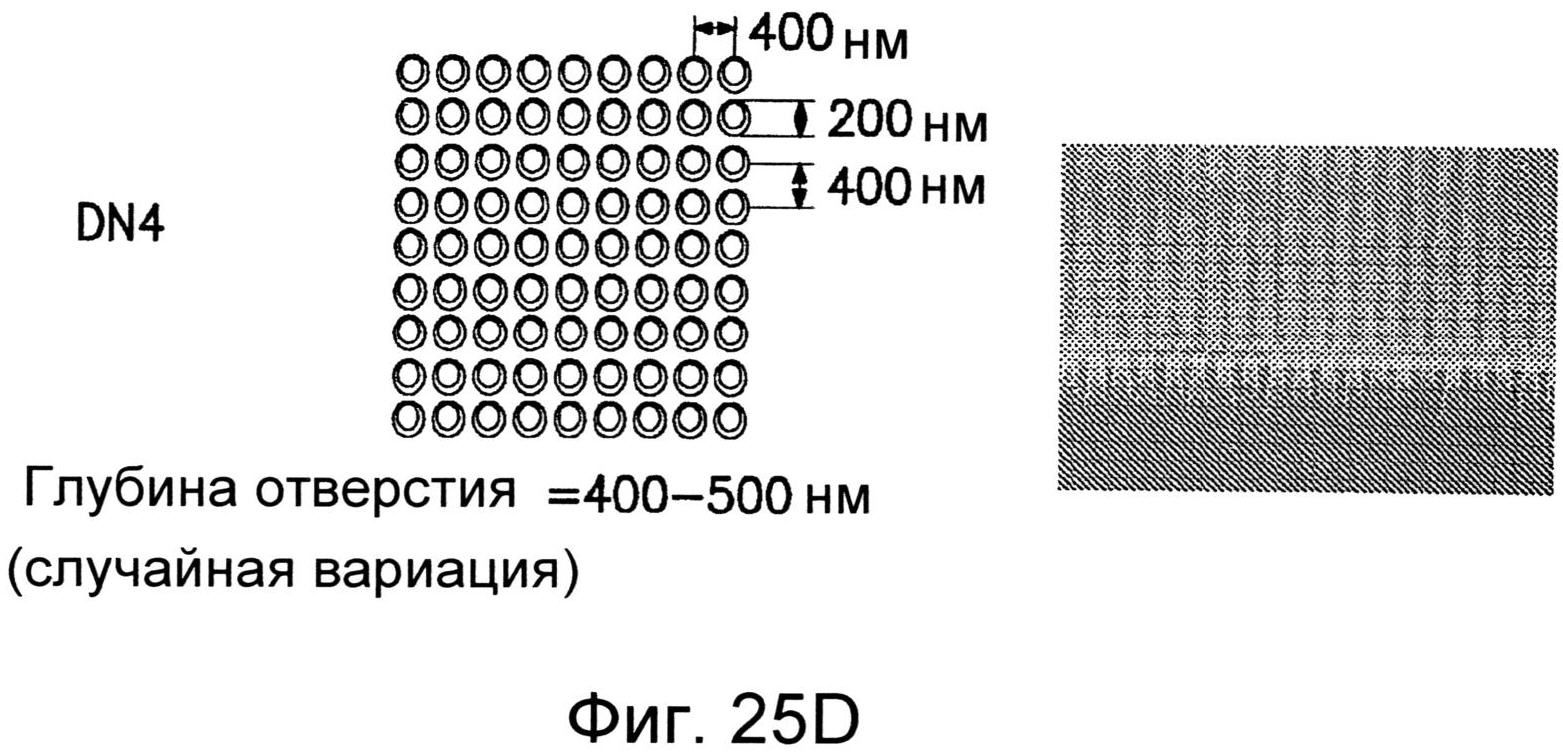
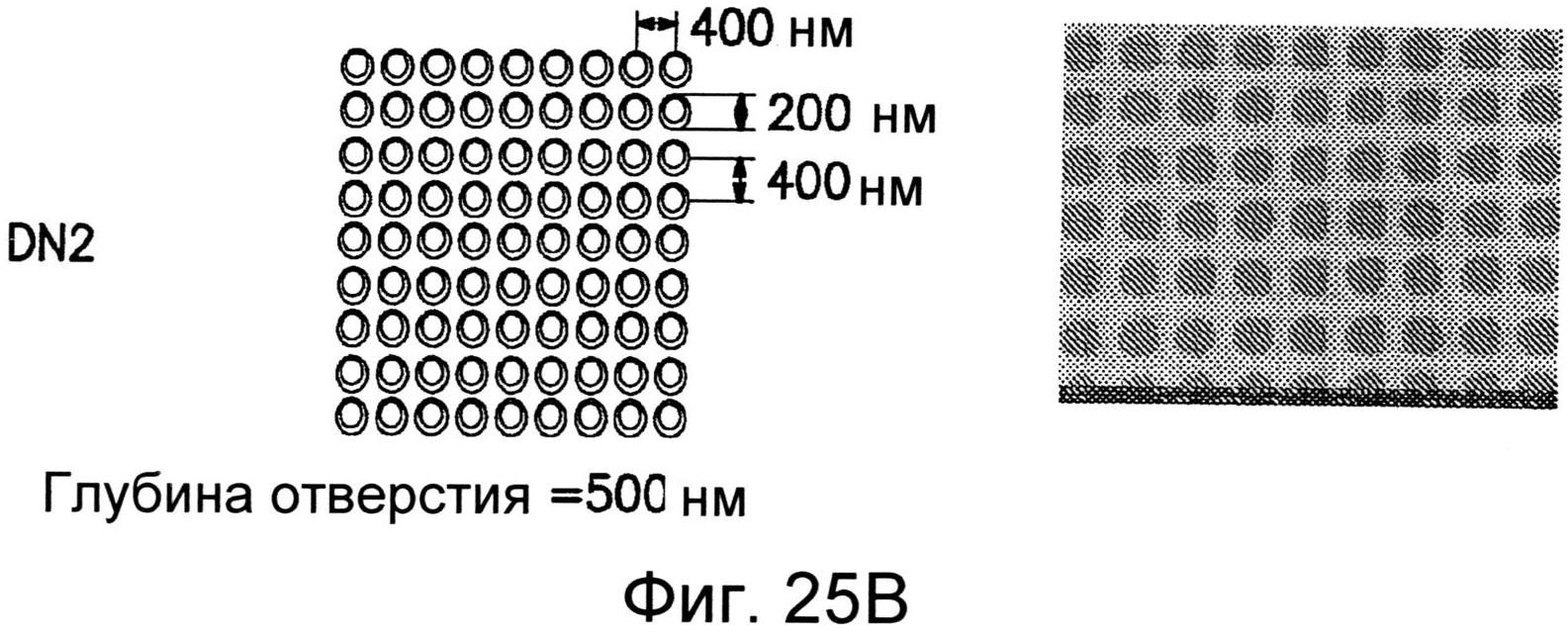
Фиг.25А-25Е иллюстрируют несколько нанотопографических рисунков, как раскрывается в настоящем изобретении.
Фиг.26 показывает SEM пленки, включая наноструктурированную поверхность.
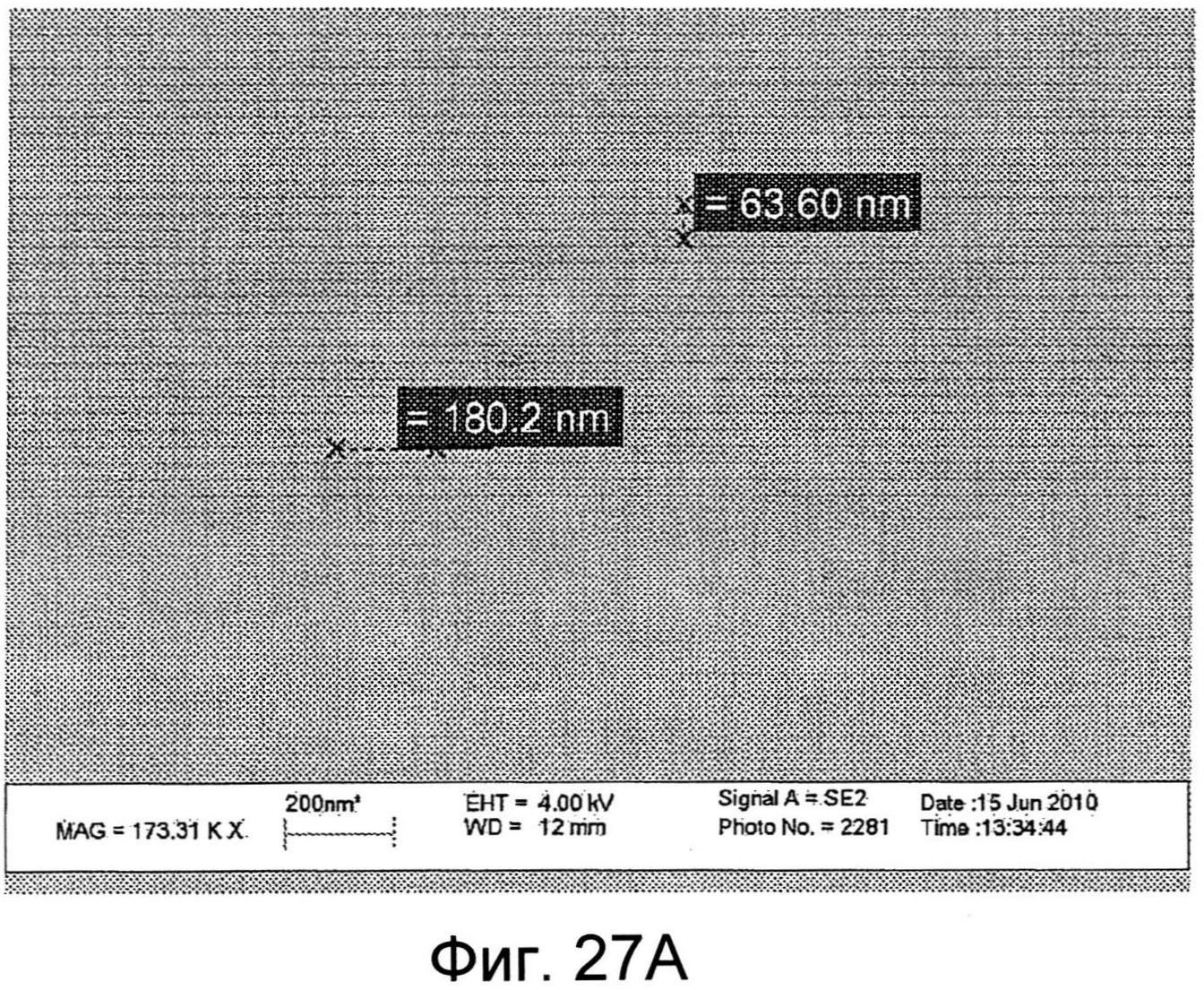
Фиг.27А и 27В показывают два SEM пленки, включая другую наноструктурированную поверхность.
Фиг.28 показывает SEM пленки, включая другую наноструктурированную поверхность.
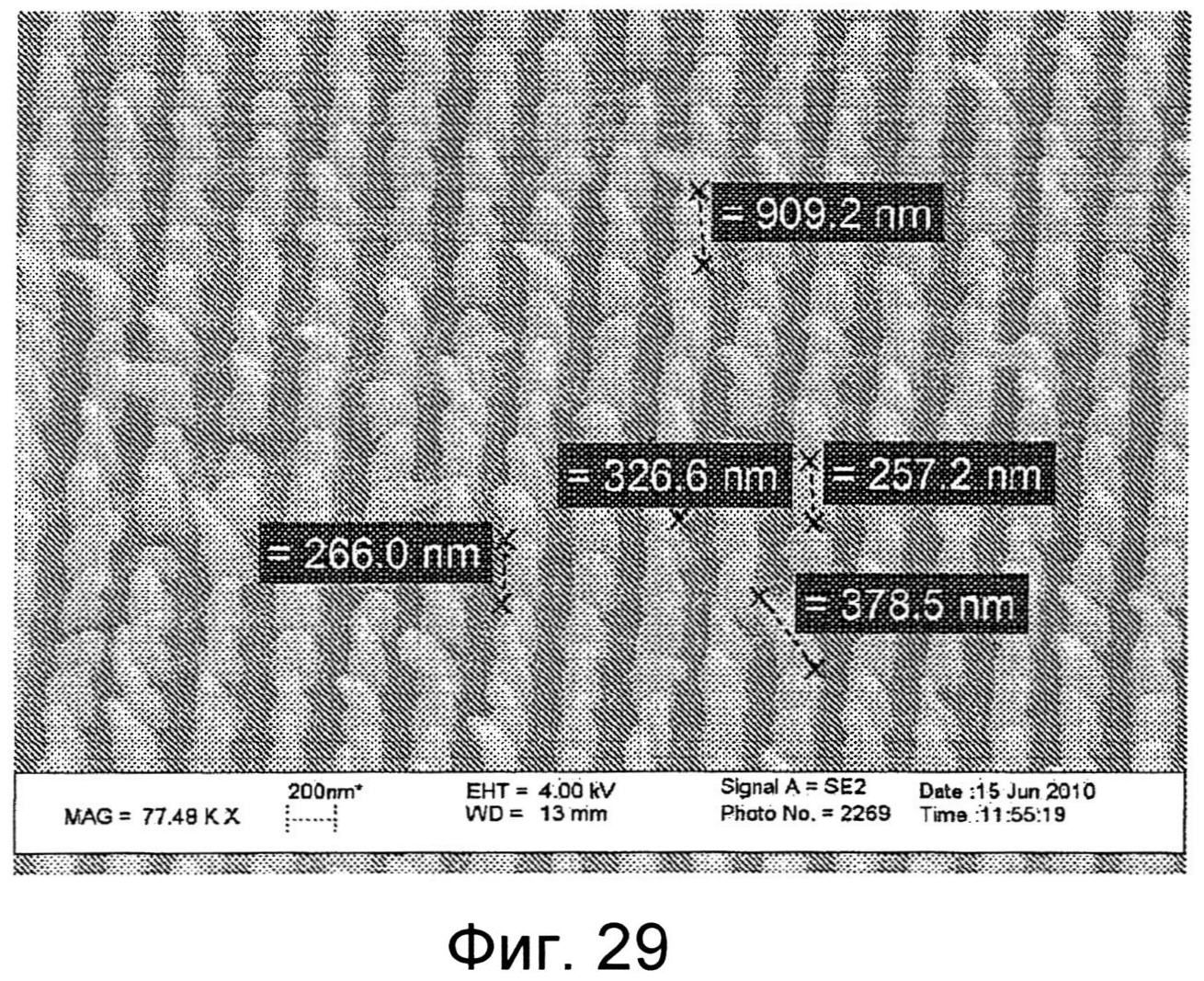
Фиг.29 показывает SEM пленки, включая другую наноструктурированную поверхность.
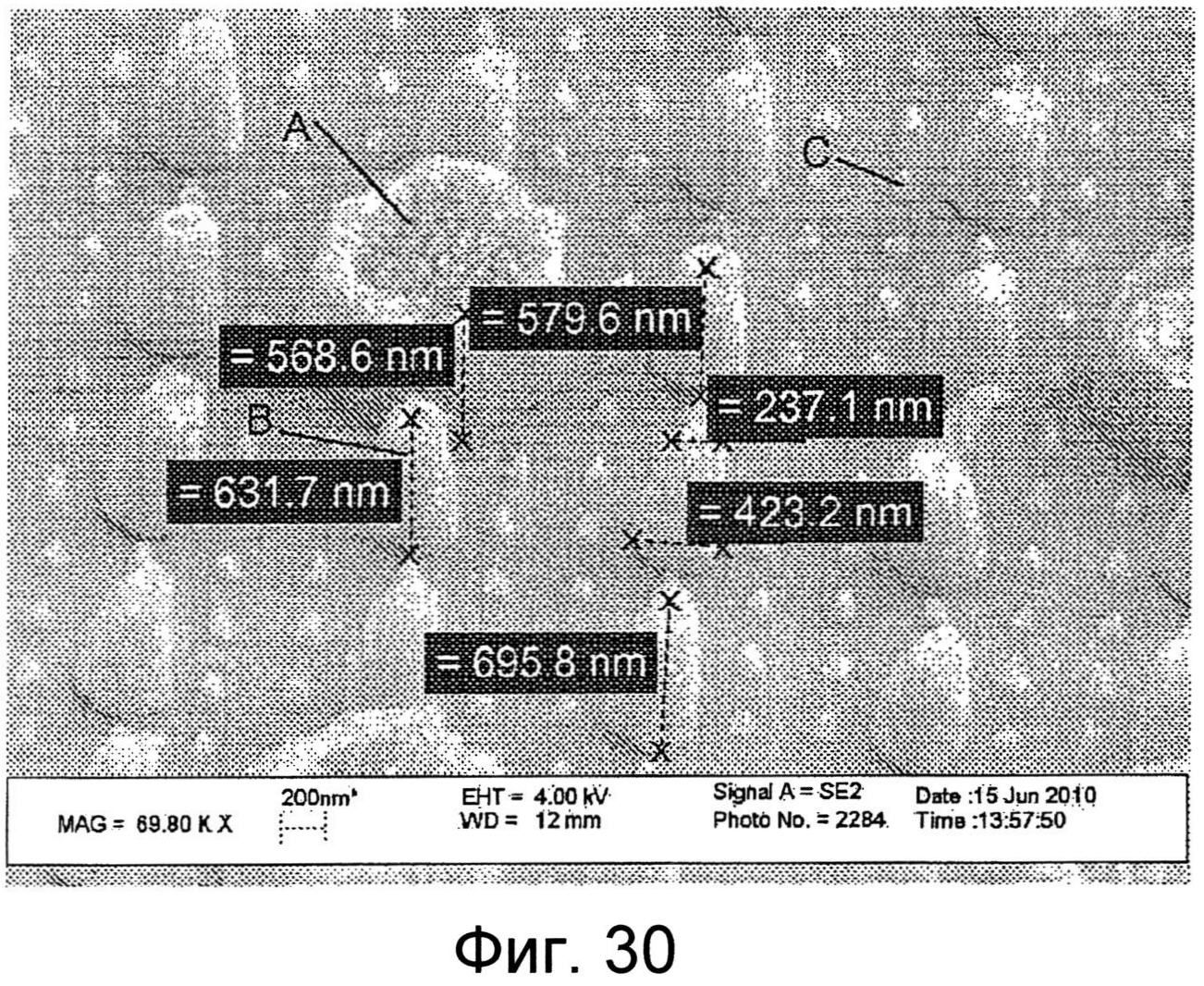
Фиг.30 показывает SEM пленки, включая другую наноструктурированную поверхность.
Фиг.31 показывает SEM пленки, включая другую наноструктурированную поверхность.
Фиг.32 показывает SEM пленки, включая другую наноструктурированную поверхность.
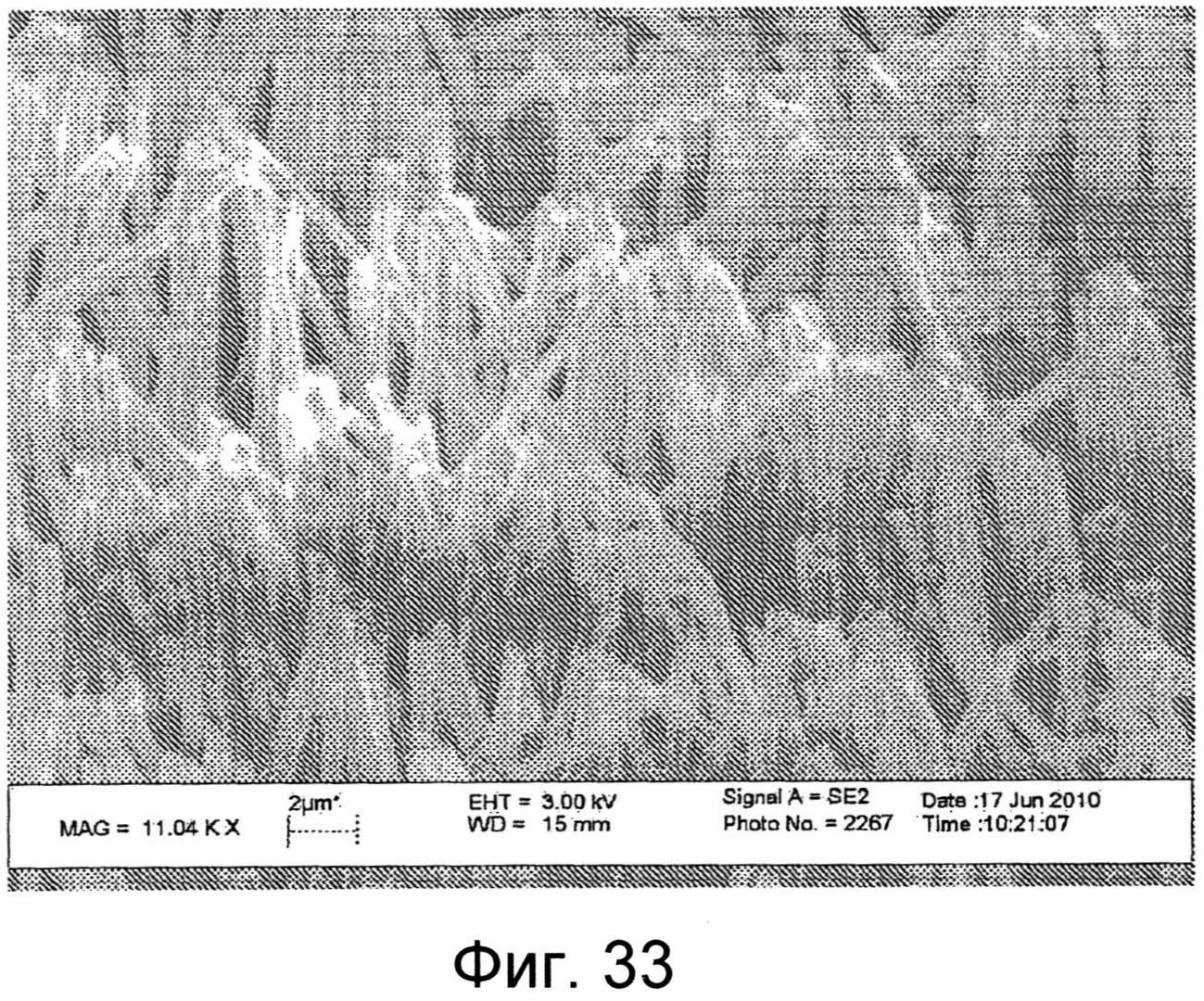
Фиг.33 показывает SEM пленки, включая другую наноструктурированную поверхность.
Фиг.34 показывает SEM пленки, включая другую наноструктурированную поверхность.
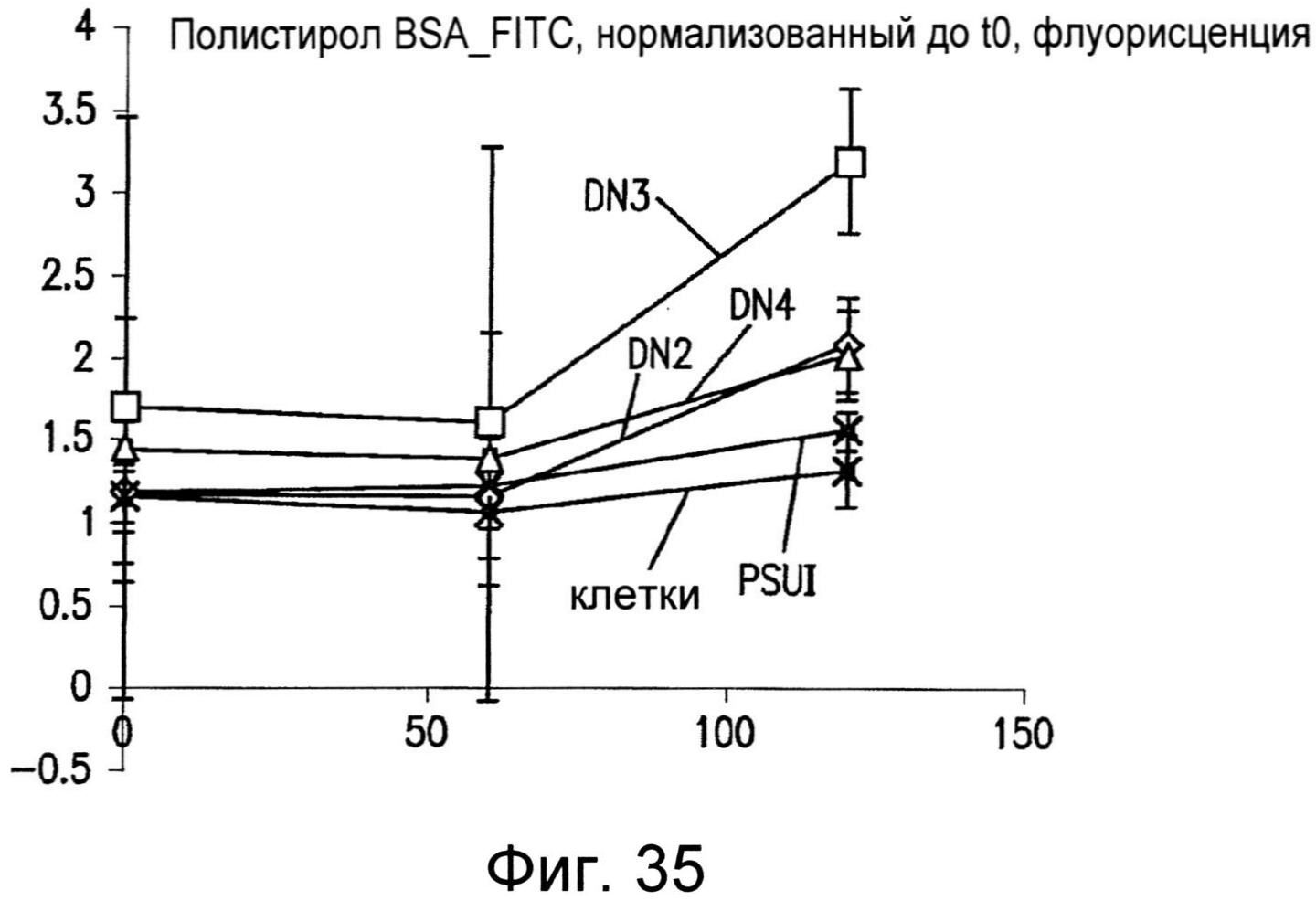
Фиг.35 графически иллюстрирует эффекты, оказываемые на проницаемость, для бычьего сывороточного альбумина (BSA) в монослое клеток на полистирольных пленках, наноструктурированных как описано в настоящем изобретении.
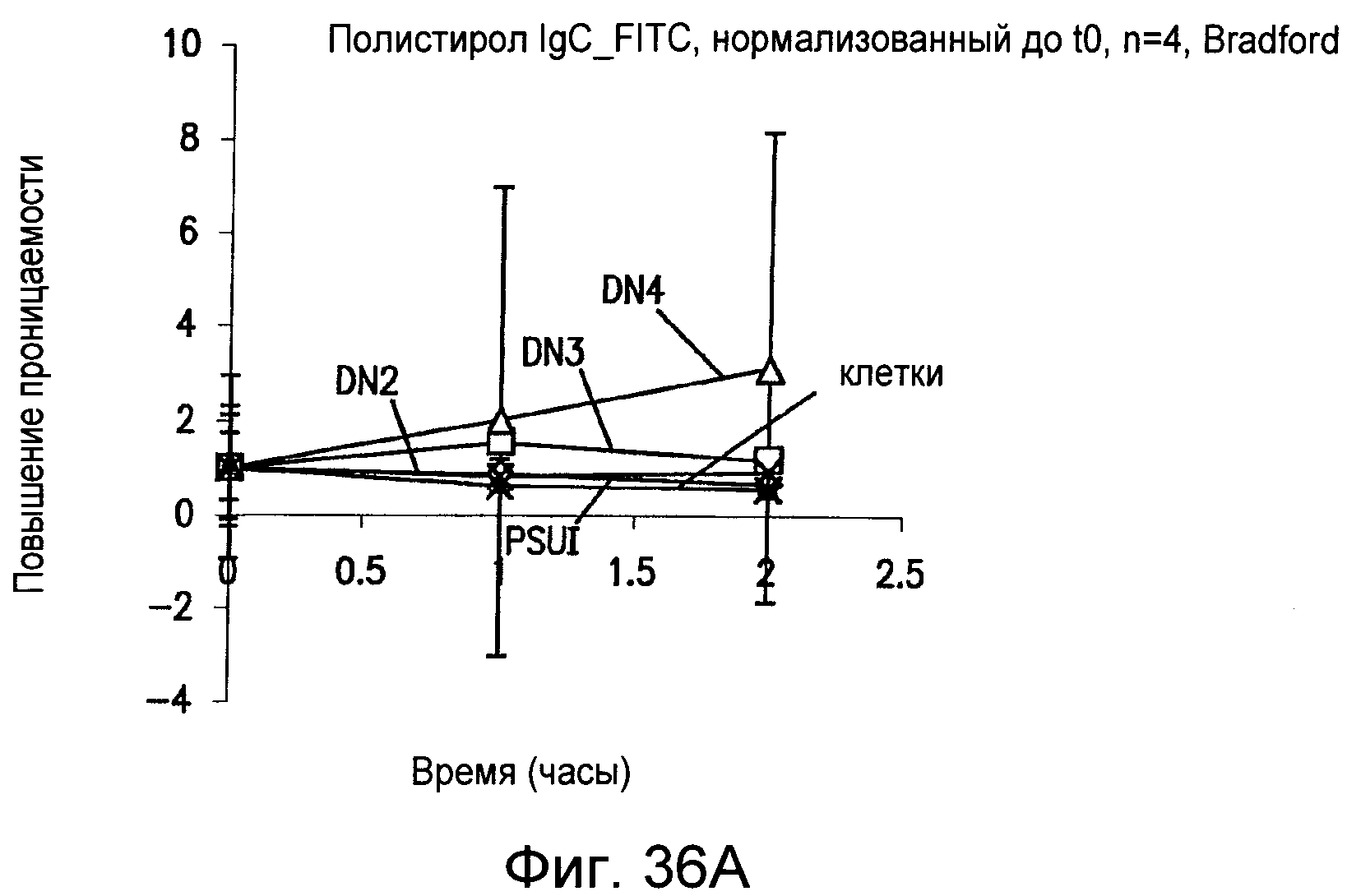
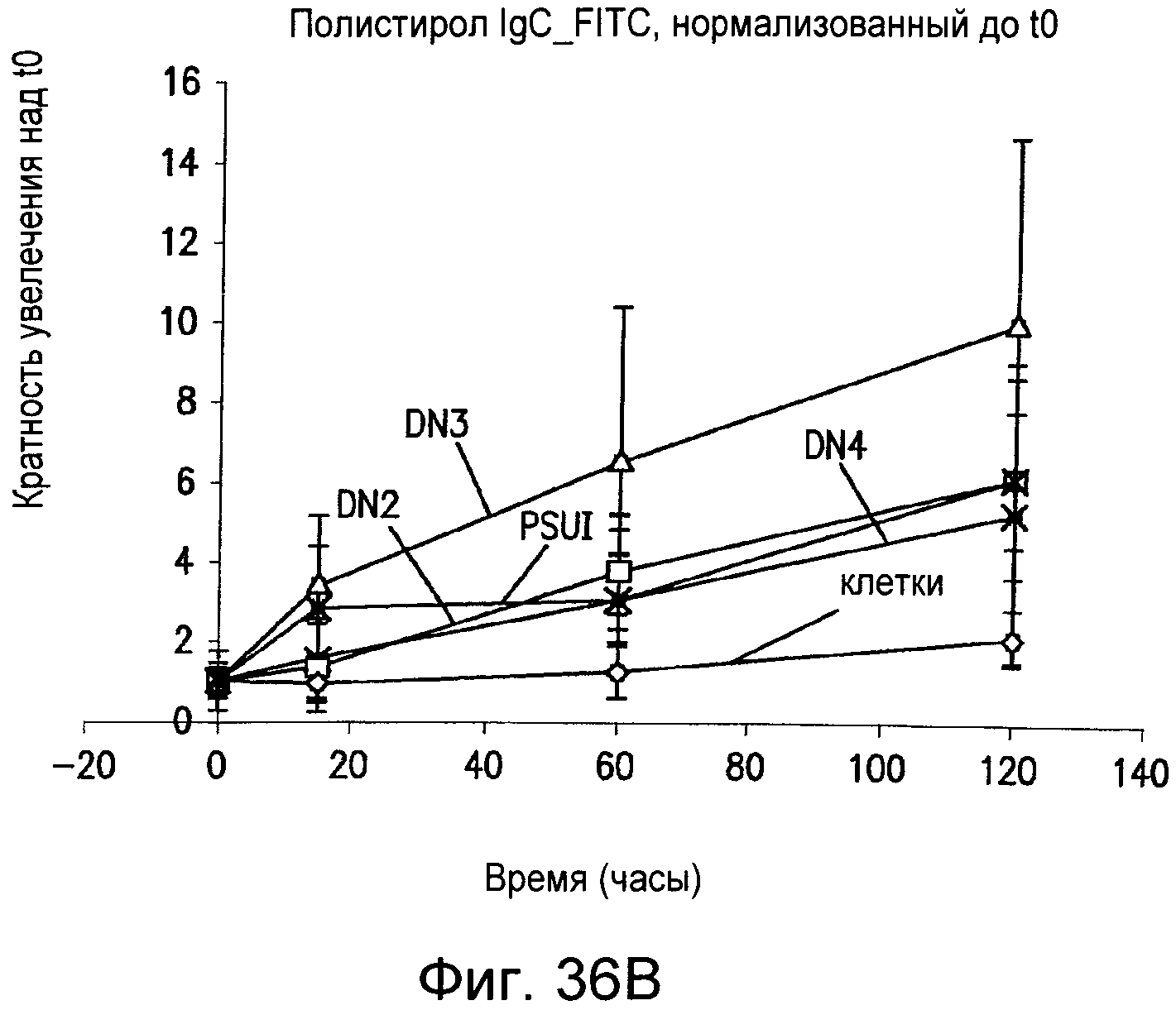
Фиг.36 графически иллюстрирует эффекты, оказываемые на проницаемость, для иммуноглобулина-G (IgG) в монослое клеток на полистирольных пленках, наноструктурированных как описано в настоящем изобретении.
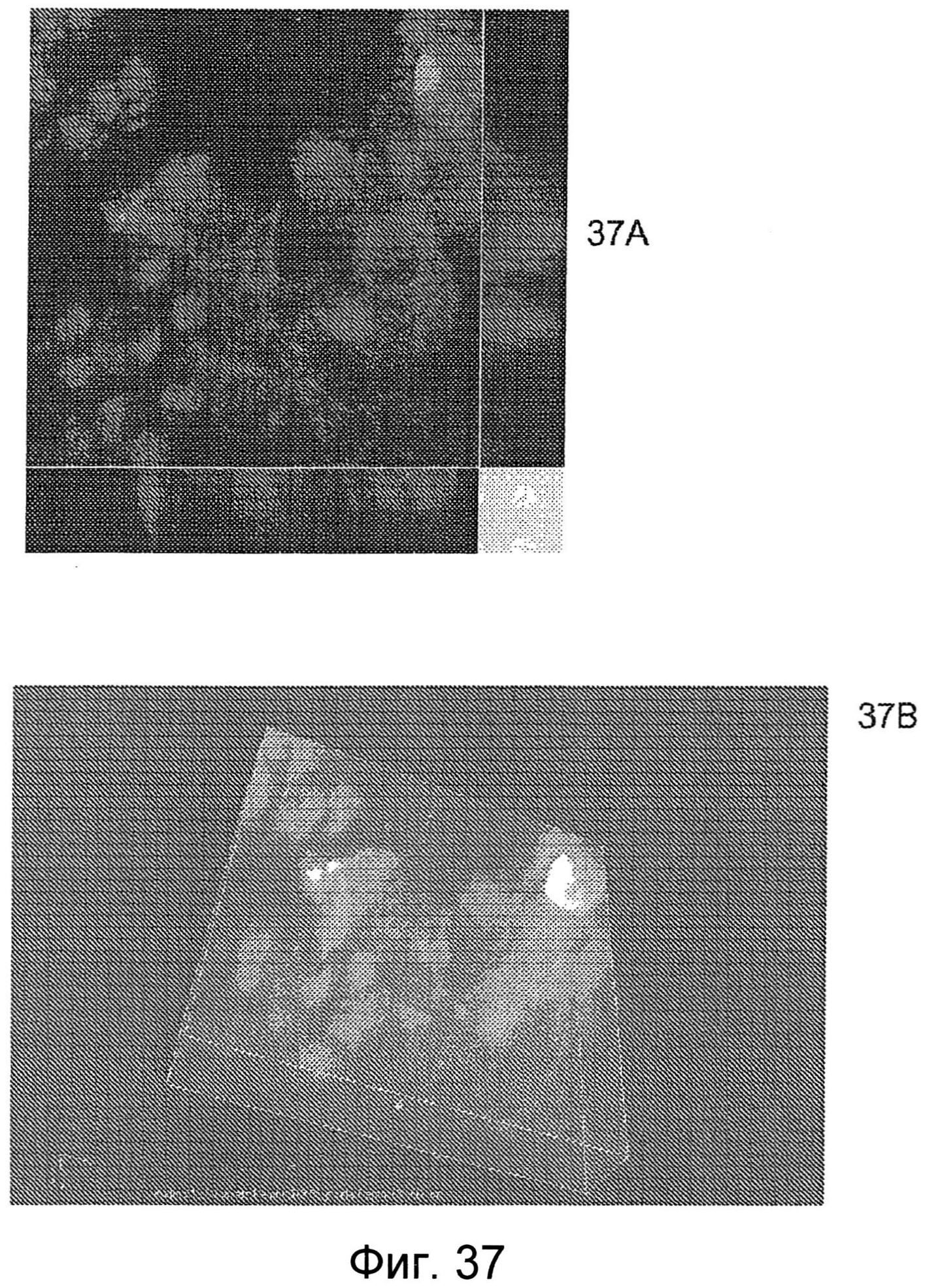
Фиг.37А и 37В показывают 3D вращающиеся/неподвижные флуоресцеин окрашенные изображения, показывающие параклеточный и трансклеточный транспорт IgG через монослой клеток на полистирольной структурированной поверхности, как описано в настоящем изобретении.
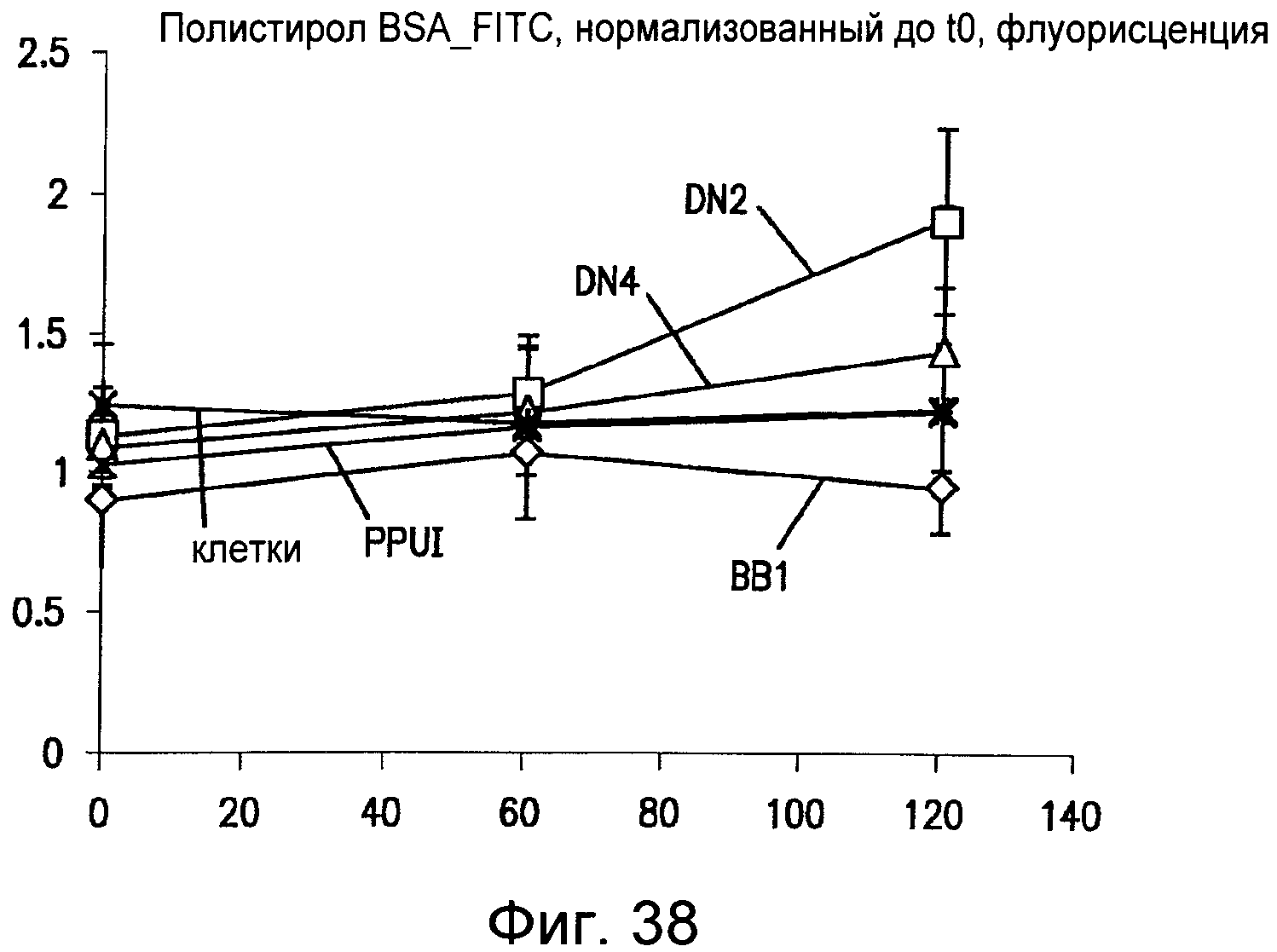
Фиг.38 графически иллюстрирует эффекты, оказываемые на проницаемость, для BSA в монослое клеток на полипропиленовых пленках, наноструктурированных как описано в настоящем изобретении.
Фиг.39 графически иллюстрирует эффекты, оказываемые на проницаемость, для IgG в монослое клеток на полипропиленовых пленках, наноструктурированных как описано в настоящем изобретении.
Фиг.40А и 40В показывают 3D вращающиеся/неподвижные флуоресцеин окрашенные изображения, показывающие параклеточный транспорт IgG через монослой клеток на полипропиленовой структурированной поверхности, как описано в настоящем изобретении.
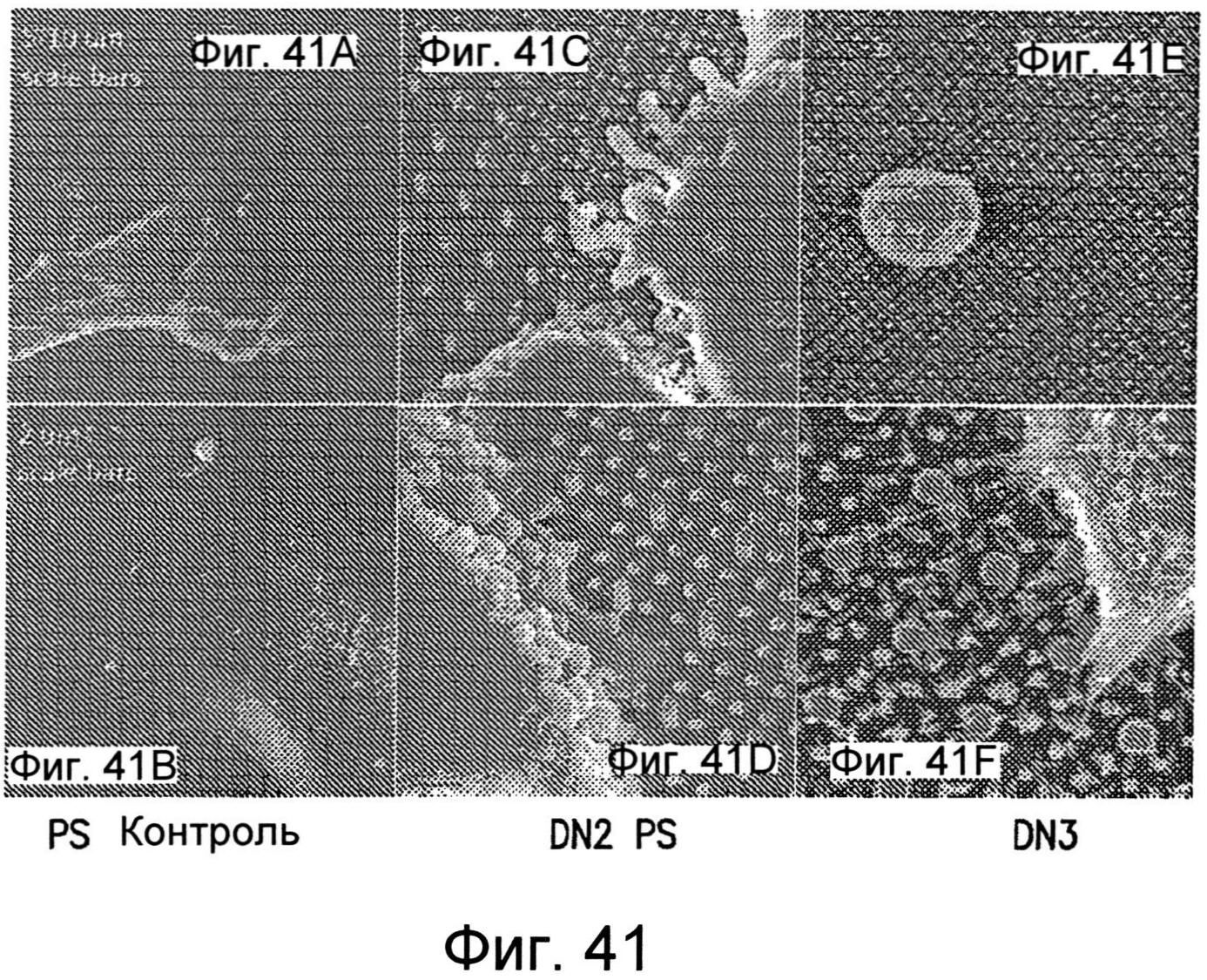
Фиг.41A-41F показывают изображения сканирующей электронной микроскопии (SEM) для клеток, культивированных на наноструктурированных поверхностях, как описано в настоящем изобретении.
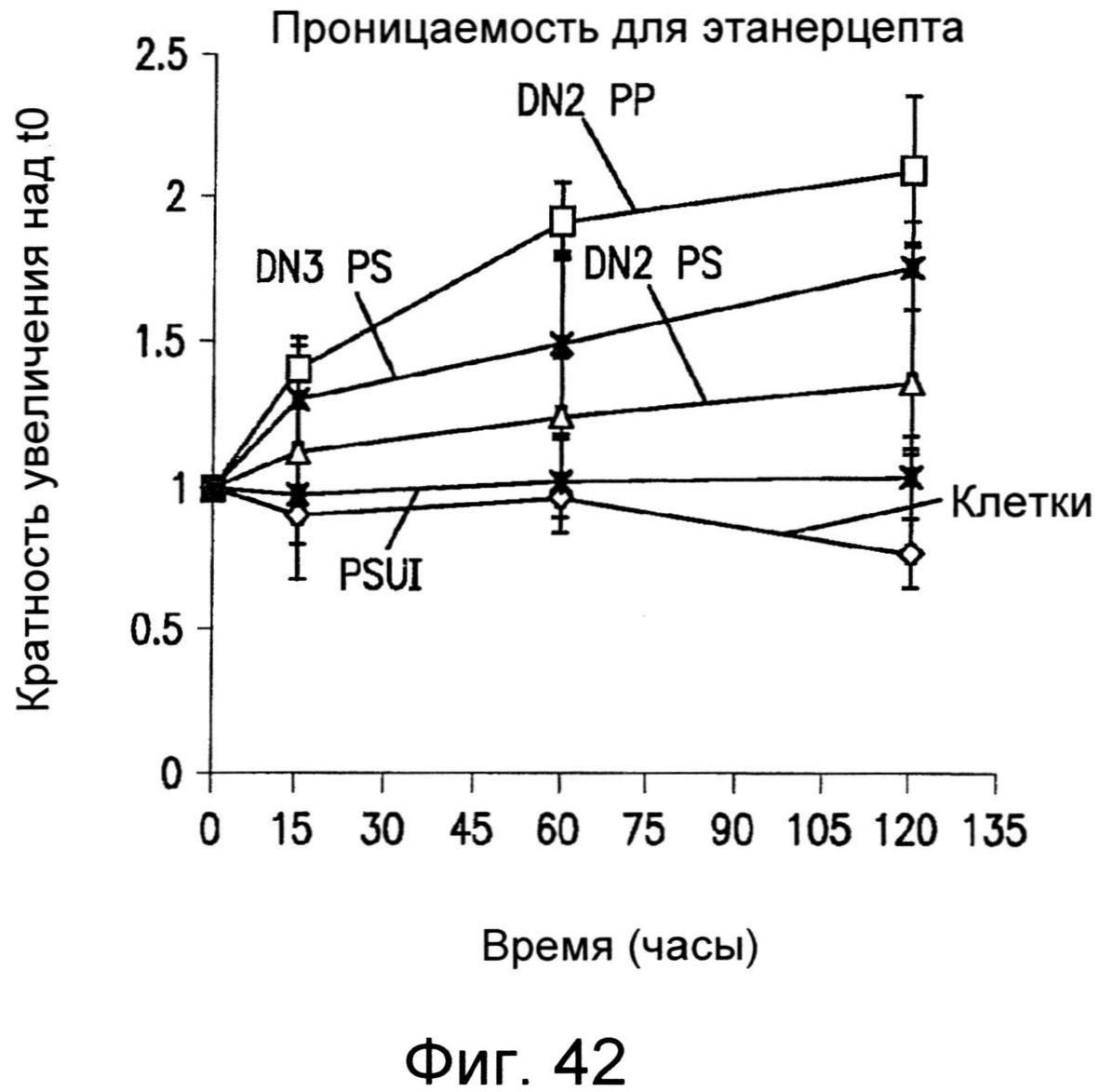
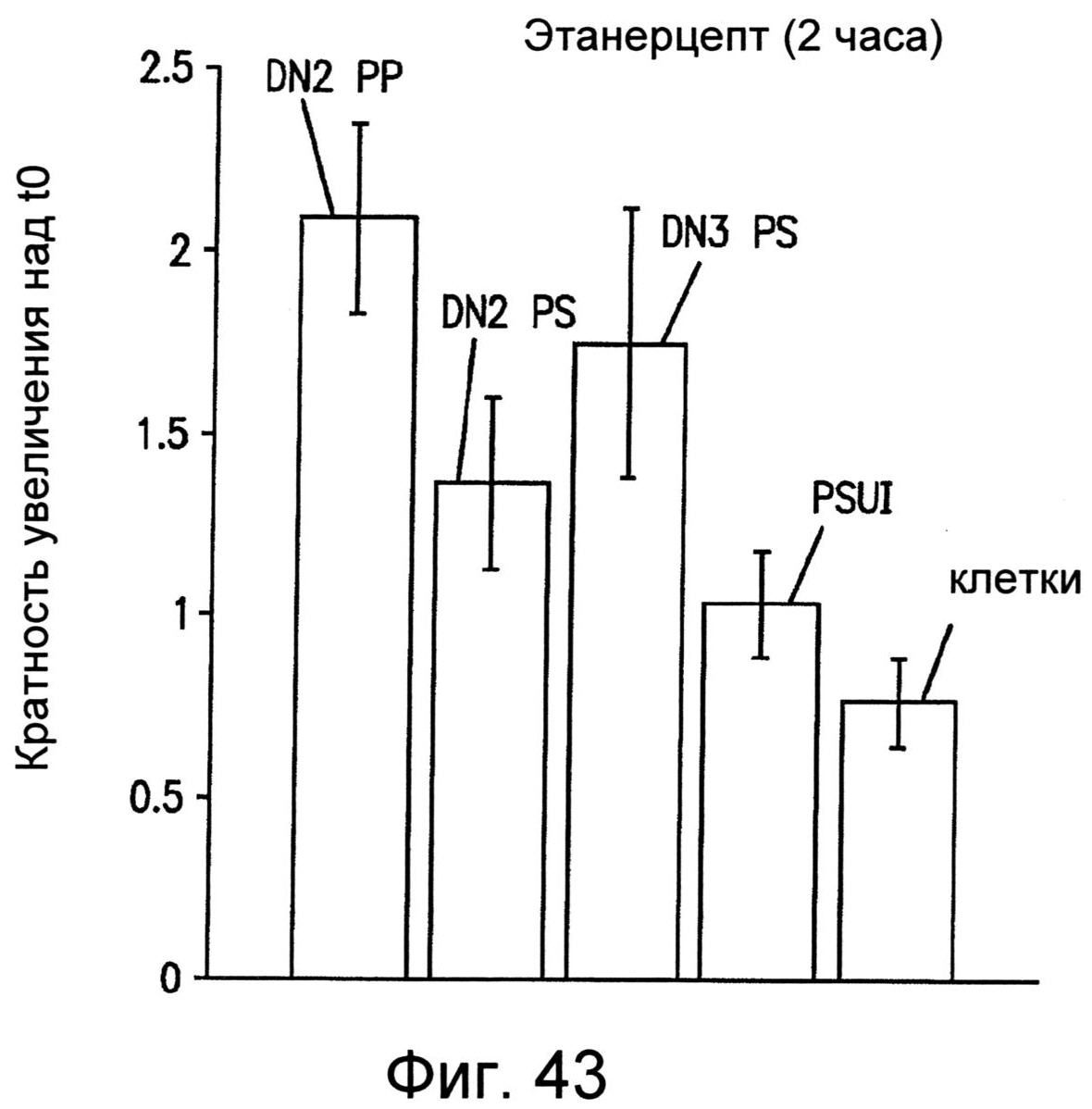
Фиг.42 иллюстрирует эффекты, оказываемые на проницаемость, для этанерцепта в монослое клеток на полипропиленовых или полистирольных пленках, наноструктурированных как описано в настоящем изобретении.
Фиг.43 иллюстрирует повышение проницаемости для этанерцепта в клеточном слое после двух часов контакта полипропиленовыми или полистирольными пленками, наноструктурированными как описано в настоящем изобретении.
Фиг.44 показывает множество микроигл, включая поверхностный слой, определяющий рисунок наноструктур на нем.
Фиг.45 показывает одну микроиглу из множества согласно Фиг.44.
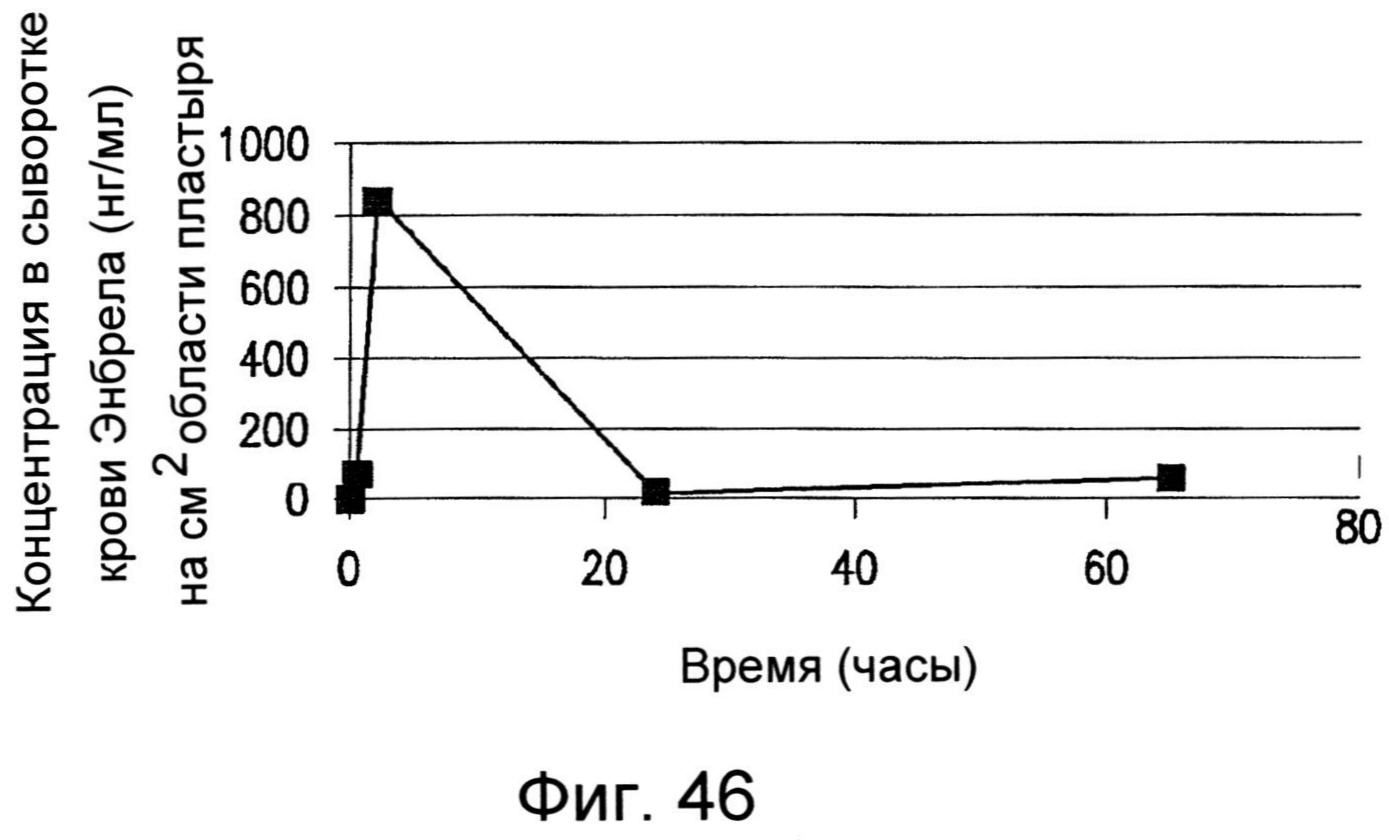
Фиг.46 графически иллюстрирует РК профиль белкового терапевтического средства, доставляемого с помощью устройства как описано в настоящем изобретении.
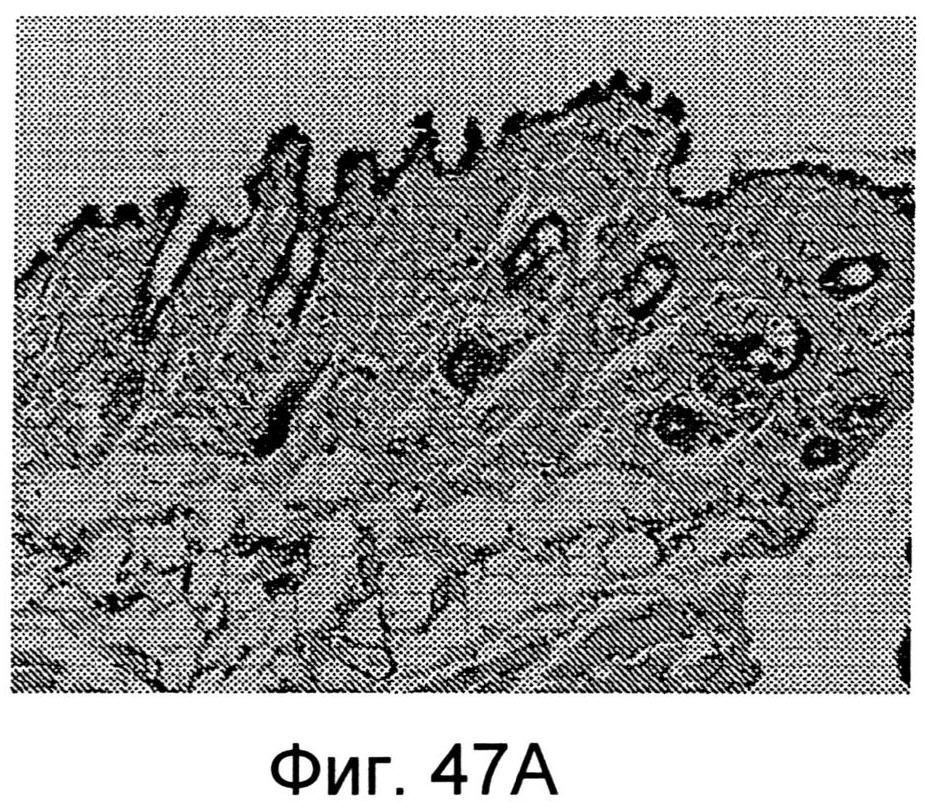
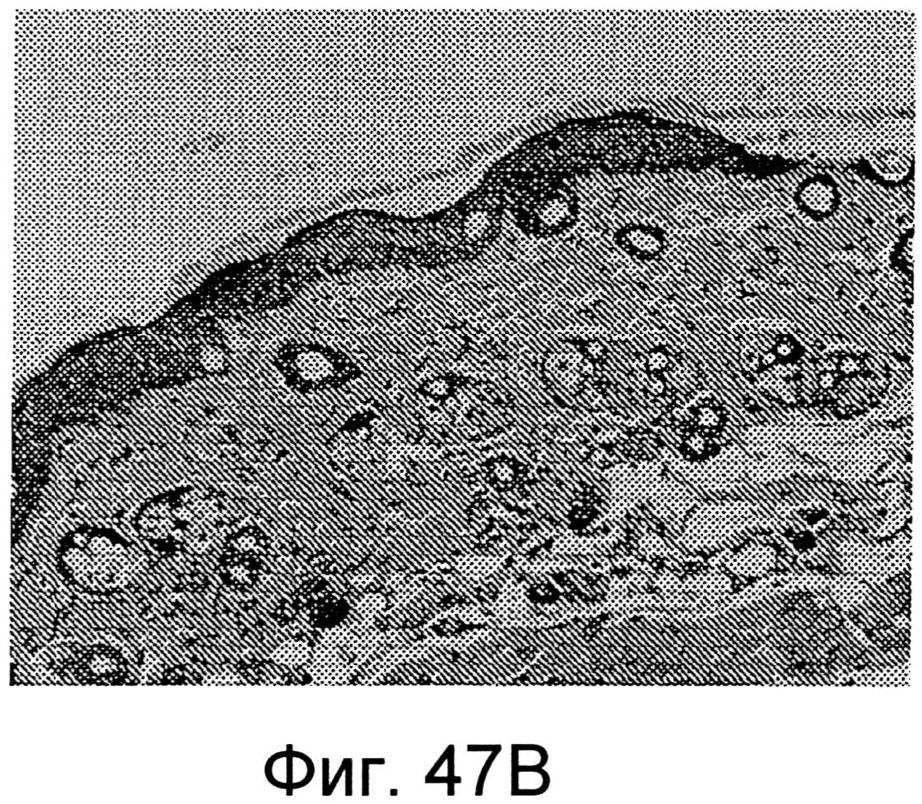
Фиг.47А и 47В показывают изображения поперечного сечения кожи после трансдермальной доставки белкового терапевтического средства через кожу. Фиг.47А показывает поперечное сечение кожи, которая была в контакте с трандермальным устройством, определяющим нанотопографию на ней, и Фиг.47В показывает поперечное сечение кожи, которая была в контакте с трандермальным устройством, без нанотопографического рисунка, сформированного на ней.
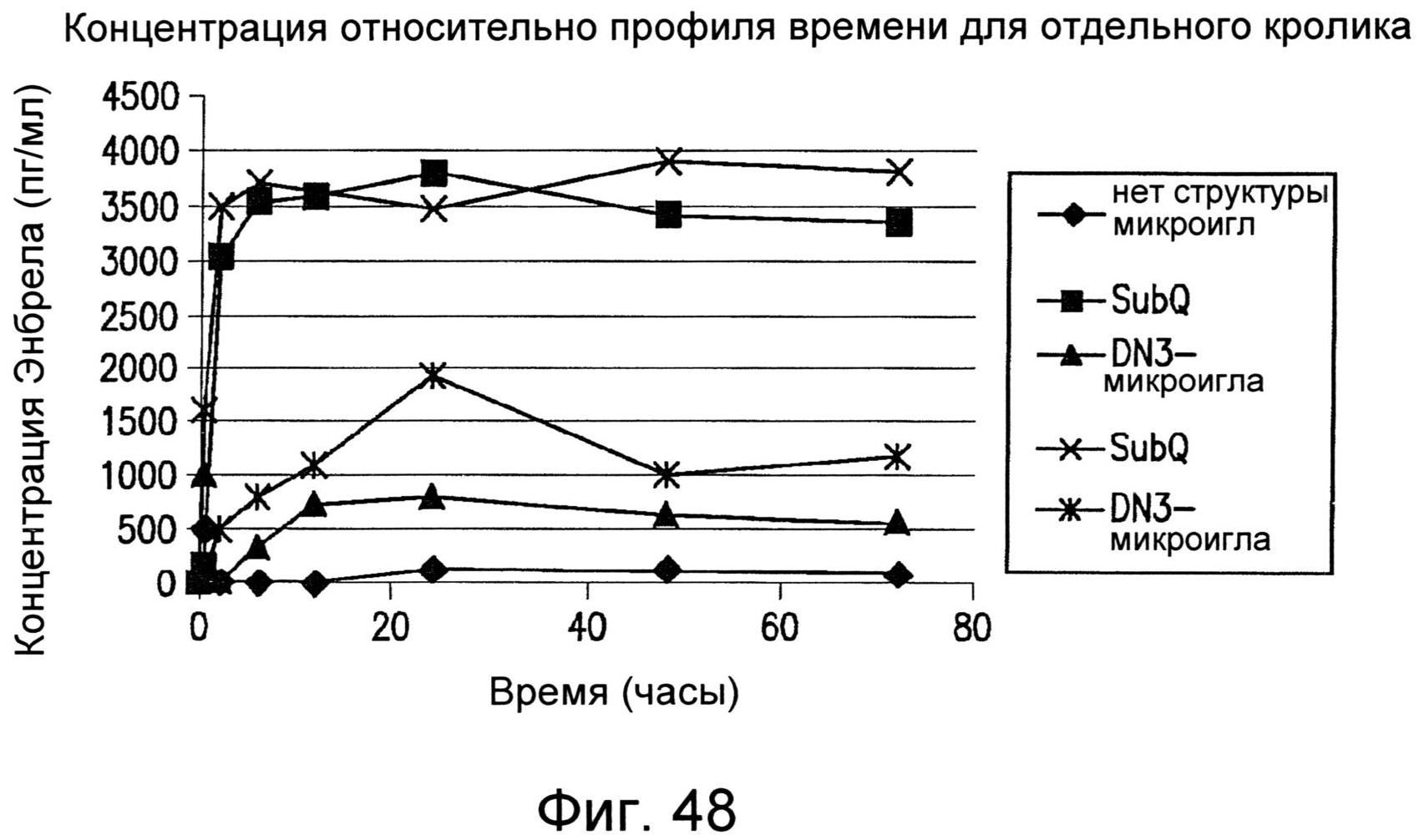
Фиг.48 графически иллюстрирует концентрацию в сыворотки крови белкового терапевтического средства, доставленного с помощью устройства, описанного в настоящем изобретении.
Подробное описание вариантов выполнения настоящего изобретения
Далее будут подробно раскрыты различные варианты выполнения объекта настоящего изобретения, один или более примеров которого раскрываются ниже. Каждый пример приводится в качестве пояснения, но не ограничения. На самом деле, специалисту в данной области техники будут очевидны различные модификации и вариации, которые могут быть сделаны без отступления от объема и сущности настоящего изобретения. Например, признаки, проиллюстрированные или описанные как часть одного варианта выполнения настоящего изобретения, могут применяться в отношении другого варианта выполнения настоящего изобретения, с получением еще одного варианта выполнения настоящего изобретения. Таким образом, подразумевается, что описание настоящего изобретения охватывает такие модификации и вариации, как входящие в объем приложенной формулы изобретения и ее эквивалентов.
В общем, раскрывается способ повышения проницаемости клеточного барьера, который включает эпителиальную ткань. Например, способы могут повышать проницаемость эпителиальной ткани кожи и могут, таким образом, способствовать трансдермальной доставки соединения. Без стремления ограничиваться какой-либо конкретной теорией, полагают, что раскрытые способы могут влиять как на параклеточный, так и на трансклеточный транспорт через клеточный барьерный слой. Например, полагают, что раскрытые способы могут влиять на образование и поддержание контактов клетка/клетка, включая плотные контакты и/или десмосомы. Открытие плотных контактов может обеспечивать параклеточный пути для улучшенной доставки активных агентов, особенно высокомолекулярных активных агентов и/или агентов, которые проявляют высокую или низкую липофильность, для которых ранее трансдермальная доставка была недоступна. Кроме того, полагают, что взаимодействие между клетками и устройством может способствовать трансклеточному транспорту через клетки и через барьер.
Согласно одному варианту выполнения настоящего изобретения, повышенная проницаемость клеточного слоя может быть определена через определение трансэпителиального электрического сопротивления (TEER, также упоминаемое в настоящей заявке как трансэпителиальное сопротивление или TER) сквозь слой. Как, в общем известно, понижение TEER сквозь клеточный слой является хорошей индикацией повышения проницаемости клеточного слоя благодаря, например, отсутствию образования или открытию плотных контактов клеточного слоя. Совершенно ясно, что в эндотелиях и определенных эпителиях, способность плотных контактов ограничивать параклеточный поток не является постоянной. Скорее это логическая функция плотных контактов, способная к динамической регуляции (Madara, 1988; Rubin, 1992). Конкретно, активация путей сигнальной трансдукции либо с помощью лигандов рецептора, либо с помощью конкретных проницаемых для мембраны модуляторов, может оказывать поразительные эффекты на проницаемость в отношении параклеточного пути. Например, активация протеинкиназы С вызывает существенное повышение проницаемости плотных контактов в MDCK клетках (Ojakian, 1981), эпителиальной клеточной линии. Повышение циклического аденозинмонофосфата (AMP) понижает проницаемость эндотелиальных клеток головного мозга в культуре, модельной системе для изучения гемоэнцефалического барьера (Rubin et al., 1991). Циклический AMP также понижает проницаемость плотных контактов в периферических эндотелиальных клетках (Stelzner et al., 1989; Langeier et al., 1991).
Свойства проницаемости плотного контакта также зависят от целостности адгезионного контакта. Разрушение адгезионного контакта путем удаления внеклеточного Са2+ приводит к открытию плотных контактов в MDCK клетках (смотрите Martinez-Palomo et al., 1980; Gumbiner and Simons, 1986) и в эндотелиальных клетках (Rutten et al., 1987). Протеинкиназы, как оказалось, участвуют в этой косвенной модуляции целостности плотного контакта в MDCK клетках (Citi, 1992). Са2+-чувствительными компонентами комплекса адгезионных контактов являются кадгерины (описано Geiger и Avalon, 1992). Эти трансдермальные белки опосредуют внутриклеточные адгезионные способности Са2+-зависимым гомофильным образом через их внеклеточные домены. Цитоплазматический домен кадгеринов связан с тремя другими белками, обозначаемыми как α-, β- и γ-катенин (Ozawa et al., 1989), которые связывают кадгерины с цитоскелетом актина и необходимы для адгезионной способности кадгерина (Hirano et al., 1987; Nagaruchi и Takeichi, 1988; Ozawa et al., 1990; Kintner, 1992; смотрите Stappert и Kemler, 1993).
Контакт между эпителиальным слоем и поверхностью устройства, которая включает рисунок из структур, образованных на поверхности, по меньшей мере часть которых создана в нанометровом масштабе, может повышать проницаемость эпителиального слоя и понижать TEER эпителиального слоя. Например, TEER эпителиального слоя может упасть до менее чем около 95%, менее чем около 85% или менее чем около 70% оот первоначального значения после контакта между слоем и наноструктурированной поверхностью в течение периода времени. Например, после около 30 минут контакта между эпителиальным слоем и поверхностью, включающей рисунок наноструктур на ней, значение TEER сквозь слой может составлять от около 90% до около 95% от его первоначального значения. Через 60 минут, значение TEER сквозь слой может составлять от около 80% до около 90% от его первоначального значения, и после 120 минут, значение TEER сквозь слой может составлять от около 60% до около 75% от его первоначального значения.
Фиг.1 иллюстрирует один способ определения значения TEER сквозь эпителиальный слой. В этом варианте выполнения настоящего изобретения клеточный слой, например, эпителиальный клеточный монослой, может быть выращен или другим образом расположен на основании апикальной камеры. Основанием апикальной камеры может быть мембрана микропористого фильтра, как показана, чтобы обеспечить поток между двумя камерами и защитить отдельные клетки от прохода в базальную камеру. Таким образом, например, мембрана микропористого фильтра может включать поры около 0.4 микрометров с плотностью около 4×106 пор на сантиметр. Конечно, конкретные параметры различных компонентов системы не являются критичными и могут быть изменены, как известно в данной области техники. Апикальная камера может быть определена транслуночной вставки, которая может быть вставлена в более большую лунку, как показана, таким образом определяя базальную камеру системы. В ходе применения первый электрод 1 и второй электрод 2 могут располагаться на любой стороне эпителиального клеточного монослоя, и омметр 4 может присоединяться между двумя электродами. Омметр 4 может обеспечивать TEER через клеточный монослой. Системы для определения TEER сквозь клеточный слой известны, например, может применяться система измерения электрической резистентности Millicell™ (доступная от Millipore, Бедфорд, Массачусетс).
Контакт между эпителиальным клеточным слоем и поверхностью, включающей наноструктуры, образованные на ней, может приводить к падению TEER, что указывает на повышение проницаемости слоя. Соответственно, после контакта между эпителиальным слоем и наноструктурированной поверхностью, способность к транспорту соединений через слой может быть существенно повышена. Это может улучшить трансдермальную доставку соединений, которые раньше не могли эффективно доставляться таким образом. Например, трансдермальная доставка высокомолекулярных соединений, липофильных соединений и/или заряженных соединений может быть улучшена с помощью применения раскрытых способов и устройств.
Устройство может включать множество наноразмерных структур, образованных на поверхности, подлежащей контакту с эпителиальным слоем. Как применяется согласно настоящему изобретению, термин «образованные», в общем, относится к структуре, которая была специальным образом спроектирована, разработана и/или сконструирована, таким образом, чтобы находиться на поверхности устройства и не равняться с элементами поверхности, которые просто являются случайным продуктом процесса производства устройства. Таким образом, на поверхности микроигл имеет предопределенный рисунок наноструктур.
Устройства включают устройства, предназначающиеся для применения в контакте с эпителиальным слоем, например, трансдермальные пластыри и тому подобное. Устройство может быть сконструировано из различных материалов, включая металлы, керамические материалы, полупроводники, органические материалы, полимеры и тому подобное, а также их композиты. Таким образом, например, могут применяться нержавеющая сталь фармацевтической категории, титан, никель, железо, золото, олово, хром, медь, их сплавы или другие металлы, материалы на основе кремния, такие как диоксид кремния, и полимеры. Как правило, устройство может быть изготовлено из биосовместимого материала, который способен создавать рисунок структур на поверхности, как описано в настоящей заявке. Термин "биосовместимый" в общем относится к материалу, который не оказывает существенного неблагоприятного влияния на клетки или ткани в области, где устройство должно осуществлять доставку. Также подразумевается, что материал не вызывает какого-либо существенного нежелательного с медицинской точки зрения эффекта в любой другой области живого субъекта. Биосовместимые материалы могут быть синтетическими или природными. Некоторые примеры подходящих биосовместимых материалов, которые также являются биоразлагаемыми, включают полимеры гидрокси кислот, как например полилактид, полигликолид, полилактид-со-гликолид молочной кислоты и гликолевой кислоты, сополимеры полиэтиленгликоля, полиангидриды, сложные поли(орто)эфиры, полиуретаны, поли(масляную кислоту), поли(валерьяновую кислоту) и поли(лактид-со-капролактон). Другие подходящие материалы могут включать, но без ограничения к этому, поликарбонат, полиметакриловую кислоту, этиленвинилацетат, политетрафторэтилен и сложные полиэфиры. Подобным образом, устройство может быть непористым или пористым по своей природе, может быть гомогенным или негомогенным по поперечному сечению устройства с точки зрения материалов, геометрии, твердости и тому подобного, и может иметь жесткое защемление или полуфиксированную форму.
Независимо от применяемых материалов, устройство может применяться для взаимодействия с эпителиальной тканью, как например, при доставке биоактивного агента через барьерный слой. Например, устройство может применяться для транспорта вещества через один или более слоев кожи. В ходе применения устройство может взаимодействовать с окружающими биологическими компонентами и регулировать или модулировать (то есть, изменять) внутриклеточную и/или межклеточную сигнальную трансдукцию, связанную с взаимодействиями клетка/клетка. Например, через взаимодействие между нанотопографией на поверхности устройства и окружающими биологическими материалами или структурами, устройство может регулировать и/или модулировать потенциал мембраны, мембранные белки и/или межклеточные контакты (например, плотные контакты, щелевые контакты и/или десмосомы), таким образом, повышая проницаемость слоя.
Кроме того, устройство может применяться для трансдермальной доставки без вызывания ответа на чужеродное тело или иммунного ответа.
Устройством может быть пластырь, который определяет нанотопографию на его контактирующей с кожей поверхностью, например, трансдермальный пластырь. Однако пластырь не ограничивается трансермальным пластырем. Например, пластырь может применяться при транспорте материала через эпителиальные барьеры в добавление к коже или альтернативно ей, как например, гемоэнцефалический барьер, относящиеся к слизистой оболочке ткани, относящиеся к желудку ткани, кровяные и лимфатические сосуды, и так далее.
В одном варианте выполнения настоящего изобретения устройство может включать микроиглу. Например, устройством может быть трансдермальный пластырь, который содержит множество микроигл на контактирующей с кожей поверхности устройства. Фиг.2 иллюстрирует типичное устройство на основе микроигл 10. Как можно увидеть, устройство включает множество отдельных игл 12; каждая из которых имеет такой размер и форму, чтобы проникать через биологический барьер без разрушения отдельных микроигл. Микроиглы могут быть твердыми, как показано на Фиг.2, пористыми или могут включать часть выемки. Микроигла может включать выемку, например, кольцеобразный канал может проходить через всю иглу или ее часть, проходя параллельно направлению иглы или ветвящимся образом, или выходя с боку иглы, соответственно. Например, Фиг.3 иллюстрирует множество микроигл 14, где каждая включает канал 16 на боковой стороне иглы, что может применяться, например, для доставки агента в подкожное расположение. Например, канал 16 может быть по меньшей мере частично выравнен с отверстием в основании 15, так чтобы формировать соединение между отверстием и каналом 16, обеспечивающее проход вещества через канал 16.
Размеры канала 16, если он присутствует, могут быть выбран специфичным образом, чтобы индуцировать капиллярный поток лекарственного соединения. Капиллярный поток, в общем, происходит когда адгезивные силы жидкости к стенкам канала больше чем когезивные силы между молекулами жидкости. Конкретно, капиллярное давление обратно-пропорционально размеру поперечного сечения канала 16 и прямо-пропорционально поверхностному натяжению жидкости, умноженному на косинус угла контакта жидкости с материалом, формирующим канал. Таким образом, чтобы ускорить капиллярный поток в пластыре, размер поперечного сечения (например, ширина, диаметр и т.д.) канала 16 могут селективно контролироваться, причем более маленькие размеры в общем приводят к более высокому капиллярному давлению. Например, в некоторых вариантах выполнения настоящего изобретения, размер поперечного сечения канала, как правило, составляет от около 1 микрометра до около 100 микрометров, в некоторых вариантах выполнения настоящего изобретения от около 5 микрометров до около 50 микрометров и в некоторых вариантах выполнения настоящего изобретения, от около 10 микрометров до около 30 микрометров. Размер может быть постоянным или может изменяться как функция от длины канала 16. Длина канала также может изменяться, чтобы приспосабливаться к различным объемам, скоростям потока и времени пребывания лекарственного соединения. Например, длина канала может составлять от около 10 микрометров до около 800 микрометров, в некоторых вариантах выполнения настоящего изобретения от около 50 микрометров до около 500 микрометров и в некоторых вариантах выполнения настоящего изобретения, от около 100 микрометров до около 300 микрометров. Площадь поперечного сечения канала может также изменяться. Например, площадь поперечного сечения может составлять от около 50 квадратных микрометров до около 1000 квадратных микрометров, в некоторых вариантах выполнения настоящего изобретения от около 100 квадратных микрометров до около 500 квадратных микрометров и в некоторых вариантах выполнения настоящего изобретения, от около 150 квадратных микрометров до около 350 квадратных микрометров. Кроме того, коэффициент пропорциональности (длина/размер поперечного-сечения) канала может находиться в интервале от около 1 до около 50, в некоторых вариантах выполнения настоящего изобретения от около 5 до около 40 и в некоторых вариантах выполнения настоящего изобретения от около 10 до около 20. В случае если размер поперечного сечения (например, ширина, диаметр и т.д.) и/или длина изменяются как функция от длины, коэффициент пропорциональности может быть определен исходя из средних размеров.
Необходимо понимать, что число микроигл, показанное на фигурах, приводится только в целях иллюстрации. Точное число микроигл, применяемое в наборе микроигл, может, например, находиться в интервале от около 500 до около 10000, в некоторых вариантах выполнения настоящего изобретения от около 2000 до около 8000, и в некоторых вариантах выполнения настоящего изобретения, от около 4000 до около 6000.
Отдельная микроигла может иметь прямой или конический вал. В одном варианте выполнения настоящего изобретения диаметр микроиглы может быть больше у основания микроиглы и постепенно сужаться к концу, удаленному от основания. Микроигла может также быть получена таким образом, чтобы иметь вал, который включает как прямую (неконическую) часть, так и коническую часть.
Микроигла может быть получена с валом, который является кольцевым или некольцевым по поперечному сечению. Например, поперечное сечение микроиглы может быть полигональным (например, звездчатой формы, квадратным, треугольным), продолговатым или любой другой формы. Вал может иметь одно или более отверстий и/или каналов.
Размер отдельных микроигл может быть оптимизирован в зависимости от желательной глубины нацеливания, требований к прочности иглы, чтобы избежать разрушения в конкретном типе ткани, и т.д. Например, размер поперечного сечения трансдермальной микроиглы может составлять от около 10 нанометров (нм) до около 1 миллиметра (мм) или от около 1 микрометра (мкм) до около 200 микрометров, или от около 10 микрометров до около 100 микрометров. Внешний диаметр может составлять от около 10 микрометров до коло 100 микрометров, и внутренний диаметр выемки иглы может составлять от около 3 микрометров до около 80 микрометров. Кончик, как правило, имеет радиус, который меньше или равен около 1 микрометр.
Длина микроиглы будет, в общем, зависеть от желательного применения. Например, длина микроиглы может составлять от около 1 микрометра до около 1 миллиметра, например, от около 500 микрометров или меньше, или от около 10 микрометров до около 500 микрометров, или от около 30 микрометров до около 200 микрометров.
Множество микроигла не обязательно должно включать все иглы, идентичные друг другу. Множество может включать микроиглы, имеющие различную длину, внешние диаметры, внутренние диаметры, формы поперечного сечения, наноструктурированные поверхности, и/или расстояния между иглами. Например, микроиглы могут быть разнесены друг от друга равномерным образом, как например, в прямоугольной или квадратной решетке или в концентрических окружностях. Расстояние может зависеть от множества факторов, включая высоту и ширину микроигл, а также количество и тип любого вещества, которое должно перемещаться через микроиглы. Тогда как применяется разнообразие расположений микроигл, особенно применяемым расположением микроигл является расстояние "от кончика к кончику" между микроиглами около 50 микрометров или более, в некоторых вариантах выполнения настоящего изобретения от около 100 до около 800 микрометров, и в некоторых вариантах выполнения настоящего изобретения от около 200 до около 600 микрометров.
Ссылаясь снова на Фиг.2, микроиглы могут удерживаться на субстрате 20 (то есть, быть присоединены к субстрату или быть одним целым с субстратом), так что они находятся перпендикулярно или под углом по отношению к субстрату. В одном варианте выполнения настоящего изобретения микроиглы могут быть ориентированы перпендикулярно к субстрату, и может быть обеспечена большая плотность микроигл на единицу площади субстрата. Однако множество микроигл может включать смесь ориентации, высот, материалов или других параметров микроигл. Субстрат 20 может быть сконструирован из жесткого или гибкого листа металла, керамики, пластмассы или другого материала. Субстрат 20 может варьироваться по толщине, удовлетворяющей иглам устройства, как например, около 1000 микрометров или менее, в некоторых вариантах выполнения настоящего изобретения от около 1 до около 500 микрометров, и в некоторых вариантах выполнения настоящего изобретения от около 10 до около 200 микрометров.
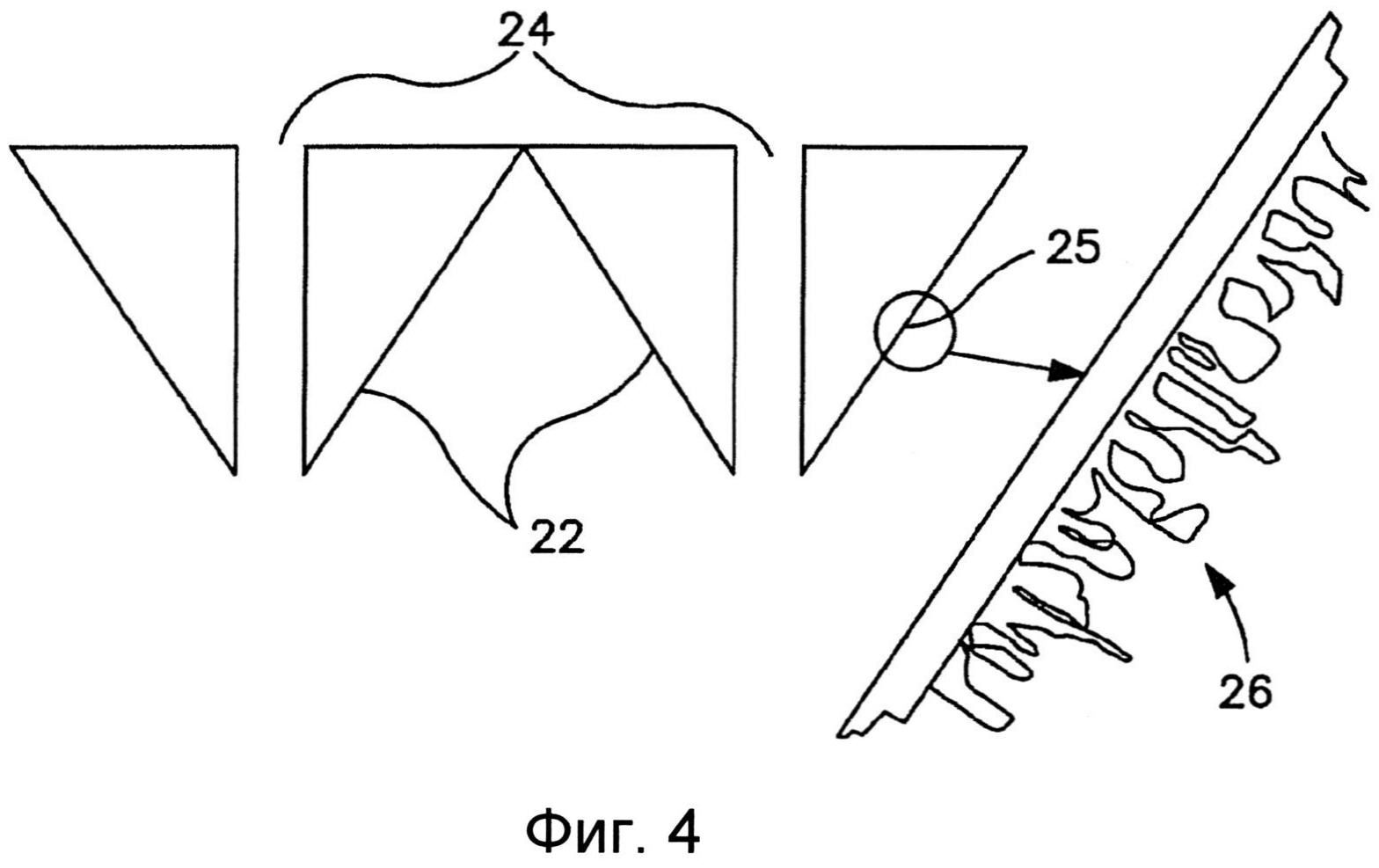
Поверхность микроигл может определять нанотопографию на ней случайным или организованным образом, так чтобы контактировать с эпителиальной тканью и повышать проницаемость ткани. Фиг.4 схематически иллюстрирует концы двух показанных в качестве примера микроигл 22, определяющих нанотопографию. В этом конкретном варианте выполнения настоящего изобретения микроиглы 22 определяют центральное отверстие 24, как может применяться для доставки активного агента через микроиглы 22. Поверхность 25 микроиглы 22 может определять нанотопографию 26. В этом конкретном варианте выполнения настоящего изобретения нанотопография 26 определяет случайный рисунок на поверхности 25 микроиглы 22.
Устройство может включать множество идентичных структур, сформированных на поверхности, или может включать различные структуры, сформированные различных размеров, форм и их комбинаций. Предпочтительный рисунок структур может включать смесь структур, имеющих различные длины, диаметры, формы поперечного сечения и/или расстояния между структурами. Например, структуры могут быть разнесены друг от друга равномерным образом, как например, прямоугольная или квадратная решетка, или в концентрических окружностях. В одном варианте выполнения настоящего изобретения, структуры могут различаться с точки зрения размера и/или формы, и могут образовывать сложную нанотопографию. Например, сложная нанотопография может определять фрактальную или фрактал-подобную геометрию.
Как применяется в описании настоящего изобретения, термин "фрактальная", в общем, относится к геометрической или физической структуре, имеющей фрагментированную форму при всех масштабах измерения от самого большого до самого маленького масштаба, так что определенные математические или физические свойства структуры являются такими, как если бы размеры структуры были больше чем размеры пространства. Рассматриваемые математические или физические свойства включают, например, периметр кривой или скорость потока в пористой среде. Геометрической формой фрактала может быть щель в частях, каждая из которых определяет самоподобие. Кроме того, фрактал имеет рекурсивное определение и тонкую структуры при произвольно маленьких масштабах.
Как применяется в описании настоящего изобретения, термин "фрактал-подобный" в общем относится к геометрической или физической структуре, имеющей одну или более, но не все, из характеристик фрактала. Например, фрактал-подобная структура может включать геометрическую форму, которая включает самоподобные части, но может не включать тонкую структуру при произвольном маленьком масштабе. В другом примере, фрактал-подобная геометрическая форма или физическая структура может не уменьшаться (или увеличиваться) в масштабе в равной степени между шагами масштаба, как может фрактал, хотя она будет повышаться или уменьшаться между рекурсивными повторами геометрической формы рисунка. Фрактал-подобный рисунок может быть проще, чем фрактальный. Например, он может быть правильной формы и относительно легче описываться традиционным языком евклидовой геометрии, тогда как фрактал не может.
Таким образом, например, поверхность трансдермального пластыря, определяющая сложную нанотопографию, может включать структуры одинаковой общей формы (например, столбы), и столбы могут быть сформированы в различных масштабах измерения (например, столбы наномасштаба, а также столбы микромасштаба). В другом варианте выполнения настоящего изобретения пластырь может включать на поверхности структуры, которые различаются как по размеру в масштабе, так и по форме, или которые различаются только по форме, тогда как имеют один и тот же наноразмерный масштаб. Кроме того, структуры могут быть сформированы организованным образом или в виде случайного распределения. В общем, по меньшей мере частью структур могут быть наноструктуры, сформированные в наноразмерном масштабе, например, определяющие размер поперечного сечения менее чем около 500 нанометров, например, менее чем около 400 нанометров, менее чем около 250 нанометров или менее чем около 100 нанометров. Размер поперечного сечения наноструктур может быть, в общем, больше чем около 5 нанометров, например, больше чем около 10 нанометров или больше чем около 20 нанометров. Например, наноструктуры могут определять размер поперечного сечения от около 5 нанометров до около 500 нанометров, от около 20 нанометров до около 400 нанометров или от около 100 нанометров до около 300 нанометров. В случаях, когда размер поперечного сечения изменяется как функция от высоты наноструктуры, размер поперечного сечения может быть определен как средний от основания до конца наноструктур, или как максимальный размер поперечного сечения структуры, например, размер поперечного сечения у основания наноструктуры конической формы.
Фиг.5 иллюстрирует один вариант выполнения сложной нанотопографии, которая может быть сформирована на поверхности. Этот конкретный рисунок включает центральный большой столб 100 и окружающие столбы 102, 104 меньших размеров, расположенные регулярным образом. Как можно увидеть, этот рисунок включает повторы столбов, каждый из которых имеет такую же общую форму, но отличается с точки зрения горизонтального размера. Этот конкретный сложный рисунок является примером фрактал-подобного рисунка, который не включает идентичное изменение масштаба между последующими рекурсивными повторами. Например, тогда как столбы 102 представляют собой первые наноструктуры, которые определяют горизонтальный размер, который составляет около одной трети от горизонтального размера более большого столба 100, который является микроструктурой, столбы 104 представляют собой вторые наноструктуры, которые определяют горизонтальный размер, который составляет около половины от горизонтального размера столбов 102.
Рисунок, который включает структуры различных размеров, может включать более большие структуры, имеющие размер поперечного сечения, сформированный в большем масштабе, например, микроструктуры, имеющие размер поперечного сечения больше чем около 500 нанометров, в комбинации с более меньшими наноструктурами. В одном варианте выполнения настоящего изобретения, микроструктуры сложно нанотопографии могут иметь размер поперечного сечения от около 500 нанометров до около 10 микрометров, от около 600 нанометров до около 1.5 микрометров или от около 650 нанометров до около 1.2 микрометров. Например, сложная нанотопография согласно Фиг.5 включает микроразмерные столбы 100, имеющие размер поперечного сечения около 1.2 микрометров.
Если рисунок включает одну или несколько более больших микроструктур, например, имеющих размер поперечного сечения больше чем около 500 нанометров, определенный либо как средний размер поперечного сечения структуры, либо как самый большой размер поперечного сечения структуры, сложная нанотопография будет также включать наноструктуры, например, первые наноструктуры, вторые наноструктуры различного размеры и/или формы, и т.д. Например, столбы 102 сложной нанотопографии на Фиг.5 имеют размер поперечного сечения около 400 нанометров, и столбы 104 имеют размер поперечного сечения около 200 нанометров.
Нанотопография может быть образована из любого числа различных компонентов. Например, рисунок элементов может включать два различных элемента, три различных элемента, пример чего проиллюстрирован на Фиг.5, четыре различных элемента или более. Относительные пропорции повторы каждого отличного элемента могут также варьироваться. В одном варианте выполнения настоящего изобретения, самые маленькие элементы рисунка будут присутствовать в большем количестве, чем более крупные элементы. Например, в рисунке согласно Фиг.5, имеется восемь столбов 104 на каждый столб 102, и восемь столбов 102 на центральный большой столб 100. Так как элементы увеличиваются по размеру, они могут, как правило, меньше повторяться в нанотопографии. Таким образом, например, первый элемент, который составляет около 0.5, например, от около 0.3 до около 0.7 по размеру поперечного сечения от второго, может присутствовать в топографии в около пять или более раз чаще, чем второй элемент. Первый элемент, который составляет около 0.25, или от около 0.15 до около 0.3 по размеру поперечного сечения от второго, может присутствовать в топографии в около десять или более раз чаще, чем второй элемент.
Расстояние между отдельными элементами может также варьироваться. Например, расстояние от центра до центра различных структур может составлять от около 50 нанометров до около 1 микрометра, например, от около 100 нанометров до около 500 нанометров. Например, расстояние от центра до центра различных структур может быть наноразмерного масштаба. Например, при рассмотрении расстояния наноразмерных структур, расстояние от центра до центра структур может быть менее чем около 500 нанометров. Это не обязательно для топографии, однако, отдельные структуры могут находиться на большом расстоянии друг от друга. Расстояние от центра до центра структур может варьироваться в зависимости от размера структур. Например, отношение среднего размера поперечного сечения двух соседних структур к расстоянию от центра до центра между этими двумя структурами может составлять от около 1:1 (например, касательно) до около 1:4, от около 1:1.5 до около 1:3.5 или от около 1:2 до около 1:3. Например, расстояние от центра до центра может составлять примерно двойную величину среднего размера поперечного сечения. В одном варианте выполнения настоящего изобретения две соседние структуры, причем каждая имеет размер поперечного сечения около 200 нанометров, могут иметь расстояние от центра до центра около 400 нанометров. Таким образом, таким образом отношение среднего размера к расстоянию от центра до центра в этом случае составляет 1:2.
Расстояние между структурами может быть одинаковым, то есть, равноотстоящие структуры, или может варьироваться для структур рисунка. Например, самые маленькие структуры рисунка могут быть отнесены друг от друга на первое расстояние, и расстояние между этими самыми маленькими структурами и более большой структурой рисунка или между двумя более большими структурами рисунка может быть таким же или отличным от этого первого расстояния.
Например, на рисунке согласно Фиг.5, самые маленькие структуры 104 имеют расстояние от центра до центра около 200 нанометров. Расстояние между более большими столбами 102 и каждым окружающим столбом 104 меньше и составляет около 100 нанометров. Расстояние между самым большим столбом 100 и каждым окружающим столбом 104 также меньше чем расстояние от центра дол центра между самыми маленькими столбами 104 и составляет около 100 нанометров. Конечно это не является обязательным, и все структуры могут быть равноотстоящими друг от друга, или возможна любая вариация в расстояниях. В одном варианте выполнения настоящего изобретения, различные структуры могут находиться в контакте друг с другом, например, одна поверх другой, как раскрывается далее, или соседствовать друг с другом или быть в контакте одна с другой.
Структуры топографии могут все быть сформированы на одной и той же высоте, в общем, от около 10 нанометров до около 1 микрометра, но это не обязательно, и отдельные структуры рисунка могут варьироваться по размеру в одном, двух или трех размерах. В одном варианте выполнения настоящего изобретения одна или все структуры топографии могут иметь высоту менее чем около 20 микрометров, менее чем около 10 микрометров или менее чем около 1 микрометр, например, менее чем около 750 нанометров, менее чем около 680 нанометров или менее чем около 500 нанометров. Например, структуры могут иметь высоту от около 50 нанометров до около 20 микрометров или от около 100 нанометров до около 700 нанометров. Например, наноструктуры или микроструктуры могут иметь высоту от около 20 нм до около 500 нм, от около 30 нм до около 300 нм или от около 100 нм до около 200 нм, хотя необходимо понимать, что структуры могут быть наноразмерными по размеру поперечного сечения и могут иметь высоту, которая может измеряться в микроразмерном масштабе, например, больше чем около 500 нм.
Микроразмерные структуры могут иметь высоту, которая является такой же или отличной наноразмерных структур того же рисунка. Например, микроразмерные структуры могут иметь высоту от около 500 нанометров до около 20 микрометров или от около 1 микрометра до около 10 микрометров, в другом варианте выполнения настоящего изобретения. Микроразмерные структуры могут также иметь размер поперечного сечения микромасштаба, больше чем около 500 нм, и могут иметь высоту наноразмерного масштаба, которая меньше чем около 500 нм.
Коэффициент пропорциональности структур (отношение высоту структуры к размеру поперечного сечения структуры) может составлять от около 0.15 до около 30, от около 0.2 до около 5, от около 0.5 до около 3.5 или от около 1 до около 2.5. Например, наноструктуры могут иметь коэффициент пропорциональности, входящий в любой из этих интервалов.
Поверхность устройства может включать один поверхностный рисунок, как показано на Фиг.5, или может включать множество повторений одинаковых или различных рисунков. Например, Фиг.6 иллюстрирует поверхностный рисунок, включающий рисунок согласно Фиг.5 при множестве повторений на поверхности.
Без стремления ограничиваться какой-либо конкретной теорией, полагают, что повышение проницаемости контактирующей эпителиальной поверхности может быть достигнуто благодаря физическим характеристикам контактирующей поверхности, включая образованные наноструктуры, по сравнению с контактирующей поверхностью, которая не включает образованные наноструктуры. Например, образование нанотопографии на поверхности может увеличивать площадь поверхности без соответствующего увеличения в объеме, которое может влиять на взаимодействие поверхности с окружающими эпителиальными клетками, и повышать проницаемость клеточного слоя. Например, увеличение отношения площади поверхности к объему, как полагают, способствует механическому взаимодействию между нанотопографией и окружающими белками, например, белками внеклеточного матрикса (ЕСМ) и/или белками плазматической мембраны. Как применяется в настоящем изобретении, термин "белок", в общем, относится к молекулярной цепи аминокислот, которая способна взаимодействовать, структурально, ферментативно или другим образом, с другими белками, полипептидами или другими органическими или неорганическими молекулами.
В общем, отношение площади поверхности к объему наноструктурированной поверхности может быть больше, чем около 10000 см-1, больше чем около 150000 см-1 или больше чем около 750000 см-1. Определение отношения площади поверхности к объему может быть осуществлено согласно любой стандартной методологии, известной в данной области техники. Например, конкретная площадь поверхности может быть получена с помощью метода физической газовой адсорбции (В.Е.Т. метод) с азотом в качестве адсорбируемого газа, как в общем известно в данной области техники и описано в документе Brunauer. Emmet, and Teller (J. Amer. Chem. Soc., vol. 60, Feb., 1938, pp.309-319), включенном в настоящую заявку посредством ссылки. BET площадь поверхности может составлять менее чем около 5 м2/г, в одном предпочтительном варианте выполнения настоящего изобретения, или от около 0.1 м2/г до около 4.5 м2/г. Значения площади поверхности и объема могут также быть оценены на основе геометрии пресс-форм, применяемых для формирования поверхности, согласно стандартным геометрическим вычислениям. Например, объем может быть оценен в соответствии с вычисленным объемом для каждого элемента рисунка, и общего числа элементов рисунка в данной области, например, на поверхности одной микроиглы.
Для устройства, которое определяет нанотопографию со сложным рисунком на поверхности, нанотопография может быть охарактеризована через определение фрактальной размерности рисунка. Фрактальная размерность - это статистическая величина, которая указывает на высокую сложность фрактала, как оказалось, чтобы заполнить пространство, так как рекурсивные повторы продолжаются до более меньшего и меньшего масштаба. Фрактальная размерность двухмерной структуры может быть выражена как:
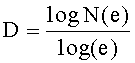
где N(e) - это число самоподобных структур, необходимое для покрытия всего объекта, когда объект уменьшается на 1/е по каждому направлению пространства.
Например, при рассмотрении двухмерного фрактала, известного как треугольник Серпинского, проиллюстрированный на Фиг.7, в котором средние точки трех сторон равностороннего треугольника соединены, и полученный внутренний треугольник отделен, фрактальная размерность вычисляется следующим образом:
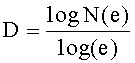
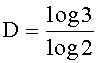
D≈1.585
Таким образом, треугольный фрактал Серпинского проявляет увеличение линейной длины по всему исходному двухмерному равностороннему треугольнику. Кроме того, это увеличение линейной длины не сопровождается соответствующим увеличением площади.
Фрактальная размерность рисунка, проиллюстрированного на Фиг.5 составляет около 1.84. В одном варианте выполнения настоящего изобретения топография поверхности устройства может проявлять фрактальную размерность более чем около 1, например, от около 1.2 до около 5, от около 1.5 до около 3 или от около 1.5 до около 2.5.
Фиг.8А и 8В иллюстрируют изображения увеличения кратности другого примера сложной нанотопографии. Нанотопография согласно Фиг.8А и 8В включает множество волокно-подобных столбов 70, расположенных на субстрате. На дистальном конце каждого отдельного столба, столб расщепляется на множество более маленьких столбов 60. На дистальном конце каждого из этих более маленьких столбов 60, каждый столб снова расщепляется на множество нитей (не видно на Фиг.8А и 8В). Структуры, сформированные на поверхности, которая имеет коэффициент пропорциональности более чем около 1, могут быть гибкими, как структуры, показанные на Фиг.8А и 8В, или могут быть жесткими.
Фиг.8С и 8D иллюстрируют другой пример сложной нанотопографии. В этом варианте выполнения настоящего изобретения множество столбов 72, где каждый включает кольцевую выемку по нему 71, сформированы на субстрате. На дистальном конце каждого столба с выемкой сформировано множество более маленьких столбов 62. Как можно увидеть, столбы на Фиг.8С и 8D сохраняют свою жесткость и вертикальную ориентацию. Кроме того, и в отличие от предшествующих рисунков, более маленькие столбы 62 этого варианта выполнения настоящего изобретения отличаются по форме от более больших столбов 72. В частности, более маленькие столбы 62 не имеют выемки, но являются твердыми. Таким образом, нанотопография, включающая структуры, сформированные в различном масштабе, не обязательно должна иметь все структуры, сформированные с одинаковой формой, и структуры могут отличать как по размеру, так и по форм, от структур отличного масштаба.
Фиг.9 иллюстрирует другой рисунок, включающий наноразмерные структуры, как они могут быть сформированы на поверхности устройства. Как можно увидеть, в этом варианте выполнения настоящего изобретения отдельные структуры рисунка могут быть сформированы одного общего размера, но отличаться друг от друга по ориентации и форме.
В дополнение к или альтернативно изучению отношения площади поверхности к объему и/или фрактальной размерности, поверхность устройства, имеющая нанотопографию, может быть охарактеризована другими способами, включая, но без ограничения к этому, шероховатость поверхности, модуль упругости, поверхностную энергию и так далее.
Способы определения шероховатости поверхности в общем известны в данной области техники. Например, способ на основе атомно-силового микроскопа в контактном или бесконтактном исполнении может применяться в соответствии со стандартной практикой для определения шероховатости поверхности. Шероховатость поверхности, которая может применяться для характеристики наноструктурированной поверхности, может включать среднюю шероховатость (RA), среднеквадратичную шероховатость, асимметрию и/или эксцесс. В общем, средняя шероховатость поверхности (то есть, средняя арифметическая высота параметра шероховатости площади поверхности, как определено в ISO 25178) поверхности, определяющей полученную нанотопографию на ней, может быть менее чем около 200 нанометров, менее чем около 190 нанометров, менее чем около 100 нанометров или менее чем около 50 нанометров. Например, средняя шероховатость поверхности может составлять от около 10 нанометров до около 200 нанометров или от около 50 нанометров до около 190 нанометров
Устройство может быть охарактеризовано модулем упругости наноструктурированной поверхности, например, по изменению модуля упругости при добавлении нанотопографии на поверхность. В общем, добавление множества структур, образующих нанотопографию на поверхности, может уменьшать модуль эластичности материала, так как добавление наноразмерных структур на поверхность будет приводить к уменьшению целостности поверхности и связанному изменению площади поверхности. По сравнению с подобной поверхностью, сформированной согласно такому же процессу из таких же материалов, но с нанотопографией на поверхности, устройство, включающее нанотопографию, может проявлять уменьшение модуля упругости от около 35% до около 99%, например, от около 50% до около 99% или от около 75% до около 80%. Таким образом, например, эффективный модуль объемной упругости наноструктурированной поверхности может составлять менее чем около 50 МПа или менее чем около 20 МПа. В одном варианте выполнения настоящего изобретения эффективный модуль объемной упругости может составлять от около 0.2 МПа до около 50 МПа, от около 5 МПа до около 35 МПа или от около 10 МПа до около 20 МПа. Эффективный модуль сдвига может составлять менее чем около 320 МПа или менее чем около 220 МПа. Например, эффективный модуль сдвига может составлять от около 4 МПа до около 320 МПа или от около 50 МПа до около 250 МПа, в одном варианте выполнения настоящего изобретения.
Устройство, имеющее нанотопографию на своей поверхности, может также проявлять увеличение поверхностной энергии по сравнению с подобным устройством, которое не имеет поверхности, определяющей рисунок нанотопографии на ней. Например, поверхность, включающая сформированную на ней нанотопографию, может проявлять увеличение поверхностной энергии, по сравнению с подобной поверхностью из таких же материалов и сформированной согласно таким же способам, но без нанотопографии на поверхности. Например, угол контакта с водой поверхности, имеющей нанотопографию на ней, может быть больше чем около 80°, больше чем около 90°, больше чем около 100° или больше чем около 110°. Например, угол контакта с водой поверхности может быть от около 80° до около 150°, от около 90° до около 130° или от около 100° до около 120°, в одном варианте выполнения настоящего изобретения.
При формировании наноструктур на поверхности устройства, плотность упаковки структур может быть доведена до максимума. Например, квадратная упаковка (Фиг.10А), гексагональная упаковка (Фиг.10В) или некоторые их вариации могут применяться для рисунка элементов на субстрате. При разработке рисунка, в котором элементы различных размеров областей поперечного сечения А, В и С находятся рядом друг с другом на подложке, может применяться кольцевая упаковка, как показано на Фиг.10С. Конечно, вариации плотности упаковки и определение связанных изменений в характеристиках поверхности входят в компетенцию специалиста в данной области техники.
В ходе применения устройство может взаимодействовать с одним или более компонентами контактирующей эпителиальной ткани с повышением проницаемости ткани. Эпителиальная ткань является одним из типов первичной ткани тела. Эпителиальная ткань, которая может стать более проницаемой в соответствии с настоящим изобретением, может включать как простой, так и многослойный эпителий, включая как кератинизированный эпителий, так и переходный эпителий. Кроме того, эпителиальная ткань согласно настоящему изобретению может включать любые типы клеток эпителиального слоя, включая, но без ограничения к этому, кератиноциты, плоские клетки, цилиндрические призматические клетки, кубовидные клетки и псевдостратифицированные клетки.
Нанотопография устройства может обеспечивать улучшенное взаимодействие между устройством и биологическими компонентами эпителиальной ткани устройства в области доставки. Например, микроиглы трансдермального устройства могут взаимодействовать непосредственно с ЕСМ белками и/или отдельными клетками, такими как кератиноциты. Более длинные иглы на трансдермальном устройстве могут применяться, чтобы достичь эпителиальных компонентов дермы, например, клеток крови капиллярного слоя. В дополнение к увеличению проницаемости эпителиального слоя и благодаря улучшенному взаимодействию между устройством и локальными биологическими компонентами, менее вероятно, что окружающая ткань будет проявлять ответ на чужеродное тело, что может уменьшить местное воспаление и улучшить доставку активных агентов. В одном варианте выполнения настоящего изобретения, устройство может играть более активную роль в доставке агента. Например, взаимодействие между нанотопографией и окружающими биологическими компонентами может способствовать доставке высокомолекулярных веществ, например, через открытие плотных контактов в зернистом слое.
Без стремления ограничиваться какой-либо конкретной теорией полагают, что образованная нанотопография способствует улучшенному взаимодействию с биологическими компонентами посредством двух механизмов. Согласно одному механизму нанотопография может улучшать способность устройства имитировать ЕСМ в сайте доставки. Например, нанотопография может имитировать один или более компонентов эпителиальной ткани в сайте доставки. При применении эпителиальная клетка может контактировать с нанотопографией устройства и реагировать образом, подобным типичному контакту с природной структурой (например, базисный мембранный белок), которую имитирует нанотопография. Соответственно, устройство может непосредственно взаимодействовать с клеткой, регулируя или модулируя (то есть, изменяя) поведение клетки, например, клеточную сигнальную трансдукцию, таким образом, улучшая доставку агента через природные барьеры.
В соответствии со вторым механизмом нанотопография может взаимодействовать с неклеточными биологическими компонентами локальной эпителиальной ткани, такими как ЕСМ белки. Например, ЕСМ белки могут адсорбироваться и десорбироваться из поверхности устройства, адсорбция/десорбция ЕСМ белков может изменять химию локального окружения, что может приводить к изменениям в поведении клетки. В соответствии с этим вторым механизмом устройство может косвенно влиять на поведение эпителиальной клетки. Например, адсорбция одного или более ЕСМ белков на поверхности устройства может косвенно регулировать или модулировать внутриклеточную и/или межклеточную сигнальную трансдукцию.
Благодаря улучшенному взаимодействию с окружающими биологическими компонентами, устройства могут способствовать улучшенному внедрению доставляемого агента. Например, фармакокинетический профиль (РК) (то есть, профиль абсорбции через эпителиальные мембраны) белкового терапевтического средства может быть усилен посредством применения устройства, включающего рисунок нанотопографии. Таким образом, например, белковое терапевтическое средство, имеющее молекулярную массу свыше 100 кДа, например, от около 100 кДа до около 200 кДа или около 150 кДа, может доставляться трансдермально с помощью пластыря, определяющего нанотопографию на его поверхности. В одном варианте выполнения настоящего изобретения, пластырь может применяться для доставки одной дозы белкового терапевтического средства, например, от около 200 до около 500 мкл, или около 250 мкл. После присоединения трансдермального пластыря к коже, реципиент может проявлять РК профиль, который отражает быстрое увеличение концентрации до от около 500 до около 1000 нанограмм терапевтического средства на миллилитр на квадратный сантиметр площади пластыря, например, от около 750 до около 850 нанограмм терапевтического средства на миллилитр на квадратный сантиметр площади пластыря, в течение от около 1 до около 4 часов после введения. Это первоначальное быстрое увеличение уровня в сыворотки крови, которое отражает быстрый проход терапевтического средства через кожный барьер, может сопровождаться менее быстрым спадом концентрации в сыворотке крови за от около 20 до около 30 часов, например, за около 24 часа, достигающим ничтожной концентрации терапевтического средства в сыворотке крови. Более того, быстрое внедрение доставляемого терапевтического средства может сопровождаться незначительным воспалением или проходить без проявления воспаления. В частности, в дополнение к стимуляции улучшенной доставки агента через трансдермальный барьер, устройства могут также ограничивать ответ на чужеродное тело и другие нежелательные реакции, такие как воспалением. Применение ранее известных устройств, таких как трансдермальные пластыри без нанотопографии на поверхности, контактирующей с кожей, часто приводило к местным областям воспаления и раздражения.
Структуры нанотопографии могут имитировать и/или взаимодействовать с одним или более ЕСМ белками, такими как коллаген, ламинин, фибронектин и т.д. Это может непосредственно или косвенно изменять белок клеточной мембраны в отношении одной или более характеристик, таки как конформация, свободная энергия и локальная плотность, которые могут, в свою очередь, влиять на взаимодействие клетки с соседями и влиять на образование или поддержание контактов между клетками, таким образом, повышая проницаемость клеточного слоя.
Более конкретно, взаимодействие устройства с компонентами эпителиального слоя, как полагают, модулирует (то есть, изменяет) структуру межклеточных контактов слоя и повышает параклеточный транспорт через слой. Межклеточным контактом может быть по меньшей мере один контакт, выбранный из группы, состоящей из плотных контактов, щелевых контактов и десмосом. Таким образом, например, взаимодействие между биологическими компонентами и структурами нанотопографии может модулировать белки клеточной сети, так чтобы индуцировать открытие плотных контактов зернистого слоя, таким образом, обеспечивая улучшенную доставку активного агента через эпидермис, и в одном конкретном варианте выполнения настоящего изобретения, высокомолекулярного агента.
Устройство может увеличивать проницаемость эпителиального клеточного слоя через изменение фокальной адгезии клеток. Фокальные адгезии представляют собой большие объединения веществ, которые могут включать 100 или более различных белков одновременно. Они являются динамичными в большинстве типов клеток и обеспечивают путь передачи информации, как механический, так и химический, от ЕСМ во внутрь клетки. Модификация фокальных адгезий происходит при изменениях в молекулярном составе, физической структуре, а также физических силах, присутствующих в ЕСМ.
Фокальные адгезий обеспечивают соединение между цитоскелетом и ЕСМ, и, в общем, рассматриваются как ядро сигнализации для передачи как механической силы, так и химического сигнала. Фокальные адгезий располагаются под клеточной мембраной, в связи с ЕСМ, в общем, через интегрины, хотя связь может осуществляться через другие трансмембранные вещества, включая гиалуронан и гепарин-сульфат связывающие белки.
Первичные белки внутри фокальных адгезий, на которые может влиять присутствие нанотопографии в области клеточной поверхности, включают винкулин, паксилин, талин, α-актинин и зиксин. Белки фокальной адгезий передают информацию цитоскелету, например, через взаимодействие с актином и через цитоплазму. Фокальные адгезий находятся в постоянном состоянии потока, однако, и белки непрерывно объединяются и разъединяются с комплексом, относя информацию от ЕСМ к другим частям клетки.
Взаимодействие между отдельными клетками и структурами нанотопографии может индуцировать проход агента через клеточный барьер и способствовать трансклеточному транспорту. Например, взаимодействие с кератиноцитами рогового слоя может способствовать проникновению агента в кератиноциты, с последующей диффузией через клетки и через липидный барьер. Тогда как агент может пересекать клеточный барьер в соответствии как с параклеточным, так и с трансклеточным путями, трансклеточный путь может быть предпочтительным для высокогидрофильных молекул, хотя, конечно, предпочтительный транспортный путь может варьироваться в зависимости от природы агента, причем гидрофильность является только одной определяющей характеристикой.
Клетки в локальной области, окружающей устройство, могут также поддерживать противовоспалительную микросреду, так как устройство может лучше имитировать локальную окружающую среду либо непосредственно, либо косвенно. Таким образом, вещества могут доставляться посредством применения устройства без развития ответа на чужеродное тело или иммунного ответа.
Конкретные типы клеток, на которые может оказываться прямое или косвенное влияние присутствием микроиглы, включают клетки окружающей кожной соединительной ткани. Например, поверхность микроиглы, определяющая нанотопографию, может быть локализована в области, которая включает клетки Лангерганса, макрофаги и/или Т-клетки, без запуска ответа на чужеродное тело или иммунного ответа. Клетки Лангерганса могут захватывать и обрабатывать антиген, становясь полностью функциональными антиген-презентирующими клетками. Макрофаги и Т-клетки играют центральную роль в инициации и поддержании иммунного ответа. После активации патологическим или иммуногенным стимулом, например через клетку Лангерганса, Т-клетки могут высвобождать IL-2, IL-4, INF-γ, и другие воспалительные цитокины. Макрофаги отвечают на этот процесс высвобождением хозяина воспалительных медиаторов, включая TNF-α, IL-1, IL-8, IL-11, IL-12, оксид азота, IL-6, GM-CSF, G-CSF, M-CSF, IFN-α IFN-β и другие. Высвобожденные цитокины активируют другие иммунные клетки, и некоторые могут также действовать в качестве независимых цитотоксических агентов. Чрезмерные высвобождение воспалительных медиаторов, производимых макрофагами и Т-клетками, может привести к повреждению нормальных клеток и окружающих тканей.
Без стремления связываться какой-либо конкретной теорией полагают, что через взаимодействие с наноструктурированным субстратом отдельные клетки могут повышающим или понижающим образом регулировать продуцирование определенных цитокинов, включая определенные хемокины. Через такое изменение в экспрессионном профиле может быть минимизирован клеточный ответ на устройство для доставки лекарственного средства. Например, воспалительный ответ и/или ответ на чужеродное тело может быть минимизирован посредством повышающей регуляции одного или более противовоспалительных цитокинов и/или понижающей регуляции одного или более провоспалительных цитокинов. Многие цитокины были охарактеризованы в соответствии с влиянием на воспаление. Провоспалительные цитокины, которые могут демонстрировать измененные экспрессионные профили, когда на экспрессирующие клетки влияет присутствие устройства, включающего нанотопографию, образованную на нем, могут включать, без ограничения к этому,, IL-1α, IL-1β, IL-2, IL-6, IL-8, IL-10, IL-12, IL16, MIG, MIP-1α, MIP-1β, КС, МСР-1, TNF-α, GM-CSI, VEGF и тому подобное. Противовоспалительные цитокины, которые могут демонстрировать измененный профиль экспрессии, могут включать, без ограничения к этому, IL-1ra, IL-4, IL-10, IL-13 и тому подобное. Цитокины, связанные с ответом на чужеродное тело, которые могут демонстрировать измененный профиль экспрессии, могут включать, без ограничения к этому, IL-4, IL-10, IL-13 и т.д.
Устройство может быть получено в соответствии с одностадийным способом, то есть. Поверхность формируется с наноструктурами на поверхности в процессе образования. Альтернативно, может применяться многостадийный процесс, в котором рисунок наноструктур образуется на предварительно сформированной поверхности. Например, множество микроигл может быть сначала сформировано, и затем случайный или неслучайный рисунок наноструктур может быть образован на поверхности сформированных микроигл. В либо одностадийном, либо двухстадийном процессе наноразмерные структуры могут образовываться на поверхности микроигл или на поверхности формы, согласно любому подходящему способу образования нанотопографии, включая, но без ограничения к этому, наноимпринтинг, инжекционное прессование, литографию, формование штамповкой и т.д.
В одном варианте выполнения настоящего изобретения, наноструктуры могут быть образованы на поверхности микроиглы. В общем, микроигла может быть сформирована в соответствии с любым стандартным микротехнологическим способом, включая, но без ограничения к этому, литографию; технологии травления, такие как влажное химическое, сухое и удаление фоторезиста; термическое окисление кислорода; нанесение покрытия методом электролитического осаждения и нанесение покрытия методом химического восстановления; диффузионные процессы, такие как диффузия бора, фосфора, мышьяка и сурьмы; ионную имплантацию; осаждение пленки, такое как выпаривание (подогреватель, электронный пучок, вспышка и затемнение, и покрытие), напыление, химическое осаждение из паровой фазы (CVD), эпитаксию (паровая фаза, жидкая фаза и молекулярный пучок), гальванопокрытие, трафаретную печать, наслоение, стереолитографию, лазерную обработку и лазерную абляцию (включая удаление выступа).
Может применяться электрохимический процесс травления, в котором электрохимическое травление твердого кремния до пористого кремния применяется для создания чрезвычайно тонких кремниевых сеток (порядка 0.01 мкм), которые могут применяться в качестве пронизывающих структур, то есть, микроигл. В этом способе может применяться электролитическое анодирование кремния в водной фотристоводородной кислоте, потенциально в комбинации со светом, для протравливания каналов в кремнии. Путем варьирования концентрации легирующей примеси кремниевой пластины, которая подлежит травлению, электролитического потенциала в ходе травления, интенсивности падающего света и концентрации электролита можно обеспечить контроль конечной пористой структуры. Невытравленный материал (то есть, оставшийся кремний) образует микроиглы.
Также может применяться плазменное травление, при котором глубокое плазменное травление кремния осуществляется с созданием микроигл с диаметрами порядка 0.1 микрометр или более. Иглы могут быть образованы непосредственно путем контроля напряжения (как при электрохимическом травлении).
Методы литографии, включая фотолитографию, литографию е-пучками, X-лучевую литографию и так далее, могут применяться для создания множества рисунков и образования эталонной матрицы. Затем может осуществляться копирование с формированием устройства, включающего нанотопорграфию на нем. Общие способы копирования включают, но без ограничения к этому, связанные с растворителем микроформование и отливку, формование штамповкой, инжекционное формование и так далее. Технологии самосборки, включая методики на основе блок-сополимера с разделенными фазами, полимерное расслоение и коллоидную литографию, могут также применяться при формировании нанотопографии на поверхности.
Как известно, могут применяться комбинации способов. Например, субстраты, структурированные с помощью коллоидов, могут подвергаться ионному травлению (RIE, также известное как сухое травление), с утончением характеристик образованной наноструктуру, таких как диаметр, профиль, высота, шаг наностолба и так далее. Влажное травление может также применяться для получения альтернативных профилей образованных наноструктур, первоначально сформированных в соответствии с другим профилем, например методикой полимерного расслоения.
Диаметр, форму и шаг структуры можно контролировать с помощью выбора соответствующих материалов и способов. Например, травление металлов, первоначально сгущенных на коллоид-структурированных субстратах, с последующим коллоидным отслаиванием, как правило, приводит к столбам в форме призмы. Процесс травления может затем применяться для завершения структур желательным образом. Упорядочные несферические полимерные наноструктуры также могут быть получены с помощью методов спекания с контролем температуры, которые позволяют получить множество упорядочных тригональных нанометровых элементов в коллоидных пустотах после селективного растворения полимерных наночастиц. Эти и другие подходящие процессы в общем известны в данной области техники (смотрите, например, Wood, J R Soc Interface, 2007 February 22; 4(12): 1-17, включенный в настоящий документ посредством ссылки).
Другие способы, которые могут применяться при формировании устройства, включающего образованную на поверхности нанотопографию, включают литографические методы наноимпринтинга, в которых используется методы обработки ультра-точным лазером, примеры которых были описаны Hunt, et al. (патент США №6,995,336) и Guo, et al. (патент США №7,374,864), оба из которых включены в настоящий документ посредством ссылки. Литография с наноимпринтингом представляет собой методику наноразмерной литографии, в которой применяется гибридная форма, которая действует как форма для литографии импринтингом, так и как фотолитографический шаблон. Схема метода литографии с наноимпринтингом проиллюстрирована на Фиг.11А-11С. В ходе производства гибридная форма 30 отпечатывается на субстрате 32 посредством приложения давления с формированием элементов на сопротивляющемся слое (Фиг.11А). В общем, поверхность субстрата 32 может быть нагрета перед соединением с формой 30 до температуры выше его температуры стеклования (Tg). В то время как гибридная форма 30 соединяется с субстратом 32, поток вязкого полимера может быть направлен в полости формы с формированием элементов 34 (Фиг.11 В). Форма и субстрат затем могут подвергаться облучению ультрафиолетом. Гибридная форма, как правило, проводит УФ-лучи, за исключением определенных отгороженных областей. Таким образом, УФ-лучи проходят через проводящие части и входят в сопротивляющийся слой. Давление поддерживается в ходе охлаждения формы и субстрата. Гибридная форма 30 затем отделяется от охлажденного субстрата 32 при температуре ниже Tg субстрата и полимера (Фиг.11С).
Для облегчения высвобождения наноотпечатанного субстрата 32, включающего образованные элементы 34, из формы 30, как показано на Фиг.11С, предпочтительно обрабатывать форму 30 покрытием с малой энергией для уменьшения сцепления с субстратом 32, так как разница между более низкой поверхностной энергией формы 30 и полученной более высокой поверхностной энергией субстрата 32 позволяет полимеру более легко высвобождаться. Таким образом, например, может применяться такое покрытие силиконовой формы как тридека-(1,1,2,2-тетрагидро)-октилтрихлорсилан (F13-TCS).
Процесс наноимпринтинга представляет собой динамический процесс, который включает заполнение формы с последующим отделением сформированного полимера от формы. Чтобы заполните элементы формы, температура полимера должна быть поднята до уровня, достаточно высокого чтобы инициировать течение при применяемом давлении. Чем выше температура, тем ниже вязкость полимера и тем быстрее и легче заполняется форма. Более высокое давление также будет повышать скорость заполнения и полноту заполнения для лучшего копирования формы. Для высвобождения наноотпечатанного субстрата из формы, температура субстрата может быть понижена до точки, в которой предел текучести превышает адгезионные силы, создаваемые формой. С помощью варьирования температуры также возможно создавать элементы поверхности полимера в ходе отделения с получением различных структур, например структур, показанных на Фиг.9.
Структуры могут также образовываться в соответствии с химическими процессами добавления. Например, осаждение пленки, напыление, химическое осаждение из паровой фазы (CVD), эпитаксия (паровая фаза, жидкая фаза и молекулярный пучок), электроосаждение и так далее могут применяться для образования структур на поверхности.
Процессы самосборки монослоя, как известно в данной области техники, могут применяться для образования узора структур на поверхности.
Например, способность блок-сополимеров к самоорганизации может применяться для формирования узора монослоя на поверхности. Затем узор может применяться как матрица для роста желательных структур, например, коллоидов, в соответствии с узором монослоя.
Например, двухмерная поперечно-сшитая полимерная сетка может быть получена из мономеров с двумя или более реакционными сайтами. Такие поперечно-сшитые монослои были сделаны с применением методики самособирающегося монослоя (SAM) (например, система золото/алкилтиол) или монослоя Ленгмюра - Блоджетта (LB) (Ahmed et al., Thin Solid Films 187: 141-153 (1990)), как известно в данной области техники. Монослой может быть поперечносшитым, что может привести к формированию более структурно прочного монослоя.
Мономеры, применяемые для формирования наноструктурированного монослоя, могут включать все структурные составляющие, необходимые для желательного метода полимеризации и/или метода образования монослоя, а также для влияния на такие свойства как общая растворимость, способы диссоциации и литографические способы. Мономер может содержать по меньшей мере одну и, более часто, по меньшей мере две реакционноспособные функциональные группы.
Молекулы, применяемые для формирования органического монослоя могут включать любые различные органические функциональные группы с включениями цепей метиленовых групп. Например, молекулой может длинноцепочечная углеродная структура, содержащая метиленовые цепи для облегчения упаковки. Упаковка между метиленовыми группами может приводить к слабому Ван-дер-ваальсовому связыванию, усиливая стабильность полученного монослоя и сопротивляясь энтропийным потерям, связанным с формированием упорядочной фазы. Кроме того, различные концевые составляющие, такие как водород-связывающие составляющие, могут присутствовать на одном конце молекул, чтобы обеспечивать рост структур на сформированном монослое, в этом случае полимеризуемые химические составляющие могут быть помещены в середине цепи или на противоположном конце. Любая подходящая химия молекулярного распознавания может применяться для формирования сборки. Например, структуры могут быть собраны на монослое посредством электростатического взаимодействия, Ван-дер-ваальсового взаимодействия, хелирования металлов, координационного связывания (то есть, взаимодействие кислота Льюиса/основание), ионного связывания, ковалентного связывания или водородного связывания.
При применении системы на основе SAM для формирования матрицы может применяться дополнительная молекула. Эта дополнительная молекула может иметь соответствующую функциональную группу на ее конце для формирования SAM. Например, на поверхности золота может быть включен терминальный тиол. Существует большое разнообразие органических молекул, которые могут применяться для воздействия на копирование. Топохимически полимеризуемые составляющие, такие как диены и диацетилены, являются особенно предпочтительными полимеризующимися компонентами. Они могут иметь включения метиленовых линкеров различной длины.
Для монослоя LB необходима только одна молекула мономера, потому что составляющая молекулярного распознавания может также служить в качестве полярной функциональной группы в целях образования LB. Литография может осуществляться на монослое LB, перенесенном на субстрат, или непосредственно во впадине. Например, монослой LB диацетиленовых мономеров может быть структурирован с помощью воздействия УФ-лучей через шаблон или путем формирования рисунка электронным лучом.
Можно облегчить образование монослоя с помощью применения молекул, которые подвергаются топохимической полимеризации в фазе монослоя. Посредством воздействия на собирающуюся пленку катализатором полимеризации может осуществляться рост пленки in situ, и может происходить изменение от динамической молекулярной сборки до более прочной полимеризованной сборки.
Любой из известных в данной области техники методов структурирования монослоя может применяться для структурирования монослоя. Полезные методики структурирования монослоя включают, но без ограничения к этому, фотолитографию, методики на основе е-пучка, методики на основе сфокусированного ионного пучка и легкую литографию. Различные схемы защиты, такие как фоторезист, могут применяться для системы на основе SAM. Подобным образом, блок-сополимерные рисунки могут образовываться на золоте и селективно вытравляться с формированием рисунков. Для двухкомпонентной системы образование рисунка может также быть достигнуто легко доступными методами.
Методики легкой литографии могут применяться для создания рисунка монослоя, где для нанесения рисунка могут применяться ультрафиолетовый свет и шаблон. Например, неструктурированный базовый монослой может применяться в качестве платформы для сборки монослоя из мономеров, реакционноспособных под действием УФ/пучка частиц. Мономерный монослой может затем быть структурирован посредством УФ фотолитографии, литографии е-пучком или литографии на основе ионного пучка, даже если базовый SAM не структурирован.
Рост структур на структурированном монослое может быть достигнут через различные механизмы роста, как например, через соответствующее восстановление солей металла и применение затравочного или опосредованного матрицей образования зародышей. При применении элементов распознавания на монослое неорганический слой может катализироваться при этом взаимодействии различными способами. Например, неорганические соединения в форме коллоидов, обеспечивающие форму структурированного органического монослоя, могут образовываться. Например, структуры из карбоната кальция или диоксида кремния могут темплатироваться различными карбонильными функциональными группами, как например, карбоновые кислоты и амиды. Посредством контроля условий роста кристаллов, можно контролировать толщину и морфологию кристалла при росте минерала. Диоксид титана также может быть темплатиорван.
Методики матричного нанесения покрытия методом химического восстановления могут применяться для синтеза металлов с применением существующих органических функциональных групп. В частности, посредством хелатирования атомов металлов до карбонильных составляющих органического рисунка, нанесение покрытия методом химического восстановления может быть катализировано на рисунке с формированием структурированных металлических коллоидов. Например, Cu, Au, Ni, Ag, Pd, Pt и многие другие металлы, наносимые в виде покрытия методом химического восстановления, могут применяться для формирования металлических структур в форме органического монослоя. Посредством контроля условий нанесения покрытия методом химического восстановления можно контролировать толщину нанесенных металлических структур.
Другие методы роста 'восходящего' типа известны в данной области техники, и может применяться, например, способ, описанный в патенте США №7,189,435 Tuominen, et al., который включен в настоящий документ посредством ссылки. Согласно этому способу проводящие или полупроводящие субстраты (например, металл, такой как золото) могут покрываться блок-сополимерной пленкой (например, блок-сополимер метилметакрилата и стирола), где один компонент сополимера образует наноразмерные цилиндры в матриксе других компонентов сополимера. Проводящий слой может затем быть размещен на поверхности сополимера с формированием сложной структуры. При вертикальном расположении сложной структуры, часть первого компонента может быть удалена, например, под воздействием УФ-лучей, пучка электронов или озона, разложения или тому подобного, с образованием наноразмерных пор в области второго компонента.
В другом варианте выполнения настоящего изобретения, как описано в патенте США №6,926,953. Nealev, et al., включенном в настоящий документ посредством ссылки, сополимерные структуры могут формироваться при воздействии на субстрат с воспроизводящим рисунок слоем, например, самособирающимся монослоем из алкилсилоксана или октадецилтрихлорсилана, двумя или более лучами выбранных длин волн, с формированием интерференционных узоров на воспроизводящим рисунок слое, с изменением смачиваемости воспроизводящего рисунок слоя в соответствии с интерференционными узорами. Слой выбранного блок-сополимера, например, сополимера полистирола и поли(метилметакрилата) может затем располагаться на открытом воспроизводящем рисунок слое и прокаливаться для разделения компонентов сополимера в соответствии с узором смачиваемости и копирования рисунка воспроизводящего рисунок слоя в сополимерном слое. Полосы и выделенные области разделенных компонентов могут, таким образом, формироваться с заданными размерами в области 100 нанометров или менее.
Поверхность устройства может включать случайное распределение образованных наноструктур. При необходимости поверхность может включать дополнительные материалы в соединении с образованными наноструктурами. Например, поверхность трарнсдермального пластыря может иметь образованный на нем электроспряденный волокнистый слой, и случайный или неслучайный узор структур может образовываться на этом электроспряденном слое.
Электропрядение включает поставщика высокого напряжения для воздействия электрическим полем на полимерный расплав или раствор, содержащийся в капиллярной трубке, включая заряд на отдельных молекулах полимера. При применении электрического поля заряд или диполярная ориентация будут индуцироваться на границе поверхности с воздухом. Индукция вызывает силу, которая противодействует поверхностному натяжению. При критической напряженности поля электростатические силы будут преобладать над силами поверхностного натяжения, и струя полимерного материала будет выбрасываться из капиллярной трубки в направлении проводящей поверхности земли. Струя удлиняется и ускоряется под действием внешнего электрического поля и покидает капиллярную трубку. Так как струя проходит по воздуху, некоторые растворители могут испаряться, с образованием заряженных полимерных волокон, которые могут собираться на поверхности. Так как волокна собираются, отдельные и все еще влажные волокна могут приклеиваться друг к другу, образуя нетканое полотно на поверхности. Узор из наноструктур может затем быть образован на электроспряденной поверхности, например с помощью методики штамповки, применяя форму, определяющую желательные наноструктуры. Воздействие формой на поверхность микроигл при подходящих температуре и давлении может привести к переносу узора на поверхность микроигл. Поверхность электроспряденных случайным образом наноразмерных волокон может далее улучшать желательные характеристики поверхности микроигл, например, одной или более областей поверхности, с точки зрения объемного отношения, шероховатости поверхности, поверхностной энергии и т.д., и может обеспечивать связанные с этим преимущества.
Поверхность устройства может быть далее функционализирована для улучшения взаимодействия с тканями и отдельными клетками в ходе применения. Например, одна или более биомолекул, таких как полинуклеотиды, полипептиды, целые белки, полисахариды и тому подобное могут быть связаны со структурированной поверхностью до применения.
В некоторых вариантах выполнения настоящего изобретения, поверхность, включающая структуры, сформированные на ней, может уже обладать подходящей реакционноспособностью, так что дополнительные желательные функциональные группы могут самопроизвольно присоединяться к поверхности без необходимости предварительной обработки поверхности. Однако в других вариантах выполнения настоящего изобретения может осуществляться предварительная обработка структурированной поверхности до присоединения желательного соединения. Например, реакционная способность структурной поверхность может быть повышена посредством добавления или создания групп амина, карбоновой кислоты, гидроксигруппы, групп альдегида, тиола или сложноэфирных групп. В одном варианте выполнения настоящего изобретения поверхность микроигл, включающая сформированный на ней узор из наноструктур, может быть аминирована через контакт с амин-содержащим соединением, таким как 3-аминопропилтриэтоксисилан, чтобы повысить аминную функциональность поверхности и привязать одну или более биомолекул к поверхности через дополнительную аминную функциональную группу.
Материалы, которые легко связываться с поверхностью устройства с нанесенным узором, могут включать ЕСМ белки, такие как ламины, тропоэластин или эластин, тропоколлаген или коллаген, фибронектин и тому подобное. Короткие полипептидные фрагменты могут связываться с поверхность устройства с нанесенным узором, как например, RGD последовательность, которая является частью последовательности распознавания интегрина, связывающего множество ЕСМ белков. Таким образом, функционализация поверхности микроигл с помощью RGD может способствовать взаимодействию устройства с ЕСМ белками и далее ограничивать ответ на чужеродное тело в отношении устройства в ходе применения.
Устройства могут быть связаны с агентом для доставки через устройство. Например, трансдермальный пластырь может применяться для повышения проницаемости эпителиального слоя и для доставки веществ под роговой слой в шиповытый слой или базальный слой, или даже глубже в дерму. В одном варианте выполнения настоящего изобретения, агент может переноситься через роговой слой в соединении с микроиглами, например, внутри микроиглы или на поверхности микроиглы.
Трансдермальный пластырь может включать резервуар, например, сосуд, пористый матрикс и т.д., который может хранить агент и предоставлять агент для доставки. Устройство может содержать резервуар внутри устройства. Например, устройство может содержать впадину или множество пор, в которых может находиться один или более агентов для доставки. Агент может высвобождаться из устройства посредством разложения части или всего устройства или через диффузию агента из устройства
На Фиг.12А и 12В приведены виды в перспективе устройства, включающего резервуар. Устройство 110 включает резервуар 112, определенный непроницаемым защитным слоем 114 и множеством микроигл 116. Защитный слой и множество микроигл 116 соединены вместе у внешней периферии устройства, как показано позицией 118. Непроницаемый защитный слой 114 может быть присоединен посредством адгезии, термосклеивания и тому подобного. Устройство 110 также включает множество микроигл 120, включающих сформированные на поверхности наноструктуры (не показано). Покровная пленка 122 может быть удалена до применения устройства для открытия микроигл 120.
Композиция, включающая один или более агентов может находиться внутри резервуара 112. Материалы, подходящие для применения в качестве непроницаемого защитного слоя 114, могут включать такие материалы, как сложные полиэфиры, полиэтилен, полипропилен и другие синтетические полимеры. Материал, как правило, подвергается термосклеиванию или прикреплению другим путем к защитному слою для обеспечения барьера в отношении поперечного потока содержимого резервуара.
Резервуар 112, определенный пространством и зазором между непроницаемым защитным слоем 14 и множеством микроигл 16, обеспечивает хранилище, в которое вводится суспензия агентов для хранения. Резервуар может формироваться из множества материалов, которые совместимы с агентом, подлежащим хранению в нем. Например, природные и синтетические полимеры, металлы, керамики, полупроводниковые материалы и их композиты могут образовывать резервуар.
В одном варианте выполнения настоящего изобретения резервуар может быть присоединен к субстрату, на котором локализованы микроиглы. Согласно другому варианту выполнения настоящего изобретения резервуар может быть отдельным и присоединяемым к множеству микроигл с возможностью удаления, или находится во взаимодействие потоком с множеством микроигл, например через трубу, зажимы Люэра и т.д..
Устройство может включать один или множество резервуаров для хранения агентов, которые подлежат доставке. Например, устройство может содержать один резервуар, в котором хранится одна композиция агента, или устройство может содержать множество резервуаров, в каждом из которых хранится один или более агентов, для доставки во все или часть множества микроигл. Во множестве резервуаров может также храниться материал, который может объединяться для доставки. Например, первый резервуар может содержать агент, например лекарственное средство, а второй резервуар может содержать носитель, например, соляной раствор. Различные агенты могут смешиваться перед доставкой. Смешение может запускаться средствами, включающими, например, механическое разрушение (то есть. прокалывание, разложение или разбиваниед), изменение пористости или электрохимическое разрушение стенок или мембран, разделяющих камеры. Множество резервуаром могут содержать различные активные агенты для доставки вместе с друг с другом или последовательно.
В одном варианте выполнения настоящего изобретения резервуар может находиться во взаимодействии потоком с одной или более микроиглами трансдермального устройства, и микроиглы могут определять структуру (например, центральное или боковое отверстие), чтобы обеспечивать транспорт доставляемых агентов под барьерный слой.
В альтернативных вариантах выполнения настоящего изобретения, устройство может включать узел микроигл и узел резервуара с предотвращением потока между ними до применения. Например, устройство может включать мембрану высвобождения, расположенную рядом как с резервуаром, так и множеством микроигл. Мембрана высвобождения может быть отделена от устройства до применения, так что в ходе применения резервуар и множество микроигл находятся во взаимодействии потоком друг с другом. Отделение может осуществляться посредством частичного или полного отсоединения мембраны высвобождения. Например, согласно Фиг.13-18, показан один вариант выполнения мембраны высвобождения, которая сконфигурирована с возможностью отделения от трансдермального пластыря с инициацией потока лекарственного соединения. Более конкретно, Фиг.13-14 показывают трансдермальный пластырь 300, который содержит узел доставки лекарственного средства 370 и узел микроигл 380. Узел доставки лекарственного средства 370 включает резервуар 306, расположенный рядом с контролирующей скорость мембраной 308.
Контролирующая скорость мембрана может способствовать замедлению скорости потока лекарственного соединения при его высвобождении- В частности, текущие лекарственные средства, выходящие из резервуара для лекарственного средства в узел микроигл через микрожидкостные каналы, могут испытывать падение давления, приводящее к уменьшению скорости потока. Если эта разность слишком велика, может создаваться некоторое противодавление, которое может препятствовать потоку соединения и потенциально превышать капиллярное давление жидкости через микрожидкостные каналы. Таким образом, применение контролирующей скорость мембраны может улучшать эту разность в давлении и обеспечивать введение лекарственного соединения в микроиглу при более контролируемой скорости потока. Конкретные материалы, толщина и т.д. контролирующей скорость мембраны могут варьироваться в зависимости от множества факторов, таких как вязкость лекарственного соединения, желательное время доставки и т.д.
Контролирующая скорость мембрана может формироваться из проницаемых, полупроницаемых и микропористых материалов, которые известны в данной области техники, чтобы контролировать скорость лекарственных соединений, и обладающих проницаемостью для более низкого проникновения, чем у резервуара для лекарственного средства. Например, материал, применяемый для образования контролирующей скорость мембраны, может иметь средний размер пор от около 50 нанометров до около 5 микрометров, в некоторых вариантах выполнения настоящего изобретения от около 100 нанометров до около 2 микрометров и в некоторых вариантах выполнения настоящего изобретения от около 300 нанометров до около 1 микрометра (например, около 600 нанометров). Подходящие материалы мембраны включают, например, волоконные полотна (например, тканные или нетканые), пленки с отверстиями, пены, губки и т.д., которые формируются из полимеров, таких как полиэтилен, полипропилен, поливинилацетат, этилен-н-бутилацетат и этилен-винилацетат сополимеры. Такие материалы мембран также более подробно описываются в патентах США №3,797,494, 4,031,894, 4,201,211, 4,379,454, 4,436,741, 4,588,580, 4,615,699, 4,661,105, 4,681,584, 4,698,062, 4,725,272, 4,832,953, 4,908,027, 5,004,610, 5,310,559, 5,342,623, 5,344,656, 5,364,630 и 6,375,978, которые включены в настоящий документ в полном объеме посредством ссылки. Особенно подходящий материал мембраны доступен от Lohmann Therapie-Systeme.
Согласно Фиг.13-14, хотя необязательно, узел 370 также содержит адгезивный слой 304, который располагается рядом с резервуаром 306. Узел микроигл 380 подобным образом подложку 312, из которой распространяется множество микроигл 330, имеющих каналы 331, такие как описано выше. Слои узла доставки лекарственного средства 370 и/или узла микроигл 380 могут быть соединены вместе, если желательно, применяя любою известную методику соединения, как например, через адгезивное соединение, термическое соединение, ультразвуковое соединение и т.д.
Независимо от конкретной применяемой конфигурации, пластырь 300 также содержит мембрану высвобождения 310, которая располагается между узлом доставки лекарственного средства 370 и узлом микроигл 380. Тогда как мембрана высвобождения 310 может при необходимости быть связана с соседней подложкой 312 и/или контролирующей скорость мембраной 308, как правило, желательно, чтобы она была только слегка связана, если вообще была связана, так чтобы мембрана высвобождения 310 могла быть легко отделена от пластыря 300. Если желательно, мембрана высвобождения 310 может также содержать лепестковую часть 371 (Фиг.13-14), которая выходит по меньшей мере частично за пределы периметра пластыря 300, чтобы облегчить пользователю стадию захвата мембраны и оттягивания ее в желательную сторону. В его "неактивной" конфигурации, как показано на Фиг.13-14, узел доставки лекарственного средства 370 пластыря 300 безопасно удерживает лекарственное соединение 307, так что оно не протекает в какой-либо существенной степени в микроиглы 330. Пластырь может быть "активирован" путем простого приложения силы к мембране высвобождения, так чтобы отсоединить ее от пластыря.
Согласно Фиг.15-16, в одном варианте активации показан пластырь 300, в котором узел мембраны высвобождения 310 отодвигается в продольном направлении. Полная мембрана высвобождения 310 может быть удалена как показано на Фиг.17-18, или она может быть просто частично отсоединена, как показано на Фиг.15-16. В любом случае, однако, уплотнение, ранее сформированное между мембраной высвобождения 310 и отверстием (не показано) подложки 312, разрушается. Таким образом лекарственное соединение 107 может вытекать из узла доставки лекарственного средства 170 в каналы 131 микроигл 130 через подложку 112. Примерная иллюстрация как лекарственное средство 307 течет из резервуара 306 в каналы 331 показано на Фиг.17-18. Необходимо отметить, что поток лекарственного соединения 307 пассивно инициируется и не требуется каких-либо активных механизмов смещения (например, насосы).
В вариантах выполнения настоящего изобретения, показанных на Фиг.13-18, отсоединение мембраны высвобождения немедленно инициирует поток лекарственного соединения в микроиглы, так как узел доставки лекарственного средства ухе помещен во взаимодействие потоком с узлом микроигл. В определенных вариантах выполнения настоящего изобретения, однако, может быть желательно обеспечить пользователю большую степень контроля над временем высвобождения лекарственного соединения. Оно может сопровождаться применением конфигурации пластыря, в которой узел микроигл первоначально не находиться во взаимодействии потоком с узлом лекарственного средства. Когда необходимо применить пластырь, пользователь может физическим путем привести два отдельных узла во взаимодействие потоком. Мембрана высвобождения может быть отделена либо до, либо после осуществления такого физического действия.
Согласно Фиг.19-24, например, показан один конкретный вариант выполнения пластыря 200. Фиг.19-20 иллюстрируют пластырь 200 до применения и показывают первую часть 250, образованную узлом микроигл 280 и вторую часть 260, образованную узлом доставки лекарственного средства 270. Узел доставки лекарственного средства 270 включает резервуар 206, расположенный рядом с контролирующей скорость мембраной 208 как описано выше. Хотя необязательно, узел 270 также содержит адгезивный слой 204, который располагается рядом с резервуаром 206. Узел микроигл 280 подобным образом включает подложку 212,из которой выходит множество микроигл 230, имеющих каналы 231, такие, как описано выше.
В этом варианте выполнения настоящего изобретения подложка 212 и контролирующая скорость мембрана 208 первоначально располагаются горизонтально рядом друг с другом, и мембрана высвобождения 210 распространяется за подложку 212 и контролирующую скорость мембрану 208. В этом конкретном варианте выполнения настоящего изобретения, в общем, желательно, чтобы мембрана высвобождения 210 отделяемым образом присоединялась к подложке 212 и контролирующей скорость мембране 208 с адгезивом (например, чувствительный к давлению адгезив). В этой "неактивной" конфигурации, как показан на Фиг.19-20, узел для доставки лекарства 270 пластыря 200 удерживает лекарственное соединение в безопасности 207, так что оно не протекает в существенной степени в микроиглы 230. Когда необходимо "активировать" пластырь, мембрана высвобождения 210 может быть ободрана и удалена, как, например, показано на Фиг.21-22, для разрушения уплотнения, сформированного между мембраной высвобождения 210 и отверстием (не показано) подложки 212. После этого вторая секция 260 может быть сложена около линии сгибы "F", как показано направляющей стрелкой на Фиг.23, так что контролирующая скорость мембрана 208 располагается вертикально рядом с подложкой 212 и находится во взаимодействии потоком с ней. Альтернативно, может быть сложена первая секция 250. Безотносительно к этому, сложение секций 250 и/или 260 инициирует течение лекарственного соединения 207 из узла для доставки лекарственного средства 270 и в каналы 231 микроигл 230 через подложку 212 (Смотрите Фиг.24).
Устройство может доставлять агент со скоростью, полезной для терапевтической пользы. В соответствии с этой целью трансдермальное устройство может включать нишу с микроэлектроникой и другими микрообработанными структурами для контроля скорости доставки либо согласно запрограммированной схеме, либо через активное взаимодействие с пациентом, профессионалов в области здравоохранения или биодатчиком. Устройство может включать материал на поверхности, имеющий заданную скорость разложения, так чтобы контролировать высвобождение агента, содержащегося в устройстве. Скорость доставки может контролироваться путем управления множеством факторов, включая характеристики подлежащей доставке композиции (например, вязкость, электрический заряд и/или химический состав); размеры каждого устройства (например, внешний диаметр и объем любых отверстий); число микроигл на трансдермальном пластыре; число отдельных устройств в матриксе-носителе; приложение движущей силы (например, градиент концентрации, градиент напряжения, градиент давления); применение клапана и т.д.
Транспорт агентов через устройство может регулироваться или контролироваться, например, с применением клапанов, насосов, датчиков, управляющих устройств и микропроцессоров. Эти компоненты могут быть получены путем применения стандартных способов производства или микропроизводства. Управляющие устройства, которые могут применяться с устройством по изобретению, включают микронасосы, микроклапаны и позиционеры. Например, микропроцессор может быть запрограммирован для контроля насоса или клапана, таким образом контролируя скорость доставки.
Поток агента через устройство может происходить на основе диффузии или капиллярного действия, или может инициироваться посредством применения обычных механических насосов или немеханических управляющих сил, таких как электроосмос или электрофорез, или конвенция. Например, при электроосмосе, электроды располагаются на биологической поверхности (например, поверхность кожи), поверхности пластыря, микроигле и/или соседнем с микроиглой субстрате, для создания конвективного потока, который несет противоположно заряженные ионные частицы и/или нейтральные молекулы по направлению или в сайт доставки.
Потоком агента можно управлять посредством выбора материала, формирующего поверхность устройства. Например, одна или более больших выемок рядом с поверхностью устройства, контактирующей с тканью, могут применяться для направления прохода лекарственного средства, особенно в жидком состоянии. Альтернативно, физическими свойствами поверхности устройства можно манипулировать, либо чтобы инициировать, либо чтобы ингибировать транспорт материала вдоль поверхности, как например, путем контроля гидрофильности или гидрофобности.
Поток агента может регулироваться с помощью применения клапанов и затворов, как известно в данной области техники. Клапаны могут неоднократно открываться и закрываться, или они могут быть одноразовыми клапанами. Например, разрушаемый барьер или односторонний затвор могут устанавливаться в устройстве между резервуаром и поверхностью с узором. При готовности использования резервуар может быть разрушен, или затвор может быть открыт, обеспечивая поток по поверхности микроигл. Другие клапаны и затворы, применяемые в устройстве, могут быть активированы термически, электрохимически, механически или магнитно для селективной инициации, модуляции или остановки потока молекул через устройство. В одном варианте выполнения настоящего изобретения поток контролируется с применением ограничивающей скорость мембраны в качестве "клапана".
В общем, любая система контроля доставки агента, включая резервуары, системы контроля потока, системы распознавания и т.д., известная из области техники, может быть включена в устройство. Например, патенты США №7,250,037, 7,315,758, 7,429,258, 7,582,069 и 7,611,481 раскрывают резервуар и системы контроля, которые могут быть включены в устройства.
Агенты, которые могут доставляться устройством, могут предназначаться для доставки в локальную области рядом с устройством или могут предназначаться для более глубокого распределения.
Нанотопография устройства может улучшать доставку агентов, при этом минимизируя ответ на чужеродное тело и иммунный ответ.
Раскрывается устройство, которое может повышать проницаемость клеточного слоя и которое может обеспечивать маршрут для доставки лекарственных соединений, ранее недоступный для доставки белковых терапевтических средств. Как применяется в настоящей заявке, термин 'белковые терапевтические средства' в общем относится к любым биологически активным белковым соединениям, включая, без ограничения к этому, природные, синтетические и рекомбинантные соединения, слитые белки, химеры и т.д., а также соединения, включающие 20 стандартных аминокислот и/или синтетические аминокислоты. Доставка белковых терапевтических средств связана с проблемами из-за естественных барьеров кожи. В одном варианте выполнения настоящего изобретения, устройство может применяться для трансдермальной доставки высокомолекулярных агентов (например агентов, имеющих молекулярную массу более около 400 Да, более около 10 кДа, более около 20 кДа или более около 100 кДа, например, около 150 кДа).
Даже когда желательно доставить низкомолекулярные агенты, устройство может обеспечивать повышенную эффективность и улучшенное внедрение благодаря повышенной проницаемости эпителиальной ткани.
Не конкретного ограничения агентов, которые могут доставляться с помощью раскрытого устройства. Агенты могут включать белковоподобные агенты, такие как инсулин, иммуноглобулины (например, IgG, IgM, IgA, IgE), TNF-α, проитвовирусные лекарственные средства и т.д.; полинуклеотидные агенты, включая плазмиды, миРНК, РНКи, нуклеозидные противораковые лекарственные средства, вакцины и т.д.; и низкомолекулярные агенты, такие как алкалоиды, гликозиды, фенолы и т.д.. Агенты могут включать противоинфикционные агенты, гормоны, лекарственные средства, регулирующие работу сердца и поток крови, контролирующие боль и т.д. Другие вещества, которые могут доставляться в соответствии с настоящим изобретением, представляют собой агенты, полезные для профилактики, диагностики, уменьшения, лечения или вылечивания заболевания. Неограничивающий список агентов включает противоангиогенезные агенты, антидепрессанты, противодиабетические агенты, антигистамины, противовоспалительные агенты, буторфанол, кальцитонин и аналоги, СОХ-11 ингибиторы, дерматологические агенты, агонисты и антагонисты допамина, энкефалины и другие опиоидные пептиды, эпидермальные факторы роста, эритропоэтин и аналоги, фолликулостимулирующий гормон, глюкагон, гормон роста и аналоги (включая гормон, высвобождающий гормон роста), антагонисты гормона роста, гепарин, гирудин и аналоги гирудина, такие как гирулог, IgE супрессоры и другие белковые ингибиторы, иммуносупрессоры, инсулин, инсулинотропин и аналоги, интерфероны, интерлейкины, лютеинизирующий гормонлютеинизирующий гормон, гормон, высвобождающий лютеинизирующий гормон, и аналоги, моноклональные или поликлональные антитела, препараты против морской болезни, релаксанты мышц, наркотические анальгетики, никотин, нестероидные противовоспалительные агенты, олигосахариды, паратиреоидный гормон и аналоги, антагонисты паратиреоидного гормона, антагонисты простагландина, простагландины, скополамин, седативные средства, агонисты и антагонисты серотонина, средства для лечения половой гипофункции, активаторы тканевого плазминогена, транквилизаторы, вакцины с носителями/адъювантами или без них, сосудорасширяющие средства, основные диагностирующие средства, такие как туберкулин и другие гиперчувствительные агенты, как описывается в патенте США №6,569,143, озаглавленном "Method of Intradermally Injecting Substances", полное содержание которого включено в настоящий документ посредством ссылки. Композиции вакцины могут включать антиген или антигенную композицию, способные вызывать иммунный ответ против патогенов человека или других вирусных патогенов.
Для лучшего понимания в описании настоящего изобретения приводятся примеры, раскрытые далее.
Пример 1
Несколько различных форм были получены с применением фотолитографической методики similar, подобно конструирование и производству электрических схем Отдельные стадии процесса в общем известны из области техники и описаны
Сначала приготовили силиконовые субстраты путем очищения ацетоном, метанолом и изопропиловым спиртом, и затем покрыли 258 нанометровым слоем диоксида кремния согласно способу химического осаждения из паровой фазы.
Затем на каждом субстрате сформировали рисунок с помощью процесса создания рисунка путем литографии с пучком электронов, как известно в данной области техники, применяя систему JEOL JBX-9300FS EBL. Условия способа были следующими:
Ток пучка = 11 нА
Ускоряющее напряжение = 100 кВ
Короткий шаг = 14 нм
Доза = 260 мкС/см2
Сопротивление = ZEP520A, ~330 нм толщины
Проявитель = n-амилацетат
Проявление = 2 мин. погружения, затем 30 с ополаскивание изпропиловым спиртом.
Затем осуществлялось травление диоксида кремния с помощью STS усиленного оксидного травления (АОЕ). Время травления составляло 50 секунд с применением 55 стандартных кубических сантиметров в минуту (сксм) Не, 22 сксм CF4, 20 сксм C4F8 при 4 мТорр, катушка 400 Вт, 200 Вт RIE и DC электрическое смещение 404-411 В.
Затем осуществляли протравливание кремния с помощью STS протравливания оксида кремния (SOE). Время травления составляло 2 секунд с применением 20 сксм Cl2 и 5 сксм Ar при 5 мТорр, катушка 600 Вт, 50 Вт RIE и DC электрическое смещение 96-102 В. Глубина протравливания кремния составляла 500 нанометров.
Буфферизованное оксидное протравливание (ВОЕ) применялось для удаления оставшегося оксида, которое включало три минуты ВОЕ погружения и затем промывку дионизированной водой.
Obducat NIL-Eitre®6 наноотпечатывающее устройство применялось для формирования узора на множестве полимерных субстратов. Внешняя вода применялась в качестве смазочно-охлаждающей жидкости. В УФ модуле применялась одна импульсная лампа при длине волны от 200 до 1000 нанометров при 1.8 Вт/см2. Применялся УФ фильтр 250-400 нанометров. Площадь воздействия составляла 6 дюймов с максимальной температурой 200°С и 80 Бар. Наноотпечатывающее устройство включало полуавтоматический узел разделения и автоматически контролируемое извлечение из формы.
Для облегчения высвобождения наноструктурированных пленок из форм, формы обрабатывали тридека-(1,1,2,2-тетрагидро)-октитрихлорсиланом (F13-TCS). Для обработки силиконовые формы сначала очищали с помощью промывки ацетоном, метанолом и изопропиловым спиртом, и высушивали газообразным азотом. Чашку Петри помещали на горячую плиту в атмосфере азота, и добавляли в чашку Петри 1-5 мл F13-TCS. Силиконовую форму помещали в чашку Петри и накрывали на 10-15 минут, позволяя F13-TCS пару смочить силиконовую форму до удаления формы.
Пять различных полимеров, приведенных в Таблице 1, показанной ниже, применялись для формирования различных нанотопографий.
|
Было сформировано несколько различных топографических рисунков, которые схематически показаны на Фиг.25A-25D. Нанотопографический рисунок, показанный на Фиг.25Е, был поверхностью плоского субстрата, полученного у NTT Advanced Technology, Токио, Япония. Рисунки были обозначены DN1 (Фиг.25А), DN2 (Фиг.25 В), DN3 (Фиг.25С), DN4 (Фиг.25D) и NTTAT2 (Фиг.25Е). SEM изображения форм показаны на Фиг.25А, 25В и 25С, и изображения пленок показаны на Фиг.25D и 25Е. Фиг.9 иллюстрирует наноструктурированную пленку, сформированную с применением формы по Фиг.25А (DN1 были созданы посредством изменения температуры, как раскрывалось ранее). Шероховатость поверхности рисунка по Фиг.25Е, как было обнаружено, составляла 34 нанометров.
Рисунок, показанный на Фиг.8С и 8D, был также сформирован в соответствии с этим процессом наноимпринтинга. Этот рисунок включал столбы 72 и столбы 62, как показано. Более крупные столбы 72 были сформированы с диаметром 3.5 микрометров (мкм) и высотой 30 мкм, с расстоянием от центра до центра 6.8 мкм. Столбы 62 имели 500 нанометров в высоту 200 нанометров в диаметре, и расстояние от центра до центра 250 нанометров.
Условия процесса наноимпринтинга с применением полипропиленовых пленок, приведены ниже в Таблице 2.
|
|
Пример 2
Пленки сформировали как описано выше в Примере 1, включая различные рисунки и формирование либо из полистирола (PS), либо полипропилена (РР). Нижележащий субстрат различался по толщине. Применяемыми рисунками были либо DN2, либо DN3, либо DN4, с применением процессов образования как описано в Примере 1. Формы для рисунков различались с точки зрения глубины отверстия и расположения элементов, с формированием множества различных по размеру элементов, имеющих разработанный рисунок. Образец №8 (обозначен ВВ1) был сформирован с применением 0.6 мкм миллипористого поликарбонатного фильтра в качестве формы. 25 мкм полипропиленовая пленка была нанесена на поверхность фильтра и затем нагрета до расплавления, так чтобы полипропилен мог втекать в поры фильтра. Затем форму охладили, и поликарбонатную форму растворили метиленхлоридным растворителем.
SEM сформированных пленок показано на Фиг.26-34, и характеристики сформированных пленок приведены в Таблице 3, показанной ниже.
|
Для каждого образца AFM применялась для характеризации пленки. Характеризация включала формирование изображения электронного сканирующего микроскопа (SEM), определение шероховатости поверхности, определение максимальной измеренной высоты элемента и определение фрактального размера.
Применяемым зондом атомно-силовой микроскопии (AFM) был силиконовый зонд серии 16, и консоль была доступна от µMasch. Консоль имела резонансную частоту 170 кГц, динамическую жесткость 40 Н/м, длину 230±5 мкм, ширину 40±3 мкм и толщину 7.0±0.5 мкм. Наконечник зонда представлял собой зонд n-типа из кремния, легированного фосфором, с типичным радиусом наконечника зонда 10 нанометров, полным коническим углом наконечника 40°, полной высотой наконечника 20-25 мкм и объемным удельным сопротивлением 0.01-0.05 ом-см.
Значение шероховатости поверхности, приведенное в Таблице 3, представляет собой арифметическое среднее высоты локального параметра шероховатости поверхности, как определено согласно ISO 25178.
Фрактальный размер вычисляли для различных углов, анализируя спектр амплитуды Фурье; для различных углов профиль амплитуды Фурье был выведен, и вычисляли логарифм от частоты и координат амплитуды. Фрактальный размер, D, для каждого направления затем вычислялся как:
D=(6+s)/2,
где s - (отрицательный) наклон кривых log - log. Приведенный фрактальный размер представляет собой среднее по всем направлениям.
Фрактальный размер также может быть вычислен из 2D спектра Фурье с помощью применения Log Log функции. Если поверхность представляет собой фрактал, Log Log диаграмма должна быть почти линейной с негативным наклоном (смотрите, например, Fractal Surfaces, John С. Russ, Springer-Verlag New York, LLC, July, 2008).
Пример З
HaCaT эпителиальные клетки кожи человека выращивали на DMEM, 10% FBS, 1% пенициллин/стрептомицин при 37°С, 5% CO2 в течение 24 часов при концентрации 25000 клеток/см2 в 6-ти луночном планшете. Планшеты либо имели полипропиленовые наноструктурированные пленки, сформированные как описано в примере 1 и обозначенные DN1, DN2 (Образец 4 Таблицы 3), DN3, или необработанную поверхность на дне лунки. Наноструктурированные пленки закрепляли на месте с помощью цианоакрилата.
Клетки отделяли от поверхностей с помощью 1 мл трипсина на лунку в течение 10 минут, гашения 1 мл среды для роста (такая же, как указано выше), затем переносили в микроцентрифужную трубку и гранулировали при 1200 оборотах в минуту в течение 7 минут.
RNA выделяли из гранулированных клеток с применением набора RNeasy miniprep от Qiagen с применением инструкции производителя. Кратко, клетки лизировали, смешивали с этанолом и помещали в колонку. Лизаты затем промывали 3 раза, обрабатывали с помощью DNase и элюировали с 40 мкл объемами.
кДнк получали из РНК, выделенной с применением набора RT first strand от SA Biosciences. Кратко, РНК снова обрабатывали DNase при 42°С в течение 5 минут .Случайные праймеры и фермента обратная транскриптаза добавляли и инкубировали при 42°С в течение 15 минут, затем инкубировали при 95°С в течение 5 минут с остановкой реакции.
ПЦР затем проводили на образцах кДНК, применяя обычный массив ПЦР RT profiler от SA Biosciences с праймерами для IL1-P, IL6, IL8, IL10, IL1R1, TNFα, TGFβ-1, PDGFA, GAPDH, HDGC, RTC и РРС. Кратко, кДНК смешивали с SYBR зеленым и водой, и затем добавляли на пластину ПЦР, предварительно фиксированную парой из смыслового и антисмыслового праймеров для представляющего интерес гена. Пластину затем обрабатывали с помощью ABI StepOnePlus устройства для ПЦР, при нагревании до 95°С в течение 10 минут, затем в течение 45 циклов: 15 секунд при 95°С и 1 минута при 60°С.
Дельта дельта СТ анализ проводили с применением GAPDH в качестве внутреннего контроля. Уровни HDGC, RTC и РРС применяли в качестве дополнительных внутренних контролей для активности и примесей геномной ДНК.
Одностадийный ANOVA и двухточечный Tukey's тесты затем применяли для определения статистической значимости при различиях между поверхностями.
Таблица 4, показанная ниже, приводи экспрессии белка, полученные как кратное изменение экспрессии на наноотпечатанных структурах, полученных на полипропиленовых ленках, относительно экспрессии на неструктурированной пленке.
|
Пример 4
Способы, описанные в Примере 3, применялись для исследования экспрессионного уровня для нескольких различных цитокинов НаСаТ эпителиальных клеток кожи человека, когда клеткам позволяли развиваться на множестве различных полипропиленовых (РР) или полистирольных (PS) пленок, сформированных и структурированных как описано выше. Экспрессионный уровень для каждого цитокина сравнивали с уровнем для того же клеточного типа, культивированного на полистироле на стандартной тканевой культуры (TCPS) и индуцированного липополисахаридом (LPS).
Клетки, полученные на полипропиленовой пленке, наноструктурированной узором DN2, как описано выше (Образец 4 Таблицы 3), как было обнаружено, повышенным образом экспрессировали IL-1β, IL-1ra, IL-10, и MIP-1β, и пониженным образом экспрессировали IL-4, IL-13, MIG, КС, IL-2, MIP-1, TNF-α, IL-12, IL-16, и IL-1α, по сравнению с TCPS.
Некоторые другие пленки были исследованы с точки зрения воздействия на клеточную экспрессию различных цитокинов. Пленки обозначили следующим образом:
1 - DN2 узор на 75 мкм полистирольной пленке (Образец 3 Таблицы 3)
2 - DN3 узор на 75 мкм полистирольной пленке (Образец 1 Таблицы 3)
3 - DN4 узор на 75 мкм полистирольной пленке (Образец 6 Таблицы 3)
4 - неотпечатанная 75 мкм полистирольной пленке
5 - DN2 узор на 25.4 мкм полипропиленовой пленке (Образец 4 Таблицы 3)
6 - DN4 узор на 25.4 мкм полипропиленовой пленке (Образец 7 Таблицы 3)
7 - DN2 узор на 5 мкм полипропиленовой пленке (Образец 2 Таблицы 3)
8 - ВВ1 полипропиленовая пленка (Образец 8 Таблицы 3)
9 - неотпечатанная 25.4 мкм полипропиленовая пленка
10 - неотпечатанная 5 мкм полипропиленовая пленка
Результаты показаны в Таблице 5, приведенной ниже. Приведены следующие результаты:
- экспрессионный уровень был ниже пороговой величины тестирования
- экспрессионный уровень был ниже, чем уровень для TCPS
= экспрессионный уровень был подобен уровню для TCPS
+ экспрессионный уровень был выше уровня для TCPS, но ниже, чем при индукции с LPS
++ экспрессионный уровень был подобен уровню для индукции с LPS
+++ экспрессионный уровень был выше уровня для индукции с LPS
|
Пример 5
НаСаТ эпителиальные клетки кожи человека выращивали на DMEM, 10% FBS, 1% пенициллин/стрептомицин при 37°С, 5% CO2 в течение 24 часов при концентрации 25000 клеток/см2 в 6-ти луночном планшете. Планшеты либо имели полипропиленовую пленку, образованную как описано выше в Примере 1 с обозначением DN1, DN2 (Sample 4 of Table 3), DN3, либо необработанную поверхность на дне лунки. Пленки закрепляли на месте с помощью цианоакрилата.
Среду собирали из каждой лунки и анализировали на продуцирование цитокинов с помощью набора Milliplex Map от Millipore. Применялись гранулы для определения IL-1β, IL-1ra, IL-6, IL-8, IL-10, PDGF-AA, PGGF-AB/BB и TNF-α. Данные были получены с помощью устройства BioRad BioPlex. Кратко, среду помещали в лунки микропланшета с фильтрами. Первичные гранулы добавляли и инкубировали при комнатной температуре в течение 1 часа при перемешивании. Планшеты затем промывали и инкубировали с обнаружением антител в течение 30 минут при комнатной температуре с перемешиванием. Стрепавидин-фикоэритрин затем добавляли и инкубировали при комнатной температуре в течение еще 30 минут. Планшеты затем промывали, гранулы ресуспендировали в буфере для анализа, и анализировали среднюю интенсивность флуоресценции на BioPlex.
Пример 6
Действие на проницаемость пленок, структурированных как описано выше, были определены на монослое клеток Caco-cells (человеческие эпителиальные клетки колоректальной аденокарциномы).
Пленки, сформированные как описано выше в Примере 1, применяли, включая полипропиленовые (РР) или полистирольные (PS) пленки, образованные с рисунками, обозначенными DN2, DN3 и DN4. Четвертая пленка, обозначенная ВВ1 (описана в Примере 2, приведенном выше), также применялась. Протокол повторяли для множества образцов для каждого типа пленки.
Общий протокол для каждой пленки был следующим:
Материалы
Клеточная культура входящая в HDPET мембрану с размером пор 0.4 мкм (BD Falcon)
24-х луночный планшет (BD Falcon)
Сасо-2 среда
Наноструктурированные мембраны, как описано выше
IgG-FITC (Sigma Aldrich)
BSA-FITC (Sigma Aldrich)
Минимальная среда без фенола красного (Invitrogen)
TEER вольтметр
Нагретая PBS
черный 96-луночный планшет
Алюминиевая фольга
Протокол
1. Осуществляли высевание Сасо-2 клеток в покрытые коллагеном луночные вставки за 2 недели до анализа проницаемости. Планшеты, покрытые коллагеном, получали с помощью 1:1 объемного отношения 100% этанола к коллагену. Сушили поверхности в стерильном кожухе всю ночь до высыхания.
2. Получили 0.1 мг/мл раствор FITC-сопряженной молекулы (BSA, IgG, и т.д.), представляющей интерес, в среде Alpha MEM, не содержащей фенол красный. Помещали в алюминиевую фольгу для защиты от света.
3. Проверяли конфлюэнтность Сасо-2 клеток путем измерения резистентности. Для конфлюэнтности резистентность должна быть выше ~600 Ом.
4. Отделяли старую среду от вставок клеточной культуры на апикальной и базально-латеральной сторонах. Добавляли PBS для удаления каких-либо остатков красителя фенола красного.
5. Добавляли 0.5 мл FITC-сопряженный раствор на апикальную сторону каждой вставки.
6. В другой 24-х луночный планшет с вставками клеточной культуры добавляли 0.5 мл теплой PBS.
7. Переносили вставки в планшет с PBS. Грунтовали дно вставки на Kim wipe для удаления остаточного фенола красного.
8. t=0 - точка времени: образец 75 мкл из базально-латеральной стороны вставки и перенос в 96-ти луночный планшет с черным дном. Замещение объема 75 мкл подогретой PBS. Запись сопротивления каждой лунки с применением "chopstick" электродов.
9. Аккуратное добавление мембраны в соответствующую помеченную лунку. Контролями являются неотпечатанные мембраны и клетки сами по себе. Проверка под микроскопом, что мембраны входят в прямой контакт с клетками. Вы должны увидеть круг с большой кривизной, указывающий на контакт с клетками.
10. t=0 точка времени: повторение стадии 7 и затем помещение в инкубатор на 1 час
11. t=1 точка времени: повторение стадии 7 и затем помещение в инкубатор на 1 час
12. t=2 точка времени: повторение стадии 7
13. Измерение флуоресцентного сигнала с применением планшетного ридера спектрофлуорометра. FITC (возбуждение=490 нм, эмиссия=520 нм)
Результаты
Использовали пленки, и полученные результаты привели в Таблице 6, показанной ниже.
|
Модули определяли в соответствии со стандартными способами, которые известны в данной области техники, как например описано Schubert, et al. (Sliding induced adhesion of stiff polymer microfiber arrays: 2. Microscale behaviour, Journal Royal Society, Interface, Jan. 22, 2008. 10.1098/rsif.2007.1309)
Углы контакта измеряли путем помещения капли воды на поверхность согласно стандартной практике. (Смотрите, например, Woodward. First Ten Angstroms, Portsmouth, VA).
Фиг.35 графически иллюстрирует действие на проницаемость для альбумина бычьей сыворотки (BSA) в монослое клеток на наноструктурированных полистирольных пленках, как описано. Узоры пленок включали DN2 узор (образец №3), DN3 узор (образец №5) и DN4 узор (образец №6), как указано. Также показаны результаты для неструктурированной PS пленки (отмечена PSUI на Фиг.35) и слоя клеток без соседней пленки (отмечено 'клетки' на Фиг.35). Результаты показаны в виде кратности увеличения проницаемости как функции от времени, измеренного в часах.
Фиг.36А и Фиг.36В графически иллюстрируют влияние на проницаемость для иммуноглобулина-G (IgG) в монослое клеток на полистирольных пленках, наноструктурированных как описано. Узоры пленок включали DN2 узор (образец №3), DN3 узор (образец №5) и DN4 узор (образец №6), как указано. Также показаны результаты для неструктурированной пленки (отмечена PSUI на Фиг.36А и 36В)и слоя клеток без соседней пленки (отмечена клетки на Фиг.36А и 36В). Два чертежа показывают данные для двух различных временных шкал.
BSA сигнал считывали на флюорометре, и IgG сигнал считывали на спектрофотометре.
Фиг.37А и 37В представляют собой 3D флуоресцеин окрашенные изображения жизнь/смерть, показывающие параклеточный и трансклеточный транспорт IgG через монослой клеток на полистирольной поверхности с DN4 узором (образец №6).
Фиг.38 графически иллюстрирует действие на проницаемость для BSA в монослое клеток на полипропиленовых пленках, наноструктурированных как описано. Узоры включают ВВ1 (образец №8), DN2 (образец №4) и DN4 (образец №7), как указано. Также показаны результаты для неструктурированной пленки (отмечена PPUI на Фиг.38) и слоя клеток без соседней пленки (отмечено 'клетки' на Фиг.38).
Фиг.39 графически иллюстрирует влияние на проницаемость для IgG в монослое клеток на полипропиленовых пленках, наноструктурированных как описано выше. Узоры включали ВВ1 (образец №8), DN2 (образец №4) и DN4 (образец №7), как указано. Также показаны результаты для неструктурированной пленки (отмечена PSUI на Фиг.39) и слоя клеток без соседней пленки (отмечено 'клетки на Фиг.39).
Фиг.40А и 40В представляют собой 3D флуоресцеин окрашенные изображения жизнь/смерть, показывающие параклеточный транспорт IgG через монослой клеток на полипропиленовой поверхности с DN2 узором (образец №4).
Фиг.41A-41F показывают изображения сканирующего электронного микроскопа (SEM) для Сасо-2 клеток, культивированных на наноструктурированных поверхностях. В частности, Фиг.41А и 29В иллюстрируют Сасо-2 клетки на плоской полистирольной контрольной пленке. Фиг.41С и 41D иллюстрируют Сасо-2 клетки на полистирольной пленке с DN2 рисунком (образец №3), как описано выше, и Фиг.41Е и 41 F иллюстрируют Сасо-2 клетки на полистирольной пленке с DN3 узором (образец №5), как описано выше.
Пример 7
Способ, как описано в Примере 6, применялся для изучения проницаемости монослоя Сасо-2 клеток слитым белком, терапевтическим средством, этанерцепт (продается под торговым наименованием Enbrel®). Фиг.42 графически иллюстрирует роста клеточного слоя на нескольких различных структурированных субстратах, включая как полипропилен (DN2 РР - образец 4 таблицы 3), так и полистирол (DN2 PS - образец 3 таблицы 3 и DN3 PS - образец 1 таблицы 3), а также неотпечатанную полистирольную мембрану (PSUI), слоя клеток без мембраны (клетки). Результаты показаны в виде кратности изменения первоначальной проницаемости со временем. Фиг.43 иллюстрирует кратность изменения проницаемости от первоначальной t=0 до двухчасовой (t=2), после добавления мембраны в лунку для субстратов и клеточного слоя по Фиг.42.
Пример 8
Был сформировано множество микроигл, включающих нанострукткрированную поверхность. Первоначально, множество микроигл, показанное на Фиг.2, было сформировано на кремниевой пластине через фотолитографический процесс. Каждая игла включала два канала, расположенные на противоположных сторонах, находящиеся на одной линии с фильерой в основании иглы (не показано на Фиг.2).
Микроиглы были сформированы согласно стандартному процессу микромеханической обработки на кремниевой пластине. На пластины наносили слои сопротивления и/или оксида, затем селективно травили (оксидное травление, DRIE травление, изотравление), удаляли резист, проводили оксидное удаление и методику литографии (например, изолитография, литография с формированием отверстия, литография с формированием щели) согласно стандартным способам формирования множества микроигл.
После образования множества микроигл, 5 мкм полипропиленовую пленку, включающую образованный на ней DN2 узор, как описано выше в примере 1, характеристики которой приводятся для образца 2 в Таблице 3, нанесли на множество микроигл. Структуру пластина/пленка хранили в подогретом вакуумном боксе (3 дюйма. H2O вакуум) при повышенной температуре (130°С) в течение одного часа для равномерного натягивания пленки по поверхности микроигл, при сохранении наноструктурированной поверхности пленки.
Фиг.44 иллюстрирует пленку на поверхности множества микроигл, и Фиг.45 показывает приближенный вид одной иглы множества, включающей наноструктурированную пленку, покрывающую поверхность иглы.
Пример 9
Были получены трансдермальные пластыри, включающие множество микроигл, сформированные как описано в Примере 8. Пластыри формировали либо с DN2 узором, либо с DN3 узором на множестве микроигл. Пленки, определяющие рисунки, которые наносились на микроиглы, описаны в Таблице 7, приведенной ниже. Пленка 1 эквивалентна образцу 2 в Таблице 3, и пленка 2, эквивалентна образцу №9 в Таблице 3.
|
Контрольные пластыри также формировали без узора на пленке, впоследствии наносящейся на множество микроигл. Трансдермальную и подкожную композиции этанерцепта (Энбрел®) получали согласно инструкциям поставщика лекарственного средства. Подкожную композицию получали для достижения подкожной дозы лекарственного средства 4 мг/кг. Концентрацию Энбрела® для трансдермальной доставки, регулировали так, чтобы предназначенная доза 200 4 мг/кг достигалась за 24 часа.
Всего в исследовании применялось 10 BALB/C мышей (обозначенных №1-№10), восьми вводили трансдермальную дозу Энбрела® (группа 1), двум вводили подкожную дозу Энбрела® (группа 2), как описано в Таблице 8, приведенной ниже. Трансдермальные пластыри наносили на выбритые области кожи, и образовывались отверстия около концов микроигл, при прикрепления пластыря к коже.
|
Применяемые Трансдермальные пластыри включали как имеющие нанотопографию на поверхности (DN2 и DN3 узоры, как описано выше), так и пластыри без узора нанотопографии.
Образцы цельной крови собирали в моменты времени, показанные в Таблице 8. Около 100-200 мкл крови собирали посредством мандибулярного кровотечения и затем центрифугировали при 1300 оборотах в минуту в течение 10 минут в охлаждаемой центрифуге (установлена на 4°С). Полученную сыворотку отделяли и переносили в течение 30 минут сбора крови/центрифугирования в соответствующим образом помеченные пробирки. Пробирки замораживали и хранили в темноте при ≤-70°С до их анализа в отношении уровней Энбрела®, с применением набора Human sTNF-receptor ELISA (R&D Systems cat №DRT200). Период между двумя отборами крови у одного субъекта составлял 24 часа, для предотвращения нежелательного стресса у субъекта.
Фиг.46 графически иллюстрирует средний РК профиль трансдермальных пластырей, которые имеют нанотопографию на них. Усредненные результаты по всем имеющим нанотопографию пластырям применялись для представления общего эффекта введения нанотопографии в трансдермальный пластырь с микроиглами. Как можно увидеть, уровень в сыворотке крови быстро рос до более 800 нг/мл/см2 площади пластыря в течение первых двух часов присоединения. Затем уровень в сыворотке крови равномерно снижался до ничтожного в течение 24 часов присоединения. Данные, применяемые для ФИГ. 46, приведены в Таблице 9.
|
Фиг.47А и 47В иллюстрируют изображения электронного микроскопа для поперечного сечения кожи, которая находилась в контакте с пластырем. Изображения получали после удаления пластыря (72 часов после присоединения). Образец Фиг.47А находился в контакте с пластырем, включающим нанотопографию на поверхности. В частности, DN2 узор, как описано выше, был сформирован на поверхности пластыря. Образец по Фиг.47В находился в контакте с трансдермальным пластырем, который не имел узор нанотопографии на поверхности. Как можно увидеть, образец Фиг.47В показывает признаки воспаления и высокую плотность присутствия макрофагов.
Пример 10
Были получены трансдермальные пластыри, включающие множество микроигл, сформированные как описано в Примере 8. Пластыри получены либо с DN2 узором, либо с DN3 узором на множестве микроигл, как раскрывается в Таблице 7 Примера 9. Контрольные пластыри получали таким образом, что они не имели узора, сформированного на пленке, впоследствии наносящейся на множество микроигл. Трансдермальную и подкожную композиции этанерцепта (Энбрела®) получали согласно инструкциям поставщика лекарственного средства.
Тестируемым субъектам (кроликам) трансдермально вводили дозу Энбрела® или подкожно (SubQ) вводили дозу Энбрела®. Результаты показаны графически на Фиг.48, на котором приводится концентрация в сыворотке крови в пг/нл как функция от времени. Данные, используемые для Фиг.48, приводятся в Таблице 10, показанной ниже.
|
Тогда как настоящее изобретение было подробно описано в отношении конкретных вариантов его выполнения, необходимо понимать, что специалист в данной области техники может легко прийти к изменениям, вариантам и эквивалентам этих вариантов выполнения настоящего изобретения. Соответственно объем настоящего изобретения должен ограничиваться только приложенной формулой изобретения и любыми ее эквивалентами.